专题5 药物合成的重要原料—卤代烃、胺、酰胺 单元检测题 (含答案)2022-2023学年高二下学期化学苏教版(2019)选择性必修3
文档属性
| 名称 | 专题5 药物合成的重要原料—卤代烃、胺、酰胺 单元检测题 (含答案)2022-2023学年高二下学期化学苏教版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 692.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-25 00:00:00 | ||
图片预览


文档简介
专题5《药物合成的重要原料—卤代烃、胺、酰胺》单元检测题
一、单选题(共13题)
1.下列有机物关系判断正确的是
A.燃烧生成黑烟的浓厚程度:乙炔>乙烯>乙烷
B.密度:石蜡>水>汽油
C.熔点:新戊烷>正戊烷>丙烷
D.同质量完全燃烧耗量:乙炔>乙烯>甲烷
2.下列对有机物结构或性质的描述,正确的是
A.0.1mol羟基中含有1mol电子
B.乙烷和丙烯任意比混合的气体1mol,完全燃烧均生成3molH2O
C.7.8g苯分子中碳碳双键的数目为0.3NA
D.有机物1-甲基环己烷()的一氯代物有4种
3.下列反应的生成物只有一种的是
A.乙烷与氯气在光照条件下发生取代反应
B.异戊二烯与Br2发生加成反应
C.2,3-二甲基-2-丁烯与HBr发生加成反应
D.2-溴丁烷与NaOH的醇溶液共热发生消去反应
4.下列实验方案正确的是( )
A.证明溴乙烷中溴元素的存在:向溴乙烷中加入NaOH溶液,共热,冷却后加入AgNO3溶液,产生浅黄色沉淀
B.银氨溶液的配制:向1mL 2%的稀氨水中逐滴滴加2%的AgNO3溶液
C.苯甲酸的提纯:将1g粗苯甲酸放到100mL的烧杯里,加入50mL水,加热完全溶解后趁热过滤,静置冷却可析出苯甲酸晶体
D.除去苯中的苯酚杂质:向混有苯酚的苯中加入浓溴水,产生白色沉淀,再过滤
5.下列有关2-氯丁烷的叙述正确的是
A.分子式为C4H8Cl2
B.与硝酸银溶液混合产生不溶于稀硝酸的白色沉淀
C.易溶于水,可混溶于乙醇、乙醚、氯仿等多数有机溶剂
D.与氢氧化钠、乙醇在加热条件下的消去反应有机产物有两种
6.为鉴别卤代烃中所含卤素原子,现有下列实验操作步骤,正确的顺序是
①加入AgNO3溶液 ②加入少许卤代烃试样 ③加热 ④加入5 mL 4 mol·L-1 NaOH溶液 ⑤加入5 mL 4 mol·L-1 HNO3溶液
A.②④③①⑤ B.②③①④⑤ C.②④③⑤① D.②⑤③①④
7.普罗帕酮为广谱高效抗心律失常药。下列说法正确的是
A.可用溴水或FeCl3溶液鉴别X和Y B.反应物X与中间体Y互为同系物
C.普罗帕酮分子中有2个手性碳原子 D.X、Y和普罗帕酮都能发生加成、水解、氧化、消去反应
8.碳链增长在有机合成中具有重要意义,它是实现由小分子有机化合物向较大分子有机化合物转化的主要途径。某同学设计了如下4个反应,其中可以实现碳链增长的是
A.CH3CH2CH2CH2Br和NaCN共热
B.CH3CH2CH2CH2Br和NaOH的乙醇溶液共热
C.CH3CH2Br和NaOH的水溶液共热
D.CH3CH2CH3和Br2(g)光照
9.下列关于有机物的说法错误的是
A.甲烷分子的空间填充模型为
B.分子式为C4H9Cl的有机物共有4种
C.有机化合物种类繁多与碳原子的成键特点有关
D.易溶于汽油、苯等有机溶剂的物质一定是有机物
10.下列物质转化中,所用的试剂、条件不合理的是
物质转化 试剂、条件
A 浓硫酸、加热
B 浓硝酸与浓硫酸、50~60℃
C 苯→溴苯 液溴、铁粉
D Na
A.A B.B C.C D.D
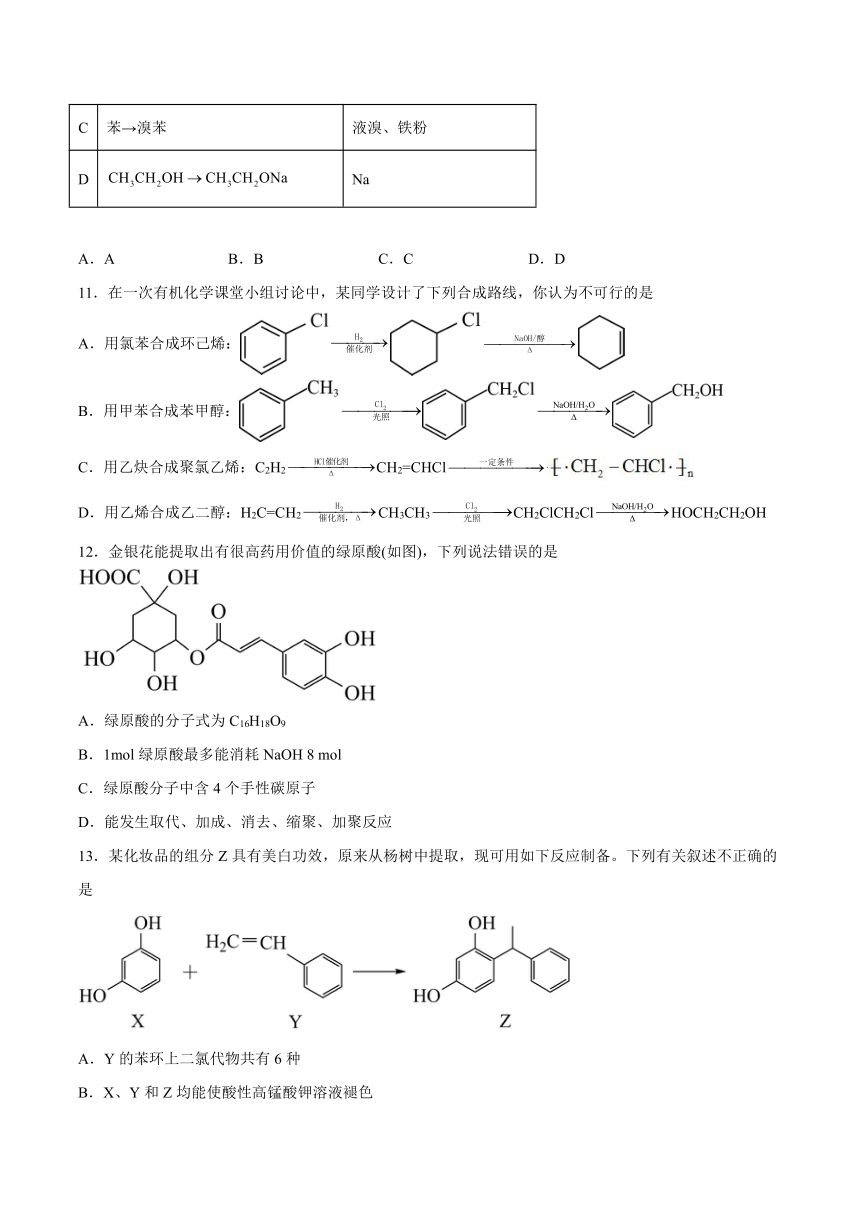
11.在一次有机化学课堂小组讨论中,某同学设计了下列合成路线,你认为不可行的是
A.用氯苯合成环己烯:
B.用甲苯合成苯甲醇:
C.用乙炔合成聚氯乙烯:C2H2CH2=CHCl
D.用乙烯合成乙二醇:H2C=CH2CH3CH3CH2ClCH2ClHOCH2CH2OH
12.金银花能提取出有很高药用价值的绿原酸(如图),下列说法错误的是
A.绿原酸的分子式为C16H18O9
B.1mol绿原酸最多能消耗NaOH 8 mol
C.绿原酸分子中含4个手性碳原子
D.能发生取代、加成、消去、缩聚、加聚反应
13.某化妆品的组分Z具有美白功效,原来从杨树中提取,现可用如下反应制备。下列有关叙述不正确的是
A.Y的苯环上二氯代物共有6种
B.X、Y和Z均能使酸性高锰酸钾溶液褪色
C.X、Y和Z分子中所有原子都可能处于同一平面
D.X、Y都可作为单体发生聚合反应生成高分子
二、非选择题(共10题)
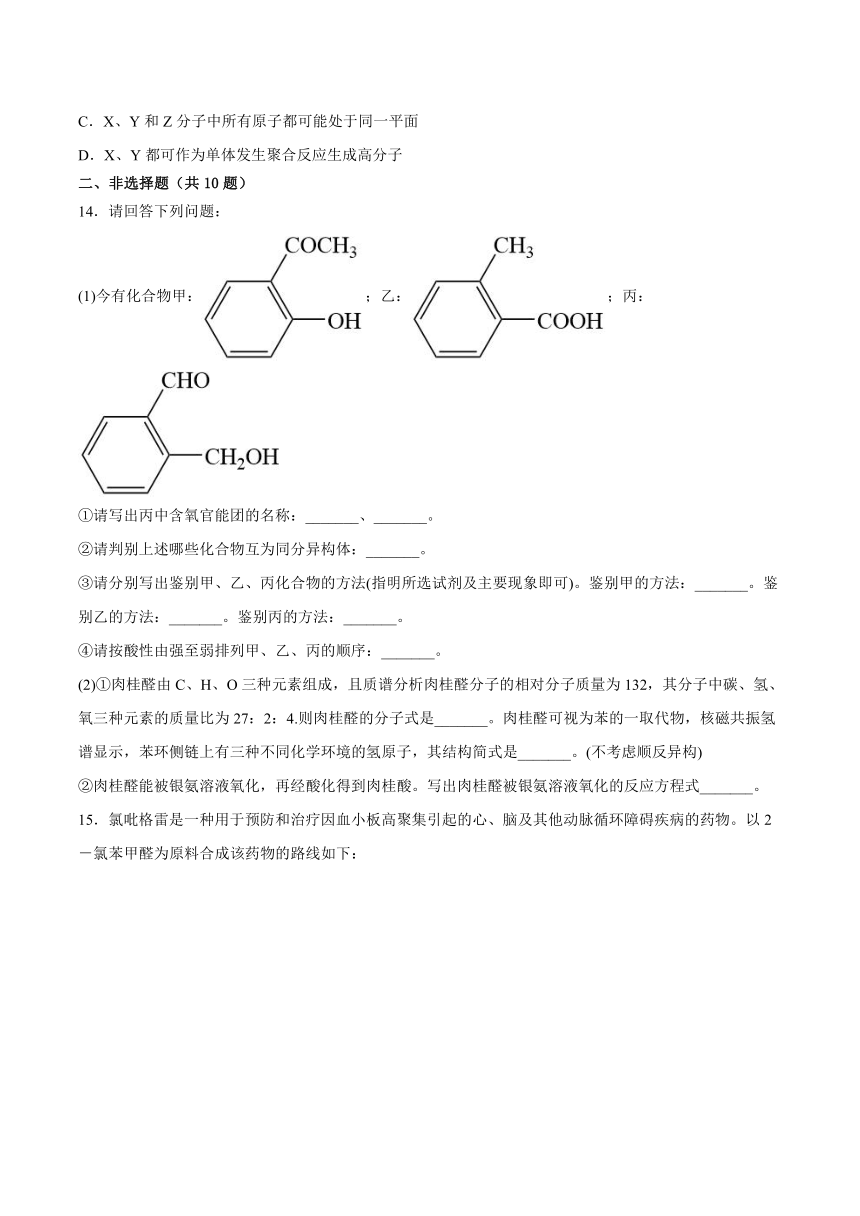
14.请回答下列问题:
(1)今有化合物甲:;乙:;丙:
①请写出丙中含氧官能团的名称:_______、_______。
②请判别上述哪些化合物互为同分异构体:_______。
③请分别写出鉴别甲、乙、丙化合物的方法(指明所选试剂及主要现象即可)。鉴别甲的方法:_______。鉴别乙的方法:_______。鉴别丙的方法:_______。
④请按酸性由强至弱排列甲、乙、丙的顺序:_______。
(2)①肉桂醛由C、H、O三种元素组成,且质谱分析肉桂醛分子的相对分子质量为132,其分子中碳、氢、氧三种元素的质量比为27:2:4.则肉桂醛的分子式是_______。肉桂醛可视为苯的一取代物,核磁共振氢谱显示,苯环侧链上有三种不同化学环境的氢原子,其结构简式是_______。(不考虑顺反异构)
②肉桂醛能被银氨溶液氧化,再经酸化得到肉桂酸。写出肉桂醛被银氨溶液氧化的反应方程式_______。
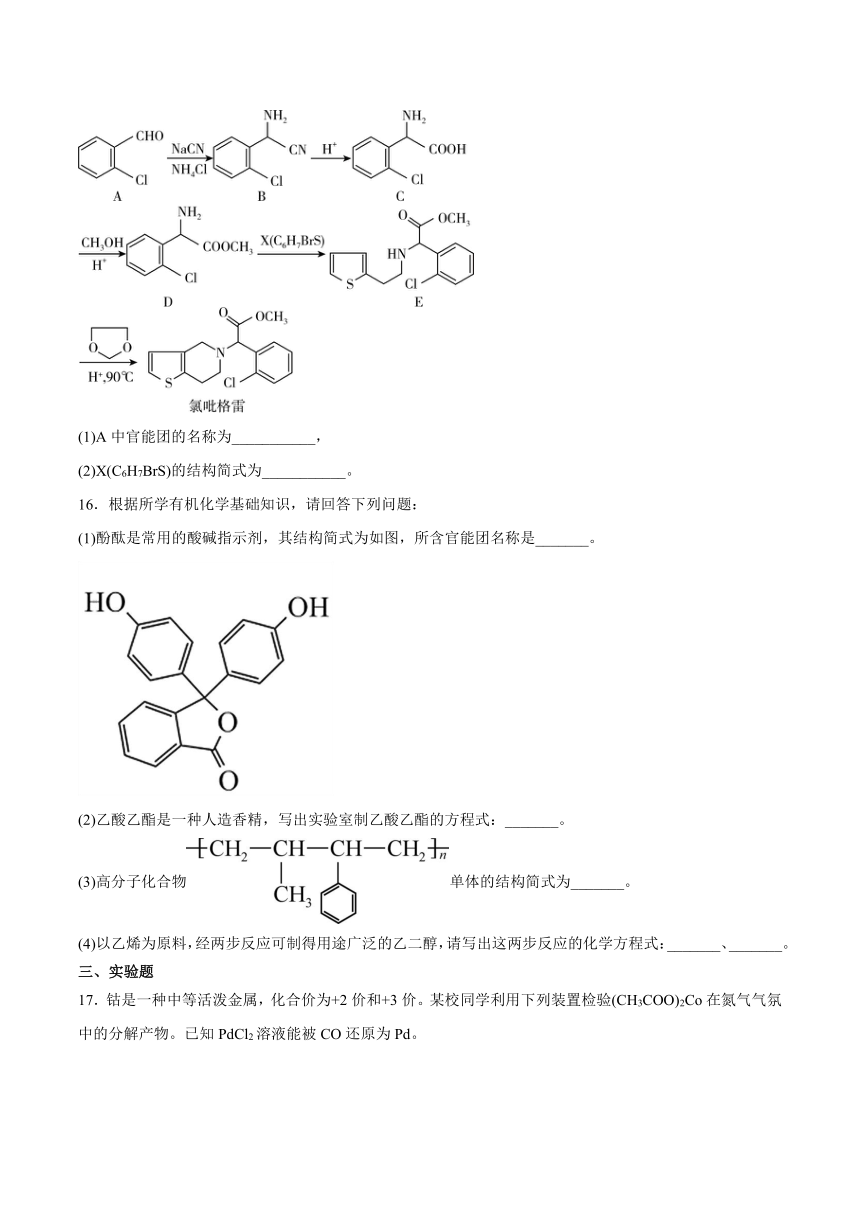
15.氯吡格雷是一种用于预防和治疗因血小板高聚集引起的心、脑及其他动脉循环障碍疾病的药物。以2-氯苯甲醛为原料合成该药物的路线如下:
(1)A中官能团的名称为___________,
(2)X(C6H7BrS)的结构简式为___________。
16.根据所学有机化学基础知识,请回答下列问题:
(1)酚酞是常用的酸碱指示剂,其结构简式为如图,所含官能团名称是_______。
(2)乙酸乙酯是一种人造香精,写出实验室制乙酸乙酯的方程式:_______。
(3)高分子化合物单体的结构简式为_______。
(4)以乙烯为原料,经两步反应可制得用途广泛的乙二醇,请写出这两步反应的化学方程式:_______、_______。
三、实验题
17.钴是一种中等活泼金属,化合价为+2价和+3价。某校同学利用下列装置检验(CH3COO)2Co在氮气气氛中的分解产物。已知PdCl2溶液能被CO还原为Pd。
(1)装置E、F是用于检验CO和CO2的,其中盛放PdCl2溶液的是装置______(填“E”或“F”)。
(2)装置G的作用是______;E、F、G中的试剂均足量且充分反应,观察到I中氧化铜变红,J中固体由白色变蓝色,K中石灰水变浑浊,则可得出的结论是______。
(3)实验结束时,先熄灭D和I处的酒精灯,一段时间后再关闭弹簧夹,其目的是______。
(4)若乙酸钴最终分解生成固态氧化物X、CO、CO2、C2H6,且n(X):n(CO):n(CO2):n(C2H6)=1:4:2:3(空气中的成分不参与反应),则乙酸钴在空气气氛中分解的化学方程式为______。
18.现有分子式均为C3H6O2的四种有机物A、B、C、D,且分子中均含甲基,把它们分别进行下列实验以鉴别之,其实验记录如下:
NaOH溶液 银氨溶液 新制Cu(OH)2 金属钠
A 中和反应 ----------- 溶解 产生氢气
B ----------- 有银镜 加热后有红色沉淀 产生氢气
C 水解反应 有银镜 加热后有红色沉淀 -----------
D 水解反应 ----------- ----------- -----------
(1)B分子中官能团的名称是:____________
(2)B、C的结构简式分别为:B_________________,C_________________。
(3)D在NaOH溶液中反应的化学方程式为______________________________。
(4)写出B与银氨溶液反应的化学方程式:_______________________________。
(5)属于A的同系物且比A少一个碳原子的物质E的同分异构体有(写结构简式)____________________。
四、计算题
19.一定质量的甲烷燃烧后得到的产物为CO、CO2和水蒸气,此混合气体质量为49.6g,当其缓慢经过无水CaCl2时,CaCl2增重25.2g,计算:
(1)参加反应的甲烷的物质的量为_______mol
(2)生成的CO的质量为_______g。
20.某仅由碳、氢、氧三种元素组成的有机化合物,经测定其相对分子质量为180。取有机物样品1.8g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.08g和2.64g。试求该有机物的分子式_____。
21.化合物F是一种重要的有机合成中间体,它的合成路线如图:
(1)化合物F中含氧官能团的名称是______和______,由A生成B的化学反应类型是______;
(2)写出化合物B的结构简式:______;
(3)写出化合物C与乙酸反应生成酯的化学方程式:______;
(4)某化合物是D的同分异构体,且分子中只有三种不同化学环境的氢。写出该化合物的结构简式:______(任写一种);
22.某兴趣小组对化合物X开展探究实验。
其中:常温常压下ⅹ是一种有特殊气味、易挥发的无色液体,由三种常见的短周期元素组成。
请回答:
(1)组成X的3种元素是_______(填元素符号),沉淀C的化学式是_______。
(2)X反应生成A和B的反应方程式是_______。
(3)B可与乙醇以物质的量之比1∶2发生取代反应生成一种酯,写出反应方程式_______。
(4)实验室保存少量物质X的仪器是_______。
A.无色广口瓶 B.棕色广口瓶 C.无色细口瓶 D.棕色细口瓶
(5)请设计一种不同于上述流程的实验方案,检验中相对原子质量最大的元素_______。
23.物质F是一种芳香酯,常用作调香剂,其合成路线如下图所示:
已知E中含有两个甲基,请回答下列问题:
(1)物质A的名称是_______。
(2)各取1 mol物质D分别与足量Na、NaOH溶液、NaHCO3溶液反应,消耗的Na、NaOH、NaHCO3的物质的量之比为_______。
(3)物质A到F中除D以外含有手性碳原子的物质是_______(填标号)。
(4)B→C的反应方程式是_______。
(5)E的同分异构体中与其含有相同种类官能团的有_______种(不含E本身)。
参考答案:
1.A 2.B 3.C 4.C 5.D 6.C 7.A 8.A 9.D 10.A 11.D 12.B 13.C
14.(1) 羟基 醛基 甲、乙、丙 加入三氯化铁溶液,溶液显紫色的为甲 加入紫色石蕊试液,溶液呈红色,则为乙 加入银氨溶液或新制的Cu(OH)2,若有银镜出现或红色的沉淀生成的则为丙 乙>甲>丙
(2) C9H8O C6H5CH=CHCHO+2Ag(NH3)2OH2Ag↓+H2O+3NH3+C6H5CH=CHCOONH4
15.(1)醛基、氯原子
(2)
16.(1)羟基、酯基
(2)CH3COOH+C2H5OHCH3COOCH2CH3+H2O
(3) 和CH2=CH-CH3
(4) CH2=CH2+Br2→BrCH2CH2Br BrCH2CH2Br+2NaOHHOCH2CH2OH+2NaBr
17. F 除去CO2 分解产物中还含有机物 防止倒吸 3(CH3COO)2CoCo3O4+4CO↑+2CO2↑+3C2H6↑
18. 羟基、醛基 CH3CH(OH)CHO HCOOCH2CH3 CH3COOCH3+NaOHCH3COONa+CH3OH CH3CH(OH)CHO+2Ag(NH3)2OHCH3CH(OH)COONH4+2Ag+3NH3+H2O CH3COOH
19. 0.7 11.2
20.C6H12O6
21. 醛基 羰基 取代反应 CH3COOH+ + H2O
22. C、H、 D 取少量Ⅹ于试管中,加入适量溶液并加热。冷却后加足量稀酸化,再加入溶液,生成白色沉淀,证明ⅹ中含有氯元素
23. 2-甲基-1-丁烯 2:1:1 BC 7
一、单选题(共13题)
1.下列有机物关系判断正确的是
A.燃烧生成黑烟的浓厚程度:乙炔>乙烯>乙烷
B.密度:石蜡>水>汽油
C.熔点:新戊烷>正戊烷>丙烷
D.同质量完全燃烧耗量:乙炔>乙烯>甲烷
2.下列对有机物结构或性质的描述,正确的是
A.0.1mol羟基中含有1mol电子
B.乙烷和丙烯任意比混合的气体1mol,完全燃烧均生成3molH2O
C.7.8g苯分子中碳碳双键的数目为0.3NA
D.有机物1-甲基环己烷()的一氯代物有4种
3.下列反应的生成物只有一种的是
A.乙烷与氯气在光照条件下发生取代反应
B.异戊二烯与Br2发生加成反应
C.2,3-二甲基-2-丁烯与HBr发生加成反应
D.2-溴丁烷与NaOH的醇溶液共热发生消去反应
4.下列实验方案正确的是( )
A.证明溴乙烷中溴元素的存在:向溴乙烷中加入NaOH溶液,共热,冷却后加入AgNO3溶液,产生浅黄色沉淀
B.银氨溶液的配制:向1mL 2%的稀氨水中逐滴滴加2%的AgNO3溶液
C.苯甲酸的提纯:将1g粗苯甲酸放到100mL的烧杯里,加入50mL水,加热完全溶解后趁热过滤,静置冷却可析出苯甲酸晶体
D.除去苯中的苯酚杂质:向混有苯酚的苯中加入浓溴水,产生白色沉淀,再过滤
5.下列有关2-氯丁烷的叙述正确的是
A.分子式为C4H8Cl2
B.与硝酸银溶液混合产生不溶于稀硝酸的白色沉淀
C.易溶于水,可混溶于乙醇、乙醚、氯仿等多数有机溶剂
D.与氢氧化钠、乙醇在加热条件下的消去反应有机产物有两种
6.为鉴别卤代烃中所含卤素原子,现有下列实验操作步骤,正确的顺序是
①加入AgNO3溶液 ②加入少许卤代烃试样 ③加热 ④加入5 mL 4 mol·L-1 NaOH溶液 ⑤加入5 mL 4 mol·L-1 HNO3溶液
A.②④③①⑤ B.②③①④⑤ C.②④③⑤① D.②⑤③①④
7.普罗帕酮为广谱高效抗心律失常药。下列说法正确的是
A.可用溴水或FeCl3溶液鉴别X和Y B.反应物X与中间体Y互为同系物
C.普罗帕酮分子中有2个手性碳原子 D.X、Y和普罗帕酮都能发生加成、水解、氧化、消去反应
8.碳链增长在有机合成中具有重要意义,它是实现由小分子有机化合物向较大分子有机化合物转化的主要途径。某同学设计了如下4个反应,其中可以实现碳链增长的是
A.CH3CH2CH2CH2Br和NaCN共热
B.CH3CH2CH2CH2Br和NaOH的乙醇溶液共热
C.CH3CH2Br和NaOH的水溶液共热
D.CH3CH2CH3和Br2(g)光照
9.下列关于有机物的说法错误的是
A.甲烷分子的空间填充模型为
B.分子式为C4H9Cl的有机物共有4种
C.有机化合物种类繁多与碳原子的成键特点有关
D.易溶于汽油、苯等有机溶剂的物质一定是有机物
10.下列物质转化中,所用的试剂、条件不合理的是
物质转化 试剂、条件
A 浓硫酸、加热
B 浓硝酸与浓硫酸、50~60℃
C 苯→溴苯 液溴、铁粉
D Na
A.A B.B C.C D.D
11.在一次有机化学课堂小组讨论中,某同学设计了下列合成路线,你认为不可行的是
A.用氯苯合成环己烯:
B.用甲苯合成苯甲醇:
C.用乙炔合成聚氯乙烯:C2H2CH2=CHCl
D.用乙烯合成乙二醇:H2C=CH2CH3CH3CH2ClCH2ClHOCH2CH2OH
12.金银花能提取出有很高药用价值的绿原酸(如图),下列说法错误的是
A.绿原酸的分子式为C16H18O9
B.1mol绿原酸最多能消耗NaOH 8 mol
C.绿原酸分子中含4个手性碳原子
D.能发生取代、加成、消去、缩聚、加聚反应
13.某化妆品的组分Z具有美白功效,原来从杨树中提取,现可用如下反应制备。下列有关叙述不正确的是
A.Y的苯环上二氯代物共有6种
B.X、Y和Z均能使酸性高锰酸钾溶液褪色
C.X、Y和Z分子中所有原子都可能处于同一平面
D.X、Y都可作为单体发生聚合反应生成高分子
二、非选择题(共10题)
14.请回答下列问题:
(1)今有化合物甲:;乙:;丙:
①请写出丙中含氧官能团的名称:_______、_______。
②请判别上述哪些化合物互为同分异构体:_______。
③请分别写出鉴别甲、乙、丙化合物的方法(指明所选试剂及主要现象即可)。鉴别甲的方法:_______。鉴别乙的方法:_______。鉴别丙的方法:_______。
④请按酸性由强至弱排列甲、乙、丙的顺序:_______。
(2)①肉桂醛由C、H、O三种元素组成,且质谱分析肉桂醛分子的相对分子质量为132,其分子中碳、氢、氧三种元素的质量比为27:2:4.则肉桂醛的分子式是_______。肉桂醛可视为苯的一取代物,核磁共振氢谱显示,苯环侧链上有三种不同化学环境的氢原子,其结构简式是_______。(不考虑顺反异构)
②肉桂醛能被银氨溶液氧化,再经酸化得到肉桂酸。写出肉桂醛被银氨溶液氧化的反应方程式_______。
15.氯吡格雷是一种用于预防和治疗因血小板高聚集引起的心、脑及其他动脉循环障碍疾病的药物。以2-氯苯甲醛为原料合成该药物的路线如下:
(1)A中官能团的名称为___________,
(2)X(C6H7BrS)的结构简式为___________。
16.根据所学有机化学基础知识,请回答下列问题:
(1)酚酞是常用的酸碱指示剂,其结构简式为如图,所含官能团名称是_______。
(2)乙酸乙酯是一种人造香精,写出实验室制乙酸乙酯的方程式:_______。
(3)高分子化合物单体的结构简式为_______。
(4)以乙烯为原料,经两步反应可制得用途广泛的乙二醇,请写出这两步反应的化学方程式:_______、_______。
三、实验题
17.钴是一种中等活泼金属,化合价为+2价和+3价。某校同学利用下列装置检验(CH3COO)2Co在氮气气氛中的分解产物。已知PdCl2溶液能被CO还原为Pd。
(1)装置E、F是用于检验CO和CO2的,其中盛放PdCl2溶液的是装置______(填“E”或“F”)。
(2)装置G的作用是______;E、F、G中的试剂均足量且充分反应,观察到I中氧化铜变红,J中固体由白色变蓝色,K中石灰水变浑浊,则可得出的结论是______。
(3)实验结束时,先熄灭D和I处的酒精灯,一段时间后再关闭弹簧夹,其目的是______。
(4)若乙酸钴最终分解生成固态氧化物X、CO、CO2、C2H6,且n(X):n(CO):n(CO2):n(C2H6)=1:4:2:3(空气中的成分不参与反应),则乙酸钴在空气气氛中分解的化学方程式为______。
18.现有分子式均为C3H6O2的四种有机物A、B、C、D,且分子中均含甲基,把它们分别进行下列实验以鉴别之,其实验记录如下:
NaOH溶液 银氨溶液 新制Cu(OH)2 金属钠
A 中和反应 ----------- 溶解 产生氢气
B ----------- 有银镜 加热后有红色沉淀 产生氢气
C 水解反应 有银镜 加热后有红色沉淀 -----------
D 水解反应 ----------- ----------- -----------
(1)B分子中官能团的名称是:____________
(2)B、C的结构简式分别为:B_________________,C_________________。
(3)D在NaOH溶液中反应的化学方程式为______________________________。
(4)写出B与银氨溶液反应的化学方程式:_______________________________。
(5)属于A的同系物且比A少一个碳原子的物质E的同分异构体有(写结构简式)____________________。
四、计算题
19.一定质量的甲烷燃烧后得到的产物为CO、CO2和水蒸气,此混合气体质量为49.6g,当其缓慢经过无水CaCl2时,CaCl2增重25.2g,计算:
(1)参加反应的甲烷的物质的量为_______mol
(2)生成的CO的质量为_______g。
20.某仅由碳、氢、氧三种元素组成的有机化合物,经测定其相对分子质量为180。取有机物样品1.8g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.08g和2.64g。试求该有机物的分子式_____。
21.化合物F是一种重要的有机合成中间体,它的合成路线如图:
(1)化合物F中含氧官能团的名称是______和______,由A生成B的化学反应类型是______;
(2)写出化合物B的结构简式:______;
(3)写出化合物C与乙酸反应生成酯的化学方程式:______;
(4)某化合物是D的同分异构体,且分子中只有三种不同化学环境的氢。写出该化合物的结构简式:______(任写一种);
22.某兴趣小组对化合物X开展探究实验。
其中:常温常压下ⅹ是一种有特殊气味、易挥发的无色液体,由三种常见的短周期元素组成。
请回答:
(1)组成X的3种元素是_______(填元素符号),沉淀C的化学式是_______。
(2)X反应生成A和B的反应方程式是_______。
(3)B可与乙醇以物质的量之比1∶2发生取代反应生成一种酯,写出反应方程式_______。
(4)实验室保存少量物质X的仪器是_______。
A.无色广口瓶 B.棕色广口瓶 C.无色细口瓶 D.棕色细口瓶
(5)请设计一种不同于上述流程的实验方案,检验中相对原子质量最大的元素_______。
23.物质F是一种芳香酯,常用作调香剂,其合成路线如下图所示:
已知E中含有两个甲基,请回答下列问题:
(1)物质A的名称是_______。
(2)各取1 mol物质D分别与足量Na、NaOH溶液、NaHCO3溶液反应,消耗的Na、NaOH、NaHCO3的物质的量之比为_______。
(3)物质A到F中除D以外含有手性碳原子的物质是_______(填标号)。
(4)B→C的反应方程式是_______。
(5)E的同分异构体中与其含有相同种类官能团的有_______种(不含E本身)。
参考答案:
1.A 2.B 3.C 4.C 5.D 6.C 7.A 8.A 9.D 10.A 11.D 12.B 13.C
14.(1) 羟基 醛基 甲、乙、丙 加入三氯化铁溶液,溶液显紫色的为甲 加入紫色石蕊试液,溶液呈红色,则为乙 加入银氨溶液或新制的Cu(OH)2,若有银镜出现或红色的沉淀生成的则为丙 乙>甲>丙
(2) C9H8O C6H5CH=CHCHO+2Ag(NH3)2OH2Ag↓+H2O+3NH3+C6H5CH=CHCOONH4
15.(1)醛基、氯原子
(2)
16.(1)羟基、酯基
(2)CH3COOH+C2H5OHCH3COOCH2CH3+H2O
(3) 和CH2=CH-CH3
(4) CH2=CH2+Br2→BrCH2CH2Br BrCH2CH2Br+2NaOHHOCH2CH2OH+2NaBr
17. F 除去CO2 分解产物中还含有机物 防止倒吸 3(CH3COO)2CoCo3O4+4CO↑+2CO2↑+3C2H6↑
18. 羟基、醛基 CH3CH(OH)CHO HCOOCH2CH3 CH3COOCH3+NaOHCH3COONa+CH3OH CH3CH(OH)CHO+2Ag(NH3)2OHCH3CH(OH)COONH4+2Ag+3NH3+H2O CH3COOH
19. 0.7 11.2
20.C6H12O6
21. 醛基 羰基 取代反应 CH3COOH+ + H2O
22. C、H、 D 取少量Ⅹ于试管中,加入适量溶液并加热。冷却后加足量稀酸化,再加入溶液,生成白色沉淀,证明ⅹ中含有氯元素
23. 2-甲基-1-丁烯 2:1:1 BC 7
