第2章《官能团与有机化学反应烃的衍生物》练习卷(含解析)2022-2023学年下学期高二化学鲁科版(2019)选择性必修3
文档属性
| 名称 | 第2章《官能团与有机化学反应烃的衍生物》练习卷(含解析)2022-2023学年下学期高二化学鲁科版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 533.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-26 00:00:00 | ||
图片预览




文档简介
第2章《官能团与有机化学反应 烃的衍生物》练习卷
一、单选题
1.下列化学方程式书写正确的是( )
A.
B.
C.
D.
2.下列物质的除杂方法中,能实现目的的是
选项 物质(杂质) 方法
A CO2 (CO) 点燃
B C2H4(SO2) 通过酸性高锰酸钾溶液
C CH3COOC2H5(CH3COOH) 加入饱和Na2CO3溶液充分振荡,分液
D Fe2O3(Al2O3) 加氨水充分反应,过滤
A.A B.B C.C D.D
3.下列说法不正确的是
A.油脂可以用来制造肥皂和油漆
B.在一定条件下,苯酚与甲醛反应生成酚醛树脂
C.向淀粉的水解液中加入碘水,溶液变蓝,不能说明淀粉未水解
D.氨基酸在溶液中的存在形态与酸碱性有关,当以两性离子存在时,其在水中的溶解度最大
4.庆祝中国共产党成立100周年大会上,总书记宣告中华大地全面建成了小康社会。化学科研人员在科技强国道路上作出了巨大贡献。下列有关化学与生产生活、科研的说法正确的是
A.白砂糖做成“棉花糖”就成了高分子化合物——多糖
B.FeCl3溶液具有酸性,可用于镀覆层前的钢铁除锈
C.氯化钙、活性炭以及硅藻上、铁粉都是食品包装袋中常见的干燥剂
D.我国发射的“嫦娥五号”球探测器中使用的碳纤维是种新型有机高分子材料
5.下列反应中,属于加成反应的是
A.
B.
C.
D.
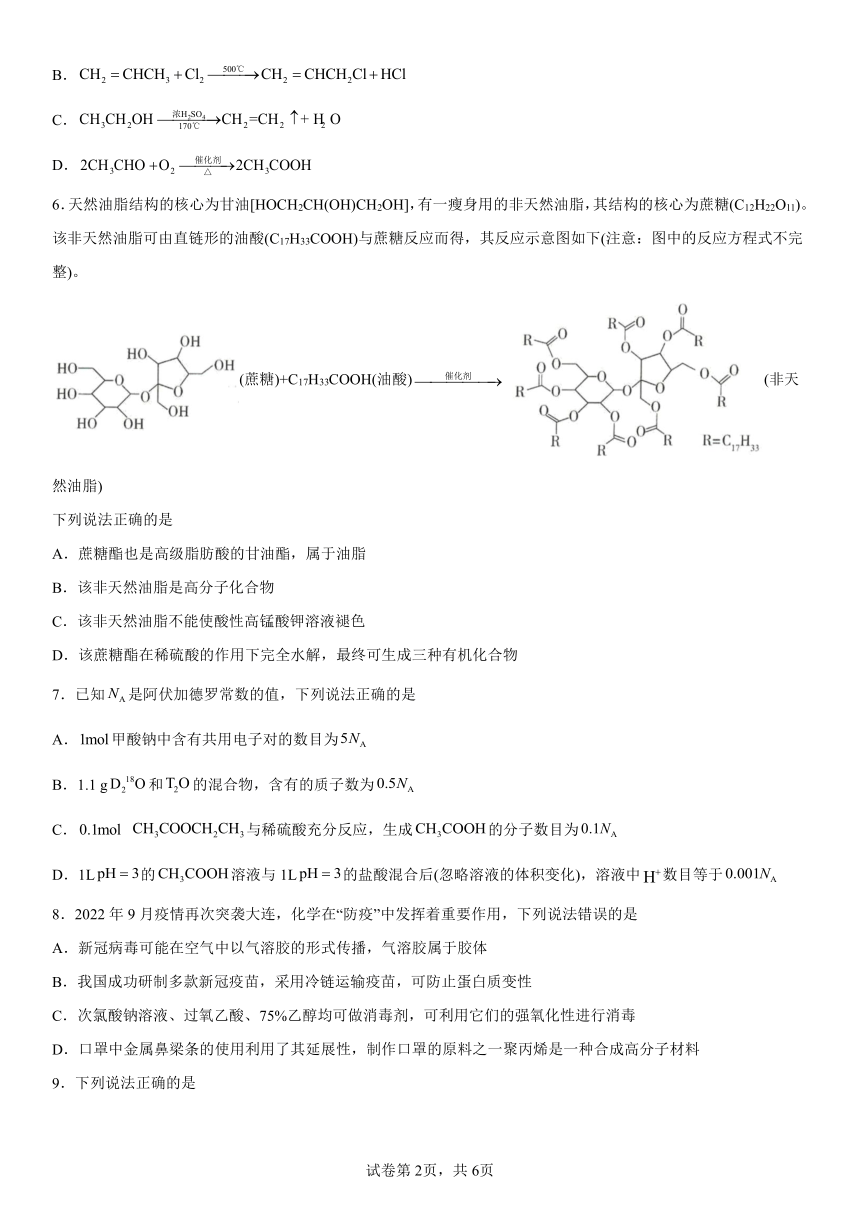
6.天然油脂结构的核心为甘油[HOCH2CH(OH)CH2OH],有一瘦身用的非天然油脂,其结构的核心为蔗糖(C12H22O11)。该非天然油脂可由直链形的油酸(C17H33COOH)与蔗糖反应而得,其反应示意图如下(注意:图中的反应方程式不完整)。
(蔗糖)+C17H33COOH(油酸) (非天然油脂)
下列说法正确的是
A.蔗糖酯也是高级脂肪酸的甘油酯,属于油脂
B.该非天然油脂是高分子化合物
C.该非天然油脂不能使酸性高锰酸钾溶液褪色
D.该蔗糖酯在稀硫酸的作用下完全水解,最终可生成三种有机化合物
7.已知是阿伏加德罗常数的值,下列说法正确的是
A.甲酸钠中含有共用电子对的数目为
B.1.1 g和的混合物,含有的质子数为
C. 与稀硫酸充分反应,生成的分子数目为
D.1L的溶液与1L的盐酸混合后(忽略溶液的体积变化),溶液中数目等于
8.2022年9月疫情再次突袭大连,化学在“防疫”中发挥着重要作用,下列说法错误的是
A.新冠病毒可能在空气中以气溶胶的形式传播,气溶胶属于胶体
B.我国成功研制多款新冠疫苗,采用冷链运输疫苗,可防止蛋白质变性
C.次氯酸钠溶液、过氧乙酸、75%乙醇均可做消毒剂,可利用它们的强氧化性进行消毒
D.口罩中金属鼻梁条的使用利用了其延展性,制作口罩的原料之一聚丙烯是一种合成高分子材料
9.下列说法正确的是
A.、 是同系物
B.用溴水或酸性高锰酸钾溶液均可鉴别乙醇、苯、、苯酚、乙酸
C.乙酸、硬脂酸都属于羧酸,且互为同系物;丙烯酸、油酸也互为同系物
D.有机物既能发生消去反应,也能发生催化氧化反应
10.下列实验对应的离子反应方程式正确的是
A.二氧化硫使酸性高锰酸钾溶液褪色:
B.将去膜的铝片投入到NaOH溶液中:
C.溶液中通入少量:
D.粗铜电解精炼(粗铜作阳极,溶液作电解液)的总反应式:
二、填空题
11.有下列三种与环境有关的物质:①SO2、②HCHO(甲醛)、③氟利昂,请按要求填空:
①由某些装修材料造成居室污染的主要物质是_______ (填序号)
②破坏臭氧层的主要物质是_______ (填序号)
12.A、B、C都是芳香化合物,可用于制作药物、香料等。
(1)上述物质互为同分异构体的是___________(填序号)。
(2)B中的含氧官能团是___________。
(3)与NaHCO3、NaOH和Na都能反应的是___________(填序号)。
13.(1)关注营养平衡和正确使用药物,有利于身心健康。现有下列四种物质:
A.淀粉 B.维生素C C.青霉素 D.胃舒平
请根据题意,选择恰当的选项用字母代号填空。
①属于治疗“胃酸过多症”的抗酸药的是_______;
②存在于蔬菜、水果中,具有还原性的物质是______;
③存在于土豆、谷类等植物中,遇碘水显蓝色的物质是_______;
④属于抗生素类药,有阻止多种细菌生长的功能,该物质是______。
(2)水是一种宝贵的自然资源。
①排放含____ (填字母代号)的化合物会导致水体富营养化;
A.磷 B.硫 C.铁 D.碳
②下列做法不会造成水污染的是_____(填字母代号)。
A 生活污水任意排放 B.油轮原油泄漏 C.水力发电 D.大量施用农药
③向含镉离于(Cd2+)的废水中加入Na2S以除去镉离子,该反应的离子方程式为_______。
(3)材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活。
①下列几种生活中常见的物质中,组成成分属于合金的是____(填字母代号》。
A.铜导线 B 玻璃 C.硬铝窗框架
②化石能源是有限的,目前人类正面临着能源短缺的问题,开发,利用太阳能和风能等新能源是解决能源短缺问题的重要措施。下列不属于化石能源的物质是____(填字母代号)。
A.木材 B.石油 C.煤
③微型理碘电池可用于植入某此心脏病人体内的心脏起搏器所用的电源。这种电池中的电解质是固体电解质LiI,总反应是2Li +I2=2LiI,该电池的负极是_______。
14.蛋白质变性属于化学变化。(_______)
三、计算题
15.一个碳原子上如果连有3个氢原子,则这样的氢原子称为伯氢,如果只连有2个氢原子,则这样的氢称为仲氢,例如:-CH3中的氢原子为伯氢,-CH2-中的氢原子为仲氢。已知在烷烃中伯氢和仲氢被取代的活性因反应的条件不同而不同。在高温下伯氢与仲氢被取代的活性相等,则可以称之活性比为1︰1。请回答下列问题:
(1)已知丙烷在高温下与氯气发生取代反应,反应式如下:
则在一氯代丙烷中1-氯丙烷在产物中的占有率为_______;
(2)常温下丙烷也能与氯气发生取代反应,反应式如下:
则在常温下伯氢和仲氢的相对活性比为_______。
16.填空
(1)下列物质中,互为同位素的有_______,互为同素异形体的有_______,互为同系物的有_______,互为同分异构体的有_______,属于同种物质有_______。
①O2和O3②35Cl和37Cl③和④+和⑤CH3(CH2)2CH3和(CH3)2CHCH3⑥乙醇和甲醚(CH3OCH3)
(2)立方烷结构为,它的结构高度对称,其二氯代物有_______种。
(3)化合物甲只含C、H两种元素,化合物乙只含C、H、F三种元素,甲、乙都是饱和化合物,且分子中都含有26个电子,据此推断:
①甲的分子式是_______;若甲分子中有两个H原子被F原子代替,所得产物可能有_______种结构。
②乙是性能优异的环保产品,可替代某些会破坏臭氧层的氟里昂产品,用作制冷剂。已知乙分子中C、H、F原子个数比为1∶2∶2,则下列对于乙的描述正确的是_______
A.其分子空间构型为正四面体 B.碳为sp3杂化
C.具有两种同分异构体 D.没有同分异构体
17.链状有机物X由C、H、O三种元素组成,0.1molX在氧气中完全燃烧后,生成CO2的体积为6.72L(标准状况),生成H2O的质量为3.6g。0.1molX与足量钠反应,产生气体的体积为3.36L(标准状况)。请确定摩尔质量最小的X的分子式和结构简式____(要求写出简要推理过程。已知: 和 结构不稳定)。
四、有机推断题
18.一种药物中间体H()的合成路线如图:
已知:R—OH+R′—FR—O—R′+HF。
请回答下列问题:
(1)写出E的结构简式:____,若检测该步骤产品中是否残留E,可使用的检验试剂是____。
(2)已知氯原子是邻位和对位取代定位基,—NO2则是间位取代定位基,那么A→B为了提高B的产率,需要先进行____反应(填“氯代”或“硝化”)。
(3)已知C的结构为,比较NaCl晶体与化合物C熔点较高的是____,理由是____。
(4)F→G的反应类型为____。
(5)G→H的化学方程式为____。
(6)K比D分子组成多1个C原子和2个H原子,则满足下列条件的K有____种。
①红外光谱显示,—F都与苯环直接相连且含有—NH2
②能与NaHCO3反应放出气体
19.常见有机物A、B、C、D、E的相互转化关系如图所示。已知D是有香味且不溶于水的油状液体:E的产量可以用来衡量一个国家的石油化工发展水平;。
请回答下列问题:
(1)E的电子式_______。
(2)B的结构简式是_______。
(3)反应①的化学方程式是_______。
(4)下列说法正确的是_______(填序号)。
a.E分子中所有原子在同一平面上
b.用饱和溶液除去D中混有的C
c.②的反应类型为取代反应
(5)由E反应制A的化学方程式_______。
(6)A生成B的化学方程式_______。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
【详解】A.乙烯加聚反应生成,A正确;
B.乙烯与溴反应生成CH2BrCH2Br,B错误;
C.该反应生成硝基苯,结构简式为,C错误;
D.该反应生成乙酸乙酯,结构简式为CH3COOCH2CH3,D错误;
故选A。
2.C
【详解】A.二氧化碳不燃烧,也不支持燃烧,二氧化碳中混有少量一氧化碳无法点燃,且使用点燃的方法容易引入新的杂质气体,A错误;
B.乙烯含有碳碳双键,会和高锰酸钾反应,B错误;
C.乙酸乙酯在饱和碳酸钠溶液中溶解度较小,乙酸和碳酸钠反应生成乙酸钠,分液可以分离出乙酸乙酯,C正确;
D.两者都不和氨水反应,不能用于除杂,D错误;
故选C。
3.D
【详解】A.油脂是高级脂肪酸的甘油酯,加入色料可制油漆,通过皂化反应可制肥皂,A项正确;
B.在一定条件下,苯酚与甲醛发生缩聚反应生成酚醛树脂,B项正确;
C.向淀粉的水解液中加入碘水,溶液变蓝,只能说明溶液中含有淀粉,不能说明淀粉未水解,C项正确;
D.在酸性条件下,氨基酸以阳离子形态存在,在碱性条件下,氨基酸以阴离子形态存在,当以两性离子存在时,其在水中的溶解度最小,D项错误;
答案选D。
4.B
【详解】A.白砂糖的主要成分是蔗糖,做成“棉花糖”是状态的变化,仍然是小分子,A错误;
B.氯化铁水解使溶液呈酸性,可用于镀覆层前的钢铁除锈,B正确;
C.活性炭不具有吸水性,不能作干燥剂,铁粉具有还原性,可用作食品抗氧化剂,不作干燥剂,C错误;
D.碳纤维是一种新型无机材料,是单质,不是高分子材料,D错误;
答案选B。
5.A
【详解】A.乙醛中碳氧双键与氢气发生加成反应,A正确;
B.甲基上的氢原子被取代,属于取代反应,B错误;
C.乙醇发生消去反应生成乙烯,属于消去反应,C错误;
D.乙醛中醛基被氧化生成乙酸,为氧化反应,D错误;
故选A。
6.D
【详解】A.蔗糖酯是由高级脂肪酸与蔗糖形成的酯,而油脂是高级脂肪酸与甘油形成的酯,故蔗糖酯不属于油脂,A错误;
B.该非天然油脂的相对分子质量较大,但不是高分子化合物,B错误;
C.该非天然油脂可由直链形的油酸和蔗糖发生酯化反应而得,油酸分子中含有碳碳双键,故该非天然油脂能使酸性KMnO4溶液褪色,C错误;
D.该蔗糖酯在稀硫酸作用下水解生成油酸和蔗糖,而蔗糖还可水解生成葡萄糖和果糖,因此该蔗搪酯水解的最终产物为油酸、葡萄糖和果糖,D正确;
答案选D。
7.B
【详解】A.甲酸钠中C和H之间共用一对电子,C和O双键之间共用两对电子,C和O单键之间共用一对电子,甲酸根和钠离子之间是离子键,故甲酸钠中含有共用电子对的数目为,A错误;
B.和的摩尔质量均为22 g/mol,1.1 g混合物的物质的量为0.05 mol,每个和分子均含有10个质子,故1.1g和的混合物,含有的质子数为,B正确;
C.在酸性条件下的水解为可逆反应,生成的的分子数目小于,C错误;
D.1L的溶液与1L的盐酸混合后pH仍然等于3,则,溶液中数目等于,D错误;
故选B。
8.C
【详解】A. 胶体按分散剂的状态可分为固溶胶、液溶胶、气溶胶,故气溶胶属于胶体,A项正确;
B. 温度过高会使蛋白质变性,病毒疫苗主要成分含蛋白质,为防止其变性,一般需要冷藏保存,B项正确;
C. 次氯酸钠溶液、过氧乙酸具有强氧化性,能够杀菌消毒,、75%乙醇能使蛋白质变性,可做消毒剂,C项错误;
D. 聚丙烯属于合成有机高分子化合物,D项正确;
故选C。
9.C
【详解】A.属于酚,属于醇,两者结构不相似,不是同系物,A错误;
B.溴水不能鉴别乙醇和乙酸,酸性高锰酸钾溶液不能鉴别乙醇和苯酚,B错误;
C.乙酸CH3COOH、硬脂酸C17H35COOH都是饱和一元羧酸,二者结构相似,组成上相差16个CH2,二者互为同系物,丙烯酸CH2=CHCOOH和油酸C17H33COOH,分子中都含有一个羧基和一个碳碳双键,二者结构相似,组成上相差15个CH2,二者互为同系物,C正确;
D.若有机物的结构简式为C(CH3)3OH,则不能发生催化氧化反应,D错误;
答案选C。
10.B
【详解】A.电荷不守恒,SO2使酸性KMnO4溶液褪色的离子方程式为5SO2+2+2H2O=5+2Mn2++4H+,A错误;
B.Al与NaOH溶液反应生成Na[Al(OH)4]和H2,反应的离子方程式为2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑,B正确;
C.C6H5ONa与少量CO2反应生成苯酚和NaHCO3,反应的离子方程式为C6H5O-+CO2+H2O→C6H5OH+,C错误;
D.粗铜电解精炼时,粗铜作阳极,粗铜中比Cu活泼的金属如Zn、Fe等优先在阳极放电,阳极电极反应有:Zn-2e-=Zn2+、Fe-2e-=Fe2+、Cu-2e-=Cu2+,精铜为阴极,阴极电极反应为Cu2++2e-=Cu,D错误;
答案选B。
11. ② ③
【详解】①装修材料造成居室污染主要因为其能产生HCHO(甲醛),故选②;
②氟利昂会破坏臭氧层,产生臭氧空洞,故选③。
12.(1)A和C
(2)醛基
(3)A
【分析】(1)
上述物质互为同分异构体的是A和C(填序号)分子式均为C8H8O2,而B的分子式为C9H8O。故答案为:A和C;
(2)
B中的含氧官能团-CHO是醛基。故答案为:醛基;
(3)
与NaHCO3、NaOH和Na都能反应的是A(填序号),B与NaHCO3、NaOH和Na均不反应,C与NaHCO3不反应,故答案为:A。
13. D B A C A C Cd2+ +S2- =CdS↓ C A 锂(或Li)
【详解】(1)①胃舒平(通用名:复方氢氧化铝)有中和胃酸,减少胃液分泌和解痉止疼的作用。故属于治疗“胃酸过多症”的抗酸药的是胃舒平,答案选D;②存在于蔬菜、水果中,具有还原性的物质是维生素C,答案选B;③存在于土豆、谷类等植物中,遇碘水显蓝色的物质是淀粉,答案选A;④属于抗生素类药,有阻止多种细菌生长的功能,该物质是青霉素,答案选C;(2)①排放含磷的化合物会导致水体富营养化,答案选A;②工农业生产用了被污染的水,会降低产品的质量,损害人类的健康.那么污染水的因素有那些呢?工业生产中的废渣、废水、废气和生活污水的任意排放,农业生产中农药、化肥不合理使用会随雨水流入河中,原油泄漏都会使水受到污染,因此保护水资源,人人有责。本题中ABD均能造成水质严重污染,所以应严加管理。答案选C;③向含镉离于(Cd2+)的废水中加入Na2S生成CdS以除去镉离子,该反应的离子方程式为Cd2+ +S2- =CdS↓;(3)①A.铜导线 属于单质,选项A不符合;B 玻璃属于无机非金属材料,选项B不符合;C.硬铝窗框架属于铝合金材料,选项C符合。答案选C;②三大化石能源是指煤、石油、天然气,木材不属于化石能源,答案选A;③电池中的电解质是固体电解质LiI,总反应是2Li +I2=2LiI,活泼金属作为负极,故电池的负极是锂(或Li)。
14.正确
【解析】略
15.(1)75%
(2)1︰4
【详解】(1)丙烷分子中含有6个伯氢、2个仲氢,而1-氯丙烷取代的是伯氢,2-氯丙烷取代的是仲氢,因此在一氯代丙烷中1-氯丙烷在产物中的占有率为;
故答案为:75%;
(2)丙烷分子中含有6个伯氢、2个仲氢,而1-氯丙烷取代的是伯氢,2-氯丙烷取代的是仲氢,由于在常温下1-氯丙烷是43%,2-氯丙烷是57%,设在常温下伯氢和仲氢的相对活性比为x:y,则,解得x:y=1:4;
故答案为:。
16.(1) ② ① ③ ⑤⑥ ④
(2)3
(3) C3H8 4 BD
【详解】(1)①氧气和臭氧是氧元素形成的不同种单质,互为同素异形体;
②35Cl和37Cl的质子数相同、中子数不同,互为同位素;
③2—甲基丙烷和2—甲基丁烷的结构相似,相差1个CH2原子团,互为同系物;
④由结构式可知,两种结构都为二氯甲烷,是同种物质;
⑤丁烷和异丁烷的分子式相同,结构不同,互为同分异构体;
⑥乙醇和甲醚的分子式相同,结构不同,互为同分异构体;
则互为同位素的为②,互为同素异形体的为①,互为同系物的为③,互为同分异构体的为⑤⑥,属于同种物质的为④,故答案为:②;①;③;⑤⑥;④;
(2)由结构简式可知,立方烷的一氯代物有1种,二氯代物有3种,故答案为:3;
(3)由甲为只含C、H两种元素的饱和化合物可知,甲为烷烃,设甲的分子式为CnH2n+2,由分子中含有26个电子可得:6n+2n+2=26,解得n=3,则甲的分子式为C3H8;由化合物乙为只含C、H、F三种元素的饱和化合物可知,乙为氟代烃,设乙的分子式为CnH2n+2—xFx,由分子中含有26个电子可得:6n+(2n+2—x)+9x=26,由乙分子中C、H、F原子个数比为1∶2∶2可得n∶x=1∶2,解得n=1、x=2,则乙的分子式为CH2F2;
①由分析可知,甲的分子式为C3H8;丙烷的一氟代物有1—氟丙烷和2—氟丙烷,共2种,其中1—氟丙烷分子和2—氟丙烷分子中氢原子被氟原子取代所得结构有4种,分别为CH3CH2CHF2、CH3CF2CH3、CH2FCHFCH3、CH2FCH2CH2F,故答案为:C3H8;4;
②由分析可知,乙的分子式为CH2F2,名称为二氟甲烷;
A.二氟甲烷分子中碳氢键和碳氟键的键长不同,的空间构型为四面体形,不是正四面体形,故错误;
B.二氟甲烷分子中饱和碳原子的杂化方式为sp3杂化,故正确;
C.甲烷分子的空间构型为四面体形,二氟甲烷分子不存在同分异构体,故错误;
D.甲烷分子的空间构型为四面体形,二氟甲烷分子不存在同分异构体,故正确;
故选BD。
17.C3H4O5、
【详解】由0.1molX在氧气中完全燃烧后,生成CO2的体积为6.72L(标准状况),生成H2O的质量为3.6g 可知,X分子在含有的碳原子个数为==3,含有氢原子的个数为==4,由0.1molX与足量钠反应,产生气体的体积为3.36L(标准状况)可知,分子中含有的羟基数目为==3,由碳、氢原子的个数可知,X分子的不饱和度为2,由 、 结构不稳定和X分子为链状可知,X分子中含有2个—COOH和1个—OH ,则分子式为C3H4O5,结构简式为 ,故答案为:C3H4O5、 。
18.(1) 酸性高锰酸钾(KMnO4)、氯化铁(FeCl3)溶液、溴水等
(2)氯代
(3) NaCl 离子化合物的熔点在离子电荷相同的条件下,离子半径越大,熔点越低。化合物C中阴阳离子半径较大,熔点低。或NaCl离子半径比化合物C小,熔点高
(4)还原反应
(5)+CH3COCl→ +HCl
(6)16
【分析】A先和液氯发生取代反应,再发生硝化反应得到B,B再经系列反应生成C,C再反应生成D,对比D和F的结构简式可知,D中硝基临位的F原子被-OC5H6取代生成F,再根据题目所给信息可知,E的结构简式应为;F中硝基被还原为氨基生成G,G中氨基和CH3COCl发生取代反应生成H。
(1)
F与D相比较多了苯氧基,再结合已知条件,得出E为苯酚;检验苯酚残留可以用FeCl3溶液遇苯酚发生显色反应;也可以用溴水,即使三溴苯酚在有机物中看不到沉淀,也能使溴颜色消失。
(2)
氯原子是邻位和对位取代定位基,-NO2则是间位取代定位基,-NO2处在氯原子对位,需要先进行氯代再硝化;
(3)
熔点较高的是NaCl,因为离子化合物的熔点在离子电荷相同的条件下,离子半径越大,熔点越低,C中阴阳离子半径较大,故熔点低。
(4)
有机物加氢去氧是还原,F→G硝基变成了氨基,反应类型为还原反应;
(5)
G→H的化学方程式为+CH3COCl→ +HCl;
(6)
K比D分子组成多1个C原子和2个H原子,满足①红外光谱显示,-F都与苯环直接相连且含有-NH2,②能与NaHCO3反应放出气体说明其含有-COOH,即苯环连两个-F,一个-NH2一个-COOH:、、、、、,共16种。
19.(1)
(2)CH3CHO
(3)CH3COOH+C2H5OHCH3COOC2H5+H2O
(4)ab
(5)CH2=CH2 + H2OCH3CH2OH
(6)2CH3CH2OH+O22CH3CHO+2H2O
【分析】D是有香味且不溶于水的油状液体,依据D的分子式,可确定D为CH3COOC2H5;E的产量可以用来衡量一个国家的石油化工发展水平,则E为CH2=CH2;A经两次氧化生成同碳原子数的C,则A为醇、C为羧酸,再由D的结构简式,可确定A是CH3CH2OH,B是CH3CHO,C是CH3COOH。
(1)
E为乙烯,电子式为 ,答案为;
(2)
由以上分析知,B的结构简式是CH3CHO。答案为:CH3CHO;
(3)
反应①是乙醇与乙酸在浓硫酸存在并加热的条件下发生酯化反应,生成乙酸乙酯和水,该反应为可逆反应,反应的化学方程式是CH3COOH+C2H5OHCH3COOC2H5+H2O。答案为:CH3COOH+C2H5OHCH3COOC2H5+H2O;
(4)
a.E是乙烯,分子中所有原子在同一平面上,a正确;
b.乙酸乙酯难溶于碳酸钠溶液,密度比碳酸钠溶液小,而乙酸能够与碳酸钠溶液反应生成乙酸钠、水和二氧化碳,因此可用饱和Na2CO3溶液除去乙酸乙酯中混有的乙酸,b正确;
c.②的反应为乙酸与乙烯发生的加成反应,c错误;
故选ab。答案为:ab。
(5)
由分析可知E为乙烯,A为乙醇,乙烯和水加成可以得到乙醇,方程式为:CH2=CH2 + H2OCH3CH2OH ;
(6)
由分析可知A为乙醇,B为CH3CHO,乙醇催化氧化得到乙醛,方程式为:2CH3CH2OH+O22CH3CHO+2H2O。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列化学方程式书写正确的是( )
A.
B.
C.
D.
2.下列物质的除杂方法中,能实现目的的是
选项 物质(杂质) 方法
A CO2 (CO) 点燃
B C2H4(SO2) 通过酸性高锰酸钾溶液
C CH3COOC2H5(CH3COOH) 加入饱和Na2CO3溶液充分振荡,分液
D Fe2O3(Al2O3) 加氨水充分反应,过滤
A.A B.B C.C D.D
3.下列说法不正确的是
A.油脂可以用来制造肥皂和油漆
B.在一定条件下,苯酚与甲醛反应生成酚醛树脂
C.向淀粉的水解液中加入碘水,溶液变蓝,不能说明淀粉未水解
D.氨基酸在溶液中的存在形态与酸碱性有关,当以两性离子存在时,其在水中的溶解度最大
4.庆祝中国共产党成立100周年大会上,总书记宣告中华大地全面建成了小康社会。化学科研人员在科技强国道路上作出了巨大贡献。下列有关化学与生产生活、科研的说法正确的是
A.白砂糖做成“棉花糖”就成了高分子化合物——多糖
B.FeCl3溶液具有酸性,可用于镀覆层前的钢铁除锈
C.氯化钙、活性炭以及硅藻上、铁粉都是食品包装袋中常见的干燥剂
D.我国发射的“嫦娥五号”球探测器中使用的碳纤维是种新型有机高分子材料
5.下列反应中,属于加成反应的是
A.
B.
C.
D.
6.天然油脂结构的核心为甘油[HOCH2CH(OH)CH2OH],有一瘦身用的非天然油脂,其结构的核心为蔗糖(C12H22O11)。该非天然油脂可由直链形的油酸(C17H33COOH)与蔗糖反应而得,其反应示意图如下(注意:图中的反应方程式不完整)。
(蔗糖)+C17H33COOH(油酸) (非天然油脂)
下列说法正确的是
A.蔗糖酯也是高级脂肪酸的甘油酯,属于油脂
B.该非天然油脂是高分子化合物
C.该非天然油脂不能使酸性高锰酸钾溶液褪色
D.该蔗糖酯在稀硫酸的作用下完全水解,最终可生成三种有机化合物
7.已知是阿伏加德罗常数的值,下列说法正确的是
A.甲酸钠中含有共用电子对的数目为
B.1.1 g和的混合物,含有的质子数为
C. 与稀硫酸充分反应,生成的分子数目为
D.1L的溶液与1L的盐酸混合后(忽略溶液的体积变化),溶液中数目等于
8.2022年9月疫情再次突袭大连,化学在“防疫”中发挥着重要作用,下列说法错误的是
A.新冠病毒可能在空气中以气溶胶的形式传播,气溶胶属于胶体
B.我国成功研制多款新冠疫苗,采用冷链运输疫苗,可防止蛋白质变性
C.次氯酸钠溶液、过氧乙酸、75%乙醇均可做消毒剂,可利用它们的强氧化性进行消毒
D.口罩中金属鼻梁条的使用利用了其延展性,制作口罩的原料之一聚丙烯是一种合成高分子材料
9.下列说法正确的是
A.、 是同系物
B.用溴水或酸性高锰酸钾溶液均可鉴别乙醇、苯、、苯酚、乙酸
C.乙酸、硬脂酸都属于羧酸,且互为同系物;丙烯酸、油酸也互为同系物
D.有机物既能发生消去反应,也能发生催化氧化反应
10.下列实验对应的离子反应方程式正确的是
A.二氧化硫使酸性高锰酸钾溶液褪色:
B.将去膜的铝片投入到NaOH溶液中:
C.溶液中通入少量:
D.粗铜电解精炼(粗铜作阳极,溶液作电解液)的总反应式:
二、填空题
11.有下列三种与环境有关的物质:①SO2、②HCHO(甲醛)、③氟利昂,请按要求填空:
①由某些装修材料造成居室污染的主要物质是_______ (填序号)
②破坏臭氧层的主要物质是_______ (填序号)
12.A、B、C都是芳香化合物,可用于制作药物、香料等。
(1)上述物质互为同分异构体的是___________(填序号)。
(2)B中的含氧官能团是___________。
(3)与NaHCO3、NaOH和Na都能反应的是___________(填序号)。
13.(1)关注营养平衡和正确使用药物,有利于身心健康。现有下列四种物质:
A.淀粉 B.维生素C C.青霉素 D.胃舒平
请根据题意,选择恰当的选项用字母代号填空。
①属于治疗“胃酸过多症”的抗酸药的是_______;
②存在于蔬菜、水果中,具有还原性的物质是______;
③存在于土豆、谷类等植物中,遇碘水显蓝色的物质是_______;
④属于抗生素类药,有阻止多种细菌生长的功能,该物质是______。
(2)水是一种宝贵的自然资源。
①排放含____ (填字母代号)的化合物会导致水体富营养化;
A.磷 B.硫 C.铁 D.碳
②下列做法不会造成水污染的是_____(填字母代号)。
A 生活污水任意排放 B.油轮原油泄漏 C.水力发电 D.大量施用农药
③向含镉离于(Cd2+)的废水中加入Na2S以除去镉离子,该反应的离子方程式为_______。
(3)材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活。
①下列几种生活中常见的物质中,组成成分属于合金的是____(填字母代号》。
A.铜导线 B 玻璃 C.硬铝窗框架
②化石能源是有限的,目前人类正面临着能源短缺的问题,开发,利用太阳能和风能等新能源是解决能源短缺问题的重要措施。下列不属于化石能源的物质是____(填字母代号)。
A.木材 B.石油 C.煤
③微型理碘电池可用于植入某此心脏病人体内的心脏起搏器所用的电源。这种电池中的电解质是固体电解质LiI,总反应是2Li +I2=2LiI,该电池的负极是_______。
14.蛋白质变性属于化学变化。(_______)
三、计算题
15.一个碳原子上如果连有3个氢原子,则这样的氢原子称为伯氢,如果只连有2个氢原子,则这样的氢称为仲氢,例如:-CH3中的氢原子为伯氢,-CH2-中的氢原子为仲氢。已知在烷烃中伯氢和仲氢被取代的活性因反应的条件不同而不同。在高温下伯氢与仲氢被取代的活性相等,则可以称之活性比为1︰1。请回答下列问题:
(1)已知丙烷在高温下与氯气发生取代反应,反应式如下:
则在一氯代丙烷中1-氯丙烷在产物中的占有率为_______;
(2)常温下丙烷也能与氯气发生取代反应,反应式如下:
则在常温下伯氢和仲氢的相对活性比为_______。
16.填空
(1)下列物质中,互为同位素的有_______,互为同素异形体的有_______,互为同系物的有_______,互为同分异构体的有_______,属于同种物质有_______。
①O2和O3②35Cl和37Cl③和④+和⑤CH3(CH2)2CH3和(CH3)2CHCH3⑥乙醇和甲醚(CH3OCH3)
(2)立方烷结构为,它的结构高度对称,其二氯代物有_______种。
(3)化合物甲只含C、H两种元素,化合物乙只含C、H、F三种元素,甲、乙都是饱和化合物,且分子中都含有26个电子,据此推断:
①甲的分子式是_______;若甲分子中有两个H原子被F原子代替,所得产物可能有_______种结构。
②乙是性能优异的环保产品,可替代某些会破坏臭氧层的氟里昂产品,用作制冷剂。已知乙分子中C、H、F原子个数比为1∶2∶2,则下列对于乙的描述正确的是_______
A.其分子空间构型为正四面体 B.碳为sp3杂化
C.具有两种同分异构体 D.没有同分异构体
17.链状有机物X由C、H、O三种元素组成,0.1molX在氧气中完全燃烧后,生成CO2的体积为6.72L(标准状况),生成H2O的质量为3.6g。0.1molX与足量钠反应,产生气体的体积为3.36L(标准状况)。请确定摩尔质量最小的X的分子式和结构简式____(要求写出简要推理过程。已知: 和 结构不稳定)。
四、有机推断题
18.一种药物中间体H()的合成路线如图:
已知:R—OH+R′—FR—O—R′+HF。
请回答下列问题:
(1)写出E的结构简式:____,若检测该步骤产品中是否残留E,可使用的检验试剂是____。
(2)已知氯原子是邻位和对位取代定位基,—NO2则是间位取代定位基,那么A→B为了提高B的产率,需要先进行____反应(填“氯代”或“硝化”)。
(3)已知C的结构为,比较NaCl晶体与化合物C熔点较高的是____,理由是____。
(4)F→G的反应类型为____。
(5)G→H的化学方程式为____。
(6)K比D分子组成多1个C原子和2个H原子,则满足下列条件的K有____种。
①红外光谱显示,—F都与苯环直接相连且含有—NH2
②能与NaHCO3反应放出气体
19.常见有机物A、B、C、D、E的相互转化关系如图所示。已知D是有香味且不溶于水的油状液体:E的产量可以用来衡量一个国家的石油化工发展水平;。
请回答下列问题:
(1)E的电子式_______。
(2)B的结构简式是_______。
(3)反应①的化学方程式是_______。
(4)下列说法正确的是_______(填序号)。
a.E分子中所有原子在同一平面上
b.用饱和溶液除去D中混有的C
c.②的反应类型为取代反应
(5)由E反应制A的化学方程式_______。
(6)A生成B的化学方程式_______。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
【详解】A.乙烯加聚反应生成,A正确;
B.乙烯与溴反应生成CH2BrCH2Br,B错误;
C.该反应生成硝基苯,结构简式为,C错误;
D.该反应生成乙酸乙酯,结构简式为CH3COOCH2CH3,D错误;
故选A。
2.C
【详解】A.二氧化碳不燃烧,也不支持燃烧,二氧化碳中混有少量一氧化碳无法点燃,且使用点燃的方法容易引入新的杂质气体,A错误;
B.乙烯含有碳碳双键,会和高锰酸钾反应,B错误;
C.乙酸乙酯在饱和碳酸钠溶液中溶解度较小,乙酸和碳酸钠反应生成乙酸钠,分液可以分离出乙酸乙酯,C正确;
D.两者都不和氨水反应,不能用于除杂,D错误;
故选C。
3.D
【详解】A.油脂是高级脂肪酸的甘油酯,加入色料可制油漆,通过皂化反应可制肥皂,A项正确;
B.在一定条件下,苯酚与甲醛发生缩聚反应生成酚醛树脂,B项正确;
C.向淀粉的水解液中加入碘水,溶液变蓝,只能说明溶液中含有淀粉,不能说明淀粉未水解,C项正确;
D.在酸性条件下,氨基酸以阳离子形态存在,在碱性条件下,氨基酸以阴离子形态存在,当以两性离子存在时,其在水中的溶解度最小,D项错误;
答案选D。
4.B
【详解】A.白砂糖的主要成分是蔗糖,做成“棉花糖”是状态的变化,仍然是小分子,A错误;
B.氯化铁水解使溶液呈酸性,可用于镀覆层前的钢铁除锈,B正确;
C.活性炭不具有吸水性,不能作干燥剂,铁粉具有还原性,可用作食品抗氧化剂,不作干燥剂,C错误;
D.碳纤维是一种新型无机材料,是单质,不是高分子材料,D错误;
答案选B。
5.A
【详解】A.乙醛中碳氧双键与氢气发生加成反应,A正确;
B.甲基上的氢原子被取代,属于取代反应,B错误;
C.乙醇发生消去反应生成乙烯,属于消去反应,C错误;
D.乙醛中醛基被氧化生成乙酸,为氧化反应,D错误;
故选A。
6.D
【详解】A.蔗糖酯是由高级脂肪酸与蔗糖形成的酯,而油脂是高级脂肪酸与甘油形成的酯,故蔗糖酯不属于油脂,A错误;
B.该非天然油脂的相对分子质量较大,但不是高分子化合物,B错误;
C.该非天然油脂可由直链形的油酸和蔗糖发生酯化反应而得,油酸分子中含有碳碳双键,故该非天然油脂能使酸性KMnO4溶液褪色,C错误;
D.该蔗糖酯在稀硫酸作用下水解生成油酸和蔗糖,而蔗糖还可水解生成葡萄糖和果糖,因此该蔗搪酯水解的最终产物为油酸、葡萄糖和果糖,D正确;
答案选D。
7.B
【详解】A.甲酸钠中C和H之间共用一对电子,C和O双键之间共用两对电子,C和O单键之间共用一对电子,甲酸根和钠离子之间是离子键,故甲酸钠中含有共用电子对的数目为,A错误;
B.和的摩尔质量均为22 g/mol,1.1 g混合物的物质的量为0.05 mol,每个和分子均含有10个质子,故1.1g和的混合物,含有的质子数为,B正确;
C.在酸性条件下的水解为可逆反应,生成的的分子数目小于,C错误;
D.1L的溶液与1L的盐酸混合后pH仍然等于3,则,溶液中数目等于,D错误;
故选B。
8.C
【详解】A. 胶体按分散剂的状态可分为固溶胶、液溶胶、气溶胶,故气溶胶属于胶体,A项正确;
B. 温度过高会使蛋白质变性,病毒疫苗主要成分含蛋白质,为防止其变性,一般需要冷藏保存,B项正确;
C. 次氯酸钠溶液、过氧乙酸具有强氧化性,能够杀菌消毒,、75%乙醇能使蛋白质变性,可做消毒剂,C项错误;
D. 聚丙烯属于合成有机高分子化合物,D项正确;
故选C。
9.C
【详解】A.属于酚,属于醇,两者结构不相似,不是同系物,A错误;
B.溴水不能鉴别乙醇和乙酸,酸性高锰酸钾溶液不能鉴别乙醇和苯酚,B错误;
C.乙酸CH3COOH、硬脂酸C17H35COOH都是饱和一元羧酸,二者结构相似,组成上相差16个CH2,二者互为同系物,丙烯酸CH2=CHCOOH和油酸C17H33COOH,分子中都含有一个羧基和一个碳碳双键,二者结构相似,组成上相差15个CH2,二者互为同系物,C正确;
D.若有机物的结构简式为C(CH3)3OH,则不能发生催化氧化反应,D错误;
答案选C。
10.B
【详解】A.电荷不守恒,SO2使酸性KMnO4溶液褪色的离子方程式为5SO2+2+2H2O=5+2Mn2++4H+,A错误;
B.Al与NaOH溶液反应生成Na[Al(OH)4]和H2,反应的离子方程式为2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑,B正确;
C.C6H5ONa与少量CO2反应生成苯酚和NaHCO3,反应的离子方程式为C6H5O-+CO2+H2O→C6H5OH+,C错误;
D.粗铜电解精炼时,粗铜作阳极,粗铜中比Cu活泼的金属如Zn、Fe等优先在阳极放电,阳极电极反应有:Zn-2e-=Zn2+、Fe-2e-=Fe2+、Cu-2e-=Cu2+,精铜为阴极,阴极电极反应为Cu2++2e-=Cu,D错误;
答案选B。
11. ② ③
【详解】①装修材料造成居室污染主要因为其能产生HCHO(甲醛),故选②;
②氟利昂会破坏臭氧层,产生臭氧空洞,故选③。
12.(1)A和C
(2)醛基
(3)A
【分析】(1)
上述物质互为同分异构体的是A和C(填序号)分子式均为C8H8O2,而B的分子式为C9H8O。故答案为:A和C;
(2)
B中的含氧官能团-CHO是醛基。故答案为:醛基;
(3)
与NaHCO3、NaOH和Na都能反应的是A(填序号),B与NaHCO3、NaOH和Na均不反应,C与NaHCO3不反应,故答案为:A。
13. D B A C A C Cd2+ +S2- =CdS↓ C A 锂(或Li)
【详解】(1)①胃舒平(通用名:复方氢氧化铝)有中和胃酸,减少胃液分泌和解痉止疼的作用。故属于治疗“胃酸过多症”的抗酸药的是胃舒平,答案选D;②存在于蔬菜、水果中,具有还原性的物质是维生素C,答案选B;③存在于土豆、谷类等植物中,遇碘水显蓝色的物质是淀粉,答案选A;④属于抗生素类药,有阻止多种细菌生长的功能,该物质是青霉素,答案选C;(2)①排放含磷的化合物会导致水体富营养化,答案选A;②工农业生产用了被污染的水,会降低产品的质量,损害人类的健康.那么污染水的因素有那些呢?工业生产中的废渣、废水、废气和生活污水的任意排放,农业生产中农药、化肥不合理使用会随雨水流入河中,原油泄漏都会使水受到污染,因此保护水资源,人人有责。本题中ABD均能造成水质严重污染,所以应严加管理。答案选C;③向含镉离于(Cd2+)的废水中加入Na2S生成CdS以除去镉离子,该反应的离子方程式为Cd2+ +S2- =CdS↓;(3)①A.铜导线 属于单质,选项A不符合;B 玻璃属于无机非金属材料,选项B不符合;C.硬铝窗框架属于铝合金材料,选项C符合。答案选C;②三大化石能源是指煤、石油、天然气,木材不属于化石能源,答案选A;③电池中的电解质是固体电解质LiI,总反应是2Li +I2=2LiI,活泼金属作为负极,故电池的负极是锂(或Li)。
14.正确
【解析】略
15.(1)75%
(2)1︰4
【详解】(1)丙烷分子中含有6个伯氢、2个仲氢,而1-氯丙烷取代的是伯氢,2-氯丙烷取代的是仲氢,因此在一氯代丙烷中1-氯丙烷在产物中的占有率为;
故答案为:75%;
(2)丙烷分子中含有6个伯氢、2个仲氢,而1-氯丙烷取代的是伯氢,2-氯丙烷取代的是仲氢,由于在常温下1-氯丙烷是43%,2-氯丙烷是57%,设在常温下伯氢和仲氢的相对活性比为x:y,则,解得x:y=1:4;
故答案为:。
16.(1) ② ① ③ ⑤⑥ ④
(2)3
(3) C3H8 4 BD
【详解】(1)①氧气和臭氧是氧元素形成的不同种单质,互为同素异形体;
②35Cl和37Cl的质子数相同、中子数不同,互为同位素;
③2—甲基丙烷和2—甲基丁烷的结构相似,相差1个CH2原子团,互为同系物;
④由结构式可知,两种结构都为二氯甲烷,是同种物质;
⑤丁烷和异丁烷的分子式相同,结构不同,互为同分异构体;
⑥乙醇和甲醚的分子式相同,结构不同,互为同分异构体;
则互为同位素的为②,互为同素异形体的为①,互为同系物的为③,互为同分异构体的为⑤⑥,属于同种物质的为④,故答案为:②;①;③;⑤⑥;④;
(2)由结构简式可知,立方烷的一氯代物有1种,二氯代物有3种,故答案为:3;
(3)由甲为只含C、H两种元素的饱和化合物可知,甲为烷烃,设甲的分子式为CnH2n+2,由分子中含有26个电子可得:6n+2n+2=26,解得n=3,则甲的分子式为C3H8;由化合物乙为只含C、H、F三种元素的饱和化合物可知,乙为氟代烃,设乙的分子式为CnH2n+2—xFx,由分子中含有26个电子可得:6n+(2n+2—x)+9x=26,由乙分子中C、H、F原子个数比为1∶2∶2可得n∶x=1∶2,解得n=1、x=2,则乙的分子式为CH2F2;
①由分析可知,甲的分子式为C3H8;丙烷的一氟代物有1—氟丙烷和2—氟丙烷,共2种,其中1—氟丙烷分子和2—氟丙烷分子中氢原子被氟原子取代所得结构有4种,分别为CH3CH2CHF2、CH3CF2CH3、CH2FCHFCH3、CH2FCH2CH2F,故答案为:C3H8;4;
②由分析可知,乙的分子式为CH2F2,名称为二氟甲烷;
A.二氟甲烷分子中碳氢键和碳氟键的键长不同,的空间构型为四面体形,不是正四面体形,故错误;
B.二氟甲烷分子中饱和碳原子的杂化方式为sp3杂化,故正确;
C.甲烷分子的空间构型为四面体形,二氟甲烷分子不存在同分异构体,故错误;
D.甲烷分子的空间构型为四面体形,二氟甲烷分子不存在同分异构体,故正确;
故选BD。
17.C3H4O5、
【详解】由0.1molX在氧气中完全燃烧后,生成CO2的体积为6.72L(标准状况),生成H2O的质量为3.6g 可知,X分子在含有的碳原子个数为==3,含有氢原子的个数为==4,由0.1molX与足量钠反应,产生气体的体积为3.36L(标准状况)可知,分子中含有的羟基数目为==3,由碳、氢原子的个数可知,X分子的不饱和度为2,由 、 结构不稳定和X分子为链状可知,X分子中含有2个—COOH和1个—OH ,则分子式为C3H4O5,结构简式为 ,故答案为:C3H4O5、 。
18.(1) 酸性高锰酸钾(KMnO4)、氯化铁(FeCl3)溶液、溴水等
(2)氯代
(3) NaCl 离子化合物的熔点在离子电荷相同的条件下,离子半径越大,熔点越低。化合物C中阴阳离子半径较大,熔点低。或NaCl离子半径比化合物C小,熔点高
(4)还原反应
(5)+CH3COCl→ +HCl
(6)16
【分析】A先和液氯发生取代反应,再发生硝化反应得到B,B再经系列反应生成C,C再反应生成D,对比D和F的结构简式可知,D中硝基临位的F原子被-OC5H6取代生成F,再根据题目所给信息可知,E的结构简式应为;F中硝基被还原为氨基生成G,G中氨基和CH3COCl发生取代反应生成H。
(1)
F与D相比较多了苯氧基,再结合已知条件,得出E为苯酚;检验苯酚残留可以用FeCl3溶液遇苯酚发生显色反应;也可以用溴水,即使三溴苯酚在有机物中看不到沉淀,也能使溴颜色消失。
(2)
氯原子是邻位和对位取代定位基,-NO2则是间位取代定位基,-NO2处在氯原子对位,需要先进行氯代再硝化;
(3)
熔点较高的是NaCl,因为离子化合物的熔点在离子电荷相同的条件下,离子半径越大,熔点越低,C中阴阳离子半径较大,故熔点低。
(4)
有机物加氢去氧是还原,F→G硝基变成了氨基,反应类型为还原反应;
(5)
G→H的化学方程式为+CH3COCl→ +HCl;
(6)
K比D分子组成多1个C原子和2个H原子,满足①红外光谱显示,-F都与苯环直接相连且含有-NH2,②能与NaHCO3反应放出气体说明其含有-COOH,即苯环连两个-F,一个-NH2一个-COOH:、、、、、,共16种。
19.(1)
(2)CH3CHO
(3)CH3COOH+C2H5OHCH3COOC2H5+H2O
(4)ab
(5)CH2=CH2 + H2OCH3CH2OH
(6)2CH3CH2OH+O22CH3CHO+2H2O
【分析】D是有香味且不溶于水的油状液体,依据D的分子式,可确定D为CH3COOC2H5;E的产量可以用来衡量一个国家的石油化工发展水平,则E为CH2=CH2;A经两次氧化生成同碳原子数的C,则A为醇、C为羧酸,再由D的结构简式,可确定A是CH3CH2OH,B是CH3CHO,C是CH3COOH。
(1)
E为乙烯,电子式为 ,答案为;
(2)
由以上分析知,B的结构简式是CH3CHO。答案为:CH3CHO;
(3)
反应①是乙醇与乙酸在浓硫酸存在并加热的条件下发生酯化反应,生成乙酸乙酯和水,该反应为可逆反应,反应的化学方程式是CH3COOH+C2H5OHCH3COOC2H5+H2O。答案为:CH3COOH+C2H5OHCH3COOC2H5+H2O;
(4)
a.E是乙烯,分子中所有原子在同一平面上,a正确;
b.乙酸乙酯难溶于碳酸钠溶液,密度比碳酸钠溶液小,而乙酸能够与碳酸钠溶液反应生成乙酸钠、水和二氧化碳,因此可用饱和Na2CO3溶液除去乙酸乙酯中混有的乙酸,b正确;
c.②的反应为乙酸与乙烯发生的加成反应,c错误;
故选ab。答案为:ab。
(5)
由分析可知E为乙烯,A为乙醇,乙烯和水加成可以得到乙醇,方程式为:CH2=CH2 + H2OCH3CH2OH ;
(6)
由分析可知A为乙醇,B为CH3CHO,乙醇催化氧化得到乙醛,方程式为:2CH3CH2OH+O22CH3CHO+2H2O。
答案第1页,共2页
答案第1页,共2页
