2023年中考化学复习 第13讲 中和反应和pH值课件(共34张PPT)
文档属性
| 名称 | 2023年中考化学复习 第13讲 中和反应和pH值课件(共34张PPT) |  | |
| 格式 | ppt | ||
| 文件大小 | 2.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-26 07:55:29 | ||
图片预览










文档简介
(共34张PPT)
第一部分
基础知识复习
第三板块 身边的化学物质
1
直击重点
2
知识梳理
3
金牌重难点
4
中考特训
5
广东真题
第13讲 中和反应和pH值
1.用酸碱指示剂(酚酞、石蕊)和pH试纸检验溶液酸碱性的方法。
2.酸碱性对人体健康和农作物生长的影响。
1.概念:酸和碱作用生成 的反应叫做中和反应。中和反应属于基本反应类型中的 反应。
(1)中和反应一定生成盐和水,但生成盐和水的反应不一定是中和反应,如:金属氧化物与酸的反应。
(2)微观实质: H++OH-===H2O。
(3)从热量变化角度看,中和反应属于放热反应。
知识点一:
中和反应
复分解
盐和水
2.应用:(1)改良土壤的酸碱性:如熟石灰改良酸性土壤;(2)处理工厂的废水;(3)用于医药和日常生活中:如常用 、
治疗胃酸过多; (4)调节溶液的酸碱性。
Mg(OH)2
Al(OH)3
1.概念:溶液 的强弱程度,即为溶液的酸碱度。
知识点二:
溶液的酸碱度
2.表示方法:溶液酸碱度通常用pH表示,pH范围在 之间。
3.pH的大小与溶液酸碱度、酸碱性的关系
溶液的酸碱度是溶液酸碱性的定量表示,可以用pH试纸测定,酸碱性还可以用酸碱指示剂测得。
pH=7,溶液呈 ;pH<7,溶液呈 ,pH越小,酸性越 ;pH>7,溶液呈 ,pH越大,碱性越 。
酸碱性
0~14
中性
强
酸性
强
碱性
4.测定方法:
(1)pH试纸:粗略测量,结果为整数。使用方法:在白瓷板或玻璃片上放一小片pH试纸,用洁净干燥的玻璃棒蘸取少许待测液滴于pH试纸上,然后把试纸显示的颜色跟标准比色卡对比,读出待测液的pH。(“放—蘸—滴—比—读”)
(2)pH计:测量结果更加精确。
5.了解溶液酸碱度的重要意义
(1)在农业生产中,农作物一般适宜在pH为7或接近7的土壤中生长。
(2)测定雨水的pH,正常雨水的pH约为 ,pH< . 的降雨称为酸雨。
5.6
5.6
1.测定溶液的pH时,所用pH试纸必须干燥,若事先用水润湿,可能会改变待测溶液的pH。若是酸性溶液,则待测溶液的酸性减弱,pH偏 ;若是碱性溶液,则待测溶液的碱性减弱,pH偏 ;若是中性溶液,则pH 。
2.酸性溶液包括酸溶液和某些盐溶液(如CuSO4溶液);碱性溶液包括碱溶液和某些盐溶液(如Na2CO3溶液);能使无色酚酞变红的溶液不一定是碱溶液,但一定是碱性溶液。
不变
大
小
(2022·鸡西)下表列出了物质在常温下的近似pH,下列说法正确的是( )
A.表中所有的食物都显酸性
B.蚊虫叮咬后,涂抹牙膏可减轻痛痒
C.厕所清洁剂与炉具清洁剂混合使用清洁油渍效果更佳
D.胃酸过多的人多食用橘子
重难点一:
溶液酸碱性和pH值
物质 厕所清洁剂 橘子 西瓜 鸡蛋清 牙膏 炉具清洁剂
pH 1-2 3-4 6-7 7-8 8-9 12-13
B
【思路点拨】 选B。A.鸡蛋清pH为7-8,显碱性,故选项说法错误。B.蚊虫叮咬后释放酸性物质,可涂抹显碱性的溶液,肥皂水的pH大于7,显碱性,可涂抹牙膏以减轻痛痒,故选项说法正确。C.厕所清洁剂的pH小于7,炉具清洁剂的pH大于7,能发生反应,厕所清洁剂与炉具清洁剂不能混合使用,故选项说法错误。D.橘子的pH小于7,显酸性,因此胃酸过多的人不宜多食用橘子,故选项说法错误。故选:B。
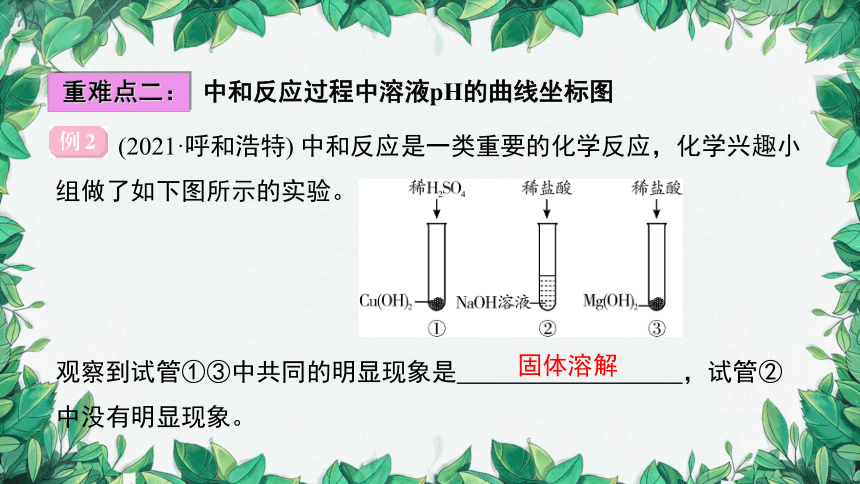
(2021·呼和浩特) 中和反应是一类重要的化学反应,化学兴趣小组做了如下图所示的实验。
观察到试管①③中共同的明显现象是 ,试管②中没有明显现象。
重难点二:
中和反应过程中溶液pH的曲线坐标图
固体溶解
【提出问题】试管②中没有明显现象,是否发生了反应?
【实验探究】
(1)化学兴趣小组取少量实验后试管②中的溶液,分别放入a、b两支试管中,向a试管中滴入酚酞溶液,观察到了 (填写现象),证明了稀盐酸和氢氧化钠溶液一定发生了化学反应。为进一步探究试管②反应后溶液中溶质成分,还可以向试管b中加入下列物质中的 (填字母)。
A.Zn B.Fe(OH)3 C.FeCl3 D.AgNO3
溶液不变色
AB
(2)化学兴趣小组又利用pH传感器探究稀盐酸和氢氧化钠溶液的反应过程。实验操作和结果测定如图所示:
①该实验中,乙溶液是 ;
稀盐酸
②加入甲溶液6mL时,烧瓶中的溶液溶质成分 (填化学式);
③根据该实验测定结果,判断发生化学反应的依据是_________________________________________________________。
HCl、NaCl
溶液pH由小于7变成等于或大于7
【思路点拨】 试管①,向Cu(OH)2固体中加入稀硫酸,Cu(OH)2与稀硫酸反应生成硫酸铜和水。试管③,向Mg(OH)2固体中加入稀盐酸,Mg(OH)2与盐酸反应生成氯化镁和水。试管①③中共同的明显现象是固体溶解。(1)化学兴趣小组取少量实验后试管②中的溶液,分别放入a、b两支试管中,向a试管中滴入酚酞溶液,溶液不变红色,说明溶液中没有氢氧化钠,故稀盐酸和氢氧化钠溶液一定发生了化学反应;溶液中的溶质一定有NaCl,可能还含有HCl;为进一步探究试管②反应后溶液中溶质成分,可以向试管b中加入Zn,有气泡生成说明
溶液中还含有HCl,反之则无;加入Fe(OH)3,溶液变成黄色,说明溶液中还含有HCl,反之则无;加入FeCl3,无明显现象,无法判断溶液中是否含有HCl;加入AgNO3,因为NaCl与AgNO3反应也会产生白色沉淀,无法判断溶液中是否含有HCl。(2)①由图像可知,加入甲溶液前,乙溶液的pH<7,说明乙溶液是稀盐酸。②加入甲溶液6mL时,烧瓶中的溶液的pH<7,说明加入的氢氧化钠的量不足,盐酸过量,故烧瓶中的溶液的溶质成分是NaCl和HCl。③根据该实验测定结果,判断发生化学反应的依据是随着氢氧化钠溶液的加入,烧瓶内溶液的pH从<7逐渐增大到≥7。
★溶液的酸碱性和pH值
1.(2022·长沙)我国有约3.4亿亩盐碱地具备种植水稻的基本条件,适宜种植耐盐碱水稻土地的pH为8.8~9.2,呈碱性。下列物质呈碱性的是( )
A.白醋 B.食盐水 C.柠檬酸溶液 D.肥皂水
基础过关
D
2.(2022·台湾)新闻报导某处养殖池的白虾大量暴毙,调查后初步推测是高温与暴雨,使养殖池的溶氧量和pH值剧烈变化,导致水质改变所造成的。专家建议为避免白虾大量死亡,应注意水温变化,可先用水车调整水中的溶氧量,并监控水中的pH值,投放熟石灰(氢氧化钙)调整至合适的pH值。关于上述专家建议的方法,下列说明何者最合理( )
A.使水中的溶氧量增加,pH值增加 B.使水中的溶氧量增加,pH值减少
C.使水中的溶氧量减少,pH值增加 D.使水中的溶氧量减少,pH值减少
A
3.(2022·黑龙江)分析推理是化学学习中常用的思维方法。下列分析推理正确的是( )
A.酸溶液的pH小于7,所以pH小于7的溶液一定呈酸性
B.胃药中的Mg(OH)2可以治疗胃酸过多,所以NaOH也可以治疗胃酸过多
C.同种元素的粒子质子数相同,质子数相同的粒子一定属于同种元素
D.氧化物中含有氧元素,含有氧元素的化合物一定是氧化物
A
4.(2022·广安)了解溶液的酸碱性,对于生活、生产以及人类的生命活动具有重要的意义。下表列出了一些物质在常温下的近似pH,下列有关说法正确的是( )
A.患有胃病的人应多喝柠檬水
B.人被蚊虫叮咬后,蚊虫在人的皮肤内分泌出蚊酸,使叮咬处肿大、痛痒,可用肥皂水涂抹,减轻痛痒
C.用炉具清洁剂去除厨具上的油污和用洗涤剂洗掉衣服、餐具上的油污原理相同
D.常温下,将牛奶加水稀释后pH大于7
物质 柠檬 牛奶 牙膏 肥皂 炉具清洁剂
pH 2-3 6-7 8-9 9-10 12-13
B
★中和反应的实质和概念
5.(2022·铜仁)从不同的角度认识NaOH+HCl===NaCl+H2O,下列选项正确的是( )
A.基本反应类型:该反应为中和反应
B.反应实质:氢离子与氧氧根离子结合生成水
C.反应物:氢氧化钠可以用来治疗胃酸过多
D.读法:氢氧化钠加氯化氢完全反应生成氯化钠加水
B
6.(2022·苏州)氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图如下。下列说法不正确的是( )
A. 盐酸中存在的微粒有水分子和氯化氢分子
B. 该反应的微观实质是H+和OH-结合生成
水分子
C. Na+和Cl-在该反应过程中没有被消耗
D. 恰好完全反应时,溶液呈中性
A
★中和反应的实际应用
7.(2021·安徽) 下列应用的主要原理不涉及中和反应的是( )
A.生石灰用于加热即热食品 B.氢氧化铝用于治疗胃酸过多
C.熟石灰用于改良酸性土壤 D.硼酸用于处理皮肤上沾有的碱
8.饮食过量,胃酸会大量分泌,以致消化不良。为缓解该症状,下列药剂不适宜的是( )
A.氢氧化铝 B.氯化钠 C.碳酸镁 D.碳酸氢钠
A
B
★中和反应过程中溶液pH的曲线坐标图
9.(2022·河北)向含有酚酞的氢氧化钠溶液中慢慢滴入稀硫酸,该过程中溶液pH的变化如图所示。下列分析正确的是( )
A.N点时的溶液一定呈红色
B.P点时的溶液能与纯碱发生反应
C.M→N过程中溶液的碱性逐渐增强
D.M→P过程中生成的硫酸钠不断增加
B
10.(2022·成都)实验小组用图1装置探究稀氢氧化钠
溶液与稀盐酸能否反应,测得数据如图2。下列说法
正确的是( )
A. 烧杯中只能盛放稀氢氧化钠溶液
B. 图2不能证明反应是放热反应
C. 60 s时溶液中溶质只有氯化钠
D. 实验证明氢氧化钠与盐酸能反应
D
11.(2022·绍兴)在做酸碱反应的实验时,向盛有氢氧化钠溶液的烧杯中,逐渐加入稀盐酸。烧杯内相关物质的质量与加入稀盐酸质量的变化关系不正确的是( )
A B C D
D
12.(2022·杭州)HCl气体通入水中可得到盐酸,室温下,将HCl气体通入盛有NaOH溶液的试管中:
(1) Cl和 Cl的中子个数相差 个。
(2)HCl气体通入NaOH溶液前后,试管中溶液的离子种类如图所示,其中能使无色酚酞试液变红的是 (选填“①”“②”或“③”)。
3517
3717
2
②
13.(2021·菏泽) 某化学兴趣小组为验证硫酸的部分化学性质,使用氢氧化钠、碳酸钠、金属铝和另外一种不同类别的物质A进行了相关实验。
(1)实验时观察到稀硫酸与A反应有蓝色溶液生成,则A物质是 。
能力提升
CuO
(2)稀硫酸与氢氧化钠溶液反应时没有明显现象,为了证明二者发生了反应,该组同学设计了如图1所示实验,传感器测定的pH和温度随溶液质量变化的情况见图2、图3。
则B溶液是 溶液,图3中的M与图2中X、Y、Z中的
数值相等。
Y
稀硫酸
(3)该化学兴趣小组又做了如右图所示实验:
【提出问题】②号试管中无色溶液的溶质是什么?
【作出猜想】猜想一:硫酸钠 猜想二:硫酸钠、硫酸
猜想三: .
【实验验证】该小组同学用试管取适量
②号试管中的无色溶液,加入一种试剂
后,根据产生的现象推断出了②号试管
中溶质的成分,该试剂是 。
硫酸钠、氢氧化钠
酚酞溶液
【质疑反思】甲同学认为猜想三不能成立,因为①②号试管中溶液混合后烧杯中没有蓝色沉淀生成。
乙同学则认为猜想三是可以成立的,理由是_____________________
________________________________________________________。
①号试管中如果有H2SO4剩余,会与②试管中的NaOH反应,即不会产生Cu(OH)2
14.(2020·广东) 某废酸液主要含H2SO4和FeSO4,该废酸液的Ph
7(选填“<”或“>”)。
15.(2019·广东) 下列常见物质的pH大于7的是( )
A.食醋 B.食盐水 C.氨水 D.柠檬水
<
C
16.(2018·广东) 下列水果中酸度最强的是( )
A.菠萝pH=4.1 B.木瓜pH=5.5
C.草莓pH=3.2 D.柠檬pH=2.3
D
17.(2017·广东) 黄蜂的毒液呈碱性,若被黄蜂蜇了,涂抹下列物质可缓解疼痛的是( )
A.食盐水(pH≈7) B.牙膏(pH≈9)
C.肥皂(pH≈10) D.米醋(pH≈3)
D
第一部分
基础知识复习
第三板块 身边的化学物质
1
直击重点
2
知识梳理
3
金牌重难点
4
中考特训
5
广东真题
第13讲 中和反应和pH值
1.用酸碱指示剂(酚酞、石蕊)和pH试纸检验溶液酸碱性的方法。
2.酸碱性对人体健康和农作物生长的影响。
1.概念:酸和碱作用生成 的反应叫做中和反应。中和反应属于基本反应类型中的 反应。
(1)中和反应一定生成盐和水,但生成盐和水的反应不一定是中和反应,如:金属氧化物与酸的反应。
(2)微观实质: H++OH-===H2O。
(3)从热量变化角度看,中和反应属于放热反应。
知识点一:
中和反应
复分解
盐和水
2.应用:(1)改良土壤的酸碱性:如熟石灰改良酸性土壤;(2)处理工厂的废水;(3)用于医药和日常生活中:如常用 、
治疗胃酸过多; (4)调节溶液的酸碱性。
Mg(OH)2
Al(OH)3
1.概念:溶液 的强弱程度,即为溶液的酸碱度。
知识点二:
溶液的酸碱度
2.表示方法:溶液酸碱度通常用pH表示,pH范围在 之间。
3.pH的大小与溶液酸碱度、酸碱性的关系
溶液的酸碱度是溶液酸碱性的定量表示,可以用pH试纸测定,酸碱性还可以用酸碱指示剂测得。
pH=7,溶液呈 ;pH<7,溶液呈 ,pH越小,酸性越 ;pH>7,溶液呈 ,pH越大,碱性越 。
酸碱性
0~14
中性
强
酸性
强
碱性
4.测定方法:
(1)pH试纸:粗略测量,结果为整数。使用方法:在白瓷板或玻璃片上放一小片pH试纸,用洁净干燥的玻璃棒蘸取少许待测液滴于pH试纸上,然后把试纸显示的颜色跟标准比色卡对比,读出待测液的pH。(“放—蘸—滴—比—读”)
(2)pH计:测量结果更加精确。
5.了解溶液酸碱度的重要意义
(1)在农业生产中,农作物一般适宜在pH为7或接近7的土壤中生长。
(2)测定雨水的pH,正常雨水的pH约为 ,pH< . 的降雨称为酸雨。
5.6
5.6
1.测定溶液的pH时,所用pH试纸必须干燥,若事先用水润湿,可能会改变待测溶液的pH。若是酸性溶液,则待测溶液的酸性减弱,pH偏 ;若是碱性溶液,则待测溶液的碱性减弱,pH偏 ;若是中性溶液,则pH 。
2.酸性溶液包括酸溶液和某些盐溶液(如CuSO4溶液);碱性溶液包括碱溶液和某些盐溶液(如Na2CO3溶液);能使无色酚酞变红的溶液不一定是碱溶液,但一定是碱性溶液。
不变
大
小
(2022·鸡西)下表列出了物质在常温下的近似pH,下列说法正确的是( )
A.表中所有的食物都显酸性
B.蚊虫叮咬后,涂抹牙膏可减轻痛痒
C.厕所清洁剂与炉具清洁剂混合使用清洁油渍效果更佳
D.胃酸过多的人多食用橘子
重难点一:
溶液酸碱性和pH值
物质 厕所清洁剂 橘子 西瓜 鸡蛋清 牙膏 炉具清洁剂
pH 1-2 3-4 6-7 7-8 8-9 12-13
B
【思路点拨】 选B。A.鸡蛋清pH为7-8,显碱性,故选项说法错误。B.蚊虫叮咬后释放酸性物质,可涂抹显碱性的溶液,肥皂水的pH大于7,显碱性,可涂抹牙膏以减轻痛痒,故选项说法正确。C.厕所清洁剂的pH小于7,炉具清洁剂的pH大于7,能发生反应,厕所清洁剂与炉具清洁剂不能混合使用,故选项说法错误。D.橘子的pH小于7,显酸性,因此胃酸过多的人不宜多食用橘子,故选项说法错误。故选:B。
(2021·呼和浩特) 中和反应是一类重要的化学反应,化学兴趣小组做了如下图所示的实验。
观察到试管①③中共同的明显现象是 ,试管②中没有明显现象。
重难点二:
中和反应过程中溶液pH的曲线坐标图
固体溶解
【提出问题】试管②中没有明显现象,是否发生了反应?
【实验探究】
(1)化学兴趣小组取少量实验后试管②中的溶液,分别放入a、b两支试管中,向a试管中滴入酚酞溶液,观察到了 (填写现象),证明了稀盐酸和氢氧化钠溶液一定发生了化学反应。为进一步探究试管②反应后溶液中溶质成分,还可以向试管b中加入下列物质中的 (填字母)。
A.Zn B.Fe(OH)3 C.FeCl3 D.AgNO3
溶液不变色
AB
(2)化学兴趣小组又利用pH传感器探究稀盐酸和氢氧化钠溶液的反应过程。实验操作和结果测定如图所示:
①该实验中,乙溶液是 ;
稀盐酸
②加入甲溶液6mL时,烧瓶中的溶液溶质成分 (填化学式);
③根据该实验测定结果,判断发生化学反应的依据是_________________________________________________________。
HCl、NaCl
溶液pH由小于7变成等于或大于7
【思路点拨】 试管①,向Cu(OH)2固体中加入稀硫酸,Cu(OH)2与稀硫酸反应生成硫酸铜和水。试管③,向Mg(OH)2固体中加入稀盐酸,Mg(OH)2与盐酸反应生成氯化镁和水。试管①③中共同的明显现象是固体溶解。(1)化学兴趣小组取少量实验后试管②中的溶液,分别放入a、b两支试管中,向a试管中滴入酚酞溶液,溶液不变红色,说明溶液中没有氢氧化钠,故稀盐酸和氢氧化钠溶液一定发生了化学反应;溶液中的溶质一定有NaCl,可能还含有HCl;为进一步探究试管②反应后溶液中溶质成分,可以向试管b中加入Zn,有气泡生成说明
溶液中还含有HCl,反之则无;加入Fe(OH)3,溶液变成黄色,说明溶液中还含有HCl,反之则无;加入FeCl3,无明显现象,无法判断溶液中是否含有HCl;加入AgNO3,因为NaCl与AgNO3反应也会产生白色沉淀,无法判断溶液中是否含有HCl。(2)①由图像可知,加入甲溶液前,乙溶液的pH<7,说明乙溶液是稀盐酸。②加入甲溶液6mL时,烧瓶中的溶液的pH<7,说明加入的氢氧化钠的量不足,盐酸过量,故烧瓶中的溶液的溶质成分是NaCl和HCl。③根据该实验测定结果,判断发生化学反应的依据是随着氢氧化钠溶液的加入,烧瓶内溶液的pH从<7逐渐增大到≥7。
★溶液的酸碱性和pH值
1.(2022·长沙)我国有约3.4亿亩盐碱地具备种植水稻的基本条件,适宜种植耐盐碱水稻土地的pH为8.8~9.2,呈碱性。下列物质呈碱性的是( )
A.白醋 B.食盐水 C.柠檬酸溶液 D.肥皂水
基础过关
D
2.(2022·台湾)新闻报导某处养殖池的白虾大量暴毙,调查后初步推测是高温与暴雨,使养殖池的溶氧量和pH值剧烈变化,导致水质改变所造成的。专家建议为避免白虾大量死亡,应注意水温变化,可先用水车调整水中的溶氧量,并监控水中的pH值,投放熟石灰(氢氧化钙)调整至合适的pH值。关于上述专家建议的方法,下列说明何者最合理( )
A.使水中的溶氧量增加,pH值增加 B.使水中的溶氧量增加,pH值减少
C.使水中的溶氧量减少,pH值增加 D.使水中的溶氧量减少,pH值减少
A
3.(2022·黑龙江)分析推理是化学学习中常用的思维方法。下列分析推理正确的是( )
A.酸溶液的pH小于7,所以pH小于7的溶液一定呈酸性
B.胃药中的Mg(OH)2可以治疗胃酸过多,所以NaOH也可以治疗胃酸过多
C.同种元素的粒子质子数相同,质子数相同的粒子一定属于同种元素
D.氧化物中含有氧元素,含有氧元素的化合物一定是氧化物
A
4.(2022·广安)了解溶液的酸碱性,对于生活、生产以及人类的生命活动具有重要的意义。下表列出了一些物质在常温下的近似pH,下列有关说法正确的是( )
A.患有胃病的人应多喝柠檬水
B.人被蚊虫叮咬后,蚊虫在人的皮肤内分泌出蚊酸,使叮咬处肿大、痛痒,可用肥皂水涂抹,减轻痛痒
C.用炉具清洁剂去除厨具上的油污和用洗涤剂洗掉衣服、餐具上的油污原理相同
D.常温下,将牛奶加水稀释后pH大于7
物质 柠檬 牛奶 牙膏 肥皂 炉具清洁剂
pH 2-3 6-7 8-9 9-10 12-13
B
★中和反应的实质和概念
5.(2022·铜仁)从不同的角度认识NaOH+HCl===NaCl+H2O,下列选项正确的是( )
A.基本反应类型:该反应为中和反应
B.反应实质:氢离子与氧氧根离子结合生成水
C.反应物:氢氧化钠可以用来治疗胃酸过多
D.读法:氢氧化钠加氯化氢完全反应生成氯化钠加水
B
6.(2022·苏州)氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图如下。下列说法不正确的是( )
A. 盐酸中存在的微粒有水分子和氯化氢分子
B. 该反应的微观实质是H+和OH-结合生成
水分子
C. Na+和Cl-在该反应过程中没有被消耗
D. 恰好完全反应时,溶液呈中性
A
★中和反应的实际应用
7.(2021·安徽) 下列应用的主要原理不涉及中和反应的是( )
A.生石灰用于加热即热食品 B.氢氧化铝用于治疗胃酸过多
C.熟石灰用于改良酸性土壤 D.硼酸用于处理皮肤上沾有的碱
8.饮食过量,胃酸会大量分泌,以致消化不良。为缓解该症状,下列药剂不适宜的是( )
A.氢氧化铝 B.氯化钠 C.碳酸镁 D.碳酸氢钠
A
B
★中和反应过程中溶液pH的曲线坐标图
9.(2022·河北)向含有酚酞的氢氧化钠溶液中慢慢滴入稀硫酸,该过程中溶液pH的变化如图所示。下列分析正确的是( )
A.N点时的溶液一定呈红色
B.P点时的溶液能与纯碱发生反应
C.M→N过程中溶液的碱性逐渐增强
D.M→P过程中生成的硫酸钠不断增加
B
10.(2022·成都)实验小组用图1装置探究稀氢氧化钠
溶液与稀盐酸能否反应,测得数据如图2。下列说法
正确的是( )
A. 烧杯中只能盛放稀氢氧化钠溶液
B. 图2不能证明反应是放热反应
C. 60 s时溶液中溶质只有氯化钠
D. 实验证明氢氧化钠与盐酸能反应
D
11.(2022·绍兴)在做酸碱反应的实验时,向盛有氢氧化钠溶液的烧杯中,逐渐加入稀盐酸。烧杯内相关物质的质量与加入稀盐酸质量的变化关系不正确的是( )
A B C D
D
12.(2022·杭州)HCl气体通入水中可得到盐酸,室温下,将HCl气体通入盛有NaOH溶液的试管中:
(1) Cl和 Cl的中子个数相差 个。
(2)HCl气体通入NaOH溶液前后,试管中溶液的离子种类如图所示,其中能使无色酚酞试液变红的是 (选填“①”“②”或“③”)。
3517
3717
2
②
13.(2021·菏泽) 某化学兴趣小组为验证硫酸的部分化学性质,使用氢氧化钠、碳酸钠、金属铝和另外一种不同类别的物质A进行了相关实验。
(1)实验时观察到稀硫酸与A反应有蓝色溶液生成,则A物质是 。
能力提升
CuO
(2)稀硫酸与氢氧化钠溶液反应时没有明显现象,为了证明二者发生了反应,该组同学设计了如图1所示实验,传感器测定的pH和温度随溶液质量变化的情况见图2、图3。
则B溶液是 溶液,图3中的M与图2中X、Y、Z中的
数值相等。
Y
稀硫酸
(3)该化学兴趣小组又做了如右图所示实验:
【提出问题】②号试管中无色溶液的溶质是什么?
【作出猜想】猜想一:硫酸钠 猜想二:硫酸钠、硫酸
猜想三: .
【实验验证】该小组同学用试管取适量
②号试管中的无色溶液,加入一种试剂
后,根据产生的现象推断出了②号试管
中溶质的成分,该试剂是 。
硫酸钠、氢氧化钠
酚酞溶液
【质疑反思】甲同学认为猜想三不能成立,因为①②号试管中溶液混合后烧杯中没有蓝色沉淀生成。
乙同学则认为猜想三是可以成立的,理由是_____________________
________________________________________________________。
①号试管中如果有H2SO4剩余,会与②试管中的NaOH反应,即不会产生Cu(OH)2
14.(2020·广东) 某废酸液主要含H2SO4和FeSO4,该废酸液的Ph
7(选填“<”或“>”)。
15.(2019·广东) 下列常见物质的pH大于7的是( )
A.食醋 B.食盐水 C.氨水 D.柠檬水
<
C
16.(2018·广东) 下列水果中酸度最强的是( )
A.菠萝pH=4.1 B.木瓜pH=5.5
C.草莓pH=3.2 D.柠檬pH=2.3
D
17.(2017·广东) 黄蜂的毒液呈碱性,若被黄蜂蜇了,涂抹下列物质可缓解疼痛的是( )
A.食盐水(pH≈7) B.牙膏(pH≈9)
C.肥皂(pH≈10) D.米醋(pH≈3)
D
同课章节目录
