人教版化学九年级上册 第六单元 课题1金刚石石墨和C60第2课时课件(共21张PPT)
文档属性
| 名称 | 人教版化学九年级上册 第六单元 课题1金刚石石墨和C60第2课时课件(共21张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 4.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-26 13:53:57 | ||
图片预览








文档简介
(共21张PPT)
第二课时 单质碳的化学性质
课题一 金刚石、石墨和C60
清明上河图
导入新课
导入新课
我国古代一些书法家、画家用墨(用炭黑等制成)书写或绘制的字画能够保存很长时间而不变色,这说明……
常温下,碳的化学性质不活泼
1、近期报纸报道,我国考古学者挖掘出一古墓,棺中一千年女尸未腐烂,肌肉有弹性,头上青丝依旧,身上纱衣完好无损,考古学家发现棺木周围埋了足有一米厚的木炭。
2、广告词“钻石恒久远,一颗永流传”的依据是什么?
3、需要长期保存的文书档案,常用碳素墨水书写。
课堂探究
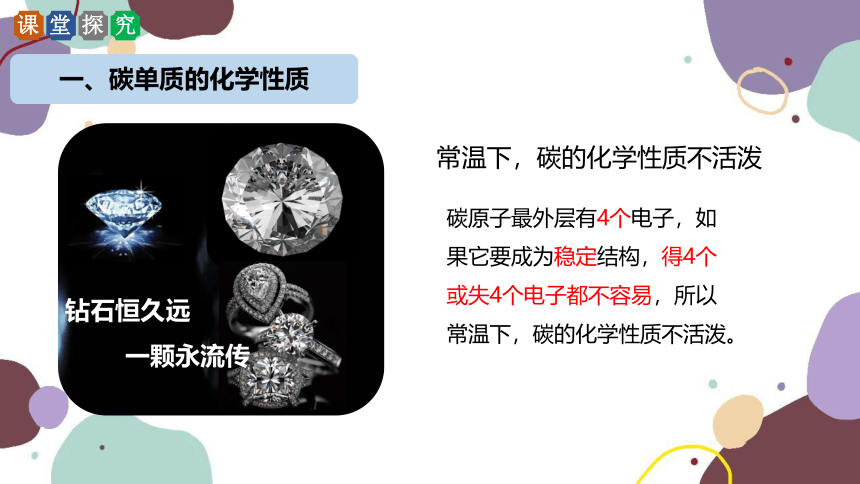
一、碳单质的化学性质
钻石恒久远
一颗永流传
常温下,碳的化学性质不活泼
碳原子最外层有4个电子,如果它要成为稳定结构,得4个或失4个电子都不容易,所以常温下,碳的化学性质不活泼。
课堂探究
1.碳与氧气反应(可燃性)
C + O2 CO2 (放热)
2C + O2 2CO (放热)
实际应用:作燃料
点燃
充分燃烧
不充分燃烧
点燃
回忆木炭在氧气中充分燃烧的现象:
发出白光,放出热量
生成一种能使澄清石灰水变浑浊的气体
你知道吗?
冬季人们为了抵御严寒常常将门窗紧闭,用煤炉来取暖,但往往会发生中毒的事故,这是为什么?使用煤炉应注意什么?
在熊熊燃烧的炭火堆中放几块孔雀石,在灰烬中会有红色的铜出现。
(提示:孔雀石是一种铜矿石,灼烧之后会生成黑色的氧化铜)
2.碳跟某些氧化物的反应(还原性)
实验目的 探究木炭与氧化铜的反应
实验装置
实验步骤
实验现象
1.检查装置的气密性;2.把刚烘干的木炭粉末和氧化铜粉末[氧化铜与木炭的质量比控制在(9~13):1的范围内]混合均匀,小心地铺放进试管;3.将试管固定在铁架台上,导管伸入澄清石灰水中;4.用酒精灯(可以加网罩以使火焰集中并提高温度,最好使用酒精喷灯)加热混合物几分钟;5.撤出导气管,熄灭酒精灯,待试管冷却后再把试管里的粉末倒在纸上。
开始加热时,导管口处有无色气泡逸出,一段时间后,黑色粉末变为红色且澄清石灰水变浑浊。
实验分析
实验结论
化学方程式
注意事项
C + 2CuO 2Cu + CO2↑
高温
开始加热时,试管中的空气因受热体积膨胀而逸出,温度达到高温后,木炭与氧化铜开始反应,生成的铜为红色固体,另一种生成物二氧化碳为无色气体,能使澄清石灰水变浑浊。
碳和氧化铜在高温下反应生成铜和二氧化碳;木炭具有还原性
1.木炭粉末要烘干,目的是排除水蒸气的干扰,使实验现象更明显;
2.固定试管时试管口略向下倾斜,防止药品潮湿产生的水蒸气冷凝回流炸裂试管;
3.开始加热时,导管口处有无色气泡逸出,但澄清石灰水不变浑浊,这是因为刚开始排出的是试管内的空气;
4.实验结束时,应先撤出导管再熄灭酒精灯,防止石灰水倒吸入试管,使试管炸裂;
5.冷却后再把试管里的粉末倒出,防止热的铜被氧化为氧化铜。
碳在高温下可以和某些氧化物反应,夺取这些氧化物里的氧,表现出还原性。
C + 2CuO 2Cu + CO2↑
这种含氧化合物里的氧被夺去的反应叫还原反应
木炭是使氧化铜还原为铜的物质,它具有还原性
工业应用:冶炼金属
高温
对碳的还原性的分析
C + 2CuO 2Cu + CO2↑
高 温
CuO Cu
失氧
氧化铜具有氧化性,是氧化剂
氧化铜在反应中被还原,发生还原反应。
C CO2
得氧
碳具有还原性,是还原剂
碳在反应中被氧化,发生氧化反应
金属的冶炼
3C + 2Fe2O3 4Fe + 3CO2↑
高 温
碳的化学性质
碳的燃烧
还原反应:含氧化合物里的氧被夺去的反应。
还原性:能夺走含氧化合物里氧的物质,具有还原性,碳具有还原性。
氧气充足时,完全燃烧
C+O2 CO2
氧气不足时,不完全燃烧
2C+O2 2CO
高温下,碳能与某些氧化物反应
2CuO+C 2Cu+CO2
高温
常温下,碳的化学性质不活泼
点燃
点燃
课堂小结
1.常温下,碳单质化学性质不活泼。下列用途没有利用这一性质的是( )
A.用墨汁绘画写字
B.用碳素笔书写档案材料
C.铁路枕木表面烧焦碳化
D.用作燃料
D
当堂达标
2.如图是木炭与氧化铜反应的实验装置图,下列说法错误的是 ( )
B
A.该实验需要较高温度
B.木炭发生了还原反应
C.实验前应把木炭粉充分烘干
D.该实验中的木炭粉可以换成活性炭
3.下列碳单质的各种用途中,利用了其化学性质的是( )
C
A.制作钻头 B.制作电极
C.冶炼金属 D.作冰箱除味剂
4.下列说法错误的是( )
A.木炭燃烧可放出大量的热,能用作燃料
B.碳和氧气反应时生成物一定是二氧化碳
C.碳的几种单质具有相似的化学性质
D.可利用焦炭的还原性冶炼金属
B
5.如图是木炭与氧化铜反应的装置图,请回答问题。
(1)木炭与氧化铜的颜色都是________。
(2)在高温条件下,试管中的固体逐渐变为光亮的______色,说明生成了________;澄清石灰水变________,说明生成了____________。
(3)写出试管中发生反应的化学方程式:
。
黑色
紫红
铜
浑浊
二氧化碳
C + 2CuO 2Cu + CO2↑
高 温
6.若8g氧化铜被木炭还原,试计算能生成铜的质量是多少。
解:设8g氧化铜被木炭还原,能生成铜的质量为x。
160 128
8g x
C + 2CuO 2Cu + CO2↑
高 温
x=6.4g
160
128
8g
x
=
答:8g氧化铜被木炭还原,能生成铜的质量为6.4g。
x=8g×
160
128
第二课时 单质碳的化学性质
课题一 金刚石、石墨和C60
清明上河图
导入新课
导入新课
我国古代一些书法家、画家用墨(用炭黑等制成)书写或绘制的字画能够保存很长时间而不变色,这说明……
常温下,碳的化学性质不活泼
1、近期报纸报道,我国考古学者挖掘出一古墓,棺中一千年女尸未腐烂,肌肉有弹性,头上青丝依旧,身上纱衣完好无损,考古学家发现棺木周围埋了足有一米厚的木炭。
2、广告词“钻石恒久远,一颗永流传”的依据是什么?
3、需要长期保存的文书档案,常用碳素墨水书写。
课堂探究
一、碳单质的化学性质
钻石恒久远
一颗永流传
常温下,碳的化学性质不活泼
碳原子最外层有4个电子,如果它要成为稳定结构,得4个或失4个电子都不容易,所以常温下,碳的化学性质不活泼。
课堂探究
1.碳与氧气反应(可燃性)
C + O2 CO2 (放热)
2C + O2 2CO (放热)
实际应用:作燃料
点燃
充分燃烧
不充分燃烧
点燃
回忆木炭在氧气中充分燃烧的现象:
发出白光,放出热量
生成一种能使澄清石灰水变浑浊的气体
你知道吗?
冬季人们为了抵御严寒常常将门窗紧闭,用煤炉来取暖,但往往会发生中毒的事故,这是为什么?使用煤炉应注意什么?
在熊熊燃烧的炭火堆中放几块孔雀石,在灰烬中会有红色的铜出现。
(提示:孔雀石是一种铜矿石,灼烧之后会生成黑色的氧化铜)
2.碳跟某些氧化物的反应(还原性)
实验目的 探究木炭与氧化铜的反应
实验装置
实验步骤
实验现象
1.检查装置的气密性;2.把刚烘干的木炭粉末和氧化铜粉末[氧化铜与木炭的质量比控制在(9~13):1的范围内]混合均匀,小心地铺放进试管;3.将试管固定在铁架台上,导管伸入澄清石灰水中;4.用酒精灯(可以加网罩以使火焰集中并提高温度,最好使用酒精喷灯)加热混合物几分钟;5.撤出导气管,熄灭酒精灯,待试管冷却后再把试管里的粉末倒在纸上。
开始加热时,导管口处有无色气泡逸出,一段时间后,黑色粉末变为红色且澄清石灰水变浑浊。
实验分析
实验结论
化学方程式
注意事项
C + 2CuO 2Cu + CO2↑
高温
开始加热时,试管中的空气因受热体积膨胀而逸出,温度达到高温后,木炭与氧化铜开始反应,生成的铜为红色固体,另一种生成物二氧化碳为无色气体,能使澄清石灰水变浑浊。
碳和氧化铜在高温下反应生成铜和二氧化碳;木炭具有还原性
1.木炭粉末要烘干,目的是排除水蒸气的干扰,使实验现象更明显;
2.固定试管时试管口略向下倾斜,防止药品潮湿产生的水蒸气冷凝回流炸裂试管;
3.开始加热时,导管口处有无色气泡逸出,但澄清石灰水不变浑浊,这是因为刚开始排出的是试管内的空气;
4.实验结束时,应先撤出导管再熄灭酒精灯,防止石灰水倒吸入试管,使试管炸裂;
5.冷却后再把试管里的粉末倒出,防止热的铜被氧化为氧化铜。
碳在高温下可以和某些氧化物反应,夺取这些氧化物里的氧,表现出还原性。
C + 2CuO 2Cu + CO2↑
这种含氧化合物里的氧被夺去的反应叫还原反应
木炭是使氧化铜还原为铜的物质,它具有还原性
工业应用:冶炼金属
高温
对碳的还原性的分析
C + 2CuO 2Cu + CO2↑
高 温
CuO Cu
失氧
氧化铜具有氧化性,是氧化剂
氧化铜在反应中被还原,发生还原反应。
C CO2
得氧
碳具有还原性,是还原剂
碳在反应中被氧化,发生氧化反应
金属的冶炼
3C + 2Fe2O3 4Fe + 3CO2↑
高 温
碳的化学性质
碳的燃烧
还原反应:含氧化合物里的氧被夺去的反应。
还原性:能夺走含氧化合物里氧的物质,具有还原性,碳具有还原性。
氧气充足时,完全燃烧
C+O2 CO2
氧气不足时,不完全燃烧
2C+O2 2CO
高温下,碳能与某些氧化物反应
2CuO+C 2Cu+CO2
高温
常温下,碳的化学性质不活泼
点燃
点燃
课堂小结
1.常温下,碳单质化学性质不活泼。下列用途没有利用这一性质的是( )
A.用墨汁绘画写字
B.用碳素笔书写档案材料
C.铁路枕木表面烧焦碳化
D.用作燃料
D
当堂达标
2.如图是木炭与氧化铜反应的实验装置图,下列说法错误的是 ( )
B
A.该实验需要较高温度
B.木炭发生了还原反应
C.实验前应把木炭粉充分烘干
D.该实验中的木炭粉可以换成活性炭
3.下列碳单质的各种用途中,利用了其化学性质的是( )
C
A.制作钻头 B.制作电极
C.冶炼金属 D.作冰箱除味剂
4.下列说法错误的是( )
A.木炭燃烧可放出大量的热,能用作燃料
B.碳和氧气反应时生成物一定是二氧化碳
C.碳的几种单质具有相似的化学性质
D.可利用焦炭的还原性冶炼金属
B
5.如图是木炭与氧化铜反应的装置图,请回答问题。
(1)木炭与氧化铜的颜色都是________。
(2)在高温条件下,试管中的固体逐渐变为光亮的______色,说明生成了________;澄清石灰水变________,说明生成了____________。
(3)写出试管中发生反应的化学方程式:
。
黑色
紫红
铜
浑浊
二氧化碳
C + 2CuO 2Cu + CO2↑
高 温
6.若8g氧化铜被木炭还原,试计算能生成铜的质量是多少。
解:设8g氧化铜被木炭还原,能生成铜的质量为x。
160 128
8g x
C + 2CuO 2Cu + CO2↑
高 温
x=6.4g
160
128
8g
x
=
答:8g氧化铜被木炭还原,能生成铜的质量为6.4g。
x=8g×
160
128
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
