专题2第二单元溶液组成的定量研究同步练习 (含解析)2022-2023学年上学期高一化学苏教版(2019)必修第一册
文档属性
| 名称 | 专题2第二单元溶液组成的定量研究同步练习 (含解析)2022-2023学年上学期高一化学苏教版(2019)必修第一册 |

|
|
| 格式 | docx | ||
| 文件大小 | 826.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-27 00:00:00 | ||
图片预览




文档简介
专题2第二单元溶液组成的定量研究同步练习
一、单选题
1. 下列叙述不正确的是( )
A. 质量分数为的,用水稀释后的质量分数大于
B. 用浓硫酸配制一定物质的量浓度的稀硫酸时,量取浓硫酸时仰视量筒,会使所配溶液浓度偏小
C. 配制的溶液,需用容量瓶
D. 同温同压下和所含的原子数之比为:
2. 室温时,甲、乙两同学配制氯化钠溶液。甲同学配制的溶液,乙同学配制的溶液时,氯化钠的溶解度为。下列说法正确的是
A. 两同学所需溶质的质量相同 B. 两同学所配溶液的质量相同
C. 两同学所需实验仪器种类相同 D. 甲同学所配溶液的物质的量浓度比乙同学的大
3. 某金属的氯化物的摩尔质量为,溶解度为,现取质量为的,在一定温度下完全溶解配成饱和溶液,若溶液的密度为,溶液的物质的量浓度为,溶液中溶质的质量分数为,则下列关系式中不正确的是( )
A. B.
C. D.
4. 将溶质质量分数为,物质的量浓度为的浓硫酸加入到水中,稀释后得到的溶质的质量分数为,物质的量浓度为的稀溶液。下列正确的是
A. 若则 B. 若则
C. 若则 D. 若则
5. 在环保、化工行业有一种溶液浓度的表示方法:质量体积浓度,用单位体积溶液中所含的溶质质量数来表示,单位或。现有一种时的饱和溶液,密度为,质量体积浓度为,则对此溶液的说法不正确的是
A. 该溶液的质量分数为
B. 该溶液的物质的量浓度为
C. 在时,硫酸铜的溶解度为
D. 在时把溶解于水中恰好得到饱和溶液
6. 某温度下,物质的饱和溶液密度为,,溶质的质量分数为,溶质的摩尔质量为,溶解度为,下列表达式正确的是
A. B. C. D.
7. 如图是配制一定物质的量浓度溶液的过程示意图。下列说法中错误的是( )
A. 所配制的溶液的物质的量浓度为
B. 操作是将溶解并放置至室温的溶液转移到容量瓶中
C. 操作如果仰视,会使配得溶液的浓度偏低
D. 操作中,定容摇匀后发现液面低于刻度线,继续加水至液面与刻度线相切
8. 向某浓度的溶液中投入铁片,充分反应后过滤、洗涤、干燥后得到固体的质量为。则该硫酸铜溶液的物质的量浓度为( )
A. B. C. D.
9. 实验室用固体配制的溶液。下列说法正确的是 ( )
A. 配制溶液时需用到的容量瓶
B. 配制溶液时需称量固体的质量为
C. 定容时俯视刻度线,所配制的溶液浓度偏大
D. 定容摇匀静置后,液面低于刻度线,再加蒸馏水至刻度线
10. 在时,将完全溶于水,得到溶液,假设该溶液的密度为,质量分数为,其中含的物质的量为。下列叙述中正确的是 ( )
A. 溶质的质量分数为
B. 溶质的物质的量浓度
C. 溶液中
D. 上述溶液中再加入水后,所得溶液的质量分数大于
11. 如图所示是配制一定物质的量浓度溶液的过程示意图。下列说法中错误的是( )
A. 所配制的溶液的物质的量浓度为
B. 操作是将溶解的溶液转移到容量瓶中
C. 操作如果仰视,结果配得溶液浓度偏低
D. 操作中,定容摇匀后发现液面低于刻度线,要继续加水至液面与刻度线平齐
12. 现实验室需要用质量分数:、密度:的浓硫酸配制的稀硫酸,下列说法中正确的是( )
A. 该浓硫酸的物质的量浓度为
B. 需要该浓硫酸的体积为
C. 配制稀硫酸时,将量好的浓硫酸注入容量瓶中,并加入适量的水
D. 该同学实际配制得到的浓度为,可能的原因是用量筒量取浓硫酸时仰视刻度线
13. 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此,下列说法错误的是
A. 该硫酸的物质的量浓度为
B. 该硫酸与等体积的水混合所得溶液的质量分数大于
C. 该硫酸与等体积的水混合所得溶液的浓度大于
D. 实验需要的稀硫酸,配制时需量取该浓硫酸
14. 相对分子质量为的气态化合物标准状况,溶于水中,得到质量分数为、物质的量浓度为、密度为的溶液,下列说法正确的是( )
A. 溶液密度 B. 物质的量浓度
C. 溶液的质量分数 D. 相对分子质量
15. 某同学参阅了“消毒液”说明中的配方,欲用固体配制含密度为的消毒液。下列说法正确的是( )
A. 配制过程中只需要三种仪器即可完成
B. 所配得的消毒液在空气中经光照、久置后,溶液中的物质的量浓度减小
C. 容量瓶用蒸馏水洗净后必须烘干才可用于溶液的配制
D. 需要称量的固体的质量为
二、实验题
16. 如图为实验室某浓盐酸试剂瓶标签上的有关数据:
试根据标签上的有关数据,回答下列问题:
取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是 ________。
A.溶液中的物质的量 溶液的浓度
C.溶液中的数目 溶液的密度
某学生欲用上述浓盐酸和蒸馏水配制物质的量浓度为的稀盐酸。
可供选用的仪器有:胶头滴管;玻璃棒;烧杯;药匙;量筒;托盘天平。
请回答下列问题:
配制稀盐酸时,还缺少的仪器有 ____________写仪器名称;该仪器上标有以下五项中的_____________;
A、温度 、浓度 、容积 、压强 、刻度线
该学生需要量取________上述浓盐酸进行配制。
在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?填“偏大”、“偏小”、“无影响”。
定容时俯视观察刻度线________。
量筒量取浓盐酸后再用蒸馏水洗涤次,并将洗液移入容量瓶中________。
17. “消毒液”能有效杀灭新型冠状病毒,某同学购买了一瓶“威露士”牌“消毒液”,该消毒液通常稀释倍体积比使用。查阅相关资料和消毒液包装说明得知其有效成分的浓度为,请回答下列问题:
某同学取该“消毒液”,按要求稀释后用于消毒,稀释后的溶液中__________。
该同学参阅该“消毒液”的配方,欲用固体配制含物质的量浓度为的消毒液已知的摩尔质量为:。请回答下列问题:
下图是该同学的部分配置过程,该同学的错误步骤有__________
下列实验过程中的说法不正确的是__________
A.用试纸检验配制好的溶液的酸碱性
B.将称量好的固体在烧杯中溶解后应立即转入容量瓶
C.容量瓶在使用前必须检查其是否漏水
D.需要称量固体的质量为
一瓶规格为上述“威露士”牌“消毒液”能吸收空气中__________的标准状况而变质。已知:
“消毒液”与稀硫酸混合使用可增强消毒能力,某消毒人员用的浓硫酸配制 的稀硫酸用于增强“消毒液”的消毒能力,请写出该原理的离子方程式___________________。
在配制过程中,下列操作中能使所配溶液的浓度偏高的有__________填代号。
用量筒量取的硫酸时俯视
洗涤量取浓硫酸的量筒,并将洗涤液转移到容量瓶中
未等稀释后的溶液冷却至室温就转移到容量瓶中
转移前,容量瓶中含有少量蒸馏水
定容时,加蒸馏水超过标线,又用胶头滴管吸出
定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
定容时,仰视刻度线
三、简答题
18. 鲜花是美丽的,但是美丽的鲜花的保鲜期却很短,在花瓶中加入“鲜花保鲜剂”却可以延长鲜花的寿命。
下表是“鲜花保鲜剂”的成分其中阿司匹林不含,其存在也不会干扰成分中其他离子的检验,回答下列问题:
成分 蔗糖 硫酸钾 阿司匹林 高锰酸钾
质量
摩尔质量
“鲜花保鲜剂”中物质的量浓度最大的成分是____________填写名称。
“鲜花保鲜剂”中的物质的量浓度为____________只要求写表达式,不用化简,不需计算。
如图所示的仪器中,在配制一定物质的量浓度的“鲜花保鲜剂”溶液时肯定不需要的是____________
填字母,还缺少的玻璃仪器有___________________填仪器名称。
市面上,有一种营养液可用于无土栽培,该营养液中有和,其中的浓度为,的浓度为,则该营养液中_____。
19. 根据要求,回答下列问题:
Ⅰ如图为实验室某浓盐酸试剂瓶标签上的有关数据。
盐酸分子式: 相对分子质量: 密度: 的质量分数:
该浓盐酸中,的物质的量浓度为______。
取用任意体积的该浓盐酸时,下列物理量中不随所取体积的多少而变化的是______填标号。
A.溶液的密度 溶质的物质的量
C.溶质的物质的量浓度 溶液中的物质的量
用该浓盐酸和蒸馏水配制物质的量浓度为的稀盐酸。
需量取______该浓盐酸进行配制保留位小数。
在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?填“偏高”、“偏低”或“无影响”
用量筒量取浓盐酸时俯视观察凹液面:______。定容后经振荡、摇匀、静置,发现液面略有下降,再加适量的蒸馏水到容量瓶颈部的刻度线:______。
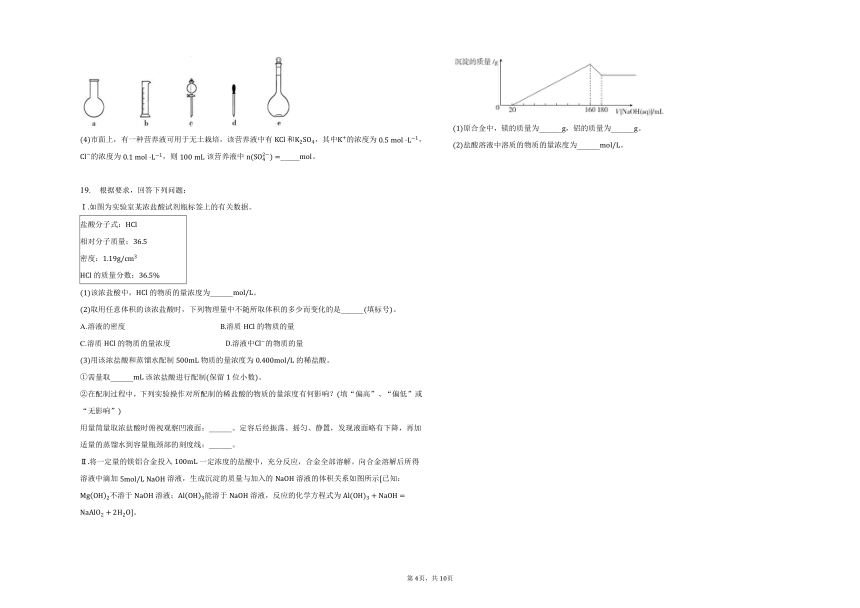
Ⅱ将一定量的镁铝合金投入一定浓度的盐酸中,充分反应,合金全部溶解。向合金溶解后所得溶液中滴加溶液,生成沉淀的质量与加入的溶液的体积关系如图所示已知:不溶于溶液;能溶于溶液,反应的化学方程式为。
原合金中,镁的质量为______,铝的质量为______。
盐酸溶液中溶质的物质的量浓度为______。
答案和解析
1.【答案】
【解析】
【分析】
本题考查物质的量的计算、溶液配制,题目难度不大,明确溶液配制方法为解答关键,注意掌握物质的量与其它物理量之间的关系,试题侧重考查学生的分析能力及化学实验、化学计算能力。
【解答】
A.浓硫酸的密度大于水的密度,加水后浓硫酸质量分数为:,故A正确;
B.用浓硫酸配制一定物质的量浓度的稀硫酸时,量取浓硫酸时仰视量筒,量取的浓硫酸体积偏大,导致所配溶液浓度偏大,故B错误;
C.实验室没有的容量瓶,应用的容量瓶进行配制,故C正确;
D.同温同压下,气体的体积比等于气体分子的物质的量比,则和的物质的量之比为::,含有的原子数之比为::,故D正确。
2.【答案】
【解析】
【分析】本题主要考查了物质的量浓度的相关知识,同时考查了质量分数的知识,解答本题的关键是掌握物质的量浓度的计算方法,一定物质的量浓度溶液的配制方法。
【解答】配制的溶液需要氯化钠的质量为,配制的溶液需要氯化钠的质量为,两同学所需氯化钠的质量不相等,A错误;
B.氯化钠溶液的密度大于,氯化钠溶液的质量大于,B错误;
C.配制一定质量分数的氯化钠溶液,需要用天平称量氯化钠的质量,用药匙取药品,用量筒量取水的体积,在烧杯内溶解,并用玻璃棒搅拌,所需仪器有托盘天平、量筒、烧杯、玻璃棒、药匙等;配制一定体积、一定物质的量浓度的氯化钠溶液,需要用天平称量氯化钠的质量,用药匙取药品,在烧杯内溶解,用玻璃棒搅拌,洗涤后移入容量瓶,加水定容,液面距离刻度线时改用胶头滴管滴加,所需仪器有托盘天平、烧杯、玻璃棒、药匙、容量瓶、胶头滴管等,两同学需要的仪器不完全相同,C错误;
D.配制的溶液,其密度大于,所以溶液的体积小于,的溶液中氯化钠的物质的量为,其浓度大于,D正确。
3.【答案】
【解析】
【分析】
本题考查物质的量浓度、质量分数、溶解度之间的换算关系,解答这类问题应熟练掌握各物理量之间的转化关系,试题难度一般。
【解答】
A.根据物质的量浓度的定义可知,故A正确;
B.根据物质的量浓度与质量分数的换算关系可知氯离子的物质的量浓度为,故B错误;
C.根据物质的量浓度与质量分数的换算关系可知,故C正确;
D.根据题目信息结合溶解度的知识可得,解得 ,故D正确。
故选B。
4.【答案】
【解析】
【分析】
本题旨在考查学生对化学计量的综合计算的应用,整体难度较大,掌握溶液稀释前后溶质质量、物质的量均不变是解答本题的关键。
【解答】
A. 稀释前后溶质的质量不变,则,若,则稀释后溶液的质量为,所以稀释时加入水的质量为,水的密度为,所以水的体积,,,稀释后溶液密度变小,故,故A错误;
B. 由中分析可知,水的体积,,故B错误;
,则,若,,溶液稀释后密度减小,则,则稀释后溶液的质量小于,所以水的体积,故C正确;
B. 由中分析可知,水的体积,,故D错误.
故选C。
5.【答案】
【解析】
【分析】
本题考查化学的综合计算,注意饱和溶液、质量分数、溶解度、物质的量浓度的概念理解和相关公式的应用,难度一般。
【解答】
A.该溶液的溶质质量分数 ,故A正确;
B.该溶液的物质的量浓度,故B正确;
C.根据硫酸铜溶液在的饱和溶液的溶质质量分数为可知, ,解得溶解度,故C正确;
D.中含有结晶水,溶于水使得溶剂的质量大于,溶质为,溶质的质量小于,因此不能得到饱和溶液,故D错误。
故选D。
6.【答案】
【解析】
【分析】本题主要考查的是化学计量之间的转化关系,要求学生具有利用字母进行计算的能力,掌握物质的量浓度、溶液质量分数、溶液密度、溶解度之间的关系式是解题的关键。
【解答】,则该物质的浓度,根据可知,,,故A、C错误;
根据溶解度的定义,有,可知,故B错误,D正确。
故选D。
7.【答案】
【解析】
【分析】
本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,难度不大。
【解答】
A、由图可知,所配溶液的体积为,碳酸钠的物质的量为,所配碳酸钠溶液的浓度为,故A正确;
B、溶解并放置至室温后再移液,故操作是移液,故B正确;
C、操作是定容,定容时仰视导致溶液体积偏高,会使配得溶液的浓度偏低,故C正确;
D、定容摇匀后发现液面低于刻度线是正常现象,再加水至液面与刻度线平齐,导致所配溶液的体积偏大,所配溶液的浓度偏小,故D错误。
故选:。
8.【答案】
【解析】设实际过程中反应的铁为,消耗的的物质的量为。
铁片增重
,解得:,说明铁片有剩余,已经全部反应,故需以的量进行计算,,解得:,故C溶液的物质的量浓度,故选C。
9.【答案】
【解析】
【分析】
本题考查了一定物质的量浓度溶液的配制,明确配制原理及操作步骤是解题关键,注意容量瓶规格选择依据。
【解答】
A.配制的溶液,实验室没有容量瓶,应选择容量瓶,故A错误;
B.配制的溶液,实验室没有容量瓶,应选择容量瓶,需要氢氧化钠质量为:,故B错误;
C.定容时俯视刻度线,导致溶液体积偏小,依据可知,溶液浓度偏大,故C正确;
D.定容摇匀静置后,液面低于刻度线,再加蒸馏水至刻度线,导致溶液体积偏大,溶液浓度偏低,故D错误。
故选C。
10.【答案】
【解析】
【分析】
本题主要考查的是化学计量的综合计算,涉及质量分数计算、物质的量浓度计算、溶液稀释的计算、水的电离等知识,意在考查学生的分析能力和知识应用能力。
【解答】
A.溶质的质量分数为,故A错误;
B.溶质的物质的量浓度,故B正确;
C.根据电荷守恒可知,溶液中,故C错误;
D.氨水的密度比水小,则上述溶液中再加入水后,溶液质量大于原来溶液质量的倍,故所得溶液的质量分数小于,故D错误。
故选B。
11.【答案】
【解析】
【分析】
本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,难度不大。
【解答】
A. 由图可知,所配溶液的体积为,碳酸钠的物质的量为,所配碳酸钠溶液的浓度为,故A正确;
B. 溶解并放置至室温后再移液,故操作是移液,故B正确;
C. 操作是定容,如果仰视,导致所配溶液的体积偏大,所配得溶液浓度偏小,故C正确;
D. 定容摇匀后发现液面低于刻度线,少量溶液残留在瓶塞与瓶口之间,再加水至液面与刻度线平齐,导致所配溶液的体积偏大,所配溶液的浓度偏小,故D错误。
故选:。
12.【答案】
【解析】
【分析】
本题考查了一定物质的量浓度溶液的配制,明确配制原理和过程是解题关键,注意误差分析的方法,题目难度不大。
【解答】
A.质量分数:,密度:的浓硫酸,物质的量浓度为,物质的量浓度的单位是,故A错误;
B.配制的稀硫酸,应选择容量瓶,设需要浓硫酸体积为,则依据溶液稀释过程中溶质物质的量不变得:,解得,故B错误;
C.容量瓶为精密仪器,不能用于稀释浓溶液,应在烧杯中稀释然后转移到容量瓶,故C错误;
D.该同学实际配制得到的浓度为,可能的原因是量筒量取浓硫酸时仰视刻度线,导致量取浓硫酸体积偏大,溶质物质的量偏大,依据可知,溶液浓度偏大,故D正确。
13.【答案】
【解析】
【分析】
本题考查物质的量浓度的计算,题目难度中等,注意掌握物质的量浓度与溶质质量分数的关系,注意硫酸的密度比水大,且浓度越大密度越大。
【解答】
A. 该硫酸的物质的量浓度为,A正确;
B. 该硫酸与等体积的水混合所得溶液的质量分数为,B正确;
C. 该硫酸与等体积的水设各为混合,所得溶液的体积小于,所得溶液的浓度大于,C正确;
D. 实验需要的稀硫酸,配制时应选择的容量瓶,需量取该浓硫酸的体积为,D错误。
14.【答案】
【解析】
【分析】
本题考查了物质的量浓度、溶质质量分数、相对分子量、溶液密度的计算,题目难度中等,注意掌握物质的量浓度与溶质的质量分数的概念及计算方法,试题培养了学生灵活应用所学知识的能力。
【解答】
A.设溶液的体积为,则溶液中溶质的质量为:,该溶液的质量为:,溶液的密度为:,故A错误;
B.溶液体积为:,溶质的物质的量为:,该溶液的浓度为:,故B错误;
C.溶液中溶质的质量为:,溶液质量为:,则溶质的质量分数为:,故C错误;
D.溶质质量分数为,则水的质量分数为:,水的质量为,则溶液的质量为:,溶质的质量为:,溶质的物质的量为:,则该化合物的摩尔质量为:,则该化合物的相对分子量为:,故D正确。
故选D。
15.【答案】
【解析】
【分析】
本题主要考查溶液配制的步骤、仪器以及误差分析等,难度不是很大,注意计算溶质的质量时,溶液的体积按计算。即如果配制的溶液体积和实验室中容量瓶的规格不符时,容量瓶应该选取比要配制的体积大且最接近的规格的容量瓶。
【解答】
A. 配制过程需要托盘天平、烧杯、玻璃棒、容量瓶和胶头滴管五种仪器即可完成,故A错误;
B. 由于易吸收空气中的、而变质,所以消毒液变质导致减少,配制的溶液中溶质的物质的量减小,则溶液的物质的量浓度偏小,故B正确;
C. 容量瓶中有水,对溶液的体积无影响,所以经洗涤干净的容量瓶不必烘干后再使用,故C错误;
D. 应选取的容量瓶进行配制,然后取出即可,所以需要的质量:,故D错误。
故选B。
16.【答案】
容量瓶;
;
偏大;偏大
【解析】
【分析】
本题主要考查物质的量浓度的定义和一定物质的量浓度溶液的配制实验操作及误差分析,难度不大。
【解答】
溶液中的物质的量大小取决于溶液体积的大小与溶液浓度,故A错误;
溶液具有均一性,溶液的浓度是与体积无关的,故B正确;
溶液中的数目与溶液浓度、溶液体积大小及溶质的化学式组成有关,故C错误;
溶液具有均一性,溶液的密度是与体积无关的,故D正确;
所以此题选BD。
配制物质的量浓度为的稀盐酸的步骤有:计算、量取、稀释、冷却、转移、洗涤、定容、摇匀等,则使用的仪器有:量筒、烧杯、玻璃棒、容量瓶、胶头滴管等,还缺少的仪器有:容量瓶;
容量瓶标有:温度、容积、刻度线;
故此题的答案是:容量瓶; ;
浓盐酸中的物质的量浓度为,
配制物质的量浓度为的稀盐酸,设需要浓盐酸的体积为,根据溶液稀释过程中溶液的物质的量不变得:
,计算得出:;
故本题正确答案为;
定容时俯视容量瓶刻度线,导致溶液体积偏小,溶液浓度偏大;
洗涤量筒,溶质的物质的量偏大,溶液浓度偏大,
故答案为:偏大;偏大。
17.【答案】
【解析】
【分析】
本题考查物质的量浓度的计算、溶液的配制,题目难度中等,注意掌握物质的量浓度的计算方法及表达式、配制一定物质的量浓度溶液的方法是解题的关键,试题培养了学生的分析能力及化学计算能力。
【解答】
稀释倍后;
中物品和砝码的位置放反了,故错误;
溶解步骤,正确;
转移时要用玻璃棒进行引流,故错误;
定容时胶头滴管不能伸入容量瓶内,故错误。
故答案为:;
溶液具有强氧化性,可将试纸漂白,不能用试纸测其,故错误;
B.溶解后应静置至室温后转入容量瓶,故错误;
C.容量瓶在使用前必须检查其是否漏水,故正确;
D.实验室无容量瓶,所以选择容量瓶,用托盘天平称量时,应记录至小数点后一位,则需要称量固体的质量为,故正确。
故答案为:;
一瓶规格为上述“威露士”牌“消毒液”中,则由方程式可知也为,标准状况下体积为;
“消毒液”与稀硫酸混合使用可增强消毒能力,是因为生成,离子方程式为;
用量筒量取的硫酸时俯视,则所取的的硫酸体积偏小,硫酸的物质的量偏小,所配浓度偏低,故不选;
洗涤量取浓硫酸的量筒,并将洗涤液转移到容量瓶中,导致硫酸的物质的量偏大,溶液浓度偏高,故选;
未等稀释后的 溶液冷却至室温就转移到容量瓶中,冷却后溶液体积偏小,溶液浓度偏高,故选;
转移前,容量瓶中含有少量蒸馏水,对溶质物质的量和溶液体积都不产生影响,溶液浓度无影响,故不选;
定容时,加蒸馏水超过标线,又用胶头滴管吸出,导致溶质物质的量偏小,溶液浓度偏低,故不选;
定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线,导致溶液体积偏大,溶液浓度偏低,故不选;
定容时,仰视刻度线,导致溶液体积偏大,溶液浓度偏低,故不选;
故选。
18.【答案】蔗糖 ;玻璃棒、烧杯
【解析】蔗糖,硫酸钾,阿司匹林
,高锰酸钾,所以“鲜花保鲜剂”中物质的量浓度最大的成分是蔗糖。
硫酸钾高锰酸钾。
配制一定物质的量浓度的溶液所需要的仪器包括托盘天平、量筒、烧杯、玻璃棒、容量瓶、胶头滴管,不需要使用烧瓶和分液漏斗。
根据电荷守恒,,。
19.【答案】Ⅰ
;偏低;偏低
Ⅱ;
【解析】
【分析】
Ⅰ本题考查一定物质的量浓度盐酸溶液的配制、计算和误差分析,难度一般,属于基础内容,细心即可。
Ⅱ本题考查镁铝合金与酸碱反应的计算,对于图像的数据分析尤为重要,属于常考题型,难度一般。
【解答】
Ⅰ该浓盐酸中,的物质的量浓度,故答案为:;
溶液是均匀的,溶液的密度、浓度不随体积变化,而的物质的量和的物质的量均与溶液体积有关。
故选AC。
设需要浓盐酸的体积为,根据稀释定律,稀释前后的物质的量不变,则,解得,故答案为:;
用量筒量取浓盐酸时俯视观察凹液面,使量取的浓盐酸体积偏小,所配制的稀盐酸的物质的量浓度偏低;定容后经振荡、摇匀、静置,发现液面略有下降,再加适量的蒸馏水到容量瓶颈部的刻度线,最终加入蒸馏水的体积偏大,所配制的稀盐酸的物质的量浓度偏低;故答案为:偏低;偏低;
Ⅱ由图可知,加入溶液阶段没有沉淀生成,是因为溶液与剩余的盐酸反应,反应的化学方程式为: ;过程中是沉淀的溶解过程,能溶解于溶液的沉淀是,反应方程式为:,该阶段消耗的的物质的量为:,则的物质的量为,故,;根据 ,可知过程中生成的消耗的物质的量为,则与反应的物质的量为:,得出的物质的量为,合金中的质量为;故答案为:;;
在沉淀达到最大的时候,溶液中的溶质为,,的物质的量浓度为:。故答案为:。
第1页,共1页
一、单选题
1. 下列叙述不正确的是( )
A. 质量分数为的,用水稀释后的质量分数大于
B. 用浓硫酸配制一定物质的量浓度的稀硫酸时,量取浓硫酸时仰视量筒,会使所配溶液浓度偏小
C. 配制的溶液,需用容量瓶
D. 同温同压下和所含的原子数之比为:
2. 室温时,甲、乙两同学配制氯化钠溶液。甲同学配制的溶液,乙同学配制的溶液时,氯化钠的溶解度为。下列说法正确的是
A. 两同学所需溶质的质量相同 B. 两同学所配溶液的质量相同
C. 两同学所需实验仪器种类相同 D. 甲同学所配溶液的物质的量浓度比乙同学的大
3. 某金属的氯化物的摩尔质量为,溶解度为,现取质量为的,在一定温度下完全溶解配成饱和溶液,若溶液的密度为,溶液的物质的量浓度为,溶液中溶质的质量分数为,则下列关系式中不正确的是( )
A. B.
C. D.
4. 将溶质质量分数为,物质的量浓度为的浓硫酸加入到水中,稀释后得到的溶质的质量分数为,物质的量浓度为的稀溶液。下列正确的是
A. 若则 B. 若则
C. 若则 D. 若则
5. 在环保、化工行业有一种溶液浓度的表示方法:质量体积浓度,用单位体积溶液中所含的溶质质量数来表示,单位或。现有一种时的饱和溶液,密度为,质量体积浓度为,则对此溶液的说法不正确的是
A. 该溶液的质量分数为
B. 该溶液的物质的量浓度为
C. 在时,硫酸铜的溶解度为
D. 在时把溶解于水中恰好得到饱和溶液
6. 某温度下,物质的饱和溶液密度为,,溶质的质量分数为,溶质的摩尔质量为,溶解度为,下列表达式正确的是
A. B. C. D.
7. 如图是配制一定物质的量浓度溶液的过程示意图。下列说法中错误的是( )
A. 所配制的溶液的物质的量浓度为
B. 操作是将溶解并放置至室温的溶液转移到容量瓶中
C. 操作如果仰视,会使配得溶液的浓度偏低
D. 操作中,定容摇匀后发现液面低于刻度线,继续加水至液面与刻度线相切
8. 向某浓度的溶液中投入铁片,充分反应后过滤、洗涤、干燥后得到固体的质量为。则该硫酸铜溶液的物质的量浓度为( )
A. B. C. D.
9. 实验室用固体配制的溶液。下列说法正确的是 ( )
A. 配制溶液时需用到的容量瓶
B. 配制溶液时需称量固体的质量为
C. 定容时俯视刻度线,所配制的溶液浓度偏大
D. 定容摇匀静置后,液面低于刻度线,再加蒸馏水至刻度线
10. 在时,将完全溶于水,得到溶液,假设该溶液的密度为,质量分数为,其中含的物质的量为。下列叙述中正确的是 ( )
A. 溶质的质量分数为
B. 溶质的物质的量浓度
C. 溶液中
D. 上述溶液中再加入水后,所得溶液的质量分数大于
11. 如图所示是配制一定物质的量浓度溶液的过程示意图。下列说法中错误的是( )
A. 所配制的溶液的物质的量浓度为
B. 操作是将溶解的溶液转移到容量瓶中
C. 操作如果仰视,结果配得溶液浓度偏低
D. 操作中,定容摇匀后发现液面低于刻度线,要继续加水至液面与刻度线平齐
12. 现实验室需要用质量分数:、密度:的浓硫酸配制的稀硫酸,下列说法中正确的是( )
A. 该浓硫酸的物质的量浓度为
B. 需要该浓硫酸的体积为
C. 配制稀硫酸时,将量好的浓硫酸注入容量瓶中,并加入适量的水
D. 该同学实际配制得到的浓度为,可能的原因是用量筒量取浓硫酸时仰视刻度线
13. 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此,下列说法错误的是
A. 该硫酸的物质的量浓度为
B. 该硫酸与等体积的水混合所得溶液的质量分数大于
C. 该硫酸与等体积的水混合所得溶液的浓度大于
D. 实验需要的稀硫酸,配制时需量取该浓硫酸
14. 相对分子质量为的气态化合物标准状况,溶于水中,得到质量分数为、物质的量浓度为、密度为的溶液,下列说法正确的是( )
A. 溶液密度 B. 物质的量浓度
C. 溶液的质量分数 D. 相对分子质量
15. 某同学参阅了“消毒液”说明中的配方,欲用固体配制含密度为的消毒液。下列说法正确的是( )
A. 配制过程中只需要三种仪器即可完成
B. 所配得的消毒液在空气中经光照、久置后,溶液中的物质的量浓度减小
C. 容量瓶用蒸馏水洗净后必须烘干才可用于溶液的配制
D. 需要称量的固体的质量为
二、实验题
16. 如图为实验室某浓盐酸试剂瓶标签上的有关数据:
试根据标签上的有关数据,回答下列问题:
取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是 ________。
A.溶液中的物质的量 溶液的浓度
C.溶液中的数目 溶液的密度
某学生欲用上述浓盐酸和蒸馏水配制物质的量浓度为的稀盐酸。
可供选用的仪器有:胶头滴管;玻璃棒;烧杯;药匙;量筒;托盘天平。
请回答下列问题:
配制稀盐酸时,还缺少的仪器有 ____________写仪器名称;该仪器上标有以下五项中的_____________;
A、温度 、浓度 、容积 、压强 、刻度线
该学生需要量取________上述浓盐酸进行配制。
在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?填“偏大”、“偏小”、“无影响”。
定容时俯视观察刻度线________。
量筒量取浓盐酸后再用蒸馏水洗涤次,并将洗液移入容量瓶中________。
17. “消毒液”能有效杀灭新型冠状病毒,某同学购买了一瓶“威露士”牌“消毒液”,该消毒液通常稀释倍体积比使用。查阅相关资料和消毒液包装说明得知其有效成分的浓度为,请回答下列问题:
某同学取该“消毒液”,按要求稀释后用于消毒,稀释后的溶液中__________。
该同学参阅该“消毒液”的配方,欲用固体配制含物质的量浓度为的消毒液已知的摩尔质量为:。请回答下列问题:
下图是该同学的部分配置过程,该同学的错误步骤有__________
下列实验过程中的说法不正确的是__________
A.用试纸检验配制好的溶液的酸碱性
B.将称量好的固体在烧杯中溶解后应立即转入容量瓶
C.容量瓶在使用前必须检查其是否漏水
D.需要称量固体的质量为
一瓶规格为上述“威露士”牌“消毒液”能吸收空气中__________的标准状况而变质。已知:
“消毒液”与稀硫酸混合使用可增强消毒能力,某消毒人员用的浓硫酸配制 的稀硫酸用于增强“消毒液”的消毒能力,请写出该原理的离子方程式___________________。
在配制过程中,下列操作中能使所配溶液的浓度偏高的有__________填代号。
用量筒量取的硫酸时俯视
洗涤量取浓硫酸的量筒,并将洗涤液转移到容量瓶中
未等稀释后的溶液冷却至室温就转移到容量瓶中
转移前,容量瓶中含有少量蒸馏水
定容时,加蒸馏水超过标线,又用胶头滴管吸出
定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
定容时,仰视刻度线
三、简答题
18. 鲜花是美丽的,但是美丽的鲜花的保鲜期却很短,在花瓶中加入“鲜花保鲜剂”却可以延长鲜花的寿命。
下表是“鲜花保鲜剂”的成分其中阿司匹林不含,其存在也不会干扰成分中其他离子的检验,回答下列问题:
成分 蔗糖 硫酸钾 阿司匹林 高锰酸钾
质量
摩尔质量
“鲜花保鲜剂”中物质的量浓度最大的成分是____________填写名称。
“鲜花保鲜剂”中的物质的量浓度为____________只要求写表达式,不用化简,不需计算。
如图所示的仪器中,在配制一定物质的量浓度的“鲜花保鲜剂”溶液时肯定不需要的是____________
填字母,还缺少的玻璃仪器有___________________填仪器名称。
市面上,有一种营养液可用于无土栽培,该营养液中有和,其中的浓度为,的浓度为,则该营养液中_____。
19. 根据要求,回答下列问题:
Ⅰ如图为实验室某浓盐酸试剂瓶标签上的有关数据。
盐酸分子式: 相对分子质量: 密度: 的质量分数:
该浓盐酸中,的物质的量浓度为______。
取用任意体积的该浓盐酸时,下列物理量中不随所取体积的多少而变化的是______填标号。
A.溶液的密度 溶质的物质的量
C.溶质的物质的量浓度 溶液中的物质的量
用该浓盐酸和蒸馏水配制物质的量浓度为的稀盐酸。
需量取______该浓盐酸进行配制保留位小数。
在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?填“偏高”、“偏低”或“无影响”
用量筒量取浓盐酸时俯视观察凹液面:______。定容后经振荡、摇匀、静置,发现液面略有下降,再加适量的蒸馏水到容量瓶颈部的刻度线:______。
Ⅱ将一定量的镁铝合金投入一定浓度的盐酸中,充分反应,合金全部溶解。向合金溶解后所得溶液中滴加溶液,生成沉淀的质量与加入的溶液的体积关系如图所示已知:不溶于溶液;能溶于溶液,反应的化学方程式为。
原合金中,镁的质量为______,铝的质量为______。
盐酸溶液中溶质的物质的量浓度为______。
答案和解析
1.【答案】
【解析】
【分析】
本题考查物质的量的计算、溶液配制,题目难度不大,明确溶液配制方法为解答关键,注意掌握物质的量与其它物理量之间的关系,试题侧重考查学生的分析能力及化学实验、化学计算能力。
【解答】
A.浓硫酸的密度大于水的密度,加水后浓硫酸质量分数为:,故A正确;
B.用浓硫酸配制一定物质的量浓度的稀硫酸时,量取浓硫酸时仰视量筒,量取的浓硫酸体积偏大,导致所配溶液浓度偏大,故B错误;
C.实验室没有的容量瓶,应用的容量瓶进行配制,故C正确;
D.同温同压下,气体的体积比等于气体分子的物质的量比,则和的物质的量之比为::,含有的原子数之比为::,故D正确。
2.【答案】
【解析】
【分析】本题主要考查了物质的量浓度的相关知识,同时考查了质量分数的知识,解答本题的关键是掌握物质的量浓度的计算方法,一定物质的量浓度溶液的配制方法。
【解答】配制的溶液需要氯化钠的质量为,配制的溶液需要氯化钠的质量为,两同学所需氯化钠的质量不相等,A错误;
B.氯化钠溶液的密度大于,氯化钠溶液的质量大于,B错误;
C.配制一定质量分数的氯化钠溶液,需要用天平称量氯化钠的质量,用药匙取药品,用量筒量取水的体积,在烧杯内溶解,并用玻璃棒搅拌,所需仪器有托盘天平、量筒、烧杯、玻璃棒、药匙等;配制一定体积、一定物质的量浓度的氯化钠溶液,需要用天平称量氯化钠的质量,用药匙取药品,在烧杯内溶解,用玻璃棒搅拌,洗涤后移入容量瓶,加水定容,液面距离刻度线时改用胶头滴管滴加,所需仪器有托盘天平、烧杯、玻璃棒、药匙、容量瓶、胶头滴管等,两同学需要的仪器不完全相同,C错误;
D.配制的溶液,其密度大于,所以溶液的体积小于,的溶液中氯化钠的物质的量为,其浓度大于,D正确。
3.【答案】
【解析】
【分析】
本题考查物质的量浓度、质量分数、溶解度之间的换算关系,解答这类问题应熟练掌握各物理量之间的转化关系,试题难度一般。
【解答】
A.根据物质的量浓度的定义可知,故A正确;
B.根据物质的量浓度与质量分数的换算关系可知氯离子的物质的量浓度为,故B错误;
C.根据物质的量浓度与质量分数的换算关系可知,故C正确;
D.根据题目信息结合溶解度的知识可得,解得 ,故D正确。
故选B。
4.【答案】
【解析】
【分析】
本题旨在考查学生对化学计量的综合计算的应用,整体难度较大,掌握溶液稀释前后溶质质量、物质的量均不变是解答本题的关键。
【解答】
A. 稀释前后溶质的质量不变,则,若,则稀释后溶液的质量为,所以稀释时加入水的质量为,水的密度为,所以水的体积,,,稀释后溶液密度变小,故,故A错误;
B. 由中分析可知,水的体积,,故B错误;
,则,若,,溶液稀释后密度减小,则,则稀释后溶液的质量小于,所以水的体积,故C正确;
B. 由中分析可知,水的体积,,故D错误.
故选C。
5.【答案】
【解析】
【分析】
本题考查化学的综合计算,注意饱和溶液、质量分数、溶解度、物质的量浓度的概念理解和相关公式的应用,难度一般。
【解答】
A.该溶液的溶质质量分数 ,故A正确;
B.该溶液的物质的量浓度,故B正确;
C.根据硫酸铜溶液在的饱和溶液的溶质质量分数为可知, ,解得溶解度,故C正确;
D.中含有结晶水,溶于水使得溶剂的质量大于,溶质为,溶质的质量小于,因此不能得到饱和溶液,故D错误。
故选D。
6.【答案】
【解析】
【分析】本题主要考查的是化学计量之间的转化关系,要求学生具有利用字母进行计算的能力,掌握物质的量浓度、溶液质量分数、溶液密度、溶解度之间的关系式是解题的关键。
【解答】,则该物质的浓度,根据可知,,,故A、C错误;
根据溶解度的定义,有,可知,故B错误,D正确。
故选D。
7.【答案】
【解析】
【分析】
本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,难度不大。
【解答】
A、由图可知,所配溶液的体积为,碳酸钠的物质的量为,所配碳酸钠溶液的浓度为,故A正确;
B、溶解并放置至室温后再移液,故操作是移液,故B正确;
C、操作是定容,定容时仰视导致溶液体积偏高,会使配得溶液的浓度偏低,故C正确;
D、定容摇匀后发现液面低于刻度线是正常现象,再加水至液面与刻度线平齐,导致所配溶液的体积偏大,所配溶液的浓度偏小,故D错误。
故选:。
8.【答案】
【解析】设实际过程中反应的铁为,消耗的的物质的量为。
铁片增重
,解得:,说明铁片有剩余,已经全部反应,故需以的量进行计算,,解得:,故C溶液的物质的量浓度,故选C。
9.【答案】
【解析】
【分析】
本题考查了一定物质的量浓度溶液的配制,明确配制原理及操作步骤是解题关键,注意容量瓶规格选择依据。
【解答】
A.配制的溶液,实验室没有容量瓶,应选择容量瓶,故A错误;
B.配制的溶液,实验室没有容量瓶,应选择容量瓶,需要氢氧化钠质量为:,故B错误;
C.定容时俯视刻度线,导致溶液体积偏小,依据可知,溶液浓度偏大,故C正确;
D.定容摇匀静置后,液面低于刻度线,再加蒸馏水至刻度线,导致溶液体积偏大,溶液浓度偏低,故D错误。
故选C。
10.【答案】
【解析】
【分析】
本题主要考查的是化学计量的综合计算,涉及质量分数计算、物质的量浓度计算、溶液稀释的计算、水的电离等知识,意在考查学生的分析能力和知识应用能力。
【解答】
A.溶质的质量分数为,故A错误;
B.溶质的物质的量浓度,故B正确;
C.根据电荷守恒可知,溶液中,故C错误;
D.氨水的密度比水小,则上述溶液中再加入水后,溶液质量大于原来溶液质量的倍,故所得溶液的质量分数小于,故D错误。
故选B。
11.【答案】
【解析】
【分析】
本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,难度不大。
【解答】
A. 由图可知,所配溶液的体积为,碳酸钠的物质的量为,所配碳酸钠溶液的浓度为,故A正确;
B. 溶解并放置至室温后再移液,故操作是移液,故B正确;
C. 操作是定容,如果仰视,导致所配溶液的体积偏大,所配得溶液浓度偏小,故C正确;
D. 定容摇匀后发现液面低于刻度线,少量溶液残留在瓶塞与瓶口之间,再加水至液面与刻度线平齐,导致所配溶液的体积偏大,所配溶液的浓度偏小,故D错误。
故选:。
12.【答案】
【解析】
【分析】
本题考查了一定物质的量浓度溶液的配制,明确配制原理和过程是解题关键,注意误差分析的方法,题目难度不大。
【解答】
A.质量分数:,密度:的浓硫酸,物质的量浓度为,物质的量浓度的单位是,故A错误;
B.配制的稀硫酸,应选择容量瓶,设需要浓硫酸体积为,则依据溶液稀释过程中溶质物质的量不变得:,解得,故B错误;
C.容量瓶为精密仪器,不能用于稀释浓溶液,应在烧杯中稀释然后转移到容量瓶,故C错误;
D.该同学实际配制得到的浓度为,可能的原因是量筒量取浓硫酸时仰视刻度线,导致量取浓硫酸体积偏大,溶质物质的量偏大,依据可知,溶液浓度偏大,故D正确。
13.【答案】
【解析】
【分析】
本题考查物质的量浓度的计算,题目难度中等,注意掌握物质的量浓度与溶质质量分数的关系,注意硫酸的密度比水大,且浓度越大密度越大。
【解答】
A. 该硫酸的物质的量浓度为,A正确;
B. 该硫酸与等体积的水混合所得溶液的质量分数为,B正确;
C. 该硫酸与等体积的水设各为混合,所得溶液的体积小于,所得溶液的浓度大于,C正确;
D. 实验需要的稀硫酸,配制时应选择的容量瓶,需量取该浓硫酸的体积为,D错误。
14.【答案】
【解析】
【分析】
本题考查了物质的量浓度、溶质质量分数、相对分子量、溶液密度的计算,题目难度中等,注意掌握物质的量浓度与溶质的质量分数的概念及计算方法,试题培养了学生灵活应用所学知识的能力。
【解答】
A.设溶液的体积为,则溶液中溶质的质量为:,该溶液的质量为:,溶液的密度为:,故A错误;
B.溶液体积为:,溶质的物质的量为:,该溶液的浓度为:,故B错误;
C.溶液中溶质的质量为:,溶液质量为:,则溶质的质量分数为:,故C错误;
D.溶质质量分数为,则水的质量分数为:,水的质量为,则溶液的质量为:,溶质的质量为:,溶质的物质的量为:,则该化合物的摩尔质量为:,则该化合物的相对分子量为:,故D正确。
故选D。
15.【答案】
【解析】
【分析】
本题主要考查溶液配制的步骤、仪器以及误差分析等,难度不是很大,注意计算溶质的质量时,溶液的体积按计算。即如果配制的溶液体积和实验室中容量瓶的规格不符时,容量瓶应该选取比要配制的体积大且最接近的规格的容量瓶。
【解答】
A. 配制过程需要托盘天平、烧杯、玻璃棒、容量瓶和胶头滴管五种仪器即可完成,故A错误;
B. 由于易吸收空气中的、而变质,所以消毒液变质导致减少,配制的溶液中溶质的物质的量减小,则溶液的物质的量浓度偏小,故B正确;
C. 容量瓶中有水,对溶液的体积无影响,所以经洗涤干净的容量瓶不必烘干后再使用,故C错误;
D. 应选取的容量瓶进行配制,然后取出即可,所以需要的质量:,故D错误。
故选B。
16.【答案】
容量瓶;
;
偏大;偏大
【解析】
【分析】
本题主要考查物质的量浓度的定义和一定物质的量浓度溶液的配制实验操作及误差分析,难度不大。
【解答】
溶液中的物质的量大小取决于溶液体积的大小与溶液浓度,故A错误;
溶液具有均一性,溶液的浓度是与体积无关的,故B正确;
溶液中的数目与溶液浓度、溶液体积大小及溶质的化学式组成有关,故C错误;
溶液具有均一性,溶液的密度是与体积无关的,故D正确;
所以此题选BD。
配制物质的量浓度为的稀盐酸的步骤有:计算、量取、稀释、冷却、转移、洗涤、定容、摇匀等,则使用的仪器有:量筒、烧杯、玻璃棒、容量瓶、胶头滴管等,还缺少的仪器有:容量瓶;
容量瓶标有:温度、容积、刻度线;
故此题的答案是:容量瓶; ;
浓盐酸中的物质的量浓度为,
配制物质的量浓度为的稀盐酸,设需要浓盐酸的体积为,根据溶液稀释过程中溶液的物质的量不变得:
,计算得出:;
故本题正确答案为;
定容时俯视容量瓶刻度线,导致溶液体积偏小,溶液浓度偏大;
洗涤量筒,溶质的物质的量偏大,溶液浓度偏大,
故答案为:偏大;偏大。
17.【答案】
【解析】
【分析】
本题考查物质的量浓度的计算、溶液的配制,题目难度中等,注意掌握物质的量浓度的计算方法及表达式、配制一定物质的量浓度溶液的方法是解题的关键,试题培养了学生的分析能力及化学计算能力。
【解答】
稀释倍后;
中物品和砝码的位置放反了,故错误;
溶解步骤,正确;
转移时要用玻璃棒进行引流,故错误;
定容时胶头滴管不能伸入容量瓶内,故错误。
故答案为:;
溶液具有强氧化性,可将试纸漂白,不能用试纸测其,故错误;
B.溶解后应静置至室温后转入容量瓶,故错误;
C.容量瓶在使用前必须检查其是否漏水,故正确;
D.实验室无容量瓶,所以选择容量瓶,用托盘天平称量时,应记录至小数点后一位,则需要称量固体的质量为,故正确。
故答案为:;
一瓶规格为上述“威露士”牌“消毒液”中,则由方程式可知也为,标准状况下体积为;
“消毒液”与稀硫酸混合使用可增强消毒能力,是因为生成,离子方程式为;
用量筒量取的硫酸时俯视,则所取的的硫酸体积偏小,硫酸的物质的量偏小,所配浓度偏低,故不选;
洗涤量取浓硫酸的量筒,并将洗涤液转移到容量瓶中,导致硫酸的物质的量偏大,溶液浓度偏高,故选;
未等稀释后的 溶液冷却至室温就转移到容量瓶中,冷却后溶液体积偏小,溶液浓度偏高,故选;
转移前,容量瓶中含有少量蒸馏水,对溶质物质的量和溶液体积都不产生影响,溶液浓度无影响,故不选;
定容时,加蒸馏水超过标线,又用胶头滴管吸出,导致溶质物质的量偏小,溶液浓度偏低,故不选;
定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线,导致溶液体积偏大,溶液浓度偏低,故不选;
定容时,仰视刻度线,导致溶液体积偏大,溶液浓度偏低,故不选;
故选。
18.【答案】蔗糖 ;玻璃棒、烧杯
【解析】蔗糖,硫酸钾,阿司匹林
,高锰酸钾,所以“鲜花保鲜剂”中物质的量浓度最大的成分是蔗糖。
硫酸钾高锰酸钾。
配制一定物质的量浓度的溶液所需要的仪器包括托盘天平、量筒、烧杯、玻璃棒、容量瓶、胶头滴管,不需要使用烧瓶和分液漏斗。
根据电荷守恒,,。
19.【答案】Ⅰ
;偏低;偏低
Ⅱ;
【解析】
【分析】
Ⅰ本题考查一定物质的量浓度盐酸溶液的配制、计算和误差分析,难度一般,属于基础内容,细心即可。
Ⅱ本题考查镁铝合金与酸碱反应的计算,对于图像的数据分析尤为重要,属于常考题型,难度一般。
【解答】
Ⅰ该浓盐酸中,的物质的量浓度,故答案为:;
溶液是均匀的,溶液的密度、浓度不随体积变化,而的物质的量和的物质的量均与溶液体积有关。
故选AC。
设需要浓盐酸的体积为,根据稀释定律,稀释前后的物质的量不变,则,解得,故答案为:;
用量筒量取浓盐酸时俯视观察凹液面,使量取的浓盐酸体积偏小,所配制的稀盐酸的物质的量浓度偏低;定容后经振荡、摇匀、静置,发现液面略有下降,再加适量的蒸馏水到容量瓶颈部的刻度线,最终加入蒸馏水的体积偏大,所配制的稀盐酸的物质的量浓度偏低;故答案为:偏低;偏低;
Ⅱ由图可知,加入溶液阶段没有沉淀生成,是因为溶液与剩余的盐酸反应,反应的化学方程式为: ;过程中是沉淀的溶解过程,能溶解于溶液的沉淀是,反应方程式为:,该阶段消耗的的物质的量为:,则的物质的量为,故,;根据 ,可知过程中生成的消耗的物质的量为,则与反应的物质的量为:,得出的物质的量为,合金中的质量为;故答案为:;;
在沉淀达到最大的时候,溶液中的溶质为,,的物质的量浓度为:。故答案为:。
第1页,共1页
