原子的结构(第一课时)(31张ppt)
文档属性
| 名称 | 原子的结构(第一课时)(31张ppt) |
|
|
| 格式 | zip | ||
| 文件大小 | 4.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2014-10-10 00:00:00 | ||
图片预览







文档简介
课件31张PPT。
第三单元 物质构成的奥秘
课题2 原子的结构(第一课时)
这些物质你熟悉吗?它们是由什么粒子构成的呢?铁是由铁原子构成的,
水是由水分子构成的,
食盐是由离子构成的。复习 1、什么是原子?原子是化学变化中的最小粒子。 2、提问:原子虽然很小,它真是最小的粒子且永远不能再分割了吗?你想象中的原子是什么样的? 原子与乒乓球体积比相当于乒乓球与地球的体积之比。 原子结构发现史1804年道尔顿
实心球模型1897年汤姆生
西瓜模型1912年卢瑟福
行星模型公元前460年--公元前370年
德谟克利特率先提出 原子论 ——万物由原子构成 人类历经约二千多年的漫长探索、发展,才有了今
天的成就。人们并未就此停步,还在继续向前迈进!卢瑟福 实验: 1912年,英国核物理学之父卢瑟福,根据α粒子散射实验现象提出原子核式结构模型:
该实验证明原子不可能
是实心球体,而是球体内部
有着相对很大空间的,且球
体内有一个体积极小、质量相对较大带正电的核。1964年10月16日,我国第一颗原子弹爆炸 原子核还能再分, 实验证明 原子核是由质子和中子构成的,其分裂后会释放出巨大的能量。新课质子一、原子的构成原子原子核 中子 核外电子(+)(每个质子带1个单位正电荷)(每个电子带1个单位负电荷)(不带电)原子的构成示意图表3-1几种原子的构成 2.质子数不一定等于中子数
3.不是所有的原子核里都含有中子
4.质子数不同原子种类也不同问:原子为什么不显电性呢?
1.在原子里:核电荷数=质子数=核外电子数 1 0 16 6 68 8 811 12 1117 18 17 1. 在同一原子中,其数目不一定相同的是( )
A.核电荷数和中子数 B.核电荷数和核外电子数 C.核电荷数和质子数 D.核外电子数和质子数
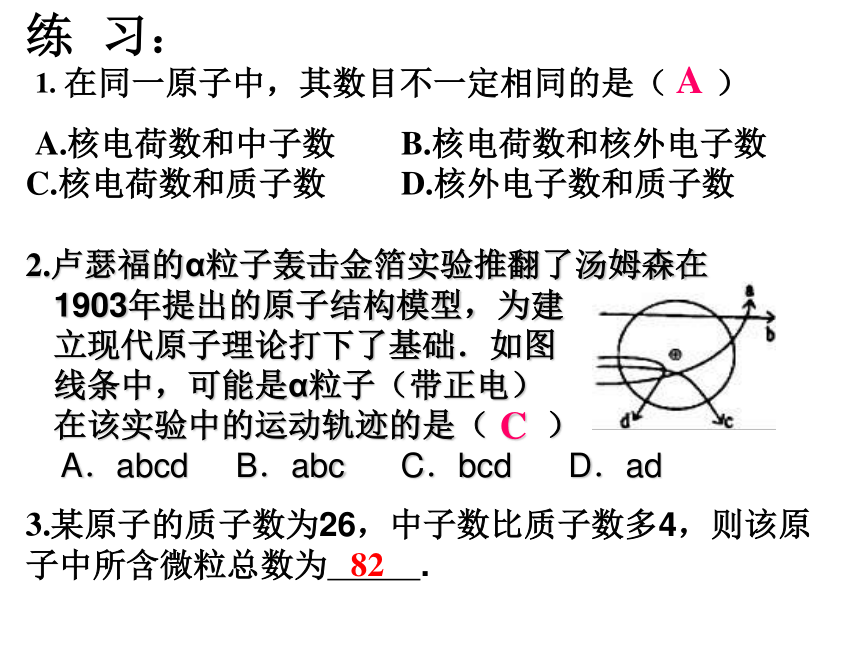
2.卢瑟福的α粒子轰击金箔实验推翻了汤姆森在
1903年提出的原子结构模型,为建
立现代原子理论打下了基础.如图
线条中,可能是α粒子(带正电)
在该实验中的运动轨迹的是( )
A.abcd B.abc? C.bcd ? D.ad
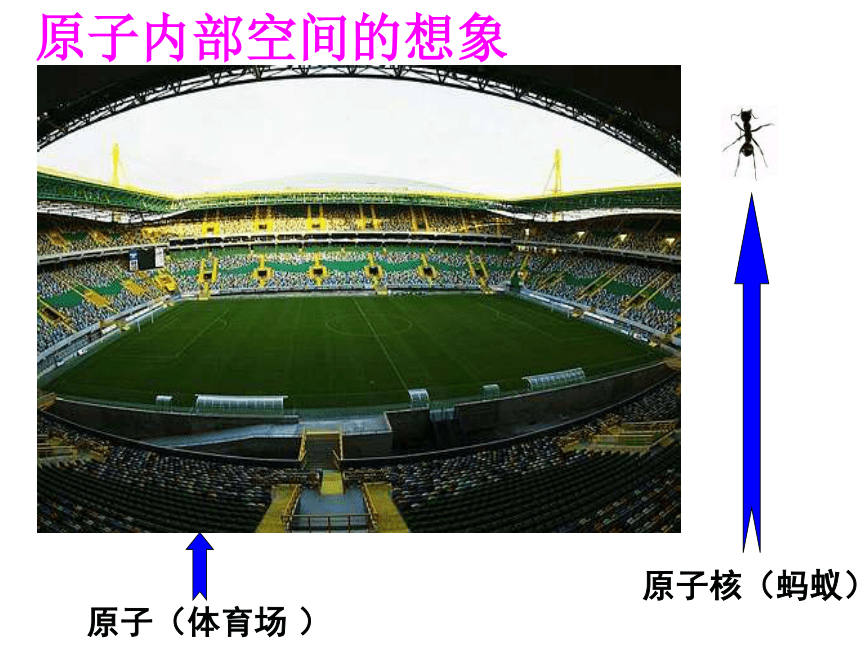
3.某原子的质子数为26,中子数比质子数多4,则该原子中所含微粒总数为 .练 习:A82C原子内部空间的想象原子(体育场 )原子核(蚂蚁)氢原子(一个电子)的核外电子运动情况 电子不像行星绕太阳旋转有固定的轨道,但有经常出现的区域,科学家把这样的区域称为电子层。多电子原子的核外电子又是怎样运动的呢?二、核外电子的排布(又叫分层运动)1、电子能量的高低与离核远、近的关系: 二 三 四 五 六 七
K L M N O P Q近 远低 高图3-10核外电子分布示意图离核远近能量高低电子层 核外电子的分层运动又称为核外电子的分层排布
核外电子的排布规律 : 原子的结构 可用原子结构示意图简明地表示。 ① 原子的第一层最多排2个电子,第二层
最多排8个电子,最外层电子数最多不超过8个
(只有1层的不超过2个)。 ② 核外电子总是先排在能量较低的电子层,
排满第一层2个电子,再排第二层,排满第二层8
个电子,再排第三层.(先排内层, 后排外层 ) ?? 三、原子结构示意图1、画 法 :画圆圈,标核电,弧 线呈扇面 ,数字一条线 。 +82 6 氧 O+11 2 8 1钠 Na2、原子结构示意图意义:Na三二一
写出下列元素的符号和原子
序数,画出其原子结构示意图。
硫 镁 铍
氯 氟 氩
练一练答案: 找一找: 根据所画出的原子结构示意图,你发现原子结构与元素的分类以及化学性质有什么样的关系?元素与最外层电子数的关系8个(He为2个)比较稳定元素与最外层电子数的关系一般少于4个易失电子元素与最外层电子数的关系一般大于或等于4个易得电子归纳 :各元素原子最外电子数目的特点
最外层电子数决定了元素的化学性质。一般大 于4个 不稳定结构 易得电子 活泼一般小于4个 不稳定结构 易失电子 活泼 8(氦为 2)个 稳定结构 稳定 稳定给你提个醒 1、原子核上的质子数决定着元素的种类。是区分不同元素的依据。 2、原子最外层上的电子数决定着元素的化学性质。
2 8 6你能做:找错误,并说出理由: 硼
Be +53 2+115 6
硅
Si+142 9 3 +18硫
S
钠
Na接着练 用原子结构示意图表示:
1、比镁原子少1个质子的原子;
2、原子核只有1个质子的原子;
3、核电荷数为18的原子;钠原子氢原子氩原子 一.质子数
二.最外层电子数
1.稀有气体原子:最外层电子数为8个(He
为2个),化学性质稳定;
2.金属原子:最外层电子数一般少于4个,
易失去电子,化学性质活泼;
3.非金属原子:最外层电于一般都多于
4个,易得到电子,化学性质活泼。
结论:结构决定性质。小结决定决定元素的种类元素的化学性质谈谈你的收获课后作业
1.P57. 1、 P58. 3
2.画出下列原子结构示意图:
氧 钠 氮 氦 ,
氯 铝 氩 硅 。
3.指出氧、钠、氮、氦、氯、铝、氩、硅等原子中哪些是金属原子、哪些是非金属原子?还有哪些是稀有气体原子?为什么? 再见一分辛劳 一分收获
有志者 事竟成
祝你取得成功!
第三单元 物质构成的奥秘
课题2 原子的结构(第一课时)
这些物质你熟悉吗?它们是由什么粒子构成的呢?铁是由铁原子构成的,
水是由水分子构成的,
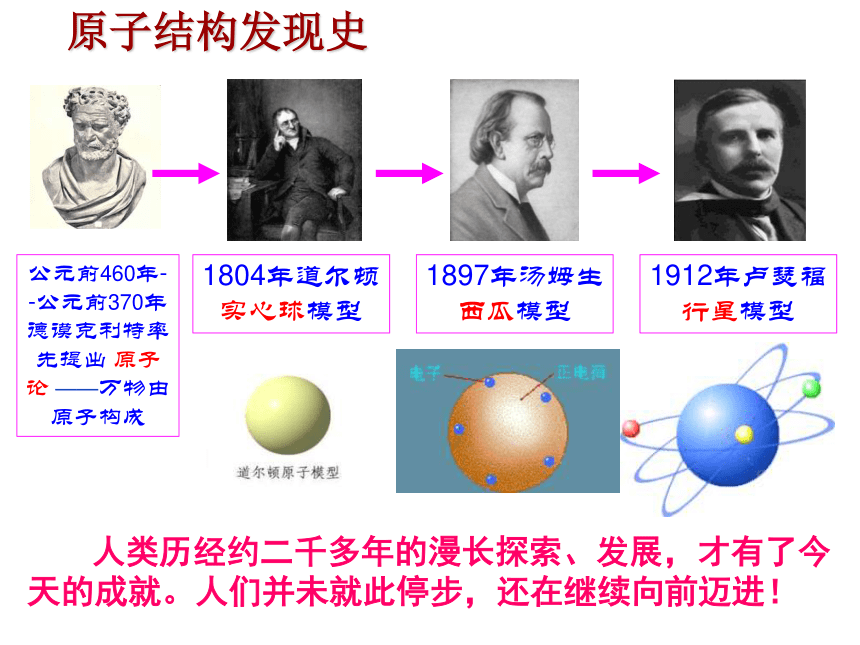
食盐是由离子构成的。复习 1、什么是原子?原子是化学变化中的最小粒子。 2、提问:原子虽然很小,它真是最小的粒子且永远不能再分割了吗?你想象中的原子是什么样的? 原子与乒乓球体积比相当于乒乓球与地球的体积之比。 原子结构发现史1804年道尔顿
实心球模型1897年汤姆生
西瓜模型1912年卢瑟福
行星模型公元前460年--公元前370年
德谟克利特率先提出 原子论 ——万物由原子构成 人类历经约二千多年的漫长探索、发展,才有了今
天的成就。人们并未就此停步,还在继续向前迈进!卢瑟福 实验: 1912年,英国核物理学之父卢瑟福,根据α粒子散射实验现象提出原子核式结构模型:
该实验证明原子不可能
是实心球体,而是球体内部
有着相对很大空间的,且球
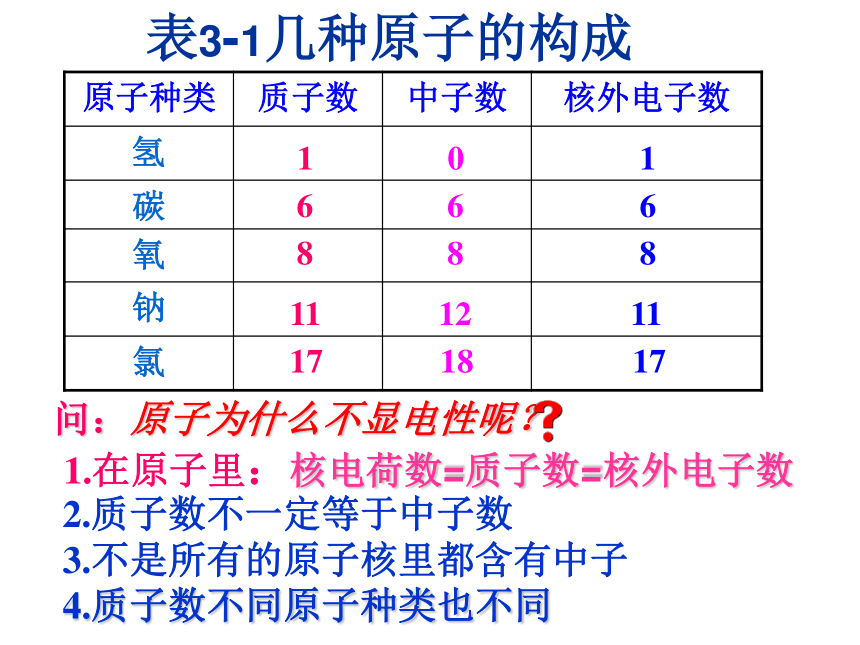
体内有一个体积极小、质量相对较大带正电的核。1964年10月16日,我国第一颗原子弹爆炸 原子核还能再分, 实验证明 原子核是由质子和中子构成的,其分裂后会释放出巨大的能量。新课质子一、原子的构成原子原子核 中子 核外电子(+)(每个质子带1个单位正电荷)(每个电子带1个单位负电荷)(不带电)原子的构成示意图表3-1几种原子的构成 2.质子数不一定等于中子数
3.不是所有的原子核里都含有中子
4.质子数不同原子种类也不同问:原子为什么不显电性呢?
1.在原子里:核电荷数=质子数=核外电子数 1 0 16 6 68 8 811 12 1117 18 17 1. 在同一原子中,其数目不一定相同的是( )
A.核电荷数和中子数 B.核电荷数和核外电子数 C.核电荷数和质子数 D.核外电子数和质子数
2.卢瑟福的α粒子轰击金箔实验推翻了汤姆森在
1903年提出的原子结构模型,为建
立现代原子理论打下了基础.如图
线条中,可能是α粒子(带正电)
在该实验中的运动轨迹的是( )
A.abcd B.abc? C.bcd ? D.ad
3.某原子的质子数为26,中子数比质子数多4,则该原子中所含微粒总数为 .练 习:A82C原子内部空间的想象原子(体育场 )原子核(蚂蚁)氢原子(一个电子)的核外电子运动情况 电子不像行星绕太阳旋转有固定的轨道,但有经常出现的区域,科学家把这样的区域称为电子层。多电子原子的核外电子又是怎样运动的呢?二、核外电子的排布(又叫分层运动)1、电子能量的高低与离核远、近的关系: 二 三 四 五 六 七
K L M N O P Q近 远低 高图3-10核外电子分布示意图离核远近能量高低电子层 核外电子的分层运动又称为核外电子的分层排布
核外电子的排布规律 : 原子的结构 可用原子结构示意图简明地表示。 ① 原子的第一层最多排2个电子,第二层
最多排8个电子,最外层电子数最多不超过8个
(只有1层的不超过2个)。 ② 核外电子总是先排在能量较低的电子层,
排满第一层2个电子,再排第二层,排满第二层8
个电子,再排第三层.(先排内层, 后排外层 ) ?? 三、原子结构示意图1、画 法 :画圆圈,标核电,弧 线呈扇面 ,数字一条线 。 +82 6 氧 O+11 2 8 1钠 Na2、原子结构示意图意义:Na三二一
写出下列元素的符号和原子
序数,画出其原子结构示意图。
硫 镁 铍
氯 氟 氩
练一练答案: 找一找: 根据所画出的原子结构示意图,你发现原子结构与元素的分类以及化学性质有什么样的关系?元素与最外层电子数的关系8个(He为2个)比较稳定元素与最外层电子数的关系一般少于4个易失电子元素与最外层电子数的关系一般大于或等于4个易得电子归纳 :各元素原子最外电子数目的特点
最外层电子数决定了元素的化学性质。一般大 于4个 不稳定结构 易得电子 活泼一般小于4个 不稳定结构 易失电子 活泼 8(氦为 2)个 稳定结构 稳定 稳定给你提个醒 1、原子核上的质子数决定着元素的种类。是区分不同元素的依据。 2、原子最外层上的电子数决定着元素的化学性质。
2 8 6你能做:找错误,并说出理由: 硼
Be +53 2+115 6
硅
Si+142 9 3 +18硫
S
钠
Na接着练 用原子结构示意图表示:
1、比镁原子少1个质子的原子;
2、原子核只有1个质子的原子;
3、核电荷数为18的原子;钠原子氢原子氩原子 一.质子数
二.最外层电子数
1.稀有气体原子:最外层电子数为8个(He
为2个),化学性质稳定;
2.金属原子:最外层电子数一般少于4个,
易失去电子,化学性质活泼;
3.非金属原子:最外层电于一般都多于
4个,易得到电子,化学性质活泼。
结论:结构决定性质。小结决定决定元素的种类元素的化学性质谈谈你的收获课后作业
1.P57. 1、 P58. 3
2.画出下列原子结构示意图:
氧 钠 氮 氦 ,
氯 铝 氩 硅 。
3.指出氧、钠、氮、氦、氯、铝、氩、硅等原子中哪些是金属原子、哪些是非金属原子?还有哪些是稀有气体原子?为什么? 再见一分辛劳 一分收获
有志者 事竟成
祝你取得成功!
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
