专题4第一单元含硫化合物的性质同步练习 (含解析)2022-2023学年上学期高一化学苏教版(2019)必修第一册
文档属性
| 名称 | 专题4第一单元含硫化合物的性质同步练习 (含解析)2022-2023学年上学期高一化学苏教版(2019)必修第一册 |
|
|
| 格式 | docx | ||
| 文件大小 | 470.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-27 00:00:00 | ||
图片预览


文档简介
专题4第一单元含硫化合物的性质同步练习
一、单选题
1. 下列有关浓硫酸的说法正确的是( )
A. 浓硫酸具有吸水性,因此可用作干燥剂,能干燥氢气、硫化氢、氨气等气体
B. 浓硫酸具有脱水性,因而能使蔗糖炭化
C. 浓硫酸在加热条件下能与单质碳反应,体现了浓硫酸的酸性和强氧化性
D. 因为浓硫酸在常温下不与铁或铝反应,因此常温下可用铁制或铝制容器储存浓硫酸
2. 下列变化的实质相似的是( )
A. 浓 和浓硝酸在空气中敞口放置时浓度均减小
B. 和 均能使品红溶液褪色
C. 浓 与稀 与金属反应时均有气体产生
D. 和 气体均不能用浓 干燥
3. 利用如图所示装置进行下列实验,能得出相应实验结论的是( )
选项 实验结论
浓硫酸 溶液褪色 有漂白性
浓盐酸 溶液变为黄色 氧化性:
稀硫酸 溶液无明显变化 不与反应
浓硫酸 蔗糖 溴水褪色 浓硫酸具有脱水性、吸水性
A. B. C. D.
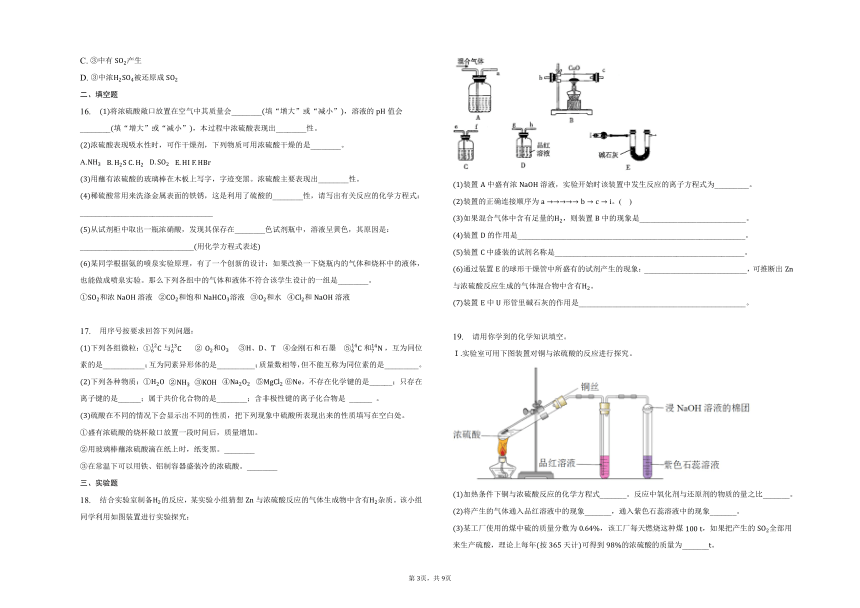
4. 叠氮酸钠是重要的化工原料。以甲醇、亚硝酸钠等为原料制备的流程如下:
已知:水合肼不稳定,具有强还原性。下列描述错误的是 ( )
A. 反应和反应中浓硫酸作用不同
B. 反应的化学方程式:
C. 步骤分离出的可导入中循环利用
D. 反应制备水合肼时应将氨水逐滴滴入溶液中
5. 某同学通过系列实验探究硫及其化合物的性质,实验现象正确且能达到目的的是( )
A. 点燃硫磺产生刺激性气味气体,该气体可以漂白纸浆
B. 向蔗糖中加入浓硫酸,蔗糖变黑色,说明浓硫酸具有强的吸水性
C. 将气体通入溶液生成沉淀
D. 将片加入浓硫酸中,反应剧烈,说明浓硫酸具有强的氧化性
6. 如图所示,将浓硫酸滴至下列物质上,无明显现象的是( )
A. 蔗糖 B. 铝片 C. 胆矾 D. 纯碱
7. 下列关于硫及其化合物的叙述中正确的是( )
A. 因具有漂白性,所以能使品红溶液、溴水、酸性溶液、石蕊试液褪色
B. 硫在自然界中只能以硫化物和硫酸盐的形态存在
C. 硫黄和黄铁矿可以作为制备硫酸的原料
D. 浓硫酸与单质碳的反应中,浓硫酸既表现了强氧化性又表现了酸性
8. 下列有关硫及其化合物的说法中正确的是( )
A. 浓硫酸具有吸水性,可作干燥剂,不能干燥,也不能干燥等还原性气体
B. 浓硫酸与灼热的炭反应,体现了浓硫酸的强氧化性和酸性
C. 和均可使品红溶液褪色,但将溶有的品红溶液加热后又恢复红色,说明的氧化性没有强
D. 以为原料生产硫酸的过程中,要用到沸腾炉、接触室、吸收塔等设备,所涉及的反应均为氧化还原反应
9. 下列有关浓硫酸性质的叙述错误的是( )
A. 在反应:浓中,浓硫酸表现酸性
B. 在反应:中,浓硫酸只表现脱水性
C. 在反应:浓中,浓硫酸只表现氧化性
D. 浓硫酸具有吸水性,因而能使转化为
10. 下列关于硫及其化合物的说法中正确的是( )
A. 自然界中不存在游离态的硫
B. 二氧化硫的排放会导致光化学烟雾的产生
C. 二氧化硫能使滴有酚酞的氢氧化钠溶液褪色,体现了其漂白性
D. 浓硫酸可用来干燥、、等气体
11. 生产硫酸最古老的方法是以绿矾为原料,在蒸镏釜中煅烧。反应的化学方程式为已知二氧化硫的沸点为,三氧化硫的沸点为。用如图所示的装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫,为干燥的试管,加热装置已略去。下列有关说法正确的是( )
A. 若将反应后的三种气体通入溶液中,产生的沉淀为、
B. 中产物用紫色石蕊试液即可检验出其中和
C. 为检验反应的另一种生成物,试管中应加入的试剂为溶液
D. 中所得到的硫酸的质量分数为
12. 下列措施或叙述不合理的是
A. 用漂白纸浆和草帽辫
B. 具有强还原性,浓硫酸具有强氧化性,故浓硫酸不能用于干燥气体
C. 将浓硫酸滴到蔗糖表面,固体变黑膨胀,说明浓硫酸有脱水性和强氧化性
D. 与的反应为氧化还原反应
13. 下列有关物质的性质与用途具有对应关系的是( )
A. 具有氧化性,可用于漂白纸浆 B. 明矾易溶于水,可用作净水剂
C. 浓硫酸具有脱水性,可用于干燥氢气 D. 、熔点高,可用于制作耐火材料
14. 下列有关浓硫酸的叙述中正确的是 ( )
浓硫酸在常温下能够使铁、铝等金属钝化
浓硫酸与铜加热反应后,铜片有剩余,硫酸完全反应
浓硫酸具有吸水性,因而能使蔗糖碳化
浓硫酸与铜加热反应后,铜片有剩余,向反应后的溶液中再加入铁片,会有氢气生成
浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
浓硫酸与铁加热反应后,铁片有剩余,生成的气体除水蒸气外还有。
浓硫酸具有强氧化性,常温下能与发生剧烈反应
浓硫酸具有强氧化性,具有还原性,所以浓硫酸不能干燥
A. B. C. D.
15. 浓硫酸分别与三种钠盐反应,现象如图。下列分析不正确的是( )
A. 中试管口白雾是遇水蒸气所致,利用硫酸的难挥发性
B. 体现了浓硫酸的强氧化性
C. 中有产生
D. 中浓被还原成
二、填空题
16. 将浓硫酸敞口放置在空气中其质量会________填“增大”或“减小”,溶液的值会________填“增大”或“减小”,本过程中浓硫酸表现出________性。
浓硫酸表现吸水性时,可作干燥剂,下列物质可用浓硫酸干燥的是________。
A.
用蘸有浓硫酸的玻璃棒在木板上写字,字迹变黑。浓硫酸主要表现出________性。
稀硫酸常用来洗涤金属表面的铁锈,这是利用了硫酸的________性,请写出有关反应的化学方程式:___________________________________
从试剂柜中取出一瓶浓硝酸,发现其保存在________色试剂瓶中,溶液呈黄色,其原因是:______________________________用化学方程式表述
某同学根据氨的喷泉实验原理,有了一个创新的设计:如果改换一下烧瓶内的气体和烧杯中的液体,也能做成喷泉实验。那么下列各组中的气体和液体不符合该学生设计的一组是________。
和浓溶液 和饱和溶液 和水 和溶液
17. 用序号按要求回答下列问题:
下列各组微粒:与 和 、、 金刚石和石墨 和 ,互为同位素的是___________;互为同素异形体的是__________;质量数相等,但不能互称为同位素的是_________。
下列各种物质: ,不存在化学键的是______;只存在离子键的是______;属于共价化合物的是________;含非极性键的离子化合物是 ______ 。
硫酸在不同的情况下会显示出不同的性质,把下列现象中硫酸所表现出来的性质填写在空白处。
盛有浓硫酸的烧杯敞口放置一段时间后,质量增加。
用玻璃棒蘸浓硫酸滴在纸上时,纸变黑。________
在常温下可以用铁、铝制容器盛装冷的浓硫酸。________
三、实验题
18. 结合实验室制备的反应,某实验小组猜想与浓硫酸反应的气体生成物中含有杂质。该小组同学利用如图装置进行实验探究:
装置中盛有浓溶液,实验开始时该装置中发生反应的离子方程式为_________。
装置的正确连接顺序为。( )
如果混合气体中含有足量的,则装置中的现象是____________________________。
装置的作用是____________________________________________________________。
装置中盛装的试剂名称是__________________________________________________。
通过装置的球形干燥管中所盛有的试剂产生的现象:___________________________,可推断出与浓硫酸反应生成的气体混合物中含有。
装置中形管里碱石灰的作用是____________________________________________。
19. 请用你学到的化学知识填空。
Ⅰ实验室可用下图装置对铜与浓硫酸的反应进行探究。
加热条件下铜与浓硫酸反应的化学方程式_______。反应中氧化剂与还原剂的物质的量之比_______。
将产生的气体通入品红溶液中的现象_______,通入紫色石蕊溶液中的现象_______。
某工厂使用的煤中硫的质量分数为,该工厂每天燃烧这种煤,如果把产生的全部用来生产硫酸,理论上每年按天计可得到的浓硫酸的质量为_______。
Ⅱ实验室制氯气可用下图装置,并进行氯气性质实验。
写出实验室制备氯气的化学方程式:_______。
将氯气通入冷的石灰乳中可制备用于环境消毒的漂白粉,写出此反应的化学方程式_______。
将氯气通入溶液中可发生置换反应,写出反应的离子方程式_______;通过单质之间的置换证明氧化性_______填“”,“”或“”。
答案和解析
1.【答案】
【解析】
【分析】
本题考查了浓硫酸的性质,难度较小,掌握浓硫酸的特性:吸水性、脱水性、强氧化性,以及能够发生的反应是关键,侧重考查基础知识的掌握和应用。
【解答】
A.浓硫酸具有吸水性,因此可用作干燥剂,但不能干燥还原性气体如:硫化氢,碱性气体如:氨气等气体,故A错误;
B.浓硫酸具有脱水性,因而能使蔗糖脱水炭化,故B正确;
C.浓硫酸在加热条件下能与单质碳反应,体现了浓硫酸的强氧化性,故C错误;
D.因为浓硫酸在常温下可使铁或铝钝化,因此常温下可用铁制或铝制容器储存浓硫酸,故D错误。
故选B。
2.【答案】
【解析】
【分析】
本题综合考查元素化合物知识,侧重于基础知识的考查,意在考查学生的识记能力,注意相关基础知识的积累,把握相关物质的性质。
【解答】
A.浓硫酸具有吸水性,硝酸易挥发,二者放置在空气中浓度都变小,但变化的实质不同,故A错误;
B.二氧化硫与有色物质发生化合反应而使有色物质漂白,氯水中的次氯酸具有强氧化性而使有色物质漂白,二者漂白原理不同,二氧化硫的漂白不稳定,加热可恢复到原来的颜色,故B错误;
C.浓硫酸与锌反应生成二氧化硫,是浓硫酸中元素化合价降低;稀硫酸与锌反应生成氢气,是稀硫酸中元素化合价降低,二者产生气体的实质不同,故C错误;
D.、都具有还原性,都可与浓硫酸发生氧化还原反应而不能用浓硫酸干燥,故D正确。
故选D。
3.【答案】
【解析】
【分析】
本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、物质的性质、反应与现象、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大。
【解答】
A.二氧化硫与高锰酸钾发生氧化还原反应,与二氧化硫的还原性有关,与漂白性无关,故A错误;
B.氯气与溶液发生氧化还原反应,亚铁离子、溴离子均被氧化,则不能说明氧化性:,故B错误;
C.稀硫酸与碳酸钠反应生成二氧化碳,盐酸的酸性大于碳酸的酸性,则不与反应,故C正确;
D.浓硫酸使蔗糖脱水后,与浓硫酸发生氧化还原反应生成二氧化硫,二氧化硫使溴水褪色,则说明浓硫酸具有脱水性、强氧化性,故D错误;
故选:。
4.【答案】
【解析】 由题给流程可知,向甲醇、亚硝酸钠的混合物中加入浓硫酸,浓硫酸先与亚硝酸钠反应生成亚硝酸,在浓硫酸作用下,甲醇与亚硝酸发生酯化反应生成亚硝酸甲酯;氨水和次氯酸钠溶液混合发生氧化还原反应得到水合肼,在氢氧化钠溶液中,亚硝酸甲酯与水合肼发生氧化还原反应生成叠氮酸钠、甲醇和水,在蒸汽加热的条件下,向反应后的溶液中加入浓硫酸,浓硫酸与叠氮酸钠反应制得叠氮酸,叠氮酸与氢氧化钠溶液反应制得产品叠氮酸钠。
由分析可知,反应中浓硫酸起酸、催化剂的作用,反应中浓硫酸只起酸的作用,作用不同,A正确;
由分析可知,反应为在氢氧化钠溶液中,亚硝酸甲酯与水合肼发生氧化还原反应生成叠氮酸钠、甲醇和水,反应的化学方程式为,B正确;
由分析可知,反应中甲醇为反应物,则步骤分离出的甲醇可导入中循环利用,C正确;
水合肼具有强还原性,若反应制备水合肼时将氨水逐滴滴入具有强氧化性的次氯酸钠溶液中,水合肼会与次氯酸钠发生氧化还原反应,而无法制得水合肼,D错误。
5.【答案】
【解析】
【分析】
本题考查含硫化合物、浓硫酸、的性质等,难度不大,熟练掌握含硫化合物的性质是解题的关键。
【解答】
A.硫燃烧生成有刺激性气味气体,该气体为具有漂白性的二氧化硫,可以漂白纸浆,故A正确;
B.向蔗糖中加入浓硫酸,蔗糖变黑色,说明浓硫酸具有强的脱水性,故B错误;
C.将气体通入溶液生成沉淀,故C错误;
D.在常温下遇浓硫酸发生钝化,加热下持续反应,现象描述不正确,故D错误。
6.【答案】
【解析】
【分析】
本题考查浓硫酸的性质,为高频考点,把握物质的性质、反应与现象为解答的关键,题目难度不大。
【解答】
A.浓硫酸滴至蔗糖,炭化变黑,体现浓硫酸的脱水性,故A不选;
B.浓硫酸滴至铝片,发生钝化,无现象,故B选;
C.浓硫酸滴至胆矾,体现浓硫酸的吸水性,蓝色晶体变成白色,故C不选;
D.浓硫酸滴至纯碱发生反应有气体生成,体现浓硫酸的强酸性,故D不选。
7.【答案】
【解析】
【分析】
本题考查含硫化合物的性质,为高频考点,综合考查元素化合物知识,把握漂白原理及发生的氧化还原反应为解答的关键,题目难度不大。
【解答】
A.具有漂白性,它能使品红溶液褪色,具有还原性使溴水、酸性高锰酸钾溶液褪色,二氧化硫使石蕊变红是因为酸性,故A错误;
B. 硫在自然界中游离态和化合态存在,故B错误;
C. 用硫黄或黄铁矿作为原料可以制备硫酸,或与氧气反应生成,再与氧气反应生成,然后与水反应生成,故C正确;
D. 浓硫酸与单质碳的反应生成二氧化硫,二氧化碳和水,浓硫酸只表现了强氧化性,故D错误。
故选C。
8.【答案】
【解析】
【分析】
本题考查了元素化合物知识,熟悉浓硫酸、二氧化硫的性质是解题关键,题目难度中等。
【解答】
A.浓硫酸有强氧化性和酸性,所以不能干燥,也不能干燥等还原性气体,故A正确;
B.浓硫酸与灼热的炭反应,硫元素化合价降低,只体现了浓硫酸的强氧化性,故B错误;
C.二氧化硫的漂白性是因为二氧化硫和有色物质反应生成无色物质,该反应中二氧化硫不体现氧化性,氯气使品红溶液褪色是利用次氯酸的强氧化性,二者漂白原理不同,不能说明二氧化硫的氧化性没有氯气强,故C错误;
D.工业制硫酸的三设备是:沸腾炉,接触室,吸收塔,沸腾炉、接触室所涉及的反应均为氧化还原反应,吸收塔所涉及的反应不是氧化还原反应,故D错误。
9.【答案】
【解析】
【分析】
本题考查浓硫酸的性质,侧重于对元素化合物知识的理解和运用的考查,注意浓硫酸的特性,难度不大。
【解答】
A.浓硫酸与氯化钠中元素化合价无变化,浓硫酸只提供,表现为酸性,项正确;
B.甲酸中的和能被浓硫酸以的形式脱出,项正确;
C.在浓中,硫元素部分化合价降低,部分化合价不变,所以浓硫酸既表现了其强氧化性又表现了其酸性,项错误;
D.中的水分子被浓硫酸夺取表现为吸水性,项正确。
10.【答案】
【解析】解:自然界中存在游离态的硫,如火山口存在游离态的硫,故A错误;
B.排放二氧化硫会污染空气,形成酸雨,但不会导致光化学烟雾产生,故B错误;
C.二氧化硫能使滴有酚酞的氢氧化钠溶液褪色,体现了酸性氧化物的性质,与漂白性无关,故C错误;
D.浓硫酸具有吸水性,可干燥、、等气体,故D正确;
故选:。
本题考查含硫物质的性质,侧重二氧化硫、浓硫酸性质的考查,注意性质与现象、用途的关系即可解答,注重基础知识的训练,题目难度不大.
11.【答案】
【解析】
【分析】
本题考查了绿矾制硫酸的反应原理和产物的性质检验,溶液质量分数的计算,主要是二氧化硫、三氧化硫性质的应用,难度不大。
【解答】
A.若将反应后的三种气体通入溶液中,产生的沉淀为,二氧化硫不能和氯化钡反应,故A错误;
B.中产物用紫色石蕊试液能检验出氢离子的存在,但检验不出硫酸根离子,故B错误;
C.氢氧化钠吸收二氧化硫无明显现象,应用品红试液检验,故C错误;
D.化学反应中生成时生成,与发生反应:,反应后溶液中含、;溶质质量分数;故D正确。
故选D。
12.【答案】
【解析】
【分析】
本题考查物质的性质和用途,难度不大,掌握二氧化硫、浓硫酸的性质、发生的反应是关键。
【解答】
A.具有漂白性,可以用于漂白纸浆和草帽辫,选项A正确;
B.浓硫酸具有强氧化性,二氧化硫具有还原性,硫元素化合价为和价,同元素相邻价态不能发生氧化还原反应,浓硫酸不能氧化二氧化硫,所以能干燥二氧化硫,选项B错误;
C.将浓硫酸滴到蔗糖表面,固体变黑,是因为浓硫酸的脱水性使蔗糖碳化;膨胀是因为有二氧化碳和二氧化硫气体生成,浓硫酸表现强氧化性,选项C正确;
D.和反应的化学方程式为,此反应中、元素发生变化,为氧化还原反应,选项D正确。
13.【答案】
【解析】
【分析】本题主要考查元素化合物的性质与用途,题目难度中等,熟练掌握常见元素化合物的性质是解题的关键。
【解答】
A.二氧化硫具有漂白性,用于漂白纸浆,与其氧化性无关,故 A错误
B.明矾能水解生成氢氧化铝胶体,氢氧化铝胶体具有吸附性,能吸附水中的悬浮颗粒而净水,与明矾
的水溶性无关,故B错误
C.浓硫酸可用于干燥氢气,因为其具有吸水性,故C错误
D.、均为离子晶体、熔点高,所以可用于制作耐火材料,故D正确
故选:。
14.【答案】
【解析】
【分析】
本题综合考查了浓硫酸的性质,涉及了浓硫酸的吸水性、脱水性、强氧化性等知识,综合性较强,注意浓硫酸吸水性与脱水性的区别。
【解答】
常温下,浓硫酸能使金属铁、铝钝化,故正确;
随着反应的进行浓硫酸逐渐变成稀硫酸,稀硫酸不与铜反应,所以硫酸有剩余,剩余的稀硫酸还能与足量的铁反应放出,故错误;
浓硫酸使蔗糖炭化,表现其脱水性,故错误;
随着反应的进行浓硫酸逐渐变成稀硫酸,稀硫酸不与铜反应,所以硫酸有剩余,剩余的稀硫酸还能与足量的铁反应放出,正确;
浓硫酸可干燥中性和酸性气体,不能干燥碱性气体,故错误;
随着反应的进行浓硫酸逐渐变成稀硫酸,剩余的稀硫酸还能与足量的铁反应放出,故错误;
浓硫酸与在常温下不反应,故错误;
浓硫酸中的硫为价,二氧化硫中的硫为价,二者不反应,故错误。
15.【答案】
【解析】
【分析】
本题考查氧化还原反应中相关概念,为高频考点,侧重于学生的分析能力的考查,注意由现象得出结论,题目难度一般。
【解答】
A.中利用硫酸的难挥发性制取,遇水蒸气产生白雾,故A正确;
B. 反应生成红棕色气体是溴蒸气,说明浓硫酸能将溴离子氧化成溴单质,体现了浓硫酸的强氧化性,故B正确;
C. 反应生成的有刺激性气味、能使品红溶液褪色的是二氧化硫气体,故C正确;
D. 反应生成是二氧化硫气体,不是氧化还原反应,而是强酸制弱酸,故D错误;
故选D。
16.【答案】增大;增大;吸水
脱水
酸;
棕;浓
【解析】
【分析】
本题综合考查浓硫酸的性质、硝酸的性质、喷泉实验的形成条件等,侧重于物质的性质的考查,解题关键是把握喷泉实验形成原理、浓硫酸的特性,学习中注意相关基础知识的积累,题目难度不大。
【解答】
浓硫酸具有吸水性,敞口久置其质量会增大,浓硫酸吸水后浓度变稀,溶液的值会增大;
浓硫酸与、、、发生反应,则不能用浓硫酸干燥、、、,故可用浓硫酸干燥的是;
用蘸有浓溶液的玻璃棒在木板上写字,字迹变黑,说明浓溶液具有脱水性;
铁锈成分为,稀硫酸常用来洗涤金属表面的铁锈,这是利用了硫酸的酸性,反应方程式为:
浓硝酸见光或受热易分解,需保存在棕色试剂瓶中,原因是浓
要形成喷泉,必须满足则烧瓶内的气体应溶于溶液或与溶液发生反应,烧瓶内的气体体积减小,导致烧瓶内的压强小于大气压,二氧化硫和浓反应而导致烧瓶内的压强小于大气压,可形成喷泉;二氧化碳和饱和不反应,不能形成喷泉;氧气和水不反应,且不溶于水,不能形成喷泉;氯气和反应生成氯化钠和次氯酸钠,导致烧瓶内的压强小于大气压,可形成喷泉;故选。
17.【答案】;;
;;;
吸水性;脱水性;强氧化性
【解析】
【分析】
本题考查同位素、同素异形体等、化学键、共价化合物和离子化合物、浓硫酸的性质,解答这类问题应明确相关概念以及硫酸的性质,试题较易。
【解答】
与中二者质子数相同,中子数不同,且均为原子,所以二者互为同位素;
和是由同种元素形成的不同单质,所以二者互为同素异形体;
、、为质子数相同,中子数不同的原子,所以三者互为同位素;
金刚石和石墨是由同种元素形成的不同单质,所以二者互为同素异形体;
和二者质量数相同,质子数不同;
只存在共价键,属于共价化合物;
只存在共价键,属于共价化合物;
既存在极性共价键又存在离子键,属于离子化合物;
既存在非极性共价键又存在离子键,属于离子化合物;
只存在离子键,属于离子化合物;
不存在化学键;
盛有浓硫酸的烧杯敞口放置一段时间后,质量增加,说明浓硫酸具有吸水性;
用玻璃棒蘸浓硫酸滴在纸上时,纸变黑体现浓硫酸的脱水性;
在常温下可以用铁、铝制容器盛装冷的浓硫酸,体现浓硫酸的强氧化性。
18.【答案】
固体由黑色变为红色
检验是否除净
浓硫酸
固体由白色变为蓝色
防止空气中水蒸气进入干燥管中干扰实验
【解析】本题考查锌与浓硫酸反应实验探究。
装置作用为吸收混合气体中的,发生反应为。
检验的存在,需要先除去混合气体中的,即在装置中盛装浓溶液,用中品红溶液检验装置是否将除尽,通过装置中的浓硫酸,除去中的水蒸气,然后干燥的与反应,最后用中球形干燥管中的无水硫酸铜检验生成的水蒸气,则装置连接顺序为。
氢气还原氧化铜生成铜,中固体由黑色粉末变为红色。
根据的分析,装置的作用是验证是否除尽。
根据的分析,装置中装浓硫酸。
根据的分析,装置中的球形干燥管中装无水硫酸铜检验是否有水生成,白色粉末变蓝说明有水生成。
因为二氧化硫在中完全吸收,装置中碱石灰的作用不是尾气吸收,应为防止外界水蒸气进入干燥管干扰实验。
19.【答案】 浓
品红溶液褪色 紫色石蕊溶液变红
浓
【解析】
【分析】
Ⅰ铜与浓硫酸混合加热发生氧化还原反应产生、、,具有漂白性,能够使品红溶液褪色;溶于水,反应产生,使溶液显酸性,可以使紫色石蕊试液变为红色,多余的气体用溶液吸收,防止大气污染;
Ⅱ与浓盐酸混合加热反应产生,由于氯气的密度比空气大,可以使用向上排空气的方法收集,多余的可根据氯气能够与碱反应的性质,用溶液吸收,防止大气污染。
在加热条件下与浓硫酸混合反应产生、、,该反应的化学方程式为:浓;
在该反应中为还原剂,为氧化剂,参加反应,只有作氧化剂,故反应中氧化剂与还原剂的物质的量之比:;
反应产生的具有漂白性,能够使品红溶液褪色;溶于水,与水反应产生,电离产生,使溶液显酸性,因此气体可以使紫色石蕊试液变为红色;
某工厂一年反应消耗的煤中含有的的质量是,其物质的量,根据元素守恒,其反应产生的全部用于生产硫酸,制取得到的的浓硫酸的质量;
在实验室中用与浓盐酸混合加热反应产生、、,该反应的化学方程式为:浓;
与石灰乳反应产生、、,即制取得到漂白粉,该反应的化学方程式为:;
将通入溶液中可发生置换反应,产生、,该反应的离子方程式为:,在该反应中,为氧化剂,为氧化产物,因此物质的氧化性:。
第1页,共1页
一、单选题
1. 下列有关浓硫酸的说法正确的是( )
A. 浓硫酸具有吸水性,因此可用作干燥剂,能干燥氢气、硫化氢、氨气等气体
B. 浓硫酸具有脱水性,因而能使蔗糖炭化
C. 浓硫酸在加热条件下能与单质碳反应,体现了浓硫酸的酸性和强氧化性
D. 因为浓硫酸在常温下不与铁或铝反应,因此常温下可用铁制或铝制容器储存浓硫酸
2. 下列变化的实质相似的是( )
A. 浓 和浓硝酸在空气中敞口放置时浓度均减小
B. 和 均能使品红溶液褪色
C. 浓 与稀 与金属反应时均有气体产生
D. 和 气体均不能用浓 干燥
3. 利用如图所示装置进行下列实验,能得出相应实验结论的是( )
选项 实验结论
浓硫酸 溶液褪色 有漂白性
浓盐酸 溶液变为黄色 氧化性:
稀硫酸 溶液无明显变化 不与反应
浓硫酸 蔗糖 溴水褪色 浓硫酸具有脱水性、吸水性
A. B. C. D.
4. 叠氮酸钠是重要的化工原料。以甲醇、亚硝酸钠等为原料制备的流程如下:
已知:水合肼不稳定,具有强还原性。下列描述错误的是 ( )
A. 反应和反应中浓硫酸作用不同
B. 反应的化学方程式:
C. 步骤分离出的可导入中循环利用
D. 反应制备水合肼时应将氨水逐滴滴入溶液中
5. 某同学通过系列实验探究硫及其化合物的性质,实验现象正确且能达到目的的是( )
A. 点燃硫磺产生刺激性气味气体,该气体可以漂白纸浆
B. 向蔗糖中加入浓硫酸,蔗糖变黑色,说明浓硫酸具有强的吸水性
C. 将气体通入溶液生成沉淀
D. 将片加入浓硫酸中,反应剧烈,说明浓硫酸具有强的氧化性
6. 如图所示,将浓硫酸滴至下列物质上,无明显现象的是( )
A. 蔗糖 B. 铝片 C. 胆矾 D. 纯碱
7. 下列关于硫及其化合物的叙述中正确的是( )
A. 因具有漂白性,所以能使品红溶液、溴水、酸性溶液、石蕊试液褪色
B. 硫在自然界中只能以硫化物和硫酸盐的形态存在
C. 硫黄和黄铁矿可以作为制备硫酸的原料
D. 浓硫酸与单质碳的反应中,浓硫酸既表现了强氧化性又表现了酸性
8. 下列有关硫及其化合物的说法中正确的是( )
A. 浓硫酸具有吸水性,可作干燥剂,不能干燥,也不能干燥等还原性气体
B. 浓硫酸与灼热的炭反应,体现了浓硫酸的强氧化性和酸性
C. 和均可使品红溶液褪色,但将溶有的品红溶液加热后又恢复红色,说明的氧化性没有强
D. 以为原料生产硫酸的过程中,要用到沸腾炉、接触室、吸收塔等设备,所涉及的反应均为氧化还原反应
9. 下列有关浓硫酸性质的叙述错误的是( )
A. 在反应:浓中,浓硫酸表现酸性
B. 在反应:中,浓硫酸只表现脱水性
C. 在反应:浓中,浓硫酸只表现氧化性
D. 浓硫酸具有吸水性,因而能使转化为
10. 下列关于硫及其化合物的说法中正确的是( )
A. 自然界中不存在游离态的硫
B. 二氧化硫的排放会导致光化学烟雾的产生
C. 二氧化硫能使滴有酚酞的氢氧化钠溶液褪色,体现了其漂白性
D. 浓硫酸可用来干燥、、等气体
11. 生产硫酸最古老的方法是以绿矾为原料,在蒸镏釜中煅烧。反应的化学方程式为已知二氧化硫的沸点为,三氧化硫的沸点为。用如图所示的装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫,为干燥的试管,加热装置已略去。下列有关说法正确的是( )
A. 若将反应后的三种气体通入溶液中,产生的沉淀为、
B. 中产物用紫色石蕊试液即可检验出其中和
C. 为检验反应的另一种生成物,试管中应加入的试剂为溶液
D. 中所得到的硫酸的质量分数为
12. 下列措施或叙述不合理的是
A. 用漂白纸浆和草帽辫
B. 具有强还原性,浓硫酸具有强氧化性,故浓硫酸不能用于干燥气体
C. 将浓硫酸滴到蔗糖表面,固体变黑膨胀,说明浓硫酸有脱水性和强氧化性
D. 与的反应为氧化还原反应
13. 下列有关物质的性质与用途具有对应关系的是( )
A. 具有氧化性,可用于漂白纸浆 B. 明矾易溶于水,可用作净水剂
C. 浓硫酸具有脱水性,可用于干燥氢气 D. 、熔点高,可用于制作耐火材料
14. 下列有关浓硫酸的叙述中正确的是 ( )
浓硫酸在常温下能够使铁、铝等金属钝化
浓硫酸与铜加热反应后,铜片有剩余,硫酸完全反应
浓硫酸具有吸水性,因而能使蔗糖碳化
浓硫酸与铜加热反应后,铜片有剩余,向反应后的溶液中再加入铁片,会有氢气生成
浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
浓硫酸与铁加热反应后,铁片有剩余,生成的气体除水蒸气外还有。
浓硫酸具有强氧化性,常温下能与发生剧烈反应
浓硫酸具有强氧化性,具有还原性,所以浓硫酸不能干燥
A. B. C. D.
15. 浓硫酸分别与三种钠盐反应,现象如图。下列分析不正确的是( )
A. 中试管口白雾是遇水蒸气所致,利用硫酸的难挥发性
B. 体现了浓硫酸的强氧化性
C. 中有产生
D. 中浓被还原成
二、填空题
16. 将浓硫酸敞口放置在空气中其质量会________填“增大”或“减小”,溶液的值会________填“增大”或“减小”,本过程中浓硫酸表现出________性。
浓硫酸表现吸水性时,可作干燥剂,下列物质可用浓硫酸干燥的是________。
A.
用蘸有浓硫酸的玻璃棒在木板上写字,字迹变黑。浓硫酸主要表现出________性。
稀硫酸常用来洗涤金属表面的铁锈,这是利用了硫酸的________性,请写出有关反应的化学方程式:___________________________________
从试剂柜中取出一瓶浓硝酸,发现其保存在________色试剂瓶中,溶液呈黄色,其原因是:______________________________用化学方程式表述
某同学根据氨的喷泉实验原理,有了一个创新的设计:如果改换一下烧瓶内的气体和烧杯中的液体,也能做成喷泉实验。那么下列各组中的气体和液体不符合该学生设计的一组是________。
和浓溶液 和饱和溶液 和水 和溶液
17. 用序号按要求回答下列问题:
下列各组微粒:与 和 、、 金刚石和石墨 和 ,互为同位素的是___________;互为同素异形体的是__________;质量数相等,但不能互称为同位素的是_________。
下列各种物质: ,不存在化学键的是______;只存在离子键的是______;属于共价化合物的是________;含非极性键的离子化合物是 ______ 。
硫酸在不同的情况下会显示出不同的性质,把下列现象中硫酸所表现出来的性质填写在空白处。
盛有浓硫酸的烧杯敞口放置一段时间后,质量增加。
用玻璃棒蘸浓硫酸滴在纸上时,纸变黑。________
在常温下可以用铁、铝制容器盛装冷的浓硫酸。________
三、实验题
18. 结合实验室制备的反应,某实验小组猜想与浓硫酸反应的气体生成物中含有杂质。该小组同学利用如图装置进行实验探究:
装置中盛有浓溶液,实验开始时该装置中发生反应的离子方程式为_________。
装置的正确连接顺序为。( )
如果混合气体中含有足量的,则装置中的现象是____________________________。
装置的作用是____________________________________________________________。
装置中盛装的试剂名称是__________________________________________________。
通过装置的球形干燥管中所盛有的试剂产生的现象:___________________________,可推断出与浓硫酸反应生成的气体混合物中含有。
装置中形管里碱石灰的作用是____________________________________________。
19. 请用你学到的化学知识填空。
Ⅰ实验室可用下图装置对铜与浓硫酸的反应进行探究。
加热条件下铜与浓硫酸反应的化学方程式_______。反应中氧化剂与还原剂的物质的量之比_______。
将产生的气体通入品红溶液中的现象_______,通入紫色石蕊溶液中的现象_______。
某工厂使用的煤中硫的质量分数为,该工厂每天燃烧这种煤,如果把产生的全部用来生产硫酸,理论上每年按天计可得到的浓硫酸的质量为_______。
Ⅱ实验室制氯气可用下图装置,并进行氯气性质实验。
写出实验室制备氯气的化学方程式:_______。
将氯气通入冷的石灰乳中可制备用于环境消毒的漂白粉,写出此反应的化学方程式_______。
将氯气通入溶液中可发生置换反应,写出反应的离子方程式_______;通过单质之间的置换证明氧化性_______填“”,“”或“”。
答案和解析
1.【答案】
【解析】
【分析】
本题考查了浓硫酸的性质,难度较小,掌握浓硫酸的特性:吸水性、脱水性、强氧化性,以及能够发生的反应是关键,侧重考查基础知识的掌握和应用。
【解答】
A.浓硫酸具有吸水性,因此可用作干燥剂,但不能干燥还原性气体如:硫化氢,碱性气体如:氨气等气体,故A错误;
B.浓硫酸具有脱水性,因而能使蔗糖脱水炭化,故B正确;
C.浓硫酸在加热条件下能与单质碳反应,体现了浓硫酸的强氧化性,故C错误;
D.因为浓硫酸在常温下可使铁或铝钝化,因此常温下可用铁制或铝制容器储存浓硫酸,故D错误。
故选B。
2.【答案】
【解析】
【分析】
本题综合考查元素化合物知识,侧重于基础知识的考查,意在考查学生的识记能力,注意相关基础知识的积累,把握相关物质的性质。
【解答】
A.浓硫酸具有吸水性,硝酸易挥发,二者放置在空气中浓度都变小,但变化的实质不同,故A错误;
B.二氧化硫与有色物质发生化合反应而使有色物质漂白,氯水中的次氯酸具有强氧化性而使有色物质漂白,二者漂白原理不同,二氧化硫的漂白不稳定,加热可恢复到原来的颜色,故B错误;
C.浓硫酸与锌反应生成二氧化硫,是浓硫酸中元素化合价降低;稀硫酸与锌反应生成氢气,是稀硫酸中元素化合价降低,二者产生气体的实质不同,故C错误;
D.、都具有还原性,都可与浓硫酸发生氧化还原反应而不能用浓硫酸干燥,故D正确。
故选D。
3.【答案】
【解析】
【分析】
本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、物质的性质、反应与现象、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大。
【解答】
A.二氧化硫与高锰酸钾发生氧化还原反应,与二氧化硫的还原性有关,与漂白性无关,故A错误;
B.氯气与溶液发生氧化还原反应,亚铁离子、溴离子均被氧化,则不能说明氧化性:,故B错误;
C.稀硫酸与碳酸钠反应生成二氧化碳,盐酸的酸性大于碳酸的酸性,则不与反应,故C正确;
D.浓硫酸使蔗糖脱水后,与浓硫酸发生氧化还原反应生成二氧化硫,二氧化硫使溴水褪色,则说明浓硫酸具有脱水性、强氧化性,故D错误;
故选:。
4.【答案】
【解析】 由题给流程可知,向甲醇、亚硝酸钠的混合物中加入浓硫酸,浓硫酸先与亚硝酸钠反应生成亚硝酸,在浓硫酸作用下,甲醇与亚硝酸发生酯化反应生成亚硝酸甲酯;氨水和次氯酸钠溶液混合发生氧化还原反应得到水合肼,在氢氧化钠溶液中,亚硝酸甲酯与水合肼发生氧化还原反应生成叠氮酸钠、甲醇和水,在蒸汽加热的条件下,向反应后的溶液中加入浓硫酸,浓硫酸与叠氮酸钠反应制得叠氮酸,叠氮酸与氢氧化钠溶液反应制得产品叠氮酸钠。
由分析可知,反应中浓硫酸起酸、催化剂的作用,反应中浓硫酸只起酸的作用,作用不同,A正确;
由分析可知,反应为在氢氧化钠溶液中,亚硝酸甲酯与水合肼发生氧化还原反应生成叠氮酸钠、甲醇和水,反应的化学方程式为,B正确;
由分析可知,反应中甲醇为反应物,则步骤分离出的甲醇可导入中循环利用,C正确;
水合肼具有强还原性,若反应制备水合肼时将氨水逐滴滴入具有强氧化性的次氯酸钠溶液中,水合肼会与次氯酸钠发生氧化还原反应,而无法制得水合肼,D错误。
5.【答案】
【解析】
【分析】
本题考查含硫化合物、浓硫酸、的性质等,难度不大,熟练掌握含硫化合物的性质是解题的关键。
【解答】
A.硫燃烧生成有刺激性气味气体,该气体为具有漂白性的二氧化硫,可以漂白纸浆,故A正确;
B.向蔗糖中加入浓硫酸,蔗糖变黑色,说明浓硫酸具有强的脱水性,故B错误;
C.将气体通入溶液生成沉淀,故C错误;
D.在常温下遇浓硫酸发生钝化,加热下持续反应,现象描述不正确,故D错误。
6.【答案】
【解析】
【分析】
本题考查浓硫酸的性质,为高频考点,把握物质的性质、反应与现象为解答的关键,题目难度不大。
【解答】
A.浓硫酸滴至蔗糖,炭化变黑,体现浓硫酸的脱水性,故A不选;
B.浓硫酸滴至铝片,发生钝化,无现象,故B选;
C.浓硫酸滴至胆矾,体现浓硫酸的吸水性,蓝色晶体变成白色,故C不选;
D.浓硫酸滴至纯碱发生反应有气体生成,体现浓硫酸的强酸性,故D不选。
7.【答案】
【解析】
【分析】
本题考查含硫化合物的性质,为高频考点,综合考查元素化合物知识,把握漂白原理及发生的氧化还原反应为解答的关键,题目难度不大。
【解答】
A.具有漂白性,它能使品红溶液褪色,具有还原性使溴水、酸性高锰酸钾溶液褪色,二氧化硫使石蕊变红是因为酸性,故A错误;
B. 硫在自然界中游离态和化合态存在,故B错误;
C. 用硫黄或黄铁矿作为原料可以制备硫酸,或与氧气反应生成,再与氧气反应生成,然后与水反应生成,故C正确;
D. 浓硫酸与单质碳的反应生成二氧化硫,二氧化碳和水,浓硫酸只表现了强氧化性,故D错误。
故选C。
8.【答案】
【解析】
【分析】
本题考查了元素化合物知识,熟悉浓硫酸、二氧化硫的性质是解题关键,题目难度中等。
【解答】
A.浓硫酸有强氧化性和酸性,所以不能干燥,也不能干燥等还原性气体,故A正确;
B.浓硫酸与灼热的炭反应,硫元素化合价降低,只体现了浓硫酸的强氧化性,故B错误;
C.二氧化硫的漂白性是因为二氧化硫和有色物质反应生成无色物质,该反应中二氧化硫不体现氧化性,氯气使品红溶液褪色是利用次氯酸的强氧化性,二者漂白原理不同,不能说明二氧化硫的氧化性没有氯气强,故C错误;
D.工业制硫酸的三设备是:沸腾炉,接触室,吸收塔,沸腾炉、接触室所涉及的反应均为氧化还原反应,吸收塔所涉及的反应不是氧化还原反应,故D错误。
9.【答案】
【解析】
【分析】
本题考查浓硫酸的性质,侧重于对元素化合物知识的理解和运用的考查,注意浓硫酸的特性,难度不大。
【解答】
A.浓硫酸与氯化钠中元素化合价无变化,浓硫酸只提供,表现为酸性,项正确;
B.甲酸中的和能被浓硫酸以的形式脱出,项正确;
C.在浓中,硫元素部分化合价降低,部分化合价不变,所以浓硫酸既表现了其强氧化性又表现了其酸性,项错误;
D.中的水分子被浓硫酸夺取表现为吸水性,项正确。
10.【答案】
【解析】解:自然界中存在游离态的硫,如火山口存在游离态的硫,故A错误;
B.排放二氧化硫会污染空气,形成酸雨,但不会导致光化学烟雾产生,故B错误;
C.二氧化硫能使滴有酚酞的氢氧化钠溶液褪色,体现了酸性氧化物的性质,与漂白性无关,故C错误;
D.浓硫酸具有吸水性,可干燥、、等气体,故D正确;
故选:。
本题考查含硫物质的性质,侧重二氧化硫、浓硫酸性质的考查,注意性质与现象、用途的关系即可解答,注重基础知识的训练,题目难度不大.
11.【答案】
【解析】
【分析】
本题考查了绿矾制硫酸的反应原理和产物的性质检验,溶液质量分数的计算,主要是二氧化硫、三氧化硫性质的应用,难度不大。
【解答】
A.若将反应后的三种气体通入溶液中,产生的沉淀为,二氧化硫不能和氯化钡反应,故A错误;
B.中产物用紫色石蕊试液能检验出氢离子的存在,但检验不出硫酸根离子,故B错误;
C.氢氧化钠吸收二氧化硫无明显现象,应用品红试液检验,故C错误;
D.化学反应中生成时生成,与发生反应:,反应后溶液中含、;溶质质量分数;故D正确。
故选D。
12.【答案】
【解析】
【分析】
本题考查物质的性质和用途,难度不大,掌握二氧化硫、浓硫酸的性质、发生的反应是关键。
【解答】
A.具有漂白性,可以用于漂白纸浆和草帽辫,选项A正确;
B.浓硫酸具有强氧化性,二氧化硫具有还原性,硫元素化合价为和价,同元素相邻价态不能发生氧化还原反应,浓硫酸不能氧化二氧化硫,所以能干燥二氧化硫,选项B错误;
C.将浓硫酸滴到蔗糖表面,固体变黑,是因为浓硫酸的脱水性使蔗糖碳化;膨胀是因为有二氧化碳和二氧化硫气体生成,浓硫酸表现强氧化性,选项C正确;
D.和反应的化学方程式为,此反应中、元素发生变化,为氧化还原反应,选项D正确。
13.【答案】
【解析】
【分析】本题主要考查元素化合物的性质与用途,题目难度中等,熟练掌握常见元素化合物的性质是解题的关键。
【解答】
A.二氧化硫具有漂白性,用于漂白纸浆,与其氧化性无关,故 A错误
B.明矾能水解生成氢氧化铝胶体,氢氧化铝胶体具有吸附性,能吸附水中的悬浮颗粒而净水,与明矾
的水溶性无关,故B错误
C.浓硫酸可用于干燥氢气,因为其具有吸水性,故C错误
D.、均为离子晶体、熔点高,所以可用于制作耐火材料,故D正确
故选:。
14.【答案】
【解析】
【分析】
本题综合考查了浓硫酸的性质,涉及了浓硫酸的吸水性、脱水性、强氧化性等知识,综合性较强,注意浓硫酸吸水性与脱水性的区别。
【解答】
常温下,浓硫酸能使金属铁、铝钝化,故正确;
随着反应的进行浓硫酸逐渐变成稀硫酸,稀硫酸不与铜反应,所以硫酸有剩余,剩余的稀硫酸还能与足量的铁反应放出,故错误;
浓硫酸使蔗糖炭化,表现其脱水性,故错误;
随着反应的进行浓硫酸逐渐变成稀硫酸,稀硫酸不与铜反应,所以硫酸有剩余,剩余的稀硫酸还能与足量的铁反应放出,正确;
浓硫酸可干燥中性和酸性气体,不能干燥碱性气体,故错误;
随着反应的进行浓硫酸逐渐变成稀硫酸,剩余的稀硫酸还能与足量的铁反应放出,故错误;
浓硫酸与在常温下不反应,故错误;
浓硫酸中的硫为价,二氧化硫中的硫为价,二者不反应,故错误。
15.【答案】
【解析】
【分析】
本题考查氧化还原反应中相关概念,为高频考点,侧重于学生的分析能力的考查,注意由现象得出结论,题目难度一般。
【解答】
A.中利用硫酸的难挥发性制取,遇水蒸气产生白雾,故A正确;
B. 反应生成红棕色气体是溴蒸气,说明浓硫酸能将溴离子氧化成溴单质,体现了浓硫酸的强氧化性,故B正确;
C. 反应生成的有刺激性气味、能使品红溶液褪色的是二氧化硫气体,故C正确;
D. 反应生成是二氧化硫气体,不是氧化还原反应,而是强酸制弱酸,故D错误;
故选D。
16.【答案】增大;增大;吸水
脱水
酸;
棕;浓
【解析】
【分析】
本题综合考查浓硫酸的性质、硝酸的性质、喷泉实验的形成条件等,侧重于物质的性质的考查,解题关键是把握喷泉实验形成原理、浓硫酸的特性,学习中注意相关基础知识的积累,题目难度不大。
【解答】
浓硫酸具有吸水性,敞口久置其质量会增大,浓硫酸吸水后浓度变稀,溶液的值会增大;
浓硫酸与、、、发生反应,则不能用浓硫酸干燥、、、,故可用浓硫酸干燥的是;
用蘸有浓溶液的玻璃棒在木板上写字,字迹变黑,说明浓溶液具有脱水性;
铁锈成分为,稀硫酸常用来洗涤金属表面的铁锈,这是利用了硫酸的酸性,反应方程式为:
浓硝酸见光或受热易分解,需保存在棕色试剂瓶中,原因是浓
要形成喷泉,必须满足则烧瓶内的气体应溶于溶液或与溶液发生反应,烧瓶内的气体体积减小,导致烧瓶内的压强小于大气压,二氧化硫和浓反应而导致烧瓶内的压强小于大气压,可形成喷泉;二氧化碳和饱和不反应,不能形成喷泉;氧气和水不反应,且不溶于水,不能形成喷泉;氯气和反应生成氯化钠和次氯酸钠,导致烧瓶内的压强小于大气压,可形成喷泉;故选。
17.【答案】;;
;;;
吸水性;脱水性;强氧化性
【解析】
【分析】
本题考查同位素、同素异形体等、化学键、共价化合物和离子化合物、浓硫酸的性质,解答这类问题应明确相关概念以及硫酸的性质,试题较易。
【解答】
与中二者质子数相同,中子数不同,且均为原子,所以二者互为同位素;
和是由同种元素形成的不同单质,所以二者互为同素异形体;
、、为质子数相同,中子数不同的原子,所以三者互为同位素;
金刚石和石墨是由同种元素形成的不同单质,所以二者互为同素异形体;
和二者质量数相同,质子数不同;
只存在共价键,属于共价化合物;
只存在共价键,属于共价化合物;
既存在极性共价键又存在离子键,属于离子化合物;
既存在非极性共价键又存在离子键,属于离子化合物;
只存在离子键,属于离子化合物;
不存在化学键;
盛有浓硫酸的烧杯敞口放置一段时间后,质量增加,说明浓硫酸具有吸水性;
用玻璃棒蘸浓硫酸滴在纸上时,纸变黑体现浓硫酸的脱水性;
在常温下可以用铁、铝制容器盛装冷的浓硫酸,体现浓硫酸的强氧化性。
18.【答案】
固体由黑色变为红色
检验是否除净
浓硫酸
固体由白色变为蓝色
防止空气中水蒸气进入干燥管中干扰实验
【解析】本题考查锌与浓硫酸反应实验探究。
装置作用为吸收混合气体中的,发生反应为。
检验的存在,需要先除去混合气体中的,即在装置中盛装浓溶液,用中品红溶液检验装置是否将除尽,通过装置中的浓硫酸,除去中的水蒸气,然后干燥的与反应,最后用中球形干燥管中的无水硫酸铜检验生成的水蒸气,则装置连接顺序为。
氢气还原氧化铜生成铜,中固体由黑色粉末变为红色。
根据的分析,装置的作用是验证是否除尽。
根据的分析,装置中装浓硫酸。
根据的分析,装置中的球形干燥管中装无水硫酸铜检验是否有水生成,白色粉末变蓝说明有水生成。
因为二氧化硫在中完全吸收,装置中碱石灰的作用不是尾气吸收,应为防止外界水蒸气进入干燥管干扰实验。
19.【答案】 浓
品红溶液褪色 紫色石蕊溶液变红
浓
【解析】
【分析】
Ⅰ铜与浓硫酸混合加热发生氧化还原反应产生、、,具有漂白性,能够使品红溶液褪色;溶于水,反应产生,使溶液显酸性,可以使紫色石蕊试液变为红色,多余的气体用溶液吸收,防止大气污染;
Ⅱ与浓盐酸混合加热反应产生,由于氯气的密度比空气大,可以使用向上排空气的方法收集,多余的可根据氯气能够与碱反应的性质,用溶液吸收,防止大气污染。
在加热条件下与浓硫酸混合反应产生、、,该反应的化学方程式为:浓;
在该反应中为还原剂,为氧化剂,参加反应,只有作氧化剂,故反应中氧化剂与还原剂的物质的量之比:;
反应产生的具有漂白性,能够使品红溶液褪色;溶于水,与水反应产生,电离产生,使溶液显酸性,因此气体可以使紫色石蕊试液变为红色;
某工厂一年反应消耗的煤中含有的的质量是,其物质的量,根据元素守恒,其反应产生的全部用于生产硫酸,制取得到的的浓硫酸的质量;
在实验室中用与浓盐酸混合加热反应产生、、,该反应的化学方程式为:浓;
与石灰乳反应产生、、,即制取得到漂白粉,该反应的化学方程式为:;
将通入溶液中可发生置换反应,产生、,该反应的离子方程式为:,在该反应中,为氧化剂,为氧化产物,因此物质的氧化性:。
第1页,共1页
