1.2 第1课时 原电池的工作原理 课件(共22张PPT)-高中化学鲁科版选择性必修第一册
文档属性
| 名称 | 1.2 第1课时 原电池的工作原理 课件(共22张PPT)-高中化学鲁科版选择性必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 10.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-28 00:00:00 | ||
图片预览





文档简介
(共22张PPT)
第1课时 原电池的工作原理
第1章 第2节
1.理解原电池的工作原理,能根据电极反应、电流方向或离子的移动方向判断
原电池的正极和负极(重点)。
2.能正确书写原电池电极反应和电池总反应方程式(难点)。
3.能设计简单的原电池并能理解原电池工作原理的应用。
学习目标
情境思考
动力系统:氢燃料电池
氢氧燃料电池被认为是利用氢能解决未来人类能源危机的途径之一。氢氧燃料电池可将化学能直接转换为电能,能量转换效率通常为60%
~ 80%,而且污染少、噪音小、装置可大可小、使用方便。
电池究竟是一种什么样的装置?它在工作时,装置中发生了什么变化?
原电池的工作原理
一
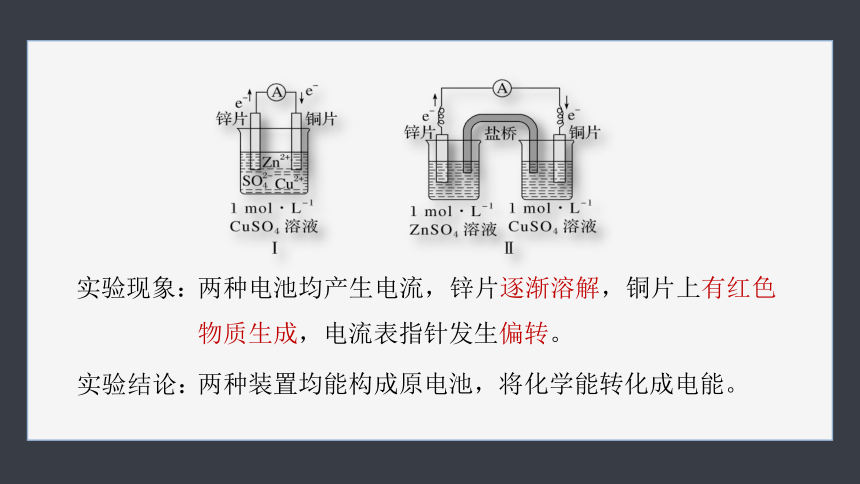
1.实验探究含盐桥的锌铜原电池的工作原理
实验结论:
实验现象:
两种电池均产生电流,锌片逐渐溶解,铜片上有红色物质生成,电流表指针发生偏转。
两种装置均能构成原电池,将化学能转化成电能。
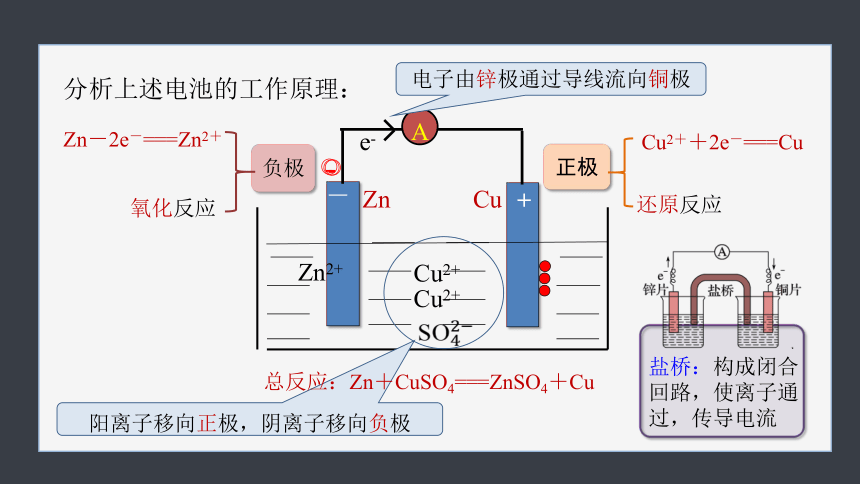
分析上述电池的工作原理:
Cu
Zn
-
-
-
Zn2+
Cu2+
Cu2+
A
e-
-
+
负极
正极
Zn-2e-===Zn2+
氧化反应
Cu2++2e-===Cu
还原反应
阳离子移向正极,阴离子移向负极
电子由锌极通过导线流向铜极
总反应:Zn+CuSO4===ZnSO4+Cu
盐桥:构成闭合回路,使离子通过,传导电流
思考交流1
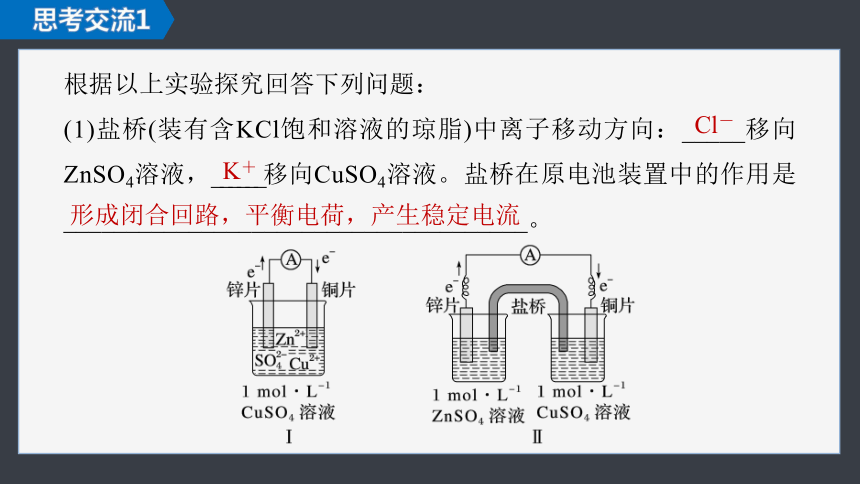
根据以上实验探究回答下列问题:
(1)盐桥(装有含KCl饱和溶液的琼脂)中离子移动方向:_____移向ZnSO4溶液,______移向CuSO4溶液。盐桥在原电池装置中的作用是
_____________________________________。
Cl-
K+
形成闭合回路,平衡电荷,产生稳定电流
思考交流1
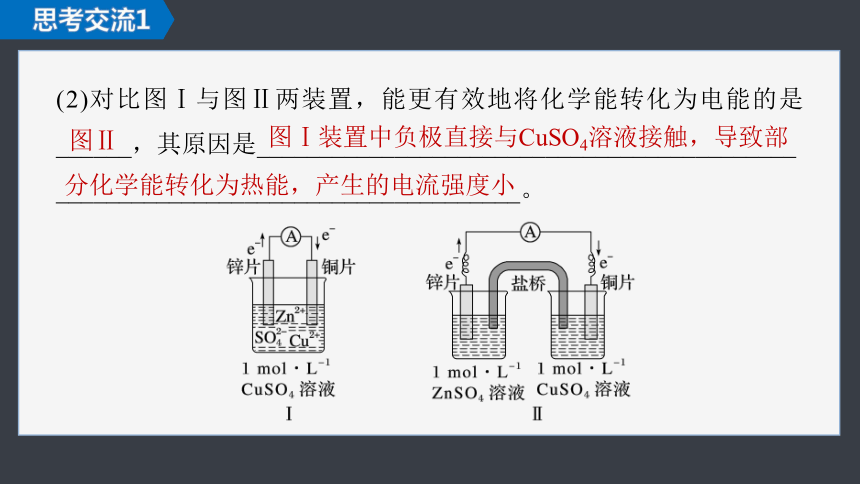
(2)对比图Ⅰ与图Ⅱ两装置,能更有效地将化学能转化为电能的是
______,其原因是___________________________________________
_____________________________________。
图Ⅱ
图Ⅰ装置中负极直接与CuSO4溶液接触,导致部
分化学能转化为热能,产生的电流强度小
2.原电池
(1)定义:利用氧化还原反应将化学能直接转化为电能的装置。
只有氧化还原反应才能有电子转移,有机会形成电流
这种装置是如何构成的呢?
氧化还原反应在这样的装置中是如何产生电流的呢?
(2)原电池的构成条件
可能是电极本身
可能是与电极接触的氧化剂、还原剂
外电路电子导体,只有电子通过
内电路离子导体,只有离子通过
自发的氧化还原反应(能对外释放能量)
反应
电极
电极反应物
导体
导电材料
金属和金属(或非金属)
电解质溶液
金属(形成闭合回路)
(3)原电池工作原理示意图
Cu
Zn
-
-
-
Zn2+
H+
H+
A
e-
-
+
负极
正极
发生还原反应
电极反应物:
活泼的非金属或其他较强氧化剂
发生氧化反应
电极反应物:活泼的金属或其他还原剂
离子导体(电解质溶液、熔盐、离子液体等)
阳离子移向
阴离子移向
电子沿导线传递产生电流
思考交流2
(1)下列反应理论上能用于设计成原电池的是______(填序号)。
①HCl(aq)+NaOH(aq)===NaCl(aq)+H2O(l) ΔH<0
②2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l) ΔH<0
③4Fe(OH)2(s)+2H2O(l)+O2(g)===4Fe(OH)3(s) ΔH<0
②③
思考交流2
(2)下列装置中,能构成原电池的是________(填序号),能构成原电池的指出电极的名称并写出电极反应。
①②⑤
答案 ①Cu是正极:2H++2e-===H2↑;Fe是负极:Fe-2e-=== Fe2+。
②Zn是负极:Zn-2e-===Zn2+;Fe是正极:Cu2++2e-===Cu。
⑤Ag是正极:2Ag++2e-=== 2Ag;Cu是负极:Cu-2e-===Cu2+。
原电池中正、负极的判断
归纳总结
判断依据 负极 正极
电子流动方向 电子流出极 电子流入极
离子导体中阴、阳离子定向移动的方向 阴离子移向的电极 阳离子移向的电极
电流方向 电流流入极 电流流出极
两极发生的反应 失电子,发生氧化反应 得电子,发生还原反应
电极材料 活动性较强的金属 活动性较弱的金属或能导电的非金属
原电池工作原理的应用
二
1.加快化学反应速率
当试管a中滴入CuSO4溶液后,观察到其中产生气泡的速率较试管b中的____,其原因是
_________________________________________________________。
快
CuSO4溶液与锌发生置换反应生成Cu,从而形成微小锌铜原电池,加快产生H2的速率
2.比较金属的活动性强弱
有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
实验 装置
部分实验现象 a极质量减小, b极质量增加 b极有气体产生, c极无变化 d极溶解,c极有气体产生 电流从a极流向d极
由此可判断这四种金属的活动性顺序是___________。
d>a>b>c
金属活动性:a>b
金属活动性:b>c
金属活动性:d>c
活动性:d>a
一般来说,负极金属的活动性强于正极金属。根据现象判断出原电池的正、负极,金属的活动性:负极强于正极。
归纳总结
3.设计原电池
利用反应2FeCl3+Cu===2FeCl2+CuCl2,设计一个原电池装置。
(1)在下图方框中画出两种原电池装置图,标明电极材料和电解质溶液。
单液原电池装置图 带盐桥的双液原电池装置图
(说明:正极材料除石墨外,还可以用银、金、铂等)
(2)写出电极反应式。
负极:__________________________________。
正极:__________________________________。
3.设计原电池
利用反应2FeCl3+Cu===2FeCl2+CuCl2,设计一个原电池装置。
Cu-2e-===Cu2+
2Fe3++2e-===2Fe2+
设计原电池的一般思路
首先将氧化还原反应拆分成氧化反应和还原反应两个半反应。
其次确定正、负极选择电极材料,还原剂(一般为比较活泼的金属)为负极,比较不活泼的金属或惰性电极为正极。
最后用导线连接两个电极并插入电解质溶液形成闭合回路,如果两个半反应分别在两个容器中进行,中间应用盐桥连接。
归纳总结
第1课时 原电池的工作原理
第1章 第2节
1.理解原电池的工作原理,能根据电极反应、电流方向或离子的移动方向判断
原电池的正极和负极(重点)。
2.能正确书写原电池电极反应和电池总反应方程式(难点)。
3.能设计简单的原电池并能理解原电池工作原理的应用。
学习目标
情境思考
动力系统:氢燃料电池
氢氧燃料电池被认为是利用氢能解决未来人类能源危机的途径之一。氢氧燃料电池可将化学能直接转换为电能,能量转换效率通常为60%
~ 80%,而且污染少、噪音小、装置可大可小、使用方便。
电池究竟是一种什么样的装置?它在工作时,装置中发生了什么变化?
原电池的工作原理
一
1.实验探究含盐桥的锌铜原电池的工作原理
实验结论:
实验现象:
两种电池均产生电流,锌片逐渐溶解,铜片上有红色物质生成,电流表指针发生偏转。
两种装置均能构成原电池,将化学能转化成电能。
分析上述电池的工作原理:
Cu
Zn
-
-
-
Zn2+
Cu2+
Cu2+
A
e-
-
+
负极
正极
Zn-2e-===Zn2+
氧化反应
Cu2++2e-===Cu
还原反应
阳离子移向正极,阴离子移向负极
电子由锌极通过导线流向铜极
总反应:Zn+CuSO4===ZnSO4+Cu
盐桥:构成闭合回路,使离子通过,传导电流
思考交流1
根据以上实验探究回答下列问题:
(1)盐桥(装有含KCl饱和溶液的琼脂)中离子移动方向:_____移向ZnSO4溶液,______移向CuSO4溶液。盐桥在原电池装置中的作用是
_____________________________________。
Cl-
K+
形成闭合回路,平衡电荷,产生稳定电流
思考交流1
(2)对比图Ⅰ与图Ⅱ两装置,能更有效地将化学能转化为电能的是
______,其原因是___________________________________________
_____________________________________。
图Ⅱ
图Ⅰ装置中负极直接与CuSO4溶液接触,导致部
分化学能转化为热能,产生的电流强度小
2.原电池
(1)定义:利用氧化还原反应将化学能直接转化为电能的装置。
只有氧化还原反应才能有电子转移,有机会形成电流
这种装置是如何构成的呢?
氧化还原反应在这样的装置中是如何产生电流的呢?
(2)原电池的构成条件
可能是电极本身
可能是与电极接触的氧化剂、还原剂
外电路电子导体,只有电子通过
内电路离子导体,只有离子通过
自发的氧化还原反应(能对外释放能量)
反应
电极
电极反应物
导体
导电材料
金属和金属(或非金属)
电解质溶液
金属(形成闭合回路)
(3)原电池工作原理示意图
Cu
Zn
-
-
-
Zn2+
H+
H+
A
e-
-
+
负极
正极
发生还原反应
电极反应物:
活泼的非金属或其他较强氧化剂
发生氧化反应
电极反应物:活泼的金属或其他还原剂
离子导体(电解质溶液、熔盐、离子液体等)
阳离子移向
阴离子移向
电子沿导线传递产生电流
思考交流2
(1)下列反应理论上能用于设计成原电池的是______(填序号)。
①HCl(aq)+NaOH(aq)===NaCl(aq)+H2O(l) ΔH<0
②2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l) ΔH<0
③4Fe(OH)2(s)+2H2O(l)+O2(g)===4Fe(OH)3(s) ΔH<0
②③
思考交流2
(2)下列装置中,能构成原电池的是________(填序号),能构成原电池的指出电极的名称并写出电极反应。
①②⑤
答案 ①Cu是正极:2H++2e-===H2↑;Fe是负极:Fe-2e-=== Fe2+。
②Zn是负极:Zn-2e-===Zn2+;Fe是正极:Cu2++2e-===Cu。
⑤Ag是正极:2Ag++2e-=== 2Ag;Cu是负极:Cu-2e-===Cu2+。
原电池中正、负极的判断
归纳总结
判断依据 负极 正极
电子流动方向 电子流出极 电子流入极
离子导体中阴、阳离子定向移动的方向 阴离子移向的电极 阳离子移向的电极
电流方向 电流流入极 电流流出极
两极发生的反应 失电子,发生氧化反应 得电子,发生还原反应
电极材料 活动性较强的金属 活动性较弱的金属或能导电的非金属
原电池工作原理的应用
二
1.加快化学反应速率
当试管a中滴入CuSO4溶液后,观察到其中产生气泡的速率较试管b中的____,其原因是
_________________________________________________________。
快
CuSO4溶液与锌发生置换反应生成Cu,从而形成微小锌铜原电池,加快产生H2的速率
2.比较金属的活动性强弱
有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
实验 装置
部分实验现象 a极质量减小, b极质量增加 b极有气体产生, c极无变化 d极溶解,c极有气体产生 电流从a极流向d极
由此可判断这四种金属的活动性顺序是___________。
d>a>b>c
金属活动性:a>b
金属活动性:b>c
金属活动性:d>c
活动性:d>a
一般来说,负极金属的活动性强于正极金属。根据现象判断出原电池的正、负极,金属的活动性:负极强于正极。
归纳总结
3.设计原电池
利用反应2FeCl3+Cu===2FeCl2+CuCl2,设计一个原电池装置。
(1)在下图方框中画出两种原电池装置图,标明电极材料和电解质溶液。
单液原电池装置图 带盐桥的双液原电池装置图
(说明:正极材料除石墨外,还可以用银、金、铂等)
(2)写出电极反应式。
负极:__________________________________。
正极:__________________________________。
3.设计原电池
利用反应2FeCl3+Cu===2FeCl2+CuCl2,设计一个原电池装置。
Cu-2e-===Cu2+
2Fe3++2e-===2Fe2+
设计原电池的一般思路
首先将氧化还原反应拆分成氧化反应和还原反应两个半反应。
其次确定正、负极选择电极材料,还原剂(一般为比较活泼的金属)为负极,比较不活泼的金属或惰性电极为正极。
最后用导线连接两个电极并插入电解质溶液形成闭合回路,如果两个半反应分别在两个容器中进行,中间应用盐桥连接。
归纳总结
同课章节目录
- 第1章 化学反应与能量转化
- 第1节 化学反应的热效应
- 第2节 化学能转化为电能——电池
- 第3节 电能转化为化学能——电解
- 第4节 金属的腐蚀与防护
- 微项目 设计载人航天器用化学电池与氧气再生方案——化学反应中能量及物质的转化利用
- 第2章 化学反应的方向、 限度与速率
- 第1节 化学反应的方向
- 第2节 化学反应的限度
- 第3节 化学反应的速率
- 第4节 化学反应条件的优化——工业合成氨
- 微项目 探讨如何利用工业废气中的二氧化碳合成甲醇——化学反应选择与反应条件优化
- 第3章 物质在水溶液中的行为
- 第1节 水与水溶液
- 第2节 弱电解质的电离 盐类的水解
- 第3节 沉淀溶解平衡
- 第4节 离子反应
- 微项目 揭秘索尔维制碱法和侯氏制碱法——化学平衡思想的创造性应用
