第3章 有机合成及其应用 合成高分子化合物 检测题(含答案) 2022-2023学年高二化学鲁科版(2019)选择性必修3
文档属性
| 名称 | 第3章 有机合成及其应用 合成高分子化合物 检测题(含答案) 2022-2023学年高二化学鲁科版(2019)选择性必修3 |  | |
| 格式 | docx | ||
| 文件大小 | 937.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-29 09:40:32 | ||
图片预览


文档简介
第三章《有机合成及其应用 合成高分子化合物》检测题
一、单选题(共13题)
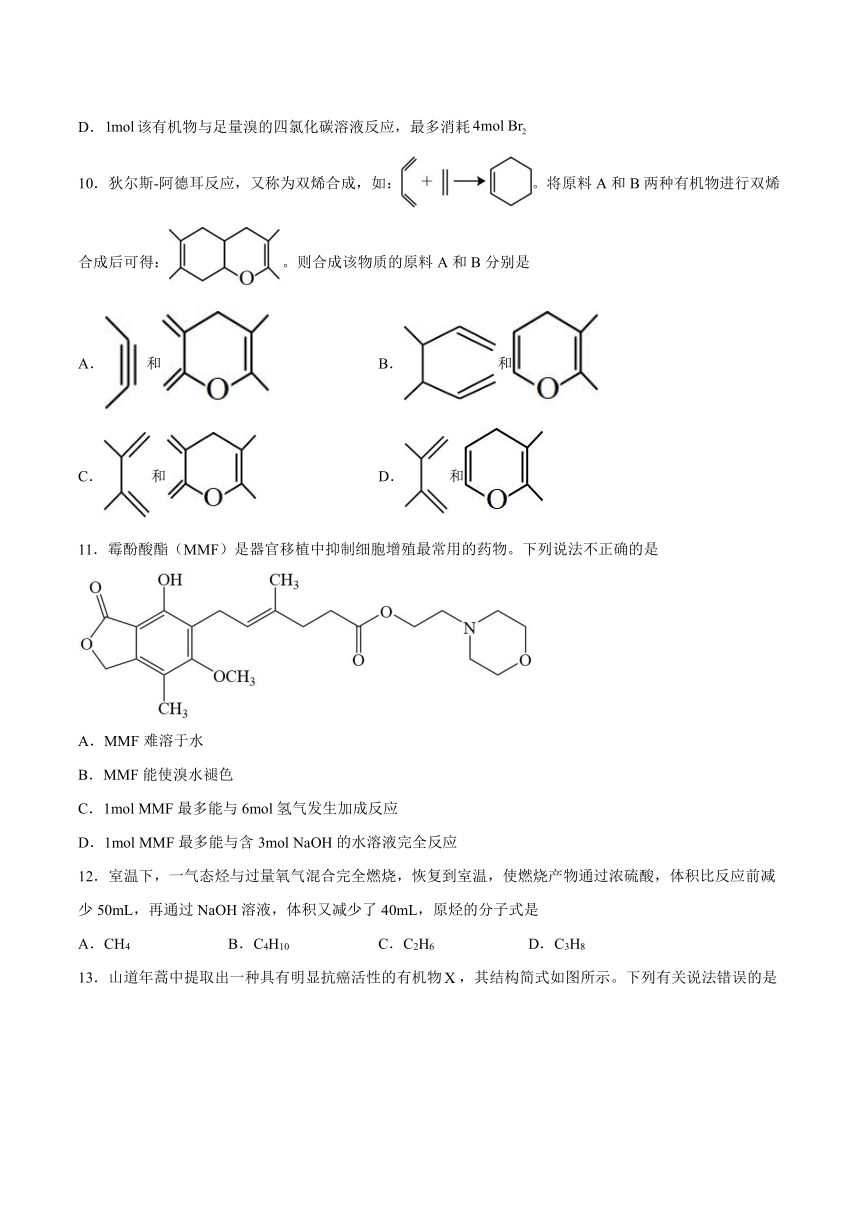
1.用来减轻感冒症状的布洛芬片的结构简式如图,下列有关说法正确的是
A.布洛芬与苯甲酸乙酯互为同系物
B.布洛芬的分子式为C13H16O2
C.布洛芬不能与Na发生反应
D.布洛芬苯环上的一溴代物有2种(不含立体结构)
2.辣椒素是辣椒辣味来源,其结构简式如下。下列有关辣椒素的说法正确的是
A.分子式为C18H26NO3
B.既存在顺反异构又存在对映异构
C.1mol辣椒素与足量的浓溴水反应最多能消耗2molBr2
D.其水解产物均可与Na2CO3溶液反应生成CO2
3.化学与生活密切相关,下列说法正确的是
A.SO2有毒,严禁将其添加到任何食品和饮料中
B.豆浆煮沸的目的是将蛋白质转化为氨基酸便于人体吸收
C.聚酯纤维、有机玻璃、酚醛树脂都属于有机高分子材料
D.电热水器用镁棒防止金属内胆腐蚀,原理是外加电流阴极保护法
4.实验室中用叔丁醇结构简式为,易溶于水与浓盐酸反应制备甲基氯丙烷(密度小于水)的流程如图,下列说法正确的是
A.洗涤时前后两次加水除去的物质相同
B.碳酸氢钠溶液换成氢氧化钠溶液洗涤效果更好
C.叔丁醇既可发生消去反应,也可发生氧化反应生成醛
D.甲基氯丙烷在核磁共振氢谱中仅显示1组吸收峰
5.科学技术在物质结构的研究中具有非常重要的作用。下列说法错误的是
A.质谱仪可以测定分子的相对分子质量
B.可通过红外光谱分析测得共价键的键长和键角
C.可通过红外光谱分析物质中含有何种化学键
D.可通过X射线衍射实验区分晶体和非晶体
6.习近平总书记说:“垃圾分类工作就是新时尚”。垃圾是放错了位置的资源,应分类回收利用。生活中废弃的塑料制品、旧轮胎、废纸属于
A.单质 B.无机物 C.氧化物 D.有机物
7.九月正是开学季,今年却因新冠肺炎疫情突发,给吉安市社会经济发展和生产生活带来了重大影响。化学在新冠肺炎疫情防控中发挥着重要的作用,下列说法正确的是
A.医用消毒酒精中乙醇的体积分数为95%
B.医用酒精和84消毒液均可杀灭新型冠状病毒,二者消毒原理不同
C.酒精与84消毒液混合,可增强消毒效果
D.医用外科口罩和防护服所用的熔喷布是一种聚丙烯材料,属于纯净物
8.下列说法正确的是
A.石油裂解是为了提高汽油等轻质油的产量和质量
B.腈纶、涤纶和氯纶属于再生纤维
C.煤的干馏是将煤隔绝空气加强热使之分解的过程
D.聚氯乙烯塑料袋可用于包装食品
9.盆栽鲜花施用诱抗素剂(结构如图)以保持鲜花盛开,说法不正确的是
A.该有机物分子式为
B.该有机物能与溶液反应放出
C.该有机物与足量钠反应产生氢气
D.该有机物与足量溴的四氯化碳溶液反应,最多消耗
10.狄尔斯-阿德耳反应,又称为双烯合成,如:。将原料A和B两种有机物进行双烯合成后可得:。则合成该物质的原料A和B分别是
A. 和 B.和
C.和 D.和
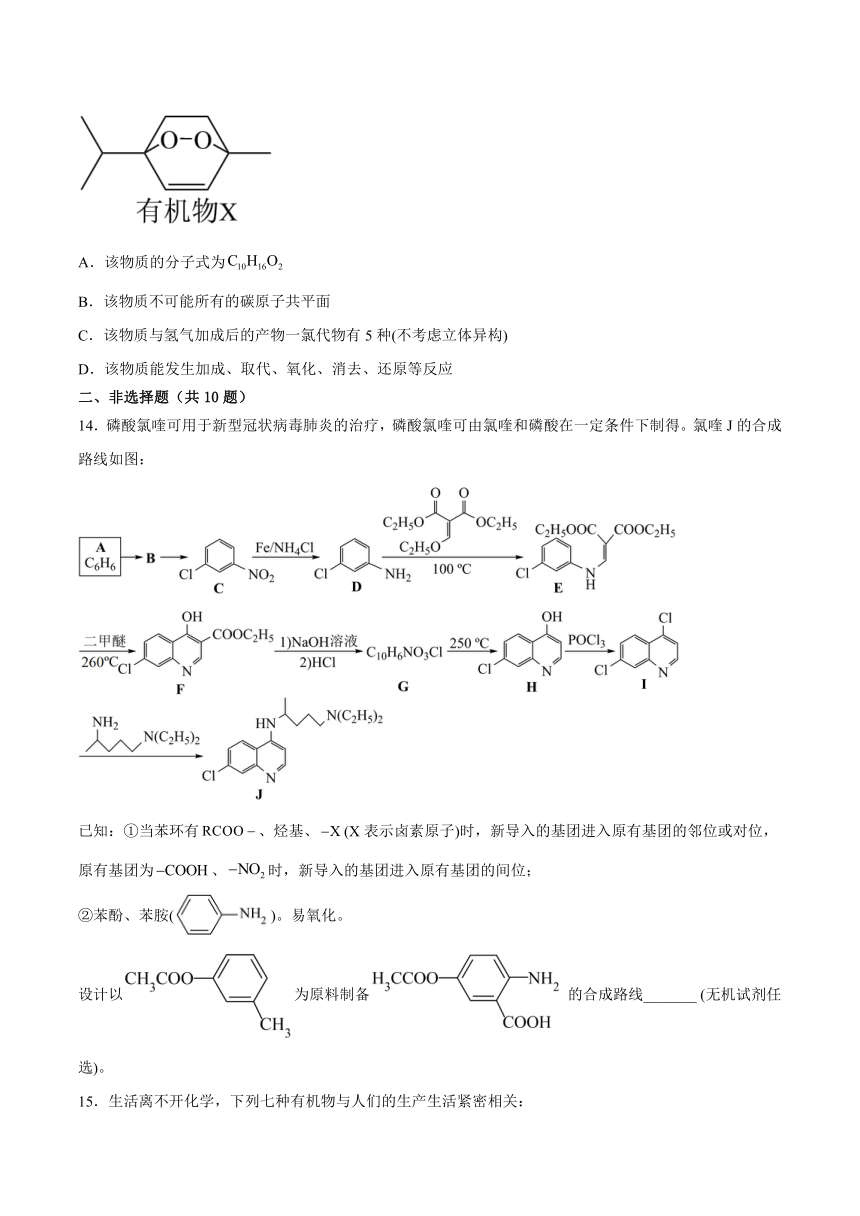
11.霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物。下列说法不正确的是
A.MMF难溶于水
B.MMF能使溴水褪色
C.1mol MMF最多能与6mol氢气发生加成反应
D.1mol MMF最多能与含3mol NaOH的水溶液完全反应
12.室温下,一气态烃与过量氧气混合完全燃烧,恢复到室温,使燃烧产物通过浓硫酸,体积比反应前减少50mL,再通过NaOH溶液,体积又减少了40mL,原烃的分子式是
A.CH4 B.C4H10 C.C2H6 D.C3H8
13.山道年蒿中提取出一种具有明显抗癌活性的有机物,其结构简式如图所示。下列有关说法错误的是
A.该物质的分子式为
B.该物质不可能所有的碳原子共平面
C.该物质与氢气加成后的产物一氯代物有5种(不考虑立体异构)
D.该物质能发生加成、取代、氧化、消去、还原等反应
二、非选择题(共10题)
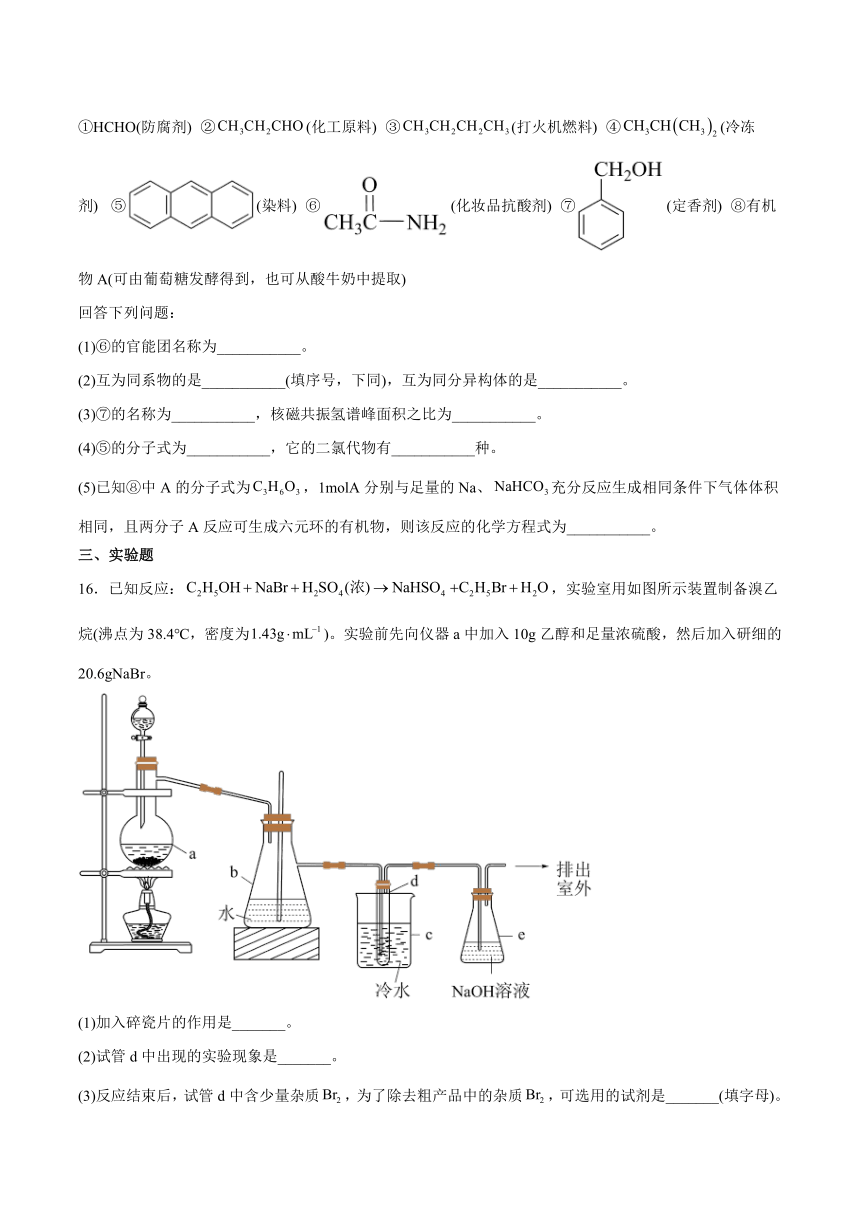
14.磷酸氯喹可用于新型冠状病毒肺炎的治疗,磷酸氯喹可由氯喹和磷酸在一定条件下制得。氯喹J的合成路线如图:
已知:①当苯环有、烃基、(X表示卤素原子)时,新导入的基团进入原有基团的邻位或对位,原有基团为、时,新导入的基团进入原有基团的间位;
②苯酚、苯胺()。易氧化。
设计以为原料制备的合成路线_______ (无机试剂任选)。
15.生活离不开化学,下列七种有机物与人们的生产生活紧密相关:
①HCHO(防腐剂) ②(化工原料) ③(打火机燃料) ④(冷冻剂) ⑤(染料) ⑥(化妆品抗酸剂) ⑦(定香剂) ⑧有机物A(可由葡萄糖发酵得到,也可从酸牛奶中提取)
回答下列问题:
(1)⑥的官能团名称为___________。
(2)互为同系物的是___________(填序号,下同),互为同分异构体的是___________。
(3)⑦的名称为___________,核磁共振氢谱峰面积之比为___________。
(4)⑤的分子式为___________,它的二氯代物有___________种。
(5)已知⑧中A的分子式为,1molA分别与足量的Na、充分反应生成相同条件下气体体积相同,且两分子A反应可生成六元环的有机物,则该反应的化学方程式为___________。
三、实验题
16.已知反应:,实验室用如图所示装置制备溴乙烷(沸点为38.4℃,密度为)。实验前先向仪器a中加入10g乙醇和足量浓硫酸,然后加入研细的20.6gNaBr。
(1)加入碎瓷片的作用是_______。
(2)试管d中出现的实验现象是_______。
(3)反应结束后,试管d中含少量杂质,为了除去粗产品中的杂质,可选用的试剂是_______(填字母)。
A.苯 B. C.溶液 D.
(4)经过分离、提纯、干燥后,该实验最终得到10.9g溴乙烷,则本实验中溴乙烷的产率为_______。
(5)通过以下实验步骤可检验溴乙烷中的溴元素,其正确的操作顺序是_______(填序号)。
①加热 ②加入溶液 ③加入稀酸化 ④加入溶液 ⑤冷却 ⑥取少量溴乙烷
17.有机物M是一种无色透明的液体,具有香味。某化学兴趣小组从粗品中分离提纯有机物M,然后借助李比希法、现代科学仪器测定有机物M的分子组成和结构,具体实验过程如下:
步骤一:用李比希法确定M的实验式:这种方法是在电炉加热下用纯氧氧化管内样品,根据产物的质量确定有机物M的组成。
(1)装置的连接顺序(从左到右)是_______(填序号,装置不能重复使用)。
(2)C装置的作用是_______
(3)E装置中反应的化学方程式为_______
(4)F装置(燃烧管)中CuO的作用是_______
若实验中所取纯样品M只含C、H、O三种元素中的两种或三种,准确称取3.70gM,经充分反应后,A管质量增加6.60g,B管质量增加2.70g。
(5)该样品M的实验式为______
步骤二:质谱法确定分子式:
(6)如图是该有机物M的质谱图,则其相对分子质量为_____,分子式为_____。
步骤三:确定M的结构简式。
(7)M的核磁共振氢谱有2个峰且面积之比为1:1,利用红外光谱仪测得M的红外光谱如图所示。
M中官能团的名称为_______,M的结构简式为_______。
四、计算题
18.某有机物,它的相对分子质量为60。 6.0g该有机物完全燃烧后的产物通过浓硫酸后增重7.2g,通过足量澄清石灰水后有30g白色沉淀生成。求:
(1)该有机物的分子式;
(2)写出能与钠反应的该有机物的所有同分异构体的结构简式。
19.某同学为测定维生素C中碳、氢的质量分数,取维生素C样品研碎,称取该试样0.352g,置于铂舟并放入燃烧管中,不断通入氧气流.用酒精喷灯持续加热样品,将生成物先后通过浓硫酸和碱石灰,两者分别增重0.144g和0.528g,生成物完全被吸收.试回答以下问题:
(1)维生素C中碳的质量分数是______,氢的质量分数______
(2)维生素中是否含有氧元素?为什么?(试通过计算说明)______________
20.0.2mol某有机物和0.4molO2在密闭容器中燃烧后,产物通过浓H2SO4后,浓H2SO4增重10.8g;通过灼热的CuO充分反应后,CuO失重3.2g;再将气体通入足量澄清石灰水,得到沉淀40g,无气体剩余。若已知等量该有机物与9.2gNa恰好完全反应,请回答:
(1)该有机物的结构简式是_______。
(2)写出该有机物的一种主要用途:_______。
21.(1)互为同分异构体的四种有机物A、B、C、D,相对分子质量为74,完全燃烧只生成CO2和H2O,经分析其含氧元素的质量分数为43.3%,则这些有机物的分子式为__________,
(2)已知A、B、C、D分子结构中均含甲基,把它们分别进行下列实验以鉴别之,其实验记录如下:
NaOH溶液 银氨溶液 新制Cu(OH)2 金属钠
A 中和反应 —— 溶解 产生氢气
B —— 有银镜 加热后有红色沉淀 产生氢气
C 水解反应 有银镜 加热后有红色沉淀 ——
D 水解反应 —— —— ——
①写出由稀氨水和硝酸银稀溶液制备银氨溶液的化学方程式__________________________
②写出B与新制Cu(OH)2悬浊液反应的化学方程式_____________________________________
③B在浓硫酸存在的条件下能反应生成E,写出以E作原料在一定条件下制备高分子化合物的化学方程式__。
22.辣椒素又名辣椒碱(capsaicin),是常见的生物碱之一、辣椒素H的合成路线如下。
请完成下列问题
(1)B的键线式是_______。
(2)E中官能团的名称是_______。
(3)C→D中反应i的化学方程式是_______,反应类型是_______。
(4)F与G反应生成H时,另一产物为_______(填化学式)。
(5)的同分异构体中,同时符合下列条件的有_______种(不含立体异构)。
①具有四取代苯结构,且核磁共振氢谱显示,其苯环上只有一种化学环境的H
②红外光谱测得其分子结构中含有和-OH
③进一步测得,该物质能与NaOH反应,且1mol该物质能消耗2molNaOH写出其中任意两种的结构简式_______。
(6)参照上述合成路线,设计以异丙醇和必要试剂为原料合成2-异丙基丙二酸()的合成路线。_______(其他试剂任选)。
23.从煤和石油中可以提炼出化工原料A和B,A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平;B是一种比水轻的油状液态烃,0.1mol该烃在足量的氧气中完全燃烧,生成0.6molCO2和0.3mol水。回答下列问题:
(1)A 的电子式为_____,B 的结构简式为______。
(2)与A 相邻的同系物C使溴的四氯化碳溶液褪色的化学反应方程式:____,反应类型:____。
(3)在碘水中加入B物质,充分振荡、静置后的现象:_________。
(4)B与浓硫酸和浓硝酸在55~60℃条件下反应的化学方程式:_______,反应类型:______。
(5)等质量的A、B完全燃烧时消耗O2的物质的量:_______(填“A>B”“A参考答案:
1.D 2.C 3.C 4.D 5.B 6.D 7.B 8.C 9.D 10.D 11.C 12.C 13.D
14.
15.(1)酰胺基
(2) ①② ③④
(3) 苯甲醇
(4) 15
(5)2+H2O
16.(1)防止液体暴沸
(2)液体分层,下层为油状液体
(3)C
(4)50%
(5)⑥④①⑤③②
17.(1)E→D→F→B→A→C
(2)防止空气中的CO2和水蒸气进入A中影响CO2的测定质量
(3)2H2O22H2O+O2↑
(4)使有机物被充分氧化生成CO2和水
(5)C3H6O2
(6) 74 C3H6O2
(7) 酯基 CH3COOCH3
18.(1)C3H8O
(2)CH3CH2CH2OH与
19. 40.9% 4.5% 含有维生素中一定含有氧元素,因为C、H元素的质量之和小于维生素的质量.
20.(1)CH2OHCH2OH
(2)汽车发动机的抗冻剂、生产聚酯纤维、合成涤纶等
21. C3H6O2 AgNO3+3NH3·H2O=Ag(NH3)2OH+NH4NO3+2H2O CH3CH(OH)CHO+2Cu(OH)2+NaOHCH3CH(OH)COONa+Cu2O↓+3H2O nCH2=CHCOOH
22. (2-甲基-7-溴-3-庚烯) 碳碳双键、羧基 +2KOH+2C2H5OH 取代(水解)反应 HCl 4 、、、
23. CH2=CHCH3+Br2→CH2BrCHBrCH3 加成反应 溶液分层,下层无色,上层呈紫红色 +HO-NO2(浓)+H2O 取代反应 A>B
一、单选题(共13题)
1.用来减轻感冒症状的布洛芬片的结构简式如图,下列有关说法正确的是
A.布洛芬与苯甲酸乙酯互为同系物
B.布洛芬的分子式为C13H16O2
C.布洛芬不能与Na发生反应
D.布洛芬苯环上的一溴代物有2种(不含立体结构)
2.辣椒素是辣椒辣味来源,其结构简式如下。下列有关辣椒素的说法正确的是
A.分子式为C18H26NO3
B.既存在顺反异构又存在对映异构
C.1mol辣椒素与足量的浓溴水反应最多能消耗2molBr2
D.其水解产物均可与Na2CO3溶液反应生成CO2
3.化学与生活密切相关,下列说法正确的是
A.SO2有毒,严禁将其添加到任何食品和饮料中
B.豆浆煮沸的目的是将蛋白质转化为氨基酸便于人体吸收
C.聚酯纤维、有机玻璃、酚醛树脂都属于有机高分子材料
D.电热水器用镁棒防止金属内胆腐蚀,原理是外加电流阴极保护法
4.实验室中用叔丁醇结构简式为,易溶于水与浓盐酸反应制备甲基氯丙烷(密度小于水)的流程如图,下列说法正确的是
A.洗涤时前后两次加水除去的物质相同
B.碳酸氢钠溶液换成氢氧化钠溶液洗涤效果更好
C.叔丁醇既可发生消去反应,也可发生氧化反应生成醛
D.甲基氯丙烷在核磁共振氢谱中仅显示1组吸收峰
5.科学技术在物质结构的研究中具有非常重要的作用。下列说法错误的是
A.质谱仪可以测定分子的相对分子质量
B.可通过红外光谱分析测得共价键的键长和键角
C.可通过红外光谱分析物质中含有何种化学键
D.可通过X射线衍射实验区分晶体和非晶体
6.习近平总书记说:“垃圾分类工作就是新时尚”。垃圾是放错了位置的资源,应分类回收利用。生活中废弃的塑料制品、旧轮胎、废纸属于
A.单质 B.无机物 C.氧化物 D.有机物
7.九月正是开学季,今年却因新冠肺炎疫情突发,给吉安市社会经济发展和生产生活带来了重大影响。化学在新冠肺炎疫情防控中发挥着重要的作用,下列说法正确的是
A.医用消毒酒精中乙醇的体积分数为95%
B.医用酒精和84消毒液均可杀灭新型冠状病毒,二者消毒原理不同
C.酒精与84消毒液混合,可增强消毒效果
D.医用外科口罩和防护服所用的熔喷布是一种聚丙烯材料,属于纯净物
8.下列说法正确的是
A.石油裂解是为了提高汽油等轻质油的产量和质量
B.腈纶、涤纶和氯纶属于再生纤维
C.煤的干馏是将煤隔绝空气加强热使之分解的过程
D.聚氯乙烯塑料袋可用于包装食品
9.盆栽鲜花施用诱抗素剂(结构如图)以保持鲜花盛开,说法不正确的是
A.该有机物分子式为
B.该有机物能与溶液反应放出
C.该有机物与足量钠反应产生氢气
D.该有机物与足量溴的四氯化碳溶液反应,最多消耗
10.狄尔斯-阿德耳反应,又称为双烯合成,如:。将原料A和B两种有机物进行双烯合成后可得:。则合成该物质的原料A和B分别是
A. 和 B.和
C.和 D.和
11.霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物。下列说法不正确的是
A.MMF难溶于水
B.MMF能使溴水褪色
C.1mol MMF最多能与6mol氢气发生加成反应
D.1mol MMF最多能与含3mol NaOH的水溶液完全反应
12.室温下,一气态烃与过量氧气混合完全燃烧,恢复到室温,使燃烧产物通过浓硫酸,体积比反应前减少50mL,再通过NaOH溶液,体积又减少了40mL,原烃的分子式是
A.CH4 B.C4H10 C.C2H6 D.C3H8
13.山道年蒿中提取出一种具有明显抗癌活性的有机物,其结构简式如图所示。下列有关说法错误的是
A.该物质的分子式为
B.该物质不可能所有的碳原子共平面
C.该物质与氢气加成后的产物一氯代物有5种(不考虑立体异构)
D.该物质能发生加成、取代、氧化、消去、还原等反应
二、非选择题(共10题)
14.磷酸氯喹可用于新型冠状病毒肺炎的治疗,磷酸氯喹可由氯喹和磷酸在一定条件下制得。氯喹J的合成路线如图:
已知:①当苯环有、烃基、(X表示卤素原子)时,新导入的基团进入原有基团的邻位或对位,原有基团为、时,新导入的基团进入原有基团的间位;
②苯酚、苯胺()。易氧化。
设计以为原料制备的合成路线_______ (无机试剂任选)。
15.生活离不开化学,下列七种有机物与人们的生产生活紧密相关:
①HCHO(防腐剂) ②(化工原料) ③(打火机燃料) ④(冷冻剂) ⑤(染料) ⑥(化妆品抗酸剂) ⑦(定香剂) ⑧有机物A(可由葡萄糖发酵得到,也可从酸牛奶中提取)
回答下列问题:
(1)⑥的官能团名称为___________。
(2)互为同系物的是___________(填序号,下同),互为同分异构体的是___________。
(3)⑦的名称为___________,核磁共振氢谱峰面积之比为___________。
(4)⑤的分子式为___________,它的二氯代物有___________种。
(5)已知⑧中A的分子式为,1molA分别与足量的Na、充分反应生成相同条件下气体体积相同,且两分子A反应可生成六元环的有机物,则该反应的化学方程式为___________。
三、实验题
16.已知反应:,实验室用如图所示装置制备溴乙烷(沸点为38.4℃,密度为)。实验前先向仪器a中加入10g乙醇和足量浓硫酸,然后加入研细的20.6gNaBr。
(1)加入碎瓷片的作用是_______。
(2)试管d中出现的实验现象是_______。
(3)反应结束后,试管d中含少量杂质,为了除去粗产品中的杂质,可选用的试剂是_______(填字母)。
A.苯 B. C.溶液 D.
(4)经过分离、提纯、干燥后,该实验最终得到10.9g溴乙烷,则本实验中溴乙烷的产率为_______。
(5)通过以下实验步骤可检验溴乙烷中的溴元素,其正确的操作顺序是_______(填序号)。
①加热 ②加入溶液 ③加入稀酸化 ④加入溶液 ⑤冷却 ⑥取少量溴乙烷
17.有机物M是一种无色透明的液体,具有香味。某化学兴趣小组从粗品中分离提纯有机物M,然后借助李比希法、现代科学仪器测定有机物M的分子组成和结构,具体实验过程如下:
步骤一:用李比希法确定M的实验式:这种方法是在电炉加热下用纯氧氧化管内样品,根据产物的质量确定有机物M的组成。
(1)装置的连接顺序(从左到右)是_______(填序号,装置不能重复使用)。
(2)C装置的作用是_______
(3)E装置中反应的化学方程式为_______
(4)F装置(燃烧管)中CuO的作用是_______
若实验中所取纯样品M只含C、H、O三种元素中的两种或三种,准确称取3.70gM,经充分反应后,A管质量增加6.60g,B管质量增加2.70g。
(5)该样品M的实验式为______
步骤二:质谱法确定分子式:
(6)如图是该有机物M的质谱图,则其相对分子质量为_____,分子式为_____。
步骤三:确定M的结构简式。
(7)M的核磁共振氢谱有2个峰且面积之比为1:1,利用红外光谱仪测得M的红外光谱如图所示。
M中官能团的名称为_______,M的结构简式为_______。
四、计算题
18.某有机物,它的相对分子质量为60。 6.0g该有机物完全燃烧后的产物通过浓硫酸后增重7.2g,通过足量澄清石灰水后有30g白色沉淀生成。求:
(1)该有机物的分子式;
(2)写出能与钠反应的该有机物的所有同分异构体的结构简式。
19.某同学为测定维生素C中碳、氢的质量分数,取维生素C样品研碎,称取该试样0.352g,置于铂舟并放入燃烧管中,不断通入氧气流.用酒精喷灯持续加热样品,将生成物先后通过浓硫酸和碱石灰,两者分别增重0.144g和0.528g,生成物完全被吸收.试回答以下问题:
(1)维生素C中碳的质量分数是______,氢的质量分数______
(2)维生素中是否含有氧元素?为什么?(试通过计算说明)______________
20.0.2mol某有机物和0.4molO2在密闭容器中燃烧后,产物通过浓H2SO4后,浓H2SO4增重10.8g;通过灼热的CuO充分反应后,CuO失重3.2g;再将气体通入足量澄清石灰水,得到沉淀40g,无气体剩余。若已知等量该有机物与9.2gNa恰好完全反应,请回答:
(1)该有机物的结构简式是_______。
(2)写出该有机物的一种主要用途:_______。
21.(1)互为同分异构体的四种有机物A、B、C、D,相对分子质量为74,完全燃烧只生成CO2和H2O,经分析其含氧元素的质量分数为43.3%,则这些有机物的分子式为__________,
(2)已知A、B、C、D分子结构中均含甲基,把它们分别进行下列实验以鉴别之,其实验记录如下:
NaOH溶液 银氨溶液 新制Cu(OH)2 金属钠
A 中和反应 —— 溶解 产生氢气
B —— 有银镜 加热后有红色沉淀 产生氢气
C 水解反应 有银镜 加热后有红色沉淀 ——
D 水解反应 —— —— ——
①写出由稀氨水和硝酸银稀溶液制备银氨溶液的化学方程式__________________________
②写出B与新制Cu(OH)2悬浊液反应的化学方程式_____________________________________
③B在浓硫酸存在的条件下能反应生成E,写出以E作原料在一定条件下制备高分子化合物的化学方程式__。
22.辣椒素又名辣椒碱(capsaicin),是常见的生物碱之一、辣椒素H的合成路线如下。
请完成下列问题
(1)B的键线式是_______。
(2)E中官能团的名称是_______。
(3)C→D中反应i的化学方程式是_______,反应类型是_______。
(4)F与G反应生成H时,另一产物为_______(填化学式)。
(5)的同分异构体中,同时符合下列条件的有_______种(不含立体异构)。
①具有四取代苯结构,且核磁共振氢谱显示,其苯环上只有一种化学环境的H
②红外光谱测得其分子结构中含有和-OH
③进一步测得,该物质能与NaOH反应,且1mol该物质能消耗2molNaOH写出其中任意两种的结构简式_______。
(6)参照上述合成路线,设计以异丙醇和必要试剂为原料合成2-异丙基丙二酸()的合成路线。_______(其他试剂任选)。
23.从煤和石油中可以提炼出化工原料A和B,A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平;B是一种比水轻的油状液态烃,0.1mol该烃在足量的氧气中完全燃烧,生成0.6molCO2和0.3mol水。回答下列问题:
(1)A 的电子式为_____,B 的结构简式为______。
(2)与A 相邻的同系物C使溴的四氯化碳溶液褪色的化学反应方程式:____,反应类型:____。
(3)在碘水中加入B物质,充分振荡、静置后的现象:_________。
(4)B与浓硫酸和浓硝酸在55~60℃条件下反应的化学方程式:_______,反应类型:______。
(5)等质量的A、B完全燃烧时消耗O2的物质的量:_______(填“A>B”“A
1.D 2.C 3.C 4.D 5.B 6.D 7.B 8.C 9.D 10.D 11.C 12.C 13.D
14.
15.(1)酰胺基
(2) ①② ③④
(3) 苯甲醇
(4) 15
(5)2+H2O
16.(1)防止液体暴沸
(2)液体分层,下层为油状液体
(3)C
(4)50%
(5)⑥④①⑤③②
17.(1)E→D→F→B→A→C
(2)防止空气中的CO2和水蒸气进入A中影响CO2的测定质量
(3)2H2O22H2O+O2↑
(4)使有机物被充分氧化生成CO2和水
(5)C3H6O2
(6) 74 C3H6O2
(7) 酯基 CH3COOCH3
18.(1)C3H8O
(2)CH3CH2CH2OH与
19. 40.9% 4.5% 含有维生素中一定含有氧元素,因为C、H元素的质量之和小于维生素的质量.
20.(1)CH2OHCH2OH
(2)汽车发动机的抗冻剂、生产聚酯纤维、合成涤纶等
21. C3H6O2 AgNO3+3NH3·H2O=Ag(NH3)2OH+NH4NO3+2H2O CH3CH(OH)CHO+2Cu(OH)2+NaOHCH3CH(OH)COONa+Cu2O↓+3H2O nCH2=CHCOOH
22. (2-甲基-7-溴-3-庚烯) 碳碳双键、羧基 +2KOH+2C2H5OH 取代(水解)反应 HCl 4 、、、
23. CH2=CHCH3+Br2→CH2BrCHBrCH3 加成反应 溶液分层,下层无色,上层呈紫红色 +HO-NO2(浓)+H2O 取代反应 A>B
