专题4生活中常用的有机物-烃的含氧衍生物(含解析)随堂测试2022-2023学年下学期高二化学苏教版(2019)选择性必修3
文档属性
| 名称 | 专题4生活中常用的有机物-烃的含氧衍生物(含解析)随堂测试2022-2023学年下学期高二化学苏教版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 331.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-29 00:00:00 | ||
图片预览




文档简介
专题4生活中常用的有机物-烃的含氧衍生物 随堂测试
一、单选题
1.下列说法不正确的是
A.向磷酸二氢钠溶液中加入过量澄清石灰水:
B.用重铬酸钾法测定白酒中乙醇的含量:
C.用碳酸钠溶液处理锅炉水垢中的硫酸钙:
D.制摩尔盐时用酒精洗涤产品,制阿司匹林时用冷水洗涤产品
2.有机化合物分子中的邻近基团间往往会有一定的相互影响,这种影响会使有机化合物表现出一些特性。下列事实不能证明这一说法的是
A.苯乙烯能与溴水反应,而苯不能与溴水反应
B.苯酚能与NaOH溶液反应,而乙醇不能与NaOH溶液反应
C.苯与硝酸反应生成硝基苯,而甲苯与硝酸反应生成三硝基甲苯
D.甲苯能使酸性高锰酸钾溶液褪色,而乙烷不能使酸性高锰酸钾溶液褪色
3.新冠肺炎病毒疫情爆发以来,我国科学家、医务工作者一直奋战在第一线,攻坚克难,成功研制出多种抑制新冠病毒药物,应用于临床,为战胜疫情立下赫赫战功。我们从化学的角度分析药物的结构,探究其性质,以此向战疫英雄致敬。2020年2月4日,中国工程院院士李兰娟团队发布最新研究成果:盐酸阿比多尔在体外细胞实验中能有效抑制冠状病毒。盐酸阿比多尔的结构简式如图所示,下列有关该有机物的说法不正确的是
A.该有机物能与FeCl3溶液发生显色反应
B.能够使酸性高锰酸钾溶液褪色
C.能与NaOH溶液发生水解反应
D.1mol该有机物最多与8molH2发生加成反应
4.乙醇和乙酸是两种常见的有机化合物,下列说法正确的是
A.乙醇和乙酸的分子结构中均含有碳氧双键
B.乙醇和乙酸均能与金属钠反应
C.乙醇能发生氧化反应,而乙酸不能发生氧化反应
D.乙醇和乙酸均能使紫色石蕊试液变红
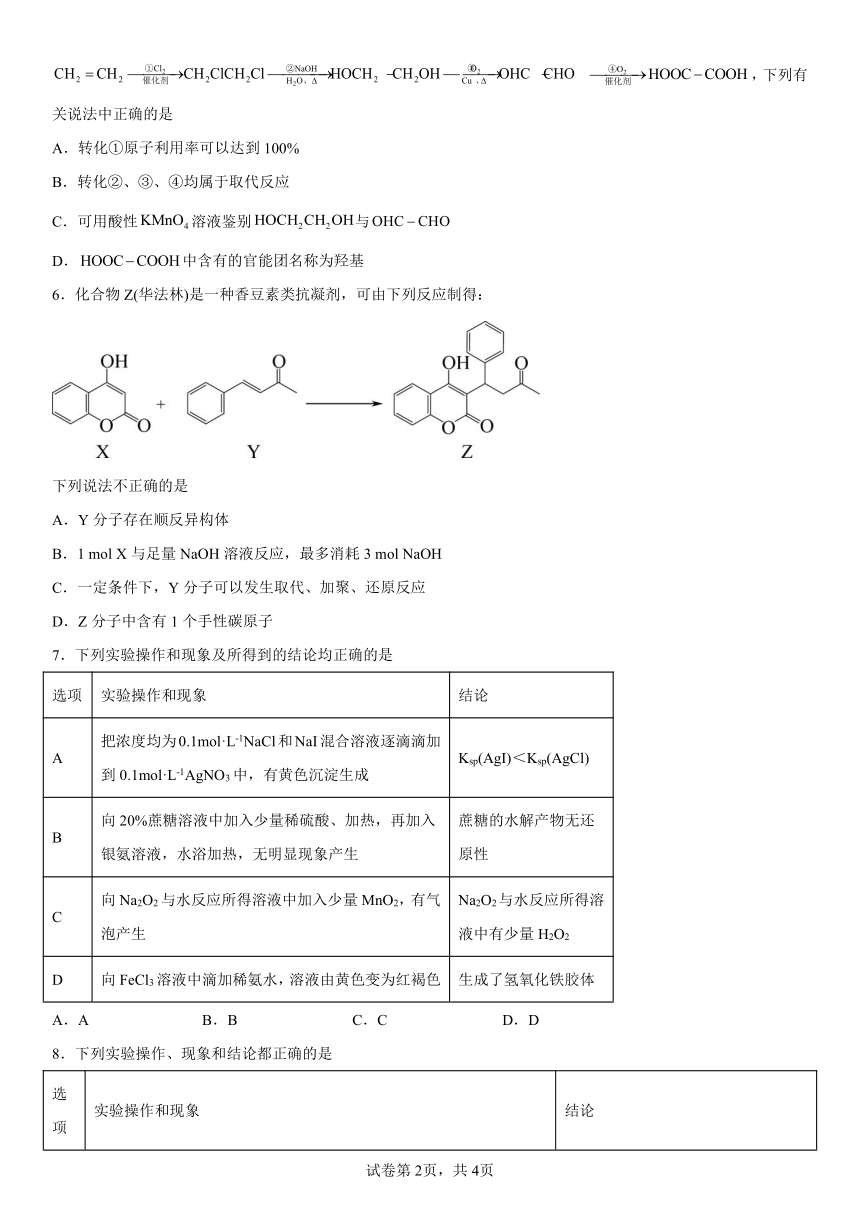
5.以乙烯为原料制备草酸的流程如下:
,下列有关说法中正确的是
A.转化①原子利用率可以达到100%
B.转化②、③、④均属于取代反应
C.可用酸性溶液鉴别与
D.中含有的官能团名称为羟基
6.化合物Z(华法林)是一种香豆素类抗凝剂,可由下列反应制得:
下列说法不正确的是
A.Y分子存在顺反异构体
B.1 mol X与足量NaOH溶液反应,最多消耗3 mol NaOH
C.一定条件下,Y分子可以发生取代、加聚、还原反应
D.Z分子中含有1个手性碳原子
7.下列实验操作和现象及所得到的结论均正确的是
选项 实验操作和现象 结论
A 把浓度均为0.1mol·L-1NaCl和NaI混合溶液逐滴滴加到0.1mol·L-1AgNO3中,有黄色沉淀生成 Ksp(AgI)<Ksp(AgCl)
B 向20%蔗糖溶液中加入少量稀硫酸、加热,再加入银氨溶液,水浴加热,无明显现象产生 蔗糖的水解产物无还原性
C 向Na2O2与水反应所得溶液中加入少量MnO2,有气泡产生 Na2O2与水反应所得溶液中有少量H2O2
D 向FeCl3溶液中滴加稀氨水,溶液由黄色变为红褐色 生成了氢氧化铁胶体
A.A B.B C.C D.D
8.下列实验操作、现象和结论都正确的是
选项 实验操作和现象 结论
A 向苯酚浊液中滴加溶液,浊液变澄清 苯酚的酸性强于的酸性
B 向溶液中通入气体,出现白色沉淀 白色沉淀为硫酸钡
C 向2 mL 10%的溶液中滴入5~6滴2%的NaOH溶液,再滴入葡萄糖溶液并加热,产生砖红色沉淀 葡萄糖含有醛基
D 相同温度下,用pH试纸测溶液试纸显蓝色;测溶液的试纸显深蓝色 相同温度下
A.A B.B C.C D.D
9.下列“类比”结果正确的是
A.Cl2、Br2、I2的沸点逐渐升高,则H2、N2、O2的沸点也逐渐升高
B.CH3CHO与H2可发生加成反应,则相同条件下CH3COOH也可以与H2发生加成反应
C.向Na2CO3中加入少量水,伴随放热现象,则向NaHCO3中加入少量水,也伴随放热现象
D.乙醇与足量酸性高锰酸钾溶液反应生成乙酸,则乙二醇与足量酸性高锰酸钾溶液反应生成乙二酸
10. 下列物质中,既可被氧化又可被氢气还原的是
A.乙烷 B.乙醛 C.乙酸 D.乙醇
11.人类利用人工合成信息素诱捕害虫、测报虫情等。一种集结信息素的分子结构简式如图所示,关于该有机物的说法不正确的是
A.该有机物分子含有三种官能团 B.该有机物能发生加成和氧化反应
C.该有机物水解产物之一能氧化成醛 D.该有机物具有一定的挥发性
二、填空题
12.羟甲香豆素是一种治疗胆结石的药物,其结构简式如图所示:
(1)该物质的分子式是___________________。
(2)该物质分子中含有的官能团有羟基、碳碳双键和___________________。
(3)1mol 该物质与足量 NaOH 溶液反应,最多消耗 NaOH___________ mol。
13.乙酸是一种弱酸,请回答以下问题:
(1)乙酸在水中的电离方程式为_______。
(2)向乙酸溶液中加入石蕊试液,产生的现象是_______;将乙酸溶液滴加到碳酸钠溶液中,产生的现象是_______,反应的方程式为_______。
(3)根据以上事实,说明乙酸的酸性比碳酸的酸性_______(填“强”或“弱”)。
14.丙烯酸(CH2=CH-COOH)是重要的有机合成原料及合成树脂单体,是最简单的不饱和羧酸。
(1)丙烯酸属于___________(填“无机化合物”或“有机化合物”)。
(2)丙烯酸中含有的官能团有___________和___________(填名称)。
(3)向丙烯酸溶液中滴入2~3滴紫色石蕊试液,溶液颜色变红,说明丙烯酸溶液具有___________性。
(4)丙烯酸和乙醇发生___________(填反应类型)生成丙烯酸乙酯和水。
(5)向丙烯酸溶液中滴入几滴溴水,实验现象为___________。
15.叶酸是维生素B族之一,可以由下列甲、乙、丙三种物质合成。
(1)甲中含氧官能团是__________(填名称)。
(2)下列关于乙的说法正确的是________(填序号)。
a.分子中碳原子与氮原子的个数比是7∶5 b.属于芳香族化合物
c.既能与盐酸又能与氢氧化钠溶液反应 d.属于苯酚的同系物
(3)丁是丙的同分异构体,且满足下列两个条件,丁的结构简式为________。
a.含有
b.在稀硫酸中水解有乙酸生成
(4)写出丁在氢氧化钠溶液中水解的化学方程式。________
16.柠檬酸()在浓硫酸、加热条件下可发生消去反应,且消去产物只有一种。(__)
17.1 mol染料木黄酮()与足量溴水反应,最多可消耗_______mol Br2;与足量NaOH溶液反应,最多可消耗_______mol NaOH。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
【详解】A.磷酸二氢钠化学式为NaH2PO4,在溶液中电离产生Na+和,首先发生反应+2OH-=+2H2O,生成的继续发生反应:3Ca2++2=Ca3(PO4)2↓,由于NaH2PO4少量,故、完全反应,两步叠加消去得总离子方程式为:2+4OH-+3Ca2+= Ca3(PO4)2↓+4H2O,A错误;
B.K2Cr2O7具有强氧化性,可将CH3CH2OH氧化为CH3COOH,K2Cr2O7在酸性条件下能稳定存在,若在碱性条件下,则会转化为K2CrO4,故此时溶液为酸性溶液,结合得失电子守恒、电荷守恒(可添加H+)、元素守恒(可添加H2O),配平得离子方程式为:2+3C2H5OH+16H+=4Cr3++3CH3COOH+11H2O,B正确;
C.Na2CO3溶液处理CaSO4利用了沉淀转化的原理,微溶的CaSO4可转化为难溶的CaCO3,对应离子方程式为:CaSO4(s)+(aq)=CaCO3(s)+(aq),C正确;
D.摩尔盐在有机溶剂中溶解度小,因此制备摩尔盐可用酒精洗涤,阿司匹林的溶解度随温度的升高而增大,因此洗涤阿司匹林时可采用冷水或冰水洗涤,D正确;
故答案选A。
2.A
【详解】A.苯乙烯含有碳碳双键,可以与溴发生加成反应,与官能团性质有关,不是邻近基团造成的影响,故A选;
B.苯酚、乙醇都含有羟基,苯酚能与NaOH溶液反应,可知苯环影响了羟基,故B不选;
C.甲基影响苯环,使苯环上H活泼,则甲苯易发生三取代,故C不选;
D.苯环、乙烷中均有甲基,而甲苯易被高锰酸钾氧化,可知苯环影响甲基,故D不选;
故选:A。
3.D
【详解】A. 该有机物含有酚羟基,能与FeCl3溶液发生显色反应,故A正确;
B. 该有机物含有碳碳双键,能够使酸性高锰酸钾溶液褪色,故B正确;
C. 该有机物含有酯基,溴原子,能与NaOH溶液发生水解反应,故C正确;
D. 两苯环各消耗3molH2、碳碳双键消耗1molH2,1mol该有机物最多与7molH2发生加成反应,故D错误;
故选D。
4.B
【详解】A.乙醇的结构式为:,无碳氧双键,乙酸的官能团羧基中含有碳氧双键,A错误;
B.乙醇中的官能团为:-OH,乙酸的官能团为:-COOH,两个官能团均与金属钠发生置换反应,B正确;
C.乙醇可以发生催化氧化、被酸性高锰酸钾氧化等,乙酸可以燃烧,发生氧化反应,C错误;
D.乙酸为一元弱酸,可以使紫色石蕊试液变红,乙醇为非电解质,不能电离,不能使紫色石蕊试液变红,D错误;
答案为:B。
5.A
【分析】反应①为加成反应,反应②为取代反应,反应③、④均属于氧化反应。
【详解】A.①为加成反应,产物只有一种,故其原子利用率可以达到100%,A正确;
B.转化③、④属于氧化反应,B项错误;
C.、均可使酸性溶液褪色,C错误;
D.中含有的官能团名称为羧基,D错误;
故选A。
6.B
【详解】A.Y分子中由于两个不饱和的C原子上连接了两个不同的原子和原子团,因此该物质的分子存在顺反异构体,A正确;
B.X分子中含有的醇羟基不能与NaOH发生反应,分子中含有的酯基水解产生的酚羟基和羧基都可以与NaOH反应,故1 mol X与足量NaOH溶液反应,最多消耗2 mol NaOH,B错误;
C.Y分子中含有不饱和的碳碳双键,在一定条件下,能够发生加聚反应;可以与H2发生加成反应,与H2的加成反应也属于还原反应;含有苯环,在一定条件下能够发生取代反应,故一定条件下Y分子可以发生取代、加聚、还原反应,C正确;
D.手性碳原子是连接4个不同的原子或原子团的C原子。根据Z的结构简式可知:Z分子中只有与两个六元环连接的C原子为手性C原子,故Z分子中含有1个手性碳原子,D正确;
故合理选项是B。
7.C
【详解】A.本实验应该将浓度均为0.1 mol·L 1NaCl和NaI混合溶液滴加到硝酸银溶液,硝酸银过量,同时产生氯化银和碘化银的沉淀,不能说明Ksp(AgI)<Ksp(AgCl),A项错误;
B.银镜反应发生的条件是碱性环境,所以不能说明蔗糖的水解产物无还原性,B项错误;
C.H2O2在MnO2的催化作用下会分解生成O2,产生气泡说明有氧气生成,也说明原溶液中有H2O2,C项正确;
D.向FeCl3溶液中滴加稀氨水,会生成氢氧化铁红褐色沉淀,D项错误;
答案选C。
8.B
【详解】A.苯酚和碳酸钠反应生成的是苯酚钠和碳酸氢钠,只能证明苯酚的酸性强于碳酸氢根,错误;
B.二氧化硫溶于水显酸性,酸性条件下硝酸根离子有强氧化性,将二氧化硫氧化为硫酸根离子,和Ba2+反应生成白色沉淀硫酸钡,正确;
C.制取氢氧化铜悬浊液时应加入过量的NaOH溶液,氢氧化钠少量时难以发生反应,错误;
D.醋酸钠和亚硫酸钠溶液的浓度未知,无法通过测定溶液的pH确定醋酸和亚硫酸的酸性强弱,错误;
故选B。
9.A
【详解】A.Cl2、Br2、I2都是由分子构成的物质,它们结构相似,物质的相对分子质量越大,分子之间作用力就越大,物质的熔沸点就越高,所以Cl2、Br2、I2的沸点逐渐升高;都是由分子构成的物质,它们结构相似,物质的相对分子质量越大,分子之间作用力就越大,物质的熔沸点就越高,所以H2、N2、O2的沸点也逐渐升高,A正确;
B.CH3CHO分子中含有醛基,那个与H2可发生加成反应产生CH3CH2OH,而CH3COOH分子中的-COOH具有独特的稳定性,在相同条件下CH3COOH不可以与H2发生加成反应,B错误;
C.向Na2CO3中加入少量水,会伴随放热现象,而向NaHCO3中加入少量水,则伴随的是吸热现象,C错误;
D.乙醇具有还原性,当其与足量酸性高锰酸钾溶液反应时会被氧化生成乙酸,而乙二醇与足量酸性高锰酸钾溶液反应生成CO2,不能反应达到乙二酸,D错误;
故合理选项是A。
10.B
【详解】乙醛能被氧化物乙酸也可与氢气反应被还原为乙醇,答案为B。
11.A
【详解】A.含有碳碳双键和酯基,则含有两个官能团,故A错误;
B.含有碳碳双键,能发生加成和氧化反应,故B正确;
C.含有酯基,能发生水解反应生成醇羟基连接在亚甲基上,具有-CH2OH结构,能发生催化氧化生成醛,故C正确;
D.可用于诱捕害虫、测报虫情,可知该化合物具有一定的挥发性,故D正确;
故选:A。
12. C10H8O3 酯基 3
【分析】根据羟甲香豆素的结构,分析所含有的官能团,再判断解析。
【详解】(1)该物质的分子式是C10H8O3;
(2)该物质分子中含有的官能团有羟基、碳碳双键和酯基;
(3) 含有的酚羟基能与NaOH溶液反应,所含酯基水解后引入的酚羟基和羧基均能和NaOH溶液反应,则1mol 该物质与足量 NaOH 溶液反应,最多消耗3molNaOH。
13.(1)CH3COOHCH3COO-+H+
(2) 溶液变红色 有无色气体产生 2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O
(3)强
【解析】(1)
乙酸是弱酸,在水中部分电离,电离方程式为CH3COOH CH3COO-+H+;
(2)
乙酸具有酸的通性,可使石蕊试液变红;乙酸与碳酸钠反应生成乙酸钠、水和二氧化碳,产生的现象是有无色气体产生;反应的方程式为2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O;
(3)
根据以上事实,说明乙酸的酸性比碳酸的酸性强。
14. 有机化合物 碳碳双键 羧基 酸 酯化反应或者取代反应 溴水褪色
【详解】(1)丙烯酸属于有机化合物;
(2)丙烯酸中含有的官能团有碳碳双键和羧基;
(3)向丙烯酸溶液中滴入2~3滴紫色石蕊试液,溶液颜色变红,说明丙烯酸溶液具有酸性;
(4)丙烯酸和乙醇发生酯化反应生成丙烯酸乙酯和水,酯化反应属于取代反应;
(5)丙烯酸含有碳碳双键,能与溴水发生加成反应,故向丙烯酸溶液中滴入几滴溴水,实验现象为溴水褪色。
15. 羧基 a、c +2NaOH → HOCH2CH(NH2)COONa+H2O+CH3COONa
【分析】(1)甲含有氨基和羧基;
(2)a.该分子中C、N原子个数分别是7、5;
b.含有苯环的有机物属于芳香族化合物;
c.氨基能和酸反应、氯原子能和碱溶液反应;
d.该分子中含有N原子;
(3)丙的同分异构体丁中含有、在稀硫酸中水解有乙酸生成,说明丁含有酯基,丁为乙酸某酯,据此判断丁的结构简式;
(4)丁为,含有酯基,可在碱性条件下水解,且羧基于氢氧化钠发生中和反应。
【详解】(1)甲含有氨基和羧基,含氧官能团为羧基;
(2)a.该分子中C、N原子个数分别是7、5,所以分子中碳原子与氮原子的个数比是7:5,a正确;
b.含有苯环的有机物属于芳香族化合物,该分子中没有苯环,所以不属于芳香族化合物,b错误;
c.氨基能和酸反应、氯原子能和碱溶液反应,所以该物质既能与盐酸又能与氢氧化钠溶液反应,c正确;
d.该分子中含有N原子,不属于苯酚的同系物,d错误;
故合理选项是ac;
(3)丙的同分异构体丁中含有、在稀硫酸中水解有乙酸生成,说明丁含有酯基,丁为乙酸某酯,所以丁的结构简式为;
(4)丁为,含有酯基,可在碱性条件下水解,且羧基于氢氧化钠发生中和反应,方程式为+2NaOH=HOCH2CH(NH2)COONa+H2O+CH3COONa。
【点睛】本题考查了有机物的结构和性质,涉及有机物合成、反应类型的判断、基本概念等知识点,根据物质反应特点确定反应类型、根据流程图中反应物及反应条件确定生成物,再结合基本概念解答。
16.
【详解】在浓硫酸作用下发生消去反应,连接-OH的碳上碳氧键断裂,连接-OH的碳的邻位碳上碳氢键断裂,同时形成碳碳双键,故产物为:
17. 5 3
【详解】酚羟基是邻对位取代基,能够与Br2在羟基在苯环上的邻位和对位上发生取代反应,不饱和的碳碳双键可以与Br2发生加成反应,该物质分子中2个苯环上有4个羟基的邻对位可以与4个Br2发生取代反应,1个不饱和的碳碳双键能够与1个Br2发生加成反应,故1个染料木黄酮与足量溴水反应会消耗5个Br2;酚羟基具有碱性,能够与NaOH发生反应产生酚钠。该物质分子中含有3个酚羟基,因此1个染料木黄酮能够与3个NaOH发生反应,故1 mol染料木黄酮与足量溴水反应时,最多可消耗5 mol Br2;1 mol染料木黄酮中含有3 mol酚羟基,故与足量NaOH溶液反应时,最多可消耗3 mol NaOH。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列说法不正确的是
A.向磷酸二氢钠溶液中加入过量澄清石灰水:
B.用重铬酸钾法测定白酒中乙醇的含量:
C.用碳酸钠溶液处理锅炉水垢中的硫酸钙:
D.制摩尔盐时用酒精洗涤产品,制阿司匹林时用冷水洗涤产品
2.有机化合物分子中的邻近基团间往往会有一定的相互影响,这种影响会使有机化合物表现出一些特性。下列事实不能证明这一说法的是
A.苯乙烯能与溴水反应,而苯不能与溴水反应
B.苯酚能与NaOH溶液反应,而乙醇不能与NaOH溶液反应
C.苯与硝酸反应生成硝基苯,而甲苯与硝酸反应生成三硝基甲苯
D.甲苯能使酸性高锰酸钾溶液褪色,而乙烷不能使酸性高锰酸钾溶液褪色
3.新冠肺炎病毒疫情爆发以来,我国科学家、医务工作者一直奋战在第一线,攻坚克难,成功研制出多种抑制新冠病毒药物,应用于临床,为战胜疫情立下赫赫战功。我们从化学的角度分析药物的结构,探究其性质,以此向战疫英雄致敬。2020年2月4日,中国工程院院士李兰娟团队发布最新研究成果:盐酸阿比多尔在体外细胞实验中能有效抑制冠状病毒。盐酸阿比多尔的结构简式如图所示,下列有关该有机物的说法不正确的是
A.该有机物能与FeCl3溶液发生显色反应
B.能够使酸性高锰酸钾溶液褪色
C.能与NaOH溶液发生水解反应
D.1mol该有机物最多与8molH2发生加成反应
4.乙醇和乙酸是两种常见的有机化合物,下列说法正确的是
A.乙醇和乙酸的分子结构中均含有碳氧双键
B.乙醇和乙酸均能与金属钠反应
C.乙醇能发生氧化反应,而乙酸不能发生氧化反应
D.乙醇和乙酸均能使紫色石蕊试液变红
5.以乙烯为原料制备草酸的流程如下:
,下列有关说法中正确的是
A.转化①原子利用率可以达到100%
B.转化②、③、④均属于取代反应
C.可用酸性溶液鉴别与
D.中含有的官能团名称为羟基
6.化合物Z(华法林)是一种香豆素类抗凝剂,可由下列反应制得:
下列说法不正确的是
A.Y分子存在顺反异构体
B.1 mol X与足量NaOH溶液反应,最多消耗3 mol NaOH
C.一定条件下,Y分子可以发生取代、加聚、还原反应
D.Z分子中含有1个手性碳原子
7.下列实验操作和现象及所得到的结论均正确的是
选项 实验操作和现象 结论
A 把浓度均为0.1mol·L-1NaCl和NaI混合溶液逐滴滴加到0.1mol·L-1AgNO3中,有黄色沉淀生成 Ksp(AgI)<Ksp(AgCl)
B 向20%蔗糖溶液中加入少量稀硫酸、加热,再加入银氨溶液,水浴加热,无明显现象产生 蔗糖的水解产物无还原性
C 向Na2O2与水反应所得溶液中加入少量MnO2,有气泡产生 Na2O2与水反应所得溶液中有少量H2O2
D 向FeCl3溶液中滴加稀氨水,溶液由黄色变为红褐色 生成了氢氧化铁胶体
A.A B.B C.C D.D
8.下列实验操作、现象和结论都正确的是
选项 实验操作和现象 结论
A 向苯酚浊液中滴加溶液,浊液变澄清 苯酚的酸性强于的酸性
B 向溶液中通入气体,出现白色沉淀 白色沉淀为硫酸钡
C 向2 mL 10%的溶液中滴入5~6滴2%的NaOH溶液,再滴入葡萄糖溶液并加热,产生砖红色沉淀 葡萄糖含有醛基
D 相同温度下,用pH试纸测溶液试纸显蓝色;测溶液的试纸显深蓝色 相同温度下
A.A B.B C.C D.D
9.下列“类比”结果正确的是
A.Cl2、Br2、I2的沸点逐渐升高,则H2、N2、O2的沸点也逐渐升高
B.CH3CHO与H2可发生加成反应,则相同条件下CH3COOH也可以与H2发生加成反应
C.向Na2CO3中加入少量水,伴随放热现象,则向NaHCO3中加入少量水,也伴随放热现象
D.乙醇与足量酸性高锰酸钾溶液反应生成乙酸,则乙二醇与足量酸性高锰酸钾溶液反应生成乙二酸
10. 下列物质中,既可被氧化又可被氢气还原的是
A.乙烷 B.乙醛 C.乙酸 D.乙醇
11.人类利用人工合成信息素诱捕害虫、测报虫情等。一种集结信息素的分子结构简式如图所示,关于该有机物的说法不正确的是
A.该有机物分子含有三种官能团 B.该有机物能发生加成和氧化反应
C.该有机物水解产物之一能氧化成醛 D.该有机物具有一定的挥发性
二、填空题
12.羟甲香豆素是一种治疗胆结石的药物,其结构简式如图所示:
(1)该物质的分子式是___________________。
(2)该物质分子中含有的官能团有羟基、碳碳双键和___________________。
(3)1mol 该物质与足量 NaOH 溶液反应,最多消耗 NaOH___________ mol。
13.乙酸是一种弱酸,请回答以下问题:
(1)乙酸在水中的电离方程式为_______。
(2)向乙酸溶液中加入石蕊试液,产生的现象是_______;将乙酸溶液滴加到碳酸钠溶液中,产生的现象是_______,反应的方程式为_______。
(3)根据以上事实,说明乙酸的酸性比碳酸的酸性_______(填“强”或“弱”)。
14.丙烯酸(CH2=CH-COOH)是重要的有机合成原料及合成树脂单体,是最简单的不饱和羧酸。
(1)丙烯酸属于___________(填“无机化合物”或“有机化合物”)。
(2)丙烯酸中含有的官能团有___________和___________(填名称)。
(3)向丙烯酸溶液中滴入2~3滴紫色石蕊试液,溶液颜色变红,说明丙烯酸溶液具有___________性。
(4)丙烯酸和乙醇发生___________(填反应类型)生成丙烯酸乙酯和水。
(5)向丙烯酸溶液中滴入几滴溴水,实验现象为___________。
15.叶酸是维生素B族之一,可以由下列甲、乙、丙三种物质合成。
(1)甲中含氧官能团是__________(填名称)。
(2)下列关于乙的说法正确的是________(填序号)。
a.分子中碳原子与氮原子的个数比是7∶5 b.属于芳香族化合物
c.既能与盐酸又能与氢氧化钠溶液反应 d.属于苯酚的同系物
(3)丁是丙的同分异构体,且满足下列两个条件,丁的结构简式为________。
a.含有
b.在稀硫酸中水解有乙酸生成
(4)写出丁在氢氧化钠溶液中水解的化学方程式。________
16.柠檬酸()在浓硫酸、加热条件下可发生消去反应,且消去产物只有一种。(__)
17.1 mol染料木黄酮()与足量溴水反应,最多可消耗_______mol Br2;与足量NaOH溶液反应,最多可消耗_______mol NaOH。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
【详解】A.磷酸二氢钠化学式为NaH2PO4,在溶液中电离产生Na+和,首先发生反应+2OH-=+2H2O,生成的继续发生反应:3Ca2++2=Ca3(PO4)2↓,由于NaH2PO4少量,故、完全反应,两步叠加消去得总离子方程式为:2+4OH-+3Ca2+= Ca3(PO4)2↓+4H2O,A错误;
B.K2Cr2O7具有强氧化性,可将CH3CH2OH氧化为CH3COOH,K2Cr2O7在酸性条件下能稳定存在,若在碱性条件下,则会转化为K2CrO4,故此时溶液为酸性溶液,结合得失电子守恒、电荷守恒(可添加H+)、元素守恒(可添加H2O),配平得离子方程式为:2+3C2H5OH+16H+=4Cr3++3CH3COOH+11H2O,B正确;
C.Na2CO3溶液处理CaSO4利用了沉淀转化的原理,微溶的CaSO4可转化为难溶的CaCO3,对应离子方程式为:CaSO4(s)+(aq)=CaCO3(s)+(aq),C正确;
D.摩尔盐在有机溶剂中溶解度小,因此制备摩尔盐可用酒精洗涤,阿司匹林的溶解度随温度的升高而增大,因此洗涤阿司匹林时可采用冷水或冰水洗涤,D正确;
故答案选A。
2.A
【详解】A.苯乙烯含有碳碳双键,可以与溴发生加成反应,与官能团性质有关,不是邻近基团造成的影响,故A选;
B.苯酚、乙醇都含有羟基,苯酚能与NaOH溶液反应,可知苯环影响了羟基,故B不选;
C.甲基影响苯环,使苯环上H活泼,则甲苯易发生三取代,故C不选;
D.苯环、乙烷中均有甲基,而甲苯易被高锰酸钾氧化,可知苯环影响甲基,故D不选;
故选:A。
3.D
【详解】A. 该有机物含有酚羟基,能与FeCl3溶液发生显色反应,故A正确;
B. 该有机物含有碳碳双键,能够使酸性高锰酸钾溶液褪色,故B正确;
C. 该有机物含有酯基,溴原子,能与NaOH溶液发生水解反应,故C正确;
D. 两苯环各消耗3molH2、碳碳双键消耗1molH2,1mol该有机物最多与7molH2发生加成反应,故D错误;
故选D。
4.B
【详解】A.乙醇的结构式为:,无碳氧双键,乙酸的官能团羧基中含有碳氧双键,A错误;
B.乙醇中的官能团为:-OH,乙酸的官能团为:-COOH,两个官能团均与金属钠发生置换反应,B正确;
C.乙醇可以发生催化氧化、被酸性高锰酸钾氧化等,乙酸可以燃烧,发生氧化反应,C错误;
D.乙酸为一元弱酸,可以使紫色石蕊试液变红,乙醇为非电解质,不能电离,不能使紫色石蕊试液变红,D错误;
答案为:B。
5.A
【分析】反应①为加成反应,反应②为取代反应,反应③、④均属于氧化反应。
【详解】A.①为加成反应,产物只有一种,故其原子利用率可以达到100%,A正确;
B.转化③、④属于氧化反应,B项错误;
C.、均可使酸性溶液褪色,C错误;
D.中含有的官能团名称为羧基,D错误;
故选A。
6.B
【详解】A.Y分子中由于两个不饱和的C原子上连接了两个不同的原子和原子团,因此该物质的分子存在顺反异构体,A正确;
B.X分子中含有的醇羟基不能与NaOH发生反应,分子中含有的酯基水解产生的酚羟基和羧基都可以与NaOH反应,故1 mol X与足量NaOH溶液反应,最多消耗2 mol NaOH,B错误;
C.Y分子中含有不饱和的碳碳双键,在一定条件下,能够发生加聚反应;可以与H2发生加成反应,与H2的加成反应也属于还原反应;含有苯环,在一定条件下能够发生取代反应,故一定条件下Y分子可以发生取代、加聚、还原反应,C正确;
D.手性碳原子是连接4个不同的原子或原子团的C原子。根据Z的结构简式可知:Z分子中只有与两个六元环连接的C原子为手性C原子,故Z分子中含有1个手性碳原子,D正确;
故合理选项是B。
7.C
【详解】A.本实验应该将浓度均为0.1 mol·L 1NaCl和NaI混合溶液滴加到硝酸银溶液,硝酸银过量,同时产生氯化银和碘化银的沉淀,不能说明Ksp(AgI)<Ksp(AgCl),A项错误;
B.银镜反应发生的条件是碱性环境,所以不能说明蔗糖的水解产物无还原性,B项错误;
C.H2O2在MnO2的催化作用下会分解生成O2,产生气泡说明有氧气生成,也说明原溶液中有H2O2,C项正确;
D.向FeCl3溶液中滴加稀氨水,会生成氢氧化铁红褐色沉淀,D项错误;
答案选C。
8.B
【详解】A.苯酚和碳酸钠反应生成的是苯酚钠和碳酸氢钠,只能证明苯酚的酸性强于碳酸氢根,错误;
B.二氧化硫溶于水显酸性,酸性条件下硝酸根离子有强氧化性,将二氧化硫氧化为硫酸根离子,和Ba2+反应生成白色沉淀硫酸钡,正确;
C.制取氢氧化铜悬浊液时应加入过量的NaOH溶液,氢氧化钠少量时难以发生反应,错误;
D.醋酸钠和亚硫酸钠溶液的浓度未知,无法通过测定溶液的pH确定醋酸和亚硫酸的酸性强弱,错误;
故选B。
9.A
【详解】A.Cl2、Br2、I2都是由分子构成的物质,它们结构相似,物质的相对分子质量越大,分子之间作用力就越大,物质的熔沸点就越高,所以Cl2、Br2、I2的沸点逐渐升高;都是由分子构成的物质,它们结构相似,物质的相对分子质量越大,分子之间作用力就越大,物质的熔沸点就越高,所以H2、N2、O2的沸点也逐渐升高,A正确;
B.CH3CHO分子中含有醛基,那个与H2可发生加成反应产生CH3CH2OH,而CH3COOH分子中的-COOH具有独特的稳定性,在相同条件下CH3COOH不可以与H2发生加成反应,B错误;
C.向Na2CO3中加入少量水,会伴随放热现象,而向NaHCO3中加入少量水,则伴随的是吸热现象,C错误;
D.乙醇具有还原性,当其与足量酸性高锰酸钾溶液反应时会被氧化生成乙酸,而乙二醇与足量酸性高锰酸钾溶液反应生成CO2,不能反应达到乙二酸,D错误;
故合理选项是A。
10.B
【详解】乙醛能被氧化物乙酸也可与氢气反应被还原为乙醇,答案为B。
11.A
【详解】A.含有碳碳双键和酯基,则含有两个官能团,故A错误;
B.含有碳碳双键,能发生加成和氧化反应,故B正确;
C.含有酯基,能发生水解反应生成醇羟基连接在亚甲基上,具有-CH2OH结构,能发生催化氧化生成醛,故C正确;
D.可用于诱捕害虫、测报虫情,可知该化合物具有一定的挥发性,故D正确;
故选:A。
12. C10H8O3 酯基 3
【分析】根据羟甲香豆素的结构,分析所含有的官能团,再判断解析。
【详解】(1)该物质的分子式是C10H8O3;
(2)该物质分子中含有的官能团有羟基、碳碳双键和酯基;
(3) 含有的酚羟基能与NaOH溶液反应,所含酯基水解后引入的酚羟基和羧基均能和NaOH溶液反应,则1mol 该物质与足量 NaOH 溶液反应,最多消耗3molNaOH。
13.(1)CH3COOHCH3COO-+H+
(2) 溶液变红色 有无色气体产生 2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O
(3)强
【解析】(1)
乙酸是弱酸,在水中部分电离,电离方程式为CH3COOH CH3COO-+H+;
(2)
乙酸具有酸的通性,可使石蕊试液变红;乙酸与碳酸钠反应生成乙酸钠、水和二氧化碳,产生的现象是有无色气体产生;反应的方程式为2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O;
(3)
根据以上事实,说明乙酸的酸性比碳酸的酸性强。
14. 有机化合物 碳碳双键 羧基 酸 酯化反应或者取代反应 溴水褪色
【详解】(1)丙烯酸属于有机化合物;
(2)丙烯酸中含有的官能团有碳碳双键和羧基;
(3)向丙烯酸溶液中滴入2~3滴紫色石蕊试液,溶液颜色变红,说明丙烯酸溶液具有酸性;
(4)丙烯酸和乙醇发生酯化反应生成丙烯酸乙酯和水,酯化反应属于取代反应;
(5)丙烯酸含有碳碳双键,能与溴水发生加成反应,故向丙烯酸溶液中滴入几滴溴水,实验现象为溴水褪色。
15. 羧基 a、c +2NaOH → HOCH2CH(NH2)COONa+H2O+CH3COONa
【分析】(1)甲含有氨基和羧基;
(2)a.该分子中C、N原子个数分别是7、5;
b.含有苯环的有机物属于芳香族化合物;
c.氨基能和酸反应、氯原子能和碱溶液反应;
d.该分子中含有N原子;
(3)丙的同分异构体丁中含有、在稀硫酸中水解有乙酸生成,说明丁含有酯基,丁为乙酸某酯,据此判断丁的结构简式;
(4)丁为,含有酯基,可在碱性条件下水解,且羧基于氢氧化钠发生中和反应。
【详解】(1)甲含有氨基和羧基,含氧官能团为羧基;
(2)a.该分子中C、N原子个数分别是7、5,所以分子中碳原子与氮原子的个数比是7:5,a正确;
b.含有苯环的有机物属于芳香族化合物,该分子中没有苯环,所以不属于芳香族化合物,b错误;
c.氨基能和酸反应、氯原子能和碱溶液反应,所以该物质既能与盐酸又能与氢氧化钠溶液反应,c正确;
d.该分子中含有N原子,不属于苯酚的同系物,d错误;
故合理选项是ac;
(3)丙的同分异构体丁中含有、在稀硫酸中水解有乙酸生成,说明丁含有酯基,丁为乙酸某酯,所以丁的结构简式为;
(4)丁为,含有酯基,可在碱性条件下水解,且羧基于氢氧化钠发生中和反应,方程式为+2NaOH=HOCH2CH(NH2)COONa+H2O+CH3COONa。
【点睛】本题考查了有机物的结构和性质,涉及有机物合成、反应类型的判断、基本概念等知识点,根据物质反应特点确定反应类型、根据流程图中反应物及反应条件确定生成物,再结合基本概念解答。
16.
【详解】在浓硫酸作用下发生消去反应,连接-OH的碳上碳氧键断裂,连接-OH的碳的邻位碳上碳氢键断裂,同时形成碳碳双键,故产物为:
17. 5 3
【详解】酚羟基是邻对位取代基,能够与Br2在羟基在苯环上的邻位和对位上发生取代反应,不饱和的碳碳双键可以与Br2发生加成反应,该物质分子中2个苯环上有4个羟基的邻对位可以与4个Br2发生取代反应,1个不饱和的碳碳双键能够与1个Br2发生加成反应,故1个染料木黄酮与足量溴水反应会消耗5个Br2;酚羟基具有碱性,能够与NaOH发生反应产生酚钠。该物质分子中含有3个酚羟基,因此1个染料木黄酮能够与3个NaOH发生反应,故1 mol染料木黄酮与足量溴水反应时,最多可消耗5 mol Br2;1 mol染料木黄酮中含有3 mol酚羟基,故与足量NaOH溶液反应时,最多可消耗3 mol NaOH。
答案第1页,共2页
答案第1页,共2页
