2022-2023学年人教版(2019)高中化学选择性必修3 4.2 蛋白质 课件(共28张PPT)
文档属性
| 名称 | 2022-2023学年人教版(2019)高中化学选择性必修3 4.2 蛋白质 课件(共28张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 17.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-30 00:00:00 | ||
图片预览






文档简介
(共28张PPT)
第二节 蛋白质
第四章生物大分子
宏观辨识与微观探析 能辨识蛋白质结构中的肽键,能说明蛋白质的基本结构特点,能判断氨基酸的缩合产物、多肽的水解产物。能分析说明氨基酸、蛋白质与人体健康的关系。
科学态度与社会责任 了解氨基酸、蛋白质与人体健康的关系。认识人工合成多肽、蛋白质的意义,体会化学学科在生命科学发展中所起的重要作用。
核心素养
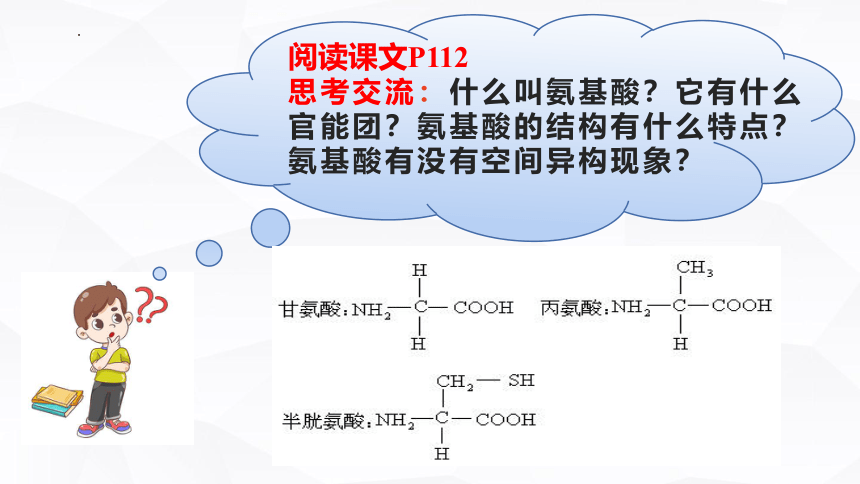
阅读课文P112
思考交流:什么叫氨基酸?它有什么官能团?氨基酸的结构有什么特点?氨基酸有没有空间异构现象?
一、氨基酸
①从结构上看,氨基酸可以看作是羧酸分子中烃基上的氢原子被氨基取代的产物。
②官能团:分子中既含有—COOH又含有—NH2。
③组成蛋白质的氨基酸主要是ɑ-氨基酸,氨基连接在与羧基相邻的ɑ位的碳原子上。
1.氨基酸定义:
R CH COOH
NH2
ɑ
当R不是H时,(即除甘氨酸外),ɑ-碳为手性碳原子
α-氨基酸除甘氨酸外,一般均含有连接四个不同原子或原子团的__________,具有___________。
手性碳原子
对映异构体
常见的氨基酸
俗名 结构简式 命名
甘氨酸
丙氨酸
谷氨酸
苯丙氨酸
半胱氨酸
CH2—COOH
H2N
氨基乙酸
2-氨基丙酸
2-氨基戊二酸
2-氨基-3-苯基丙酸
2-氨基-3-巯基丙酸
CH3—CH—COOH
NH2
HOOC—(CH2)2—CH—COOH
NH2
一、氨基酸
天然氨基酸均为无色晶体,熔点较高,在200~3000C时熔化分解,一般能溶于水而难溶于乙醇、乙醚等有机溶剂.
2.氨基酸的物理性质
大家思考一下,氨基酸的官能团决定了它具有什么样的性质?
酸性基团
碱性基团
3.氨基酸的化学性质:
一、氨基酸
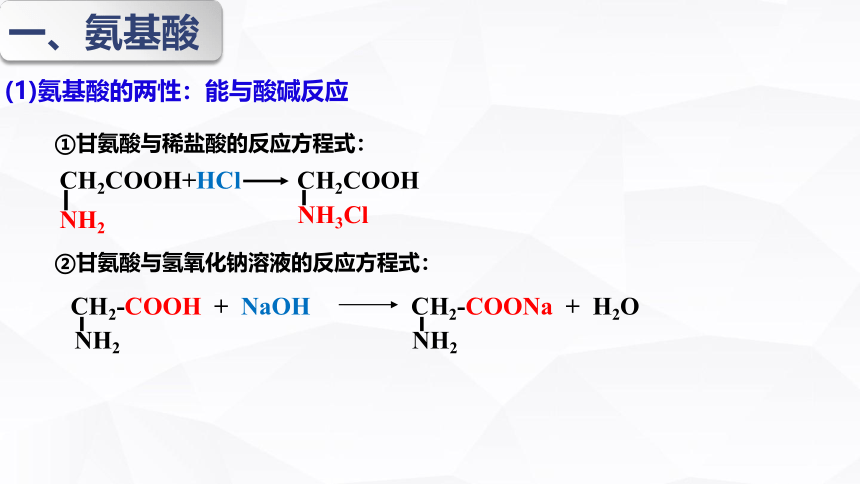
(1)氨基酸的两性:能与酸碱反应
①甘氨酸与稀盐酸的反应方程式:
②甘氨酸与氢氧化钠溶液的反应方程式:
CH2COOH+HCl CH2COOH
NH2
NH3Cl
CH2-COOH + NaOH
NH2
CH2-COONa + H2O
NH2
一、氨基酸
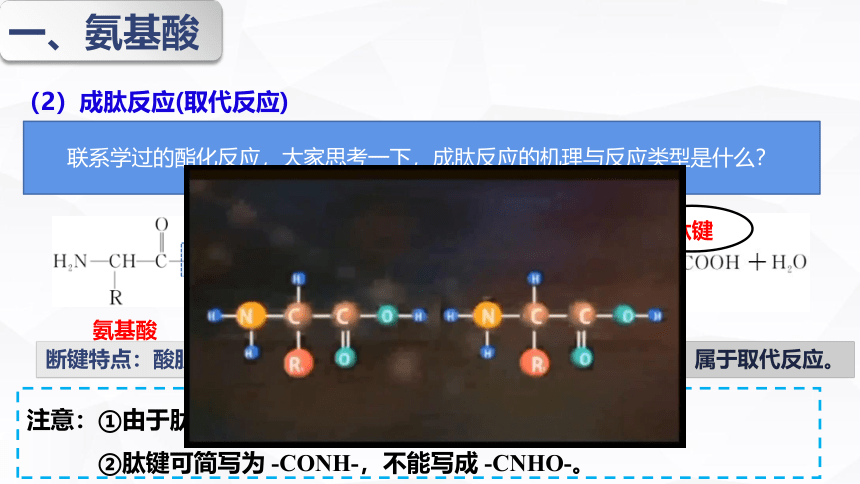
(2)成肽反应(取代反应)
氨基酸
氨基酸
二肽
肽键
注意:①由于肽中仍含有-NH2和-COOH,肽也有两性。
②肽键可简写为 -CONH-,不能写成 -CNHO-。
两个氨基酸分子(可以相同,也可以不同)在一定条件下,通过氨基与羧基间缩合脱去水,形成含有肽键 的化合物,发生成肽反应。
断键特点:酸脱羟基,氨脱氢
成肽反应是分子间脱水反应,属于取代反应。
联系学过的酯化反应,大家思考一下,成肽反应的机理与反应类型是什么?
一、氨基酸
学以致用
一、氨基酸
甘氨酸和丙氨酸以1∶1的配比两两缩合后,得到的产物可能有( )种,它们是:
4
两分子氨基酸
缩合
二肽
三肽
缩合
+氨基酸
缩合
+氨基酸
四肽
缩合
+氨基酸
多肽
· · · ··
呈链状
肽链
又称
相互结合形成
盘曲、折叠
蛋白质
Mr>10000
具有一定的空间结构
一、氨基酸
(1)定义:蛋白质是由多种氨基酸通过肽键等相互连接形成的一类生物大分子。
(2)组成: 蛋白质中主要含有C、H、O、N、S等元素,有些蛋白质还含有
P、Fe、Zn、Cu等元素,属于天然有机高分子。其溶液具有胶
体的某些性质。
人体内所具有的蛋白质种类达到了10万种以上。那它们具有什么样的空间结构呢?
1.蛋白质的定义、组成与存在
—— 四级空间结构
→ 各种蛋白质都有其特殊功能和活性
2.蛋白质的结构
(3)存在:
蛋白质主要存在于生物体内,如肌肉、毛发、皮肤、角、酶、抗体、病毒等;在植物中也很丰富,如大豆、花生、谷物。
二、蛋白质
例如,血红蛋白分子中的________会因遗传因素变成________,这一微小差别会导致红细胞的形态由正常的圆饼状变为异常的镰刀状,使人患镰状细胞贫血。
蛋白质分子中氨基酸单体的排列顺序
一级结构是蛋白质高级结构的基础,对蛋白质的性质和功能起着决定性作用
谷氨酸
缬氨酸
二、蛋白质
肽键中的氧原子与氢原子之间存在氢键,会使肽链盘绕或折叠成特定的空间结构
一级结构
二级结构
蛋白质一级结构怎么组成?有什么意义?二级结构又是怎么组成的?
3.蛋白质的化学性质
蛋白质分子中两端的氨基和羧基说明什么?
(1)蛋白质具有两性:能与酸碱反应
二、蛋白质
(2)水解反应
在酸、碱或酶作用下,逐步水解成相对分子质量较小的_____,最终水解得到________。
多肽
氨基酸
二、蛋白质
食物中的蛋白质在人体内各种蛋白酶的作用下水解成氨基酸,氨基酸被肠壁吸收进入血液,再在体内重新合成人体所需要的蛋白质。
水解断键特点:碳加羟基,氮加氢
二、蛋白质
振荡
白色沉淀
加水
沉淀溶解
饱和(NH4)2SO4溶液
—鸡蛋清溶液
原理:
少量的某些可溶性盐(如硫酸铵、硫酸钠、氯化钠等)能促进蛋白质的溶解。但当这些盐在蛋白质溶液中达到一定浓度时,反而使蛋白质的溶解度降低而使其从溶液中析出,这种作用称为盐析。
特点:
蛋白质的盐析是一个可逆过程,盐析出的蛋白质在水中仍能溶解,并不影响其活性。属于物理变化过程。
应用:
采用多次盐析和溶解,可以分离提纯蛋白质。
(3)盐析
二、蛋白质
振荡
白色沉淀
加水
沉淀不溶解
酒精
—鸡蛋清溶液
概 念
影响因素 物理
化学
特 点 变性会使蛋白质的结构发生变化,使其失去原有的__________,
在水中不能重新溶解,是 过程
应 用
在某些物理或化学因素的影响下,蛋白质的性质和生理功能发生改变的现象
加热、加压、搅拌、振荡、紫外线和放射线、超声波等
强酸、强碱、重金属盐、乙醇、甲醛、丙酮等
不可逆
生理活性
杀菌、消毒、防中毒
(4)变性
二、蛋白质
二、蛋白质
【思考与讨论 】
(1)因误服铅、汞等重金属盐中毒的患者在急救时,为什么可口服牛奶、
蛋清或豆浆?
(2)为什么紫外线可用于环境和物品消毒,放射线可用于医疗器械灭菌?
(3)鸡、鱼、肉、蛋等蛋白质食品做熟食用的原理是什么?
牛奶、蛋清、豆浆中含大量的蛋白质,让铅、汞等重金属盐使他们变性,减少对人体伤害。
紫外线、放射线能使病毒、细菌蛋白蛋变性而灭活。
高温使蛋白质的空间结构变得伸展、松散,易于水解,便于吸收
振荡
白色沉淀
加热
沉淀变黄色
浓硝酸
—鸡蛋清溶液
蛋白质变性
含有苯环的蛋白质均能发生这个反应
固体蛋白质如皮肤、指甲遇浓硝酸变______色。
黄
其他一些试剂也可以与蛋白质作用,呈现特定颜色
可用于蛋白质的分析检测
(5)显色反应
二、蛋白质
其他鉴别方法:
燃烧产生烧焦羽毛的气味。
阅读P117-118科学史话和资料卡片,思考与交流
1、烫发的原理是什么?
2、人们对蛋白质结构、性质和功能的研究有什么意义
二、蛋白质
头发主要由角蛋白组成,二硫键(-S-S-)是维持头发弹性和形状的一个重要结构。烫发时使用的还原剂可以使头发中的二硫键断裂,产生游离的巯基(-SH )。定型后再用氧化剂使巯基之间发生反应,生成新的二硫键,使头发的形状得以固定。频繁烫发会对头发造成一定程度的损害。
人们对蛋白质结构、性质和功能的研究,为蛋白质的合成与应用奠定了基础。蛋白质
的人工合成,不仅为生命起源的化学途径提供了有力的证据,而且可以为人们提供性能
优异的药物和生物催化剂,对探索生命活动规律、促进人类健康具有重要意义。
蛋白质社会价值:
从2020年2月初疫苗项目立项,到当年12月30日,国药集团中国生物的新冠病毒灭活疫苗成为我国首个获批附条件上市的新冠疫苗,98天研发出新冠灭活疫苗,335天实现上市——正是无数相关工作人员不舍昼夜,与时间赛跑,才得以创造出疫苗研发的“中国速度”。
二、蛋白质
1.下列过程中,不可逆的是( )
A.蛋白质的盐析 B.酯的水解 C.蛋白质白变性 D.氯化铁的水解
2.欲将蛋白质从水中析出而又不改变它的性质应加入( )
A.甲醛溶液 B.CuSO4溶液 C.饱和Na2SO4溶液 D.浓硫酸
C
C
3.关于蛋白质的叙述错误的是( )
A.浓HNO3溅在皮肤上,使皮肤呈黄色,是由于浓HNO3和蛋白质发生了颜色反应
B.蛋白质溶液中加入饱和(NH4)2SO4溶液,蛋白质析出,再加水也不溶解
C.蛋白质水解的最终产物是氨基酸
D.高温灭菌的原理是加热后使蛋白质变性,从而使细菌死亡
B
学以致用
二、蛋白质
三、酶
在酶的作用下,生物才能进行新陈代谢,完成消化、呼吸、运动、生长、发育、繁殖等生命活动。
2.功能:
酶是一类由细胞产生的、对生物体内的化学反应具有催化作用的有机化合物,其中绝大多数是蛋白质。
1.定义:
阅读课文P115,思考酶的定义与功能
观察超效加酶洗衣粉使用说明,思考酶的特性
(1)高度的专一性. (一种酶只催化一种反应)
(2)高效性. (比普通催化剂高107)
(3)条件温和, 不需加热.
(一般在接近体温和中性的条件下进行,此时酶的
活性最高。超过适宜的温度时,酶将失去活性)
新冠病毒主要蛋白酶结构
3.酶催化作用有什么特点
目前,酶已经得到了广泛的应用,如蛋白酶用于医药、制革等工业,
淀粉酶用于食品、发酵、纺织等工业,有的酶还可用于疾病的诊断。
4.酶的应用:
三、酶
B
三、酶
学以致用
1.下列有关酶的说法中错误的是( )
A.大多数酶是具有催化作用的蛋白质
B.酶的催化作用具有高效性和专一性
C.高温或重金属盐能使大多数酶失去活性
D.酶只有在强酸、强碱条件下才能发挥作用
2.市场上有一种加酶洗衣粉,即在洗衣粉中加入少量的碱性蛋白酶,它的催化活性很强,衣服上的汗渍、血迹及人体排出的蛋白质、油渍遇到它,皆能水解而除去。下列衣料不能用加酶洗衣粉洗涤的是( )
①棉织品 ②羊毛织品 ③腈纶织品
④蚕丝织品 ⑤涤纶织品 ⑥锦纶织品
A.①②③ B.②④ C.③④⑤ D.③⑤⑥
D
二、蛋白质
作业
1、分层检测
2、限时过关卷
感谢观看
第二节 蛋白质
第四章生物大分子
宏观辨识与微观探析 能辨识蛋白质结构中的肽键,能说明蛋白质的基本结构特点,能判断氨基酸的缩合产物、多肽的水解产物。能分析说明氨基酸、蛋白质与人体健康的关系。
科学态度与社会责任 了解氨基酸、蛋白质与人体健康的关系。认识人工合成多肽、蛋白质的意义,体会化学学科在生命科学发展中所起的重要作用。
核心素养
阅读课文P112
思考交流:什么叫氨基酸?它有什么官能团?氨基酸的结构有什么特点?氨基酸有没有空间异构现象?
一、氨基酸
①从结构上看,氨基酸可以看作是羧酸分子中烃基上的氢原子被氨基取代的产物。
②官能团:分子中既含有—COOH又含有—NH2。
③组成蛋白质的氨基酸主要是ɑ-氨基酸,氨基连接在与羧基相邻的ɑ位的碳原子上。
1.氨基酸定义:
R CH COOH
NH2
ɑ
当R不是H时,(即除甘氨酸外),ɑ-碳为手性碳原子
α-氨基酸除甘氨酸外,一般均含有连接四个不同原子或原子团的__________,具有___________。
手性碳原子
对映异构体
常见的氨基酸
俗名 结构简式 命名
甘氨酸
丙氨酸
谷氨酸
苯丙氨酸
半胱氨酸
CH2—COOH
H2N
氨基乙酸
2-氨基丙酸
2-氨基戊二酸
2-氨基-3-苯基丙酸
2-氨基-3-巯基丙酸
CH3—CH—COOH
NH2
HOOC—(CH2)2—CH—COOH
NH2
一、氨基酸
天然氨基酸均为无色晶体,熔点较高,在200~3000C时熔化分解,一般能溶于水而难溶于乙醇、乙醚等有机溶剂.
2.氨基酸的物理性质
大家思考一下,氨基酸的官能团决定了它具有什么样的性质?
酸性基团
碱性基团
3.氨基酸的化学性质:
一、氨基酸
(1)氨基酸的两性:能与酸碱反应
①甘氨酸与稀盐酸的反应方程式:
②甘氨酸与氢氧化钠溶液的反应方程式:
CH2COOH+HCl CH2COOH
NH2
NH3Cl
CH2-COOH + NaOH
NH2
CH2-COONa + H2O
NH2
一、氨基酸
(2)成肽反应(取代反应)
氨基酸
氨基酸
二肽
肽键
注意:①由于肽中仍含有-NH2和-COOH,肽也有两性。
②肽键可简写为 -CONH-,不能写成 -CNHO-。
两个氨基酸分子(可以相同,也可以不同)在一定条件下,通过氨基与羧基间缩合脱去水,形成含有肽键 的化合物,发生成肽反应。
断键特点:酸脱羟基,氨脱氢
成肽反应是分子间脱水反应,属于取代反应。
联系学过的酯化反应,大家思考一下,成肽反应的机理与反应类型是什么?
一、氨基酸
学以致用
一、氨基酸
甘氨酸和丙氨酸以1∶1的配比两两缩合后,得到的产物可能有( )种,它们是:
4
两分子氨基酸
缩合
二肽
三肽
缩合
+氨基酸
缩合
+氨基酸
四肽
缩合
+氨基酸
多肽
· · · ··
呈链状
肽链
又称
相互结合形成
盘曲、折叠
蛋白质
Mr>10000
具有一定的空间结构
一、氨基酸
(1)定义:蛋白质是由多种氨基酸通过肽键等相互连接形成的一类生物大分子。
(2)组成: 蛋白质中主要含有C、H、O、N、S等元素,有些蛋白质还含有
P、Fe、Zn、Cu等元素,属于天然有机高分子。其溶液具有胶
体的某些性质。
人体内所具有的蛋白质种类达到了10万种以上。那它们具有什么样的空间结构呢?
1.蛋白质的定义、组成与存在
—— 四级空间结构
→ 各种蛋白质都有其特殊功能和活性
2.蛋白质的结构
(3)存在:
蛋白质主要存在于生物体内,如肌肉、毛发、皮肤、角、酶、抗体、病毒等;在植物中也很丰富,如大豆、花生、谷物。
二、蛋白质
例如,血红蛋白分子中的________会因遗传因素变成________,这一微小差别会导致红细胞的形态由正常的圆饼状变为异常的镰刀状,使人患镰状细胞贫血。
蛋白质分子中氨基酸单体的排列顺序
一级结构是蛋白质高级结构的基础,对蛋白质的性质和功能起着决定性作用
谷氨酸
缬氨酸
二、蛋白质
肽键中的氧原子与氢原子之间存在氢键,会使肽链盘绕或折叠成特定的空间结构
一级结构
二级结构
蛋白质一级结构怎么组成?有什么意义?二级结构又是怎么组成的?
3.蛋白质的化学性质
蛋白质分子中两端的氨基和羧基说明什么?
(1)蛋白质具有两性:能与酸碱反应
二、蛋白质
(2)水解反应
在酸、碱或酶作用下,逐步水解成相对分子质量较小的_____,最终水解得到________。
多肽
氨基酸
二、蛋白质
食物中的蛋白质在人体内各种蛋白酶的作用下水解成氨基酸,氨基酸被肠壁吸收进入血液,再在体内重新合成人体所需要的蛋白质。
水解断键特点:碳加羟基,氮加氢
二、蛋白质
振荡
白色沉淀
加水
沉淀溶解
饱和(NH4)2SO4溶液
—鸡蛋清溶液
原理:
少量的某些可溶性盐(如硫酸铵、硫酸钠、氯化钠等)能促进蛋白质的溶解。但当这些盐在蛋白质溶液中达到一定浓度时,反而使蛋白质的溶解度降低而使其从溶液中析出,这种作用称为盐析。
特点:
蛋白质的盐析是一个可逆过程,盐析出的蛋白质在水中仍能溶解,并不影响其活性。属于物理变化过程。
应用:
采用多次盐析和溶解,可以分离提纯蛋白质。
(3)盐析
二、蛋白质
振荡
白色沉淀
加水
沉淀不溶解
酒精
—鸡蛋清溶液
概 念
影响因素 物理
化学
特 点 变性会使蛋白质的结构发生变化,使其失去原有的__________,
在水中不能重新溶解,是 过程
应 用
在某些物理或化学因素的影响下,蛋白质的性质和生理功能发生改变的现象
加热、加压、搅拌、振荡、紫外线和放射线、超声波等
强酸、强碱、重金属盐、乙醇、甲醛、丙酮等
不可逆
生理活性
杀菌、消毒、防中毒
(4)变性
二、蛋白质
二、蛋白质
【思考与讨论 】
(1)因误服铅、汞等重金属盐中毒的患者在急救时,为什么可口服牛奶、
蛋清或豆浆?
(2)为什么紫外线可用于环境和物品消毒,放射线可用于医疗器械灭菌?
(3)鸡、鱼、肉、蛋等蛋白质食品做熟食用的原理是什么?
牛奶、蛋清、豆浆中含大量的蛋白质,让铅、汞等重金属盐使他们变性,减少对人体伤害。
紫外线、放射线能使病毒、细菌蛋白蛋变性而灭活。
高温使蛋白质的空间结构变得伸展、松散,易于水解,便于吸收
振荡
白色沉淀
加热
沉淀变黄色
浓硝酸
—鸡蛋清溶液
蛋白质变性
含有苯环的蛋白质均能发生这个反应
固体蛋白质如皮肤、指甲遇浓硝酸变______色。
黄
其他一些试剂也可以与蛋白质作用,呈现特定颜色
可用于蛋白质的分析检测
(5)显色反应
二、蛋白质
其他鉴别方法:
燃烧产生烧焦羽毛的气味。
阅读P117-118科学史话和资料卡片,思考与交流
1、烫发的原理是什么?
2、人们对蛋白质结构、性质和功能的研究有什么意义
二、蛋白质
头发主要由角蛋白组成,二硫键(-S-S-)是维持头发弹性和形状的一个重要结构。烫发时使用的还原剂可以使头发中的二硫键断裂,产生游离的巯基(-SH )。定型后再用氧化剂使巯基之间发生反应,生成新的二硫键,使头发的形状得以固定。频繁烫发会对头发造成一定程度的损害。
人们对蛋白质结构、性质和功能的研究,为蛋白质的合成与应用奠定了基础。蛋白质
的人工合成,不仅为生命起源的化学途径提供了有力的证据,而且可以为人们提供性能
优异的药物和生物催化剂,对探索生命活动规律、促进人类健康具有重要意义。
蛋白质社会价值:
从2020年2月初疫苗项目立项,到当年12月30日,国药集团中国生物的新冠病毒灭活疫苗成为我国首个获批附条件上市的新冠疫苗,98天研发出新冠灭活疫苗,335天实现上市——正是无数相关工作人员不舍昼夜,与时间赛跑,才得以创造出疫苗研发的“中国速度”。
二、蛋白质
1.下列过程中,不可逆的是( )
A.蛋白质的盐析 B.酯的水解 C.蛋白质白变性 D.氯化铁的水解
2.欲将蛋白质从水中析出而又不改变它的性质应加入( )
A.甲醛溶液 B.CuSO4溶液 C.饱和Na2SO4溶液 D.浓硫酸
C
C
3.关于蛋白质的叙述错误的是( )
A.浓HNO3溅在皮肤上,使皮肤呈黄色,是由于浓HNO3和蛋白质发生了颜色反应
B.蛋白质溶液中加入饱和(NH4)2SO4溶液,蛋白质析出,再加水也不溶解
C.蛋白质水解的最终产物是氨基酸
D.高温灭菌的原理是加热后使蛋白质变性,从而使细菌死亡
B
学以致用
二、蛋白质
三、酶
在酶的作用下,生物才能进行新陈代谢,完成消化、呼吸、运动、生长、发育、繁殖等生命活动。
2.功能:
酶是一类由细胞产生的、对生物体内的化学反应具有催化作用的有机化合物,其中绝大多数是蛋白质。
1.定义:
阅读课文P115,思考酶的定义与功能
观察超效加酶洗衣粉使用说明,思考酶的特性
(1)高度的专一性. (一种酶只催化一种反应)
(2)高效性. (比普通催化剂高107)
(3)条件温和, 不需加热.
(一般在接近体温和中性的条件下进行,此时酶的
活性最高。超过适宜的温度时,酶将失去活性)
新冠病毒主要蛋白酶结构
3.酶催化作用有什么特点
目前,酶已经得到了广泛的应用,如蛋白酶用于医药、制革等工业,
淀粉酶用于食品、发酵、纺织等工业,有的酶还可用于疾病的诊断。
4.酶的应用:
三、酶
B
三、酶
学以致用
1.下列有关酶的说法中错误的是( )
A.大多数酶是具有催化作用的蛋白质
B.酶的催化作用具有高效性和专一性
C.高温或重金属盐能使大多数酶失去活性
D.酶只有在强酸、强碱条件下才能发挥作用
2.市场上有一种加酶洗衣粉,即在洗衣粉中加入少量的碱性蛋白酶,它的催化活性很强,衣服上的汗渍、血迹及人体排出的蛋白质、油渍遇到它,皆能水解而除去。下列衣料不能用加酶洗衣粉洗涤的是( )
①棉织品 ②羊毛织品 ③腈纶织品
④蚕丝织品 ⑤涤纶织品 ⑥锦纶织品
A.①②③ B.②④ C.③④⑤ D.③⑤⑥
D
二、蛋白质
作业
1、分层检测
2、限时过关卷
感谢观看
