专题4《分子空间结构与物质性质》练习题(含解析)2022-2023学年下学期高二化学苏教版(2019)选择性必修2
文档属性
| 名称 | 专题4《分子空间结构与物质性质》练习题(含解析)2022-2023学年下学期高二化学苏教版(2019)选择性必修2 |

|
|
| 格式 | docx | ||
| 文件大小 | 691.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-30 00:00:00 | ||
图片预览




文档简介
专题4《分子空间结构与物质性质》练习题
一、单选题
1.共价键、离子键和范德华力都是微粒间的作用力,下列物质:①Na2O2;②SiO2;③石墨;④金刚石;⑤CaCl2;⑥白磷,含有上述结合力中的两种的组合是
A.①③⑤⑥ B.①③⑥ C.②④⑥ D.①②③⑥
2.物质M的组成为CoCl3 4NH3,以强碱处理并没有NH3放出;向1molM中加入足量AgNO3溶液生成1mol白色沉淀。下列说法不正确的是
A.该配合物的配体是Cl-和NH3 B.该配合物可表示为[Co(NH3)4Cl2]Cl
C.M中的配离子可能是平面正方形 D.该配合物中心离子的电荷数为3,配位数为6
3.下列分子的空间结构为正四面体形的是
①P4;②NH3;③CCl4;④CH4;⑤H2S;⑥CO2
A.①③④⑤ B.①③④⑤⑥ C.①③④ D.②④⑤
4.下列说法不正确的是
A.水玻璃浸渍过的棉麻布不容易点燃,常以此法处理电影银幕
B.人造棉、人造丝的主要成分都是纤维素
C.氢键在形成蛋白质二级结构和DNA双螺旋结构中起关键作用
D.在燃煤中添加石膏能减少酸雨的产生
5.下列叙述正确的是
①冰中存在极性共价键和氢键两种化学键的作用
②C60晶体的晶胞是面心立方结构
③As是ⅤA族的一个主族元素,其外围电子排布式为4s24p3,属于p区元素
④熔融状态的HgCl2不能导电,HgCl2的稀溶液有弱的导电能力且可作手术刀的消毒液,从不同角度分类HgCl2是一种共价化合物、非电解质、盐、分子晶体
A.①② B.②③ C.①③ D.②④
6.氨分子中,两个N-H键的键角是
A.90o B.107o C.109o28 D.120°
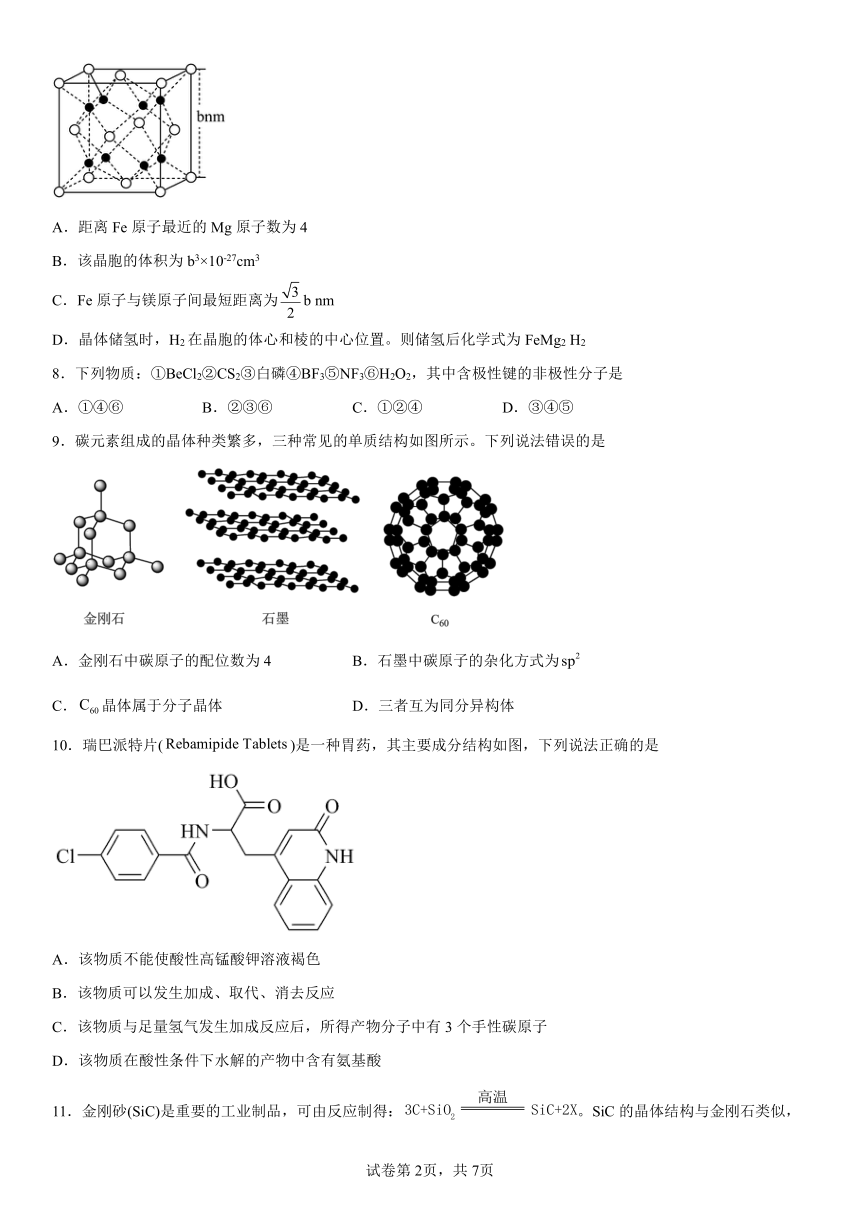
7.铁与镁组成的储氢合金的立方晶胞结构如图所示。铁原子位于顶点和面心的位置,镁原子位于将晶胞平分为8个立方单位的体心位置。下列说法正确的是
A.距离Fe原子最近的Mg原子数为4
B.该晶胞的体积为b3×10-27cm3
C.Fe原子与镁原子间最短距离为b nm
D.晶体储氢时,H2在晶胞的体心和棱的中心位置。则储氢后化学式为FeMg2 H2
8.下列物质:①BeCl2②CS2③白磷④BF3⑤NF3⑥H2O2,其中含极性键的非极性分子是
A.①④⑥ B.②③⑥ C.①②④ D.③④⑤
9.碳元素组成的晶体种类繁多,三种常见的单质结构如图所示。下列说法错误的是
A.金刚石中碳原子的配位数为4 B.石墨中碳原子的杂化方式为
C.晶体属于分子晶体 D.三者互为同分异构体
10.瑞巴派特片()是一种胃药,其主要成分结构如图,下列说法正确的是
A.该物质不能使酸性高锰酸钾溶液褐色
B.该物质可以发生加成、取代、消去反应
C.该物质与足量氢气发生加成反应后,所得产物分子中有3个手性碳原子
D.该物质在酸性条件下水解的产物中含有氨基酸
11.金刚砂(SiC)是重要的工业制品,可由反应制得:。SiC的晶体结构与金刚石类似,如图所示。下列说法错误的是
A.Si属于p区元素,在SiC中的化合价为+4价
B.X可与氧气反应生成Y,Y分子的中心原子杂化方式为sp杂化
C.金刚石熔点比SiC晶体熔点高
D.已知Si-C键键能为akJ/mol,则理论上分解1molSiC形成气态原子需要的能量为akJ
12.NF3是一种优良的蚀刻气体。HF、F2均可用于制备NF3,F2制备NF3的反应为4NH3+3F2NF3+3NH4F。Ka(HF)=6.3×10 4,Kb(NH3·H2O)=1.8×10 5。下列关于氨和铵盐的说法正确的是
A.氨气易溶于水,是因为氨分子间能形成氢键
B.HF酸性强,所以不能用玻璃瓶盛装
C.25℃,0.1 mol·L 1 NH4F溶液的pH<7
D.25℃,NH3与HNO3反应生成N2和H2O
13.下列各组微粒的空间结构相同的是
①和;②和;③和;④和
A.①②③④ B.①②④ C.①③④ D.②④
二、填空题
14.(1)是有机合成中常用的还原剂,中的阴离子空间构型是_______,中心原子的杂化形式为_______。
(2)根据价层电子对互斥理论,、、的气态分子中,中心原子价层电子对数不同于其他分子的是_______。
(3)《中华本草》等中医典籍中,记载了炉甘石入药,可用于治疗皮肤炎症或表面创伤.中,阴离子空间构型为_______,C原子的杂化形式为_______。
(4) X射线衍射测定等发现,中存在离子,离子的几何构型为_______,中心原子的杂化形式为_______。
15.氮是地球上极为丰富的元素。
(1)中N以形式存在,基态的电子排布式为______。
(2)为三角锥形分子,键键能的含义是______(填字母)。
A.由N和H形成所放出的能量
B.把中的共价键全部拆开所吸收的能量
C.拆开约个键所吸收的能量
D.形成1个键所放出的能量
(3)键的键能为,键的键能为,计算说明中的______(填“”或“”,下同)键比______键稳定。
(4)已知:,,,。计算反应的反应热______。
16.判断下列物质熔沸点高低(填>或<):
(1)_______
(2)_______
(3)_______
(4)异戊烷_______新戊烷
(5)_______
(6) _______
17.磷化铝(AlP)和磷化氢(PH3)都是粮食储备常用的高效熏蒸杀虫剂。
(1)磷元素在元素周期表中的位置:_______,AlP遇水蒸气会发生反应放出PH3气体,PH3中的P原子的杂化方式为_______杂化,该反应的另一种产物的化学式为_______。
(2)具有强还原性,能与溶液反应,配平该反应的化学方程式:_______。
(3)工业制备的流程如图所示。
① 次磷酸属于_______元酸。
② 白磷和烧碱溶液反应的化学方程式为:_______。
③ 若起始时有1 mol P4参加反应,则整个工业流程中共生成_______mol (不考虑产物损失)
18.溶质在溶剂中的溶解度取决于多种因素,请回答下列问题:
(1)实验发现:CH4极难溶于水,而HF极易溶于水,其原因是_______。
(2)通常条件下,1体积的水可溶解700体积的NH3,请说明三点理由:_______。
19.回答下列问题:
(1)三价铬离子能形成多种配位化合物。中提供电子对形成配位键的原子是___________,中心离子的配位数为___________。
(2)与N-甲基咪唑()反应可以得到,其结构如图所示:
N-甲基咪唑分子中碳原子的杂化轨道类型为___________,1个中含有___________个键。
20.实验室制备溴代烃的反应如下: ①
②
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br-被浓硫酸氧化为Br2等。有关数据列表如下;
乙醇 溴乙烷 正丁醇 1-溴丁烷
密度/g·cm-3 0.7893 1.4604 0.8098 1.2758
沸点/℃ 78.5 38.4 117.2 101.6
请回答下列问题:
(1)在溴乙烷和1-溴丁烷的制备实验中,下列仪器最不可能用到的是______ 。
a.圆底烧瓶 b. 容量瓶 c.锥形瓶 d.量筒
(2)溴代烃的水溶性 _____(填“大于”、“等于”或“小于”)相应的醇;其原因是___________________________ 。
(3)将1-溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在________(填“上层”、“下层”或“不分层”)。
(4)制备操作中,加入的浓硫酸必须进行稀释,其目的不正确的是___________。
a. 水是反应的催化剂 b.减少的生成
c.减少HBr的挥发 d. 减少副产物烯和醚的生成
(5)在制备溴乙烷时,采用边反应边蒸出产物的方法,其原因是_____________ ;但在制备1-溴丁烷时却不能边反应边蒸出产物,其原因是______________________________。
21.回答下列问题:
(1)化合物III也是一种汞解毒剂。化合物IV是一种强酸。下列说法正确的有_____。
A.在I中S原子采取sp3杂化
B.在II中S元素的电负性最大
C.在III中C-C-C键角是180°
D.在III中存在离子键与共价键
E.在IV中硫氧键的键能均相等
(2)汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。化合物I与化合物III相比,水溶性较好的是_____。
(3)NH3、PH3、AsH3分子的键角分别为107.3°、93.3°、91.8°,其键角逐渐减小的原因是____。
(4)中含有各元素的电负性由小到大的顺序为____;该物质中,含有σ键和π键数目之比为____。
(5)在CO分子中每个原子均为8电子稳定结构,则C与O之间形成_____个σ键____个π键,在这些化学键中,O原子共提供了____个电子。
(6)乙腈(CH3CN)分子中碳原子的杂化类型有____,与N同周期的主族元素中,第一电离能大于N的有_____种,写出一种与N互为等电子体的分子的化学式_____,NO离子的立体构型是____。
(7)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据列于表:
元素 Mn Fe
电离能/kJ mol-1 I1 717 759
I2 1509 1561
I3 3248 2957
锰元素位于第四周期第VIIB族。请写出基态Mn2+的价电子排布式:_____,比较两元素的I2、I3可知,气态Mn2+再失去1个电子比气态Fe2+再失去1个电子难,对此你的解释是_____。
22.按要求完成下列填空:
(1)有以下8种分子:①HF,②Cl2,③H2O,④N2,⑤C2H4,⑥C2H6,⑦H2O2,⑧HCN(H-C≡N),其中只有含有σ键的是__________________(填序号);既含有σ键,又含有π键的是__________________(填序号)。
(2)X、Y、Z是元素周期表中的短周期元素,其中X、Y同周期,Y、Z同主族,Y原子最外层p轨道上的电子数等于前一电子层电子总数,X原子最外层的p能级中只有一个轨道填充了2个电子,而且这三种元素可以形成化合物YX2、ZX2。根据上述信息回答下列问题:
a.写出下列元素符号:X______,Y______,Z______。
b.YX2分子中含_______个σ键,含_______个π键。
23.铬、铁、镍、铜等金属及其化合物在工业上有重要用途。
(1)基态铬原子的电子排布式为____。
(2)CrO2Cl2和NaClO均可作化工生产的氧化剂或氯化剂。制备CrO2Cl2的反应为K2Cr2O7+3CCl4=2KC1+2CrO2Cl2+3COCl2↑。
①上述反应式中非金属元素电负性由大到小的顺序是____(用元素符号表示)。
②常温下CrO2Cl2是一种易溶于CCl4的液体,则固态CrO2Cl2属于____晶体。
③COCl2分子中所有原子均满足8电子结构,则COCl2分子中σ键和π键的个数比为____。
④CuCl的盐酸溶液能吸收CO生成复合物氯化羰基亚铜[Cu2Cl2(CO)2·2H2O],其结构如图所示。
下列说法不正确的是____(填字母序号)。
A.该复合物中只含有离子键和配位键
B.该复合物中Cl原子的杂化类型为sp3
C.该复合物中只有CO和H2O作为配位体
D.该溶液中滴入硝酸酸化的硝酸银不产生沉淀
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
【详解】①Na2O2是离子化合物,含有离子键、非极性共价键,正确;
②SiO2是原子晶体,只含有极性共价键,错误;
③石墨是混合型晶体,层内含有非极性共价键,层间含有分子间作用力,正确;
④金刚石是原子晶体,只含有非极性共价键,错误;
⑤CaCl2是离子晶体,只含有离子键,错误;
⑥白磷是分子晶体,分子间含有分子间作用力,分子内含有非极性共价键,正确。
含有上述结合力中的两种的组合是①③⑥,选项是B。
2.C
【分析】其水溶液显弱酸性,说明界外没有氨分子,向1molM中加入足量AgNO3溶液生成1mol白色沉淀,说明三个氯离子1个位于外界,所以该配合物的化学式最可能为[Co(NH3)4Cl2]Cl。
【详解】A.配合物的化学式最可能为[Co(NH3)4Cl2]Cl,该配合物的配体是Cl-和NH3,故A正确;
B.根据分析可得,该配合物可表示为[Co(NH3)4Cl2]Cl,故B正确;
C.M中的配位数为6,故配离子不可能是平面正方形,故C错误;
D.该配合物中心离子的电荷数为+3,配位数为6,故D正确;
故选C。
3.C
【详解】①P4由4个P构成正四面体构型;
②NH3的空间结构是三角锥形;
③CCl4由4个Cl构成正四面体构型;
④CH4由4个H构成正四面体构型;
⑤H2S的空间结构是V形;
⑥CO2的空间结构是直线形;
故选C。
4.D
【详解】A.水玻璃是硅酸钠溶液,硅酸钠不燃烧、不支持燃烧,所以电影银幕用水玻璃浸泡的主要目的是为了防火,故A正确;
B.人造棉、人造丝的主要成分都是纤维素,故B正确;
C.氢键对维持生物大分子的空间构型和生理活性具有重要意义,所以氢键在形成蛋白质二级结构和DNA双螺旋结构中起关键作用,故C正确;
D.石膏的主要成分是硫酸钙,燃煤中添加石膏不能减少SO2的排放,不能达到减少酸雨的目的,故D错误。
答案选D。
5.B
【详解】①氢键不是化学键,错误;
②在C60晶体的晶胞中,在晶胞的顶点和面心上各有一个C60分子,是面心立方结构,正确;
③As是ⅤA族的一个主族元素,其外围电子排布式为4s24p3,属于p区元素,正确;
④HgCl2的稀溶液有弱的导电能力,说明其属于电解质,错误;
②③正确,故选B。
6.B
【详解】氨分子中,N原子的价层电子数为 ,N采取sp3杂化,有一对孤电子对,氨气为三角锥形,孤电子对—成键电子对的斥力大于成键电子对—成键电子对的斥力,N-H键的键角为107°,略小于正四面体构型的键角109o28′,故选B。
7.D
【详解】A.由晶胞结构可知,位于顶点的铁原子与位于体对角线上镁原子的距离最近,则铁原子的配位数为8,故A错误;
B.由晶胞结构可知晶胞参数为bnm,则该晶胞体积为:b3×10-21cm3,故B错误;
C.由晶胞结构可知,位于顶点的铁原子与镁原子的距离为体对角线的,则铁原子与镁原子间最短距离为b nm,故C错误;
D.由晶胞结构可知,晶胞中位于顶点和面心的铁原子个数为8×+6×=4,位于体内的镁原子个数为8,位于体心和棱的中心位置的氢分子个数为12×+1=4,氢后化学式为FeMg2H2,故D正确;
故选D。
8.C
【详解】①BeCl2中含有极性键,为直线形分子,其结构对称,正、负电荷的中心重合,为非极性分子,①符合题意;
②CS2中含有C=S极性键,为直线形分子,其结构对称,正、负电荷的中心重合,为非极性分子,②符合题意;
③P4为单质,分子中只含有非极性键,为非极性分子,③不符合题意;
④BF3中含有极性键,为平面三角形分子,正、负电荷的中心重合,为非极性分子,④符合题意;
⑤NF3中含有极性键,为三角锥形分子,正、负电荷的中心不重合,为极性分子,⑤不符合题意;
⑥H2O2中含有极性键,但氧原子上有孤电子对,其结构不对称,正、负电荷的中心不重合,为极性分子,⑥不符合题意;
综上所述①②④符合题意;
故选C。
9.D
【详解】A. 由金刚石的结构图可知,金刚石中每个碳原子周期连接4个碳原子,故碳原子的配位数为4,故A正确;
B. 石墨的每一层呈平面结构,每个碳原子连接3个碳原子,价层电子对数为3,碳原子的杂化方式为,故B正确;
C. 晶体属于分子晶体,故C正确;
D. 金刚石和石墨没有分子,三者不互为同分异构体,而是由C元素组成的不同单质,互为同素异形体,故D错误;
故选D。
10.D
【详解】A.含碳碳双键,可被高锰酸钾氧化,则能使酸性高锰酸钾溶液褪色,故A错误;
B.含有苯环,能发生加成反应和取代反应,苯环上的氯原子不能发生消去反应,故B错误;
C.该物质与足量氢气发生加成反应后,所得产物分子中有4个手性碳原子(),故C错误;
D.由结构可知含肽键,则该物质能水解,且水解产物中含有氨基酸,故D正确;
故选D。
11.D
【详解】A.Si位于第三周期ⅣA族,属于p区,电负性Si<C,所以SiC中Si元素的化合价为+4价,A正确;
B.根据原子守恒可知X为CO,CO与氧气反应生成的Y为CO2,CO2分子中中心C原子的价层电子对数为=2,为sp杂化,B正确;
C.碳原子半径小于硅原子半径,则碳碳键键能大于碳硅键键能,导致金刚石熔点比SiC晶体熔点高,C正确;
D.据图可知每个Si原子形成4个Si-C键,所以1molSiC中含有4molSi-C键,分解1molSiC形成气态原子需要的能量为4akJ,D错误;
综上所述答案为D。
12.C
【详解】A.氨气易溶于水,是因为氨气分子和水分子间能形成氢键,A错误;
B.HF为弱酸,不能用玻璃瓶盛装是因为HF会和二氧化硅反应,B错误;
C.HF的电离平衡常数大于NH3·H2O,所以NH的水解程度大于F-,0.1 mol·L 1 NH4F溶液显酸性,pH<7,C正确;
D.25 ℃,NH3与HNO3反应生成硝酸铵,D错误;
综上所述答案为C。
13.C
【详解】
微粒 中心原子上的孤电子对数 中心原子上的价层电子对数 空间结构
① 2 直线形
2 直线形
② 2 直线形
4 V形
③ 3 V形
3 V形
④ 4 正四面体形
4 正四面体形
综合以上分析,①③④符合题意,故答案选C。
14. 正四面体 平面三角形 V形
【详解】(1)中的阴离子是,中心原子铝原子的价层电子对数是4,且不存在孤电子对,所以其空间构型是正四面体;中心原子的杂化轨道类型是杂化;
(2)根据价层电子对互斥模型可知,、、的气态分子中,中心原子价层电子对数分别是、、,因此中心原子价层电子对数不同于其他分子的是;
(3)碳酸锌中的阴离子为,根据价层电子对互斥模型,其中心C原子的价层电子对数为,不含孤电子对,所以其空间构型为平面三角形,C原子为杂化;
(4)的中心I原子形成2个键,孤电子对数为,即中心I原子形成2个键,还有2个孤电子对,故的几何构型为V形;中心I原子采取杂化。
15. C π -456
【详解】(1)基态N原子的电子排布式为,得到3个电子转化为,故基态的电子排布式为。
(2)键的键能是指形成键放出的能量或拆开键所吸收的能量,不是指形成1个键释放的能量。分子中含有键,拆开或形成吸收或放出的能量应是键键能的3倍。
(3)键中有两个π键和一个键,而键为键,键能为,键的键能为,则键的键能大于键键能的3倍,故中键的稳定性比π键弱。
(4)
。
16.(1)<
(2)<
(3)>
(4)>
(5)<
(6)<
【解析】(1)
金属晶体中金属原子的价电子数越多,原子半径就越小,金属阳离子与自由电子的静电作用越强,金属键越强,熔沸点越高,故熔沸点Mg(2)
离子晶体的熔沸点是根据离子所带的电荷数和离子半径来比较的,离子所带的电荷数越高,离子的半径就越小,则该离子的熔沸点就越高,氧化镁中阴阳离子所带电荷数多,离子半径而且小,所以熔沸点NaCl(3)
水和硫化氢是同族元素形成的氢化物,但因为水中存在氢键使水的熔沸点升高,所以熔沸点H2O>H2S,故答案为:>;
(4)
异戊烷和新戊烷是同分异构体,支链越多熔沸点越低,所以熔沸点是异戊烷>新戊烷,故答案为:>;
(5)
组成和结构相似的分子晶体,相对分子质量越大,熔沸点越高,所以<,故答案为:<;
(6)
对羟基苯甲醛形成分子间氢键使溶沸点升高,而邻羟基苯甲醛形成的是分子内氢键 ,对羟基苯甲醛的溶沸点高于邻羟基苯甲醛,故熔沸点<,故答案为:<。
17.(1) 第三周期第VA族 sp3 Al(OH)3
(2)24,11,12=8,3,24
(3) 一 P4 +3NaOH + 3H2O =PH3 + 3NaH2PO2 2.5mol
【详解】(1)P处于第三周期ⅤA族,AlP遇水蒸气会发生反应放出PH3气体,PH3中的P原子的杂化方式为sp3,根据元素守恒,确定该反应的另一种产物是Al(OH)3,故答案为:第三周期第VA族;sp3;Al(OH)3;
(2)该方程式中Cu价态由+2下降为+1,P价态由-3升高为+5,为保证化合价升降数相等,Cu3P与H3PO4计量数分别为8、3,CuSO4的系数是24,H2SO4系数是24,根据元素守恒,得到:,故答案为:24,11,12,8,3,24;
(3)①根据氢氧化钠过量时只能生成NaH2PO2可知次磷酸只能电离出1个氢离子,因此次磷酸属于一元酸,故答案为:一;
②根据图示信息:白磷和烧碱溶液反应生成PH3、NaH2PO2,方程式为:;故答案为:;
③P4+3NaOH+3H2O=PH3↑+3NaH2PO2;2H3PO2=PH3↑+H3PO4,即P4~2.5PH3,若起始时有1molP4参加反应,则整个工业流程中共生成2.5molPH3;故答案为:2.5。
18.(1)CH4是非极性分子,水是极性溶剂,所以CH4极难溶于水;HF是极性分子且能与水分子形成氢键,所以HF极易溶于水
(2)NH3与H2O均为极性分子;NH3与H2O分子间易形成氢键;NH3与H2O易反应生成
【解析】(1)
的空间构型为正四面体、是非极性分子,而的空间构型为V形、是极性分子,的空间构型为直线型,只含H-F极性键,是极性分子,依据相似相溶原理,CH4极难溶于水,HF极易溶于水,且能与水分子形成分子间氢键。
(2)
的空间构型为V形、是极性分子,NH3的空间构型为三角锥形,是极性分子,依据相似相溶原理,NH3极易溶于水,N、O的电负性大,NH3可与H2O形成分子间氢键,使得NH3极易溶于水,NH3能与H2O反应生成,增大了NH3在H2O中的溶解度。
19.(1) N、O、Cl 6
(2) 、 54
【解析】(1)
中的氧原子、中的氮原子和中都有孤电子对,可作配位原子,故配位原子为O、N、Cl;
中心离子的配位数为。
(2)
由结构可知,N-甲基咪唑含有甲基和碳碳双键,则该分子中碳原子的杂化轨道类型为、;
1个N-甲基咪唑中含有6个键、4个键、1个碳碳双键和1个碳氮双键,单键、配位键属于键,1个双键中有1个O键和1个键,所以1个中含有个键。
20.(1)b
(2) 小于 醇可与水分子之间形成氢键,溴代烃不能与水分子之间形成氢键
(3)下层
(4)a
(5) 平衡向生成溴乙烷的方向移动(或反应②向右移动) 1-溴丁烷与正丁醇的沸点差较小,若边反应边蒸馏,会有较多的正丁醇被蒸出
【详解】(1)容量瓶用于一定物质的量浓度溶液的配制,在该实验中最不可能用到,答案选b;
(2)醇可与水分子之间形成氢键,溴代烃不能与水分子之间形成氢键,所以溴代烃的水溶性小于相应醇的水溶性;
(3)根据表中数据可知,1-溴丁烷的密度大于水的密度,因此将1-溴丁烷的粗产品置于分液漏斗中加水,振荡后静止,产物即1-溴丁烷应在下层;
(4)由于加入的浓硫酸在稀释时放出大量的热且具有强氧化性,因此在准备操作过程中,加入的浓硫酸必须进行稀释,其目的就是防止放热导致副产物烯和醚的生成并减小HBr的挥发,同时也减少的生成,即答案选a;
(5)根据平衡移动原理,蒸出产物平衡相有利于生成溴乙烷的方向移动;在准备1-溴丁烷时不能采取此方法,原因是1-溴丁烷与正丁醇的沸点相差较小,如果边反应边蒸,会有较多的正丁醇被蒸出。
21.(1)AD
(2)化合物III
(3)中心原子电负性越大,相应的键角就越大
(4) H(5) 1 2 4
(6) sp3、sp 1 N2O或CO2 平面三角形
(7) 3d5 Mn2+价电子排布为3d5,处于半满状态,能量比较低,再失去一个电子需要的能量较大
【详解】(1)A.中S原子的价层电子对数=2+=4,因此S原子采取sp3杂化,故A正确;
B.中含有的元素为H、C、O、S、Hg,同周期元素从左至右元素的电负性逐渐增大,同主族元素从上至下元素的电负性逐渐减小,因此5种元素中电负性最大的为O元素,故B错误;
C.中C原子成键均为单键,因此C原子采取sp3杂化,所以C-C-C键角接近109 28’,故C错误;
D.中存在C-H、C-C、C-S、S=O、S-O、S-H共价键和 与Na+之间的离子键,故D正确;
E.在Ⅳ中存在硫氧单键和硫氧双键,硫氧键的键能不相等,故E错误;
正确答案选AD。
(2)中羟基能与水分子之间形成分子间氢键,为易溶于水的钠盐,溶于水后电离出的 中O原子均能与水分子之间形成氢键,相同物质的量两种物质溶于水后, 形成的氢键更多,因此化合物III更易溶于水。
(3)NH3、PH3、AsH3分子均为三角锥形,结构相似,中心原子电负性越大,中心原子周围电子云密度越大,化学键之间的相互排斥作用越大,相应的键角就越大,而三者电负性大小顺序是:N>P>As,所以NH3、PH3、AsH3键角依次减小。
(4)中含有C、N、O、H,各元素的电负性由小到大的顺序为H(5)在CO分子中,C与O之间形成碳氧叁键,存在1个σ键、2个π键,在这些化学键中,π键由氧原子提供孤电子对、碳提供空轨道,O原子共提供了4个电子。
(6)乙腈(CH3CN)分子的结构简式为:,根据形成4个单键判断杂化类型是,成三键判断是sp杂化,故答案为:、sp;与N同周期的主族元素中,第一电离能大于N的有F元素,按洪特规则氮元素处于半充满状态稳定,比氧元素的电离能大;根据原子数相等、价电子数也相等的微粒互为等电子体进行判断与N互为等电子体的分子的化学式N2O或CO2;NO离子的立体构型根据价层电子对互斥理论进行判断中心原子N采用sp2杂化,且形成三个共价键,故为平面三角形。
(7)锰元素位于第四周期第Ⅶ B族,则Mn原子的价电子排布式为3d54s2,则Mn2+的价电子排布式为3d5;Fe为26号元素,Fe原子的价电子排布式为3d64s2,Fe2+的价电子排布式为3d6,由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态需要的能量较多;而Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态需要的能量相对要少,所以气态Mn2+再失去1个电子比气态Fe2+再失去1个电子难,故答案为:由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态需吸收能量。
22. ①②③④⑤⑥⑦ ④⑤⑧ O C Si 2 2
【分析】多原子分子中都有σ键,含有双键、叁键或苯环的物质既有σ键又有π键。
X、Y、Z是元素周期表中的短周期元素,其中X、Y同周期,Y、Z同主族,Y原子最外层p轨道上的电子数等于前一电子层电子总数,则Y为C元素;X原子最外层的p能级中只有一个轨道填充了2个电子,则该p轨道有4个电子,而且这三种元素可以形成化合物YX2、ZX2,则X为O元素,Z为Si元素。
【详解】(1)①HF,②Cl2,③H2O,④N2,⑤C2H4,⑥C2H6,⑦H2O2,⑧HCN(H-C≡N),其中只含有σ键的是①②③④⑤⑥⑦;乙烯分子中有碳碳双键,氮气分子和HCN中都有叁键,故既含有σ键、又含有π键的是④⑤⑧。
(2)a.X、Y、Z元素的符号分别是O、C、Si。
b.CO2分子的结构式为O=C=O,故其中含2个σ键,含2个π键。
23.(1)1s22s22p63s23p63d54s1
(2) O>Cl>C 分子 3:1 AC
【解析】(1)
基态铬原子的电子排布式为1s22s22p63s23p63d54s1,故答案为:1s22s22p63s23p63d54s1;
(2)
①反应式中非金属元素有O、C、Cl,它们的电负性由大到小顺序为O>Cl>C,故答案为:O>Cl>C;
②分子晶体熔沸点较低,该物质的熔沸点较低,所以为分子晶体,故答案为:分子;
③COCl2分子中有1个C=O键和2个C-Cl键,所以COCl2分子中σ键的数目为3,π键的数目为1,个数比3:1,故答案为:3:1;
④A.该复合物中存在化学键类型有离子键、配位键、极性共价键等,故A错误;
B.该复合物中Cl原子形成2个σ键,还含有2个未成键电子对,其杂化类型为sp3,故B正确;
C.该复合物中配位体有CO、H2O和Cl原子,故C错误;
D.Cu2Cl2(CO)2·2H2O 中Cl原子是配原子,在溶液中不存在Cl-,则滴入硝酸酸化的硝酸银不产生沉淀,故D正确;
故答案为:AC。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.共价键、离子键和范德华力都是微粒间的作用力,下列物质:①Na2O2;②SiO2;③石墨;④金刚石;⑤CaCl2;⑥白磷,含有上述结合力中的两种的组合是
A.①③⑤⑥ B.①③⑥ C.②④⑥ D.①②③⑥
2.物质M的组成为CoCl3 4NH3,以强碱处理并没有NH3放出;向1molM中加入足量AgNO3溶液生成1mol白色沉淀。下列说法不正确的是
A.该配合物的配体是Cl-和NH3 B.该配合物可表示为[Co(NH3)4Cl2]Cl
C.M中的配离子可能是平面正方形 D.该配合物中心离子的电荷数为3,配位数为6
3.下列分子的空间结构为正四面体形的是
①P4;②NH3;③CCl4;④CH4;⑤H2S;⑥CO2
A.①③④⑤ B.①③④⑤⑥ C.①③④ D.②④⑤
4.下列说法不正确的是
A.水玻璃浸渍过的棉麻布不容易点燃,常以此法处理电影银幕
B.人造棉、人造丝的主要成分都是纤维素
C.氢键在形成蛋白质二级结构和DNA双螺旋结构中起关键作用
D.在燃煤中添加石膏能减少酸雨的产生
5.下列叙述正确的是
①冰中存在极性共价键和氢键两种化学键的作用
②C60晶体的晶胞是面心立方结构
③As是ⅤA族的一个主族元素,其外围电子排布式为4s24p3,属于p区元素
④熔融状态的HgCl2不能导电,HgCl2的稀溶液有弱的导电能力且可作手术刀的消毒液,从不同角度分类HgCl2是一种共价化合物、非电解质、盐、分子晶体
A.①② B.②③ C.①③ D.②④
6.氨分子中,两个N-H键的键角是
A.90o B.107o C.109o28 D.120°
7.铁与镁组成的储氢合金的立方晶胞结构如图所示。铁原子位于顶点和面心的位置,镁原子位于将晶胞平分为8个立方单位的体心位置。下列说法正确的是
A.距离Fe原子最近的Mg原子数为4
B.该晶胞的体积为b3×10-27cm3
C.Fe原子与镁原子间最短距离为b nm
D.晶体储氢时,H2在晶胞的体心和棱的中心位置。则储氢后化学式为FeMg2 H2
8.下列物质:①BeCl2②CS2③白磷④BF3⑤NF3⑥H2O2,其中含极性键的非极性分子是
A.①④⑥ B.②③⑥ C.①②④ D.③④⑤
9.碳元素组成的晶体种类繁多,三种常见的单质结构如图所示。下列说法错误的是
A.金刚石中碳原子的配位数为4 B.石墨中碳原子的杂化方式为
C.晶体属于分子晶体 D.三者互为同分异构体
10.瑞巴派特片()是一种胃药,其主要成分结构如图,下列说法正确的是
A.该物质不能使酸性高锰酸钾溶液褐色
B.该物质可以发生加成、取代、消去反应
C.该物质与足量氢气发生加成反应后,所得产物分子中有3个手性碳原子
D.该物质在酸性条件下水解的产物中含有氨基酸
11.金刚砂(SiC)是重要的工业制品,可由反应制得:。SiC的晶体结构与金刚石类似,如图所示。下列说法错误的是
A.Si属于p区元素,在SiC中的化合价为+4价
B.X可与氧气反应生成Y,Y分子的中心原子杂化方式为sp杂化
C.金刚石熔点比SiC晶体熔点高
D.已知Si-C键键能为akJ/mol,则理论上分解1molSiC形成气态原子需要的能量为akJ
12.NF3是一种优良的蚀刻气体。HF、F2均可用于制备NF3,F2制备NF3的反应为4NH3+3F2NF3+3NH4F。Ka(HF)=6.3×10 4,Kb(NH3·H2O)=1.8×10 5。下列关于氨和铵盐的说法正确的是
A.氨气易溶于水,是因为氨分子间能形成氢键
B.HF酸性强,所以不能用玻璃瓶盛装
C.25℃,0.1 mol·L 1 NH4F溶液的pH<7
D.25℃,NH3与HNO3反应生成N2和H2O
13.下列各组微粒的空间结构相同的是
①和;②和;③和;④和
A.①②③④ B.①②④ C.①③④ D.②④
二、填空题
14.(1)是有机合成中常用的还原剂,中的阴离子空间构型是_______,中心原子的杂化形式为_______。
(2)根据价层电子对互斥理论,、、的气态分子中,中心原子价层电子对数不同于其他分子的是_______。
(3)《中华本草》等中医典籍中,记载了炉甘石入药,可用于治疗皮肤炎症或表面创伤.中,阴离子空间构型为_______,C原子的杂化形式为_______。
(4) X射线衍射测定等发现,中存在离子,离子的几何构型为_______,中心原子的杂化形式为_______。
15.氮是地球上极为丰富的元素。
(1)中N以形式存在,基态的电子排布式为______。
(2)为三角锥形分子,键键能的含义是______(填字母)。
A.由N和H形成所放出的能量
B.把中的共价键全部拆开所吸收的能量
C.拆开约个键所吸收的能量
D.形成1个键所放出的能量
(3)键的键能为,键的键能为,计算说明中的______(填“”或“”,下同)键比______键稳定。
(4)已知:,,,。计算反应的反应热______。
16.判断下列物质熔沸点高低(填>或<):
(1)_______
(2)_______
(3)_______
(4)异戊烷_______新戊烷
(5)_______
(6) _______
17.磷化铝(AlP)和磷化氢(PH3)都是粮食储备常用的高效熏蒸杀虫剂。
(1)磷元素在元素周期表中的位置:_______,AlP遇水蒸气会发生反应放出PH3气体,PH3中的P原子的杂化方式为_______杂化,该反应的另一种产物的化学式为_______。
(2)具有强还原性,能与溶液反应,配平该反应的化学方程式:_______。
(3)工业制备的流程如图所示。
① 次磷酸属于_______元酸。
② 白磷和烧碱溶液反应的化学方程式为:_______。
③ 若起始时有1 mol P4参加反应,则整个工业流程中共生成_______mol (不考虑产物损失)
18.溶质在溶剂中的溶解度取决于多种因素,请回答下列问题:
(1)实验发现:CH4极难溶于水,而HF极易溶于水,其原因是_______。
(2)通常条件下,1体积的水可溶解700体积的NH3,请说明三点理由:_______。
19.回答下列问题:
(1)三价铬离子能形成多种配位化合物。中提供电子对形成配位键的原子是___________,中心离子的配位数为___________。
(2)与N-甲基咪唑()反应可以得到,其结构如图所示:
N-甲基咪唑分子中碳原子的杂化轨道类型为___________,1个中含有___________个键。
20.实验室制备溴代烃的反应如下: ①
②
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br-被浓硫酸氧化为Br2等。有关数据列表如下;
乙醇 溴乙烷 正丁醇 1-溴丁烷
密度/g·cm-3 0.7893 1.4604 0.8098 1.2758
沸点/℃ 78.5 38.4 117.2 101.6
请回答下列问题:
(1)在溴乙烷和1-溴丁烷的制备实验中,下列仪器最不可能用到的是______ 。
a.圆底烧瓶 b. 容量瓶 c.锥形瓶 d.量筒
(2)溴代烃的水溶性 _____(填“大于”、“等于”或“小于”)相应的醇;其原因是___________________________ 。
(3)将1-溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在________(填“上层”、“下层”或“不分层”)。
(4)制备操作中,加入的浓硫酸必须进行稀释,其目的不正确的是___________。
a. 水是反应的催化剂 b.减少的生成
c.减少HBr的挥发 d. 减少副产物烯和醚的生成
(5)在制备溴乙烷时,采用边反应边蒸出产物的方法,其原因是_____________ ;但在制备1-溴丁烷时却不能边反应边蒸出产物,其原因是______________________________。
21.回答下列问题:
(1)化合物III也是一种汞解毒剂。化合物IV是一种强酸。下列说法正确的有_____。
A.在I中S原子采取sp3杂化
B.在II中S元素的电负性最大
C.在III中C-C-C键角是180°
D.在III中存在离子键与共价键
E.在IV中硫氧键的键能均相等
(2)汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。化合物I与化合物III相比,水溶性较好的是_____。
(3)NH3、PH3、AsH3分子的键角分别为107.3°、93.3°、91.8°,其键角逐渐减小的原因是____。
(4)中含有各元素的电负性由小到大的顺序为____;该物质中,含有σ键和π键数目之比为____。
(5)在CO分子中每个原子均为8电子稳定结构,则C与O之间形成_____个σ键____个π键,在这些化学键中,O原子共提供了____个电子。
(6)乙腈(CH3CN)分子中碳原子的杂化类型有____,与N同周期的主族元素中,第一电离能大于N的有_____种,写出一种与N互为等电子体的分子的化学式_____,NO离子的立体构型是____。
(7)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据列于表:
元素 Mn Fe
电离能/kJ mol-1 I1 717 759
I2 1509 1561
I3 3248 2957
锰元素位于第四周期第VIIB族。请写出基态Mn2+的价电子排布式:_____,比较两元素的I2、I3可知,气态Mn2+再失去1个电子比气态Fe2+再失去1个电子难,对此你的解释是_____。
22.按要求完成下列填空:
(1)有以下8种分子:①HF,②Cl2,③H2O,④N2,⑤C2H4,⑥C2H6,⑦H2O2,⑧HCN(H-C≡N),其中只有含有σ键的是__________________(填序号);既含有σ键,又含有π键的是__________________(填序号)。
(2)X、Y、Z是元素周期表中的短周期元素,其中X、Y同周期,Y、Z同主族,Y原子最外层p轨道上的电子数等于前一电子层电子总数,X原子最外层的p能级中只有一个轨道填充了2个电子,而且这三种元素可以形成化合物YX2、ZX2。根据上述信息回答下列问题:
a.写出下列元素符号:X______,Y______,Z______。
b.YX2分子中含_______个σ键,含_______个π键。
23.铬、铁、镍、铜等金属及其化合物在工业上有重要用途。
(1)基态铬原子的电子排布式为____。
(2)CrO2Cl2和NaClO均可作化工生产的氧化剂或氯化剂。制备CrO2Cl2的反应为K2Cr2O7+3CCl4=2KC1+2CrO2Cl2+3COCl2↑。
①上述反应式中非金属元素电负性由大到小的顺序是____(用元素符号表示)。
②常温下CrO2Cl2是一种易溶于CCl4的液体,则固态CrO2Cl2属于____晶体。
③COCl2分子中所有原子均满足8电子结构,则COCl2分子中σ键和π键的个数比为____。
④CuCl的盐酸溶液能吸收CO生成复合物氯化羰基亚铜[Cu2Cl2(CO)2·2H2O],其结构如图所示。
下列说法不正确的是____(填字母序号)。
A.该复合物中只含有离子键和配位键
B.该复合物中Cl原子的杂化类型为sp3
C.该复合物中只有CO和H2O作为配位体
D.该溶液中滴入硝酸酸化的硝酸银不产生沉淀
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
【详解】①Na2O2是离子化合物,含有离子键、非极性共价键,正确;
②SiO2是原子晶体,只含有极性共价键,错误;
③石墨是混合型晶体,层内含有非极性共价键,层间含有分子间作用力,正确;
④金刚石是原子晶体,只含有非极性共价键,错误;
⑤CaCl2是离子晶体,只含有离子键,错误;
⑥白磷是分子晶体,分子间含有分子间作用力,分子内含有非极性共价键,正确。
含有上述结合力中的两种的组合是①③⑥,选项是B。
2.C
【分析】其水溶液显弱酸性,说明界外没有氨分子,向1molM中加入足量AgNO3溶液生成1mol白色沉淀,说明三个氯离子1个位于外界,所以该配合物的化学式最可能为[Co(NH3)4Cl2]Cl。
【详解】A.配合物的化学式最可能为[Co(NH3)4Cl2]Cl,该配合物的配体是Cl-和NH3,故A正确;
B.根据分析可得,该配合物可表示为[Co(NH3)4Cl2]Cl,故B正确;
C.M中的配位数为6,故配离子不可能是平面正方形,故C错误;
D.该配合物中心离子的电荷数为+3,配位数为6,故D正确;
故选C。
3.C
【详解】①P4由4个P构成正四面体构型;
②NH3的空间结构是三角锥形;
③CCl4由4个Cl构成正四面体构型;
④CH4由4个H构成正四面体构型;
⑤H2S的空间结构是V形;
⑥CO2的空间结构是直线形;
故选C。
4.D
【详解】A.水玻璃是硅酸钠溶液,硅酸钠不燃烧、不支持燃烧,所以电影银幕用水玻璃浸泡的主要目的是为了防火,故A正确;
B.人造棉、人造丝的主要成分都是纤维素,故B正确;
C.氢键对维持生物大分子的空间构型和生理活性具有重要意义,所以氢键在形成蛋白质二级结构和DNA双螺旋结构中起关键作用,故C正确;
D.石膏的主要成分是硫酸钙,燃煤中添加石膏不能减少SO2的排放,不能达到减少酸雨的目的,故D错误。
答案选D。
5.B
【详解】①氢键不是化学键,错误;
②在C60晶体的晶胞中,在晶胞的顶点和面心上各有一个C60分子,是面心立方结构,正确;
③As是ⅤA族的一个主族元素,其外围电子排布式为4s24p3,属于p区元素,正确;
④HgCl2的稀溶液有弱的导电能力,说明其属于电解质,错误;
②③正确,故选B。
6.B
【详解】氨分子中,N原子的价层电子数为 ,N采取sp3杂化,有一对孤电子对,氨气为三角锥形,孤电子对—成键电子对的斥力大于成键电子对—成键电子对的斥力,N-H键的键角为107°,略小于正四面体构型的键角109o28′,故选B。
7.D
【详解】A.由晶胞结构可知,位于顶点的铁原子与位于体对角线上镁原子的距离最近,则铁原子的配位数为8,故A错误;
B.由晶胞结构可知晶胞参数为bnm,则该晶胞体积为:b3×10-21cm3,故B错误;
C.由晶胞结构可知,位于顶点的铁原子与镁原子的距离为体对角线的,则铁原子与镁原子间最短距离为b nm,故C错误;
D.由晶胞结构可知,晶胞中位于顶点和面心的铁原子个数为8×+6×=4,位于体内的镁原子个数为8,位于体心和棱的中心位置的氢分子个数为12×+1=4,氢后化学式为FeMg2H2,故D正确;
故选D。
8.C
【详解】①BeCl2中含有极性键,为直线形分子,其结构对称,正、负电荷的中心重合,为非极性分子,①符合题意;
②CS2中含有C=S极性键,为直线形分子,其结构对称,正、负电荷的中心重合,为非极性分子,②符合题意;
③P4为单质,分子中只含有非极性键,为非极性分子,③不符合题意;
④BF3中含有极性键,为平面三角形分子,正、负电荷的中心重合,为非极性分子,④符合题意;
⑤NF3中含有极性键,为三角锥形分子,正、负电荷的中心不重合,为极性分子,⑤不符合题意;
⑥H2O2中含有极性键,但氧原子上有孤电子对,其结构不对称,正、负电荷的中心不重合,为极性分子,⑥不符合题意;
综上所述①②④符合题意;
故选C。
9.D
【详解】A. 由金刚石的结构图可知,金刚石中每个碳原子周期连接4个碳原子,故碳原子的配位数为4,故A正确;
B. 石墨的每一层呈平面结构,每个碳原子连接3个碳原子,价层电子对数为3,碳原子的杂化方式为,故B正确;
C. 晶体属于分子晶体,故C正确;
D. 金刚石和石墨没有分子,三者不互为同分异构体,而是由C元素组成的不同单质,互为同素异形体,故D错误;
故选D。
10.D
【详解】A.含碳碳双键,可被高锰酸钾氧化,则能使酸性高锰酸钾溶液褪色,故A错误;
B.含有苯环,能发生加成反应和取代反应,苯环上的氯原子不能发生消去反应,故B错误;
C.该物质与足量氢气发生加成反应后,所得产物分子中有4个手性碳原子(),故C错误;
D.由结构可知含肽键,则该物质能水解,且水解产物中含有氨基酸,故D正确;
故选D。
11.D
【详解】A.Si位于第三周期ⅣA族,属于p区,电负性Si<C,所以SiC中Si元素的化合价为+4价,A正确;
B.根据原子守恒可知X为CO,CO与氧气反应生成的Y为CO2,CO2分子中中心C原子的价层电子对数为=2,为sp杂化,B正确;
C.碳原子半径小于硅原子半径,则碳碳键键能大于碳硅键键能,导致金刚石熔点比SiC晶体熔点高,C正确;
D.据图可知每个Si原子形成4个Si-C键,所以1molSiC中含有4molSi-C键,分解1molSiC形成气态原子需要的能量为4akJ,D错误;
综上所述答案为D。
12.C
【详解】A.氨气易溶于水,是因为氨气分子和水分子间能形成氢键,A错误;
B.HF为弱酸,不能用玻璃瓶盛装是因为HF会和二氧化硅反应,B错误;
C.HF的电离平衡常数大于NH3·H2O,所以NH的水解程度大于F-,0.1 mol·L 1 NH4F溶液显酸性,pH<7,C正确;
D.25 ℃,NH3与HNO3反应生成硝酸铵,D错误;
综上所述答案为C。
13.C
【详解】
微粒 中心原子上的孤电子对数 中心原子上的价层电子对数 空间结构
① 2 直线形
2 直线形
② 2 直线形
4 V形
③ 3 V形
3 V形
④ 4 正四面体形
4 正四面体形
综合以上分析,①③④符合题意,故答案选C。
14. 正四面体 平面三角形 V形
【详解】(1)中的阴离子是,中心原子铝原子的价层电子对数是4,且不存在孤电子对,所以其空间构型是正四面体;中心原子的杂化轨道类型是杂化;
(2)根据价层电子对互斥模型可知,、、的气态分子中,中心原子价层电子对数分别是、、,因此中心原子价层电子对数不同于其他分子的是;
(3)碳酸锌中的阴离子为,根据价层电子对互斥模型,其中心C原子的价层电子对数为,不含孤电子对,所以其空间构型为平面三角形,C原子为杂化;
(4)的中心I原子形成2个键,孤电子对数为,即中心I原子形成2个键,还有2个孤电子对,故的几何构型为V形;中心I原子采取杂化。
15. C π -456
【详解】(1)基态N原子的电子排布式为,得到3个电子转化为,故基态的电子排布式为。
(2)键的键能是指形成键放出的能量或拆开键所吸收的能量,不是指形成1个键释放的能量。分子中含有键,拆开或形成吸收或放出的能量应是键键能的3倍。
(3)键中有两个π键和一个键,而键为键,键能为,键的键能为,则键的键能大于键键能的3倍,故中键的稳定性比π键弱。
(4)
。
16.(1)<
(2)<
(3)>
(4)>
(5)<
(6)<
【解析】(1)
金属晶体中金属原子的价电子数越多,原子半径就越小,金属阳离子与自由电子的静电作用越强,金属键越强,熔沸点越高,故熔沸点Mg
离子晶体的熔沸点是根据离子所带的电荷数和离子半径来比较的,离子所带的电荷数越高,离子的半径就越小,则该离子的熔沸点就越高,氧化镁中阴阳离子所带电荷数多,离子半径而且小,所以熔沸点NaCl
水和硫化氢是同族元素形成的氢化物,但因为水中存在氢键使水的熔沸点升高,所以熔沸点H2O>H2S,故答案为:>;
(4)
异戊烷和新戊烷是同分异构体,支链越多熔沸点越低,所以熔沸点是异戊烷>新戊烷,故答案为:>;
(5)
组成和结构相似的分子晶体,相对分子质量越大,熔沸点越高,所以<,故答案为:<;
(6)
对羟基苯甲醛形成分子间氢键使溶沸点升高,而邻羟基苯甲醛形成的是分子内氢键 ,对羟基苯甲醛的溶沸点高于邻羟基苯甲醛,故熔沸点<,故答案为:<。
17.(1) 第三周期第VA族 sp3 Al(OH)3
(2)24,11,12=8,3,24
(3) 一 P4 +3NaOH + 3H2O =PH3 + 3NaH2PO2 2.5mol
【详解】(1)P处于第三周期ⅤA族,AlP遇水蒸气会发生反应放出PH3气体,PH3中的P原子的杂化方式为sp3,根据元素守恒,确定该反应的另一种产物是Al(OH)3,故答案为:第三周期第VA族;sp3;Al(OH)3;
(2)该方程式中Cu价态由+2下降为+1,P价态由-3升高为+5,为保证化合价升降数相等,Cu3P与H3PO4计量数分别为8、3,CuSO4的系数是24,H2SO4系数是24,根据元素守恒,得到:,故答案为:24,11,12,8,3,24;
(3)①根据氢氧化钠过量时只能生成NaH2PO2可知次磷酸只能电离出1个氢离子,因此次磷酸属于一元酸,故答案为:一;
②根据图示信息:白磷和烧碱溶液反应生成PH3、NaH2PO2,方程式为:;故答案为:;
③P4+3NaOH+3H2O=PH3↑+3NaH2PO2;2H3PO2=PH3↑+H3PO4,即P4~2.5PH3,若起始时有1molP4参加反应,则整个工业流程中共生成2.5molPH3;故答案为:2.5。
18.(1)CH4是非极性分子,水是极性溶剂,所以CH4极难溶于水;HF是极性分子且能与水分子形成氢键,所以HF极易溶于水
(2)NH3与H2O均为极性分子;NH3与H2O分子间易形成氢键;NH3与H2O易反应生成
【解析】(1)
的空间构型为正四面体、是非极性分子,而的空间构型为V形、是极性分子,的空间构型为直线型,只含H-F极性键,是极性分子,依据相似相溶原理,CH4极难溶于水,HF极易溶于水,且能与水分子形成分子间氢键。
(2)
的空间构型为V形、是极性分子,NH3的空间构型为三角锥形,是极性分子,依据相似相溶原理,NH3极易溶于水,N、O的电负性大,NH3可与H2O形成分子间氢键,使得NH3极易溶于水,NH3能与H2O反应生成,增大了NH3在H2O中的溶解度。
19.(1) N、O、Cl 6
(2) 、 54
【解析】(1)
中的氧原子、中的氮原子和中都有孤电子对,可作配位原子,故配位原子为O、N、Cl;
中心离子的配位数为。
(2)
由结构可知,N-甲基咪唑含有甲基和碳碳双键,则该分子中碳原子的杂化轨道类型为、;
1个N-甲基咪唑中含有6个键、4个键、1个碳碳双键和1个碳氮双键,单键、配位键属于键,1个双键中有1个O键和1个键,所以1个中含有个键。
20.(1)b
(2) 小于 醇可与水分子之间形成氢键,溴代烃不能与水分子之间形成氢键
(3)下层
(4)a
(5) 平衡向生成溴乙烷的方向移动(或反应②向右移动) 1-溴丁烷与正丁醇的沸点差较小,若边反应边蒸馏,会有较多的正丁醇被蒸出
【详解】(1)容量瓶用于一定物质的量浓度溶液的配制,在该实验中最不可能用到,答案选b;
(2)醇可与水分子之间形成氢键,溴代烃不能与水分子之间形成氢键,所以溴代烃的水溶性小于相应醇的水溶性;
(3)根据表中数据可知,1-溴丁烷的密度大于水的密度,因此将1-溴丁烷的粗产品置于分液漏斗中加水,振荡后静止,产物即1-溴丁烷应在下层;
(4)由于加入的浓硫酸在稀释时放出大量的热且具有强氧化性,因此在准备操作过程中,加入的浓硫酸必须进行稀释,其目的就是防止放热导致副产物烯和醚的生成并减小HBr的挥发,同时也减少的生成,即答案选a;
(5)根据平衡移动原理,蒸出产物平衡相有利于生成溴乙烷的方向移动;在准备1-溴丁烷时不能采取此方法,原因是1-溴丁烷与正丁醇的沸点相差较小,如果边反应边蒸,会有较多的正丁醇被蒸出。
21.(1)AD
(2)化合物III
(3)中心原子电负性越大,相应的键角就越大
(4) H
(6) sp3、sp 1 N2O或CO2 平面三角形
(7) 3d5 Mn2+价电子排布为3d5,处于半满状态,能量比较低,再失去一个电子需要的能量较大
【详解】(1)A.中S原子的价层电子对数=2+=4,因此S原子采取sp3杂化,故A正确;
B.中含有的元素为H、C、O、S、Hg,同周期元素从左至右元素的电负性逐渐增大,同主族元素从上至下元素的电负性逐渐减小,因此5种元素中电负性最大的为O元素,故B错误;
C.中C原子成键均为单键,因此C原子采取sp3杂化,所以C-C-C键角接近109 28’,故C错误;
D.中存在C-H、C-C、C-S、S=O、S-O、S-H共价键和 与Na+之间的离子键,故D正确;
E.在Ⅳ中存在硫氧单键和硫氧双键,硫氧键的键能不相等,故E错误;
正确答案选AD。
(2)中羟基能与水分子之间形成分子间氢键,为易溶于水的钠盐,溶于水后电离出的 中O原子均能与水分子之间形成氢键,相同物质的量两种物质溶于水后, 形成的氢键更多,因此化合物III更易溶于水。
(3)NH3、PH3、AsH3分子均为三角锥形,结构相似,中心原子电负性越大,中心原子周围电子云密度越大,化学键之间的相互排斥作用越大,相应的键角就越大,而三者电负性大小顺序是:N>P>As,所以NH3、PH3、AsH3键角依次减小。
(4)中含有C、N、O、H,各元素的电负性由小到大的顺序为H
(6)乙腈(CH3CN)分子的结构简式为:,根据形成4个单键判断杂化类型是,成三键判断是sp杂化,故答案为:、sp;与N同周期的主族元素中,第一电离能大于N的有F元素,按洪特规则氮元素处于半充满状态稳定,比氧元素的电离能大;根据原子数相等、价电子数也相等的微粒互为等电子体进行判断与N互为等电子体的分子的化学式N2O或CO2;NO离子的立体构型根据价层电子对互斥理论进行判断中心原子N采用sp2杂化,且形成三个共价键,故为平面三角形。
(7)锰元素位于第四周期第Ⅶ B族,则Mn原子的价电子排布式为3d54s2,则Mn2+的价电子排布式为3d5;Fe为26号元素,Fe原子的价电子排布式为3d64s2,Fe2+的价电子排布式为3d6,由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态需要的能量较多;而Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态需要的能量相对要少,所以气态Mn2+再失去1个电子比气态Fe2+再失去1个电子难,故答案为:由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态需吸收能量。
22. ①②③④⑤⑥⑦ ④⑤⑧ O C Si 2 2
【分析】多原子分子中都有σ键,含有双键、叁键或苯环的物质既有σ键又有π键。
X、Y、Z是元素周期表中的短周期元素,其中X、Y同周期,Y、Z同主族,Y原子最外层p轨道上的电子数等于前一电子层电子总数,则Y为C元素;X原子最外层的p能级中只有一个轨道填充了2个电子,则该p轨道有4个电子,而且这三种元素可以形成化合物YX2、ZX2,则X为O元素,Z为Si元素。
【详解】(1)①HF,②Cl2,③H2O,④N2,⑤C2H4,⑥C2H6,⑦H2O2,⑧HCN(H-C≡N),其中只含有σ键的是①②③④⑤⑥⑦;乙烯分子中有碳碳双键,氮气分子和HCN中都有叁键,故既含有σ键、又含有π键的是④⑤⑧。
(2)a.X、Y、Z元素的符号分别是O、C、Si。
b.CO2分子的结构式为O=C=O,故其中含2个σ键,含2个π键。
23.(1)1s22s22p63s23p63d54s1
(2) O>Cl>C 分子 3:1 AC
【解析】(1)
基态铬原子的电子排布式为1s22s22p63s23p63d54s1,故答案为:1s22s22p63s23p63d54s1;
(2)
①反应式中非金属元素有O、C、Cl,它们的电负性由大到小顺序为O>Cl>C,故答案为:O>Cl>C;
②分子晶体熔沸点较低,该物质的熔沸点较低,所以为分子晶体,故答案为:分子;
③COCl2分子中有1个C=O键和2个C-Cl键,所以COCl2分子中σ键的数目为3,π键的数目为1,个数比3:1,故答案为:3:1;
④A.该复合物中存在化学键类型有离子键、配位键、极性共价键等,故A错误;
B.该复合物中Cl原子形成2个σ键,还含有2个未成键电子对,其杂化类型为sp3,故B正确;
C.该复合物中配位体有CO、H2O和Cl原子,故C错误;
D.Cu2Cl2(CO)2·2H2O 中Cl原子是配原子,在溶液中不存在Cl-,则滴入硝酸酸化的硝酸银不产生沉淀,故D正确;
故答案为:AC。
答案第1页,共2页
答案第1页,共2页
