福建省三年(2021-2023)中考化学真题分题型分类汇编-01填空题(含解析)
文档属性
| 名称 | 福建省三年(2021-2023)中考化学真题分题型分类汇编-01填空题(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 750.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-06-30 00:00:00 | ||
图片预览




文档简介
福建省三年(2021-2023)中考化学真题分题型分类汇编-01填空题
一、填空题
1.(2021·福建·统考中考真题)“嫦娥五号”月球采样返回,“天问一号”成功抵达火星,标志着我国航天事业取得突破性进展。
(1)月壤含CaAl2Si2O8以及可作为核聚变燃料的氦-3等物质。
①CaAl2Si2O8中,Si、O两种元素的质量比为____________。
②如图为氦在元素周期表中的部分信息。氦-3原子的质子数与中子数之和为3则其中子数为_______、核外电子数为_______。
(2)着陆器上的仪器可探测水。若月球上存在大量的水,可利用光催化分解水技术得到氧气,对人类在月球上活动意义重大,该反应的化学方程式为__________________。
(3)火星拥有丰富的金属矿物和二氧化碳等资源。火星低层大气的主要成分如下表。
气体成分 CO2 N2 Ar O2 其他
体积分数/% 95.32 2.7 1.6 0.13 0.25
①为鉴别一瓶模拟“火星低层大气”组成的气体和一瓶空气,可采用的化学方法是___________。
②若为满足人类未来在火星上生活,下列研究设想不合理的是___________(填标号)。
a.将CO2转化为O2,提高O2含量
b.将CO2分解转化为N2,提高N2含量
c.寻找水的存在和开发水循环技术
d.利用火星上的金属矿物冶炼金属
2.(2021·福建·统考中考真题)钢铁是应用广泛的金属材料。
(1)英国学者R·坦普尔论证了我国古代冶铁技术世界第一。早在公元前4世纪,中国已广泛利用铁矿石与木炭生产生铁,并加入“黑土”以降低生铁的熔化温度;公元前2世纪,中国人发明了“充氧”等炼钢法。
①“黑土”含有磷酸铁(FePO4),其中磷元素的化合价为______________。
②生铁生产过程中,一氧化碳与氧化铁在高温下反应的化学方程式为______________。
③炼钢中“充氧”的目的是降低生铁中的______________,获得性能更好的钢。
(2)对钢铁制品进行“发蓝”处理,使其表面生成一层致密的氧化膜,能有效防止钢铁锈蚀。
①“发蓝”过程发生了______________(填“物理变化”或“化学变化”)。
②致密氧化膜能防止钢铁锈蚀的原因是______________。
3.(2021·福建·统考中考真题)如图为我国古代“布灰种盐”生产海盐的部分场景,其过程为“烧草为灰,布在滩场,然后以海水渍之,俟晒结浮白,扫而复淋”。
(1)“晒结浮白”是指海水浸渍的草灰经日晒后出现白色海盐颗粒的过程,化学上称之为______________。
(2)经过多次“扫而复淋”,提高卤水浓度获得“上等卤水”(氯化钠的质量分数约为15%),用于煎炼海盐。
①1000g“上等卤水”蒸干后,可得氯化钠的质量约为________g。
②从燃料利用角度分析,用获得的“上等卤水”而不直接用海水煎炼海盐的原因是______________。
③将“上等卤水”在100℃恒温蒸发至刚有晶体析出,所得溶液的组成为:150g溶液中含水100g、NaCl 39.8g、MgCl27.65g及其他成分2.55g。将150g此溶液降温至20℃,有_______g NaCl析出(溶解度见表)。此时,________(填“有”或“没有”)MgCl2析出,原因是____________。
温度/℃ 20 60 100
溶解度/g NaCl 36.0 37.3 39.8
MgCl2 54.8 61.3 73.0
4.(2021·福建·统考中考真题)为方便推测某些复杂物质的化学性质,可将其化学式改用常见物质的化学式表示。如碱式碳酸铜【Cu2(OH)2CO3】可改写为Cu(OH)2·CuCO3,推测其兼具Cu(OH)2和CuCO3的化学性质。
(1)举重运动员常用碱式碳酸镁【Mg2(OH)2CO3】粉末抹在手掌以增大摩擦力。
①参照上述方法,碱式碳酸镁的化学式可改写为__________。
②该物质兼具__________(填“酸”或“碱”)和碳酸盐的化学性质。
③该物质分解的化学方程式为 ,X的化学式为__________。
(2)某种茶垢清洁剂的主要成分为过碳酸钠(可表示为2Na2CO3·3H2O2)。将过碳酸钠溶解于热水中,有大量气泡产生,其原因是________;当不再产生气泡后,往溶液中加入足量澄清石灰水,反应的化学方程式为__________。
5.(2022·福建·统考中考真题)钙是人体必需元素。
(1)下图为钙元素在元素周期表中的部分信息。钙元素的相对原子质量为_______,钙原子的核外电子数为_______。
(2)牛奶、豆类等食物含钙丰富,这里的“钙”指的是_______(填“单质”“元素”或“原子”)。
(3)人体若缺钙,可服用补钙剂。
①缺钙可能导致的健康问题是_______(填“骨质疏松”或“贫血”)。
②服用主要成分为CaCO3的某钙片,与胃酸(含有HCl)反应后钙才能被吸收。该反应的化学方程式为_______。
6.(2022·福建·统考中考真题)水是生命之源。通常所说的水为H2O,而更广义的水还包括矿物中的氢氧基团(OH)、其他形式的氢(H),它们在高温下才以水分子的形式释放出来。A~C是氢、氧原子及其构成微粒的示意图。
(1)一定条件下由A生成C的化学方程式为____。A→B→C的变化过程中,不变的是__。
(2)参照上图微粒表示方法,画出“氢氧基团(OH)和氢(H)结合成水分子”的微观示意图:___。
(3)科研工作者将“嫦娥五号”采集的月球玄武岩中的磷灰石分解,其化学方程式为。则X的化学式为____。
(4)理论上,通过测量外星球矿样中氢元素的质量,可换算出矿样中水的质量。若1.0g某矿样含氢的质量为8.0×10-5g,则含水的质量m(H2O)=____g
7.(2022·福建·统考中考真题)兴趣小组用稀盐酸清洗铁夹表面的铁锈(主要成分为氧化铁),并进行保护实验。
(1)除铁锈的反应属于_______(填基本反应类型)。
(2)铁夹在稀盐酸中浸泡较长时间,有气体产生。产生气体的化学方程式为_______。
(3)将清洗过的铁夹进行“发蓝”处理,形成致密的氧化物保护膜,其主要成分与铁在氧气中燃烧的产物相同,该氧化物的化学式为_______。
(4)验证废液显酸性,可选用的一种试剂或用品是_______。
(5)用氢氧化钠中和废液中的盐酸,反应的化学方程式为_______。
8.(2023·福建·统考中考真题)福建盛产茶叶,茶文化源远流长。为了了解茶叶的组成和作用,学习小组查得某茶叶样品的成分及含量如下图所示:
(1)茶叶属于_________________(填“纯净物”或“混合物”),其中含量最高的基本营养素是___________________。
(2)茶多酚具有强血管、降血脂的作用。某种茶多酚的化学式为C6H6O2,其氢、氧元素的质量比为_________________。
(3)茶叶含氟较高,对预防龋齿有一定效果。这里的“氟”指的是_________________(填“元素”或“单质”)。
(4)茶叶中的硒有防癌作用。硒在元素周期表中的部分信息如图所示,硒原子的核外电子数为_________________。
9.(2023·福建·统考中考真题)中国科学家首次从月壤样品中发现新矿物——嫦娥石。学习小组查得资料:嫦娥石是从月壤样品的14万个颗粒中,利用针尖和颗粒之间静电吸附作用,分离出的一个粒径约1.0×10-5m的单晶颗粒,其化学式Ca9NaMg(PO4)7。请和小组同学起研究。
(1)嫦娥石的吸附分离过程属于________________(填“物理变化”或“化学变化”)。
(2)嫦娥石由_________________种元素组成。
(3)围绕“人类在月球上生活”的话题,展开月球上嫦娥石应用的讨论:
①助力农业生产:嫦娥石可作为生产________________(填“氮肥”“磷肥”或“钾肥”)的原料。
②提炼金属单质:若用107.2g嫦娥石提炼金属镁,最多可得镁的质量为________________g(嫦娥石的相对分子质量为1072)。
③展望更多应用:根据嫦娥石的组成推测,其可能另有的用途是________________(填一种)。
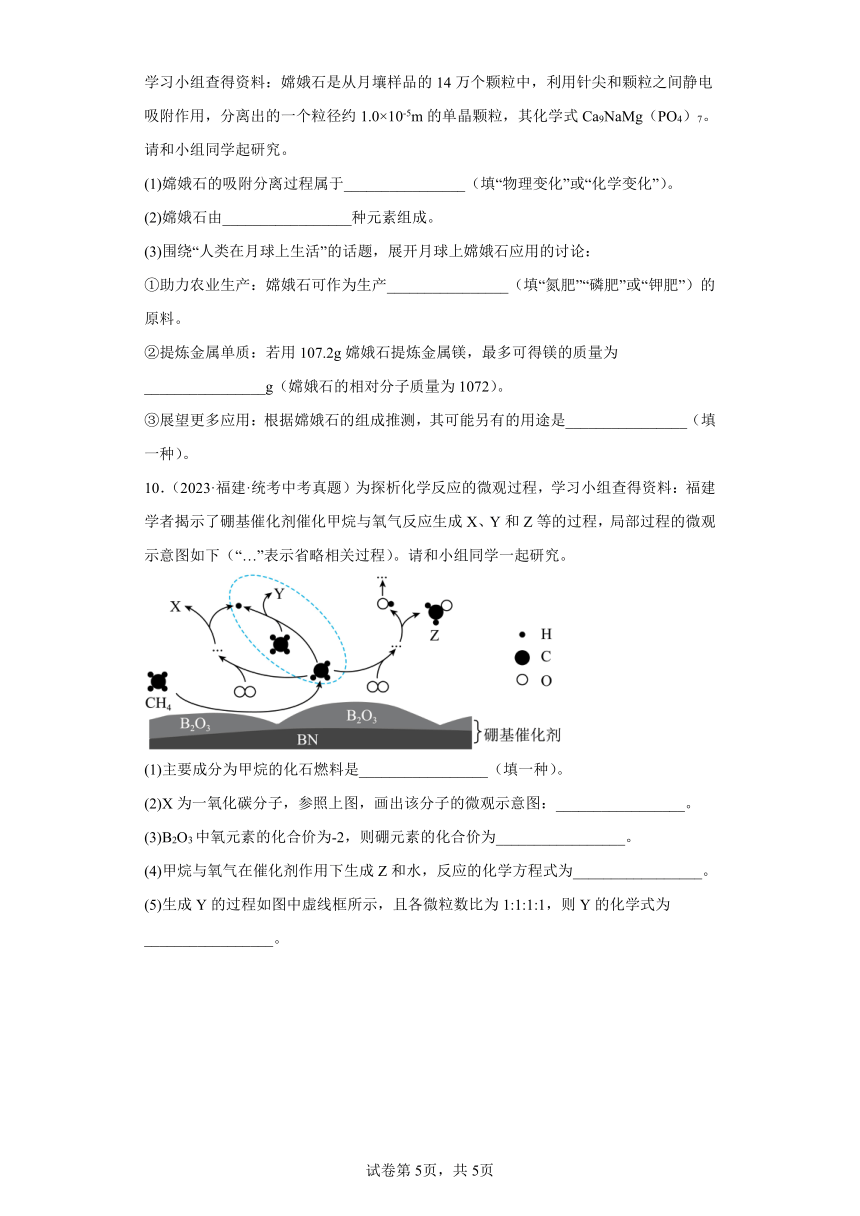
10.(2023·福建·统考中考真题)为探析化学反应的微观过程,学习小组查得资料:福建学者揭示了硼基催化剂催化甲烷与氧气反应生成X、Y和Z等的过程,局部过程的微观示意图如下(“…”表示省略相关过程)。请和小组同学一起研究。
(1)主要成分为甲烷的化石燃料是_________________(填一种)。
(2)X为一氧化碳分子,参照上图,画出该分子的微观示意图:_________________。
(3)B2O3中氧元素的化合价为-2,则硼元素的化合价为_________________。
(4)甲烷与氧气在催化剂作用下生成Z和水,反应的化学方程式为_________________。
(5)生成Y的过程如图中虚线框所示,且各微粒数比为1:1:1:1,则Y的化学式为_________________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1. 7:16 1 2 分别将燃着的木条深入两瓶气体中,若木条熄灭,则说明该气体是模拟“火星低层大气”组成的气体,若木条燃烧无明显变化,则该气体是空气。 b
【详解】(1)①CaAl2Si2O8中,Si、O两种元素的质量比为(28×2):(16×8)=7:16。
②由氦在元素周期表中的部分信息可知氦的原子序数为2,即氦原子核内的质子数为2,又氦-3原子的质子数与中子数之和为3,故其中子数为3-2=1,核外电子数=核内质子数=2。
(2)分析信息可知水在光催化下分解得到氧气和氢气,故反应方程式为:。
(3)①空气中二氧化碳约占总体积的0.03%,而模拟“火星低层大气”组成的气体中二氧化碳气体的体积含量是95.32%,故可根据二氧化碳不能燃烧也不能燃烧的性质进行鉴别。具体操作方法是:分别将燃着的木条深入两瓶气体中,若木条熄灭,则说明该气体是模拟“火星低层大气”组成的气体,若木条燃烧无明显变化,则该气体是空气。
②a. 模拟“火星低层大气”组成的气体中氧气含量比空气中少,且二氧化碳中含有氧元素,可通过将二氧化碳转化为氧气,以提高氧气的含量,此选项设想合理;
b.二氧化碳中不含氮元素,故无法将二氧化碳转化为氮气,此设想不合理;
c.水是人类生存不可缺少的物质,故应寻找水的存在和开发水循环技术,此设想合理;
d.火星拥有丰富的金属矿物,故可利用火星上的金属矿物冶炼金属供人类使用,此设想合理。故选b。
2. +5 含碳量 化学变化 隔绝氧气和水
【详解】(1)①磷酸铁中铁元素显+3价,氧元素显-2价,设磷元素的化合价为x,根据化合物中,正、负化合价的代数和为零,可得:(+3)+x+(-2)×4=0,x=+5;
②一氧化碳与氧化铁在高温下反应生成铁和二氧化碳,该反应的化学方程式为:;
③碳能与氧气在点燃的条件下反应生成二氧化碳,炼钢中“充氧”的目的是降低生铁中的含碳量,获得性能更好的钢;
(2)①“发蓝”过程有金属氧化物生成,属于化学变化;
②铁生锈的条件是铁与氧气和水接触,致密氧化膜能防止钢铁锈蚀的原因是:隔绝氧气和水。
3. 蒸发结晶 150 海水中氯化钠浓度低,浪费燃料 3.8 没有 20℃时,100g水中最多能溶解54.8g氯化镁,而该溶液中氯化镁只有7.65g,能全部溶解
【详解】(1)“晒结浮白”是指海水浸渍的草灰经日晒后出现白色海盐颗粒的过程,化学上称之为蒸发结晶;
(2)①1000g“上等卤水”蒸干后,可得氯化钠的质量约为:1000g×15%=150g;
②用获得的“上等卤水”而不直接用海水煎炼海盐的原因是:海水中氯化钠浓度低,浪费燃料;
③20℃时,氯化钠的溶解度为36.0g,即该温度下,100g水中只能溶解36.0g氯化钠,故将150g此溶液降温至20℃,有39.8g-36.0g=3.8g氯化钠析出;
没有氯化镁析出,因为100℃时,氯化镁的溶解度为73.0g,20℃时,氯化镁的溶解度为54.8g,即20℃时,100g水中最多能溶解54.8g氯化镁,而该溶液中氯化镁只有7.65g,能全部溶解。
4. Mg(OH)2·MgCO3 碱 MgO 过氧化氢受热分解生成水和氧气
【详解】(1)①碱式碳酸镁的化学式可改写为Mg(OH)2·MgCO3;
②该物质兼具氢氧化镁和碳酸镁的化学性质,氢氧化镁是电离时产生的阴离子都是氢氧根离子的化合物,属于碱,碳酸镁是由镁离子和碳酸根离子构成的化合物,属于碳酸盐,故填:碱;
③根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含Mg、O、H、C的个数分别是2、5、2、1,生成物中含Mg、O、H、C的个数分别是0、3、2、1,故生成物中还应含2个Mg、2个O,故X的化学式为:MgO;
(2)过碳酸钠兼具碳酸钠和过氧化氢的化学性质,将过碳酸钠溶解于热水中,有大量气泡产生,其原因是:过氧化氢受热分解生成水和氧气;
当不再产生气泡后,往溶液中加入足量澄清石灰水,氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠,该反应的化学方程式为:。
5.(1) 40.08 20
(2)元素
(3) 骨质疏松
【详解】(1)根据元素周期表标签最下面数字表示相对原子质量,故如图可知钙元素的相对原子质量为40.08,故填:40.08;
根据元素周期表标签左上角数字表示原子序数,原子序数等于质子数等于原子的核外电子数,如图可知钙原子的核外电子数为20,故填:20;
(2)牛奶、豆类等食物含钙丰富,这里的“钙”指的是钙元素,故填:元素;
(3)①人体的骨骼主要含钙元素,故人体缺钙儿童会引起佝偻病,成年人会引起骨质疏松,故填:骨质疏松;
②碳酸钙和胃液中的盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:。
6.(1) 氢原子和氧原子(或H、O)
(2)
(3)H2O
(4)7.2×10-4
【详解】(1)如图可知A中的物质是氢气和氧气,C是水,故氢气和氧气在一定条件下反应生成水的化学方程式为:;如图反应过程中氢分子分解为氢原子,氧分子分解为氧原子,氢原子和氧原子再从新结合,故反应过程中不变的是氢原子和氧原子,故填:氢原子和氧原子或H、O;
(2)“氢氧基团(OH)和氢(H)结合成水分子”的微观示意图:
(3)根据质量守恒定律反应前后原子的种类和个数不变,反应前钙原子、磷原子、氧原子、氢原子的个数分别是10、6、26、2,反应后钙原子、磷原子、氧原子、氢原子的个数分别是10、6、25、0,故X中含有2个氢原子和1个氧原子,则X的化学式为:;
(4)1.0g某矿样含水的质量是,故填:。
7.(1)复分解反应
(2)
(3)Fe3O4
(4)pH试纸(或“石蕊溶液”等)
(5)
【详解】(1)盐酸除铁锈是盐酸和氧化铁反应生成氯化铁和水,化学方程式为:,该反应是两种化合物互相交换成分生成两外两种化合物,属于复分解反应,故填:复分解反应;
(2)铁和稀盐酸反应生成氯化亚铁和氢气,化学方程式:;
(3)铁在氧气中燃烧生成四氧化三铁,故铁夹进行“发蓝”处理,形成致密的氧化物的化学式是:;
(4)根据酸性溶液pH<7,使用pH试纸可以测出或是酸性溶液能使石蕊试液变红,故可选用紫色石蕊试液,故填:pH试纸(或“石蕊溶液”等);
(5)氢氧化钠和盐酸反应生成氯化钠和水,化学方程式为:。
8.(1) 混合物 蛋白质
(2)3:16
(3)元素
(4)34
【详解】(1)由图知,茶叶含茶多酚、蛋白质等多种物质,属于混合物。基本营养素为糖类、油脂、蛋白质、维生素、无机盐和水,茶叶中含量最高的基本营养素是蛋白质。
(2)由茶多酚的化学式C6H6O2知,其氢、氧元素的质量比为(1×6):(16×2)=3:16。
(3)这里的“氟”不是强调以单质、分子、原子等形式存在,是强调存在的元素,与具体形态无关。
(4)由元素周期表一格知,左上角的数字为原子序数,原子中原子序数等于核外电子数,则硒原子的核外电子数为34。
9.(1)物理变化
(2)5/五
(3) 磷肥 2.4 制取氧气(或其他合理答案)
【详解】(1)嫦娥石的吸附分离过程没有产生新物质,属于物理变化。
(2)嫦娥石的化学式为:Ca9NaMg(PO4)7,由Ca、Na、Mg、P、O五种元素组成。
(3)①嫦娥石中含有磷元素,所以可作为生产磷肥的原料。
②若用107.2g嫦娥石提炼金属镁,最多可得镁的质量=。
③嫦娥石中含有氧元素,所以可以用来作为制取氧气的原料。(合理即可)
10.(1)天然气(或其他合理答案)
(2)
(3)+3
(4)
(5)C2H6
【详解】(1)天然气的主要成分是甲烷。
(2)X为一氧化碳分子,一个一氧化碳分子由1个碳原子和1个氢原子构成,故微观示意图为:。
(3)B2O3中氧元素的化合价为-2,设硼元素的化合价是x,根据在化合物中正负化合价代数和为零,可知2x+(-2)×3=0,则x=+3。
(4)甲烷与氧气在催化剂作用下生成Z和水,根据微观示意图可知Z是CH2O,故化学方程式为:。
(5)虚线框中是-CH3和CH4生成Y和-H,各微粒数比为1:1:1:1,则反应物中有两个碳原子和七个氢原子,生成物有一个氢原子,所以Y的化学式为C2H6。
答案第1页,共2页
答案第1页,共2页
一、填空题
1.(2021·福建·统考中考真题)“嫦娥五号”月球采样返回,“天问一号”成功抵达火星,标志着我国航天事业取得突破性进展。
(1)月壤含CaAl2Si2O8以及可作为核聚变燃料的氦-3等物质。
①CaAl2Si2O8中,Si、O两种元素的质量比为____________。
②如图为氦在元素周期表中的部分信息。氦-3原子的质子数与中子数之和为3则其中子数为_______、核外电子数为_______。
(2)着陆器上的仪器可探测水。若月球上存在大量的水,可利用光催化分解水技术得到氧气,对人类在月球上活动意义重大,该反应的化学方程式为__________________。
(3)火星拥有丰富的金属矿物和二氧化碳等资源。火星低层大气的主要成分如下表。
气体成分 CO2 N2 Ar O2 其他
体积分数/% 95.32 2.7 1.6 0.13 0.25
①为鉴别一瓶模拟“火星低层大气”组成的气体和一瓶空气,可采用的化学方法是___________。
②若为满足人类未来在火星上生活,下列研究设想不合理的是___________(填标号)。
a.将CO2转化为O2,提高O2含量
b.将CO2分解转化为N2,提高N2含量
c.寻找水的存在和开发水循环技术
d.利用火星上的金属矿物冶炼金属
2.(2021·福建·统考中考真题)钢铁是应用广泛的金属材料。
(1)英国学者R·坦普尔论证了我国古代冶铁技术世界第一。早在公元前4世纪,中国已广泛利用铁矿石与木炭生产生铁,并加入“黑土”以降低生铁的熔化温度;公元前2世纪,中国人发明了“充氧”等炼钢法。
①“黑土”含有磷酸铁(FePO4),其中磷元素的化合价为______________。
②生铁生产过程中,一氧化碳与氧化铁在高温下反应的化学方程式为______________。
③炼钢中“充氧”的目的是降低生铁中的______________,获得性能更好的钢。
(2)对钢铁制品进行“发蓝”处理,使其表面生成一层致密的氧化膜,能有效防止钢铁锈蚀。
①“发蓝”过程发生了______________(填“物理变化”或“化学变化”)。
②致密氧化膜能防止钢铁锈蚀的原因是______________。
3.(2021·福建·统考中考真题)如图为我国古代“布灰种盐”生产海盐的部分场景,其过程为“烧草为灰,布在滩场,然后以海水渍之,俟晒结浮白,扫而复淋”。
(1)“晒结浮白”是指海水浸渍的草灰经日晒后出现白色海盐颗粒的过程,化学上称之为______________。
(2)经过多次“扫而复淋”,提高卤水浓度获得“上等卤水”(氯化钠的质量分数约为15%),用于煎炼海盐。
①1000g“上等卤水”蒸干后,可得氯化钠的质量约为________g。
②从燃料利用角度分析,用获得的“上等卤水”而不直接用海水煎炼海盐的原因是______________。
③将“上等卤水”在100℃恒温蒸发至刚有晶体析出,所得溶液的组成为:150g溶液中含水100g、NaCl 39.8g、MgCl27.65g及其他成分2.55g。将150g此溶液降温至20℃,有_______g NaCl析出(溶解度见表)。此时,________(填“有”或“没有”)MgCl2析出,原因是____________。
温度/℃ 20 60 100
溶解度/g NaCl 36.0 37.3 39.8
MgCl2 54.8 61.3 73.0
4.(2021·福建·统考中考真题)为方便推测某些复杂物质的化学性质,可将其化学式改用常见物质的化学式表示。如碱式碳酸铜【Cu2(OH)2CO3】可改写为Cu(OH)2·CuCO3,推测其兼具Cu(OH)2和CuCO3的化学性质。
(1)举重运动员常用碱式碳酸镁【Mg2(OH)2CO3】粉末抹在手掌以增大摩擦力。
①参照上述方法,碱式碳酸镁的化学式可改写为__________。
②该物质兼具__________(填“酸”或“碱”)和碳酸盐的化学性质。
③该物质分解的化学方程式为 ,X的化学式为__________。
(2)某种茶垢清洁剂的主要成分为过碳酸钠(可表示为2Na2CO3·3H2O2)。将过碳酸钠溶解于热水中,有大量气泡产生,其原因是________;当不再产生气泡后,往溶液中加入足量澄清石灰水,反应的化学方程式为__________。
5.(2022·福建·统考中考真题)钙是人体必需元素。
(1)下图为钙元素在元素周期表中的部分信息。钙元素的相对原子质量为_______,钙原子的核外电子数为_______。
(2)牛奶、豆类等食物含钙丰富,这里的“钙”指的是_______(填“单质”“元素”或“原子”)。
(3)人体若缺钙,可服用补钙剂。
①缺钙可能导致的健康问题是_______(填“骨质疏松”或“贫血”)。
②服用主要成分为CaCO3的某钙片,与胃酸(含有HCl)反应后钙才能被吸收。该反应的化学方程式为_______。
6.(2022·福建·统考中考真题)水是生命之源。通常所说的水为H2O,而更广义的水还包括矿物中的氢氧基团(OH)、其他形式的氢(H),它们在高温下才以水分子的形式释放出来。A~C是氢、氧原子及其构成微粒的示意图。
(1)一定条件下由A生成C的化学方程式为____。A→B→C的变化过程中,不变的是__。
(2)参照上图微粒表示方法,画出“氢氧基团(OH)和氢(H)结合成水分子”的微观示意图:___。
(3)科研工作者将“嫦娥五号”采集的月球玄武岩中的磷灰石分解,其化学方程式为。则X的化学式为____。
(4)理论上,通过测量外星球矿样中氢元素的质量,可换算出矿样中水的质量。若1.0g某矿样含氢的质量为8.0×10-5g,则含水的质量m(H2O)=____g
7.(2022·福建·统考中考真题)兴趣小组用稀盐酸清洗铁夹表面的铁锈(主要成分为氧化铁),并进行保护实验。
(1)除铁锈的反应属于_______(填基本反应类型)。
(2)铁夹在稀盐酸中浸泡较长时间,有气体产生。产生气体的化学方程式为_______。
(3)将清洗过的铁夹进行“发蓝”处理,形成致密的氧化物保护膜,其主要成分与铁在氧气中燃烧的产物相同,该氧化物的化学式为_______。
(4)验证废液显酸性,可选用的一种试剂或用品是_______。
(5)用氢氧化钠中和废液中的盐酸,反应的化学方程式为_______。
8.(2023·福建·统考中考真题)福建盛产茶叶,茶文化源远流长。为了了解茶叶的组成和作用,学习小组查得某茶叶样品的成分及含量如下图所示:
(1)茶叶属于_________________(填“纯净物”或“混合物”),其中含量最高的基本营养素是___________________。
(2)茶多酚具有强血管、降血脂的作用。某种茶多酚的化学式为C6H6O2,其氢、氧元素的质量比为_________________。
(3)茶叶含氟较高,对预防龋齿有一定效果。这里的“氟”指的是_________________(填“元素”或“单质”)。
(4)茶叶中的硒有防癌作用。硒在元素周期表中的部分信息如图所示,硒原子的核外电子数为_________________。
9.(2023·福建·统考中考真题)中国科学家首次从月壤样品中发现新矿物——嫦娥石。学习小组查得资料:嫦娥石是从月壤样品的14万个颗粒中,利用针尖和颗粒之间静电吸附作用,分离出的一个粒径约1.0×10-5m的单晶颗粒,其化学式Ca9NaMg(PO4)7。请和小组同学起研究。
(1)嫦娥石的吸附分离过程属于________________(填“物理变化”或“化学变化”)。
(2)嫦娥石由_________________种元素组成。
(3)围绕“人类在月球上生活”的话题,展开月球上嫦娥石应用的讨论:
①助力农业生产:嫦娥石可作为生产________________(填“氮肥”“磷肥”或“钾肥”)的原料。
②提炼金属单质:若用107.2g嫦娥石提炼金属镁,最多可得镁的质量为________________g(嫦娥石的相对分子质量为1072)。
③展望更多应用:根据嫦娥石的组成推测,其可能另有的用途是________________(填一种)。
10.(2023·福建·统考中考真题)为探析化学反应的微观过程,学习小组查得资料:福建学者揭示了硼基催化剂催化甲烷与氧气反应生成X、Y和Z等的过程,局部过程的微观示意图如下(“…”表示省略相关过程)。请和小组同学一起研究。
(1)主要成分为甲烷的化石燃料是_________________(填一种)。
(2)X为一氧化碳分子,参照上图,画出该分子的微观示意图:_________________。
(3)B2O3中氧元素的化合价为-2,则硼元素的化合价为_________________。
(4)甲烷与氧气在催化剂作用下生成Z和水,反应的化学方程式为_________________。
(5)生成Y的过程如图中虚线框所示,且各微粒数比为1:1:1:1,则Y的化学式为_________________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1. 7:16 1 2 分别将燃着的木条深入两瓶气体中,若木条熄灭,则说明该气体是模拟“火星低层大气”组成的气体,若木条燃烧无明显变化,则该气体是空气。 b
【详解】(1)①CaAl2Si2O8中,Si、O两种元素的质量比为(28×2):(16×8)=7:16。
②由氦在元素周期表中的部分信息可知氦的原子序数为2,即氦原子核内的质子数为2,又氦-3原子的质子数与中子数之和为3,故其中子数为3-2=1,核外电子数=核内质子数=2。
(2)分析信息可知水在光催化下分解得到氧气和氢气,故反应方程式为:。
(3)①空气中二氧化碳约占总体积的0.03%,而模拟“火星低层大气”组成的气体中二氧化碳气体的体积含量是95.32%,故可根据二氧化碳不能燃烧也不能燃烧的性质进行鉴别。具体操作方法是:分别将燃着的木条深入两瓶气体中,若木条熄灭,则说明该气体是模拟“火星低层大气”组成的气体,若木条燃烧无明显变化,则该气体是空气。
②a. 模拟“火星低层大气”组成的气体中氧气含量比空气中少,且二氧化碳中含有氧元素,可通过将二氧化碳转化为氧气,以提高氧气的含量,此选项设想合理;
b.二氧化碳中不含氮元素,故无法将二氧化碳转化为氮气,此设想不合理;
c.水是人类生存不可缺少的物质,故应寻找水的存在和开发水循环技术,此设想合理;
d.火星拥有丰富的金属矿物,故可利用火星上的金属矿物冶炼金属供人类使用,此设想合理。故选b。
2. +5 含碳量 化学变化 隔绝氧气和水
【详解】(1)①磷酸铁中铁元素显+3价,氧元素显-2价,设磷元素的化合价为x,根据化合物中,正、负化合价的代数和为零,可得:(+3)+x+(-2)×4=0,x=+5;
②一氧化碳与氧化铁在高温下反应生成铁和二氧化碳,该反应的化学方程式为:;
③碳能与氧气在点燃的条件下反应生成二氧化碳,炼钢中“充氧”的目的是降低生铁中的含碳量,获得性能更好的钢;
(2)①“发蓝”过程有金属氧化物生成,属于化学变化;
②铁生锈的条件是铁与氧气和水接触,致密氧化膜能防止钢铁锈蚀的原因是:隔绝氧气和水。
3. 蒸发结晶 150 海水中氯化钠浓度低,浪费燃料 3.8 没有 20℃时,100g水中最多能溶解54.8g氯化镁,而该溶液中氯化镁只有7.65g,能全部溶解
【详解】(1)“晒结浮白”是指海水浸渍的草灰经日晒后出现白色海盐颗粒的过程,化学上称之为蒸发结晶;
(2)①1000g“上等卤水”蒸干后,可得氯化钠的质量约为:1000g×15%=150g;
②用获得的“上等卤水”而不直接用海水煎炼海盐的原因是:海水中氯化钠浓度低,浪费燃料;
③20℃时,氯化钠的溶解度为36.0g,即该温度下,100g水中只能溶解36.0g氯化钠,故将150g此溶液降温至20℃,有39.8g-36.0g=3.8g氯化钠析出;
没有氯化镁析出,因为100℃时,氯化镁的溶解度为73.0g,20℃时,氯化镁的溶解度为54.8g,即20℃时,100g水中最多能溶解54.8g氯化镁,而该溶液中氯化镁只有7.65g,能全部溶解。
4. Mg(OH)2·MgCO3 碱 MgO 过氧化氢受热分解生成水和氧气
【详解】(1)①碱式碳酸镁的化学式可改写为Mg(OH)2·MgCO3;
②该物质兼具氢氧化镁和碳酸镁的化学性质,氢氧化镁是电离时产生的阴离子都是氢氧根离子的化合物,属于碱,碳酸镁是由镁离子和碳酸根离子构成的化合物,属于碳酸盐,故填:碱;
③根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含Mg、O、H、C的个数分别是2、5、2、1,生成物中含Mg、O、H、C的个数分别是0、3、2、1,故生成物中还应含2个Mg、2个O,故X的化学式为:MgO;
(2)过碳酸钠兼具碳酸钠和过氧化氢的化学性质,将过碳酸钠溶解于热水中,有大量气泡产生,其原因是:过氧化氢受热分解生成水和氧气;
当不再产生气泡后,往溶液中加入足量澄清石灰水,氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠,该反应的化学方程式为:。
5.(1) 40.08 20
(2)元素
(3) 骨质疏松
【详解】(1)根据元素周期表标签最下面数字表示相对原子质量,故如图可知钙元素的相对原子质量为40.08,故填:40.08;
根据元素周期表标签左上角数字表示原子序数,原子序数等于质子数等于原子的核外电子数,如图可知钙原子的核外电子数为20,故填:20;
(2)牛奶、豆类等食物含钙丰富,这里的“钙”指的是钙元素,故填:元素;
(3)①人体的骨骼主要含钙元素,故人体缺钙儿童会引起佝偻病,成年人会引起骨质疏松,故填:骨质疏松;
②碳酸钙和胃液中的盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:。
6.(1) 氢原子和氧原子(或H、O)
(2)
(3)H2O
(4)7.2×10-4
【详解】(1)如图可知A中的物质是氢气和氧气,C是水,故氢气和氧气在一定条件下反应生成水的化学方程式为:;如图反应过程中氢分子分解为氢原子,氧分子分解为氧原子,氢原子和氧原子再从新结合,故反应过程中不变的是氢原子和氧原子,故填:氢原子和氧原子或H、O;
(2)“氢氧基团(OH)和氢(H)结合成水分子”的微观示意图:
(3)根据质量守恒定律反应前后原子的种类和个数不变,反应前钙原子、磷原子、氧原子、氢原子的个数分别是10、6、26、2,反应后钙原子、磷原子、氧原子、氢原子的个数分别是10、6、25、0,故X中含有2个氢原子和1个氧原子,则X的化学式为:;
(4)1.0g某矿样含水的质量是,故填:。
7.(1)复分解反应
(2)
(3)Fe3O4
(4)pH试纸(或“石蕊溶液”等)
(5)
【详解】(1)盐酸除铁锈是盐酸和氧化铁反应生成氯化铁和水,化学方程式为:,该反应是两种化合物互相交换成分生成两外两种化合物,属于复分解反应,故填:复分解反应;
(2)铁和稀盐酸反应生成氯化亚铁和氢气,化学方程式:;
(3)铁在氧气中燃烧生成四氧化三铁,故铁夹进行“发蓝”处理,形成致密的氧化物的化学式是:;
(4)根据酸性溶液pH<7,使用pH试纸可以测出或是酸性溶液能使石蕊试液变红,故可选用紫色石蕊试液,故填:pH试纸(或“石蕊溶液”等);
(5)氢氧化钠和盐酸反应生成氯化钠和水,化学方程式为:。
8.(1) 混合物 蛋白质
(2)3:16
(3)元素
(4)34
【详解】(1)由图知,茶叶含茶多酚、蛋白质等多种物质,属于混合物。基本营养素为糖类、油脂、蛋白质、维生素、无机盐和水,茶叶中含量最高的基本营养素是蛋白质。
(2)由茶多酚的化学式C6H6O2知,其氢、氧元素的质量比为(1×6):(16×2)=3:16。
(3)这里的“氟”不是强调以单质、分子、原子等形式存在,是强调存在的元素,与具体形态无关。
(4)由元素周期表一格知,左上角的数字为原子序数,原子中原子序数等于核外电子数,则硒原子的核外电子数为34。
9.(1)物理变化
(2)5/五
(3) 磷肥 2.4 制取氧气(或其他合理答案)
【详解】(1)嫦娥石的吸附分离过程没有产生新物质,属于物理变化。
(2)嫦娥石的化学式为:Ca9NaMg(PO4)7,由Ca、Na、Mg、P、O五种元素组成。
(3)①嫦娥石中含有磷元素,所以可作为生产磷肥的原料。
②若用107.2g嫦娥石提炼金属镁,最多可得镁的质量=。
③嫦娥石中含有氧元素,所以可以用来作为制取氧气的原料。(合理即可)
10.(1)天然气(或其他合理答案)
(2)
(3)+3
(4)
(5)C2H6
【详解】(1)天然气的主要成分是甲烷。
(2)X为一氧化碳分子,一个一氧化碳分子由1个碳原子和1个氢原子构成,故微观示意图为:。
(3)B2O3中氧元素的化合价为-2,设硼元素的化合价是x,根据在化合物中正负化合价代数和为零,可知2x+(-2)×3=0,则x=+3。
(4)甲烷与氧气在催化剂作用下生成Z和水,根据微观示意图可知Z是CH2O,故化学方程式为:。
(5)虚线框中是-CH3和CH4生成Y和-H,各微粒数比为1:1:1:1,则反应物中有两个碳原子和七个氢原子,生成物有一个氢原子,所以Y的化学式为C2H6。
答案第1页,共2页
答案第1页,共2页
同课章节目录
