第一章 有机化合物的结构与性质--烃 检测题 (含答案)高二下学期化学鲁科版(2019)选择性必修3
文档属性
| 名称 | 第一章 有机化合物的结构与性质--烃 检测题 (含答案)高二下学期化学鲁科版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-01 00:00:00 | ||
图片预览




文档简介
第一章《有机化合物的结构与性质—烃》检测题
一、单选题(共13题)
1.化学用语是化学必备知识之一,下列化学用语的表示正确的是
A.硝基苯的结构简式:
B.基态Fe3+价电子排布式为3d5
C.CH2=CH2分子中含有2个π键
D.基态碳原子价电子轨道表示式为
2.一种2-甲基色酮内酯(Y)可通过下列反应合成,下列说法正确的是
A.一定条件下,X可以发生加成、缩聚、消去、氧化反应
B.X、Y分子中所有碳原子均可能处于同一平面
C.1molX最多能与含4molBr2的浓溴水发生反应
D.Y与H2完全加成,每个产物分子中含有6个手性碳原子
3.2005年度的诺贝尔化学奖分别奖给美国和法国的三位科学家,表彰他们对“烯烃复分 解”反应研究方面作出的贡献。“烯烃复分解”是指在金属钨或钼等催化剂的作用下,碳碳双键断裂并重新组合的过程。例如:
+ → +
则对于有机物CH2=CHCH2CH=CH2发生烯烃复分解反应时可能生成产物的判断中正确的 是( )
① ②CH2=CH2 ③ ④CH2=C=CH2
A.只有③ B.只有②③ C.只有①②③ D.只有④
4.维生素B5的结构如图所示,下列有关维生素B5的说法正确的是
A.分子内不存在手性碳原子
B.一定条件下能发生缩聚反应
C.不能使酸性KMnO4溶液褪色
D.分子内有5种官能团
5.下列对实验方案的评价合理的是
选项 实验方案 评价
A 除去溴苯中的少量溴单质:用NaOH溶液洗涤、分液 错误,Br2不会与NaOH溶液反应
B 分离乙醇和乙酸:加入过量氢氧化钠,蒸馏分离出乙醇,再加入过量浓硫酸,蒸馏分离出乙酸 错误,直接蒸馏即可分离得到纯净的乙醇和乙酸
C 提取饱和碘水中的碘单质:用乙醇萃取 正确,单质碘易溶于乙醇等有机溶剂
D 除去乙烷中混有的少量乙烯:用溴水洗气 正确,乙烯能与溴水发生加成反应
A.A B.B C.C D.D
6.某有机物结构简式为,关于该有机物叙述不正确的是
A.能使酸性KMnO4溶液褪色 B.能使溴水褪色
C.在加热和催化剂作用下,最多与5molH2反应 D.能发生取代反应
7.设NA为阿伏加德罗常数的值.下列说法正确的是
A.1L0.01mol L-1氯水中含有的Cl-、HClO和ClO-的总数为0.02NA
B.7.8g苯中含有的σ键数目为0.6NA
C.58g23Na35Cl中含有的中子数目为28NA
D.由CoO制得1molCo3O4时转移的电子数目为2NA
8.下列叙述不正确的是
A.乙烷可以与氯气发生取代反应 B.聚乙烯可以用作生产食品包装材料的原料
C.环己烷与溴苯可用水来签别 D.汽油和甘油属于同一类的有机物
9.下列说法或表示方法正确的是
A.C2H4O的结构简式为
B.键线式为的有机物不存在顺反异构
C.氯溴碘代甲烷的两种对映异构体如图:
D.与互为同分异构体
10.关于CH3CH3、CH3-O-CH3和CH3CHO的结构与性质,下列说法正确的是
A.三种有机物中碳原子的杂化方式完全相同
B.CH3- O- CH3和CH3CH3均为非极性分子
C.CH3CHO分子中所有原子共平面
D.三种分子形成的晶体均为分子晶体
11.下列说法不正确的是
A.苯和溴水在铁作催化剂的条件可以制取溴苯
B.煤通过干馏,可以得到苯 、甲苯、二甲苯等有机化合物
C.油脂可以制造肥皂和油漆等
D.化学式为C9H18O2且有芳香气味的有机物,在酸性条件下 加热水解产生相对分子质量相同的两种有机物,则符合此条件的C9H18O2的结构有16种
12.奥司他韦可以用于治疗流行性感冒,其结构如图所示。下列关于奥司他韦的说法正确的是
A.含有4个手性碳原子
B.1mol奥司他韦最多能与3mol发生加成反应
C.存在芳香族化合物的同分异构体
D.分子中至少有7个碳原子共平面
13.有机化合物含有的官能团有
A.3种 B.4种 C.5种 D.6种
二、非选择题(共10题)
14.按要求填空:
(1)官能团-COOH的名称是_______;
(2)(CH3CH2)2C(CH3)2的名称为_______;
(3)ClCH=CH-CH=CH2所含官能团的名称是_______;
(4)乙烯在一定条件下发生反应:CH2=CH2+H2OCH3CH2OH,该反应的类型是_____反应
15.现有下列几种有机物。按要求答题。
(1)分子式为的烯烃有___________种。
(2)的一氯代物有___________种。
(3)用系统命名法命名有机物___________。
(4)有机物的分子式为___________。
(5)根据有机物名称写出相应的结构简式:2,2,5-三甲基-3-乙基己烷___________。
(6)中含有的官能团的名称为___________、___________。
三、实验题
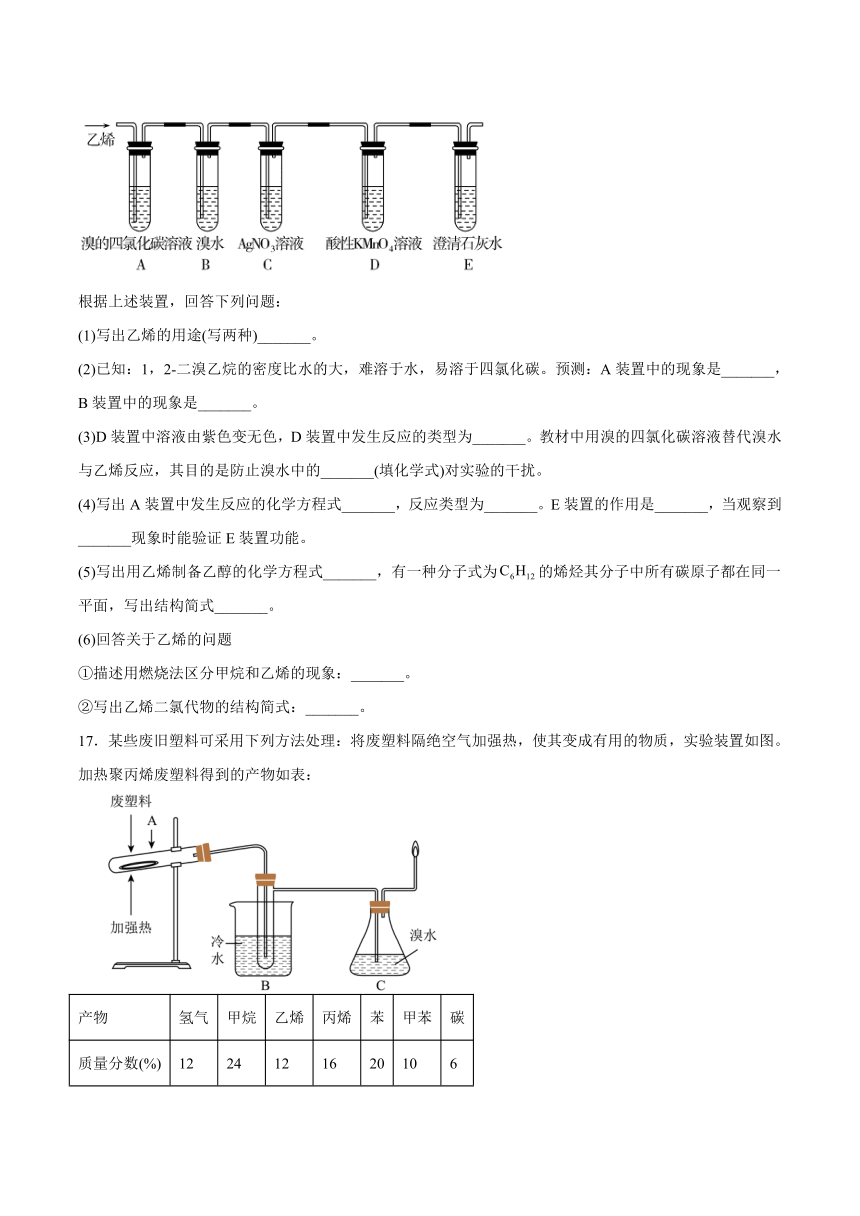
16.在炽热条件下,将石蜡油分解产生的乙烯通入下列各试管里,装置如图所示。
根据上述装置,回答下列问题:
(1)写出乙烯的用途(写两种)_______。
(2)已知:1,2-二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。预测:A装置中的现象是_______,B装置中的现象是_______。
(3)D装置中溶液由紫色变无色,D装置中发生反应的类型为_______。教材中用溴的四氯化碳溶液替代溴水与乙烯反应,其目的是防止溴水中的_______(填化学式)对实验的干扰。
(4)写出A装置中发生反应的化学方程式_______,反应类型为_______。E装置的作用是_______,当观察到_______现象时能验证E装置功能。
(5)写出用乙烯制备乙醇的化学方程式_______,有一种分子式为的烯烃其分子中所有碳原子都在同一平面,写出结构简式_______。
(6)回答关于乙烯的问题
①描述用燃烧法区分甲烷和乙烯的现象:_______。
②写出乙烯二氯代物的结构简式:_______。
17.某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图。加热聚丙烯废塑料得到的产物如表:
产物 氢气 甲烷 乙烯 丙烯 苯 甲苯 碳
质量分数(%) 12 24 12 16 20 10 6
(1)试管A中残余物有多种用途,如图列转化就可制取高聚物聚乙炔。
A中残留物电石乙炔聚乙炔
写出反应③的化学方程式:__。
(2)试管B收集到的产品中,能使高锰酸钾酸性溶液褪色的物质,其一氯代物有___种。
(3)锥形瓶C中观察到的现象___。
(4)写出C中逸出的气体在工业上的两种用途:__。
18.乙醛是有机化工的重要原料,由于乙醇氧化法要消耗大量粮食,工业上常采用以下方法合成乙醛:
(1)乙炔水化法:在75℃左右,用做催化剂,乙炔可水化为乙醛,但遇到某些特定物质常会发生催化剂中毒而失去催化作用,就是其中一种。实验装置如图所示:
已知:F装置中已按顺序加入了氧化汞、水、浓硫酸。
①实验开始时,仪器A中盛放电石,B中应装_______。
②仪器D中盛放水,作用是_______,进一步提纯乙醛的操作是_______。
③装置图中,所选用温度计G的量程为_______(填标号)。
A.0~50℃ B.0~100℃ C.0~200℃
(2)乙烯氧化法:将乙烯、氧气和催化剂(和盐酸的混合溶液),在温度120~130℃,压力0.3MPa条件下,直接反应生成乙醛。下表是这两种方法的部分数据
物质/项目 乙炔水化法 乙烯氧化法
平衡转化率 乙炔平衡转化率90%左右 乙烯平衡转化率80%左右
日产量 2.5吨(某设备条件下) 3.6吨(相同设备条件下)
从化学反应速率角度分析,在相同设备条件下,选用_______法制取乙醛快。
(3)以上反应都用到了催化剂,Cu、Fe、Ni、Pd、Hg等元素都是催化剂的重要元素,关于这些元素以下说法正确的是_______(填标号)。
A.向2mL10%的NaOH溶液中滴入2%的溶液4滴,振荡后加入0.5mL乙醛溶液,加热,有红色沉淀生成,说明乙醛有氧化性
B.向硫酸亚铁溶液中滴加溶液,溶液变蓝
C.把铬、镍等加入普通钢中制成不锈钢是一种金属防护方法
D.任何反应的催化剂必须含有过渡金属元素
四、计算题
19.回答下列问题:
(1)分子式为C3H6的化合物X具有如下性质:X+溴的四氯化碳溶液→使溴的四氯化碳溶液褪色。 X所含官能团的名称_______,X与溴的四氯化碳溶液反应的化学方程式_______,X发生加聚反应的化学方程式为_______。
(2)标准状况下1mol某烃完全燃烧时,生成89.6LCO2,又知0.1mol此烃能与标准状况下4.48LH2加成,则此烃的结构简式可能是(两个碳碳双键连一起不稳定)_______。
(3)一种能使溴水褪色的烃,标准状况下5.6 L 完全燃烧时生成28L二氧化碳和22.5g水。则该烃的结构简式有_______种(不考虑顺反异构)。
(4)分子式为C6H14的化合物的同分异构体中,写出其中含有四个甲基的物质的结构简式为_______。
20.在25℃和101KPa时,乙烷、乙炔和丙烯组成的混合烃32mL,与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小了72mL,原混合烃中乙炔的体积分数是_____。
21.以天然气、焦炭、水为初始原料,可以制得CO和H2,进而人工合成汽油。(流程示意图如下,反应③的H2也由反应①得到。)
若反应①、②、③的转化率均为100%,且将反应①中得到的CO2和H2全部用于合成人工汽油。
(1)通过计算说明上述方案能否得到理想的产品_______________。
(2)当CO2的使用量应控制为反应①中CO2产量的______________(填比例范围),可以得到理想的产品。
22.A、B、C、D、E五种短周期元素,A是周期表中原子半径最小的元素,其中B、C同周期,B、D同主族,原子半径E>D>B>C>A。D原子核内质子数等于B、C原子电子数之和,D原子最外层电子数是E原子最外层电子数的4倍。试回答:
(1)B与C形成的三原子分子甲的结构式是___________,C与E形成的原子个数比为1∶1的化合物乙的电子式是___________,乙物质中含有的共价键是___________(填“极性”或“非极性”)
(2)B的简单氢化物与氯气的第一步反应的方程式为___________;
(3)A和B可以形成一类化合物.这类化合物中,其中丙是一种重要的基本化工原料,其产量可以用来衡量一个国家的石油化工发展水平,写出由丙制得高聚物的反应方程式___________,该反应类型是___________;其中丁的相对分子质量为120,不能使溴的四氯化碳溶液褪色,其一氯代物只有两种结构,丁的结构简式为___________.
23.下图表示各物质之间的转化关系。已知:A、B、I都是XY2型化合物,且阳离子相同,A、B晶体中阴、阳离子个数比都是1∶1,但I晶体中阴、阳离子个数比是2∶1,I常用作干燥剂。
请按要求填空:
(1)I的电子式是___________;
(2)反应⑥的化学方程式是__________,反应③在工业上的一个重要用途是___________;
(3)反应④的化学方程式是_____________________;
(4)根据上图中物质之间的转化关系及题中所给信息判断,B的化学式是___________。
参考答案:
1.B 2.D 3.C 4.B 5.D 6.C 7.D 8.D 9.C 10.D 11.A 12.C 13.C
14. 羧基 3,3-二甲基戊烷 碳碳双键、氯原子 加成
15.(1)5
(2)5
(3)2-甲基-3-乙基戊烷
(4)C9H10O3
(5)
(6) 酚羟基 酯基
16.(1)制备聚乙烯、果实催熟、合成乙醇等(合理就可)
(2) 红棕色褪去,液体不分层 橙黄色褪去,液体分层
(3) 氧化反应 HBrO
(4) 加成反应 检验乙烯与酸性溶液反应的产物二氧化碳 澄清石灰水变浑浊
(5)
(6) 甲烷燃烧是淡蓝色火焰,无黑烟;乙烯燃烧是明亮的火焰,有少量黑烟 、
17. nCHCH 4 黄色溶液变为无色或颜色变浅 合成氨原料;作燃料或有机化工原料
18.(1) 溶液或NaOH溶液 冷却并吸收乙醛蒸气 蒸馏 B
(2)乙烯氧化法
(3)C
19.(1) 碳碳双键 CH3CH=CH2+Br2 n CH3CH=CH2
(2)HC≡CCH2CH3、CH3 C≡CCH3、CH2=CHCH=CH2
(3)5
(4)
20.25%
21. 不能得到理想产品
22.(1) O=C=O 非极性
(2)CH4+Cl2CH3Cl+HCl
(3) nCH2═CH2 加聚反应 、
23. Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO 制漂白粉或漂白精 2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O CaO2
一、单选题(共13题)
1.化学用语是化学必备知识之一,下列化学用语的表示正确的是
A.硝基苯的结构简式:
B.基态Fe3+价电子排布式为3d5
C.CH2=CH2分子中含有2个π键
D.基态碳原子价电子轨道表示式为
2.一种2-甲基色酮内酯(Y)可通过下列反应合成,下列说法正确的是
A.一定条件下,X可以发生加成、缩聚、消去、氧化反应
B.X、Y分子中所有碳原子均可能处于同一平面
C.1molX最多能与含4molBr2的浓溴水发生反应
D.Y与H2完全加成,每个产物分子中含有6个手性碳原子
3.2005年度的诺贝尔化学奖分别奖给美国和法国的三位科学家,表彰他们对“烯烃复分 解”反应研究方面作出的贡献。“烯烃复分解”是指在金属钨或钼等催化剂的作用下,碳碳双键断裂并重新组合的过程。例如:
+ → +
则对于有机物CH2=CHCH2CH=CH2发生烯烃复分解反应时可能生成产物的判断中正确的 是( )
① ②CH2=CH2 ③ ④CH2=C=CH2
A.只有③ B.只有②③ C.只有①②③ D.只有④
4.维生素B5的结构如图所示,下列有关维生素B5的说法正确的是
A.分子内不存在手性碳原子
B.一定条件下能发生缩聚反应
C.不能使酸性KMnO4溶液褪色
D.分子内有5种官能团
5.下列对实验方案的评价合理的是
选项 实验方案 评价
A 除去溴苯中的少量溴单质:用NaOH溶液洗涤、分液 错误,Br2不会与NaOH溶液反应
B 分离乙醇和乙酸:加入过量氢氧化钠,蒸馏分离出乙醇,再加入过量浓硫酸,蒸馏分离出乙酸 错误,直接蒸馏即可分离得到纯净的乙醇和乙酸
C 提取饱和碘水中的碘单质:用乙醇萃取 正确,单质碘易溶于乙醇等有机溶剂
D 除去乙烷中混有的少量乙烯:用溴水洗气 正确,乙烯能与溴水发生加成反应
A.A B.B C.C D.D
6.某有机物结构简式为,关于该有机物叙述不正确的是
A.能使酸性KMnO4溶液褪色 B.能使溴水褪色
C.在加热和催化剂作用下,最多与5molH2反应 D.能发生取代反应
7.设NA为阿伏加德罗常数的值.下列说法正确的是
A.1L0.01mol L-1氯水中含有的Cl-、HClO和ClO-的总数为0.02NA
B.7.8g苯中含有的σ键数目为0.6NA
C.58g23Na35Cl中含有的中子数目为28NA
D.由CoO制得1molCo3O4时转移的电子数目为2NA
8.下列叙述不正确的是
A.乙烷可以与氯气发生取代反应 B.聚乙烯可以用作生产食品包装材料的原料
C.环己烷与溴苯可用水来签别 D.汽油和甘油属于同一类的有机物
9.下列说法或表示方法正确的是
A.C2H4O的结构简式为
B.键线式为的有机物不存在顺反异构
C.氯溴碘代甲烷的两种对映异构体如图:
D.与互为同分异构体
10.关于CH3CH3、CH3-O-CH3和CH3CHO的结构与性质,下列说法正确的是
A.三种有机物中碳原子的杂化方式完全相同
B.CH3- O- CH3和CH3CH3均为非极性分子
C.CH3CHO分子中所有原子共平面
D.三种分子形成的晶体均为分子晶体
11.下列说法不正确的是
A.苯和溴水在铁作催化剂的条件可以制取溴苯
B.煤通过干馏,可以得到苯 、甲苯、二甲苯等有机化合物
C.油脂可以制造肥皂和油漆等
D.化学式为C9H18O2且有芳香气味的有机物,在酸性条件下 加热水解产生相对分子质量相同的两种有机物,则符合此条件的C9H18O2的结构有16种
12.奥司他韦可以用于治疗流行性感冒,其结构如图所示。下列关于奥司他韦的说法正确的是
A.含有4个手性碳原子
B.1mol奥司他韦最多能与3mol发生加成反应
C.存在芳香族化合物的同分异构体
D.分子中至少有7个碳原子共平面
13.有机化合物含有的官能团有
A.3种 B.4种 C.5种 D.6种
二、非选择题(共10题)
14.按要求填空:
(1)官能团-COOH的名称是_______;
(2)(CH3CH2)2C(CH3)2的名称为_______;
(3)ClCH=CH-CH=CH2所含官能团的名称是_______;
(4)乙烯在一定条件下发生反应:CH2=CH2+H2OCH3CH2OH,该反应的类型是_____反应
15.现有下列几种有机物。按要求答题。
(1)分子式为的烯烃有___________种。
(2)的一氯代物有___________种。
(3)用系统命名法命名有机物___________。
(4)有机物的分子式为___________。
(5)根据有机物名称写出相应的结构简式:2,2,5-三甲基-3-乙基己烷___________。
(6)中含有的官能团的名称为___________、___________。
三、实验题
16.在炽热条件下,将石蜡油分解产生的乙烯通入下列各试管里,装置如图所示。
根据上述装置,回答下列问题:
(1)写出乙烯的用途(写两种)_______。
(2)已知:1,2-二溴乙烷的密度比水的大,难溶于水,易溶于四氯化碳。预测:A装置中的现象是_______,B装置中的现象是_______。
(3)D装置中溶液由紫色变无色,D装置中发生反应的类型为_______。教材中用溴的四氯化碳溶液替代溴水与乙烯反应,其目的是防止溴水中的_______(填化学式)对实验的干扰。
(4)写出A装置中发生反应的化学方程式_______,反应类型为_______。E装置的作用是_______,当观察到_______现象时能验证E装置功能。
(5)写出用乙烯制备乙醇的化学方程式_______,有一种分子式为的烯烃其分子中所有碳原子都在同一平面,写出结构简式_______。
(6)回答关于乙烯的问题
①描述用燃烧法区分甲烷和乙烯的现象:_______。
②写出乙烯二氯代物的结构简式:_______。
17.某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图。加热聚丙烯废塑料得到的产物如表:
产物 氢气 甲烷 乙烯 丙烯 苯 甲苯 碳
质量分数(%) 12 24 12 16 20 10 6
(1)试管A中残余物有多种用途,如图列转化就可制取高聚物聚乙炔。
A中残留物电石乙炔聚乙炔
写出反应③的化学方程式:__。
(2)试管B收集到的产品中,能使高锰酸钾酸性溶液褪色的物质,其一氯代物有___种。
(3)锥形瓶C中观察到的现象___。
(4)写出C中逸出的气体在工业上的两种用途:__。
18.乙醛是有机化工的重要原料,由于乙醇氧化法要消耗大量粮食,工业上常采用以下方法合成乙醛:
(1)乙炔水化法:在75℃左右,用做催化剂,乙炔可水化为乙醛,但遇到某些特定物质常会发生催化剂中毒而失去催化作用,就是其中一种。实验装置如图所示:
已知:F装置中已按顺序加入了氧化汞、水、浓硫酸。
①实验开始时,仪器A中盛放电石,B中应装_______。
②仪器D中盛放水,作用是_______,进一步提纯乙醛的操作是_______。
③装置图中,所选用温度计G的量程为_______(填标号)。
A.0~50℃ B.0~100℃ C.0~200℃
(2)乙烯氧化法:将乙烯、氧气和催化剂(和盐酸的混合溶液),在温度120~130℃,压力0.3MPa条件下,直接反应生成乙醛。下表是这两种方法的部分数据
物质/项目 乙炔水化法 乙烯氧化法
平衡转化率 乙炔平衡转化率90%左右 乙烯平衡转化率80%左右
日产量 2.5吨(某设备条件下) 3.6吨(相同设备条件下)
从化学反应速率角度分析,在相同设备条件下,选用_______法制取乙醛快。
(3)以上反应都用到了催化剂,Cu、Fe、Ni、Pd、Hg等元素都是催化剂的重要元素,关于这些元素以下说法正确的是_______(填标号)。
A.向2mL10%的NaOH溶液中滴入2%的溶液4滴,振荡后加入0.5mL乙醛溶液,加热,有红色沉淀生成,说明乙醛有氧化性
B.向硫酸亚铁溶液中滴加溶液,溶液变蓝
C.把铬、镍等加入普通钢中制成不锈钢是一种金属防护方法
D.任何反应的催化剂必须含有过渡金属元素
四、计算题
19.回答下列问题:
(1)分子式为C3H6的化合物X具有如下性质:X+溴的四氯化碳溶液→使溴的四氯化碳溶液褪色。 X所含官能团的名称_______,X与溴的四氯化碳溶液反应的化学方程式_______,X发生加聚反应的化学方程式为_______。
(2)标准状况下1mol某烃完全燃烧时,生成89.6LCO2,又知0.1mol此烃能与标准状况下4.48LH2加成,则此烃的结构简式可能是(两个碳碳双键连一起不稳定)_______。
(3)一种能使溴水褪色的烃,标准状况下5.6 L 完全燃烧时生成28L二氧化碳和22.5g水。则该烃的结构简式有_______种(不考虑顺反异构)。
(4)分子式为C6H14的化合物的同分异构体中,写出其中含有四个甲基的物质的结构简式为_______。
20.在25℃和101KPa时,乙烷、乙炔和丙烯组成的混合烃32mL,与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小了72mL,原混合烃中乙炔的体积分数是_____。
21.以天然气、焦炭、水为初始原料,可以制得CO和H2,进而人工合成汽油。(流程示意图如下,反应③的H2也由反应①得到。)
若反应①、②、③的转化率均为100%,且将反应①中得到的CO2和H2全部用于合成人工汽油。
(1)通过计算说明上述方案能否得到理想的产品_______________。
(2)当CO2的使用量应控制为反应①中CO2产量的______________(填比例范围),可以得到理想的产品。
22.A、B、C、D、E五种短周期元素,A是周期表中原子半径最小的元素,其中B、C同周期,B、D同主族,原子半径E>D>B>C>A。D原子核内质子数等于B、C原子电子数之和,D原子最外层电子数是E原子最外层电子数的4倍。试回答:
(1)B与C形成的三原子分子甲的结构式是___________,C与E形成的原子个数比为1∶1的化合物乙的电子式是___________,乙物质中含有的共价键是___________(填“极性”或“非极性”)
(2)B的简单氢化物与氯气的第一步反应的方程式为___________;
(3)A和B可以形成一类化合物.这类化合物中,其中丙是一种重要的基本化工原料,其产量可以用来衡量一个国家的石油化工发展水平,写出由丙制得高聚物的反应方程式___________,该反应类型是___________;其中丁的相对分子质量为120,不能使溴的四氯化碳溶液褪色,其一氯代物只有两种结构,丁的结构简式为___________.
23.下图表示各物质之间的转化关系。已知:A、B、I都是XY2型化合物,且阳离子相同,A、B晶体中阴、阳离子个数比都是1∶1,但I晶体中阴、阳离子个数比是2∶1,I常用作干燥剂。
请按要求填空:
(1)I的电子式是___________;
(2)反应⑥的化学方程式是__________,反应③在工业上的一个重要用途是___________;
(3)反应④的化学方程式是_____________________;
(4)根据上图中物质之间的转化关系及题中所给信息判断,B的化学式是___________。
参考答案:
1.B 2.D 3.C 4.B 5.D 6.C 7.D 8.D 9.C 10.D 11.A 12.C 13.C
14. 羧基 3,3-二甲基戊烷 碳碳双键、氯原子 加成
15.(1)5
(2)5
(3)2-甲基-3-乙基戊烷
(4)C9H10O3
(5)
(6) 酚羟基 酯基
16.(1)制备聚乙烯、果实催熟、合成乙醇等(合理就可)
(2) 红棕色褪去,液体不分层 橙黄色褪去,液体分层
(3) 氧化反应 HBrO
(4) 加成反应 检验乙烯与酸性溶液反应的产物二氧化碳 澄清石灰水变浑浊
(5)
(6) 甲烷燃烧是淡蓝色火焰,无黑烟;乙烯燃烧是明亮的火焰,有少量黑烟 、
17. nCHCH 4 黄色溶液变为无色或颜色变浅 合成氨原料;作燃料或有机化工原料
18.(1) 溶液或NaOH溶液 冷却并吸收乙醛蒸气 蒸馏 B
(2)乙烯氧化法
(3)C
19.(1) 碳碳双键 CH3CH=CH2+Br2 n CH3CH=CH2
(2)HC≡CCH2CH3、CH3 C≡CCH3、CH2=CHCH=CH2
(3)5
(4)
20.25%
21. 不能得到理想产品
22.(1) O=C=O 非极性
(2)CH4+Cl2CH3Cl+HCl
(3) nCH2═CH2 加聚反应 、
23. Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO 制漂白粉或漂白精 2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O CaO2
