人教版九年级化学 第五单元 课题1 质量守恒定律 课时2 质量守恒定律的应用课件(共16张PPT)
文档属性
| 名称 | 人教版九年级化学 第五单元 课题1 质量守恒定律 课时2 质量守恒定律的应用课件(共16张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 336.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-01 00:00:00 | ||
图片预览






文档简介
(共16张PPT)
第五单元 化学方程式
课题1 质量守恒定律
课时2 质量守恒定律的应用
目录
01
课程要求
02
课前预习
03
知识点精讲
04
课堂检测
1. 能运用质量守恒定律解决一些相关问题。
2. 能依据化学反应过程中元素不变的规律,推断反应物或生成物的元素组成。
计算下列常见物质的相对分子质量。
O2: 32 H2O: 18
CO2: 44 SO2: 64
CaO: 56 H2O2: 34
CaCO3: 100 H2SO4: 98
32
18
44
64
56
34
100
98
知识点 质量守恒定律的应用
1. 用质量差确定某反应物或生成物的质量。
2. 依据化学反应前后元素种类不变推断反应物或生成物的组成元素。
3. 解释反应前后物质的质量变化。
4. 根据化学反应前后原子的种类、数目不变,求化学方程式中反应物或生成物的化学式。
5. 揭露伪科学。
课堂练习
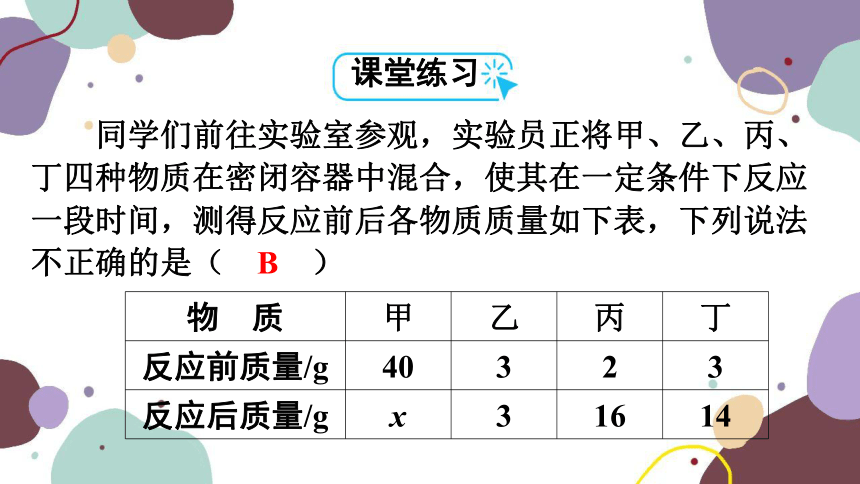
同学们前往实验室参观,实验员正将甲、乙、丙、丁四种物质在密闭容器中混合,使其在一定条件下反应一段时间,测得反应前后各物质质量如下表,下列说法不正确的是( B )
B
物 质 甲 乙 丙 丁
反应前质量/g 40 3 2 3
反应后质量/g x 3 16 14
A. 乙可能是催化剂
B. x的值为25
C. 该反应是分解反应
D. 生成的丙、丁质量之比为14 ∶11
思路点拨 根据质量守恒,反应前质量之和等于反应后质量之和,可以算出x的值。再看每种物质反应前后质量变化,质量增加的是生成物,质量减少的是反应物,质量不变的可能是催化剂,也可能根本没有参与反应。根据数据变化,写出反应表达式,变化的质量写在对应物质下面,就可以知道各物质的质量比。
1. 某化学反应可表示为二氧化碳+水→ M+氧气,据以上信息关于M的说法正确的( A )
A. 一定含有碳、氢元素,可能含有氧元素
B. 只含有碳、氢两种元素
C. 一定含有碳、氢、氧三种元素
D. 不能确定
A
2. 某纯净物X稍稍加热就分解成NH3、H2O和CO2,由此不能得出的结论是( C )
A. X不稳定 B. X是化合物
C. X中含有水 D. X由四种元素组成
C
3. (2022广州期末)一定条件下,密闭容器中发生了某一化学反应,涉及的物质为甲、乙、丙、丁,如图5-1-4为各物质在反应前和反应后某时刻的质量关系。下列说法不正确的是( B )
B
图5-1-4
A. x的值是31
B. 甲、丁的相对分子质量之比
为7 ∶11
C. 丙可能为催化剂
D. 反应中消耗甲和乙的质量比为7 ∶4
4. (2022衡阳)甲、乙、丙、丁四种物质在一定条件下充分混合,此时各物质的质量分数如图5-1-5Ⅰ所示。一段时间后,各物质的质量分数如图5-1-5Ⅱ所示。下列说法正确的是( A )
A
图5-1-5
A. 丁是反应物
B. x的值为20
C. 乙是此化学反应的催化剂
D. 生成38 g甲,需消耗60 g丁
5. 通过电催化的方式,可以在常压和低温下将氮气和水直接转化为氨气和氧气,如图5-1-6是该反应的微观示意图。
图5-1-6
(1)请将图5-1-6中第一、三个方框中的微观粒子补画齐全。
如答图5-1-1所示。
答图5-1-1
(2)第二个方框中的物质属于 化合物 (填“单质”“化合物”或“混合物”)。
化合物
(3)图中参加反应的粒子是 氮分子和水分子 (填粒子名称)。
氮分子和水分子
谢 谢!
第五单元 化学方程式
课题1 质量守恒定律
课时2 质量守恒定律的应用
目录
01
课程要求
02
课前预习
03
知识点精讲
04
课堂检测
1. 能运用质量守恒定律解决一些相关问题。
2. 能依据化学反应过程中元素不变的规律,推断反应物或生成物的元素组成。
计算下列常见物质的相对分子质量。
O2: 32 H2O: 18
CO2: 44 SO2: 64
CaO: 56 H2O2: 34
CaCO3: 100 H2SO4: 98
32
18
44
64
56
34
100
98
知识点 质量守恒定律的应用
1. 用质量差确定某反应物或生成物的质量。
2. 依据化学反应前后元素种类不变推断反应物或生成物的组成元素。
3. 解释反应前后物质的质量变化。
4. 根据化学反应前后原子的种类、数目不变,求化学方程式中反应物或生成物的化学式。
5. 揭露伪科学。
课堂练习
同学们前往实验室参观,实验员正将甲、乙、丙、丁四种物质在密闭容器中混合,使其在一定条件下反应一段时间,测得反应前后各物质质量如下表,下列说法不正确的是( B )
B
物 质 甲 乙 丙 丁
反应前质量/g 40 3 2 3
反应后质量/g x 3 16 14
A. 乙可能是催化剂
B. x的值为25
C. 该反应是分解反应
D. 生成的丙、丁质量之比为14 ∶11
思路点拨 根据质量守恒,反应前质量之和等于反应后质量之和,可以算出x的值。再看每种物质反应前后质量变化,质量增加的是生成物,质量减少的是反应物,质量不变的可能是催化剂,也可能根本没有参与反应。根据数据变化,写出反应表达式,变化的质量写在对应物质下面,就可以知道各物质的质量比。
1. 某化学反应可表示为二氧化碳+水→ M+氧气,据以上信息关于M的说法正确的( A )
A. 一定含有碳、氢元素,可能含有氧元素
B. 只含有碳、氢两种元素
C. 一定含有碳、氢、氧三种元素
D. 不能确定
A
2. 某纯净物X稍稍加热就分解成NH3、H2O和CO2,由此不能得出的结论是( C )
A. X不稳定 B. X是化合物
C. X中含有水 D. X由四种元素组成
C
3. (2022广州期末)一定条件下,密闭容器中发生了某一化学反应,涉及的物质为甲、乙、丙、丁,如图5-1-4为各物质在反应前和反应后某时刻的质量关系。下列说法不正确的是( B )
B
图5-1-4
A. x的值是31
B. 甲、丁的相对分子质量之比
为7 ∶11
C. 丙可能为催化剂
D. 反应中消耗甲和乙的质量比为7 ∶4
4. (2022衡阳)甲、乙、丙、丁四种物质在一定条件下充分混合,此时各物质的质量分数如图5-1-5Ⅰ所示。一段时间后,各物质的质量分数如图5-1-5Ⅱ所示。下列说法正确的是( A )
A
图5-1-5
A. 丁是反应物
B. x的值为20
C. 乙是此化学反应的催化剂
D. 生成38 g甲,需消耗60 g丁
5. 通过电催化的方式,可以在常压和低温下将氮气和水直接转化为氨气和氧气,如图5-1-6是该反应的微观示意图。
图5-1-6
(1)请将图5-1-6中第一、三个方框中的微观粒子补画齐全。
如答图5-1-1所示。
答图5-1-1
(2)第二个方框中的物质属于 化合物 (填“单质”“化合物”或“混合物”)。
化合物
(3)图中参加反应的粒子是 氮分子和水分子 (填粒子名称)。
氮分子和水分子
谢 谢!
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
