第三章 有机合成及其应用 合成高分子化合物 检测(含解析) 高二化学鲁科版(2019)选择性必修3
文档属性
| 名称 | 第三章 有机合成及其应用 合成高分子化合物 检测(含解析) 高二化学鲁科版(2019)选择性必修3 |  | |
| 格式 | docx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-04 08:47:11 | ||
图片预览


文档简介
第三章《有机合成及其应用 合成高分子化合物》检测题
一、单选题(共13题)
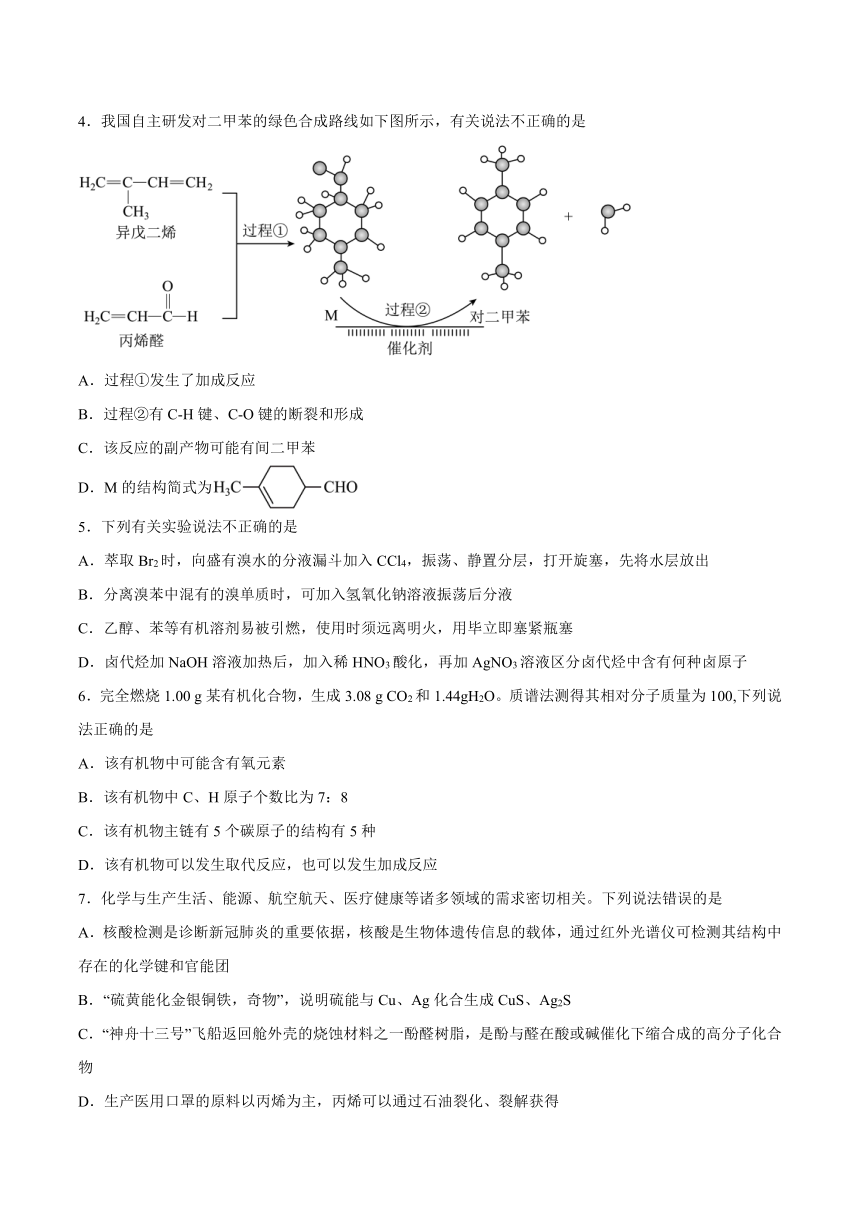
1.化合物Y是一种药物中间体,可由X制得。下列有关化合物X、Y的说法正确的是
A.1molX最多能与3mol反应 B.Y分子中所有碳原子可能处于同一平面
C.用溶液可以区分X、Y D.X、Y分子中手性碳原子数目不相等
2.聚乳酸是一种新型的生物可降解高分子材料,其合成路线如下:
下列说法正确的是
A.,乳酸变为聚乳酸为缩聚反应 B.聚乳酸分子中含有两种官能团
C.1mol乳酸与1mol Na反应生成1mol D.两分子乳酸反应能够生成含六元环的分子
3.下列操作能达到相应实验目的的是
实验目的 操作
A 检验绿茶中是否含有酚类物质 向茶水中滴加FeCl3溶液
B 判断某卤代烃中的卤素 取2 mL卤代烃样品于试管中,加入5 mL 20% KOH水溶液混合后加热,再滴加AgNO3溶液
C 除去苯中混有的少量苯酚 向苯和苯酚的混合物中滴加溴水,过滤后分液
D 实验室制备乙酸乙酯 向试管中依次加入浓硫酸、乙醇、乙酸和碎瓷片,加热
A.A B.B C.C D.D
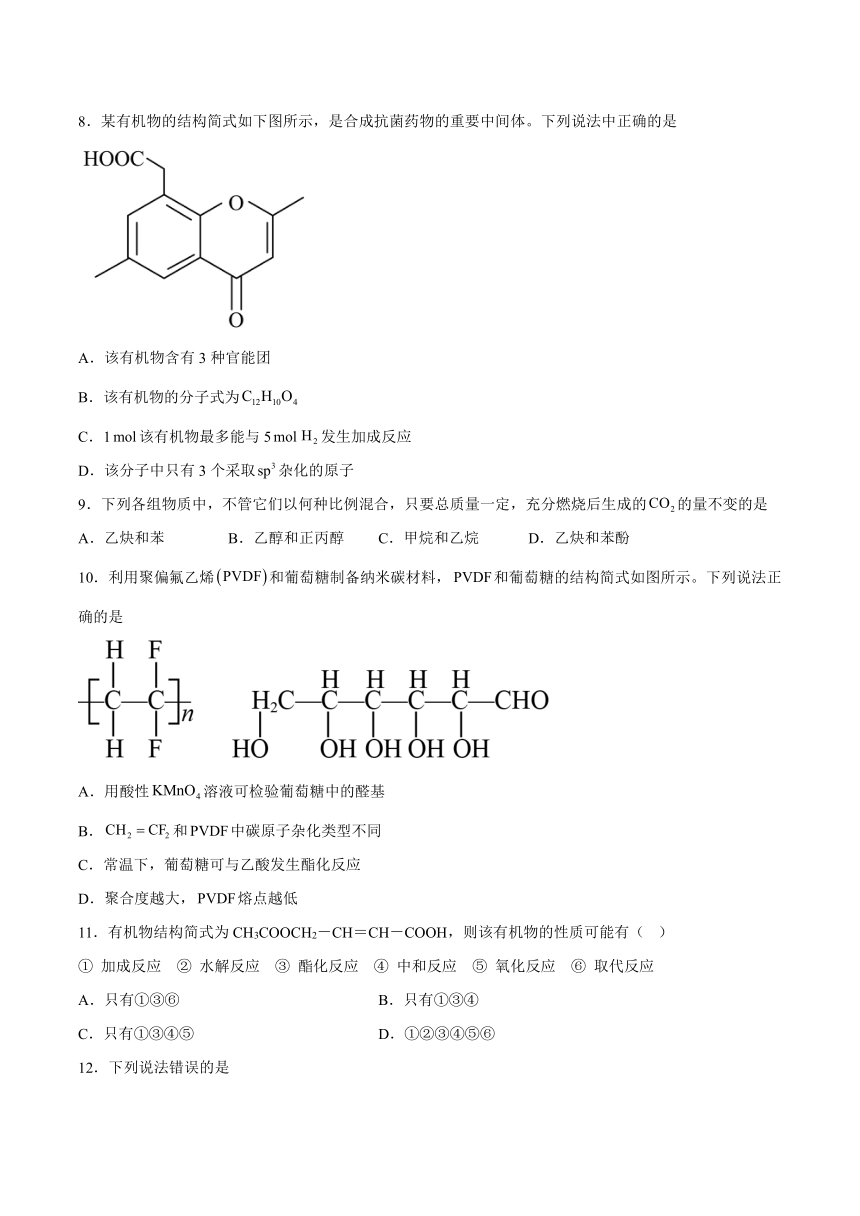
4.我国自主研发对二甲苯的绿色合成路线如下图所示,有关说法不正确的是
A.过程①发生了加成反应
B.过程②有C-H键、C-O键的断裂和形成
C.该反应的副产物可能有间二甲苯
D.M的结构简式为
5.下列有关实验说法不正确的是
A.萃取Br2时,向盛有溴水的分液漏斗加入CCl4,振荡、静置分层,打开旋塞,先将水层放出
B.分离溴苯中混有的溴单质时,可加入氢氧化钠溶液振荡后分液
C.乙醇、苯等有机溶剂易被引燃,使用时须远离明火,用毕立即塞紧瓶塞
D.卤代烃加NaOH溶液加热后,加入稀HNO3酸化,再加AgNO3溶液区分卤代烃中含有何种卤原子
6.完全燃烧1.00 g某有机化合物,生成3.08 g CO2和1.44gH2O。质谱法测得其相对分子质量为100,下列说法正确的是
A.该有机物中可能含有氧元素
B.该有机物中C、H原子个数比为7:8
C.该有机物主链有5个碳原子的结构有5种
D.该有机物可以发生取代反应,也可以发生加成反应
7.化学与生产生活、能源、航空航天、医疗健康等诸多领域的需求密切相关。下列说法错误的是
A.核酸检测是诊断新冠肺炎的重要依据,核酸是生物体遗传信息的载体,通过红外光谱仪可检测其结构中存在的化学键和官能团
B.“硫黄能化金银铜铁,奇物”,说明硫能与Cu、Ag化合生成CuS、Ag2S
C.“神舟十三号”飞船返回舱外壳的烧蚀材料之一酚醛树脂,是酚与醛在酸或碱催化下缩合成的高分子化合物
D.生产医用口罩的原料以丙烯为主,丙烯可以通过石油裂化、裂解获得
8.某有机物的结构简式如下图所示,是合成抗菌药物的重要中间体。下列说法中正确的是
A.该有机物含有3种官能团
B.该有机物的分子式为
C.1该有机物最多能与5发生加成反应
D.该分子中只有3个采取杂化的原子
9.下列各组物质中,不管它们以何种比例混合,只要总质量一定,充分燃烧后生成的的量不变的是
A.乙炔和苯 B.乙醇和正丙醇 C.甲烷和乙烷 D.乙炔和苯酚
10.利用聚偏氟乙烯和葡萄糖制备纳米碳材料,和葡萄糖的结构简式如图所示。下列说法正确的是
A.用酸性溶液可检验葡萄糖中的醛基
B.和中碳原子杂化类型不同
C.常温下,葡萄糖可与乙酸发生酯化反应
D.聚合度越大,熔点越低
11.有机物结构简式为CH3COOCH2-CH=CH-COOH,则该有机物的性质可能有( )
① 加成反应 ② 水解反应 ③ 酯化反应 ④ 中和反应 ⑤ 氧化反应 ⑥ 取代反应
A.只有①③⑥ B.只有①③④
C.只有①③④⑤ D.①②③④⑤⑥
12.下列说法错误的是
A.聚碳酸酯可通过缩聚反应制得
B.合成高聚物的单体一共有三种
C.已知:,则合成的原料可以是1-丁炔和2-异丙基-1,3-丁二烯
D.某中性有机物在稀硫酸的作用下加热得到X和Y两种有机物,Y经氧化可最终得到X,则Y的结构有2种
13.咖啡酸(结构如图所示)有较广泛的抑菌和抗病毒活性作用,可在化妆品中安全使用。有关该化合物,下列叙述错误的是
A.分子式为C9H8O4
B.能与NaOH、NaHCO3反应
C.能够发生酯化反应
D.所有原子不可能共平面
二、非选择题(共10题)
14.0.2mol某烃A在氧气中充分燃烧后,生成化合物B、C各1.2mol。请回答下列问题:
(1)烃A的分子式为___。
(2)若烃A不能使溴水褪色,但在一定条件下,能与氯气发生取代反应,其一氯代物只有一种,则烃A的结构简式为___。
(3)若烃A可与HBr加成,与HBr加成后只能得到一种产物,且烃A的一氯代物只有一种。A的结构简式为___;名称是___。
(4)某芳香烃结构为。它一氯代物有___种。
(5)分子式为C8H10的芳香烃,苯环上的一氯代物只有一种,该芳香烃的结构简式是__。
15.完成下列问题。
(1)用系统命名法命名下列有机物。
①:_______。
②:_______。
③CH2=C(CH3)CH=CH2:_______。
④:_______。
(2)写出下列有机物的结构简式或分子式:
①某气态烃(标准状况下)224mL与含有3.2g溴的溴水恰好完全加成,生成物的每个碳原子上都有1个溴原子,该烃的结构简式为_______。
②相对分子质量为84的烃的分子式为_______。
③某炔烃和H2充分加成生成2,5-二甲基己烷,该炔烃的结构简式为_______。
三、实验题
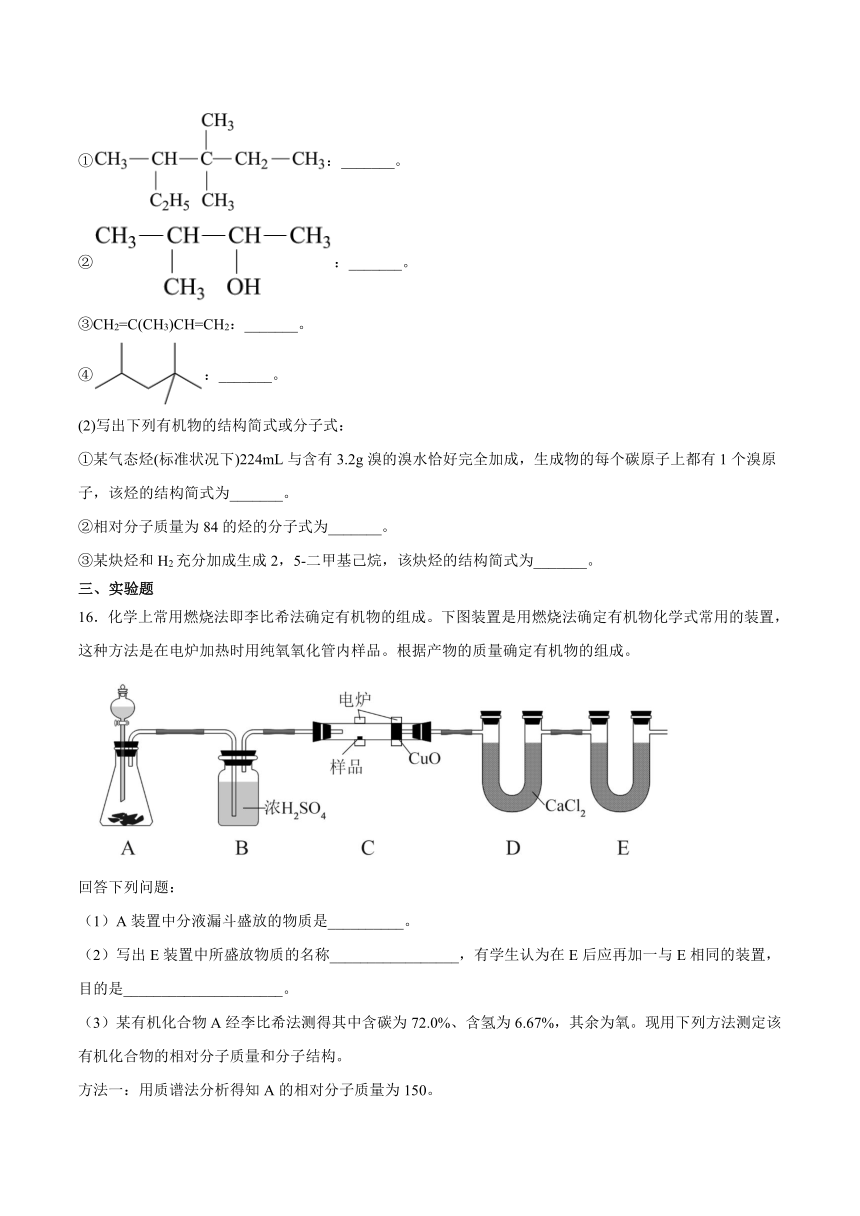
16.化学上常用燃烧法即李比希法确定有机物的组成。下图装置是用燃烧法确定有机物化学式常用的装置,这种方法是在电炉加热时用纯氧氧化管内样品。根据产物的质量确定有机物的组成。
回答下列问题:
(1)A装置中分液漏斗盛放的物质是__________。
(2)写出E装置中所盛放物质的名称_________________,有学生认为在E后应再加一与E相同的装置,目的是_____________________。
(3)某有机化合物A经李比希法测得其中含碳为72.0%、含氢为6.67%,其余为氧。现用下列方法测定该有机化合物的相对分子质量和分子结构。
方法一:用质谱法分析得知A的相对分子质量为150。
方法二:核磁共振仪测出A的核磁共振氢谱有5个峰,其面积之比为1:2:2:2:3,如下图
方法三:利用红外光谱仪测得A分子的红外光谱如下图所示。
请填空:
①A的分子式为________;结构简式为________
②A的芳香类同分异构体有多种,其中符合下列条件:
1)分子结构中只含一个官能团;2)分子结构中含有一个甲基;3)苯环上只有一个取代基。
则该类A的同分异构体共有____种,写出其中一种核磁共振氢谱有6个峰,且面积之比为1:1:1:2:2:3的同分异构体的结构简式:_____________________。
17.已知某种燃料含有碳、氢、氧三种元素。为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的O2中燃烧,并使产生的气体全部通过如图所示装置中,得到如表中所列的实验结果(假设产生的气体完全被吸收)。
实验前 实验后
(干燥剂+U形管)的质量 101.1 g 102.9 g
(石灰水+广口瓶)的质量 312.0 g 314.2 g
根据实验数据完成下列问题:
(1)实验完毕后,生成物中水的质量为________g。假设广口瓶里生成一种正盐,其质量为________g。
(2)生成的水中氢元素的质量为________g。
(3)生成的二氧化碳中碳元素的质量为________g。
(4)该燃料中碳元素与氢元素的质量比为________。
(5)已知这种燃料的每个分子中含有一个氧原子,则该燃料的分子式为________,结构简式为________________。
四、计算题
18.计算。
(1)蚂蚁分泌的信息素中含有十一烷,其分子中碳、氢两元素质量比为_______。
(2)在标准状况下的密度为2.59g·L-1的烷烃,相对分子质量为_______,写出其带有支链的同分异构体的结构简式。_______。
19.燃烧法是测定有机物分子式的一种重要方法。某烃蒸气密度是相同条件下氢气的29倍,完全燃烧5.8g此烃后,测得生成的二氧化碳为8.96 L(标准状况),生成的水为9.0g。请通过计算:
(1)推导该烃的分子式_____。
(2)写出它可能存在的全部结构简式_____。
20.某有机物蒸气0.1L与aLO2在一定条件下恰好燃烧,生成0.3L水蒸气、0.1LCO2和0.1LCO(气体体积均在相同条件下测得)。
(1)a的最大值为_________,有机物的结构简式为________________。
(2)当有机物为乙二醇时,a的值为_____________。
21.从煤和石油中可以提炼出化工原料A和B,A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平;B是一种比水轻的油状液态烃,0.1mol该烃在足量的氧气中完全燃烧,生成0.6molCO2和0.3mol水。回答下列问题:
(1)A 的电子式为_____,B 的结构简式为______。
(2)与A 相邻的同系物C使溴的四氯化碳溶液褪色的化学反应方程式:____,反应类型:____。
(3)在碘水中加入B物质,充分振荡、静置后的现象:_________。
(4)B与浓硫酸和浓硝酸在55~60℃条件下反应的化学方程式:_______,反应类型:______。
(5)等质量的A、B完全燃烧时消耗O2的物质的量:_______(填“A>B”“A22.物质F是一种芳香酯,常用作调香剂,其合成路线如下图所示:
已知E中含有两个甲基,请回答下列问题:
(1)物质A的名称是_______。
(2)各取1 mol物质D分别与足量Na、NaOH溶液、NaHCO3溶液反应,消耗的Na、NaOH、NaHCO3的物质的量之比为_______。
(3)物质A到F中除D以外含有手性碳原子的物质是_______(填标号)。
(4)B→C的反应方程式是_______。
(5)E的同分异构体中与其含有相同种类官能团的有_______种(不含E本身)。
23.0.2mol有机物和0.4molO2在密闭容器中燃烧后产物为CO2、CO和H2O(g)。产物经过浓H2SO4后,浓H2SO4质量增加10.8g;再通过灼热的CuO,充分反应后,CuO质量减轻3.2g,最后气体再通过碱石灰被完全吸收,碱石灰质量增加17.6g。
(1)试推断该有机物的分子式。_____________。
(2)若0.2mol该有机物恰好能与9.2g金属钠完全反应,试确定该有机物的结构简式。_____________。
参考答案:
1.D 2.D 3.A 4.B 5.A 6.C 7.B 8.C 9.A 10.B 11.D 12.B 13.D
14. C6H12 (CH3)2C=C(CH3)2 2,3-二甲基-2-丁烯 4
15.(1) 3、3、4-三甲基己烷 3-甲基-2-丁醇 2-甲基-1、3-丁二烯 2、2、4-三甲基戊烷
(2) CH2=CHCH=CH2 C6H12 CH3CH(CH3)C≡CCH(CH3)2
16. H2O2 碱石灰或生石灰 避免空气中的水和二氧化碳对结果有所干扰 C9H10O2 5种 或 (任写一种)
17. 1.8 5 0.2 0.6 3∶1 CH4O CH3OH
18.(1)11:2
(2) 58 CH3CH(CH3)2
19.(1)C4H10
(2)CH3CH2CH2CH3,CH3CH(CH3)CH3
20. 0.3 CH3CH3 0.2
21. CH2=CHCH3+Br2→CH2BrCHBrCH3 加成反应 溶液分层,下层无色,上层呈紫红色 +HO-NO2(浓)+H2O 取代反应 A>B
22. 2-甲基-1-丁烯 2:1:1 BC 7
23. C2H6O2 CH2OHCH2OH
一、单选题(共13题)
1.化合物Y是一种药物中间体,可由X制得。下列有关化合物X、Y的说法正确的是
A.1molX最多能与3mol反应 B.Y分子中所有碳原子可能处于同一平面
C.用溶液可以区分X、Y D.X、Y分子中手性碳原子数目不相等
2.聚乳酸是一种新型的生物可降解高分子材料,其合成路线如下:
下列说法正确的是
A.,乳酸变为聚乳酸为缩聚反应 B.聚乳酸分子中含有两种官能团
C.1mol乳酸与1mol Na反应生成1mol D.两分子乳酸反应能够生成含六元环的分子
3.下列操作能达到相应实验目的的是
实验目的 操作
A 检验绿茶中是否含有酚类物质 向茶水中滴加FeCl3溶液
B 判断某卤代烃中的卤素 取2 mL卤代烃样品于试管中,加入5 mL 20% KOH水溶液混合后加热,再滴加AgNO3溶液
C 除去苯中混有的少量苯酚 向苯和苯酚的混合物中滴加溴水,过滤后分液
D 实验室制备乙酸乙酯 向试管中依次加入浓硫酸、乙醇、乙酸和碎瓷片,加热
A.A B.B C.C D.D
4.我国自主研发对二甲苯的绿色合成路线如下图所示,有关说法不正确的是
A.过程①发生了加成反应
B.过程②有C-H键、C-O键的断裂和形成
C.该反应的副产物可能有间二甲苯
D.M的结构简式为
5.下列有关实验说法不正确的是
A.萃取Br2时,向盛有溴水的分液漏斗加入CCl4,振荡、静置分层,打开旋塞,先将水层放出
B.分离溴苯中混有的溴单质时,可加入氢氧化钠溶液振荡后分液
C.乙醇、苯等有机溶剂易被引燃,使用时须远离明火,用毕立即塞紧瓶塞
D.卤代烃加NaOH溶液加热后,加入稀HNO3酸化,再加AgNO3溶液区分卤代烃中含有何种卤原子
6.完全燃烧1.00 g某有机化合物,生成3.08 g CO2和1.44gH2O。质谱法测得其相对分子质量为100,下列说法正确的是
A.该有机物中可能含有氧元素
B.该有机物中C、H原子个数比为7:8
C.该有机物主链有5个碳原子的结构有5种
D.该有机物可以发生取代反应,也可以发生加成反应
7.化学与生产生活、能源、航空航天、医疗健康等诸多领域的需求密切相关。下列说法错误的是
A.核酸检测是诊断新冠肺炎的重要依据,核酸是生物体遗传信息的载体,通过红外光谱仪可检测其结构中存在的化学键和官能团
B.“硫黄能化金银铜铁,奇物”,说明硫能与Cu、Ag化合生成CuS、Ag2S
C.“神舟十三号”飞船返回舱外壳的烧蚀材料之一酚醛树脂,是酚与醛在酸或碱催化下缩合成的高分子化合物
D.生产医用口罩的原料以丙烯为主,丙烯可以通过石油裂化、裂解获得
8.某有机物的结构简式如下图所示,是合成抗菌药物的重要中间体。下列说法中正确的是
A.该有机物含有3种官能团
B.该有机物的分子式为
C.1该有机物最多能与5发生加成反应
D.该分子中只有3个采取杂化的原子
9.下列各组物质中,不管它们以何种比例混合,只要总质量一定,充分燃烧后生成的的量不变的是
A.乙炔和苯 B.乙醇和正丙醇 C.甲烷和乙烷 D.乙炔和苯酚
10.利用聚偏氟乙烯和葡萄糖制备纳米碳材料,和葡萄糖的结构简式如图所示。下列说法正确的是
A.用酸性溶液可检验葡萄糖中的醛基
B.和中碳原子杂化类型不同
C.常温下,葡萄糖可与乙酸发生酯化反应
D.聚合度越大,熔点越低
11.有机物结构简式为CH3COOCH2-CH=CH-COOH,则该有机物的性质可能有( )
① 加成反应 ② 水解反应 ③ 酯化反应 ④ 中和反应 ⑤ 氧化反应 ⑥ 取代反应
A.只有①③⑥ B.只有①③④
C.只有①③④⑤ D.①②③④⑤⑥
12.下列说法错误的是
A.聚碳酸酯可通过缩聚反应制得
B.合成高聚物的单体一共有三种
C.已知:,则合成的原料可以是1-丁炔和2-异丙基-1,3-丁二烯
D.某中性有机物在稀硫酸的作用下加热得到X和Y两种有机物,Y经氧化可最终得到X,则Y的结构有2种
13.咖啡酸(结构如图所示)有较广泛的抑菌和抗病毒活性作用,可在化妆品中安全使用。有关该化合物,下列叙述错误的是
A.分子式为C9H8O4
B.能与NaOH、NaHCO3反应
C.能够发生酯化反应
D.所有原子不可能共平面
二、非选择题(共10题)
14.0.2mol某烃A在氧气中充分燃烧后,生成化合物B、C各1.2mol。请回答下列问题:
(1)烃A的分子式为___。
(2)若烃A不能使溴水褪色,但在一定条件下,能与氯气发生取代反应,其一氯代物只有一种,则烃A的结构简式为___。
(3)若烃A可与HBr加成,与HBr加成后只能得到一种产物,且烃A的一氯代物只有一种。A的结构简式为___;名称是___。
(4)某芳香烃结构为。它一氯代物有___种。
(5)分子式为C8H10的芳香烃,苯环上的一氯代物只有一种,该芳香烃的结构简式是__。
15.完成下列问题。
(1)用系统命名法命名下列有机物。
①:_______。
②:_______。
③CH2=C(CH3)CH=CH2:_______。
④:_______。
(2)写出下列有机物的结构简式或分子式:
①某气态烃(标准状况下)224mL与含有3.2g溴的溴水恰好完全加成,生成物的每个碳原子上都有1个溴原子,该烃的结构简式为_______。
②相对分子质量为84的烃的分子式为_______。
③某炔烃和H2充分加成生成2,5-二甲基己烷,该炔烃的结构简式为_______。
三、实验题
16.化学上常用燃烧法即李比希法确定有机物的组成。下图装置是用燃烧法确定有机物化学式常用的装置,这种方法是在电炉加热时用纯氧氧化管内样品。根据产物的质量确定有机物的组成。
回答下列问题:
(1)A装置中分液漏斗盛放的物质是__________。
(2)写出E装置中所盛放物质的名称_________________,有学生认为在E后应再加一与E相同的装置,目的是_____________________。
(3)某有机化合物A经李比希法测得其中含碳为72.0%、含氢为6.67%,其余为氧。现用下列方法测定该有机化合物的相对分子质量和分子结构。
方法一:用质谱法分析得知A的相对分子质量为150。
方法二:核磁共振仪测出A的核磁共振氢谱有5个峰,其面积之比为1:2:2:2:3,如下图
方法三:利用红外光谱仪测得A分子的红外光谱如下图所示。
请填空:
①A的分子式为________;结构简式为________
②A的芳香类同分异构体有多种,其中符合下列条件:
1)分子结构中只含一个官能团;2)分子结构中含有一个甲基;3)苯环上只有一个取代基。
则该类A的同分异构体共有____种,写出其中一种核磁共振氢谱有6个峰,且面积之比为1:1:1:2:2:3的同分异构体的结构简式:_____________________。
17.已知某种燃料含有碳、氢、氧三种元素。为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的O2中燃烧,并使产生的气体全部通过如图所示装置中,得到如表中所列的实验结果(假设产生的气体完全被吸收)。
实验前 实验后
(干燥剂+U形管)的质量 101.1 g 102.9 g
(石灰水+广口瓶)的质量 312.0 g 314.2 g
根据实验数据完成下列问题:
(1)实验完毕后,生成物中水的质量为________g。假设广口瓶里生成一种正盐,其质量为________g。
(2)生成的水中氢元素的质量为________g。
(3)生成的二氧化碳中碳元素的质量为________g。
(4)该燃料中碳元素与氢元素的质量比为________。
(5)已知这种燃料的每个分子中含有一个氧原子,则该燃料的分子式为________,结构简式为________________。
四、计算题
18.计算。
(1)蚂蚁分泌的信息素中含有十一烷,其分子中碳、氢两元素质量比为_______。
(2)在标准状况下的密度为2.59g·L-1的烷烃,相对分子质量为_______,写出其带有支链的同分异构体的结构简式。_______。
19.燃烧法是测定有机物分子式的一种重要方法。某烃蒸气密度是相同条件下氢气的29倍,完全燃烧5.8g此烃后,测得生成的二氧化碳为8.96 L(标准状况),生成的水为9.0g。请通过计算:
(1)推导该烃的分子式_____。
(2)写出它可能存在的全部结构简式_____。
20.某有机物蒸气0.1L与aLO2在一定条件下恰好燃烧,生成0.3L水蒸气、0.1LCO2和0.1LCO(气体体积均在相同条件下测得)。
(1)a的最大值为_________,有机物的结构简式为________________。
(2)当有机物为乙二醇时,a的值为_____________。
21.从煤和石油中可以提炼出化工原料A和B,A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平;B是一种比水轻的油状液态烃,0.1mol该烃在足量的氧气中完全燃烧,生成0.6molCO2和0.3mol水。回答下列问题:
(1)A 的电子式为_____,B 的结构简式为______。
(2)与A 相邻的同系物C使溴的四氯化碳溶液褪色的化学反应方程式:____,反应类型:____。
(3)在碘水中加入B物质,充分振荡、静置后的现象:_________。
(4)B与浓硫酸和浓硝酸在55~60℃条件下反应的化学方程式:_______,反应类型:______。
(5)等质量的A、B完全燃烧时消耗O2的物质的量:_______(填“A>B”“A
已知E中含有两个甲基,请回答下列问题:
(1)物质A的名称是_______。
(2)各取1 mol物质D分别与足量Na、NaOH溶液、NaHCO3溶液反应,消耗的Na、NaOH、NaHCO3的物质的量之比为_______。
(3)物质A到F中除D以外含有手性碳原子的物质是_______(填标号)。
(4)B→C的反应方程式是_______。
(5)E的同分异构体中与其含有相同种类官能团的有_______种(不含E本身)。
23.0.2mol有机物和0.4molO2在密闭容器中燃烧后产物为CO2、CO和H2O(g)。产物经过浓H2SO4后,浓H2SO4质量增加10.8g;再通过灼热的CuO,充分反应后,CuO质量减轻3.2g,最后气体再通过碱石灰被完全吸收,碱石灰质量增加17.6g。
(1)试推断该有机物的分子式。_____________。
(2)若0.2mol该有机物恰好能与9.2g金属钠完全反应,试确定该有机物的结构简式。_____________。
参考答案:
1.D 2.D 3.A 4.B 5.A 6.C 7.B 8.C 9.A 10.B 11.D 12.B 13.D
14. C6H12 (CH3)2C=C(CH3)2 2,3-二甲基-2-丁烯 4
15.(1) 3、3、4-三甲基己烷 3-甲基-2-丁醇 2-甲基-1、3-丁二烯 2、2、4-三甲基戊烷
(2) CH2=CHCH=CH2 C6H12 CH3CH(CH3)C≡CCH(CH3)2
16. H2O2 碱石灰或生石灰 避免空气中的水和二氧化碳对结果有所干扰 C9H10O2 5种 或 (任写一种)
17. 1.8 5 0.2 0.6 3∶1 CH4O CH3OH
18.(1)11:2
(2) 58 CH3CH(CH3)2
19.(1)C4H10
(2)CH3CH2CH2CH3,CH3CH(CH3)CH3
20. 0.3 CH3CH3 0.2
21. CH2=CHCH3+Br2→CH2BrCHBrCH3 加成反应 溶液分层,下层无色,上层呈紫红色 +HO-NO2(浓)+H2O 取代反应 A>B
22. 2-甲基-1-丁烯 2:1:1 BC 7
23. C2H6O2 CH2OHCH2OH
