第3章第3节饮食中的有机化合物同步练习 (含解析)2022-2023学年下学期高一化学鲁科版(2019)必修第二册
文档属性
| 名称 | 第3章第3节饮食中的有机化合物同步练习 (含解析)2022-2023学年下学期高一化学鲁科版(2019)必修第二册 |

|
|
| 格式 | docx | ||
| 文件大小 | 242.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-04 00:00:00 | ||
图片预览




文档简介
第3章第3节饮食中的有机化合物同步练习
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列反应属于加成反应的是
A.乙烯与氢气反应生成乙烷 B.乙酸与乙醇反应生成乙酸乙酯和水
C.乙醇在空气中燃烧生成二氧化碳和水 D.甲烷与氯气反应生成一氯甲烷和氯化氢
2.植物油水解后,高级脂肪酸的成分是
A.油酸的成分多 B.硬脂酸的成分多
C.软脂酸的成分多 D.甘油的成分多
3.将碘水滴到新切开的马铃薯(又称土豆)表面上,马铃薯表面变蓝色,该现象表明马铃薯含有
A.葡萄糖 B.蔗糖 C.淀粉 D.纤维素
4.血糖是指血液中的葡萄糖,下列有关说法不正确的是
A.葡萄糖的分子式可表示为C6(H2O)6,则葡萄糖分子中含有6个H2O分子
B.葡萄糖与果糖互为同分异构体
C.葡萄糖与麦芽糖均含有醛基,但二者不互为同系物
D.淀粉与纤维素不互为同分异构体
5.葡萄糖的结构简式为CH2OH—CHOH—CHOH—CHOH—CHOH—CHO,下列有关葡萄糖的叙述不正确的是
A.1 mol葡萄糖最多可以与5 mol金属钠反应放出氢气
B.1 mol葡萄糖最多可以与5 mol乙酸发生酯化反应
C.可与新制氢氧化铜悬浊液反应产生砖红色沉淀
D.可与小苏打溶液反应冒出汽泡
6.蒙古牧民喜欢用银器盛鲜牛奶,现代科学证明,用银器盛放鲜牛奶确有其科学依据,其科学依据是
A.溶有极微量的银离子,可杀死牛奶中的细菌防止牛奶变质
B.用银器盛放牛奶,可以补充入体所必需的银元素
C.银易导热,牛奶凉得快
D.银的化学性质稳定,坚固耐用
7.用来证明棉花和淀粉都是多糖的实验方法是
A.放入氧气中燃烧,检验燃烧产物都是CO2和H2O
B.放入银氨溶液中微热,都不发生银镜反应
C.加入浓硫酸后微热,都脱水而变黑
D.分别放入稀酸后煮沸几分钟,用NaOH溶液中和反应后的溶液,再加入新制的Cu(OH)2悬浊液共热,都生成红色沉淀
8.能区别地沟油与矿物油的方法是
A.点燃,能燃烧的是矿物油
B.测定沸点,有固定沸点的是矿物油
C.加入水中,浮在水面上的是地沟油
D.加入足量氢氧化钠溶液共热,不分层的是地沟油
9.误食重金属盐后,应采取有效应急措施是
A.服用大量葡萄糖溶液 B.喝大量的生理盐水
C.喝大量的豆浆或牛奶 D.注射大量盐水
10.用括号内的试剂和分离方法除去下列物质中的少量杂质,不正确的是
A.乙酸乙酯中混有乙酸(饱和溶液,分液)
B.乙醇中混有乙酸(NaOH溶液,蒸馏)
C.甲烷中混有乙烯(溴的四氯化碳溶液,分液)
D.溴苯中混有溴(NaOH溶液,分液)
11.下列物质中,只表示一种分子的是
A.二溴甲烷() B.分子组成为的有机物
C.分子组成为的有机物 D.聚乙烯
12.清洁能源乙醇汽油是将燃料乙醇和汽油以一定比例混合形成的一种汽车燃料。下列关于乙醇汽油的说法中,错误的是
A.使用乙醇汽油可以有效减少有害气体的排放
B.乙醇可由植物油水解制得
C.乙醇中含有氧元素,可使汽油燃烧得更加充分
D.乙醇属于可再生能源
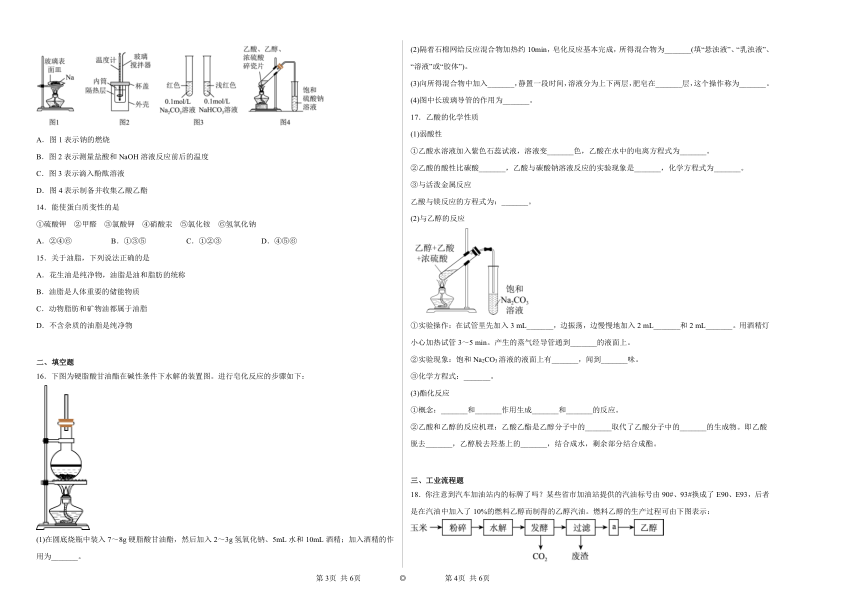
13.如图实验装置(部分夹持装置略)或现象错误的是
A.图1表示钠的燃烧
B.图2表示测量盐酸和NaOH溶液反应前后的温度
C.图3表示滴入酚酞溶液
D.图4表示制备并收集乙酸乙酯
14.能使蛋白质变性的是
①硫酸钾 ②甲醛 ③氯酸钾 ④硝酸汞 ⑤氯化铵 ⑥氢氧化钠
A.②④⑥ B.①③⑤ C.①②③ D.④⑤⑥
15.关于油脂,下列说法正确的是
A.花生油是纯净物,油脂是油和脂肪的统称
B.油脂是人体重要的储能物质
C.动物脂肪和矿物油都属于油脂
D.不含杂质的油脂是纯净物
二、填空题
16.下图为硬脂酸甘油酯在碱性条件下水解的装置图。进行皂化反应的步骤如下:
(1)在圆底烧瓶中装入7~8g硬脂酸甘油酯,然后加入2~3g氢氧化钠、5mL水和10mL酒精;加入酒精的作用为_______。
(2)隔着石棉网给反应混合物加热约10min,皂化反应基本完成,所得混合物为_______(填“悬浊液”、“乳浊液”、“溶液”或“胶体”)。
(3)向所得混合物中加入_______,静置一段时间,溶液分为上下两层,肥皂在_______层,这个操作称为_______。
(4)图中长玻璃导管的作用为_______。
17.乙酸的化学性质
(1)弱酸性
①乙酸水溶液加入紫色石蕊试液,溶液变_______色,乙酸在水中的电离方程式为_______。
②乙酸的酸性比碳酸_______,乙酸与碳酸钠溶液反应的实验现象是_______,化学方程式为_______。
③与活泼金属反应
乙酸与镁反应的方程式为:_______。
(2)与乙醇的反应
①实验操作:在试管里先加入3 mL_______,边振荡,边慢慢地加入2 mL_______和2 mL_______。用酒精灯小心加热试管3~5 min。产生的蒸气经导管通到_______的液面上。
②实验现象:饱和Na2CO3溶液的液面上有_______,闻到_______味。
③化学方程式:_______。
(3)酯化反应
①概念:_______和_______作用生成_______和_______的反应。
②乙酸和乙醇的反应机理:乙酸乙酯是乙醇分子中的_______取代了乙酸分子中的_______的生成物。即乙酸脱去_______,乙醇脱去羟基上的_______,结合成水,剩余部分结合成酯。
三、工业流程题
18.你注意到汽车加油站内的标牌了吗?某些省市加油站提供的汽油标号由90#、93#换成了E90、E93,后者是在汽油中加入了10%的燃料乙醇而制得的乙醇汽油。燃料乙醇的生产过程可由下图表示:
(1)粉碎玉米的目的是______。
(2)生产过程中为了检验淀粉水解是否完全,可使用的试剂是______。
(3)步骤a的操作是______(填字母)。
A.蒸发 B.萃取 C.蒸馏 D.分液
(4)发酵产生的CO2纯度可达到99%,能回收利用,请举出它的两项用途:______、______。
(5)以玉米淀粉为原料生产乙醇的化学反应可用下式表示:
(C6H10O5)n+nH2OnC6H12O6
C6H12O6―→2C2H5OH+2CO2↑
根据上述反应式,可以算出100 kg淀粉理论上可生产无水乙醇______ kg。
四、有机推断题
19.A是植物秸秆的主要成分,以A为原料在一定条件下可获得多种有机物,它们的相互转化关系如图所示。已知F是最简单的烯烃。
请回答:
(1)F→C的反应类型是___________。
(2)C→D的化学方程式是___________。
(3)下列说法正确的是___________。
A.D能被氧化成E,但D不能被还原成C
B.实验室制备G时可用浓硫酸作催化剂和吸水剂
C.B或E均能与银氨溶液反应形成银镜
D.相同质量的B和G完全燃烧生成水的质量相等
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.A
【详解】A.乙烯与氢气发生加成反应生成乙烷,故选A;
B.乙酸与乙醇发生酯化反应生成乙酸乙酯和水,酯化反应属于取代反应,故不选B;
C.乙醇在空气中燃烧生成二氧化碳和水,反应类型为氧化反应,故不选C;
D.甲烷与氯气发生取代反应生成一氯甲烷和氯化氢,故不选D;
选A。
2.A
【详解】植物油是由3分子的高级不饱和脂肪酸和1分子甘油形成的酯,植物油水解后成分最多的为油酸,故选A。
3.C
【详解】淀粉遇到碘变蓝,是淀粉的性质,加碘水变蓝说明马铃薯中含有淀粉,故答案为C。
4.A
【详解】A.葡萄糖的分子式可表示为C6(H2O)6,表示葡萄糖分子中含有H、O两种元素的原子个数相当于6个H2O的组成,没有水分子存在,A错误;
B.葡萄糖与果糖的分子式相同,结构不同,二者互为同分异构体,B正确;
C.葡萄糖的分子式为C6H12O6,麦芽糖的分子式为C12H22O11,分子组成上不是相差“CH2”的整数倍,不互为同系物,C正确;
D.淀粉和纤维素的化学式均可用(C6H10O5)n表示,但n值不同,故两者不互为同分异构体,D正确;
故选A。
5.D
【详解】A.每个葡萄糖分子中含有5个羟基,故1 mol葡萄糖最多可以与5 mol金属钠反应放出氢气,A项正确;
B.每个葡萄糖分子中含有5个羟基,故1 mol葡萄糖最多可以与5 mol乙酸发生酯化反应,B项正确;
C.葡萄糖中含有醛基,可与新制氢氧化铜悬浊液反应产生砖红色沉淀,C项正确;
D.葡萄糖中不含羧基,与小苏打溶液不反应,D项错误;
故选D。
6.A
【详解】A.银离子是重金属离子,可使细菌(蛋白质)变性,选项A正确;
B.银元素不是人体必需元素,不需要补充,选项B错误;
C.内蒙古天气寒冷,凉得快不利于饮用,选项C错误;
D.银器并不坚固耐用,选项D错误;
答案选A。
7.D
【详解】A.棉花和淀粉放入氧气中燃烧,检验燃烧产物都是CO2和H2O,不能证明棉花和淀粉都是多糖,故A错误;
B.棉花和淀粉中没有醛基,放入银氨溶液中微热,都不发生银镜反应,不能证明棉花和淀粉都是多糖,故B错误;
C.棉花和淀粉加入浓硫酸后微热,都脱水而变黑,不能证明棉花和淀粉都是多糖,故C错误;
D.多糖在H2SO4存在下水解生成单糖(葡萄糖),再加入新制的Cu(OH)2悬浊液共热时生成Cu2O沉淀,该操作可以证明棉花和淀粉都是多糖,故D正确;
故选D。
8.D
【详解】A.地沟油和矿物油均可燃烧,A错误;
B.地沟油和矿物油均为混合物,均没有固定的沸点,B错误;
C.地沟油和矿物油密度均小于水,均难溶于水,C错误;
D.地沟油主要成分为油脂,可在碱性条件下水解,因此地沟油与NaOH溶液共热后不再分层,矿物油为烃的混合物,不能与NaOH溶液反应,因此溶液分层,D正确;
故选D。
9.C
【详解】可溶性的重金属盐能电离出重金属离子,会破坏人体蛋白质的结构,使它失去生理功能,中毒后进行急救,最好的方法就是食用富含蛋白质的食品,以防止它破坏人体的蛋白质。
A.葡萄糖溶液是糖类,A不可以;
B.生理盐水是电解质溶液,B不可以;
C.豆浆和牛奶都是富含蛋白质的食品,C可以;
D.盐水属于电解质溶液,D不可以;
综上所述,选C。
10.C
【详解】A.用饱和Na2CO3溶液除去乙酸乙酯中的乙酸,然后使用分液的方法分离有机层和水层,A正确;
B.氢氧化钠和乙醇不反应,和乙酸生成乙酸钠,然后利用乙醇沸点较低的性质,蒸馏得到乙醇,B正确;
C.溴可以和乙烯反应而进入溶液,甲烷为气体逸出,不需分液,C错误;
D.氢氧化钠和溴苯不反应、和溴反应生成盐溶液,然后使用分液的方法分离有机层和水层,D正确;
故选C。
11.A
【详解】A.为四面体结构,只能表示二溴甲烷一种分子,A项正确;
B.的有机物可能是乙醇,也可能是甲醚,B项错误;
C.的有机物可能是正丁烷,也可能是异丁烷,C项错误;
D.聚乙烯是高分子化合物,由于聚合度不确定,聚乙烯是混合物,不能只表示一种分子,D项错误;
答案选A。
12.B
【详解】A.乙醇是清洁燃料,使用乙醇汽油可以有效减少有害气体的排放,故A正确;
B.植物油是高级脂肪酸甘油酯,水解生成丙三醇和高级脂肪酸盐,故B错误;
C.乙醇中含有氧元素,可使汽油燃烧得更加充分,降低CO等有害气体的排放,故C正确;
D.乙醇可通过谷类、薯类等淀粉植物进行水解、发酵再次获得,乙醇属于可再生能源,故D正确;
选B。
13.A
【详解】A.钠的燃烧反应需要在坩埚中进行,不能在表面皿中加热,故A错误;
B.中和热测量实验中,主要是在量热器中测定反应前后的温度,该装置可以测量中和热,故B正确;
C.Na2CO3、NaHCO3溶液都呈碱性,碳酸钠碱性较强,酚酞遇碱溶液呈红色,所以向相同浓度的Na2CO3、NaHCO3溶液中滴加几滴酚酞,前者呈红色、后者为浅红色,故C正确;
D.乙酸、乙醇在浓硫酸催化下发生酯化反应,饱和碳酸钠溶液可以溶解乙醇、吸收乙酸、分离乙酸乙酯,该装置正确,故D正确;
故选:A。
14.A
【详解】在某些物理因素或化学因素的影响下,蛋白质的理化性质和生理功能发生改变的现象称为蛋白质的变性。物理因素有:加热、加压、搅拌、振荡、紫外线照射、超声波等;化学因素有:强酸、强碱、重金属盐、三氯乙酸、乙醇、丙酮等。甲醛有杀菌、防腐性能,硝酸汞是重金属盐,氢氧化钠是强碱,所以②甲醛、④硝酸汞、⑥氢氧化钠能使蛋白质变性;
故选:A。
15.B
【详解】A.花生油是多种油脂的混合物,A错误;
B.人体内含脂肪,能为人体提供能量,即油脂是人体内的重要的储能和供能物质,B正确;
C.油脂是高级脂肪酸的甘油酯,而矿物油是多种烃的混合物,不属于油脂,C错误;
D.油脂的结构有多种,即使油脂中不含其它杂质时,油脂也为混合物,D错误;
故选B。
16.(1)溶解硬脂酸甘油酯
(2)胶体
(3) 食盐 上 盐析
(4)冷凝回流
【分析】硬脂酸甘油酯(油脂)在碱性条件下的水解为皂化反应。
【详解】(1)加入酒精的作用为溶解硬脂酸甘油酯;
(2)皂化反应完成后所得混合物为胶体;
(3)混合物为胶体,向混合液中加入食盐,静置一段时间,溶液分为上下两层,肥皂在上层,这个操作称为盐析;
(4)油脂的沸点较低,加热易挥发,长导管的作用是冷凝回流。
17.(1) 红 CH3COOHCH3COO-+H+ 强
有无色气体产生 2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O 2CH3COOH+Mg→(CH3COO)2Mg+H2↑
(2) 乙醇 98%浓硫酸 冰醋酸 饱和碳酸钠溶液 油状液体生成 香 CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O
(3) 醇 酸 酯 水 乙氧基(CH3CH2O-) 羟基(-OH) 氢原子 氢
【解析】(1)
①乙酸有酸的通性,遇到紫色石蕊变红;乙酸是弱酸,水中部分电离,电离方程式为CH3COOH CH3COO-+H+;
②乙酸的酸性比碳酸强,乙酸与碳酸钠反应生成乙酸钠、水和二氧化碳,实验现象是有无色气体产生;化学方程式为2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O;
③乙酸与镁反应生成乙酸镁和氢气,方程式为2CH3COOH+Mg→(CH3COO)2Mg+H2↑;
(2)
①乙醇与乙酸反应制备乙酸乙酯的过程中,应先加入3 mL乙醇,边振荡,边慢慢地加入2 mL98%浓硫酸和2 mL冰醋酸,反应中用饱和碳酸钠溶液吸收;
②乙酸乙酯在饱和碳酸钠溶液中溶解度比较小,且密度比碳酸钠溶液小,故饱和Na2CO3溶液的液面上有油状液体生成,低级酯具有香味,故可以闻到香味;
③化学方程式为CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O;
(3)
①酯化反应是醇和酸作用生成酯和水的反应;
②乙酸乙酯是乙醇分子中的乙氧基(CH3CH2O-)取代了乙酸分子中的羟基(-OH) 的生成物;即乙酸脱去氢原子,乙醇脱去羟基上的氢,结合成水,剩余部分结合成酯。
18.(1)增大反应物的接触面积或加快反应速率或使反应充分进行
(2)碘(I2)或碘酒或革兰氏碘液
(3)C
(4) 制饮料 制干冰
(5)56.8
【解析】(1)
粉碎玉米是增大反应的接触面积,加快反应速率,提高原料的利用率,故答案为:增大反应物的接触面积或加快反应速率或使反应充分进行;
(2)
因为淀粉遇I2变蓝色,只要有淀粉存在,加I2一定变蓝色,因此可用I2或碘酒来检验淀粉是否水解完全,故答案为:碘(I2)或碘酒或革兰氏碘液;
(3)
滤去废渣后得到的是水和乙醇的混合溶液,由于乙醇和水互溶,但沸点不同,乙醇的沸点低于水,用蒸馏的方法可使乙醇从混合液中分离出来,故答案为:C;
(4)
纯度为99%的CO2,可以很好的利用。因为CO2可以做碳酸饮料,也可以制干冰,也可制纯碱或制碳酸钙等,故答案为:制饮料;制干冰;
(5)
由(C6H10O5)n+nH2OnC6H12O6 C6H12O6―→2C2H5OH+2CO2↑可得到关系式:(C6H10O5)n~2nC2H5OH,设理论上可生产无水乙醇的质量为x,
,,故答案为:56.8。
19. 加成反应 B
【详解】分析流程可知A为纤维素,B为葡萄糖,C为乙醇,D为乙醛,E为乙酸,F为乙烯,G为乙酸乙酯。
(1)由为乙烯与水反应生成乙醇,为加成反应;
(2)为乙醇氧化生成乙醛,反应方程式为:;
(3) A.乙醛可以被氧化生成乙酸,同时可以被氢气还原生成乙醇,A项错误;
B.在制备乙酸乙酯时,浓硫酸起催化剂和吸水剂的作用,B项正确;
C.乙酸不能与银氨溶液反应形成银镜,C项错误;
D.葡萄糖的分子式为,乙酸乙酯的分子式为,相同质量的葡萄糖和乙酸乙酯中氢元素的含量不相同,生成水的质量也不相等,D项错误;故答案为:B。
答案第1页,共2页
答案第1页,共2页
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列反应属于加成反应的是
A.乙烯与氢气反应生成乙烷 B.乙酸与乙醇反应生成乙酸乙酯和水
C.乙醇在空气中燃烧生成二氧化碳和水 D.甲烷与氯气反应生成一氯甲烷和氯化氢
2.植物油水解后,高级脂肪酸的成分是
A.油酸的成分多 B.硬脂酸的成分多
C.软脂酸的成分多 D.甘油的成分多
3.将碘水滴到新切开的马铃薯(又称土豆)表面上,马铃薯表面变蓝色,该现象表明马铃薯含有
A.葡萄糖 B.蔗糖 C.淀粉 D.纤维素
4.血糖是指血液中的葡萄糖,下列有关说法不正确的是
A.葡萄糖的分子式可表示为C6(H2O)6,则葡萄糖分子中含有6个H2O分子
B.葡萄糖与果糖互为同分异构体
C.葡萄糖与麦芽糖均含有醛基,但二者不互为同系物
D.淀粉与纤维素不互为同分异构体
5.葡萄糖的结构简式为CH2OH—CHOH—CHOH—CHOH—CHOH—CHO,下列有关葡萄糖的叙述不正确的是
A.1 mol葡萄糖最多可以与5 mol金属钠反应放出氢气
B.1 mol葡萄糖最多可以与5 mol乙酸发生酯化反应
C.可与新制氢氧化铜悬浊液反应产生砖红色沉淀
D.可与小苏打溶液反应冒出汽泡
6.蒙古牧民喜欢用银器盛鲜牛奶,现代科学证明,用银器盛放鲜牛奶确有其科学依据,其科学依据是
A.溶有极微量的银离子,可杀死牛奶中的细菌防止牛奶变质
B.用银器盛放牛奶,可以补充入体所必需的银元素
C.银易导热,牛奶凉得快
D.银的化学性质稳定,坚固耐用
7.用来证明棉花和淀粉都是多糖的实验方法是
A.放入氧气中燃烧,检验燃烧产物都是CO2和H2O
B.放入银氨溶液中微热,都不发生银镜反应
C.加入浓硫酸后微热,都脱水而变黑
D.分别放入稀酸后煮沸几分钟,用NaOH溶液中和反应后的溶液,再加入新制的Cu(OH)2悬浊液共热,都生成红色沉淀
8.能区别地沟油与矿物油的方法是
A.点燃,能燃烧的是矿物油
B.测定沸点,有固定沸点的是矿物油
C.加入水中,浮在水面上的是地沟油
D.加入足量氢氧化钠溶液共热,不分层的是地沟油
9.误食重金属盐后,应采取有效应急措施是
A.服用大量葡萄糖溶液 B.喝大量的生理盐水
C.喝大量的豆浆或牛奶 D.注射大量盐水
10.用括号内的试剂和分离方法除去下列物质中的少量杂质,不正确的是
A.乙酸乙酯中混有乙酸(饱和溶液,分液)
B.乙醇中混有乙酸(NaOH溶液,蒸馏)
C.甲烷中混有乙烯(溴的四氯化碳溶液,分液)
D.溴苯中混有溴(NaOH溶液,分液)
11.下列物质中,只表示一种分子的是
A.二溴甲烷() B.分子组成为的有机物
C.分子组成为的有机物 D.聚乙烯
12.清洁能源乙醇汽油是将燃料乙醇和汽油以一定比例混合形成的一种汽车燃料。下列关于乙醇汽油的说法中,错误的是
A.使用乙醇汽油可以有效减少有害气体的排放
B.乙醇可由植物油水解制得
C.乙醇中含有氧元素,可使汽油燃烧得更加充分
D.乙醇属于可再生能源
13.如图实验装置(部分夹持装置略)或现象错误的是
A.图1表示钠的燃烧
B.图2表示测量盐酸和NaOH溶液反应前后的温度
C.图3表示滴入酚酞溶液
D.图4表示制备并收集乙酸乙酯
14.能使蛋白质变性的是
①硫酸钾 ②甲醛 ③氯酸钾 ④硝酸汞 ⑤氯化铵 ⑥氢氧化钠
A.②④⑥ B.①③⑤ C.①②③ D.④⑤⑥
15.关于油脂,下列说法正确的是
A.花生油是纯净物,油脂是油和脂肪的统称
B.油脂是人体重要的储能物质
C.动物脂肪和矿物油都属于油脂
D.不含杂质的油脂是纯净物
二、填空题
16.下图为硬脂酸甘油酯在碱性条件下水解的装置图。进行皂化反应的步骤如下:
(1)在圆底烧瓶中装入7~8g硬脂酸甘油酯,然后加入2~3g氢氧化钠、5mL水和10mL酒精;加入酒精的作用为_______。
(2)隔着石棉网给反应混合物加热约10min,皂化反应基本完成,所得混合物为_______(填“悬浊液”、“乳浊液”、“溶液”或“胶体”)。
(3)向所得混合物中加入_______,静置一段时间,溶液分为上下两层,肥皂在_______层,这个操作称为_______。
(4)图中长玻璃导管的作用为_______。
17.乙酸的化学性质
(1)弱酸性
①乙酸水溶液加入紫色石蕊试液,溶液变_______色,乙酸在水中的电离方程式为_______。
②乙酸的酸性比碳酸_______,乙酸与碳酸钠溶液反应的实验现象是_______,化学方程式为_______。
③与活泼金属反应
乙酸与镁反应的方程式为:_______。
(2)与乙醇的反应
①实验操作:在试管里先加入3 mL_______,边振荡,边慢慢地加入2 mL_______和2 mL_______。用酒精灯小心加热试管3~5 min。产生的蒸气经导管通到_______的液面上。
②实验现象:饱和Na2CO3溶液的液面上有_______,闻到_______味。
③化学方程式:_______。
(3)酯化反应
①概念:_______和_______作用生成_______和_______的反应。
②乙酸和乙醇的反应机理:乙酸乙酯是乙醇分子中的_______取代了乙酸分子中的_______的生成物。即乙酸脱去_______,乙醇脱去羟基上的_______,结合成水,剩余部分结合成酯。
三、工业流程题
18.你注意到汽车加油站内的标牌了吗?某些省市加油站提供的汽油标号由90#、93#换成了E90、E93,后者是在汽油中加入了10%的燃料乙醇而制得的乙醇汽油。燃料乙醇的生产过程可由下图表示:
(1)粉碎玉米的目的是______。
(2)生产过程中为了检验淀粉水解是否完全,可使用的试剂是______。
(3)步骤a的操作是______(填字母)。
A.蒸发 B.萃取 C.蒸馏 D.分液
(4)发酵产生的CO2纯度可达到99%,能回收利用,请举出它的两项用途:______、______。
(5)以玉米淀粉为原料生产乙醇的化学反应可用下式表示:
(C6H10O5)n+nH2OnC6H12O6
C6H12O6―→2C2H5OH+2CO2↑
根据上述反应式,可以算出100 kg淀粉理论上可生产无水乙醇______ kg。
四、有机推断题
19.A是植物秸秆的主要成分,以A为原料在一定条件下可获得多种有机物,它们的相互转化关系如图所示。已知F是最简单的烯烃。
请回答:
(1)F→C的反应类型是___________。
(2)C→D的化学方程式是___________。
(3)下列说法正确的是___________。
A.D能被氧化成E,但D不能被还原成C
B.实验室制备G时可用浓硫酸作催化剂和吸水剂
C.B或E均能与银氨溶液反应形成银镜
D.相同质量的B和G完全燃烧生成水的质量相等
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.A
【详解】A.乙烯与氢气发生加成反应生成乙烷,故选A;
B.乙酸与乙醇发生酯化反应生成乙酸乙酯和水,酯化反应属于取代反应,故不选B;
C.乙醇在空气中燃烧生成二氧化碳和水,反应类型为氧化反应,故不选C;
D.甲烷与氯气发生取代反应生成一氯甲烷和氯化氢,故不选D;
选A。
2.A
【详解】植物油是由3分子的高级不饱和脂肪酸和1分子甘油形成的酯,植物油水解后成分最多的为油酸,故选A。
3.C
【详解】淀粉遇到碘变蓝,是淀粉的性质,加碘水变蓝说明马铃薯中含有淀粉,故答案为C。
4.A
【详解】A.葡萄糖的分子式可表示为C6(H2O)6,表示葡萄糖分子中含有H、O两种元素的原子个数相当于6个H2O的组成,没有水分子存在,A错误;
B.葡萄糖与果糖的分子式相同,结构不同,二者互为同分异构体,B正确;
C.葡萄糖的分子式为C6H12O6,麦芽糖的分子式为C12H22O11,分子组成上不是相差“CH2”的整数倍,不互为同系物,C正确;
D.淀粉和纤维素的化学式均可用(C6H10O5)n表示,但n值不同,故两者不互为同分异构体,D正确;
故选A。
5.D
【详解】A.每个葡萄糖分子中含有5个羟基,故1 mol葡萄糖最多可以与5 mol金属钠反应放出氢气,A项正确;
B.每个葡萄糖分子中含有5个羟基,故1 mol葡萄糖最多可以与5 mol乙酸发生酯化反应,B项正确;
C.葡萄糖中含有醛基,可与新制氢氧化铜悬浊液反应产生砖红色沉淀,C项正确;
D.葡萄糖中不含羧基,与小苏打溶液不反应,D项错误;
故选D。
6.A
【详解】A.银离子是重金属离子,可使细菌(蛋白质)变性,选项A正确;
B.银元素不是人体必需元素,不需要补充,选项B错误;
C.内蒙古天气寒冷,凉得快不利于饮用,选项C错误;
D.银器并不坚固耐用,选项D错误;
答案选A。
7.D
【详解】A.棉花和淀粉放入氧气中燃烧,检验燃烧产物都是CO2和H2O,不能证明棉花和淀粉都是多糖,故A错误;
B.棉花和淀粉中没有醛基,放入银氨溶液中微热,都不发生银镜反应,不能证明棉花和淀粉都是多糖,故B错误;
C.棉花和淀粉加入浓硫酸后微热,都脱水而变黑,不能证明棉花和淀粉都是多糖,故C错误;
D.多糖在H2SO4存在下水解生成单糖(葡萄糖),再加入新制的Cu(OH)2悬浊液共热时生成Cu2O沉淀,该操作可以证明棉花和淀粉都是多糖,故D正确;
故选D。
8.D
【详解】A.地沟油和矿物油均可燃烧,A错误;
B.地沟油和矿物油均为混合物,均没有固定的沸点,B错误;
C.地沟油和矿物油密度均小于水,均难溶于水,C错误;
D.地沟油主要成分为油脂,可在碱性条件下水解,因此地沟油与NaOH溶液共热后不再分层,矿物油为烃的混合物,不能与NaOH溶液反应,因此溶液分层,D正确;
故选D。
9.C
【详解】可溶性的重金属盐能电离出重金属离子,会破坏人体蛋白质的结构,使它失去生理功能,中毒后进行急救,最好的方法就是食用富含蛋白质的食品,以防止它破坏人体的蛋白质。
A.葡萄糖溶液是糖类,A不可以;
B.生理盐水是电解质溶液,B不可以;
C.豆浆和牛奶都是富含蛋白质的食品,C可以;
D.盐水属于电解质溶液,D不可以;
综上所述,选C。
10.C
【详解】A.用饱和Na2CO3溶液除去乙酸乙酯中的乙酸,然后使用分液的方法分离有机层和水层,A正确;
B.氢氧化钠和乙醇不反应,和乙酸生成乙酸钠,然后利用乙醇沸点较低的性质,蒸馏得到乙醇,B正确;
C.溴可以和乙烯反应而进入溶液,甲烷为气体逸出,不需分液,C错误;
D.氢氧化钠和溴苯不反应、和溴反应生成盐溶液,然后使用分液的方法分离有机层和水层,D正确;
故选C。
11.A
【详解】A.为四面体结构,只能表示二溴甲烷一种分子,A项正确;
B.的有机物可能是乙醇,也可能是甲醚,B项错误;
C.的有机物可能是正丁烷,也可能是异丁烷,C项错误;
D.聚乙烯是高分子化合物,由于聚合度不确定,聚乙烯是混合物,不能只表示一种分子,D项错误;
答案选A。
12.B
【详解】A.乙醇是清洁燃料,使用乙醇汽油可以有效减少有害气体的排放,故A正确;
B.植物油是高级脂肪酸甘油酯,水解生成丙三醇和高级脂肪酸盐,故B错误;
C.乙醇中含有氧元素,可使汽油燃烧得更加充分,降低CO等有害气体的排放,故C正确;
D.乙醇可通过谷类、薯类等淀粉植物进行水解、发酵再次获得,乙醇属于可再生能源,故D正确;
选B。
13.A
【详解】A.钠的燃烧反应需要在坩埚中进行,不能在表面皿中加热,故A错误;
B.中和热测量实验中,主要是在量热器中测定反应前后的温度,该装置可以测量中和热,故B正确;
C.Na2CO3、NaHCO3溶液都呈碱性,碳酸钠碱性较强,酚酞遇碱溶液呈红色,所以向相同浓度的Na2CO3、NaHCO3溶液中滴加几滴酚酞,前者呈红色、后者为浅红色,故C正确;
D.乙酸、乙醇在浓硫酸催化下发生酯化反应,饱和碳酸钠溶液可以溶解乙醇、吸收乙酸、分离乙酸乙酯,该装置正确,故D正确;
故选:A。
14.A
【详解】在某些物理因素或化学因素的影响下,蛋白质的理化性质和生理功能发生改变的现象称为蛋白质的变性。物理因素有:加热、加压、搅拌、振荡、紫外线照射、超声波等;化学因素有:强酸、强碱、重金属盐、三氯乙酸、乙醇、丙酮等。甲醛有杀菌、防腐性能,硝酸汞是重金属盐,氢氧化钠是强碱,所以②甲醛、④硝酸汞、⑥氢氧化钠能使蛋白质变性;
故选:A。
15.B
【详解】A.花生油是多种油脂的混合物,A错误;
B.人体内含脂肪,能为人体提供能量,即油脂是人体内的重要的储能和供能物质,B正确;
C.油脂是高级脂肪酸的甘油酯,而矿物油是多种烃的混合物,不属于油脂,C错误;
D.油脂的结构有多种,即使油脂中不含其它杂质时,油脂也为混合物,D错误;
故选B。
16.(1)溶解硬脂酸甘油酯
(2)胶体
(3) 食盐 上 盐析
(4)冷凝回流
【分析】硬脂酸甘油酯(油脂)在碱性条件下的水解为皂化反应。
【详解】(1)加入酒精的作用为溶解硬脂酸甘油酯;
(2)皂化反应完成后所得混合物为胶体;
(3)混合物为胶体,向混合液中加入食盐,静置一段时间,溶液分为上下两层,肥皂在上层,这个操作称为盐析;
(4)油脂的沸点较低,加热易挥发,长导管的作用是冷凝回流。
17.(1) 红 CH3COOHCH3COO-+H+ 强
有无色气体产生 2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O 2CH3COOH+Mg→(CH3COO)2Mg+H2↑
(2) 乙醇 98%浓硫酸 冰醋酸 饱和碳酸钠溶液 油状液体生成 香 CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O
(3) 醇 酸 酯 水 乙氧基(CH3CH2O-) 羟基(-OH) 氢原子 氢
【解析】(1)
①乙酸有酸的通性,遇到紫色石蕊变红;乙酸是弱酸,水中部分电离,电离方程式为CH3COOH CH3COO-+H+;
②乙酸的酸性比碳酸强,乙酸与碳酸钠反应生成乙酸钠、水和二氧化碳,实验现象是有无色气体产生;化学方程式为2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O;
③乙酸与镁反应生成乙酸镁和氢气,方程式为2CH3COOH+Mg→(CH3COO)2Mg+H2↑;
(2)
①乙醇与乙酸反应制备乙酸乙酯的过程中,应先加入3 mL乙醇,边振荡,边慢慢地加入2 mL98%浓硫酸和2 mL冰醋酸,反应中用饱和碳酸钠溶液吸收;
②乙酸乙酯在饱和碳酸钠溶液中溶解度比较小,且密度比碳酸钠溶液小,故饱和Na2CO3溶液的液面上有油状液体生成,低级酯具有香味,故可以闻到香味;
③化学方程式为CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O;
(3)
①酯化反应是醇和酸作用生成酯和水的反应;
②乙酸乙酯是乙醇分子中的乙氧基(CH3CH2O-)取代了乙酸分子中的羟基(-OH) 的生成物;即乙酸脱去氢原子,乙醇脱去羟基上的氢,结合成水,剩余部分结合成酯。
18.(1)增大反应物的接触面积或加快反应速率或使反应充分进行
(2)碘(I2)或碘酒或革兰氏碘液
(3)C
(4) 制饮料 制干冰
(5)56.8
【解析】(1)
粉碎玉米是增大反应的接触面积,加快反应速率,提高原料的利用率,故答案为:增大反应物的接触面积或加快反应速率或使反应充分进行;
(2)
因为淀粉遇I2变蓝色,只要有淀粉存在,加I2一定变蓝色,因此可用I2或碘酒来检验淀粉是否水解完全,故答案为:碘(I2)或碘酒或革兰氏碘液;
(3)
滤去废渣后得到的是水和乙醇的混合溶液,由于乙醇和水互溶,但沸点不同,乙醇的沸点低于水,用蒸馏的方法可使乙醇从混合液中分离出来,故答案为:C;
(4)
纯度为99%的CO2,可以很好的利用。因为CO2可以做碳酸饮料,也可以制干冰,也可制纯碱或制碳酸钙等,故答案为:制饮料;制干冰;
(5)
由(C6H10O5)n+nH2OnC6H12O6 C6H12O6―→2C2H5OH+2CO2↑可得到关系式:(C6H10O5)n~2nC2H5OH,设理论上可生产无水乙醇的质量为x,
,,故答案为:56.8。
19. 加成反应 B
【详解】分析流程可知A为纤维素,B为葡萄糖,C为乙醇,D为乙醛,E为乙酸,F为乙烯,G为乙酸乙酯。
(1)由为乙烯与水反应生成乙醇,为加成反应;
(2)为乙醇氧化生成乙醛,反应方程式为:;
(3) A.乙醛可以被氧化生成乙酸,同时可以被氢气还原生成乙醇,A项错误;
B.在制备乙酸乙酯时,浓硫酸起催化剂和吸水剂的作用,B项正确;
C.乙酸不能与银氨溶液反应形成银镜,C项错误;
D.葡萄糖的分子式为,乙酸乙酯的分子式为,相同质量的葡萄糖和乙酸乙酯中氢元素的含量不相同,生成水的质量也不相等,D项错误;故答案为:B。
答案第1页,共2页
答案第1页,共2页
