【教材全解】14-15学年人教化学必修1学案:1.1化学实验基本方法(第2课时)
文档属性
| 名称 | 【教材全解】14-15学年人教化学必修1学案:1.1化学实验基本方法(第2课时) | 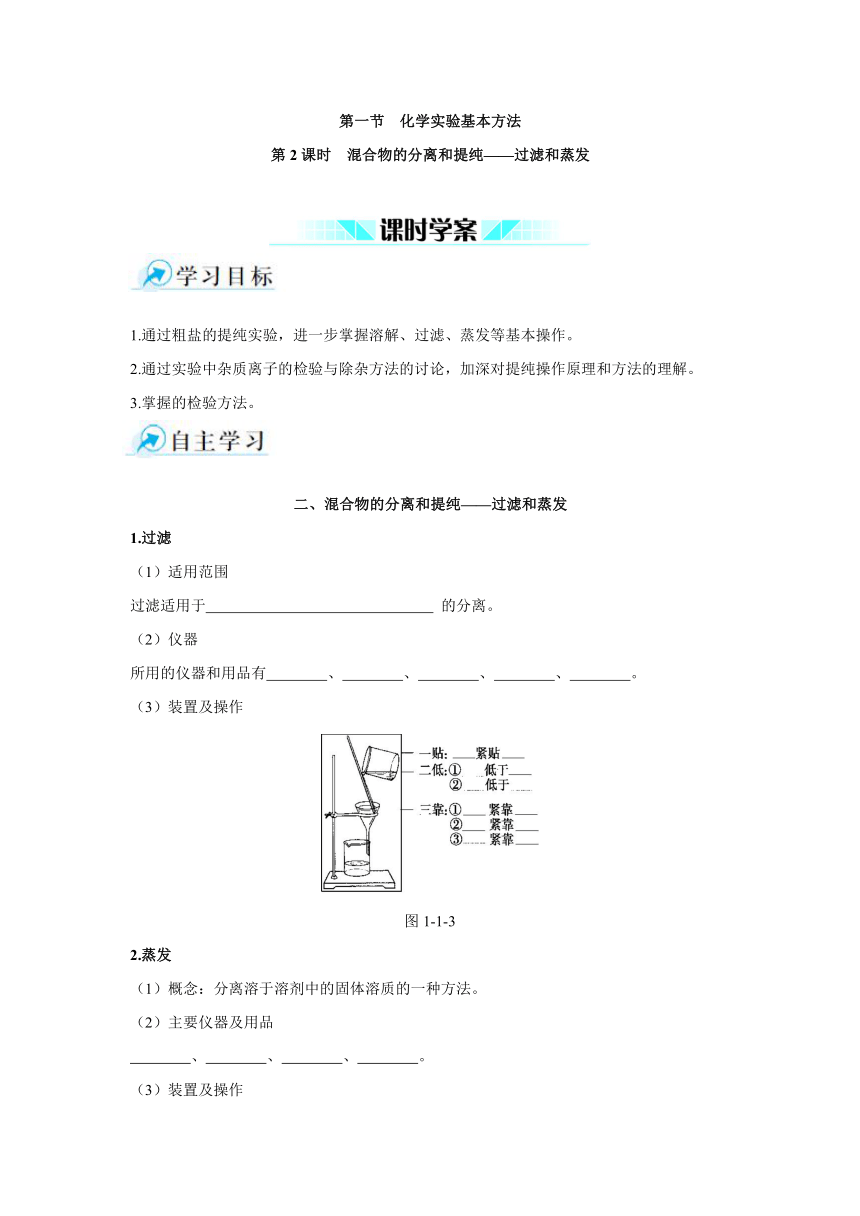 | |
| 格式 | zip | ||
| 文件大小 | 231.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2014-10-17 11:32:17 | ||
图片预览




文档简介
第一节 化学实验基本方法
第2课时 混合物的分离和提纯——过滤和蒸发
1.通过粗盐的提纯实验,进一步掌握溶解、过滤、蒸发等基本操作。
2.通过实验中杂质离子的检验与除杂方法的讨论,加深对提纯操作原理和方法的理解。
3.掌握的检验方法。
二、混合物的分离和提纯——过滤和蒸发
1.过滤
(1)适用范围
过滤适用于 的分离。
(2)仪器
所用的仪器和用品有 、 、 、 、 。
(3)装置及操作
( http: / / www.21cnjy.com )
图1-1-3
2.蒸发
(1)概念:分离溶于溶剂中的固体溶质的一种方法。
(2)主要仪器及用品
、 、 、 。
(3)装置及操作
( http: / / www.21cnjy.com )
图1-1-4
3.粗盐的提纯
(1)粗盐中含有泥沙、氯化钙、氯化镁、硫 ( http: / / www.21cnjy.com )酸盐等杂质,要通过 、 、 进行提纯。以上操作都要用到玻璃棒,它们的作用依次是:① 溶解;②引流;③ 。
(2)粗盐中可溶性杂质的去除方法
杂质 加入的试剂 发生反应的化学方程式
硫酸盐
多余的 、 适量
4. 的检验
(1)试剂: ;
(2)步骤:
沉淀,证明原溶液中有。
1.进行过滤操作应选用的一组仪器是( )
A.滤纸、烧杯、试管夹、漏斗、玻璃棒
B.烧杯、酒精灯、试管、漏斗
C.漏斗、玻璃棒、烧杯、铁架台、滤纸
D.玻璃棒、滤纸、烧瓶、漏斗、铁架台
2.下列混合物能用过滤法分离的是( )
A.汽油和水 B.食盐和蔗糖 C.泥沙和食盐 D.铜粉和铝粉
3.某学生发现滴瓶中的溶液有悬浮物,拟用如图1-1-5所示操作进行过滤,错误的操作有( )
( http: / / www.21cnjy.com )
图1-1-5
A.0处 B.3处 C.2处 D.1处
4.下列确定某溶液中一定有的方法中,正确的是( )
A.先加溶液有白色沉淀,再加稀盐酸沉淀不消失
B.先加溶液有白色沉淀,再加稀硝酸沉淀不消失
C.先加溶液有白色沉淀,再加稀盐酸沉淀不消失
D.先加稀盐酸无明显现象,再加溶液有白色沉淀
二、混合物的分离和提纯——过滤和蒸发
1.过滤和蒸发
【问题1】(1)你知道沙里淘金吗?淘金者是用什么原理和方法将金从沙里分离出来的?
(2)你能用哪些方法将铁屑分离出来?
【问题2】分离和提纯物质就是要除掉杂质。化学上所指的杂质都是有害和无价值的吗?你怎样看待这个问题?能举出一些例子吗?
【问题3】在初中,我们已经学习了粗盐的提纯,请同学们结合初中所学知识,思考:
(1)粗盐的提纯实验所用的仪器有哪些?
(2)提纯有哪些主要步骤?
(3)在粗盐的提纯实验中,应注意哪些问题?
(4)在粗盐的提纯实验中,几次用到了玻璃棒,其作用和目的是什么?
(5)阅读教材第5页实验1-1,填写下表:
步骤 现象
①溶解:
②过滤:
③蒸发:
例1 “粗盐的提纯”实验中,蒸发时,正确的操作是( )
A.把浑浊的液体倒入蒸发皿内加热
B.开始析出晶体后用玻璃棒搅拌
C.待水分完全蒸干后停止加热
D.蒸发皿中出现较多量固体时即停止加热
【思考与交流】
(1)过滤和蒸发都适用于固体和液体混合物的分离,它们适用的对象一样吗?
(2)若有两种固体,要使它们分离开来,可以采用什么办法?
2.的检验
【问题4】我们推测在提纯后的食盐中含有,你能否设计一个简单的实验,验证此盐中是否含有?
(1)试剂: 。
(2)步骤:
沉淀,证明原溶液中有。
(3)原理: 。
3.除去粗盐中含有的可溶性杂质
【问题5】如果要除去粗盐中含有的可溶性杂质、及一些硫酸盐,应加入什么试剂?请填写下表(可参考相应物质的溶解性)。
杂质 加入的试剂 化学方程式
硫酸盐
【问题6】在实际操作中,还要考虑所加试剂的 ( http: / / www.21cnjy.com )先后顺序、试剂用量,以及试剂过量后如何处理等。你设计的除去杂质的方法中有没有引入其他离子?想一想可用什么方法把它们除去?
分析:为了全部除去杂质离子,所加试剂必须过量(适量是难以控制的),这就带来了过量试剂如何除去的问题。
过量的应用 除去,过量的和应用 除去。必须在 后面加入, 在过滤后加入。
所以试剂添加顺序为: 。
例2 (2014·大纲全国高考)下列除杂方案错误的是( )
选项 被提纯的物质 杂质 除杂试剂 除杂方法
A CO(g) (g) NaOH溶液、 浓 洗气
B (aq) (aq) NaOH溶液 过滤
C (g) HCl(g) 饱和食盐水、 浓 洗气
D (s) (s) — 灼烧
1.有关化学实验的下列操作中,一般情况下不能相互接触的是( )
A.过滤操作中,玻璃棒与三层滤纸
B.过滤操作中,漏斗颈与烧杯内壁
C.过滤操作中,玻璃棒与烧杯口
D.用胶头滴管向试管中滴加液体时,滴管尖端与试管内壁
2.下列各组物质中,可按溶解、过滤、蒸发的操作顺序分离的是( )
A.氧化铜和炭粉 B.硝酸钾和氯化钠
C.水和酒精 D.碳酸钠和硫酸钡
3.某溶液中含有较大量的、、三种阴离子,如果只取一次该溶液就能够分别将三种阴离子依次检验出来,下列实验操作顺序正确的是( )
①滴加溶液 ②过滤 ③滴加溶液 ④滴加溶液
A.①②④②③ B.④②①②③ C.①②③②④ D.④②③②①
4.由海水制备无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是( )
A.②④⑤③① B.③②④①⑤ C.③④②⑤① D.②④③⑤①
作业一
作业内容见课本第10页第3、6、7题。
作业二
作业内容见“课时练案”。
作业三
作业内容见“课时学案”中的“自主学习”和“自我检测”。
[自主学习]答案
1.(1)不溶性固体与液体
(2)漏斗 玻璃棒 烧杯 铁架台(带铁圈) 滤纸
(3)一贴:滤纸 漏斗内壁
二低:①滤纸边沿 漏斗边沿 ②液面 滤纸边沿
三靠:①漏斗下端 烧杯内壁 ②玻璃棒下端 三层滤纸处 烧杯嘴 玻璃棒
2.(2)铁架台 酒精灯 玻璃棒 蒸发皿
(3)①搅拌 ②出现大量固体
3.(1)溶解 过滤 蒸发 ①加速 ③搅拌,防止液体溅出
溶液 +═2NaCl+↓ NaOH溶液 ( http: / / www.21cnjy.com ) +2NaOH═↓+2NaCl 溶液 +═↓+2NaCl 溶液 NaOH溶液 稀盐酸 +2HCl═2NaCl+↑+、NaOH+HCl═NaCl+
溶液、稀盐酸 (2)白色
[自我检测]答案与解析
1.C
2.C 解析:过滤适用于 ( http: / / www.21cnjy.com )不溶性固体与液体的分离。将C项中物质加入足量水中,食盐完全溶解形成食盐溶液(液体),而泥沙不溶于水,可用过滤法分离。
3.B 解析:操作上错误的地方有3处:①液体未用玻璃棒引流;②标签没有对着手心;③漏斗颈的末端未与烧杯的内壁相接触。
4.D 解析:先加稀盐酸提供,可排除杂质离子的干扰,再加溶液,有白色沉淀产生,可证明一定有。
[课内巩固练习]答案与解析
1.D 解析:A、B、C三个选项是过 ( http: / / www.21cnjy.com )滤操作中“三靠”的基本内容,故必须相互接触;用胶头滴管向试管中滴加液体时,滴管尖端与试管内壁不能接触,否则会污染滴管。
2.D 解析:A项,氧化铜和炭粉 ( http: / / www.21cnjy.com )均不溶于水,无法按上述顺序分离;B项,硝酸钾和氯化钠均溶于水,无法按上述顺序分离;C项,水和酒精相互溶解,无法按上述顺序分离;D项,碳酸钠易溶于水,硫酸钡不溶于水,能按上述顺序分离。
3.B 解析:首先滴加足量溶液, ( http: / / www.21cnjy.com )如果出现白色沉淀,证明有,同时除去;过滤后,在滤液中加入足量溶液,如果出现白色沉淀,证明有,同时除去;过滤后,滴加溶液,如果出现白色沉淀,证明有。
4.D 解析:要从海水中得到无水,首先要加 ( http: / / www.21cnjy.com )熟石灰得到沉淀,然后过滤,再将沉淀加盐酸溶解,得到溶液,然后对溶液浓缩结晶,再对晶体脱水干燥即可,故选D。
[课外作业]答案与解析
作业一
3.CD 解析:加热时应用酒精灯外焰;向试管中滴加液体时,应使胶头滴管在试管口上方竖直滴加。
6.实验仪器:试管两个、玻璃导管两段、橡胶管一段、橡胶塞一个、药匙一个。
实验药品:小颗粒状大理石、稀盐酸、澄清石灰水。
( http: / / www.21cnjy.com )
图1-1-6
实验步骤:(1)按图1-1-6所示将各仪器组装在一起。
(2)检验组装好的实验装置的气密性,并使装置的气密性良好。
(3)将约10 mL澄清的 ( http: / / www.21cnjy.com )石灰水装入试管Ⅱ,将约2 g大理石装入试管Ⅰ(小心不要打破试管),将约 5 mL 稀盐酸倒入试管Ⅰ,再将试管、导管和橡胶塞按图1-1-6组装好。观察试管Ⅱ中的澄清石灰水是否变浑浊。
实验现象:试管Ⅱ中的澄清石灰水变浑浊。
实验结论:大理石中含有。
+2HCl═↑ ═↓
同理实验,说明纯碱中含有,陶瓷片、玻璃片中不存在碳酸盐。
解析:命题目的是要求应用实验原理,会设计离子检验的实验步骤并通过实验操作解决实际问题。
7.不可靠。若被检样品中含有或,加入的化学试剂又是溶液,它们也会发生化学反应生成白色沉淀。如:
═↓+2NaCl ═2AgCl↓
应该先加稀盐酸酸化,若无沉淀生成,再加入溶液,若生成白色沉淀,说明被检的样品中含有硫酸盐。
解析:命题目的是要求掌握的检验,实验中要排除和的干扰。
第2课时 混合物的分离和提纯——过滤和蒸发
1.通过粗盐的提纯实验,进一步掌握溶解、过滤、蒸发等基本操作。
2.通过实验中杂质离子的检验与除杂方法的讨论,加深对提纯操作原理和方法的理解。
3.掌握的检验方法。
二、混合物的分离和提纯——过滤和蒸发
1.过滤
(1)适用范围
过滤适用于 的分离。
(2)仪器
所用的仪器和用品有 、 、 、 、 。
(3)装置及操作
( http: / / www.21cnjy.com )
图1-1-3
2.蒸发
(1)概念:分离溶于溶剂中的固体溶质的一种方法。
(2)主要仪器及用品
、 、 、 。
(3)装置及操作
( http: / / www.21cnjy.com )
图1-1-4
3.粗盐的提纯
(1)粗盐中含有泥沙、氯化钙、氯化镁、硫 ( http: / / www.21cnjy.com )酸盐等杂质,要通过 、 、 进行提纯。以上操作都要用到玻璃棒,它们的作用依次是:① 溶解;②引流;③ 。
(2)粗盐中可溶性杂质的去除方法
杂质 加入的试剂 发生反应的化学方程式
硫酸盐
多余的 、 适量
4. 的检验
(1)试剂: ;
(2)步骤:
沉淀,证明原溶液中有。
1.进行过滤操作应选用的一组仪器是( )
A.滤纸、烧杯、试管夹、漏斗、玻璃棒
B.烧杯、酒精灯、试管、漏斗
C.漏斗、玻璃棒、烧杯、铁架台、滤纸
D.玻璃棒、滤纸、烧瓶、漏斗、铁架台
2.下列混合物能用过滤法分离的是( )
A.汽油和水 B.食盐和蔗糖 C.泥沙和食盐 D.铜粉和铝粉
3.某学生发现滴瓶中的溶液有悬浮物,拟用如图1-1-5所示操作进行过滤,错误的操作有( )
( http: / / www.21cnjy.com )
图1-1-5
A.0处 B.3处 C.2处 D.1处
4.下列确定某溶液中一定有的方法中,正确的是( )
A.先加溶液有白色沉淀,再加稀盐酸沉淀不消失
B.先加溶液有白色沉淀,再加稀硝酸沉淀不消失
C.先加溶液有白色沉淀,再加稀盐酸沉淀不消失
D.先加稀盐酸无明显现象,再加溶液有白色沉淀
二、混合物的分离和提纯——过滤和蒸发
1.过滤和蒸发
【问题1】(1)你知道沙里淘金吗?淘金者是用什么原理和方法将金从沙里分离出来的?
(2)你能用哪些方法将铁屑分离出来?
【问题2】分离和提纯物质就是要除掉杂质。化学上所指的杂质都是有害和无价值的吗?你怎样看待这个问题?能举出一些例子吗?
【问题3】在初中,我们已经学习了粗盐的提纯,请同学们结合初中所学知识,思考:
(1)粗盐的提纯实验所用的仪器有哪些?
(2)提纯有哪些主要步骤?
(3)在粗盐的提纯实验中,应注意哪些问题?
(4)在粗盐的提纯实验中,几次用到了玻璃棒,其作用和目的是什么?
(5)阅读教材第5页实验1-1,填写下表:
步骤 现象
①溶解:
②过滤:
③蒸发:
例1 “粗盐的提纯”实验中,蒸发时,正确的操作是( )
A.把浑浊的液体倒入蒸发皿内加热
B.开始析出晶体后用玻璃棒搅拌
C.待水分完全蒸干后停止加热
D.蒸发皿中出现较多量固体时即停止加热
【思考与交流】
(1)过滤和蒸发都适用于固体和液体混合物的分离,它们适用的对象一样吗?
(2)若有两种固体,要使它们分离开来,可以采用什么办法?
2.的检验
【问题4】我们推测在提纯后的食盐中含有,你能否设计一个简单的实验,验证此盐中是否含有?
(1)试剂: 。
(2)步骤:
沉淀,证明原溶液中有。
(3)原理: 。
3.除去粗盐中含有的可溶性杂质
【问题5】如果要除去粗盐中含有的可溶性杂质、及一些硫酸盐,应加入什么试剂?请填写下表(可参考相应物质的溶解性)。
杂质 加入的试剂 化学方程式
硫酸盐
【问题6】在实际操作中,还要考虑所加试剂的 ( http: / / www.21cnjy.com )先后顺序、试剂用量,以及试剂过量后如何处理等。你设计的除去杂质的方法中有没有引入其他离子?想一想可用什么方法把它们除去?
分析:为了全部除去杂质离子,所加试剂必须过量(适量是难以控制的),这就带来了过量试剂如何除去的问题。
过量的应用 除去,过量的和应用 除去。必须在 后面加入, 在过滤后加入。
所以试剂添加顺序为: 。
例2 (2014·大纲全国高考)下列除杂方案错误的是( )
选项 被提纯的物质 杂质 除杂试剂 除杂方法
A CO(g) (g) NaOH溶液、 浓 洗气
B (aq) (aq) NaOH溶液 过滤
C (g) HCl(g) 饱和食盐水、 浓 洗气
D (s) (s) — 灼烧
1.有关化学实验的下列操作中,一般情况下不能相互接触的是( )
A.过滤操作中,玻璃棒与三层滤纸
B.过滤操作中,漏斗颈与烧杯内壁
C.过滤操作中,玻璃棒与烧杯口
D.用胶头滴管向试管中滴加液体时,滴管尖端与试管内壁
2.下列各组物质中,可按溶解、过滤、蒸发的操作顺序分离的是( )
A.氧化铜和炭粉 B.硝酸钾和氯化钠
C.水和酒精 D.碳酸钠和硫酸钡
3.某溶液中含有较大量的、、三种阴离子,如果只取一次该溶液就能够分别将三种阴离子依次检验出来,下列实验操作顺序正确的是( )
①滴加溶液 ②过滤 ③滴加溶液 ④滴加溶液
A.①②④②③ B.④②①②③ C.①②③②④ D.④②③②①
4.由海水制备无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是( )
A.②④⑤③① B.③②④①⑤ C.③④②⑤① D.②④③⑤①
作业一
作业内容见课本第10页第3、6、7题。
作业二
作业内容见“课时练案”。
作业三
作业内容见“课时学案”中的“自主学习”和“自我检测”。
[自主学习]答案
1.(1)不溶性固体与液体
(2)漏斗 玻璃棒 烧杯 铁架台(带铁圈) 滤纸
(3)一贴:滤纸 漏斗内壁
二低:①滤纸边沿 漏斗边沿 ②液面 滤纸边沿
三靠:①漏斗下端 烧杯内壁 ②玻璃棒下端 三层滤纸处 烧杯嘴 玻璃棒
2.(2)铁架台 酒精灯 玻璃棒 蒸发皿
(3)①搅拌 ②出现大量固体
3.(1)溶解 过滤 蒸发 ①加速 ③搅拌,防止液体溅出
溶液 +═2NaCl+↓ NaOH溶液 ( http: / / www.21cnjy.com ) +2NaOH═↓+2NaCl 溶液 +═↓+2NaCl 溶液 NaOH溶液 稀盐酸 +2HCl═2NaCl+↑+、NaOH+HCl═NaCl+
溶液、稀盐酸 (2)白色
[自我检测]答案与解析
1.C
2.C 解析:过滤适用于 ( http: / / www.21cnjy.com )不溶性固体与液体的分离。将C项中物质加入足量水中,食盐完全溶解形成食盐溶液(液体),而泥沙不溶于水,可用过滤法分离。
3.B 解析:操作上错误的地方有3处:①液体未用玻璃棒引流;②标签没有对着手心;③漏斗颈的末端未与烧杯的内壁相接触。
4.D 解析:先加稀盐酸提供,可排除杂质离子的干扰,再加溶液,有白色沉淀产生,可证明一定有。
[课内巩固练习]答案与解析
1.D 解析:A、B、C三个选项是过 ( http: / / www.21cnjy.com )滤操作中“三靠”的基本内容,故必须相互接触;用胶头滴管向试管中滴加液体时,滴管尖端与试管内壁不能接触,否则会污染滴管。
2.D 解析:A项,氧化铜和炭粉 ( http: / / www.21cnjy.com )均不溶于水,无法按上述顺序分离;B项,硝酸钾和氯化钠均溶于水,无法按上述顺序分离;C项,水和酒精相互溶解,无法按上述顺序分离;D项,碳酸钠易溶于水,硫酸钡不溶于水,能按上述顺序分离。
3.B 解析:首先滴加足量溶液, ( http: / / www.21cnjy.com )如果出现白色沉淀,证明有,同时除去;过滤后,在滤液中加入足量溶液,如果出现白色沉淀,证明有,同时除去;过滤后,滴加溶液,如果出现白色沉淀,证明有。
4.D 解析:要从海水中得到无水,首先要加 ( http: / / www.21cnjy.com )熟石灰得到沉淀,然后过滤,再将沉淀加盐酸溶解,得到溶液,然后对溶液浓缩结晶,再对晶体脱水干燥即可,故选D。
[课外作业]答案与解析
作业一
3.CD 解析:加热时应用酒精灯外焰;向试管中滴加液体时,应使胶头滴管在试管口上方竖直滴加。
6.实验仪器:试管两个、玻璃导管两段、橡胶管一段、橡胶塞一个、药匙一个。
实验药品:小颗粒状大理石、稀盐酸、澄清石灰水。
( http: / / www.21cnjy.com )
图1-1-6
实验步骤:(1)按图1-1-6所示将各仪器组装在一起。
(2)检验组装好的实验装置的气密性,并使装置的气密性良好。
(3)将约10 mL澄清的 ( http: / / www.21cnjy.com )石灰水装入试管Ⅱ,将约2 g大理石装入试管Ⅰ(小心不要打破试管),将约 5 mL 稀盐酸倒入试管Ⅰ,再将试管、导管和橡胶塞按图1-1-6组装好。观察试管Ⅱ中的澄清石灰水是否变浑浊。
实验现象:试管Ⅱ中的澄清石灰水变浑浊。
实验结论:大理石中含有。
+2HCl═↑ ═↓
同理实验,说明纯碱中含有,陶瓷片、玻璃片中不存在碳酸盐。
解析:命题目的是要求应用实验原理,会设计离子检验的实验步骤并通过实验操作解决实际问题。
7.不可靠。若被检样品中含有或,加入的化学试剂又是溶液,它们也会发生化学反应生成白色沉淀。如:
═↓+2NaCl ═2AgCl↓
应该先加稀盐酸酸化,若无沉淀生成,再加入溶液,若生成白色沉淀,说明被检的样品中含有硫酸盐。
解析:命题目的是要求掌握的检验,实验中要排除和的干扰。
