第1章第2节化学能转化为电能——电池同步练习 (含解析)2022-2023学年上学期高二化学鲁科版(2019)选择性必修1
文档属性
| 名称 | 第1章第2节化学能转化为电能——电池同步练习 (含解析)2022-2023学年上学期高二化学鲁科版(2019)选择性必修1 |
|
|
| 格式 | docx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-05 00:00:00 | ||
图片预览



文档简介
第1章第2节化学能转化为电能——电池同步练习
学校:___________姓名:___________班级:___________考号:___________
一、单选题
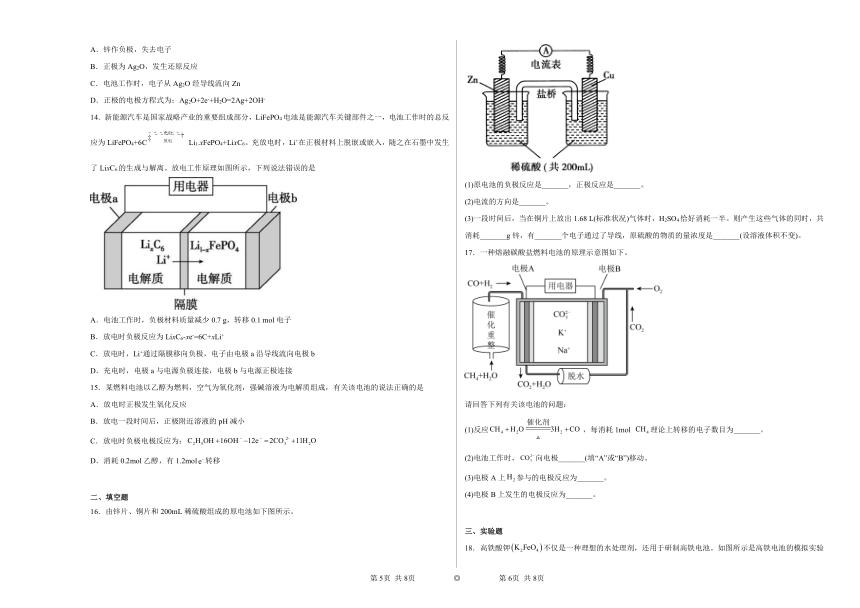
1.锂空气电池因其比能量非常高,具有广阔应用前景。下图是一种锂空气电池的工作示意图,下列分析正确的是
A.放电时,a电极的反应式为
B.有机电解液可换成水溶液
C.转移4mol电子,b电极消耗22.4L的氧气
D.放电时,电流从a电极经外电路流回b电极
2.我国科研工作者发明了一种高性能的水系锰基锌电池[],电池工作示意图如图,该电池工作一段时间后,的浓度增大。下列说法正确的是
A.电极X的材料为Zn
B.膜a、b分别为阳、阴离于交换膜
C.正极反应式为
D.当的物质的量增大0.1mol时,电路中转移0.4mol电子
3.下列原电池装置图示中电子或离子流向、正极或负极等标注不正确的是
A B C D
铅蓄电池 锌银纽扣电池 燃料电池 锌铜原电池
A.A B.B C.C D.D
4.科学家近年来研制出一种新型细菌燃料电池,利用细菌将有机酸转化为氢气,氢气进入以磷酸为电解质的燃料电池中发电,电池负极反应式为
A.H2+2OH--2e-=2H2O B.O2+4H++4e-=2H2O
C.H2-2e-=2H+ D.O2+2H2O+4e-=4OH-
5.下列电池不属于二次电池的是
A B C D
手机用锂电池 电动汽车用电池 铅酸蓄电池 锌锰干电池
A.A B.B C.C D.D
6.一种酸性生物燃料电池应用的原理如图所示,下列说法错误的是
A.Ca2+、Mg2+透过离子交换膜X移向a极
B.负极反应式为C6H12O6+6H2O-24e-=6CO2↑+24H+
C.1molC6H12O6转化为CO2,迁移到正极区的离子总数为12NA
D.该装置可用于硬水软化,同时还可产生电能
7.碱性锌锰电池的总反应为:Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2。下列说法正确的是
A.Zn为正极,MnO2为负极
B.该电池为二次电池
C.负极的电极反应式为:Zn+2OH--2e-=Zn(OH)2
D.工作时电子由MnO2经外电路流向
8.一种燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧作用生成水和二氧化碳。该电池负极发生的反应是
A.
B.
C.
D.
9.某汽车尾气分析仪以燃料电池为工作原理测定CO的浓度,其装置如图所示,该电池中电解质为氧化钇—氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法不正确的是
A.工作时电极b作正极,O2-由电极b流向电极a
B.负极的电极反应式为:
C.当传感器中通过2×10-3mol电子时,通过的尾气中含有2.24mLCO
D.传感器中通过的电流越大,尾气中CO的含量越高
10.美国《时代周刊》将氢燃料电池评为21世纪对人类生活具有重大影响的技术之一、培根电池是一种碱性的氢氧燃料电池,已经应用在“阿波罗六号”太空船上。将多个培根电池组合为电池组,向外供电,电池组工作稳定后,它的电动势和内阻基本保持不变。电池所产生的水可以作为饮用水,今欲得常温下水1L,则电池内电子转移的物质的量约为
A.8.9×10-3 mol B.4.5×10-2 mol
C.1.1×102 mol D.5.6×10 mol
11.用选项中的电极、溶液和如图所示装置可组成原电池。下列现象或结论的叙述正确的是
选项 电极a 电极b A溶液 B溶液 现象或结论
A Cu Zn CuSO4 ZnSO4 一段时间后,a增加的质量与b减少的质量相等
B Cu Zn 稀H2SO4 ZnSO4 盐桥中阳离子向b极移动
C Fe C NaCl FeCl3 外电路电子转移方向:b→a
D C C FeCl3 KI、淀粉混合液 若开始时只增大FeCl3溶液浓度,b极附近溶液变蓝的速度加快
A.A B.B C.C D.D
12.有A、B、D、E四种金属,当A、B组成原电池时,电子流动方向A→B;当A、D组成原电池时,A为正极;B与E构成原电池时,电极反应式为:E2++2e-=E,B-2e-=B2+则A、B、D、E金属性由强到弱的顺序为
A.A﹥B﹥E﹥D B.A﹥B﹥D﹥E
C.D﹥E﹥A﹥B D.D﹥A﹥B﹥E
13.银锌纽扣电池的电池反应式为:Zn+Ag2O+H2O=Zn(OH)2+2Ag。下列说法不正确的是
A.锌作负极,失去电子
B.正极为Ag2O,发生还原反应
C.电池工作时,电子从Ag2O经导线流向Zn
D.正极的电极方程式为:Ag2O+2e-+H2O=2Ag+2OH-
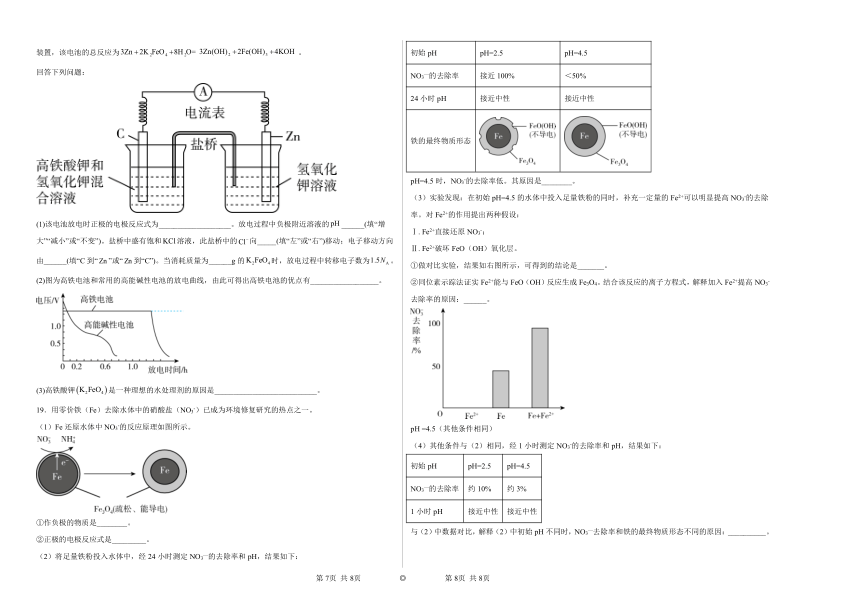
14.新能源汽车是国家战略产业的重要组成部分,LiFePO4电池是能源汽车关键部件之一,电池工作时的总反应为LiFePO4+6CLi1-xFePO4+LixC6。充放电时,Li+在正极材料上脱嵌或嵌入,随之在石墨中发生了LixC6的生成与解离。放电工作原理如图所示,下列说法错误的是
A.电池工作时,负极材料质量减少0.7 g,转移0.1 mol电子
B.放电时负极反应为LixC6-xe-=6C+xLi+
C.放电时,Li+通过隔膜移向负极,电子由电极a沿导线流向电极b
D.充电时,电极a与电源负极连接,电极b与电源正极连接
15.某燃料电池以乙醇为燃料,空气为氧化剂,强碱溶液为电解质组成,有关该电池的说法正确的是
A.放电时正极发生氧化反应
B.放电一段时间后,正极附近溶液的pH减小
C.放电时负极电极反应为:
D.消耗0.2mol乙醇,有1.2mol转移
二、填空题
16.由锌片、铜片和200mL稀硫酸组成的原电池如下图所示。
(1)原电池的负极反应是_______,正极反应是_______。
(2)电流的方向是_______。
(3)一段时间后,当在铜片上放出1.68 L(标准状况)气体时,H2SO4恰好消耗一半。则产生这些气体的同时,共消耗_______g锌,有_______个电子通过了导线,原硫酸的物质的量浓度是_______(设溶液体积不变)。
17.一种熔融碳酸盐燃料电池的原理示意图如下。
请回答下列有关该电池的问题:
(1)反应,每消耗1mol 理论上转移的电子数目为_______。
(2)电池工作时,向电极_______(填“A”或“B”)移动。
(3)电极A上参与的电极反应为_______。
(4)电极B上发生的电极反应为_______。
三、实验题
18.高铁酸钾不仅是一种理想的水处理剂,还用于研制高铁电池。如图所示是高铁电池的模拟实验装置,该电池的总反应为。
回答下列问题:
(1)该电池放电时正极的电极反应式为___________________。放电过程中负极附近溶液的______(填“增大”“减小”或“不变”)。盐桥中盛有饱和溶液,此盐桥中的向_____(填“左”或“右”)移动;电子移动方向由______(填“C到“”或“到“C”)。当消耗质量为______g的时,放电过程中转移电子数为。
(2)图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有__________________。
(3)高铁酸钾是一种理想的水处理剂的原因是___________________________。
19.用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如图所示。
①作负极的物质是________。
②正极的电极反应式是_________。
(2)将足量铁粉投入水体中,经24小时测定NO3—的去除率和pH,结果如下:
初始pH pH=2.5 pH=4.5
NO3—的去除率 接近100% <50%
24小时pH 接近中性 接近中性
铁的最终物质形态
pH=4.5时,NO3-的去除率低。其原因是________。
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3-的去除率。对Fe2+的作用提出两种假设:
Ⅰ. Fe2+直接还原NO3-;
Ⅱ. Fe2+破坏FeO(OH)氧化层。
①做对比实验,结果如右图所示,可得到的结论是_______。
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4。结合该反应的离子方程式,解释加入Fe2+提高NO3-去除率的原因:______。
pH =4.5(其他条件相同)
(4)其他条件与(2)相同,经1小时测定NO3-的去除率和pH,结果如下:
初始pH pH=2.5 pH=4.5
NO3—的去除率 约10% 约3%
1小时pH 接近中性 接近中性
与(2)中数据对比,解释(2)中初始pH不同时,NO3—去除率和铁的最终物质形态不同的原因:__________。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.A
【分析】结合图示装置,Li失去电子为负极,则a为负极,b为正极,据此判断。
【详解】A.放电时,图中负极为Li,根据电解液传导离子为锂离子,故电极反应为:Li-e-=Li+,A正确;
B.Li和水反应,不能把有机电解液换成水溶液,B错误;
C.气体未说明存在状态,无法计算,C错误;
D.a为负极,b为正极,放电时,电流从b电极经外电路流回a电极,D错误;
故选A。
2.C
【详解】A.由图中电子流动方向可知电极Y为负极,材料为Zn,电极X为正极,材料为,故A错误;
B.一段时间后,的浓度增大说明程a、b分别为阴、阳离子交换膜,故B错误;
C.根据总反应,锰化合价降低,则正极反应式为,故C正确;
D.的物质的量增大0.1m时,电路中转移0.2ml电子,故D错误。
综上所述,答案为C。
3.C
【详解】A.铅蓄电池中二氧化铅作正极,铅作负极,标注正确,故A不符合题意;
B.锌银纽扣电池中锌作负极,氧化银作正极,标注正确,故B不符合题意;
C.氢氧燃料电池中氢气作负极,是电子流出极,溶液中氢离子通过质子交换膜从左向右移动,标注错误,故C符合题意;
D.锌铜原电池中锌作负极,铜作正极,钾离子向正极即向左移动,标注正确,故D不符合题意;
故答案选C。
4.C
【详解】根据题给信息,该燃料电池的总反应为2H2+O2=2H2O。
A.电解液为酸性溶液,电极反应式中不能出现OH-,选项A错误;
B.因为燃料电池中负极通入氢气,正极通入氧气,选项B错误;
C.燃料电池中负极通入氢气,氢气失电子产生H+,电极反应式为H2-2e-=2H+,选项C正确;
D.电解液为酸性溶液,电极反应式中不能出现OH-,选项D错误;
答案选C。
5.D
【详解】A.手机用锂电池,可充电,属于二次电池,故A不选;
B.电动汽车用电池,可充电,属于二次电池,故B不选;
C.铅酸蓄电池,可充电,属于二次电池,故C不选;
D.锌锰干电池不可充电,属于一次电池,故D选;
故选D。
6.A
【分析】根据电子流向可知,a为负极、b为正极;
【详解】A.原电池中阳离子向正极移动,则Ca2+、Mg2+透过离子交换膜Y移向b极,A错误;
B.负极中C6H12O6得到电子发生氧化反应生成二氧化碳,反应式为C6H12O6+6H2O-24e-=6CO2↑+24H+,B正确;
C.由B电极式可知,1molC6H12O6转化为CO2,则会有24mol氯离子迁移到负极区;钙离子、镁离子均带2个单位正电荷,根据电荷守恒可知,迁移到正极区的离子总数为12NA,C正确;
D.该装置为化学能转化为电能的装置,且得到软水,故可用于硬水软化,同时还可产生电能,D正确;
故选A。
7.C
【详解】A.碱性锌锰电池的总反应为:Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2,Zn的化合价升高,失去电子,被氧化,则Zn为负极,Mn元素的化合价降低,得到电子,被还原,MnO2为正极,故A错误;
B.碱性锌锰电池为一次电池,故B错误;
C.Zn为负极,Zn失去电子转化为Zn(OH)2,负极的电极反应式为:Zn+2OH--2e-=Zn(OH)2,故C正确;
D.Zn为负极,MnO2为正极,原电池中电子从负极经导线流向正极,则工作时电子由经外电路流向MnO2,故D错误;
故选C。
8.C
【详解】该燃料电池的总反应为2CH3OH+3O2=4H2O+2CO2①
正极反应为O2+4H++4e-=2H2O②
①-②×3得:2CH3OH+2H2O-12e-=2CO2+12H+,即CH3OH+H2O-6e-=CO2+6H+。故C正确;
故选:C。
9.C
【分析】该电池为燃料电池,燃料为负极,空气为正极。
【详解】A.b为正极,阴离子向负极移动,正确;
B.负极发生氧化反应,正确;
C.通过2×10-3mol电子时,反应的CO为0.001mol,在标准状况下,体积为2.24mL,错误;
D.CO含量高,转移电子多,电流大,正确。
故选C。
10.C
【详解】负极:2H2-4e-+4OH-=4H2O 正极:O2+4e-+2H2O=4OH-。所以产生2 mol水,转移4 mol电子。制得1 L水转移电子数为×2=1.1×102 mol。故C正确;
故选:C。
11.D
【分析】原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。
【详解】A.电极b的电极反应为Zn-2e-=Zn2+,电极a的电极反应为Cu2++2e-=Cu,所以一段时间后,a增加的质量小于b减少的质量,A错误;
B.由于b极上锌失电子为负极,盐桥中阴离子向b极移动,B错误;
C.Fe做负极,C做正极,外电路电子转移方向:a→b,C错误;
D.I-失去电子生成I2,淀粉溶液遇碘变蓝色,则b极附近溶液变蓝,若开始时增大FeCl3溶液浓度,反应速率加快,则b极附近溶液变蓝的速度加快,D正确;
故选D。
12.D
【详解】当A、B组成原电池时,电子流动方向A→B,则金属活泼性为A>B;当A、D组成原电池时,A为正极,则金属活泼性为D>A;B与E构成原电池时,电极反应式为:E2-+2e-→E,B-2e-→B2+,B失去电子,则金属活泼性为B>E,综上所述,金属活泼性为D>A>B>E,故答案为:D。
13.C
【分析】该原电池Zn+Ag2O+H2O= Zn(OH)2+2Ag中,负极反应为Zn+2OH--2e-= Zn(OH)2、正极反应为Ag2O+H2O+2e-=2Ag+2OH-,电子由负极流向正极,以此来解答。
【详解】A.Zn失电子发生氧化反应而作负极,故A正确;
B.正极上Ag2O得电子发生还原反应,故B正确;
C.原电池中电子从负极沿导线流向正极,该原电池中Zn是负极、Ag2O是正极,所以放电时电子从Zn经导线流向Ag2O极,故C错误;
D.正极上Ag2O得电子,正极反应为Ag2O+H2O+2e-=2Ag+2OH-,故D正确;
故选:C。
14.C
【分析】二次电池放电时是原电池,还原剂在负极失去电子发生氧化反应,正极上氧化剂得到电子发生还原反应,内电路中阴离子移向负极、阳离子移向正极,由图知,Li+向右侧区域移动,则电极b为原电池的正极、电极a为负极,据此回答。
【详解】A.由题干中电池反应式、结合图示可知:放电时负极反应为:LixC6-xe-=6C+xLi+,则电池工作时,负极材料质量减少0.7 g,即产生0.1molLi+、转移0.1 mol电子,A正确;
B.由题干中电池反应式、结合图示可知:放电时负极反应为:LixC6-xe-=6C+xLi+,B正确;
C.在原电池中阳离子向正极移动,C错误;
D.据分析,放电时电极b为原电池的正极、电极a为负极,则充电时,电极a为阴极、与电源负极连接,电极b为阳极与电源正极连接,D正确;
故选C。
15.C
【分析】由题意可知,乙醇燃料电池中通入乙醇的一极为负极,碱性条件下,乙醇在负极失去电子发生还原反应生成碳酸根离子和水,电极反应式为C2H5OH+16OH--12e-=2CO+11H2O,通入氧气的一极为正极,氧气在正极上得到电子发生还原反应生成氢氧根离子,电极反应式为O2+4e-+2H2O=4OH-。
【详解】
A.由分析可知,放电时,通入氧气的一极为正极,氧气在正极上得到电子发生还原反应生成氢氧根离子,A错误;
B.由分析可知,通入氧气的一极为正极,氧气在正极上得到电子发生还原反应生成氢氧根离子,正极附近溶液的氢氧根离子浓度增大,溶液碱性增强,B错误;
C.由分析可知,放电时,通入乙醇的一极为负极,碱性条件下,乙醇在负极失去电子发生还原反应生成碳酸根离子和水,电极反应式为C2H5OH+16OH--12e-=2CO+11H2O,C正确;
D.由分析可知,放电时,通入乙醇的一极为负极,碱性条件下,乙醇在负极失去电子发生还原反应生成碳酸根离子和水,电极反应式为C2H5OH+16OH--12e-=2CO+11H2O,由电极反应式可知,消耗0.2 mol乙醇,转移电子的物质的量为2.4mol,D错误;
故选C。
16.(1) Zn-2e-=Zn2+ 2H++2e-=H2↑
(2)由Cu极流向Zn极
(3) 4.875 9.03×1022 0.75 mol·L-1
【分析】由题干图示信息可知,Zn电极是负极,电极反应为:Zn-2e-=Zn2+,Cu电极为正极,电极反应为:2H++2e-=H2↑,据此分析解题:
【详解】(1)由分析可知,原电池的负极反应是Zn-2e-=Zn2+,正极反应是2H++2e-=H2↑,故答案为:Zn-2e-=Zn2+;2H++2e-=H2↑;
(2)由分析可知,Zn比Cu活泼,故Zn电极为负极,Cu电极为正极,电流的方向是由正极经导线流向负极即由Cu极流向Zn极,故答案为:由Cu极流向Zn极;
(3)产生0.075 mol H2,通过0.075×2=0.15 mol电子,消耗0.075 mol Zn和0.075 mol H2SO4.所以m(Zn)=0.075 mol×65 g·mol-1=4.875 g,N(e-)=0.15 mol×6.02×1023 mol-1=9.03×1022,c(H2SO4)==0.75 mol·L-1,故答案为:4.875;9.03×1022;0.75 mol·L-1。
17.(1)6NA
(2)A
(3)
(4)
【详解】(1)CH4中的C由-4价升高到+2价,失去6个电子,则1molCH4参与反应转移6mol电子,电子数目为6NA;
(2)由题目图像可分析出A电极上CO与H2的混合气体反应后生成CO2和H2O,C、H的化合价上升,发生氧化反应,可得A电极为负极,原电池的电解池中阴离子向负极移动,故向A电极移动;
(3)根据图中信息和电解质的成分,可得A电极上CO与H2失4个电子,发生氧化反应生成CO2和H2O,电极反应式为;
(4)B电极上O2得4个电子,发生还原反应,与CO2结合生成,电极反应式为。
18. 减小 右 到C 99 使用时间长、工作电压稳定 具有强氧化性,可以杀菌消毒,且生成的胶体具有吸附性,可以吸附水中的杂质
【详解】(1)由电池总反应可知,发生还原反应,是电池正极反应物,故正极反应是;为负极,负极反应是,反应消耗,故放电时负极附近溶液的减小;原电池中,阴离子移向负极,则盐桥中的向右移动;电子经外电路由负极流向正极,即由到C。放电时,铁元素化合价由降为,故消耗的质量;故答案为:;减小;右;到C;99;
(2)比较题图中的两条曲线可知,高铁电池的放电时间长,且放电时的电压稳定;故答案为:使用时间长、工作电压稳定
(3)中的化合价为,价态高,氧化性强,有杀菌消毒效果,且生成的胶体比表面积大,具有较强的吸附能力,能吸附水中的杂质,故答案为:具有强氧化性,可以杀菌消毒,且生成的胶体具有吸附性,可以吸附水中的杂质。
19. 铁 NO3-+8e-+10H+=NH4++3H2O FeO(OH)不导电,阻碍电子转移 本实验条件下,Fe2+不能直接还原NO3-;在Fe和Fe2+共同作用下能提高NO3-的去除率。 Fe2++2FeO(OH)=Fe3O4+2H+, Fe2+将不导电的FeO(OH)转化为可导电的Fe3O4,利于电子的转移。 初始pH低时,产生的Fe2+充足;初始pH高时,产生的Fe2+不足。
【详解】(1)①由图中物质变化分析,Fe变化为Fe3O4是被氧化过程,则铁作原电池的负极;②由硝酸根到铵根可知,硝酸根被还原为氨气,氨气在酸性环境中生成铵根,正极的电极反应式为:NO3-+8e-+10H+=NH4++3H2O;
(2)从pH对硝酸根去除率的影响来看,初始pH=4.5时去除率低,主要是因为铁离子容易水解生成FeO(OH),同时生成的Fe3O4产率降低,且生成的FeO(OH)不导电,所以NO3-的去除率低;
(3)①从图中可以看出只加入铁粉和只加入Fe2+,NO3-的去除率都不如同时加入铁和亚铁离子的去除率高,说明不是由于亚铁离子的还原性提高了硝酸根的去除率,而是由于Fe2+破坏FeO(OH)生成了四氧化三铁;②同位素示踪法证实亚铁离子秘FeO(OH)反应生成四氧化铁,该反应离子方程式为:Fe2++2FeO(OH)=Fe3O4+2H+,加入亚铁离子之所以可以提高硝酸根离子的转化率主要因为减少了FeO(OH)的生成,生成更多的四氧化三铁,增强了导电性,另外pH较小,可以使pH增大的速度减慢,使硝酸根离子转化率增大;
(4)铁与盐酸反应,初始pH较小,氢离子浓度高,产生的亚铁离子浓度大,促使FeO(OH)转化为可导电的四氧化三铁,使反应进行的更完全;初始pH较大时,由于三价铁的水解,三价铁越容易生成FeO(OH),产生的亚铁离子浓度高小,从而造成硝酸根离子去除率和的铁的最终物质。
答案第1页,共2页
答案第1页,共2页
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.锂空气电池因其比能量非常高,具有广阔应用前景。下图是一种锂空气电池的工作示意图,下列分析正确的是
A.放电时,a电极的反应式为
B.有机电解液可换成水溶液
C.转移4mol电子,b电极消耗22.4L的氧气
D.放电时,电流从a电极经外电路流回b电极
2.我国科研工作者发明了一种高性能的水系锰基锌电池[],电池工作示意图如图,该电池工作一段时间后,的浓度增大。下列说法正确的是
A.电极X的材料为Zn
B.膜a、b分别为阳、阴离于交换膜
C.正极反应式为
D.当的物质的量增大0.1mol时,电路中转移0.4mol电子
3.下列原电池装置图示中电子或离子流向、正极或负极等标注不正确的是
A B C D
铅蓄电池 锌银纽扣电池 燃料电池 锌铜原电池
A.A B.B C.C D.D
4.科学家近年来研制出一种新型细菌燃料电池,利用细菌将有机酸转化为氢气,氢气进入以磷酸为电解质的燃料电池中发电,电池负极反应式为
A.H2+2OH--2e-=2H2O B.O2+4H++4e-=2H2O
C.H2-2e-=2H+ D.O2+2H2O+4e-=4OH-
5.下列电池不属于二次电池的是
A B C D
手机用锂电池 电动汽车用电池 铅酸蓄电池 锌锰干电池
A.A B.B C.C D.D
6.一种酸性生物燃料电池应用的原理如图所示,下列说法错误的是
A.Ca2+、Mg2+透过离子交换膜X移向a极
B.负极反应式为C6H12O6+6H2O-24e-=6CO2↑+24H+
C.1molC6H12O6转化为CO2,迁移到正极区的离子总数为12NA
D.该装置可用于硬水软化,同时还可产生电能
7.碱性锌锰电池的总反应为:Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2。下列说法正确的是
A.Zn为正极,MnO2为负极
B.该电池为二次电池
C.负极的电极反应式为:Zn+2OH--2e-=Zn(OH)2
D.工作时电子由MnO2经外电路流向
8.一种燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧作用生成水和二氧化碳。该电池负极发生的反应是
A.
B.
C.
D.
9.某汽车尾气分析仪以燃料电池为工作原理测定CO的浓度,其装置如图所示,该电池中电解质为氧化钇—氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法不正确的是
A.工作时电极b作正极,O2-由电极b流向电极a
B.负极的电极反应式为:
C.当传感器中通过2×10-3mol电子时,通过的尾气中含有2.24mLCO
D.传感器中通过的电流越大,尾气中CO的含量越高
10.美国《时代周刊》将氢燃料电池评为21世纪对人类生活具有重大影响的技术之一、培根电池是一种碱性的氢氧燃料电池,已经应用在“阿波罗六号”太空船上。将多个培根电池组合为电池组,向外供电,电池组工作稳定后,它的电动势和内阻基本保持不变。电池所产生的水可以作为饮用水,今欲得常温下水1L,则电池内电子转移的物质的量约为
A.8.9×10-3 mol B.4.5×10-2 mol
C.1.1×102 mol D.5.6×10 mol
11.用选项中的电极、溶液和如图所示装置可组成原电池。下列现象或结论的叙述正确的是
选项 电极a 电极b A溶液 B溶液 现象或结论
A Cu Zn CuSO4 ZnSO4 一段时间后,a增加的质量与b减少的质量相等
B Cu Zn 稀H2SO4 ZnSO4 盐桥中阳离子向b极移动
C Fe C NaCl FeCl3 外电路电子转移方向:b→a
D C C FeCl3 KI、淀粉混合液 若开始时只增大FeCl3溶液浓度,b极附近溶液变蓝的速度加快
A.A B.B C.C D.D
12.有A、B、D、E四种金属,当A、B组成原电池时,电子流动方向A→B;当A、D组成原电池时,A为正极;B与E构成原电池时,电极反应式为:E2++2e-=E,B-2e-=B2+则A、B、D、E金属性由强到弱的顺序为
A.A﹥B﹥E﹥D B.A﹥B﹥D﹥E
C.D﹥E﹥A﹥B D.D﹥A﹥B﹥E
13.银锌纽扣电池的电池反应式为:Zn+Ag2O+H2O=Zn(OH)2+2Ag。下列说法不正确的是
A.锌作负极,失去电子
B.正极为Ag2O,发生还原反应
C.电池工作时,电子从Ag2O经导线流向Zn
D.正极的电极方程式为:Ag2O+2e-+H2O=2Ag+2OH-
14.新能源汽车是国家战略产业的重要组成部分,LiFePO4电池是能源汽车关键部件之一,电池工作时的总反应为LiFePO4+6CLi1-xFePO4+LixC6。充放电时,Li+在正极材料上脱嵌或嵌入,随之在石墨中发生了LixC6的生成与解离。放电工作原理如图所示,下列说法错误的是
A.电池工作时,负极材料质量减少0.7 g,转移0.1 mol电子
B.放电时负极反应为LixC6-xe-=6C+xLi+
C.放电时,Li+通过隔膜移向负极,电子由电极a沿导线流向电极b
D.充电时,电极a与电源负极连接,电极b与电源正极连接
15.某燃料电池以乙醇为燃料,空气为氧化剂,强碱溶液为电解质组成,有关该电池的说法正确的是
A.放电时正极发生氧化反应
B.放电一段时间后,正极附近溶液的pH减小
C.放电时负极电极反应为:
D.消耗0.2mol乙醇,有1.2mol转移
二、填空题
16.由锌片、铜片和200mL稀硫酸组成的原电池如下图所示。
(1)原电池的负极反应是_______,正极反应是_______。
(2)电流的方向是_______。
(3)一段时间后,当在铜片上放出1.68 L(标准状况)气体时,H2SO4恰好消耗一半。则产生这些气体的同时,共消耗_______g锌,有_______个电子通过了导线,原硫酸的物质的量浓度是_______(设溶液体积不变)。
17.一种熔融碳酸盐燃料电池的原理示意图如下。
请回答下列有关该电池的问题:
(1)反应,每消耗1mol 理论上转移的电子数目为_______。
(2)电池工作时,向电极_______(填“A”或“B”)移动。
(3)电极A上参与的电极反应为_______。
(4)电极B上发生的电极反应为_______。
三、实验题
18.高铁酸钾不仅是一种理想的水处理剂,还用于研制高铁电池。如图所示是高铁电池的模拟实验装置,该电池的总反应为。
回答下列问题:
(1)该电池放电时正极的电极反应式为___________________。放电过程中负极附近溶液的______(填“增大”“减小”或“不变”)。盐桥中盛有饱和溶液,此盐桥中的向_____(填“左”或“右”)移动;电子移动方向由______(填“C到“”或“到“C”)。当消耗质量为______g的时,放电过程中转移电子数为。
(2)图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有__________________。
(3)高铁酸钾是一种理想的水处理剂的原因是___________________________。
19.用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如图所示。
①作负极的物质是________。
②正极的电极反应式是_________。
(2)将足量铁粉投入水体中,经24小时测定NO3—的去除率和pH,结果如下:
初始pH pH=2.5 pH=4.5
NO3—的去除率 接近100% <50%
24小时pH 接近中性 接近中性
铁的最终物质形态
pH=4.5时,NO3-的去除率低。其原因是________。
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3-的去除率。对Fe2+的作用提出两种假设:
Ⅰ. Fe2+直接还原NO3-;
Ⅱ. Fe2+破坏FeO(OH)氧化层。
①做对比实验,结果如右图所示,可得到的结论是_______。
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4。结合该反应的离子方程式,解释加入Fe2+提高NO3-去除率的原因:______。
pH =4.5(其他条件相同)
(4)其他条件与(2)相同,经1小时测定NO3-的去除率和pH,结果如下:
初始pH pH=2.5 pH=4.5
NO3—的去除率 约10% 约3%
1小时pH 接近中性 接近中性
与(2)中数据对比,解释(2)中初始pH不同时,NO3—去除率和铁的最终物质形态不同的原因:__________。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.A
【分析】结合图示装置,Li失去电子为负极,则a为负极,b为正极,据此判断。
【详解】A.放电时,图中负极为Li,根据电解液传导离子为锂离子,故电极反应为:Li-e-=Li+,A正确;
B.Li和水反应,不能把有机电解液换成水溶液,B错误;
C.气体未说明存在状态,无法计算,C错误;
D.a为负极,b为正极,放电时,电流从b电极经外电路流回a电极,D错误;
故选A。
2.C
【详解】A.由图中电子流动方向可知电极Y为负极,材料为Zn,电极X为正极,材料为,故A错误;
B.一段时间后,的浓度增大说明程a、b分别为阴、阳离子交换膜,故B错误;
C.根据总反应,锰化合价降低,则正极反应式为,故C正确;
D.的物质的量增大0.1m时,电路中转移0.2ml电子,故D错误。
综上所述,答案为C。
3.C
【详解】A.铅蓄电池中二氧化铅作正极,铅作负极,标注正确,故A不符合题意;
B.锌银纽扣电池中锌作负极,氧化银作正极,标注正确,故B不符合题意;
C.氢氧燃料电池中氢气作负极,是电子流出极,溶液中氢离子通过质子交换膜从左向右移动,标注错误,故C符合题意;
D.锌铜原电池中锌作负极,铜作正极,钾离子向正极即向左移动,标注正确,故D不符合题意;
故答案选C。
4.C
【详解】根据题给信息,该燃料电池的总反应为2H2+O2=2H2O。
A.电解液为酸性溶液,电极反应式中不能出现OH-,选项A错误;
B.因为燃料电池中负极通入氢气,正极通入氧气,选项B错误;
C.燃料电池中负极通入氢气,氢气失电子产生H+,电极反应式为H2-2e-=2H+,选项C正确;
D.电解液为酸性溶液,电极反应式中不能出现OH-,选项D错误;
答案选C。
5.D
【详解】A.手机用锂电池,可充电,属于二次电池,故A不选;
B.电动汽车用电池,可充电,属于二次电池,故B不选;
C.铅酸蓄电池,可充电,属于二次电池,故C不选;
D.锌锰干电池不可充电,属于一次电池,故D选;
故选D。
6.A
【分析】根据电子流向可知,a为负极、b为正极;
【详解】A.原电池中阳离子向正极移动,则Ca2+、Mg2+透过离子交换膜Y移向b极,A错误;
B.负极中C6H12O6得到电子发生氧化反应生成二氧化碳,反应式为C6H12O6+6H2O-24e-=6CO2↑+24H+,B正确;
C.由B电极式可知,1molC6H12O6转化为CO2,则会有24mol氯离子迁移到负极区;钙离子、镁离子均带2个单位正电荷,根据电荷守恒可知,迁移到正极区的离子总数为12NA,C正确;
D.该装置为化学能转化为电能的装置,且得到软水,故可用于硬水软化,同时还可产生电能,D正确;
故选A。
7.C
【详解】A.碱性锌锰电池的总反应为:Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2,Zn的化合价升高,失去电子,被氧化,则Zn为负极,Mn元素的化合价降低,得到电子,被还原,MnO2为正极,故A错误;
B.碱性锌锰电池为一次电池,故B错误;
C.Zn为负极,Zn失去电子转化为Zn(OH)2,负极的电极反应式为:Zn+2OH--2e-=Zn(OH)2,故C正确;
D.Zn为负极,MnO2为正极,原电池中电子从负极经导线流向正极,则工作时电子由经外电路流向MnO2,故D错误;
故选C。
8.C
【详解】该燃料电池的总反应为2CH3OH+3O2=4H2O+2CO2①
正极反应为O2+4H++4e-=2H2O②
①-②×3得:2CH3OH+2H2O-12e-=2CO2+12H+,即CH3OH+H2O-6e-=CO2+6H+。故C正确;
故选:C。
9.C
【分析】该电池为燃料电池,燃料为负极,空气为正极。
【详解】A.b为正极,阴离子向负极移动,正确;
B.负极发生氧化反应,正确;
C.通过2×10-3mol电子时,反应的CO为0.001mol,在标准状况下,体积为2.24mL,错误;
D.CO含量高,转移电子多,电流大,正确。
故选C。
10.C
【详解】负极:2H2-4e-+4OH-=4H2O 正极:O2+4e-+2H2O=4OH-。所以产生2 mol水,转移4 mol电子。制得1 L水转移电子数为×2=1.1×102 mol。故C正确;
故选:C。
11.D
【分析】原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。
【详解】A.电极b的电极反应为Zn-2e-=Zn2+,电极a的电极反应为Cu2++2e-=Cu,所以一段时间后,a增加的质量小于b减少的质量,A错误;
B.由于b极上锌失电子为负极,盐桥中阴离子向b极移动,B错误;
C.Fe做负极,C做正极,外电路电子转移方向:a→b,C错误;
D.I-失去电子生成I2,淀粉溶液遇碘变蓝色,则b极附近溶液变蓝,若开始时增大FeCl3溶液浓度,反应速率加快,则b极附近溶液变蓝的速度加快,D正确;
故选D。
12.D
【详解】当A、B组成原电池时,电子流动方向A→B,则金属活泼性为A>B;当A、D组成原电池时,A为正极,则金属活泼性为D>A;B与E构成原电池时,电极反应式为:E2-+2e-→E,B-2e-→B2+,B失去电子,则金属活泼性为B>E,综上所述,金属活泼性为D>A>B>E,故答案为:D。
13.C
【分析】该原电池Zn+Ag2O+H2O= Zn(OH)2+2Ag中,负极反应为Zn+2OH--2e-= Zn(OH)2、正极反应为Ag2O+H2O+2e-=2Ag+2OH-,电子由负极流向正极,以此来解答。
【详解】A.Zn失电子发生氧化反应而作负极,故A正确;
B.正极上Ag2O得电子发生还原反应,故B正确;
C.原电池中电子从负极沿导线流向正极,该原电池中Zn是负极、Ag2O是正极,所以放电时电子从Zn经导线流向Ag2O极,故C错误;
D.正极上Ag2O得电子,正极反应为Ag2O+H2O+2e-=2Ag+2OH-,故D正确;
故选:C。
14.C
【分析】二次电池放电时是原电池,还原剂在负极失去电子发生氧化反应,正极上氧化剂得到电子发生还原反应,内电路中阴离子移向负极、阳离子移向正极,由图知,Li+向右侧区域移动,则电极b为原电池的正极、电极a为负极,据此回答。
【详解】A.由题干中电池反应式、结合图示可知:放电时负极反应为:LixC6-xe-=6C+xLi+,则电池工作时,负极材料质量减少0.7 g,即产生0.1molLi+、转移0.1 mol电子,A正确;
B.由题干中电池反应式、结合图示可知:放电时负极反应为:LixC6-xe-=6C+xLi+,B正确;
C.在原电池中阳离子向正极移动,C错误;
D.据分析,放电时电极b为原电池的正极、电极a为负极,则充电时,电极a为阴极、与电源负极连接,电极b为阳极与电源正极连接,D正确;
故选C。
15.C
【分析】由题意可知,乙醇燃料电池中通入乙醇的一极为负极,碱性条件下,乙醇在负极失去电子发生还原反应生成碳酸根离子和水,电极反应式为C2H5OH+16OH--12e-=2CO+11H2O,通入氧气的一极为正极,氧气在正极上得到电子发生还原反应生成氢氧根离子,电极反应式为O2+4e-+2H2O=4OH-。
【详解】
A.由分析可知,放电时,通入氧气的一极为正极,氧气在正极上得到电子发生还原反应生成氢氧根离子,A错误;
B.由分析可知,通入氧气的一极为正极,氧气在正极上得到电子发生还原反应生成氢氧根离子,正极附近溶液的氢氧根离子浓度增大,溶液碱性增强,B错误;
C.由分析可知,放电时,通入乙醇的一极为负极,碱性条件下,乙醇在负极失去电子发生还原反应生成碳酸根离子和水,电极反应式为C2H5OH+16OH--12e-=2CO+11H2O,C正确;
D.由分析可知,放电时,通入乙醇的一极为负极,碱性条件下,乙醇在负极失去电子发生还原反应生成碳酸根离子和水,电极反应式为C2H5OH+16OH--12e-=2CO+11H2O,由电极反应式可知,消耗0.2 mol乙醇,转移电子的物质的量为2.4mol,D错误;
故选C。
16.(1) Zn-2e-=Zn2+ 2H++2e-=H2↑
(2)由Cu极流向Zn极
(3) 4.875 9.03×1022 0.75 mol·L-1
【分析】由题干图示信息可知,Zn电极是负极,电极反应为:Zn-2e-=Zn2+,Cu电极为正极,电极反应为:2H++2e-=H2↑,据此分析解题:
【详解】(1)由分析可知,原电池的负极反应是Zn-2e-=Zn2+,正极反应是2H++2e-=H2↑,故答案为:Zn-2e-=Zn2+;2H++2e-=H2↑;
(2)由分析可知,Zn比Cu活泼,故Zn电极为负极,Cu电极为正极,电流的方向是由正极经导线流向负极即由Cu极流向Zn极,故答案为:由Cu极流向Zn极;
(3)产生0.075 mol H2,通过0.075×2=0.15 mol电子,消耗0.075 mol Zn和0.075 mol H2SO4.所以m(Zn)=0.075 mol×65 g·mol-1=4.875 g,N(e-)=0.15 mol×6.02×1023 mol-1=9.03×1022,c(H2SO4)==0.75 mol·L-1,故答案为:4.875;9.03×1022;0.75 mol·L-1。
17.(1)6NA
(2)A
(3)
(4)
【详解】(1)CH4中的C由-4价升高到+2价,失去6个电子,则1molCH4参与反应转移6mol电子,电子数目为6NA;
(2)由题目图像可分析出A电极上CO与H2的混合气体反应后生成CO2和H2O,C、H的化合价上升,发生氧化反应,可得A电极为负极,原电池的电解池中阴离子向负极移动,故向A电极移动;
(3)根据图中信息和电解质的成分,可得A电极上CO与H2失4个电子,发生氧化反应生成CO2和H2O,电极反应式为;
(4)B电极上O2得4个电子,发生还原反应,与CO2结合生成,电极反应式为。
18. 减小 右 到C 99 使用时间长、工作电压稳定 具有强氧化性,可以杀菌消毒,且生成的胶体具有吸附性,可以吸附水中的杂质
【详解】(1)由电池总反应可知,发生还原反应,是电池正极反应物,故正极反应是;为负极,负极反应是,反应消耗,故放电时负极附近溶液的减小;原电池中,阴离子移向负极,则盐桥中的向右移动;电子经外电路由负极流向正极,即由到C。放电时,铁元素化合价由降为,故消耗的质量;故答案为:;减小;右;到C;99;
(2)比较题图中的两条曲线可知,高铁电池的放电时间长,且放电时的电压稳定;故答案为:使用时间长、工作电压稳定
(3)中的化合价为,价态高,氧化性强,有杀菌消毒效果,且生成的胶体比表面积大,具有较强的吸附能力,能吸附水中的杂质,故答案为:具有强氧化性,可以杀菌消毒,且生成的胶体具有吸附性,可以吸附水中的杂质。
19. 铁 NO3-+8e-+10H+=NH4++3H2O FeO(OH)不导电,阻碍电子转移 本实验条件下,Fe2+不能直接还原NO3-;在Fe和Fe2+共同作用下能提高NO3-的去除率。 Fe2++2FeO(OH)=Fe3O4+2H+, Fe2+将不导电的FeO(OH)转化为可导电的Fe3O4,利于电子的转移。 初始pH低时,产生的Fe2+充足;初始pH高时,产生的Fe2+不足。
【详解】(1)①由图中物质变化分析,Fe变化为Fe3O4是被氧化过程,则铁作原电池的负极;②由硝酸根到铵根可知,硝酸根被还原为氨气,氨气在酸性环境中生成铵根,正极的电极反应式为:NO3-+8e-+10H+=NH4++3H2O;
(2)从pH对硝酸根去除率的影响来看,初始pH=4.5时去除率低,主要是因为铁离子容易水解生成FeO(OH),同时生成的Fe3O4产率降低,且生成的FeO(OH)不导电,所以NO3-的去除率低;
(3)①从图中可以看出只加入铁粉和只加入Fe2+,NO3-的去除率都不如同时加入铁和亚铁离子的去除率高,说明不是由于亚铁离子的还原性提高了硝酸根的去除率,而是由于Fe2+破坏FeO(OH)生成了四氧化三铁;②同位素示踪法证实亚铁离子秘FeO(OH)反应生成四氧化铁,该反应离子方程式为:Fe2++2FeO(OH)=Fe3O4+2H+,加入亚铁离子之所以可以提高硝酸根离子的转化率主要因为减少了FeO(OH)的生成,生成更多的四氧化三铁,增强了导电性,另外pH较小,可以使pH增大的速度减慢,使硝酸根离子转化率增大;
(4)铁与盐酸反应,初始pH较小,氢离子浓度高,产生的亚铁离子浓度大,促使FeO(OH)转化为可导电的四氧化三铁,使反应进行的更完全;初始pH较大时,由于三价铁的水解,三价铁越容易生成FeO(OH),产生的亚铁离子浓度高小,从而造成硝酸根离子去除率和的铁的最终物质。
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第1章 化学反应与能量转化
- 第1节 化学反应的热效应
- 第2节 化学能转化为电能——电池
- 第3节 电能转化为化学能——电解
- 第4节 金属的腐蚀与防护
- 微项目 设计载人航天器用化学电池与氧气再生方案——化学反应中能量及物质的转化利用
- 第2章 化学反应的方向、 限度与速率
- 第1节 化学反应的方向
- 第2节 化学反应的限度
- 第3节 化学反应的速率
- 第4节 化学反应条件的优化——工业合成氨
- 微项目 探讨如何利用工业废气中的二氧化碳合成甲醇——化学反应选择与反应条件优化
- 第3章 物质在水溶液中的行为
- 第1节 水与水溶液
- 第2节 弱电解质的电离 盐类的水解
- 第3节 沉淀溶解平衡
- 第4节 离子反应
- 微项目 揭秘索尔维制碱法和侯氏制碱法——化学平衡思想的创造性应用
