第2章官能团与有机化学反应烃的衍生物单元练习(含解析)高二下学期化学鲁科版(2019)选择性必修3
文档属性
| 名称 | 第2章官能团与有机化学反应烃的衍生物单元练习(含解析)高二下学期化学鲁科版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-05 00:00:00 | ||
图片预览



文档简介
第2章《官能团与有机化学反应 烃的衍生物》
一、选择题
1.下列关于有机物的说法错误的是
A.生活中常用的硬肥皂是由高级脂肪酸钾盐制成的肥皂
B.乙酸乙酯在稀硫酸中水解的产物都能与钠反应
C.葡萄糖和麦芽糖都能发生银镜反应
D.天然油脂不是高分子化合物,没有恒定的熔点、沸点
2.下列有关蛋白质的叙述中不正确的是
A.蛋白质溶液中加入饱和硫酸铵溶液, 有蛋白质析出, 如再加水也不溶解
B.蛋白质溶液中的蛋白质分子能透过滤纸, 但不能透过半透膜
C.重金属盐能使蛋白质变性, 但吞服“钡餐”(BaSO4)不会引起中毒
D.浓硝酸溅在皮肤上, 能使皮肤呈黄色是因为蛋白质和浓硝酸发生颜色反应
3.将淀粉浆和淀粉酶(含苯环)的混合物放入半透膜(允许葡萄糖分子通过)袋中,扎好后浸入流动的温水中,经过足够长的时间后,取出袋内的液体,分别与①碘水、②新制Cu(OH)2(加热)、③浓硝酸(微热)作用,其现象依次是
A.显蓝色;无砖红色沉淀;显黄色
B.不显蓝色;无砖红色沉淀;显黄色
C.显蓝色;有砖红色沉淀;不显黄色
D.不显蓝色;有砖红色沉淀;不显黄色
4.化学与生活密切相关。下列叙述错误的是
A.纯碱溶液可以用于清洗餐具油污
B.玉米淀粉和废弃秸秆可生产乙醇
C.珠江三角洲的形成与胶体聚沉有关
D.“84消毒液”可以喷洒于衣物上进行杀菌消毒
5.从科技前沿到日常生活,化学无处不在。下列说法错误的是
A.在三星堆“祭祀坑”提取到丝绸制品残留物,其中丝绸主要成分为蛋白质
B.2022年北京冬奥会吉祥物“冰墩墩”使用的聚乙烯属于高分子材料
C.“天和”核心舱中使用的氮化硼陶瓷基复合材料属于高分子材料
D.“空气捕捉”法能实现从空气中捕获二氧化碳,利于碳达峰、碳中和
6.2022年北京冬奥会成功举办,展现了我国化学科学的迅猛发展,下列说法错误的是
A.开幕式专用演出服采用石墨烯智能发热材料,石墨烯属于新型无机非金属材料
B.速滑竞赛服使用了蜂窝样式的聚氨酯材料,属于天然有机高分子材料
C.滑雪板板心木质材料的主要成分为纤维素,属于天然有机高分子化合物
D.首钢单板滑雪大跳台的主体结构采用高强钢和耐火耐候钢,属于合金材料
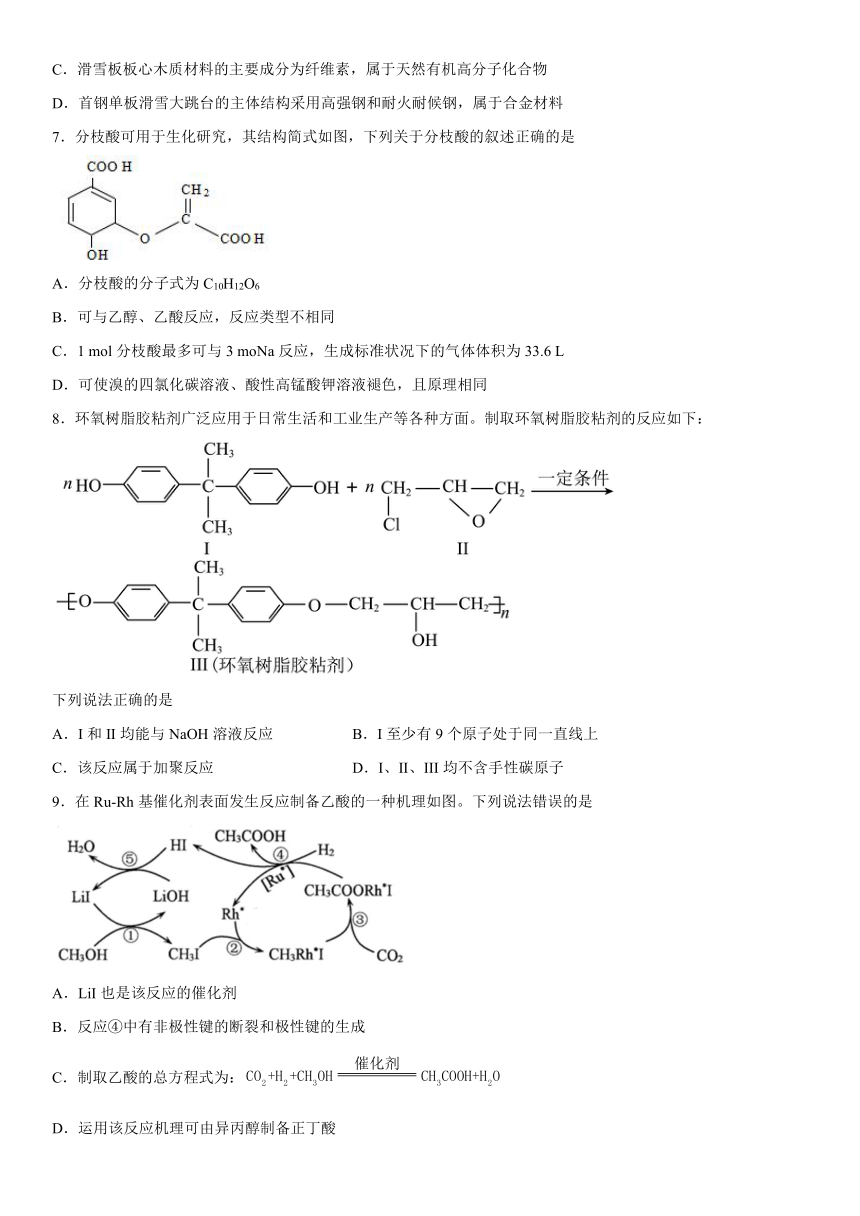
7.分枝酸可用于生化研究,其结构简式如图,下列关于分枝酸的叙述正确的是
A.分枝酸的分子式为C10H12O6
B.可与乙醇、乙酸反应,反应类型不相同
C.1 mol分枝酸最多可与3 moNa反应,生成标准状况下的气体体积为33.6 L
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
8.环氧树脂胶粘剂广泛应用于日常生活和工业生产等各种方面。制取环氧树脂胶粘剂的反应如下:
下列说法正确的是
A.I和II均能与NaOH溶液反应 B.I至少有9个原子处于同一直线上
C.该反应属于加聚反应 D.I、II、III均不含手性碳原子
9.在Ru-Rh基催化剂表面发生反应制备乙酸的一种机理如图。下列说法错误的是
A.LiI也是该反应的催化剂
B.反应④中有非极性键的断裂和极性键的生成
C.制取乙酸的总方程式为:
D.运用该反应机理可由异丙醇制备正丁酸
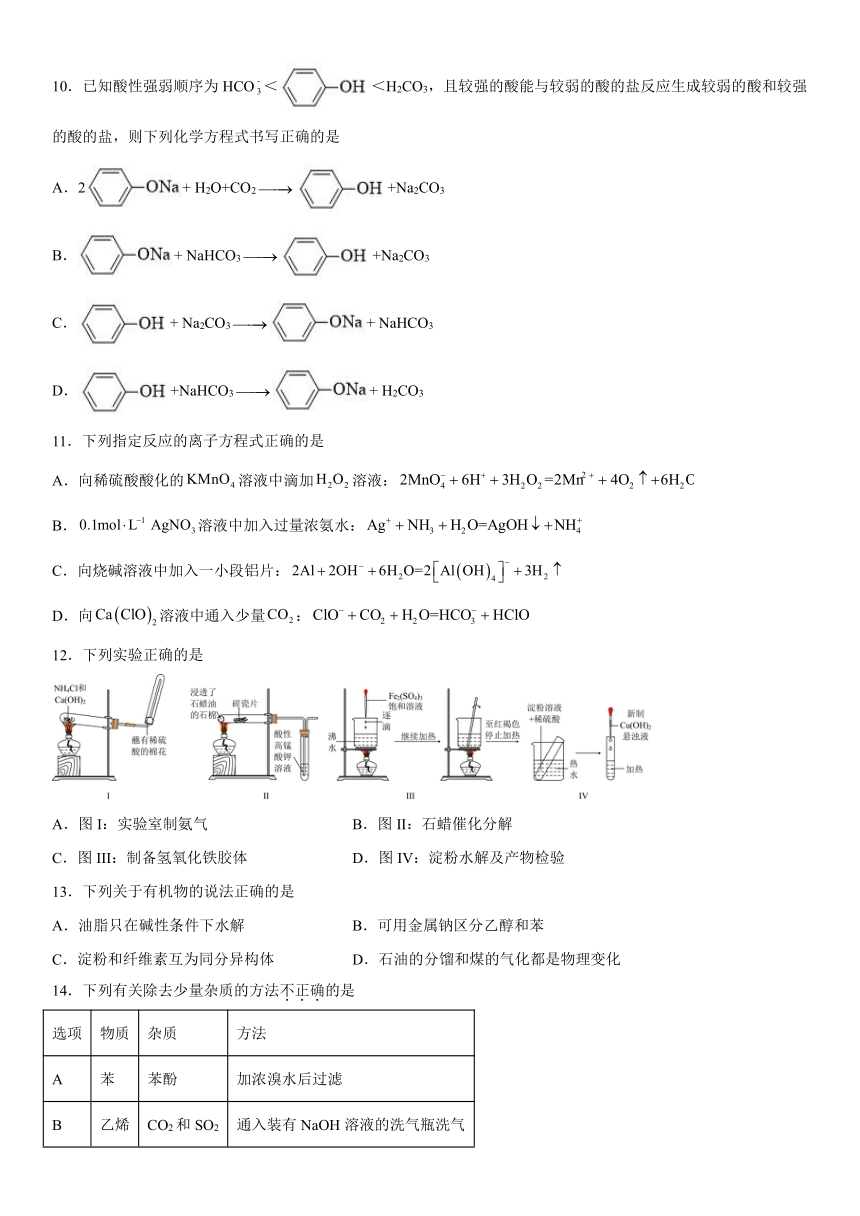
10.已知酸性强弱顺序为HCO<<H2CO3,且较强的酸能与较弱的酸的盐反应生成较弱的酸和较强的酸的盐,则下列化学方程式书写正确的是
A.2+ H2O+CO2+Na2CO3
B.+ NaHCO3+Na2CO3
C.+ Na2CO3+ NaHCO3
D.+NaHCO3+ H2CO3
11.下列指定反应的离子方程式正确的是
A.向稀硫酸酸化的溶液中滴加溶液:
B.溶液中加入过量浓氨水:
C.向烧碱溶液中加入一小段铝片:
D.向溶液中通入少量:
12.下列实验正确的是
A.图I:实验室制氨气 B.图II:石蜡催化分解
C.图III:制备氢氧化铁胶体 D.图IV:淀粉水解及产物检验
13.下列关于有机物的说法正确的是
A.油脂只在碱性条件下水解 B.可用金属钠区分乙醇和苯
C.淀粉和纤维素互为同分异构体 D.石油的分馏和煤的气化都是物理变化
14.下列有关除去少量杂质的方法不正确的是
选项 物质 杂质 方法
A 苯 苯酚 加浓溴水后过滤
B 乙烯 CO2和SO2 通入装有NaOH溶液的洗气瓶洗气
C 溴苯 Br2 加NaOH溶液后分液
D 乙烷 乙烯 通入装有溴水的洗气瓶洗气
A.A B.B C.C D.D
二、填空题
15.羧酸的物理性质
(1)溶解性
甲酸、乙酸等分子中碳原子数较少的羧酸能够与水____,随着分子中碳原子数的增加,一元羧酸在水中的溶解度迅速____,甚至不溶于水。高级脂肪酸是_____水的蜡状固体。
(2)熔、沸点
羧酸的熔、沸点随碳原子数的增多而____,且与相对分子质量相当的其他有机化合物相比,沸点____,这与羧酸分子间可以形成____有关。
16.按题给要求填空
(1)写出以乙炔为原料制备聚氯乙烯反应方程式(无机物不限)
①_______ ;
②_______。
(2)用CH3CH2Br制取CH2OHCH2OH的三步反应方程式:
① _______;
②_______;
③ _______。
(3)写出用CH2OHCH2OH为原料制取的三步反应方程式:
①_______;
②_______;
③ _______。
17.实验室用如图所示装置制取乙烯。
(1)乙醇和浓硫酸的体积比为___________。
(2)①装置在170oC时主要反应的化学方程是___________;
②升温经过140oC左右时,发生副反应,主要生成物的结构简为___________;
(3)实验后期制得的乙烯气体中常含有两种杂质气体,将此混合气体直接通入溴水中能否证明乙烯发生加成反应的性质?___________(填“能”或“否”)仪器B中盛装的试剂应是___________。
18.水杨酸是合成阿司匹林的重要原料。水杨酸的学名邻羟基苯甲酸,结构简式为,,请回答下列问题:
(1)请写出水杨酸中具有的官能团名称_____________________;
(2)请写出与水杨酸互为同分异构体,既属于酚类又属于醛类化合物的结构简式(写一种即可):____________________________________;
(3)水杨酸的另一种同分异构体的结构简式为,1mol该有机物在适宜条件下与氢氧化钠经过一系列反应,最多能消耗氢氧化钠的物质的量为(填序号)______;
A.1mol B.2mol C.3mol D.4mol
(4)已知有机物CH3COOH可以表示为:,在一定条件下,水杨酸与乙酸酐可合成阿司匹林,阿司匹林可表示为:,则阿司匹林的分子式为__________;
(5)阿司匹林药片需要保存在干燥处,受潮的药片易变质不宜服用;检验受潮药片是否变质的试剂是(只选一种试剂即可)______________________。
19.现有7瓶失去了标签的液体,它们可能是①乙醇②乙酸③苯④乙酸乙酯⑤油脂⑥葡萄糖溶液⑦蔗糖溶液。现通过如下实验步骤来确定各试剂瓶中所装的液体名称:
实验步骤和方法 实验现象
①把7瓶液体依次标号A、B、C、D、E、F、G后闻气味 只有F、G两种液体没有气味
②分别取少量7种液体于试管中加水稀释 只有C、D、E三种液体不溶解而浮在水上层
③分别取少量7种液体于试管中,加入新制的Cu(OH)2并加热 只有B使沉淀溶解,F中产生砖红色沉淀
④各取少量C、D、E于试管中,加稀NaOH溶液并加热 只有C仍有分层现象,且在D的试管中闻到特殊香味
(1)试给它们的试剂瓶重新贴上标签(填物质序号):A___,B___,C___,D___,E___,F__,G___。
(2)写出在乙酸苯酚酯中加入NaOH溶液并加热的化学方程式:___。
(3)写出苯酚钠中通入少量的二氧化碳的化学方程式:___。
(4)写乙二醇和乙二酸脱水生成六元环酯的化学方程式:__。
20.回答下列问题:
(1)戊烷有三种同分异构体,其沸点如下:
正戊烷 异戊烷 新戊烷
沸点 36.1℃ 27.9℃ 9.5℃
请说明其沸点差异的原因___________。
(2)甘氨酸()在水中的溶解度与溶液的pH有关,当pH约为6时主要以内盐()的形态存在,其溶解度最小。请解析随着溶液pH的增大或减少,其溶解度变大的原因___________。
21.回答下列问题:
(1)常温常压下苯酚为无色晶体,而苯酚在水中以液态形式存在,原因是___________。
(2)和比较,热稳定性较好的是___________,理由是___________。
三、有机推断题
22.烃A是一种基础化工原料,标准状况下密度为1.25g L-1,B与G互为同系物。H是有芳香味的油状液体。有关物质转化关系如下图:
请回答下列问题:
(1)化合物A名称为____,化合物B的官能团为____,化合物G的结构简式为____。
(2)A→B→C反应的反应类型依次是____、____。
(3)化合物E分子式为C3H4O2,能与碳酸钠溶液反应放出CO2,E→X的化学方程式是____。
(4)下列说法正确的是____。
A.D+G→H过程,浓硫酸作催化剂和吸水剂
B.H在碱性条件下水解是皂化反应
C.用碳酸钠溶液可以鉴别D、G和H
D.相同物质的量的B、C、D完全燃烧消耗的氧气量依次减少
(5)写出C5H10O2的两种同分异构体的结构简式,分别属于羧酸和酯类:____,___。
23.石油分馏得到的轻汽油可在Pt催化下脱氢环化,逐步转化为芳香烃。以链烃A为原料合成两种高分子材料的路线如下:
已知以下信息:
①B的核磁共振氢谱中只有一组峰;G 为一氯代烃。
②R-x+R'-xR-R'(x为卤素原子,R、R'为烃基)
回答以下问题:
(1)H的化学名称为________,C 的官能团名称为________。
(2)J的结构简式为________,G生成H的反应类型为________ 。
(3)F合成丁苯橡胶的化学方程式为_________。
(4)I的同分异构体中能同时满足下列条件的共有________种(不含立体异构)。
①能与饱和NaHCO3溶液反应产生气体;
②既能发生银镜反应,又能发生水解反应。
其中核磁共振氢谱为4组峰,且面积比为6:2:1:1的是_________ (写出其中一种的结构简式)。
(5)参照上述合成路线,以2 -甲基己烷和一氯甲烷为原料(无机试剂任选),设计制备化合物E的合成路线:________。
参考答案:
1.A
【详解】A.硬肥皂的主要成分为高级脂肪酸钠盐,A错误;
B.乙酸乙酯在稀硫酸中水解的产物为乙酸和乙醇,都能与钠反应,B正确;
C.葡萄糖含醛基、麦芽糖是一种还原性糖,都能发生银镜反应,C正确;
D.天然油脂是各种高级脂肪酸的甘油酯组成的混合物,不是高分子化合物,没有恒定的熔点、沸点,D正确;
答案选A。
2.A
【详解】A.在蛋白质溶液中加入饱和硫酸铵溶液,蛋白质析出,说明饱和硫酸铵溶液可使蛋白质的溶解性变小,此过程叫做蛋白质的“盐析”为物理变化,若再加水,还能溶解,此为蛋白质的再生,故A错误;
B.蛋白质溶液是胶体,胶粒能透过滤纸,但不能透过半透膜,故B正确;
C.钡餐”的成分是硫酸钡,硫酸钡不溶于盐酸,无法生成钡离子,不会引起中毒,故C错误;
D.皮肤中的蛋白质,遇浓硝酸发生颜色反应,显黄色,故D正确;
故答案为A。
3.B
【详解】淀粉在淀粉酶催化作用下经足够长时间后,完全水解为葡萄糖渗透到半透膜袋外的温水中,而淀粉酶是蛋白质,属于高分子化合物,留在半透膜袋内,因此袋内的液体为含苯环的蛋白质,因此遇淀粉不显蓝色,与新制氢氧化铜不产生砖红色沉淀,遇浓硝酸显黄色,B满足题意;
答案选B。
4.D
【详解】A.纯碱是碳酸钠,水解成碱性,油脂为酯类,碱性条件下会水解成溶于水的甘油和脂肪酸钠,所以碳酸钠可以用于清洗餐具油污,A正确;
B.玉米淀粉和废弃秸秆均可水解产生葡萄糖,在微生物发酵作用下可产生乙醇,B正确;
C.珠江三角洲的形成与胶体的聚沉有关,C正确;
D.84消毒液具有漂白性,会使衣物漂白,D错误;
答案选D。
5.C
【详解】A.丝绸为蚕丝制品,主要成分为蛋白质,故A正确;
B.聚乙烯是乙烯发生加聚反应生成的高分子化合物,故B正确;
C.氮化硼是无机物,氮化硼陶瓷基复合材料属于新型无机非金属材料,故C错误;
D.“空气捕捉”法能实现从空气中捕获二氧化碳,减少空气中二氧化碳含量,利于碳达峰、碳中和,故D正确;
答案选C。
6.B
【详解】A.石墨烯为碳单质,属于新型无机非金属材料,A正确;
B.聚氨酯材料是人工合成的材料,属于合成有机高分子材料,B错误;
C.纤维素为天然存在的高分子化合物,属于天然有机高分子化合物,C正确;
D.采用的高强钢和耐火耐候钢均为铁碳合金,属于合金材料,D正确;
故答案选B。
7.C
【分析】由结构简式可知,分子中含-COOH、-OH、碳碳双键、醚键等,结合羧酸、醇、烯烃的性质分析判断。
【详解】A.根据结构简式可知,分枝酸的分子式为C10H10O6,故A错误;
B.含-COOH与乙醇发生酯化反应,含-OH与乙酸发生酯化反应,反应类型相同,故B错误;
C.-COOH和-OH能够与Na反应放出氢气,则1mol分枝酸最多可与3molNa反应生成1.5mol氢气,标准状况下氢气的体积为1.5mol ×22.4L/mol =33.6 L,故C正确;
D.碳碳双键与溴的四氯化碳溶液发生加成反应,碳碳双键与-OH均能被酸性高锰酸钾溶液氧化,原理不同,故D错误;
故选C。
8.A
【详解】A.由结构简式可知,有机物Ⅰ分子中含有的酚羟基和有机物Ⅱ分子中含有的碳氯键均能与氢氧化钠溶液反应,故A正确;
B.苯环对角线上的碳及其所连原子共直线,4个原子处于同一直线,故B错误;
C.由反应方程式可知,有机物Ⅰ和有机物Ⅱ发生缩聚反应生成有机物Ⅲ,故C错误;
D.由结构简式可知,有机物Ⅱ和有机物Ⅲ中都含有连有4个不同原子或原子团的手性碳原子,故D错误;
故选A。
9.D
【详解】A.据图可知反应①中消耗LiI,反应⑤中又生成LiI,所以LiI也是该反应的催化剂,A正确;
B.反应④中氢气中的非极性键断裂,形成O-H键、I-H键,均为极性键,B正确;
C.据图可知反应物有CH3OH、CO2、H2,最终产物有CH3COOH和H2O,化学方程式为,C正确;
D.异丙醇为,根据图示反应机理可知,羧基取代羟基的位置生成异丁酸,而不是正丁酸,D错误;
综上所述答案为D。
10.C
【详解】A.酸性强弱顺序为HCO<<H2CO3,故苯酚钠和二氧化碳反应生成苯酚和碳酸氢钠,A错误;
B.酸性强弱顺序为HCO<,故碳酸氢钠不会生成苯酚,B错误;
C.由于苯酚的酸性比HCO的酸性强,所以能与Na2CO3反应生成和NaHCO3,C正确;
D.H2CO3的比强,苯酚不会生成碳酸,D错误;
故选C。
11.C
【详解】A.酸性高锰酸钾具有强氧化性,能将H2O2全部氧化为氧气,H2O2作还原剂,KMnO4作氧化剂,正确的离子方程式为:,故A错误;
B.AgOH能溶于氨水生成[Ag(NH3)2]+,正确的离子方程式为:,故B错误;
C.铝和NaOH溶液反应生成Na[Al(OH)4]和氢气,选项中的离子方程式正确;
D.向次氯酸钠溶液中通入少量CO2,生成的是正盐,正确的离子方程式为:,故D错误;
故选C。
12.A
【详解】A.实验室通过加热氢氧化钙和氯化铵的混合物制备氨气,故A正确;
B.石蜡催化分解实验过程中,酒精灯应该加热碎瓷片部位,故B错误;
C.制备氢氧化铁胶体的方法是向沸水中滴加饱和FeCl3溶液,故C错误;
D.淀粉水解及产物检验过程中淀粉在稀硫酸中水解完后要先加入过量NaOH溶液营造碱性环境,再滴加新制氢氧化铜悬浊液,故D错误;
故选A。
13.B
【详解】A.油脂在碱性、酸性条件及脂肪酶的作用下都能发生水解,A不正确;
B.乙醇分子中存在活泼氢原子,能与金属钠反应产生氢气,而苯不能与金属钠反应,所以可用金属钠区分乙醇和苯,B正确;
C.淀粉和纤维素的链节相同,但聚合度不同,所以二者不互为同分异构体,C不正确;
D.石油的分馏是物理变化,但煤的气化是化学变化,D不正确;
故选B。
14.A
【详解】A.苯酚和溴水反应生成的三溴苯酚能溶于苯,故没有沉淀、不能过滤,A错误;
B.NaOH溶液能吸收CO2和SO2、不能吸收乙烯, B正确;
C. 常温常压下NaOH溶液能吸收溴、不与溴苯反应,C正确;
D.乙烯与溴水发生加成反应、被吸收、溴水不能吸收乙烷,D正确;
答案选A。
15.(1) 互溶 减小 不溶于
(2) 升高 较高 氢键
【解析】略
16.(1)
(2)
(3) OHCCHO+O2HOOCCOOH
【详解】(1)乙炔先于氯化氢发生加成反应得到氯乙烯,氯乙烯发生加聚反应得到聚氯乙烯,化学方程式为:、;
(2)CH3CH2Br先发生消去反应得到乙烯,乙烯与溴单质加成得到1,2-二溴乙烷,水解即可得到乙二醇,化学方程式为:、、;
(3)乙二醇催化氧化得到乙二醛,乙二醛催化氧化得到乙二酸,乙二酸与乙二醇发生酯化反应得到乙二酸乙二醇酯,化学方程式为:、
OHCCHO+O2HOOCCOOH、。
17.(1)1:3
(2) CH3CH2OHCH2= CH2↑+H2O CH3CH2OCH2CH3
(3) 否 NaOH溶液
【解析】(1)
在烧瓶里注入乙醇和浓硫酸的体积比约是1:3;
(2)
①乙醇在浓硫酸、加热到170℃,发生消去反应,生成乙烯和水,方程式为CH3CH2OHCH2= CH2↑+H2O;
②升温经过140℃左右时,发生副反应,主要生成物的结构简式为CH3CH2OCH2CH3;
(3)
乙醇和浓硫酸反应生成单质炭,炭和浓硫酸在加热条件下反应生成二氧化硫、二氧化碳和水,二氧化硫具有还原性,能和溴单质反应,使溴水褪色,不能检验出乙烯的生成;氢氧化钠溶液可以除去生成的二氧化硫,而不和乙烯反应;故答案为:否;NaOH溶液。
18. 羟基(酚羟基)、羧基 C C9H8O4 三氯化铁溶液或浓溴水
【分析】(1)根据水杨酸的结构简式判断;
(2)符合条件的同分异构体中含酚羟基和醛基;
(3)根据结构简式判断能与NaOH反应的官能团及物质的量的关系;
(4)结合不饱和度和结构简式确定分子式;
(5)阿司匹林受潮发生水解,检验水解产物即可。
【详解】(1)水杨酸的结构简式为,其具有的官能团的名称为:酚羟基和羧基;
故答案为:酚羟基和羧基;
(2)与水杨酸互为同分异构体,既属于酚类又属于醛类的化合物的结构简式为:、、、、、;
故答案为: ;
(3)中的酚羟基和酯基都能与NaOH溶液反应,1mol该有机物最多可消耗3molNaOH;
故答案为:C;
(4)的不饱和度为6,1个阿司匹林分子中含9个C、8个H和4个O,阿司匹林的分子式为C9H8O4;
故答案为:C9H8O4。
(5)阿司匹林受潮发生水解反应生成和CH3COOH,阿司匹林中官能团为羧基和酯基,中官能团为酚羟基和羧基,故检验受潮的阿司匹林是否变质即检验是否有,可选用FeCl3溶液或浓溴水;
故答案为:三氯化铁溶液或浓溴水。
19. 乙醇 乙酸 苯 乙酸乙酯 油脂 葡萄糖溶液 蔗糖溶液 CH3COOC6H5+2NaOHCH3COONa++H2O +CO2+H2O→+NaHCO3 HOCH2CH2OH+HOOC-COOH+2H2O
【分析】由实验①可知,只有F G两种液体没有气味,则F、G为葡萄糖溶液、蔗糖溶液;由实验③可知,F中产生砖红色沉淀,F为葡萄糖,则G为蔗糖,只有B使沉淀溶解,B为乙酸;由实验②可知,只有C E D三种液体不溶解而浮在水面上,则C、E、D为苯、乙酸乙酯、油脂,则A为乙醇;由实验④可知,C仍有分层现象,且在D的试管中闻到特殊香味,则C为苯,D为乙酸乙酯,E为油脂,结合物质的性质分析解答。
【详解】(1)由实验①可知,只有F G两种液体没有气味,则F、G为葡萄糖溶液、蔗糖溶液;由实验③可知,F中产生砖红色沉淀,F为葡萄糖,则G为蔗糖,只有B使沉淀溶解,B为乙酸;由实验②可知,只有C E D三种液体不溶解而浮在水面上,则C、E、D为苯、乙酸乙酯、油脂,则A为乙醇;由实验④可知,C仍有分层现象,且在D的试管中闻到特殊香味,则C为苯,D为乙酸乙酯,E为油脂,故答案为:乙醇;乙酸;苯;乙酸乙酯;油脂;葡萄糖溶液;蔗糖溶液;
(2) 乙酸苯酚酯与NaOH溶液的化学反应方程式CH3COOC6H5+2NaOHCH3COONa++H2O,故答案为:CH3COOC6H5+2NaOHCH3COONa++H2O;
(3)苯酚钠中通入少量二氧化碳生成苯酚与碳酸氢钠,反应的化学方程式:+CO2+H2O→+NaHCO3,故答案为:+CO2+H2O→+NaHCO3;
(4)乙二醇和乙二酸在浓硫酸加热的条件下发生酯化反应生成六元环酯,反应的化学方程式为HOCH2CH2OH+HOOC-COOH+2H2O,故答案为:HOCH2CH2OH+HOOC-COOH+2H2O。
20.(1)支链越多,分子间的位阻越大,导致分子间作用力越小,沸点降低
(2)当溶液pH减小时,氨基酸主要以存在,当溶液pH增大时,氨基酸主要以存在,这两类离子溶解于溶液中使氨基酸溶解度增大
【解析】(1)
正戊烷的结构简式为CH3CH2CH2CH2CH3,异戊烷的结构简式为,新戊烷的结构简式为,由结构简式可知正戊烷、异戊烷和新戊烷中支链数目依次增多,支链越多,分子间的位阻越大,导致分子间作用力越小,烷烃的沸点降低,故答案为:支链越多,分子间的位阻越大,导致分子间作用力越小,沸点降低;
(2)
氨基酸分子中含有氨基和羧基,既能与酸反应,也能与碱反应,当氨基酸溶液pH偏小时,氨基与氢离子反应生成离子,增大在水中的溶解度,当溶液pH偏大时,羧基与氢氧根离子反应生成离子,增大在水中的溶解度,则随着溶液pH的增大或减少,氨基酸的溶解度都会变大,故答案为:当溶液pH减小时,氨基酸主要以存在,当溶液pH增大时,氨基酸主要以存在,这两类离子溶解于溶液中使氨基酸溶解度增大。
21.(1)苯酚分之间存在氢键,熔点较高,常温常压下以固体形式存在;溶于水后,苯酚与水分子间形成氢键,削弱了苯酚分子间的作用力,熔融温度下降,常温常压下以液体形式存在
(2) 键长小于,键能大于,稳定性大于
【分析】(1)
苯酚中含有羟基,苯酚分子之间存在氢键,故在常温常压下以固体形式存在;苯酚与水分子间形成氢键,削弱了苯酚分子间的作用力,熔融温度下降,常温常压下以液体形式存在;
(2)
非金属性越强,简单氢化物的热稳定性越强,N和P是同主族元素,同主族元素从上往下非金属性减弱,故 热稳定性较好; 中 键长小于 , 键能大于 ,稳定性 大于 ;
【点睛】
22. 乙烯 羟基 加成反应 氧化反应 nCH2=CHCOOH ACD
【分析】F还原得到G为,F氧化为E:,E经加聚生成X:,D与G经酯化反应生成H,H为:,可知D为CH3COOH,逆推则C为CH3COH,B为C2H5OH,A为乙烯,据此分析解题,
【详解】(1)化合物A名称为乙烯,化合物B为C2H5OH,官能团为羟基,F还原得到G化合物G的结构简式为。
(2)A→B→C反应的反应类型依次是加成生成醇、氧化生成醛。
(3)化合物E分子式为C3H4O2,能与碳酸钠溶液反应放出CO2,说明含有羧基,E的结构式为,E→X的化学方程式是nCH2=CHCOOH。
(4) A.D+G→H为酯化过程,浓硫酸作催化剂和吸水剂,A正确;
B.油脂在碱性条件下水解生成高级脂肪酸盐,甘油的反应叫皂化反应,B错误;
C.用碳酸钠溶液可以鉴别乙酸、和,现象分别为:混溶不分层、溶解有气泡产生、浮在溶液表面一层油状液体,C正确;
D.B、C、D的物质的量均为1mol,完全燃烧消耗的氧气量为3mol、2.5mol、2mol,依次减少,D正确;
(5) C5H10O2的两种同分异构体的结构简式,分别属于羧酸和酯类:,。
23. 环己烯 氯原子 消去反应 12 或
【详解】由A的分子式,可知A为烷烃,A在高温下通过Pt催化重整脱氢环化生成B,B的核磁共振氢谱中只有一组峰,可推知B为、A为CH3(CH2)4CH3;由I的结构简式可知,B与氯气发生取代反应生成G为,G发生消去反应生成H为;I与乙二醇发生缩聚反应生成聚酯纤维J为,结合C的分子式可知,B脱氢生成C为,C与氯气发生取代反应生成D为,结合信息②可知氯苯与氯乙烷发生取代反应生成E为,对比E、F的分子式,且F能与1,3-丁二烯形成高聚物,可推知F为、丁苯橡胶为,则:
(1)(1)H的化学名称为:环己烯,C的官能团名称为:氯原子。
(2)J的结构简式为,G生成H的反应类型为消去反应。
(3)由以上分析,F为,F合成丁苯橡胶的化学方程式为。
(4)I为HOOC(CH2)4COOH,①能与饱和NaHCO3溶液反应产生气体,则含有-COOH;②既能发生银镜反应,又能发生水解反应,则含有-CHO和-COO-;结合I分子中O原子个数可知,应含有HCOO-结构,剩余4个碳原子的碳链结构由两种:C-C-C-C和,则:
①-COOH和HCOO-连在同一个碳原子上,有3种不同结构;
②-COOH和HCOO-连在的不同碳原子上,有3种不同结构;
③-COOH和HCOO-连在C-C-C-C的不同碳原子上,有6种不同结构;
共有3+3+6=12种;
其中核磁共振氢谱为4组峰有机物分子中有4种不同化学环境的氢原子,且峰面积之比为6:2:1:1,则该有机物的结构简式为或
(5)2-甲基己烷在Pt催化、高温下发生脱氢环化生成,再在Pt催化、高温下发生脱氢环化生成甲苯,甲苯中甲基上的氢原子与氯气在光照条件下发生取代反应生成,结合已知信息②,与CH3Cl在Na、20℃下发生取代反应即可得到,则以2-甲基己烷和一氯甲烷为原料(无机试剂任选)制备化合物E的合成路线为
一、选择题
1.下列关于有机物的说法错误的是
A.生活中常用的硬肥皂是由高级脂肪酸钾盐制成的肥皂
B.乙酸乙酯在稀硫酸中水解的产物都能与钠反应
C.葡萄糖和麦芽糖都能发生银镜反应
D.天然油脂不是高分子化合物,没有恒定的熔点、沸点
2.下列有关蛋白质的叙述中不正确的是
A.蛋白质溶液中加入饱和硫酸铵溶液, 有蛋白质析出, 如再加水也不溶解
B.蛋白质溶液中的蛋白质分子能透过滤纸, 但不能透过半透膜
C.重金属盐能使蛋白质变性, 但吞服“钡餐”(BaSO4)不会引起中毒
D.浓硝酸溅在皮肤上, 能使皮肤呈黄色是因为蛋白质和浓硝酸发生颜色反应
3.将淀粉浆和淀粉酶(含苯环)的混合物放入半透膜(允许葡萄糖分子通过)袋中,扎好后浸入流动的温水中,经过足够长的时间后,取出袋内的液体,分别与①碘水、②新制Cu(OH)2(加热)、③浓硝酸(微热)作用,其现象依次是
A.显蓝色;无砖红色沉淀;显黄色
B.不显蓝色;无砖红色沉淀;显黄色
C.显蓝色;有砖红色沉淀;不显黄色
D.不显蓝色;有砖红色沉淀;不显黄色
4.化学与生活密切相关。下列叙述错误的是
A.纯碱溶液可以用于清洗餐具油污
B.玉米淀粉和废弃秸秆可生产乙醇
C.珠江三角洲的形成与胶体聚沉有关
D.“84消毒液”可以喷洒于衣物上进行杀菌消毒
5.从科技前沿到日常生活,化学无处不在。下列说法错误的是
A.在三星堆“祭祀坑”提取到丝绸制品残留物,其中丝绸主要成分为蛋白质
B.2022年北京冬奥会吉祥物“冰墩墩”使用的聚乙烯属于高分子材料
C.“天和”核心舱中使用的氮化硼陶瓷基复合材料属于高分子材料
D.“空气捕捉”法能实现从空气中捕获二氧化碳,利于碳达峰、碳中和
6.2022年北京冬奥会成功举办,展现了我国化学科学的迅猛发展,下列说法错误的是
A.开幕式专用演出服采用石墨烯智能发热材料,石墨烯属于新型无机非金属材料
B.速滑竞赛服使用了蜂窝样式的聚氨酯材料,属于天然有机高分子材料
C.滑雪板板心木质材料的主要成分为纤维素,属于天然有机高分子化合物
D.首钢单板滑雪大跳台的主体结构采用高强钢和耐火耐候钢,属于合金材料
7.分枝酸可用于生化研究,其结构简式如图,下列关于分枝酸的叙述正确的是
A.分枝酸的分子式为C10H12O6
B.可与乙醇、乙酸反应,反应类型不相同
C.1 mol分枝酸最多可与3 moNa反应,生成标准状况下的气体体积为33.6 L
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
8.环氧树脂胶粘剂广泛应用于日常生活和工业生产等各种方面。制取环氧树脂胶粘剂的反应如下:
下列说法正确的是
A.I和II均能与NaOH溶液反应 B.I至少有9个原子处于同一直线上
C.该反应属于加聚反应 D.I、II、III均不含手性碳原子
9.在Ru-Rh基催化剂表面发生反应制备乙酸的一种机理如图。下列说法错误的是
A.LiI也是该反应的催化剂
B.反应④中有非极性键的断裂和极性键的生成
C.制取乙酸的总方程式为:
D.运用该反应机理可由异丙醇制备正丁酸
10.已知酸性强弱顺序为HCO<<H2CO3,且较强的酸能与较弱的酸的盐反应生成较弱的酸和较强的酸的盐,则下列化学方程式书写正确的是
A.2+ H2O+CO2+Na2CO3
B.+ NaHCO3+Na2CO3
C.+ Na2CO3+ NaHCO3
D.+NaHCO3+ H2CO3
11.下列指定反应的离子方程式正确的是
A.向稀硫酸酸化的溶液中滴加溶液:
B.溶液中加入过量浓氨水:
C.向烧碱溶液中加入一小段铝片:
D.向溶液中通入少量:
12.下列实验正确的是
A.图I:实验室制氨气 B.图II:石蜡催化分解
C.图III:制备氢氧化铁胶体 D.图IV:淀粉水解及产物检验
13.下列关于有机物的说法正确的是
A.油脂只在碱性条件下水解 B.可用金属钠区分乙醇和苯
C.淀粉和纤维素互为同分异构体 D.石油的分馏和煤的气化都是物理变化
14.下列有关除去少量杂质的方法不正确的是
选项 物质 杂质 方法
A 苯 苯酚 加浓溴水后过滤
B 乙烯 CO2和SO2 通入装有NaOH溶液的洗气瓶洗气
C 溴苯 Br2 加NaOH溶液后分液
D 乙烷 乙烯 通入装有溴水的洗气瓶洗气
A.A B.B C.C D.D
二、填空题
15.羧酸的物理性质
(1)溶解性
甲酸、乙酸等分子中碳原子数较少的羧酸能够与水____,随着分子中碳原子数的增加,一元羧酸在水中的溶解度迅速____,甚至不溶于水。高级脂肪酸是_____水的蜡状固体。
(2)熔、沸点
羧酸的熔、沸点随碳原子数的增多而____,且与相对分子质量相当的其他有机化合物相比,沸点____,这与羧酸分子间可以形成____有关。
16.按题给要求填空
(1)写出以乙炔为原料制备聚氯乙烯反应方程式(无机物不限)
①_______ ;
②_______。
(2)用CH3CH2Br制取CH2OHCH2OH的三步反应方程式:
① _______;
②_______;
③ _______。
(3)写出用CH2OHCH2OH为原料制取的三步反应方程式:
①_______;
②_______;
③ _______。
17.实验室用如图所示装置制取乙烯。
(1)乙醇和浓硫酸的体积比为___________。
(2)①装置在170oC时主要反应的化学方程是___________;
②升温经过140oC左右时,发生副反应,主要生成物的结构简为___________;
(3)实验后期制得的乙烯气体中常含有两种杂质气体,将此混合气体直接通入溴水中能否证明乙烯发生加成反应的性质?___________(填“能”或“否”)仪器B中盛装的试剂应是___________。
18.水杨酸是合成阿司匹林的重要原料。水杨酸的学名邻羟基苯甲酸,结构简式为,,请回答下列问题:
(1)请写出水杨酸中具有的官能团名称_____________________;
(2)请写出与水杨酸互为同分异构体,既属于酚类又属于醛类化合物的结构简式(写一种即可):____________________________________;
(3)水杨酸的另一种同分异构体的结构简式为,1mol该有机物在适宜条件下与氢氧化钠经过一系列反应,最多能消耗氢氧化钠的物质的量为(填序号)______;
A.1mol B.2mol C.3mol D.4mol
(4)已知有机物CH3COOH可以表示为:,在一定条件下,水杨酸与乙酸酐可合成阿司匹林,阿司匹林可表示为:,则阿司匹林的分子式为__________;
(5)阿司匹林药片需要保存在干燥处,受潮的药片易变质不宜服用;检验受潮药片是否变质的试剂是(只选一种试剂即可)______________________。
19.现有7瓶失去了标签的液体,它们可能是①乙醇②乙酸③苯④乙酸乙酯⑤油脂⑥葡萄糖溶液⑦蔗糖溶液。现通过如下实验步骤来确定各试剂瓶中所装的液体名称:
实验步骤和方法 实验现象
①把7瓶液体依次标号A、B、C、D、E、F、G后闻气味 只有F、G两种液体没有气味
②分别取少量7种液体于试管中加水稀释 只有C、D、E三种液体不溶解而浮在水上层
③分别取少量7种液体于试管中,加入新制的Cu(OH)2并加热 只有B使沉淀溶解,F中产生砖红色沉淀
④各取少量C、D、E于试管中,加稀NaOH溶液并加热 只有C仍有分层现象,且在D的试管中闻到特殊香味
(1)试给它们的试剂瓶重新贴上标签(填物质序号):A___,B___,C___,D___,E___,F__,G___。
(2)写出在乙酸苯酚酯中加入NaOH溶液并加热的化学方程式:___。
(3)写出苯酚钠中通入少量的二氧化碳的化学方程式:___。
(4)写乙二醇和乙二酸脱水生成六元环酯的化学方程式:__。
20.回答下列问题:
(1)戊烷有三种同分异构体,其沸点如下:
正戊烷 异戊烷 新戊烷
沸点 36.1℃ 27.9℃ 9.5℃
请说明其沸点差异的原因___________。
(2)甘氨酸()在水中的溶解度与溶液的pH有关,当pH约为6时主要以内盐()的形态存在,其溶解度最小。请解析随着溶液pH的增大或减少,其溶解度变大的原因___________。
21.回答下列问题:
(1)常温常压下苯酚为无色晶体,而苯酚在水中以液态形式存在,原因是___________。
(2)和比较,热稳定性较好的是___________,理由是___________。
三、有机推断题
22.烃A是一种基础化工原料,标准状况下密度为1.25g L-1,B与G互为同系物。H是有芳香味的油状液体。有关物质转化关系如下图:
请回答下列问题:
(1)化合物A名称为____,化合物B的官能团为____,化合物G的结构简式为____。
(2)A→B→C反应的反应类型依次是____、____。
(3)化合物E分子式为C3H4O2,能与碳酸钠溶液反应放出CO2,E→X的化学方程式是____。
(4)下列说法正确的是____。
A.D+G→H过程,浓硫酸作催化剂和吸水剂
B.H在碱性条件下水解是皂化反应
C.用碳酸钠溶液可以鉴别D、G和H
D.相同物质的量的B、C、D完全燃烧消耗的氧气量依次减少
(5)写出C5H10O2的两种同分异构体的结构简式,分别属于羧酸和酯类:____,___。
23.石油分馏得到的轻汽油可在Pt催化下脱氢环化,逐步转化为芳香烃。以链烃A为原料合成两种高分子材料的路线如下:
已知以下信息:
①B的核磁共振氢谱中只有一组峰;G 为一氯代烃。
②R-x+R'-xR-R'(x为卤素原子,R、R'为烃基)
回答以下问题:
(1)H的化学名称为________,C 的官能团名称为________。
(2)J的结构简式为________,G生成H的反应类型为________ 。
(3)F合成丁苯橡胶的化学方程式为_________。
(4)I的同分异构体中能同时满足下列条件的共有________种(不含立体异构)。
①能与饱和NaHCO3溶液反应产生气体;
②既能发生银镜反应,又能发生水解反应。
其中核磁共振氢谱为4组峰,且面积比为6:2:1:1的是_________ (写出其中一种的结构简式)。
(5)参照上述合成路线,以2 -甲基己烷和一氯甲烷为原料(无机试剂任选),设计制备化合物E的合成路线:________。
参考答案:
1.A
【详解】A.硬肥皂的主要成分为高级脂肪酸钠盐,A错误;
B.乙酸乙酯在稀硫酸中水解的产物为乙酸和乙醇,都能与钠反应,B正确;
C.葡萄糖含醛基、麦芽糖是一种还原性糖,都能发生银镜反应,C正确;
D.天然油脂是各种高级脂肪酸的甘油酯组成的混合物,不是高分子化合物,没有恒定的熔点、沸点,D正确;
答案选A。
2.A
【详解】A.在蛋白质溶液中加入饱和硫酸铵溶液,蛋白质析出,说明饱和硫酸铵溶液可使蛋白质的溶解性变小,此过程叫做蛋白质的“盐析”为物理变化,若再加水,还能溶解,此为蛋白质的再生,故A错误;
B.蛋白质溶液是胶体,胶粒能透过滤纸,但不能透过半透膜,故B正确;
C.钡餐”的成分是硫酸钡,硫酸钡不溶于盐酸,无法生成钡离子,不会引起中毒,故C错误;
D.皮肤中的蛋白质,遇浓硝酸发生颜色反应,显黄色,故D正确;
故答案为A。
3.B
【详解】淀粉在淀粉酶催化作用下经足够长时间后,完全水解为葡萄糖渗透到半透膜袋外的温水中,而淀粉酶是蛋白质,属于高分子化合物,留在半透膜袋内,因此袋内的液体为含苯环的蛋白质,因此遇淀粉不显蓝色,与新制氢氧化铜不产生砖红色沉淀,遇浓硝酸显黄色,B满足题意;
答案选B。
4.D
【详解】A.纯碱是碳酸钠,水解成碱性,油脂为酯类,碱性条件下会水解成溶于水的甘油和脂肪酸钠,所以碳酸钠可以用于清洗餐具油污,A正确;
B.玉米淀粉和废弃秸秆均可水解产生葡萄糖,在微生物发酵作用下可产生乙醇,B正确;
C.珠江三角洲的形成与胶体的聚沉有关,C正确;
D.84消毒液具有漂白性,会使衣物漂白,D错误;
答案选D。
5.C
【详解】A.丝绸为蚕丝制品,主要成分为蛋白质,故A正确;
B.聚乙烯是乙烯发生加聚反应生成的高分子化合物,故B正确;
C.氮化硼是无机物,氮化硼陶瓷基复合材料属于新型无机非金属材料,故C错误;
D.“空气捕捉”法能实现从空气中捕获二氧化碳,减少空气中二氧化碳含量,利于碳达峰、碳中和,故D正确;
答案选C。
6.B
【详解】A.石墨烯为碳单质,属于新型无机非金属材料,A正确;
B.聚氨酯材料是人工合成的材料,属于合成有机高分子材料,B错误;
C.纤维素为天然存在的高分子化合物,属于天然有机高分子化合物,C正确;
D.采用的高强钢和耐火耐候钢均为铁碳合金,属于合金材料,D正确;
故答案选B。
7.C
【分析】由结构简式可知,分子中含-COOH、-OH、碳碳双键、醚键等,结合羧酸、醇、烯烃的性质分析判断。
【详解】A.根据结构简式可知,分枝酸的分子式为C10H10O6,故A错误;
B.含-COOH与乙醇发生酯化反应,含-OH与乙酸发生酯化反应,反应类型相同,故B错误;
C.-COOH和-OH能够与Na反应放出氢气,则1mol分枝酸最多可与3molNa反应生成1.5mol氢气,标准状况下氢气的体积为1.5mol ×22.4L/mol =33.6 L,故C正确;
D.碳碳双键与溴的四氯化碳溶液发生加成反应,碳碳双键与-OH均能被酸性高锰酸钾溶液氧化,原理不同,故D错误;
故选C。
8.A
【详解】A.由结构简式可知,有机物Ⅰ分子中含有的酚羟基和有机物Ⅱ分子中含有的碳氯键均能与氢氧化钠溶液反应,故A正确;
B.苯环对角线上的碳及其所连原子共直线,4个原子处于同一直线,故B错误;
C.由反应方程式可知,有机物Ⅰ和有机物Ⅱ发生缩聚反应生成有机物Ⅲ,故C错误;
D.由结构简式可知,有机物Ⅱ和有机物Ⅲ中都含有连有4个不同原子或原子团的手性碳原子,故D错误;
故选A。
9.D
【详解】A.据图可知反应①中消耗LiI,反应⑤中又生成LiI,所以LiI也是该反应的催化剂,A正确;
B.反应④中氢气中的非极性键断裂,形成O-H键、I-H键,均为极性键,B正确;
C.据图可知反应物有CH3OH、CO2、H2,最终产物有CH3COOH和H2O,化学方程式为,C正确;
D.异丙醇为,根据图示反应机理可知,羧基取代羟基的位置生成异丁酸,而不是正丁酸,D错误;
综上所述答案为D。
10.C
【详解】A.酸性强弱顺序为HCO<<H2CO3,故苯酚钠和二氧化碳反应生成苯酚和碳酸氢钠,A错误;
B.酸性强弱顺序为HCO<,故碳酸氢钠不会生成苯酚,B错误;
C.由于苯酚的酸性比HCO的酸性强,所以能与Na2CO3反应生成和NaHCO3,C正确;
D.H2CO3的比强,苯酚不会生成碳酸,D错误;
故选C。
11.C
【详解】A.酸性高锰酸钾具有强氧化性,能将H2O2全部氧化为氧气,H2O2作还原剂,KMnO4作氧化剂,正确的离子方程式为:,故A错误;
B.AgOH能溶于氨水生成[Ag(NH3)2]+,正确的离子方程式为:,故B错误;
C.铝和NaOH溶液反应生成Na[Al(OH)4]和氢气,选项中的离子方程式正确;
D.向次氯酸钠溶液中通入少量CO2,生成的是正盐,正确的离子方程式为:,故D错误;
故选C。
12.A
【详解】A.实验室通过加热氢氧化钙和氯化铵的混合物制备氨气,故A正确;
B.石蜡催化分解实验过程中,酒精灯应该加热碎瓷片部位,故B错误;
C.制备氢氧化铁胶体的方法是向沸水中滴加饱和FeCl3溶液,故C错误;
D.淀粉水解及产物检验过程中淀粉在稀硫酸中水解完后要先加入过量NaOH溶液营造碱性环境,再滴加新制氢氧化铜悬浊液,故D错误;
故选A。
13.B
【详解】A.油脂在碱性、酸性条件及脂肪酶的作用下都能发生水解,A不正确;
B.乙醇分子中存在活泼氢原子,能与金属钠反应产生氢气,而苯不能与金属钠反应,所以可用金属钠区分乙醇和苯,B正确;
C.淀粉和纤维素的链节相同,但聚合度不同,所以二者不互为同分异构体,C不正确;
D.石油的分馏是物理变化,但煤的气化是化学变化,D不正确;
故选B。
14.A
【详解】A.苯酚和溴水反应生成的三溴苯酚能溶于苯,故没有沉淀、不能过滤,A错误;
B.NaOH溶液能吸收CO2和SO2、不能吸收乙烯, B正确;
C. 常温常压下NaOH溶液能吸收溴、不与溴苯反应,C正确;
D.乙烯与溴水发生加成反应、被吸收、溴水不能吸收乙烷,D正确;
答案选A。
15.(1) 互溶 减小 不溶于
(2) 升高 较高 氢键
【解析】略
16.(1)
(2)
(3) OHCCHO+O2HOOCCOOH
【详解】(1)乙炔先于氯化氢发生加成反应得到氯乙烯,氯乙烯发生加聚反应得到聚氯乙烯,化学方程式为:、;
(2)CH3CH2Br先发生消去反应得到乙烯,乙烯与溴单质加成得到1,2-二溴乙烷,水解即可得到乙二醇,化学方程式为:、、;
(3)乙二醇催化氧化得到乙二醛,乙二醛催化氧化得到乙二酸,乙二酸与乙二醇发生酯化反应得到乙二酸乙二醇酯,化学方程式为:、
OHCCHO+O2HOOCCOOH、。
17.(1)1:3
(2) CH3CH2OHCH2= CH2↑+H2O CH3CH2OCH2CH3
(3) 否 NaOH溶液
【解析】(1)
在烧瓶里注入乙醇和浓硫酸的体积比约是1:3;
(2)
①乙醇在浓硫酸、加热到170℃,发生消去反应,生成乙烯和水,方程式为CH3CH2OHCH2= CH2↑+H2O;
②升温经过140℃左右时,发生副反应,主要生成物的结构简式为CH3CH2OCH2CH3;
(3)
乙醇和浓硫酸反应生成单质炭,炭和浓硫酸在加热条件下反应生成二氧化硫、二氧化碳和水,二氧化硫具有还原性,能和溴单质反应,使溴水褪色,不能检验出乙烯的生成;氢氧化钠溶液可以除去生成的二氧化硫,而不和乙烯反应;故答案为:否;NaOH溶液。
18. 羟基(酚羟基)、羧基 C C9H8O4 三氯化铁溶液或浓溴水
【分析】(1)根据水杨酸的结构简式判断;
(2)符合条件的同分异构体中含酚羟基和醛基;
(3)根据结构简式判断能与NaOH反应的官能团及物质的量的关系;
(4)结合不饱和度和结构简式确定分子式;
(5)阿司匹林受潮发生水解,检验水解产物即可。
【详解】(1)水杨酸的结构简式为,其具有的官能团的名称为:酚羟基和羧基;
故答案为:酚羟基和羧基;
(2)与水杨酸互为同分异构体,既属于酚类又属于醛类的化合物的结构简式为:、、、、、;
故答案为: ;
(3)中的酚羟基和酯基都能与NaOH溶液反应,1mol该有机物最多可消耗3molNaOH;
故答案为:C;
(4)的不饱和度为6,1个阿司匹林分子中含9个C、8个H和4个O,阿司匹林的分子式为C9H8O4;
故答案为:C9H8O4。
(5)阿司匹林受潮发生水解反应生成和CH3COOH,阿司匹林中官能团为羧基和酯基,中官能团为酚羟基和羧基,故检验受潮的阿司匹林是否变质即检验是否有,可选用FeCl3溶液或浓溴水;
故答案为:三氯化铁溶液或浓溴水。
19. 乙醇 乙酸 苯 乙酸乙酯 油脂 葡萄糖溶液 蔗糖溶液 CH3COOC6H5+2NaOHCH3COONa++H2O +CO2+H2O→+NaHCO3 HOCH2CH2OH+HOOC-COOH+2H2O
【分析】由实验①可知,只有F G两种液体没有气味,则F、G为葡萄糖溶液、蔗糖溶液;由实验③可知,F中产生砖红色沉淀,F为葡萄糖,则G为蔗糖,只有B使沉淀溶解,B为乙酸;由实验②可知,只有C E D三种液体不溶解而浮在水面上,则C、E、D为苯、乙酸乙酯、油脂,则A为乙醇;由实验④可知,C仍有分层现象,且在D的试管中闻到特殊香味,则C为苯,D为乙酸乙酯,E为油脂,结合物质的性质分析解答。
【详解】(1)由实验①可知,只有F G两种液体没有气味,则F、G为葡萄糖溶液、蔗糖溶液;由实验③可知,F中产生砖红色沉淀,F为葡萄糖,则G为蔗糖,只有B使沉淀溶解,B为乙酸;由实验②可知,只有C E D三种液体不溶解而浮在水面上,则C、E、D为苯、乙酸乙酯、油脂,则A为乙醇;由实验④可知,C仍有分层现象,且在D的试管中闻到特殊香味,则C为苯,D为乙酸乙酯,E为油脂,故答案为:乙醇;乙酸;苯;乙酸乙酯;油脂;葡萄糖溶液;蔗糖溶液;
(2) 乙酸苯酚酯与NaOH溶液的化学反应方程式CH3COOC6H5+2NaOHCH3COONa++H2O,故答案为:CH3COOC6H5+2NaOHCH3COONa++H2O;
(3)苯酚钠中通入少量二氧化碳生成苯酚与碳酸氢钠,反应的化学方程式:+CO2+H2O→+NaHCO3,故答案为:+CO2+H2O→+NaHCO3;
(4)乙二醇和乙二酸在浓硫酸加热的条件下发生酯化反应生成六元环酯,反应的化学方程式为HOCH2CH2OH+HOOC-COOH+2H2O,故答案为:HOCH2CH2OH+HOOC-COOH+2H2O。
20.(1)支链越多,分子间的位阻越大,导致分子间作用力越小,沸点降低
(2)当溶液pH减小时,氨基酸主要以存在,当溶液pH增大时,氨基酸主要以存在,这两类离子溶解于溶液中使氨基酸溶解度增大
【解析】(1)
正戊烷的结构简式为CH3CH2CH2CH2CH3,异戊烷的结构简式为,新戊烷的结构简式为,由结构简式可知正戊烷、异戊烷和新戊烷中支链数目依次增多,支链越多,分子间的位阻越大,导致分子间作用力越小,烷烃的沸点降低,故答案为:支链越多,分子间的位阻越大,导致分子间作用力越小,沸点降低;
(2)
氨基酸分子中含有氨基和羧基,既能与酸反应,也能与碱反应,当氨基酸溶液pH偏小时,氨基与氢离子反应生成离子,增大在水中的溶解度,当溶液pH偏大时,羧基与氢氧根离子反应生成离子,增大在水中的溶解度,则随着溶液pH的增大或减少,氨基酸的溶解度都会变大,故答案为:当溶液pH减小时,氨基酸主要以存在,当溶液pH增大时,氨基酸主要以存在,这两类离子溶解于溶液中使氨基酸溶解度增大。
21.(1)苯酚分之间存在氢键,熔点较高,常温常压下以固体形式存在;溶于水后,苯酚与水分子间形成氢键,削弱了苯酚分子间的作用力,熔融温度下降,常温常压下以液体形式存在
(2) 键长小于,键能大于,稳定性大于
【分析】(1)
苯酚中含有羟基,苯酚分子之间存在氢键,故在常温常压下以固体形式存在;苯酚与水分子间形成氢键,削弱了苯酚分子间的作用力,熔融温度下降,常温常压下以液体形式存在;
(2)
非金属性越强,简单氢化物的热稳定性越强,N和P是同主族元素,同主族元素从上往下非金属性减弱,故 热稳定性较好; 中 键长小于 , 键能大于 ,稳定性 大于 ;
【点睛】
22. 乙烯 羟基 加成反应 氧化反应 nCH2=CHCOOH ACD
【分析】F还原得到G为,F氧化为E:,E经加聚生成X:,D与G经酯化反应生成H,H为:,可知D为CH3COOH,逆推则C为CH3COH,B为C2H5OH,A为乙烯,据此分析解题,
【详解】(1)化合物A名称为乙烯,化合物B为C2H5OH,官能团为羟基,F还原得到G化合物G的结构简式为。
(2)A→B→C反应的反应类型依次是加成生成醇、氧化生成醛。
(3)化合物E分子式为C3H4O2,能与碳酸钠溶液反应放出CO2,说明含有羧基,E的结构式为,E→X的化学方程式是nCH2=CHCOOH。
(4) A.D+G→H为酯化过程,浓硫酸作催化剂和吸水剂,A正确;
B.油脂在碱性条件下水解生成高级脂肪酸盐,甘油的反应叫皂化反应,B错误;
C.用碳酸钠溶液可以鉴别乙酸、和,现象分别为:混溶不分层、溶解有气泡产生、浮在溶液表面一层油状液体,C正确;
D.B、C、D的物质的量均为1mol,完全燃烧消耗的氧气量为3mol、2.5mol、2mol,依次减少,D正确;
(5) C5H10O2的两种同分异构体的结构简式,分别属于羧酸和酯类:,。
23. 环己烯 氯原子 消去反应 12 或
【详解】由A的分子式,可知A为烷烃,A在高温下通过Pt催化重整脱氢环化生成B,B的核磁共振氢谱中只有一组峰,可推知B为、A为CH3(CH2)4CH3;由I的结构简式可知,B与氯气发生取代反应生成G为,G发生消去反应生成H为;I与乙二醇发生缩聚反应生成聚酯纤维J为,结合C的分子式可知,B脱氢生成C为,C与氯气发生取代反应生成D为,结合信息②可知氯苯与氯乙烷发生取代反应生成E为,对比E、F的分子式,且F能与1,3-丁二烯形成高聚物,可推知F为、丁苯橡胶为,则:
(1)(1)H的化学名称为:环己烯,C的官能团名称为:氯原子。
(2)J的结构简式为,G生成H的反应类型为消去反应。
(3)由以上分析,F为,F合成丁苯橡胶的化学方程式为。
(4)I为HOOC(CH2)4COOH,①能与饱和NaHCO3溶液反应产生气体,则含有-COOH;②既能发生银镜反应,又能发生水解反应,则含有-CHO和-COO-;结合I分子中O原子个数可知,应含有HCOO-结构,剩余4个碳原子的碳链结构由两种:C-C-C-C和,则:
①-COOH和HCOO-连在同一个碳原子上,有3种不同结构;
②-COOH和HCOO-连在的不同碳原子上,有3种不同结构;
③-COOH和HCOO-连在C-C-C-C的不同碳原子上,有6种不同结构;
共有3+3+6=12种;
其中核磁共振氢谱为4组峰有机物分子中有4种不同化学环境的氢原子,且峰面积之比为6:2:1:1,则该有机物的结构简式为或
(5)2-甲基己烷在Pt催化、高温下发生脱氢环化生成,再在Pt催化、高温下发生脱氢环化生成甲苯,甲苯中甲基上的氢原子与氯气在光照条件下发生取代反应生成,结合已知信息②,与CH3Cl在Na、20℃下发生取代反应即可得到,则以2-甲基己烷和一氯甲烷为原料(无机试剂任选)制备化合物E的合成路线为
