人教版九年级化学 第十一单元复习课件(共31张PPT)
文档属性
| 名称 | 人教版九年级化学 第十一单元复习课件(共31张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-07 00:00:00 | ||
图片预览


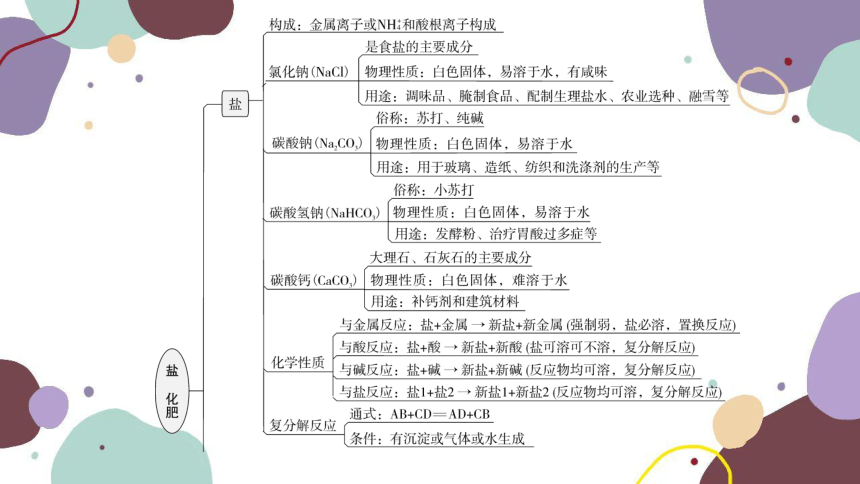









文档简介
(共31张PPT)
单 元 复 习
第十一单元复习
目录
01
思维导图
02
易错点透析
03
重点突破
易错点1 易混淆几种常见物质的俗称和用途
生活中的盐通常指的是食盐,它的主要成分是NaCl;碳酸钠(Na2CO3)俗称纯碱、苏打;碳酸氢钠(NaHCO3)俗称小苏打;碳酸钙(CaCO3)是石灰石、大理石的主要成分;氧化钙(CaO)俗称生石灰;氢氧化钠(NaOH)俗称火碱、烧碱、苛性钠;氢氧化钙[Ca(OH)2]俗称熟石灰、消石灰。
【例1】下列关于碳酸钠与碳酸氢钠的说法错误的是( )
A. 碳酸钠溶液呈碱性
B. 碳酸氢钠是盐,但其水溶液呈酸性
C. 碳酸钠俗称纯碱,但不是碱
D. 碳酸氢钠可用于制作糕点
易错提醒:纯碱是碳酸钠的俗名,纯碱不是碱而是一种显碱性的盐。
正解:A. 碳酸钠溶液能使无色酚酞溶液变红,呈碱性,故A正确;B. 碳酸氢钠是由钠离子和碳酸氢根离子构成的化合物,属于盐,但其水溶液呈碱性,故B错误;C. 碳酸钠俗称纯碱、苏打,是一种盐,故C正确;D. 碳酸氢钠是常见的发酵粉,俗称小苏打,可用于烘焙糕点,故D正确。
答案:B
学以致用
1. 下列关于物质俗称、用途的说法正确的是( B )
A. Na2CO3——小苏打——炉具清洁剂
B. NaOH——烧碱——纺织、造纸
C. CaO——熟石灰——改良酸性土壤
D. CaCO3——生石灰——建筑材料
B
易错点2 不清楚化肥的种类、作用和鉴别
农作物生长所必需的营养元素有许多种,但需求量最大的是氮、磷、钾三种元素。氮、磷、钾的作用分别对应植物的叶、根、茎。可通过“一看二闻三溶四加碱”的方法鉴别化肥。
A. (NH4)2SO4属于复合肥料
B. 农作物所必需的营养元素只有氮、磷和钾三种
C. 磷肥能使作物根系发达,耐寒耐旱
D. 铵态氮肥与熟石灰混合施用可以明显提高肥效
【例2】“庄稼一枝花,全靠肥当家。”下列关于农作物和化肥的说法正确的是( )
易错提醒:判断化肥的种类,关键是看化肥中含有哪种营养元素,含有钾元素的为钾肥,含有氮元素的为氮肥,含有磷元素的为磷肥,含有氮、磷、钾三种营养元素中的两种或两种以上的为复合肥。
正解:A. (NH4)2SO4中只含有氮、磷、钾中的氮元素,属于氮肥,故A错误;B. 农作物所必需的营养元素有碳、氢、氧、氮、磷、钾、钙、镁等,故B错误;C. 磷肥能使作物根系发达,耐寒耐旱,故C正确;D. 铵态氮肥与熟石灰混合施用会产生氨气,使肥效降低,故D错误。
答案:C
学以致用
2. (2019广东)化学肥料是农作物的“粮食”。下列关于化学肥料的说法正确的是( C )
A. 尿素[CO(NH2)2]属于复合肥料
B. 大量施用化肥以提高农作物产量
C. 铵态氮肥与草木灰混用,会降低肥效
D. 棉花叶片枯黄,应施用硫酸钾等钾肥
C
重点1 化学方程式书写
1. 含钙化合物的转化:(如图11-F-1)
图11-F-1
2. 盐的化学性质:(如图11-F-2)
图11-F-2
Cu(OH)2↓
重点2 盐的化学性质
3. 使用如图11-F-3所示的装置(搅拌装置略)探究溶液离子浓度变化,已知反应产物全部是沉淀(或沉淀和水)时灯光变暗。下列灯光变化可能出现“亮→暗(或灭)→亮”现象的是( D )
D
图11-F-3
选 项 A B C D
试剂a NaCl K2CO3 HCl H2SO4
试剂b AgNO3 HNO3 NaOH Ba(OH)2
4. 归纳和总结是学习化学的重要方法。小李同学在复习单质、氧化物、酸、碱和盐的化学性质时,发现许多不同类别的物质反应都能生成盐,于是他构建了如图11-F-4甲所示的知识网络图。
图11-F-4
(1)图中①处可填入的内容是 酸+盐(或金属+盐) (不能与图中已有的信息重复)。
酸+盐(或金属+盐)
图11-F-4
(3)掌握了物质的化学性质,老师带领大家设计了一款新游戏——“化学棋”。游戏规则:①每粒棋子代表一种物质;②吃子:所选棋子能与棋盘(如图11-F-4乙)中的某棋子发生反应,则棋盘中的该棋子被吃掉;
图11-F-4
③连吃:前一次反应的生成物能与另一个棋子发生反应时,则该棋子也被吃掉。若小李想用一颗棋子连续吃掉棋盘上的所有棋子,应选择的棋子是 B (填字母)。
B
重点3 化学肥料种类、作用与鉴别
5. 如图11-F-5是根据组成元素对化学肥料的分类图。下列叙述错误的是( B )
图11-F-5
B
A. 氨水(NH3·H2O)属于氮肥
B. 氯化钾属于钾肥,可大量施用
C. 图中①表示的是磷肥
D. 图中②表示的是复合肥
6. 实验室有三瓶化肥未贴标签,只知道它们分别是NH4HCO3、NH4Cl和CO(NH2)2中的一种。为鉴别这三瓶化肥,某同学分别取少量样品编号为A、B、C,并进行如图11-F-6所示实验。
图11-F-6
(1)写出三种化肥的名称:A 尿素 ;B 碳酸氢 ;C 氯化铵 。
(2)如果操作Ⅱ中B、C两种样品没有另取,对实验结果 无 (填“有”或“无”)影响。
(3)常温下如果要鉴别B、C两种样品, 能 (填“能”或“不能”)采取闻气味的方法。
尿素
碳酸氢铵
氯化铵
无
能
重点4 复分解反应及其应用
7. 下列四组实验均是向盛有不同物质的烧杯中逐滴加入X溶液至过量。生成沉淀或气体的质量与加入X溶液的质量关系,符合图11-F-7所示的图像的是( D )
D
图11-F-7
选项 烧杯中的物质 X溶液
A CuSO4和Na2SO4溶液 NaOH溶液
B 铜锌合金 稀H2SO4
C 稀HNO3和稀H2SO4 BaCl2溶液
D NaOH和Na2CO3溶液 稀盐酸
8. 下列各组溶液,不用其他试剂就不能鉴别出来的是( C )
A. NaOH、KCl、稀硝酸、FeCl3
B. 稀盐酸、KNO3、Na2CO3、Ca(NO3)2
C. Na2SO4、BaCl2、Na2CO3、NaCl
D. BaCl2、MgSO4、稀硝酸、NaOH
C
重点5 粗盐提纯
9. “粗盐中难溶性杂质的去除”实验中,称取5.0 g粗盐,溶解后剩余1.0 g,经过过滤、蒸发得到3.0 g精盐,下列有关该实验的说法错误的是( C )
A. 得到的精盐为混合物
B. 使用次数最多的仪器是玻璃棒
C. 该实验得到的精盐产率为60%
D. 蒸发后,所得精盐潮湿,会导致产率偏高
C
10. 某食盐样品中含有少量沙土、CaCl2和MgCl2。如图11-F-8所示是除去食盐样品中沙土、CaCl2和MgCl2的实验流程。
图11-F-8
(1)操作Ⅰ的名称是 过滤 ,加入的试剂A是 Na2CO3 (填化学式,下同),沉淀是 CaCO3 。
(3)加入试剂B的目的是 除去过量的NaOH和Na2C 。
过滤
Na2CO3
CaCO3
2NaOH+
除去过量的NaOH和Na2CO3
(4)蒸发结晶时用到玻璃棒的作用是 搅拌,防止局部温度过高造成液滴飞溅
搅拌,防止局部
温度过高造成液滴飞溅
谢 谢!
单 元 复 习
第十一单元复习
目录
01
思维导图
02
易错点透析
03
重点突破
易错点1 易混淆几种常见物质的俗称和用途
生活中的盐通常指的是食盐,它的主要成分是NaCl;碳酸钠(Na2CO3)俗称纯碱、苏打;碳酸氢钠(NaHCO3)俗称小苏打;碳酸钙(CaCO3)是石灰石、大理石的主要成分;氧化钙(CaO)俗称生石灰;氢氧化钠(NaOH)俗称火碱、烧碱、苛性钠;氢氧化钙[Ca(OH)2]俗称熟石灰、消石灰。
【例1】下列关于碳酸钠与碳酸氢钠的说法错误的是( )
A. 碳酸钠溶液呈碱性
B. 碳酸氢钠是盐,但其水溶液呈酸性
C. 碳酸钠俗称纯碱,但不是碱
D. 碳酸氢钠可用于制作糕点
易错提醒:纯碱是碳酸钠的俗名,纯碱不是碱而是一种显碱性的盐。
正解:A. 碳酸钠溶液能使无色酚酞溶液变红,呈碱性,故A正确;B. 碳酸氢钠是由钠离子和碳酸氢根离子构成的化合物,属于盐,但其水溶液呈碱性,故B错误;C. 碳酸钠俗称纯碱、苏打,是一种盐,故C正确;D. 碳酸氢钠是常见的发酵粉,俗称小苏打,可用于烘焙糕点,故D正确。
答案:B
学以致用
1. 下列关于物质俗称、用途的说法正确的是( B )
A. Na2CO3——小苏打——炉具清洁剂
B. NaOH——烧碱——纺织、造纸
C. CaO——熟石灰——改良酸性土壤
D. CaCO3——生石灰——建筑材料
B
易错点2 不清楚化肥的种类、作用和鉴别
农作物生长所必需的营养元素有许多种,但需求量最大的是氮、磷、钾三种元素。氮、磷、钾的作用分别对应植物的叶、根、茎。可通过“一看二闻三溶四加碱”的方法鉴别化肥。
A. (NH4)2SO4属于复合肥料
B. 农作物所必需的营养元素只有氮、磷和钾三种
C. 磷肥能使作物根系发达,耐寒耐旱
D. 铵态氮肥与熟石灰混合施用可以明显提高肥效
【例2】“庄稼一枝花,全靠肥当家。”下列关于农作物和化肥的说法正确的是( )
易错提醒:判断化肥的种类,关键是看化肥中含有哪种营养元素,含有钾元素的为钾肥,含有氮元素的为氮肥,含有磷元素的为磷肥,含有氮、磷、钾三种营养元素中的两种或两种以上的为复合肥。
正解:A. (NH4)2SO4中只含有氮、磷、钾中的氮元素,属于氮肥,故A错误;B. 农作物所必需的营养元素有碳、氢、氧、氮、磷、钾、钙、镁等,故B错误;C. 磷肥能使作物根系发达,耐寒耐旱,故C正确;D. 铵态氮肥与熟石灰混合施用会产生氨气,使肥效降低,故D错误。
答案:C
学以致用
2. (2019广东)化学肥料是农作物的“粮食”。下列关于化学肥料的说法正确的是( C )
A. 尿素[CO(NH2)2]属于复合肥料
B. 大量施用化肥以提高农作物产量
C. 铵态氮肥与草木灰混用,会降低肥效
D. 棉花叶片枯黄,应施用硫酸钾等钾肥
C
重点1 化学方程式书写
1. 含钙化合物的转化:(如图11-F-1)
图11-F-1
2. 盐的化学性质:(如图11-F-2)
图11-F-2
Cu(OH)2↓
重点2 盐的化学性质
3. 使用如图11-F-3所示的装置(搅拌装置略)探究溶液离子浓度变化,已知反应产物全部是沉淀(或沉淀和水)时灯光变暗。下列灯光变化可能出现“亮→暗(或灭)→亮”现象的是( D )
D
图11-F-3
选 项 A B C D
试剂a NaCl K2CO3 HCl H2SO4
试剂b AgNO3 HNO3 NaOH Ba(OH)2
4. 归纳和总结是学习化学的重要方法。小李同学在复习单质、氧化物、酸、碱和盐的化学性质时,发现许多不同类别的物质反应都能生成盐,于是他构建了如图11-F-4甲所示的知识网络图。
图11-F-4
(1)图中①处可填入的内容是 酸+盐(或金属+盐) (不能与图中已有的信息重复)。
酸+盐(或金属+盐)
图11-F-4
(3)掌握了物质的化学性质,老师带领大家设计了一款新游戏——“化学棋”。游戏规则:①每粒棋子代表一种物质;②吃子:所选棋子能与棋盘(如图11-F-4乙)中的某棋子发生反应,则棋盘中的该棋子被吃掉;
图11-F-4
③连吃:前一次反应的生成物能与另一个棋子发生反应时,则该棋子也被吃掉。若小李想用一颗棋子连续吃掉棋盘上的所有棋子,应选择的棋子是 B (填字母)。
B
重点3 化学肥料种类、作用与鉴别
5. 如图11-F-5是根据组成元素对化学肥料的分类图。下列叙述错误的是( B )
图11-F-5
B
A. 氨水(NH3·H2O)属于氮肥
B. 氯化钾属于钾肥,可大量施用
C. 图中①表示的是磷肥
D. 图中②表示的是复合肥
6. 实验室有三瓶化肥未贴标签,只知道它们分别是NH4HCO3、NH4Cl和CO(NH2)2中的一种。为鉴别这三瓶化肥,某同学分别取少量样品编号为A、B、C,并进行如图11-F-6所示实验。
图11-F-6
(1)写出三种化肥的名称:A 尿素 ;B 碳酸氢 ;C 氯化铵 。
(2)如果操作Ⅱ中B、C两种样品没有另取,对实验结果 无 (填“有”或“无”)影响。
(3)常温下如果要鉴别B、C两种样品, 能 (填“能”或“不能”)采取闻气味的方法。
尿素
碳酸氢铵
氯化铵
无
能
重点4 复分解反应及其应用
7. 下列四组实验均是向盛有不同物质的烧杯中逐滴加入X溶液至过量。生成沉淀或气体的质量与加入X溶液的质量关系,符合图11-F-7所示的图像的是( D )
D
图11-F-7
选项 烧杯中的物质 X溶液
A CuSO4和Na2SO4溶液 NaOH溶液
B 铜锌合金 稀H2SO4
C 稀HNO3和稀H2SO4 BaCl2溶液
D NaOH和Na2CO3溶液 稀盐酸
8. 下列各组溶液,不用其他试剂就不能鉴别出来的是( C )
A. NaOH、KCl、稀硝酸、FeCl3
B. 稀盐酸、KNO3、Na2CO3、Ca(NO3)2
C. Na2SO4、BaCl2、Na2CO3、NaCl
D. BaCl2、MgSO4、稀硝酸、NaOH
C
重点5 粗盐提纯
9. “粗盐中难溶性杂质的去除”实验中,称取5.0 g粗盐,溶解后剩余1.0 g,经过过滤、蒸发得到3.0 g精盐,下列有关该实验的说法错误的是( C )
A. 得到的精盐为混合物
B. 使用次数最多的仪器是玻璃棒
C. 该实验得到的精盐产率为60%
D. 蒸发后,所得精盐潮湿,会导致产率偏高
C
10. 某食盐样品中含有少量沙土、CaCl2和MgCl2。如图11-F-8所示是除去食盐样品中沙土、CaCl2和MgCl2的实验流程。
图11-F-8
(1)操作Ⅰ的名称是 过滤 ,加入的试剂A是 Na2CO3 (填化学式,下同),沉淀是 CaCO3 。
(3)加入试剂B的目的是 除去过量的NaOH和Na2C 。
过滤
Na2CO3
CaCO3
2NaOH+
除去过量的NaOH和Na2CO3
(4)蒸发结晶时用到玻璃棒的作用是 搅拌,防止局部温度过高造成液滴飞溅
搅拌,防止局部
温度过高造成液滴飞溅
谢 谢!
同课章节目录
