人教版九年级化学 第十一单元 (一)酸、碱、盐化学性质归纳课件(共30张PPT)
文档属性
| 名称 | 人教版九年级化学 第十一单元 (一)酸、碱、盐化学性质归纳课件(共30张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-07 00:00:00 | ||
图片预览





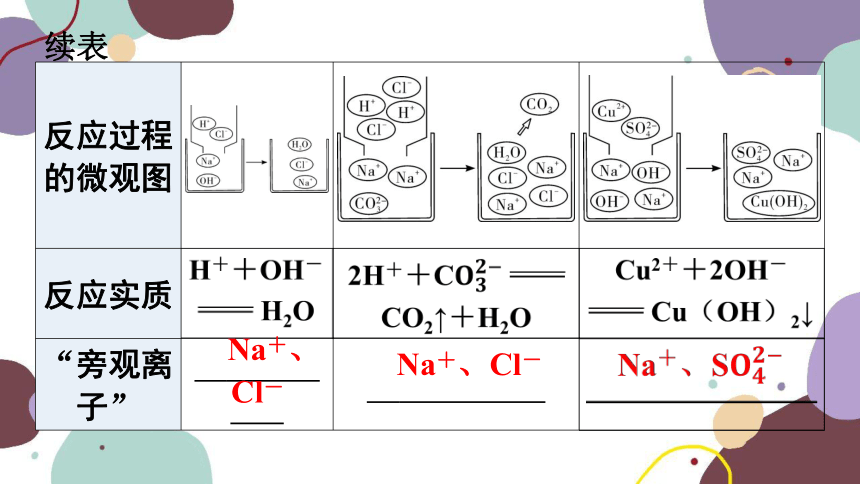


文档简介
(共30张PPT)
酸、碱、盐专题复习
(一)酸、碱、盐化学性质归纳
目录
01
知识点精讲
02
课堂检测
知识点1 酸、碱、盐的化学性质
1. 酸的化学性质:酸能和 酸碱指示剂 、 活泼金属 、 金属氧化物 、 碱 、 盐 反应。
2. 碱的化学性质:碱能和 酸碱指示剂 、 部分非金属氧化物 、 酸 、 盐 反应。
3. 盐的化学性质:盐能和 金属 、 酸 、 碱 、 盐 反应。
酸碱指示剂
活泼金
属
金属氧化物
碱
盐
酸碱指示剂
部分非金
属氧化物
酸
盐
金
属
酸
碱
盐
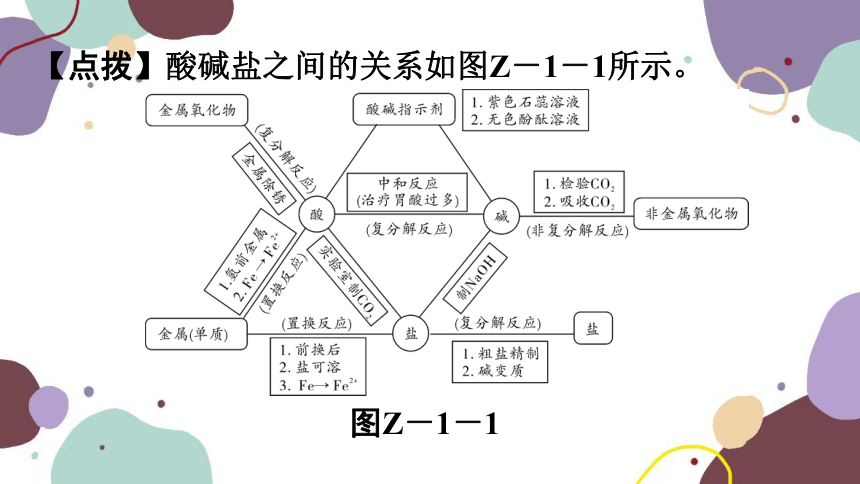
【点拨】酸碱盐之间的关系如图Z-1-1所示。
图Z-1-1
课堂练习
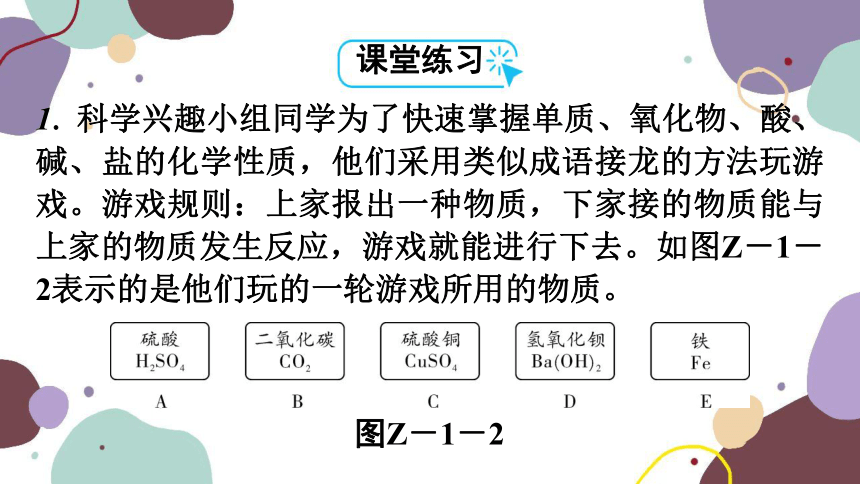
1. 科学兴趣小组同学为了快速掌握单质、氧化物、酸、碱、盐的化学性质,他们采用类似成语接龙的方法玩游戏。游戏规则:上家报出一种物质,下家接的物质能与上家的物质发生反应,游戏就能进行下去。如图Z-1-2表示的是他们玩的一轮游戏所用的物质。
图Z-1-2
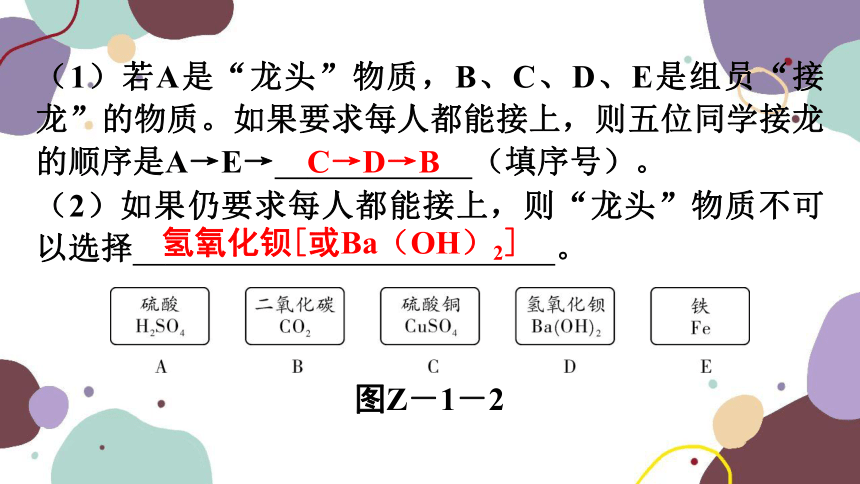
(1)若A是“龙头”物质,B、C、D、E是组员“接龙”的物质。如果要求每人都能接上,则五位同学接龙的顺序是A→E→ C→D→B (填序号)。
(2)如果仍要求每人都能接上,则“龙头”物质不可以选择 氢氧化钡[或Ba(OH)2] 。
C→D→B
氢氧化钡[或Ba(OH)2]
图Z-1-2
思路点拨 中考对酸、碱、盐化学性质的考查是重中之重,学生要熟记酸的五条化学性质、碱和盐的四条化学性质。
知识点2 从微观角度看复分解反应的实质
4. 复分解反应发生的条件:两种化合物互相交换成分,生成物中有 水 或有 气体 或有 沉淀 生成。
水
气体
沉淀
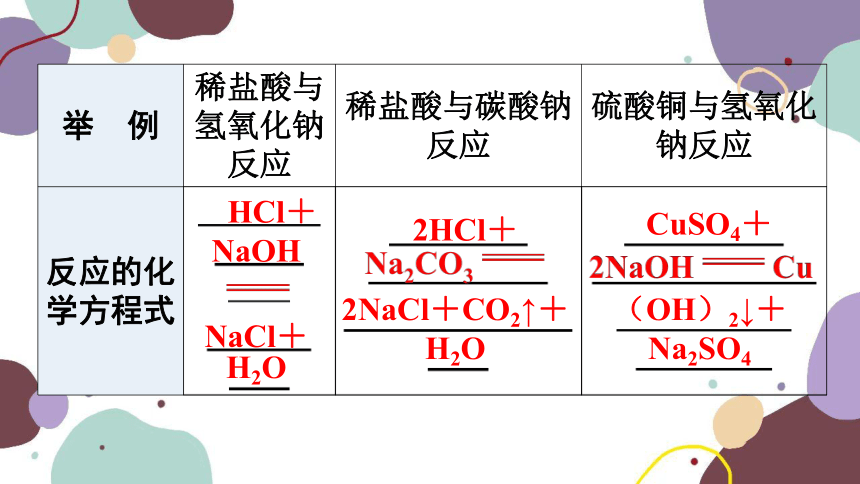
举 例 稀盐酸与氢氧化钠反应 稀盐酸与碳酸钠反应 硫酸铜与氢氧化钠反应
反应的化学方程式
HCl+
NaOH
NaCl+
H2O
2HCl+
2NaCl+CO2↑+
H2O
CuSO4+
(OH)2↓+
Na2SO4
反应过程的微观图
反应实质
“旁观离子” Na+、Cl- Na+、Cl-
Na+、
Cl-
Na+、Cl-
续表
【小结】酸、碱、盐之间发生复分解反应的实质是离子之间的反应,两种离子之间如果能结合生成水或生成气体或生成沉淀,反应就能发生。
【归纳总结】近几年各地的中考试题中经常出现“物质共存”“离子共存”的题型,对于物质在溶液中的共存,从实质上来讲也就是构成物质的离子间的共存。初中部分只需掌握复分解反应中的离子共存问题,即同一溶液中如离子之间符合下列三个条件之一就会发生离子反应,离子之间便不能在溶液中共存。
(1)常见不能共存的离子对:
②碱性溶液中不存在与OH-起反应的离子;酸性溶液中肯定不存在与H+起反应的离子。酸性溶液、pH=1的溶液、能使pH试纸变红的溶液、使紫色石蕊溶液变红等,在分析各选项组的离子时,还需考虑H+的存在;碱性溶液、pH=14的溶液、能使pH试纸变蓝的溶液,使紫色石蕊溶液变蓝或使酚酞溶液变红的溶液等,在分析各选项组的离子时,还需考虑OH-的存在。
③能与金属反应产生H2的溶液,在分析离子时,还需考虑H+或OH-的存在。
课堂练习
2. 如图Z-1-3是某同学在学习酸和碱之间的反应后画出的NaOH溶液与稀盐酸恰好完全反应的微观示意图。由此得出的结论正确的是( D )
图Z-1-3
D
A. 反应后溶液中的粒子只有Na+、Cl-
B. 反应前后阴、阳离子的总数不变
D. 该反应属于复分解反应,反应后溶剂质量增加
3. 在pH=2的无色溶液中,下列离子能大量共存的是( B )
B
思路点拨 (1)分析问题时还要看清楚题目要求回答的是能大量共存还是不能大量共存,不要选出相反的答案。(2)具体到题目中,可能是这些条件之一,也可能是这些条件的组合,分析问题时,要逐一找出,同时满足要求,才能作出正确答案。
1. 某同学进行酸碱盐性质实验如图Z-1-4所示,在图甲反应后的混合物中滴入NaOH溶液后,生成沉淀的质量和加入NaOH溶液的质量关系如图乙所示。以下分析不正确的是( D )
D
图Z-1-4
A. ab段一定发生HCl与NaOH的反应
B. bc段发生的是过量的CuSO4与NaOH的反应
C. bc段试管中有两种不同颜色的沉淀
D. c点溶液的溶质一定含有NaCl,可能含有BaCl2
2. 下列各组物质能相互反应且反应后溶液总质量减少的是( A )
A. 铁和硫酸铜溶液
B. 氢氧化钙溶液和稀盐酸
C. 碳酸钠粉末和稀硫酸
D. 氯化钡溶液和硝酸钾溶液
A
3. 能在同一溶液中大量共存,且溶液无色透明的一组物质是( C )
A. Fe2 (SO4)3、NaCl、Zn(NO3)2
B. MgCl2、Na2SO4、NaOH
C. CaCl2、NaNO3、Ba(NO3)2
D. H2SO4、NaNO3、NaHCO3
C
4. 化学小组的同学用思维导图绘制出了酸、碱、盐的化学性质及相互反应关系图Z-1-5(每一个反应表示酸、碱、盐不同的化学性质),据此回答下列问题。
图Z-1-5
(1)图中A、B处是初中化学常见的物质,它们分别为 Fe、CO2(合理即可) (填化学式)。
Fe、CO2(合理即
可)
Fe2O3+
(3)反应③无明显现象,可向反应后的溶液中加入 CuSO4 ,若无沉淀产生,证明酸碱发生了反应。
CuSO4
图Z-1-5
(4)反应⑨体现了碳酸钠的一条化学性质,反应过程中一定能观察到的现象是 有白色沉淀生成 。
有白色沉淀生成
图Z-1-5
5. 查阅资料:复分解反应发生的实质是溶液中的一些阴、阳离子结合生成沉淀或气体或水。
(1)图Z-1-6甲反应的实质是 H+ (填离子符号,下同)和 OH- 结合生成水分子。
H+
OH-
图Z-1-6
(2)图Z-1-6乙是向Na2CO3溶液中滴入Ba(NO3)2溶液至恰好完全反应前后溶液中的主要离子。
图Z-1-6
BaCO3↓+2NaNO3
产生白色沉淀
Na+
Ba2+
BaCO3
A. NaOH B. HCl
C. BaCl2 D. Ba(OH)2
③下列物质能与Na2CO3溶液反应,且反应实质与图乙反应相同的是 CD (填字母,多选)。
CD
谢 谢!
酸、碱、盐专题复习
(一)酸、碱、盐化学性质归纳
目录
01
知识点精讲
02
课堂检测
知识点1 酸、碱、盐的化学性质
1. 酸的化学性质:酸能和 酸碱指示剂 、 活泼金属 、 金属氧化物 、 碱 、 盐 反应。
2. 碱的化学性质:碱能和 酸碱指示剂 、 部分非金属氧化物 、 酸 、 盐 反应。
3. 盐的化学性质:盐能和 金属 、 酸 、 碱 、 盐 反应。
酸碱指示剂
活泼金
属
金属氧化物
碱
盐
酸碱指示剂
部分非金
属氧化物
酸
盐
金
属
酸
碱
盐
【点拨】酸碱盐之间的关系如图Z-1-1所示。
图Z-1-1
课堂练习
1. 科学兴趣小组同学为了快速掌握单质、氧化物、酸、碱、盐的化学性质,他们采用类似成语接龙的方法玩游戏。游戏规则:上家报出一种物质,下家接的物质能与上家的物质发生反应,游戏就能进行下去。如图Z-1-2表示的是他们玩的一轮游戏所用的物质。
图Z-1-2
(1)若A是“龙头”物质,B、C、D、E是组员“接龙”的物质。如果要求每人都能接上,则五位同学接龙的顺序是A→E→ C→D→B (填序号)。
(2)如果仍要求每人都能接上,则“龙头”物质不可以选择 氢氧化钡[或Ba(OH)2] 。
C→D→B
氢氧化钡[或Ba(OH)2]
图Z-1-2
思路点拨 中考对酸、碱、盐化学性质的考查是重中之重,学生要熟记酸的五条化学性质、碱和盐的四条化学性质。
知识点2 从微观角度看复分解反应的实质
4. 复分解反应发生的条件:两种化合物互相交换成分,生成物中有 水 或有 气体 或有 沉淀 生成。
水
气体
沉淀
举 例 稀盐酸与氢氧化钠反应 稀盐酸与碳酸钠反应 硫酸铜与氢氧化钠反应
反应的化学方程式
HCl+
NaOH
NaCl+
H2O
2HCl+
2NaCl+CO2↑+
H2O
CuSO4+
(OH)2↓+
Na2SO4
反应过程的微观图
反应实质
“旁观离子” Na+、Cl- Na+、Cl-
Na+、
Cl-
Na+、Cl-
续表
【小结】酸、碱、盐之间发生复分解反应的实质是离子之间的反应,两种离子之间如果能结合生成水或生成气体或生成沉淀,反应就能发生。
【归纳总结】近几年各地的中考试题中经常出现“物质共存”“离子共存”的题型,对于物质在溶液中的共存,从实质上来讲也就是构成物质的离子间的共存。初中部分只需掌握复分解反应中的离子共存问题,即同一溶液中如离子之间符合下列三个条件之一就会发生离子反应,离子之间便不能在溶液中共存。
(1)常见不能共存的离子对:
②碱性溶液中不存在与OH-起反应的离子;酸性溶液中肯定不存在与H+起反应的离子。酸性溶液、pH=1的溶液、能使pH试纸变红的溶液、使紫色石蕊溶液变红等,在分析各选项组的离子时,还需考虑H+的存在;碱性溶液、pH=14的溶液、能使pH试纸变蓝的溶液,使紫色石蕊溶液变蓝或使酚酞溶液变红的溶液等,在分析各选项组的离子时,还需考虑OH-的存在。
③能与金属反应产生H2的溶液,在分析离子时,还需考虑H+或OH-的存在。
课堂练习
2. 如图Z-1-3是某同学在学习酸和碱之间的反应后画出的NaOH溶液与稀盐酸恰好完全反应的微观示意图。由此得出的结论正确的是( D )
图Z-1-3
D
A. 反应后溶液中的粒子只有Na+、Cl-
B. 反应前后阴、阳离子的总数不变
D. 该反应属于复分解反应,反应后溶剂质量增加
3. 在pH=2的无色溶液中,下列离子能大量共存的是( B )
B
思路点拨 (1)分析问题时还要看清楚题目要求回答的是能大量共存还是不能大量共存,不要选出相反的答案。(2)具体到题目中,可能是这些条件之一,也可能是这些条件的组合,分析问题时,要逐一找出,同时满足要求,才能作出正确答案。
1. 某同学进行酸碱盐性质实验如图Z-1-4所示,在图甲反应后的混合物中滴入NaOH溶液后,生成沉淀的质量和加入NaOH溶液的质量关系如图乙所示。以下分析不正确的是( D )
D
图Z-1-4
A. ab段一定发生HCl与NaOH的反应
B. bc段发生的是过量的CuSO4与NaOH的反应
C. bc段试管中有两种不同颜色的沉淀
D. c点溶液的溶质一定含有NaCl,可能含有BaCl2
2. 下列各组物质能相互反应且反应后溶液总质量减少的是( A )
A. 铁和硫酸铜溶液
B. 氢氧化钙溶液和稀盐酸
C. 碳酸钠粉末和稀硫酸
D. 氯化钡溶液和硝酸钾溶液
A
3. 能在同一溶液中大量共存,且溶液无色透明的一组物质是( C )
A. Fe2 (SO4)3、NaCl、Zn(NO3)2
B. MgCl2、Na2SO4、NaOH
C. CaCl2、NaNO3、Ba(NO3)2
D. H2SO4、NaNO3、NaHCO3
C
4. 化学小组的同学用思维导图绘制出了酸、碱、盐的化学性质及相互反应关系图Z-1-5(每一个反应表示酸、碱、盐不同的化学性质),据此回答下列问题。
图Z-1-5
(1)图中A、B处是初中化学常见的物质,它们分别为 Fe、CO2(合理即可) (填化学式)。
Fe、CO2(合理即
可)
Fe2O3+
(3)反应③无明显现象,可向反应后的溶液中加入 CuSO4 ,若无沉淀产生,证明酸碱发生了反应。
CuSO4
图Z-1-5
(4)反应⑨体现了碳酸钠的一条化学性质,反应过程中一定能观察到的现象是 有白色沉淀生成 。
有白色沉淀生成
图Z-1-5
5. 查阅资料:复分解反应发生的实质是溶液中的一些阴、阳离子结合生成沉淀或气体或水。
(1)图Z-1-6甲反应的实质是 H+ (填离子符号,下同)和 OH- 结合生成水分子。
H+
OH-
图Z-1-6
(2)图Z-1-6乙是向Na2CO3溶液中滴入Ba(NO3)2溶液至恰好完全反应前后溶液中的主要离子。
图Z-1-6
BaCO3↓+2NaNO3
产生白色沉淀
Na+
Ba2+
BaCO3
A. NaOH B. HCl
C. BaCl2 D. Ba(OH)2
③下列物质能与Na2CO3溶液反应,且反应实质与图乙反应相同的是 CD (填字母,多选)。
CD
谢 谢!
同课章节目录
