第一章 第一节 第1课时 物质的分类及胶体
文档属性
| 名称 | 第一章 第一节 第1课时 物质的分类及胶体 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-07 00:00:00 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
第一章 第一节 物质的分类及转化
第1课时 物质的分类及胶体
【学习目标】
1.学会根据物质的组成和性质对物质进行分类,了解分散系的分类方法。
2.学会制备氢氧化铁胶体。
【素养目标】
1.通过从物质微观粒子的组成和性质角度进行物质分类,培养学生“宏观辨识与微观探析”的学科核心素养。
2.通过Fe(OH)3胶体的实验制备和性质探究,培养“科学态度与科学探究”的学科核心素养。
必备知识与关键能力
知识点一:物质的组成和性质分类
1.物质的组成
(1)元素与物质的组成
①元素:具有相同核电荷数的一类原子的总称。
②物质:宏观上物质是由元素组成的,微观上物质是由分子、原子或离子构成的。
(2)纯净物和混合物的辨析
①纯净物:由同种单质或化合物组成的物质。
②混合物:由几种不同的单质或化合物组成的物质。
(3)同素异形体的解读
①概念:同种元素形成的不同单质叫同素异形体。
②形成方式
原子个数不同 如O2和O3
原子排列方式不同 如金刚石和石墨
③性质差异:物理性质差别较大,同素异形体之间的转化属于化学变化。
【点拨】(1)由同种元素组成的物质不一定是纯净物。若某物质是由一种元素组成的不同单质混合而成,如O2、O3组成的混合气体就是混合物。
(2)由同位素的不同原子构成的单质(或化合物)是纯净物,如H2和D2、H2O和D2O,由12C和13C组成的石墨也是纯净物。
(3)冰水混合物、结晶水合物(如CuSO4·5H2O)属于纯净物而不是混合物;高分子化合物(如聚乙烯?CH2—CH2?)属于混合物而不是纯净物。
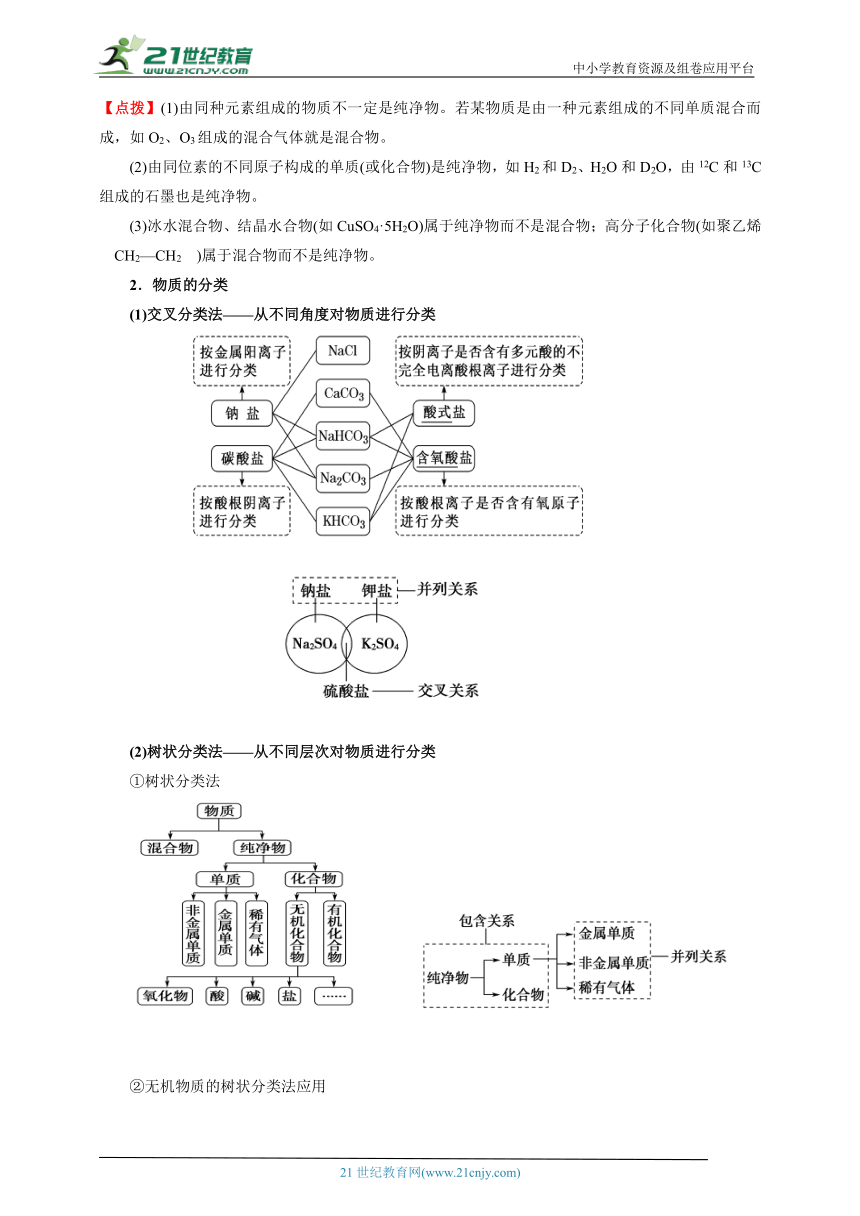
2.物质的分类
(1)交叉分类法——从不同角度对物质进行分类
(2)树状分类法——从不同层次对物质进行分类
①树状分类法
②无机物质的树状分类法应用
【点拨】 有关氧化物的易错点
①金属氧化物不一定是碱性氧化物,如Mn2O7是酸性氧化物,Al2O3是两性氧化物。
②非金属氧化物不一定是酸性氧化物,如NO、CO是不成盐氧化物。
③酸性氧化物不一定是非金属氧化物,如Mn2O7是金属氧化物。
④碱性氧化物都是金属氧化物。
⑤酸性氧化物、碱性氧化物不一定能与水反应生成相应的酸或碱,如SiO2、Fe2O3都不溶于水,也不与水反应。
⑥与碱反应生成盐和水的氧化物不一定是酸性氧化物,如2NO2+2NaOH===NaNO3+NaNO2+H2O,NO2不是酸性氧化物。
典例1.下列物质分类正确的是( )
选项 酸性氧化物 碱性氧化物 酸 碱 盐
A CO2 Mn2O7 H2SO4 KOH NaHCO3
B CO Na2O HCl NaOH NaCl
C SO2 CuO CH3COOH Na2CO3 CaF2
D SO3 CaO HNO3 Ca(OH)2 CaCO3
【答案】D
【解析】Mn2O7为酸性氧化物,A项错误;CO既不能与酸反应生成盐和水,又不能与碱反应生成盐和水,属于不成盐氧化物,B项错误;Na2CO3是盐,C项错误。
典例2.如图表示的一些物质或概念间的从属关系不正确的是( )
A.X为含氧酸、Y为酸、Z为化合物
B.X为氧化物、Y为化合物、Z为纯净物
C.X为强碱、Y为碱、Z为化合物
D.X为非金属氧化物、Y为酸性氧化物、Z为氧化物
【答案】D
【解析】化合物可以分为酸、碱、盐、氧化物等,按分子组成中是否含氧元素,酸可分为含氧酸和无氧酸,A项正确;纯净物分为单质和化合物,化合物可以分为酸、碱、盐、氧化物等,B项正确;化合物可以分为酸、碱、盐、氧化物等,按解离程度不同,碱可分为强碱、弱碱等,C项正确;氧化物可以分为酸性氧化物、碱性氧化物、两性氧化物、不成盐氧化物,酸性氧化物不一定是非金属氧化物(如Mn2O7等),非金属氧化物也不一定是酸性氧化物(如CO等),酸性氧化物和非金属氧化物属于交叉关系,D项错误。
知识点二:分散系及胶体
1.分散系
(1)概念:把一种(或多种)物质以粒子形式分散到另一种(或多种)物质中所形成的混合物。
(2)分类
①若按分散质或分散剂的状态分类,可分为9种分散系,如图:
烟属于固气分散系;雾属于液气分散系;
悬浊液属于固液分散系;合金属于固固分散系。
②根据分散质粒子的直径大小将分散系分为溶液、浊液和胶体,可用如下直观地表示。
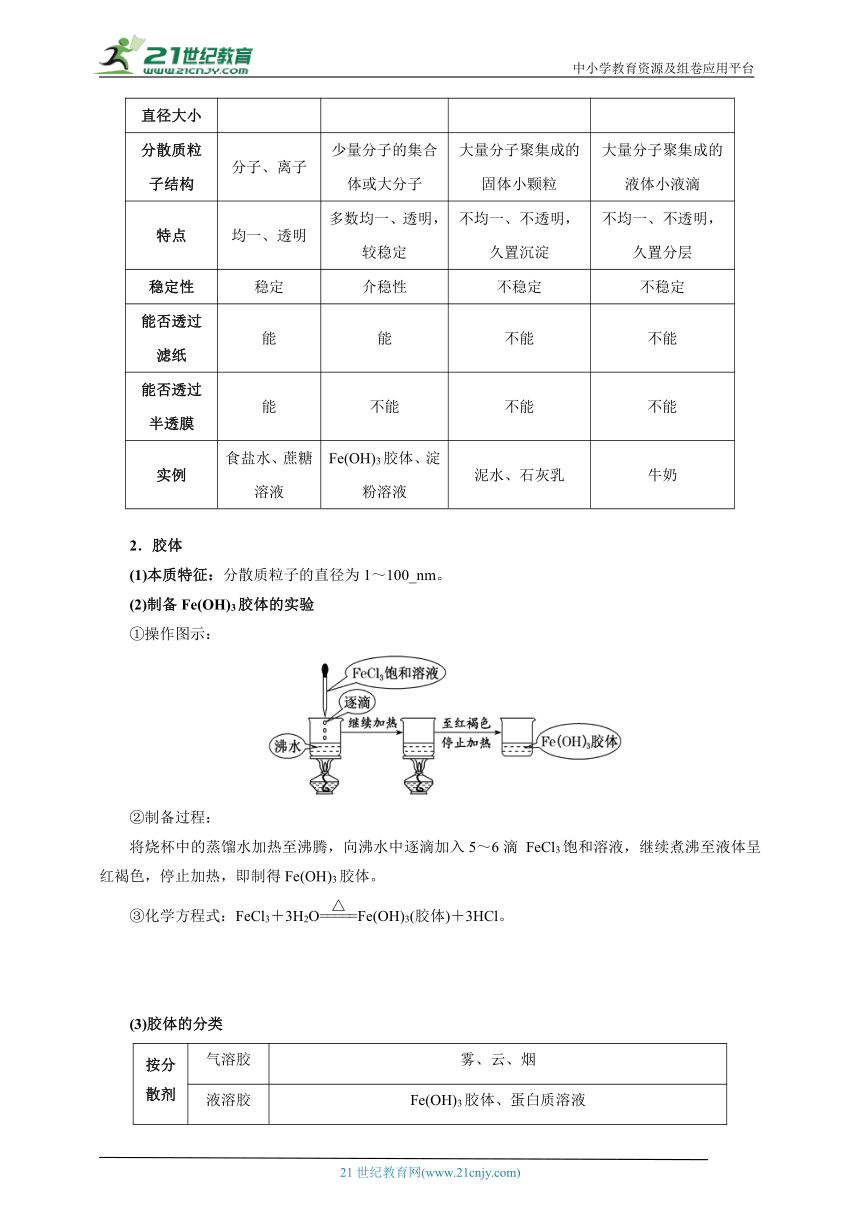
(3)三种分散系的比较
分散系 溶液 胶体 浊液
悬浊液 乳浊液
分散质粒子 直径大小 <1 nm 1~100 nm >100 nm >100 nm
分散质粒 子结构 分子、离子 少量分子的集合体或大分子 大量分子聚集成的固体小颗粒 大量分子聚集成的液体小液滴
特点 均一、透明 多数均一、透明,较稳定 不均一、不透明,久置沉淀 不均一、不透明,久置分层
稳定性 稳定 介稳性 不稳定 不稳定
能否透过 滤纸 能 能 不能 不能
能否透过 半透膜 能 不能 不能 不能
实例 食盐水、蔗糖溶液 Fe(OH)3胶体、淀粉溶液 泥水、石灰乳 牛奶
2.胶体
(1)本质特征:分散质粒子的直径为1~100_nm。
(2)制备Fe(OH)3胶体的实验
①操作图示:
②制备过程:
将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴 FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热,即制得Fe(OH)3胶体。
③化学方程式:FeCl3+3H2OFe(OH)3(胶体)+3HCl。
(3)胶体的分类
按分散剂状态 气溶胶 雾、云、烟
液溶胶 Fe(OH)3胶体、蛋白质溶液
固溶胶 烟水晶、有色玻璃
按分散质 粒子胶体 分散质粒子是很多小分子或离子的集合体,如Fe(OH)3胶体
分子胶体 分散质粒子是高分子化合物,如淀粉溶液、蛋白质溶液
(4)胶体的性质及应用
内容 主要应用举例
性 质 丁达尔效应 胶体粒子对可见光的散射而产生的,是一种物理现象 鉴别胶体与溶液
介稳性 胶体的稳定性介于溶液和浊液之间,在一定条件下相对稳定 生产涂料、颜料、墨水、洗涤剂等
电泳 胶体粒子在外加电场作用下做定向移动 静电除尘、电泳、电镀等
聚沉 胶体粒子聚集成较大的颗粒形成沉淀 明矾净水、制豆腐、制肥皂等
提纯 渗析 胶体粒子较大不能通过半透膜,而离子、小分子较小可通过半透膜,用此法将胶体提纯 用于胶体的提纯、血液透析
典例3.有下列分散系:①饱和食盐水 ②食醋 ③雾 ④云 ⑤淀粉溶液⑥血液 ⑦泥水 ⑧烟水晶 ⑨有色玻璃 ⑩石灰乳 豆浆 牛奶
请思考回答下列问题:
(1)上述分散系中属于溶液的有________(填序号,下同),属于浊液的有________,属于胶体的有________。
(2)分散系②⑤⑥⑦⑩中分散质能透过滤纸的有 。
(3)上述分散系是气溶胶的有 ,固溶胶的有 。
(4)证明淀粉溶液是胶体的方法叫做______________。
【答案】 (1)①② ⑦⑩ ③④⑤⑥⑧⑨ (2)②⑤⑥ (3)③④ ⑧⑨ (4)丁达尔效应
典例4.FeCl3溶液、Fe(OH)3胶体、Fe(OH)3浊液是三种重要的分散系,下列叙述中错误的是( )
A.Fe(OH)3胶体区别于其他分散系的本质特征是分散质粒子的直径在1~100 nm之间
B.分别用一束光透过三种分散系,只有Fe(OH)3胶体具有丁达尔效应
C.三种分散系的颜色都相同,且均能与盐酸反应,具有吸附性
D.三种分散系均属于混合物
【答案】D
【解析】A项,胶体区别于溶液或浊液的本质特征是胶体粒子的直径在1~100 nm之间,正确;B项,胶体能产生丁达尔效应,溶液和浊液不会产生丁达尔效应,正确;C项,只有胶体具有吸附性,FeCl3溶液和Fe(OH)3浊液没有吸附性,FeCl3溶液为棕黄色,而Fe(OH)3胶体和Fe(OH)3浊液都为红褐色,错误;D项,溶液、胶体、浊液均属于混合物,正确。
核心价值与学科素养
典例5. 2019年12月以来,我国部分地区突发的新型冠状病毒肺炎威胁着人们的身体健康。“84”消毒液(主要成分为NaClO)是人们常用的消毒剂。下列关于“84”消毒液及其主要成分的说法正确的是( )
A.“84”消毒液是纯净物 B.NaClO属于氧化物
C.NaClO属于盐 D.NaClO属于碱
【答案】C
【解析】“84”消毒液的主要成分为NaClO,NaClO属于盐。
典例6.国家质检部门检测出端午节包粽子的“返青粽叶”多以胆矾(化学式为CuSO4·5H2O)为添加剂,长期食用有害健康。胆矾是一种( )
A.氧化物 B.盐 C.碱 D.酸
【答案】B
【解析】胆矾、绿矾(FeSO4·7H2O)等结晶水合物都属于盐,为纯净物。
典例7.科学家发现C60后,近年又合成了许多球形分子(富勒烯),如C50、C70、C120、C540等,它们之间的关系是( )
A.同一物质 B.同种化合物
C.互为同素异形体 D.无法判断
【答案】C
【解析】C50、C70、C120、C540都是由碳元素组成的不同单质,它们互称为同素异形体。
典例8.我国科学家预言的T 碳(四个碳原子构成的正四面体分别取代金刚石结构中所有碳原子,如图)已在实验室成功合成。T 碳属于( )
A.混合物 B.化合物 C.氧化物 D.单质
【答案】D
【解析】该物质只由一种元素即碳元素组成,属于单质。
【跟踪练习】 基础过关
1. 按照物质的交叉分类方法判断,HNO3属于( )
①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤难挥发性酸
⑥挥发性酸 ⑦一元酸 ⑧化合物 ⑨混合物
A.②④⑤⑥⑦⑧ B.①④⑥⑦⑧
C.①③⑤⑨ D.①④⑤⑦⑧
【答案】B
【解析】HNO3属于酸、含氧酸、挥发性酸、 一元酸、化合物。
2. 朱自清在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里……月光是隔了树照过来的,高处丛生的灌木,落下参差的斑驳的黑影……”。结合这段文字及所学的化学知识判断下列说法正确的是( )
A.荷塘上方的薄雾是水蒸气
B.月光通过薄雾时产生了丁达尔效应
C.薄雾中的微观粒子直径大约是2.5 pm
D.“大漠孤烟直”中的孤烟成分和这种薄雾的成分相同
【答案】B
【解析】荷塘上方的薄雾是空气中的小液滴,不是水蒸气,薄雾属于胶体,胶体粒子的直径为1~100 nm,可以产生丁达尔效应,A、C项错误,B项正确;“大漠孤烟直”中的孤烟指的是固体小颗粒,与这种薄雾的成分不同,D项错误。
3. 纳米材料是粒子直径为1~100 nm的材料,其研究成果已应用于医学、化工、军事等领域。纳米碳就是其中的一种,若将纳米碳均匀地分散到蒸馏水中,下列有关形成的物质的判断正确的是( )
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸
⑤不能透过滤纸 ⑥静置后会析出黑色沉淀
A.①②③④ B.②③⑤⑥ C.②③④ D.②③④⑥
【答案】C
【解析】①因纳米碳其粒子直径为l~100 nm之间,纳米碳分子分散到水中,所形成的分散系为胶体分散系,不属于溶液,故①错误、②正确;③因形成的是胶体分散系,则具有丁达尔效应,故③正确;④溶液和胶体分散系中粒子的直径都比滤纸中小孔直径小,则能全部透过滤纸,故④正确;故⑤错误;⑥因形成的是胶体分散系,处于介稳定状态,则不会形成黑色沉淀,故⑥错误。
4. 关于氯化铁溶液与氢氧化铁胶体的说法正确的是( )
A.分散质微粒直径都在10 9 ~ 10 7m之间
B.都能发生丁达尔效应
C.Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的
D.都是无色透明、均一、稳定的分散系
【答案】C
【解析】A.氯化铁溶液中分散质微粒直径小于10 9 m,氢氧化铁胶体分散质微粒直径介于10 9 m~10 7m,A错误;B.氯化铁溶液无丁达尔效应,氢氧化铁胶体能产生丁达尔效应,B错误;C.Fe(OH)3胶体具有吸附性,能够吸附水中的悬浮物,可以净水,C正确;D.氯化铁溶液呈黄色,氢氧化铁胶体呈透明的红褐色,胶体属于介稳体系,D错误;答案选C。
5. 下列现象与胶体知识无关的是( )
A.向碳酸氢钠溶液中加入氯化钙溶液时溶液没有浑浊
B.夏日的傍晚常常看到万丈霞光穿云而过美不胜收
C.食品加工厂利用豆浆中加入盐卤做豆腐
D.上海宝钢厂利用静电除尘技术去除废气中的固体悬浮物
【答案】A
【解析】向碳酸氢钠溶液中加入氯化钙溶液,溶液中离子之间不发生反应,则没有浑浊,属于溶液分散系,与胶体无关,A正确;因云属于胶体分散系,则具有丁达尔现象,所以夏日的傍晚常常看到万丈霞光穿云而过美不胜收,与胶体有关,B错误;豆浆属于胶体分散系,盐卤属于电解质,食品加工厂利用豆浆中加入盐卤做豆腐是利用胶体遇电解质发生聚沉的性质,与胶体有关,C错误;废气中的固体悬浮物属于胶体分散系,胶体粒子带电,在外压的作用下发生电泳而达到工厂利用静电除尘的目的,与胶体有关,D错误;正确选项为A。
折
能力达成
6. 有人设想通过特殊的方法将碳酸钙加工成为纳米碳酸钙(即碳酸钙粒子直径达到纳米级),这将使建筑材料的性能发生巨大的变化。下列关于纳米碳酸钙的说法正确的是( )
A.纳米碳酸钙是与胶体相似的分散系
B.纳米碳酸钙分散到水中所得到的分散系会产生丁达尔效应
C.纳米碳酸钙的化学性质与原来碳酸钙完全不同
D.纳米碳酸钙粒子不能透过滤纸
【答案】B
【解析】纳米碳酸钙是纯净物,分散系是混合物,A项错误;纳米碳酸钙的化学性质与原来碳酸钙相比不会发生改变,C项错误;与胶体中的胶粒(微粒直径在10-9~10-7 m之间)能透过滤纸一样,纳米碳酸钙粒子也能透过滤纸,D项错误。
7. 向含有一定浓度的FeCl3、FeCl2的混合溶液中滴加稀NaOH溶液,可得到一种黑色分散系,其分散质粒子是直径约为9.3 nm的金属氧化物。下列有关说法正确的是( )
A.该分散系的分散质为Fe2O3
B.在电场作用下,若直流电源负极附近的液体的颜色变深,则说明该分散系带正电荷
C.该分散系能产生丁达尔效应
D.可用过滤的方法将该金属氧化物与Na+分离开。
【答案】C
【解析】Fe2O3是红色的,该金属氧化物有可能是Fe3O4,A项错误;分散系呈电中性,不带电,B项错误;该分散系是胶体,能产生丁达尔效应,C项正确;胶体中的分散质粒子和Na+都能透过滤纸,D项错误。
8. 将饱和FeCl3 溶液逐滴滴入沸水中,液体变为_________色,得到的是Fe(OH)3胶体;反应的化学方程式为 。
用此分散系进行实验:
(1)将其装入U型管内,用石墨棒做电极,接通直流电源,通电一段时间后发现阴极附近颜色____________,这表明___________________,这种现象称为_______________。
(2)向其中加入饱和的(NH4)2SO4溶液,发生的现象是_______________;原因是______________。
(3)向其中逐滴加入过量稀硫酸,现象是__________________;原因是________。
(4)提纯此分散系的方法叫________________。
【答案】红褐 FeCl3+3H2OFe(OH)3(胶体)+ 3HCl
(1)逐渐变深 Fe(OH)3胶粒带正电荷 胶体的电泳
(2)形成红褐色沉淀 硫酸铵电离出的SO42 和 Fe(OH)3胶粒所带正电荷,使微粒变大,以沉淀形式析出
(3)先出现红褐色沉淀,后沉淀消失 H2SO4电离出的SO42 使Fe(OH)3胶体发生聚沉,H+使Fe(OH)3沉淀溶解
(4)渗析
【解析】Fe(OH)3胶粒带正电荷,通电后会向阴极移动,所以阴极附近颜色逐渐变深;加入(NH4)2SO4溶液,酸铵电离出的SO42 和 Fe(OH)3胶粒所带正电荷,使微粒变大,以沉淀形式析出;加入过量稀硫酸,H2SO4电离出的SO42 使Fe(OH)3胶体发生聚沉,H+使Fe(OH)3沉淀溶解。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
第一章 第一节 物质的分类及转化
第1课时 物质的分类及胶体
【学习目标】
1.学会根据物质的组成和性质对物质进行分类,了解分散系的分类方法。
2.学会制备氢氧化铁胶体。
【素养目标】
1.通过从物质微观粒子的组成和性质角度进行物质分类,培养学生“宏观辨识与微观探析”的学科核心素养。
2.通过Fe(OH)3胶体的实验制备和性质探究,培养“科学态度与科学探究”的学科核心素养。
必备知识与关键能力
知识点一:物质的组成和性质分类
1.物质的组成
(1)元素与物质的组成
①元素:具有相同核电荷数的一类原子的总称。
②物质:宏观上物质是由元素组成的,微观上物质是由分子、原子或离子构成的。
(2)纯净物和混合物的辨析
①纯净物:由同种单质或化合物组成的物质。
②混合物:由几种不同的单质或化合物组成的物质。
(3)同素异形体的解读
①概念:同种元素形成的不同单质叫同素异形体。
②形成方式
原子个数不同 如O2和O3
原子排列方式不同 如金刚石和石墨
③性质差异:物理性质差别较大,同素异形体之间的转化属于化学变化。
【点拨】(1)由同种元素组成的物质不一定是纯净物。若某物质是由一种元素组成的不同单质混合而成,如O2、O3组成的混合气体就是混合物。
(2)由同位素的不同原子构成的单质(或化合物)是纯净物,如H2和D2、H2O和D2O,由12C和13C组成的石墨也是纯净物。
(3)冰水混合物、结晶水合物(如CuSO4·5H2O)属于纯净物而不是混合物;高分子化合物(如聚乙烯?CH2—CH2?)属于混合物而不是纯净物。
2.物质的分类
(1)交叉分类法——从不同角度对物质进行分类
(2)树状分类法——从不同层次对物质进行分类
①树状分类法
②无机物质的树状分类法应用
【点拨】 有关氧化物的易错点
①金属氧化物不一定是碱性氧化物,如Mn2O7是酸性氧化物,Al2O3是两性氧化物。
②非金属氧化物不一定是酸性氧化物,如NO、CO是不成盐氧化物。
③酸性氧化物不一定是非金属氧化物,如Mn2O7是金属氧化物。
④碱性氧化物都是金属氧化物。
⑤酸性氧化物、碱性氧化物不一定能与水反应生成相应的酸或碱,如SiO2、Fe2O3都不溶于水,也不与水反应。
⑥与碱反应生成盐和水的氧化物不一定是酸性氧化物,如2NO2+2NaOH===NaNO3+NaNO2+H2O,NO2不是酸性氧化物。
典例1.下列物质分类正确的是( )
选项 酸性氧化物 碱性氧化物 酸 碱 盐
A CO2 Mn2O7 H2SO4 KOH NaHCO3
B CO Na2O HCl NaOH NaCl
C SO2 CuO CH3COOH Na2CO3 CaF2
D SO3 CaO HNO3 Ca(OH)2 CaCO3
【答案】D
【解析】Mn2O7为酸性氧化物,A项错误;CO既不能与酸反应生成盐和水,又不能与碱反应生成盐和水,属于不成盐氧化物,B项错误;Na2CO3是盐,C项错误。
典例2.如图表示的一些物质或概念间的从属关系不正确的是( )
A.X为含氧酸、Y为酸、Z为化合物
B.X为氧化物、Y为化合物、Z为纯净物
C.X为强碱、Y为碱、Z为化合物
D.X为非金属氧化物、Y为酸性氧化物、Z为氧化物
【答案】D
【解析】化合物可以分为酸、碱、盐、氧化物等,按分子组成中是否含氧元素,酸可分为含氧酸和无氧酸,A项正确;纯净物分为单质和化合物,化合物可以分为酸、碱、盐、氧化物等,B项正确;化合物可以分为酸、碱、盐、氧化物等,按解离程度不同,碱可分为强碱、弱碱等,C项正确;氧化物可以分为酸性氧化物、碱性氧化物、两性氧化物、不成盐氧化物,酸性氧化物不一定是非金属氧化物(如Mn2O7等),非金属氧化物也不一定是酸性氧化物(如CO等),酸性氧化物和非金属氧化物属于交叉关系,D项错误。
知识点二:分散系及胶体
1.分散系
(1)概念:把一种(或多种)物质以粒子形式分散到另一种(或多种)物质中所形成的混合物。
(2)分类
①若按分散质或分散剂的状态分类,可分为9种分散系,如图:
烟属于固气分散系;雾属于液气分散系;
悬浊液属于固液分散系;合金属于固固分散系。
②根据分散质粒子的直径大小将分散系分为溶液、浊液和胶体,可用如下直观地表示。
(3)三种分散系的比较
分散系 溶液 胶体 浊液
悬浊液 乳浊液
分散质粒子 直径大小 <1 nm 1~100 nm >100 nm >100 nm
分散质粒 子结构 分子、离子 少量分子的集合体或大分子 大量分子聚集成的固体小颗粒 大量分子聚集成的液体小液滴
特点 均一、透明 多数均一、透明,较稳定 不均一、不透明,久置沉淀 不均一、不透明,久置分层
稳定性 稳定 介稳性 不稳定 不稳定
能否透过 滤纸 能 能 不能 不能
能否透过 半透膜 能 不能 不能 不能
实例 食盐水、蔗糖溶液 Fe(OH)3胶体、淀粉溶液 泥水、石灰乳 牛奶
2.胶体
(1)本质特征:分散质粒子的直径为1~100_nm。
(2)制备Fe(OH)3胶体的实验
①操作图示:
②制备过程:
将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴 FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热,即制得Fe(OH)3胶体。
③化学方程式:FeCl3+3H2OFe(OH)3(胶体)+3HCl。
(3)胶体的分类
按分散剂状态 气溶胶 雾、云、烟
液溶胶 Fe(OH)3胶体、蛋白质溶液
固溶胶 烟水晶、有色玻璃
按分散质 粒子胶体 分散质粒子是很多小分子或离子的集合体,如Fe(OH)3胶体
分子胶体 分散质粒子是高分子化合物,如淀粉溶液、蛋白质溶液
(4)胶体的性质及应用
内容 主要应用举例
性 质 丁达尔效应 胶体粒子对可见光的散射而产生的,是一种物理现象 鉴别胶体与溶液
介稳性 胶体的稳定性介于溶液和浊液之间,在一定条件下相对稳定 生产涂料、颜料、墨水、洗涤剂等
电泳 胶体粒子在外加电场作用下做定向移动 静电除尘、电泳、电镀等
聚沉 胶体粒子聚集成较大的颗粒形成沉淀 明矾净水、制豆腐、制肥皂等
提纯 渗析 胶体粒子较大不能通过半透膜,而离子、小分子较小可通过半透膜,用此法将胶体提纯 用于胶体的提纯、血液透析
典例3.有下列分散系:①饱和食盐水 ②食醋 ③雾 ④云 ⑤淀粉溶液⑥血液 ⑦泥水 ⑧烟水晶 ⑨有色玻璃 ⑩石灰乳 豆浆 牛奶
请思考回答下列问题:
(1)上述分散系中属于溶液的有________(填序号,下同),属于浊液的有________,属于胶体的有________。
(2)分散系②⑤⑥⑦⑩中分散质能透过滤纸的有 。
(3)上述分散系是气溶胶的有 ,固溶胶的有 。
(4)证明淀粉溶液是胶体的方法叫做______________。
【答案】 (1)①② ⑦⑩ ③④⑤⑥⑧⑨ (2)②⑤⑥ (3)③④ ⑧⑨ (4)丁达尔效应
典例4.FeCl3溶液、Fe(OH)3胶体、Fe(OH)3浊液是三种重要的分散系,下列叙述中错误的是( )
A.Fe(OH)3胶体区别于其他分散系的本质特征是分散质粒子的直径在1~100 nm之间
B.分别用一束光透过三种分散系,只有Fe(OH)3胶体具有丁达尔效应
C.三种分散系的颜色都相同,且均能与盐酸反应,具有吸附性
D.三种分散系均属于混合物
【答案】D
【解析】A项,胶体区别于溶液或浊液的本质特征是胶体粒子的直径在1~100 nm之间,正确;B项,胶体能产生丁达尔效应,溶液和浊液不会产生丁达尔效应,正确;C项,只有胶体具有吸附性,FeCl3溶液和Fe(OH)3浊液没有吸附性,FeCl3溶液为棕黄色,而Fe(OH)3胶体和Fe(OH)3浊液都为红褐色,错误;D项,溶液、胶体、浊液均属于混合物,正确。
核心价值与学科素养
典例5. 2019年12月以来,我国部分地区突发的新型冠状病毒肺炎威胁着人们的身体健康。“84”消毒液(主要成分为NaClO)是人们常用的消毒剂。下列关于“84”消毒液及其主要成分的说法正确的是( )
A.“84”消毒液是纯净物 B.NaClO属于氧化物
C.NaClO属于盐 D.NaClO属于碱
【答案】C
【解析】“84”消毒液的主要成分为NaClO,NaClO属于盐。
典例6.国家质检部门检测出端午节包粽子的“返青粽叶”多以胆矾(化学式为CuSO4·5H2O)为添加剂,长期食用有害健康。胆矾是一种( )
A.氧化物 B.盐 C.碱 D.酸
【答案】B
【解析】胆矾、绿矾(FeSO4·7H2O)等结晶水合物都属于盐,为纯净物。
典例7.科学家发现C60后,近年又合成了许多球形分子(富勒烯),如C50、C70、C120、C540等,它们之间的关系是( )
A.同一物质 B.同种化合物
C.互为同素异形体 D.无法判断
【答案】C
【解析】C50、C70、C120、C540都是由碳元素组成的不同单质,它们互称为同素异形体。
典例8.我国科学家预言的T 碳(四个碳原子构成的正四面体分别取代金刚石结构中所有碳原子,如图)已在实验室成功合成。T 碳属于( )
A.混合物 B.化合物 C.氧化物 D.单质
【答案】D
【解析】该物质只由一种元素即碳元素组成,属于单质。
【跟踪练习】 基础过关
1. 按照物质的交叉分类方法判断,HNO3属于( )
①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤难挥发性酸
⑥挥发性酸 ⑦一元酸 ⑧化合物 ⑨混合物
A.②④⑤⑥⑦⑧ B.①④⑥⑦⑧
C.①③⑤⑨ D.①④⑤⑦⑧
【答案】B
【解析】HNO3属于酸、含氧酸、挥发性酸、 一元酸、化合物。
2. 朱自清在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里……月光是隔了树照过来的,高处丛生的灌木,落下参差的斑驳的黑影……”。结合这段文字及所学的化学知识判断下列说法正确的是( )
A.荷塘上方的薄雾是水蒸气
B.月光通过薄雾时产生了丁达尔效应
C.薄雾中的微观粒子直径大约是2.5 pm
D.“大漠孤烟直”中的孤烟成分和这种薄雾的成分相同
【答案】B
【解析】荷塘上方的薄雾是空气中的小液滴,不是水蒸气,薄雾属于胶体,胶体粒子的直径为1~100 nm,可以产生丁达尔效应,A、C项错误,B项正确;“大漠孤烟直”中的孤烟指的是固体小颗粒,与这种薄雾的成分不同,D项错误。
3. 纳米材料是粒子直径为1~100 nm的材料,其研究成果已应用于医学、化工、军事等领域。纳米碳就是其中的一种,若将纳米碳均匀地分散到蒸馏水中,下列有关形成的物质的判断正确的是( )
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸
⑤不能透过滤纸 ⑥静置后会析出黑色沉淀
A.①②③④ B.②③⑤⑥ C.②③④ D.②③④⑥
【答案】C
【解析】①因纳米碳其粒子直径为l~100 nm之间,纳米碳分子分散到水中,所形成的分散系为胶体分散系,不属于溶液,故①错误、②正确;③因形成的是胶体分散系,则具有丁达尔效应,故③正确;④溶液和胶体分散系中粒子的直径都比滤纸中小孔直径小,则能全部透过滤纸,故④正确;故⑤错误;⑥因形成的是胶体分散系,处于介稳定状态,则不会形成黑色沉淀,故⑥错误。
4. 关于氯化铁溶液与氢氧化铁胶体的说法正确的是( )
A.分散质微粒直径都在10 9 ~ 10 7m之间
B.都能发生丁达尔效应
C.Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的
D.都是无色透明、均一、稳定的分散系
【答案】C
【解析】A.氯化铁溶液中分散质微粒直径小于10 9 m,氢氧化铁胶体分散质微粒直径介于10 9 m~10 7m,A错误;B.氯化铁溶液无丁达尔效应,氢氧化铁胶体能产生丁达尔效应,B错误;C.Fe(OH)3胶体具有吸附性,能够吸附水中的悬浮物,可以净水,C正确;D.氯化铁溶液呈黄色,氢氧化铁胶体呈透明的红褐色,胶体属于介稳体系,D错误;答案选C。
5. 下列现象与胶体知识无关的是( )
A.向碳酸氢钠溶液中加入氯化钙溶液时溶液没有浑浊
B.夏日的傍晚常常看到万丈霞光穿云而过美不胜收
C.食品加工厂利用豆浆中加入盐卤做豆腐
D.上海宝钢厂利用静电除尘技术去除废气中的固体悬浮物
【答案】A
【解析】向碳酸氢钠溶液中加入氯化钙溶液,溶液中离子之间不发生反应,则没有浑浊,属于溶液分散系,与胶体无关,A正确;因云属于胶体分散系,则具有丁达尔现象,所以夏日的傍晚常常看到万丈霞光穿云而过美不胜收,与胶体有关,B错误;豆浆属于胶体分散系,盐卤属于电解质,食品加工厂利用豆浆中加入盐卤做豆腐是利用胶体遇电解质发生聚沉的性质,与胶体有关,C错误;废气中的固体悬浮物属于胶体分散系,胶体粒子带电,在外压的作用下发生电泳而达到工厂利用静电除尘的目的,与胶体有关,D错误;正确选项为A。
折
能力达成
6. 有人设想通过特殊的方法将碳酸钙加工成为纳米碳酸钙(即碳酸钙粒子直径达到纳米级),这将使建筑材料的性能发生巨大的变化。下列关于纳米碳酸钙的说法正确的是( )
A.纳米碳酸钙是与胶体相似的分散系
B.纳米碳酸钙分散到水中所得到的分散系会产生丁达尔效应
C.纳米碳酸钙的化学性质与原来碳酸钙完全不同
D.纳米碳酸钙粒子不能透过滤纸
【答案】B
【解析】纳米碳酸钙是纯净物,分散系是混合物,A项错误;纳米碳酸钙的化学性质与原来碳酸钙相比不会发生改变,C项错误;与胶体中的胶粒(微粒直径在10-9~10-7 m之间)能透过滤纸一样,纳米碳酸钙粒子也能透过滤纸,D项错误。
7. 向含有一定浓度的FeCl3、FeCl2的混合溶液中滴加稀NaOH溶液,可得到一种黑色分散系,其分散质粒子是直径约为9.3 nm的金属氧化物。下列有关说法正确的是( )
A.该分散系的分散质为Fe2O3
B.在电场作用下,若直流电源负极附近的液体的颜色变深,则说明该分散系带正电荷
C.该分散系能产生丁达尔效应
D.可用过滤的方法将该金属氧化物与Na+分离开。
【答案】C
【解析】Fe2O3是红色的,该金属氧化物有可能是Fe3O4,A项错误;分散系呈电中性,不带电,B项错误;该分散系是胶体,能产生丁达尔效应,C项正确;胶体中的分散质粒子和Na+都能透过滤纸,D项错误。
8. 将饱和FeCl3 溶液逐滴滴入沸水中,液体变为_________色,得到的是Fe(OH)3胶体;反应的化学方程式为 。
用此分散系进行实验:
(1)将其装入U型管内,用石墨棒做电极,接通直流电源,通电一段时间后发现阴极附近颜色____________,这表明___________________,这种现象称为_______________。
(2)向其中加入饱和的(NH4)2SO4溶液,发生的现象是_______________;原因是______________。
(3)向其中逐滴加入过量稀硫酸,现象是__________________;原因是________。
(4)提纯此分散系的方法叫________________。
【答案】红褐 FeCl3+3H2OFe(OH)3(胶体)+ 3HCl
(1)逐渐变深 Fe(OH)3胶粒带正电荷 胶体的电泳
(2)形成红褐色沉淀 硫酸铵电离出的SO42 和 Fe(OH)3胶粒所带正电荷,使微粒变大,以沉淀形式析出
(3)先出现红褐色沉淀,后沉淀消失 H2SO4电离出的SO42 使Fe(OH)3胶体发生聚沉,H+使Fe(OH)3沉淀溶解
(4)渗析
【解析】Fe(OH)3胶粒带正电荷,通电后会向阴极移动,所以阴极附近颜色逐渐变深;加入(NH4)2SO4溶液,酸铵电离出的SO42 和 Fe(OH)3胶粒所带正电荷,使微粒变大,以沉淀形式析出;加入过量稀硫酸,H2SO4电离出的SO42 使Fe(OH)3胶体发生聚沉,H+使Fe(OH)3沉淀溶解。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
