人教版化学九上第六单元课题3 二氧化碳和一氧化碳(第4课时)课件(共24张PPT)
文档属性
| 名称 | 人教版化学九上第六单元课题3 二氧化碳和一氧化碳(第4课时)课件(共24张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 851.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-07 00:00:00 | ||
图片预览



文档简介
(共24张PPT)
第六单元 碳和碳的氧化物
课题3 二氧化碳和一氧化碳(第4课时)
1.关于一氧化碳和二氧化碳的叙述中,正确的是( )
A.都是无色有毒的气体
B.都能用排空气法收集
C.它们之间可以相互转化
D.都能溶于水,并能使紫色石蕊试液变红
C
2.将N2、CO、CO2的混合气体先通过足量石灰水,再通过足量灼热氧化铜,最后剩余的气体是( )
A.氮气
B.二氧化碳
C.一氧化碳
D.二氧化碳和氮气
D
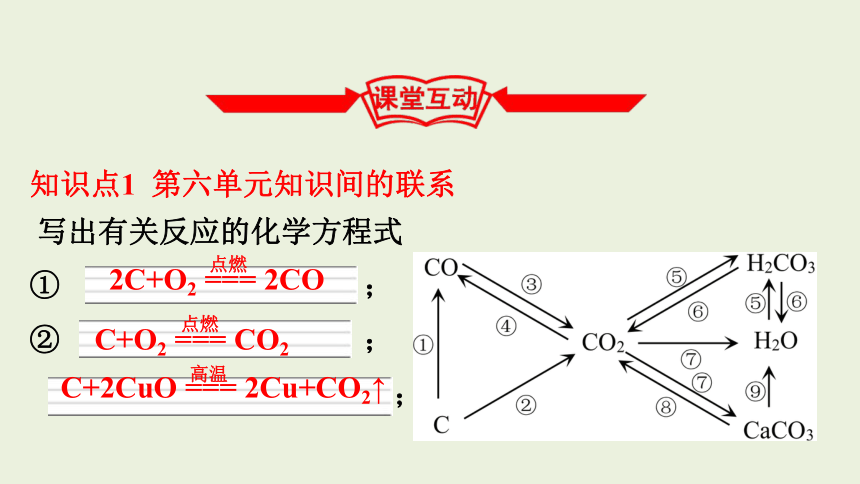
知识点1 第六单元知识间的联系
写出有关反应的化学方程式
① ;
② ;
;
C+O2 === CO2
点燃
C+2CuO === 2Cu+CO2↑
高温
2C+O2 === 2CO
点燃
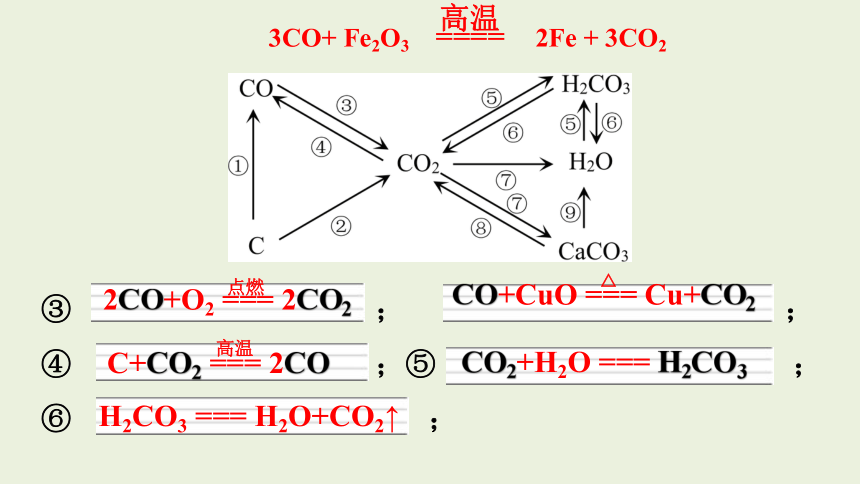
③ ; ;
④ ;⑤ ;
⑥ ;
CO2+H2O === H2CO3
H2CO3 === H2O+CO2↑
2CO+O2 === 2CO2
点燃
C+CO2 === 2CO
高温
CO+CuO === Cu+CO2
△
3CO+ Fe2O3 2Fe + 3CO2
====
高温
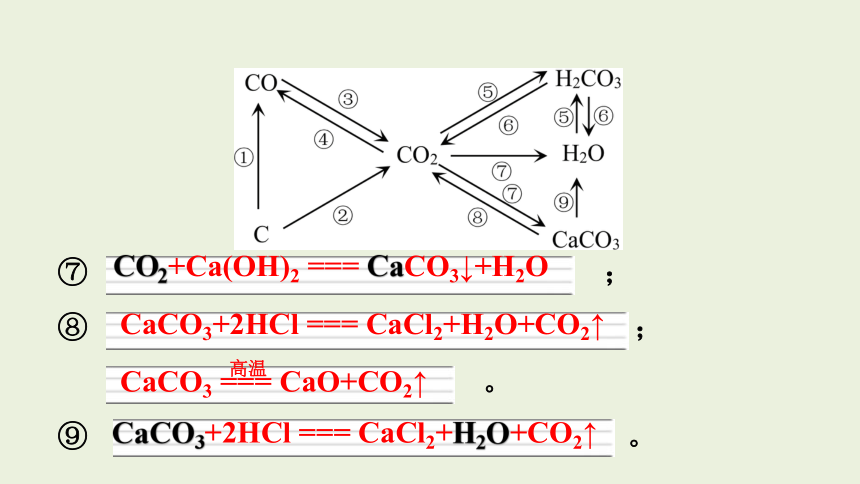
⑦ ;
⑧ ;
。
⑨ 。
CO2+Ca(OH)2 === CaCO3↓+H2O
CaCO3+2HCl === CaCl2+H2O+CO2↑
CaCO3+2HCl === CaCl2+H2O+CO2↑
CaCO3 === CaO+CO2↑
高温
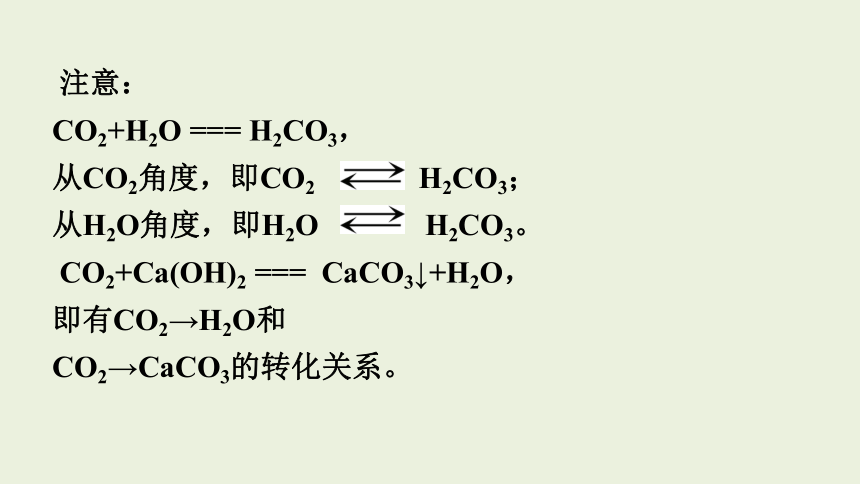
注意:
CO2+H2O === H2CO3,
从CO2角度,即CO2 H2CO3;
从H2O角度,即H2O H2CO3。
CO2+Ca(OH)2 === CaCO3↓+H2O,
即有CO2→H2O和
CO2→CaCO3的转化关系。
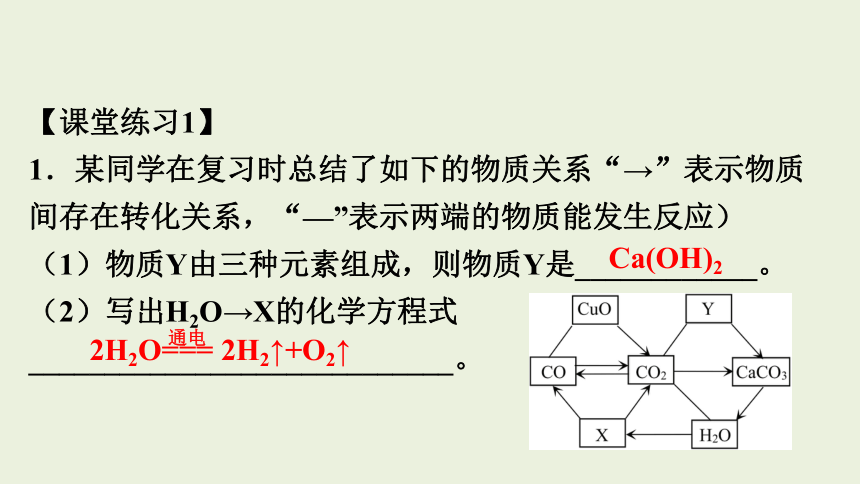
【课堂练习1】
1.某同学在复习时总结了如下的物质关系“→”表示物质间存在转化关系,“—”表示两端的物质能发生反应)
(1)物质Y由三种元素组成,则物质Y是____________。
(2)写出H2O→X的化学方程式____________________________。
Ca(OH)2
2H2O=== 2H2↑+O2↑
通电
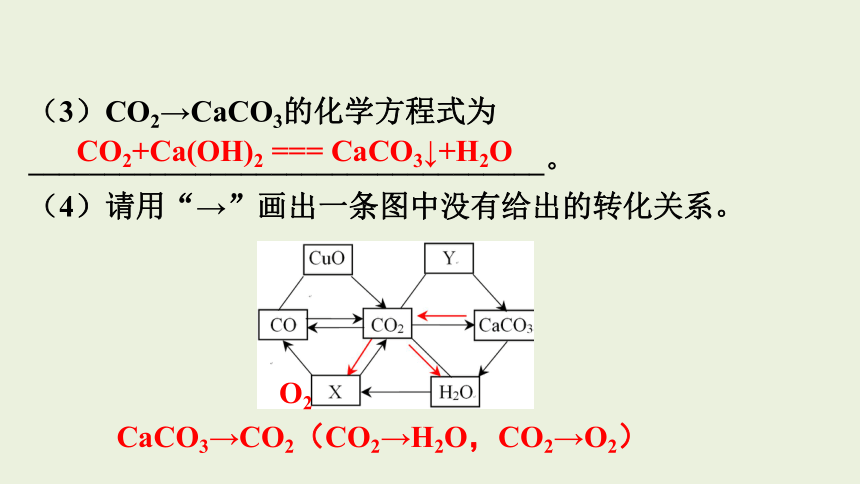
(3)CO2→CaCO3的化学方程式为__________________________________。
(4)请用“→”画出一条图中没有给出的转化关系。
CO2+Ca(OH)2 === CaCO3↓+H2O
CaCO3→CO2(CO2→H2O,CO2→O2)
O2
2.已知在常温下A为液体,B、C、F是气体;其中C是最轻的气体,F是造成温室效应的主要气体;G为黑色固体单质,H是白色不溶于水固体,它们之间的转化关系如图,回答下列问题:
H2O
H2
O2
CaCO3
CO2
CO
Cu
C
CuO
C
C
黑 C、CuO、Fe3O4、MnO2
红 Cu Fe2O3
通电 H2O
Cu
(1)写出有关物质的化学式:
C是_____;G是____;H是__________;I是______。
(2)写出下列化学方程式:
③ ;
⑤ ;
⑥ 。
H2
C
CaCO3
CO
CO2+Ca(OH)2 === CaCO3↓+H2O
C+2CuO === 2Cu+CO2↑
高温
CO+CuO === CO2+Cu
△
不增杂
不伤主
易分离
不增、不减、易分离
除杂
除去CO 中的CO2最合理的方法是
石灰水
CO2和CO
让混合气体通过澄清的石灰水
让混合气体通过通过灼热的碳层
一般不宜用水除去CO中的CO2,溶解于水中的CO2的量不多,且CO2与水反应生成的碳酸不稳定,易分解。
CO2 + Ca(OH)2 =CaCO3↓+ H2O
CO2+C 2CO
高温
CO
除去CO2 中的CO最合理的方法是____________
化学方程式________________________
通过灼热的氧化铜
不能通过点燃除去因为气体中如果含有大量的CO2的话,是无法点燃的,而且无法确定混入其中的O2恰好反应,带入新的杂质。
知识点2 气体的提纯
被提纯物质 杂质 方法或操作 化学方程式
二氧化碳 氧气
一氧化碳 二氧化碳
二氧化碳 一氧化碳
通过灼热
的铜网
CO2+Ca(OH)2 ===
CaCO3↓+H2O
通过足量的
澄清石灰水
通过灼热的
氧化铜
2Cu+O2 === 2CuO
△
CO+CuO === Cu+CO2
△
【课堂练习2】
1.除去CO2中混有少量O2的最佳方法是( )
A.点燃 B.通过灼热的铜网
C.通过澄清石灰水 D.通过灼热的木炭层
B
2.除去二氧化碳中混有的少量一氧化碳,可采用的方法是( )
A.通过澄清石灰水 B.用燃着的木条点燃
C.通过灼热木炭粉 D.通过灼热氧化铜
D
1.下列有关碳及其化合物的说法错误的是( )
A.二氧化碳的水溶液使石蕊显红色
B.干冰用于人工降雨
C.紧闭门窗用木炭烤火易使人中毒
D.金刚石导电性能良好
D
测评反馈
2.除去一氧化碳气体中混有的少量二氧化碳,可采用的方法是( )
A.把混合气体通过足量澄清的石灰水
B.把混合气体点燃
C.把混合气体通过灼热的氧化铜
D.把混合气体倾倒到另一个容器中
A
3.含碳元素的物质间发生转化:C→CO→CO2→H2CO3,其中碳元素化合价发生变化的是( )
A.② B.①② C.③ D.①③
① ② ③
B
4.有甲、乙、丙三种纯净物,甲为黑色固体,乙、丙为无色气体。点燃时,甲既能生成乙,也能生成丙,丙点燃也能生成乙。在以下关于这三种物质推断的叙述中,正确的是( )
A.甲是一种化合物 B.乙是一氧化碳
C.丙是一氧化碳 D.丙是二氧化碳
C
5.甲、乙、丙三种物质,在一定条件下可以通过一步化学
反应实现下列转化。(“→”表示反应生成,部分反应物、成物及反应条件省略),则甲、乙、丙可能依次是( )
A.H2O2、H2O、H2
B.CuO、Cu、O2
C.KClO3、O2、KCl
D.C、CO2、CO
D
1.推断中重要的物质转化关系
(1)组成相同的气体一般为CO和CO2;组成相同的液体为H2O和H2O2;它们化学性质差异的原因是分子构成不同。
名师点睛
(2)重要的转化关系列举
(3)二氧化碳转变成水:CO2+Ca(OH)2 === CaCO3↓+H2O。
课堂小结
C
CO
CO2
C +CO2 == 2CO
高温
2C + O2 == 2CO
点燃
C +CO2 == 2CO
高温
C + O2 == CO2
点燃
C + 2CuO == 2Cu + CO2↑
高温
C、CO和CO2之间的转化关系
2CO + O2 == 2CO2
点燃
CO + CuO == Cu + CO2
△
2.易错点(1)不能用在空气中灼烧的方法除去铜粉中的炭粉,因铜会与氧气反应生成氧化铜。
(2)不能用点燃的方法除去二氧化碳中的一氧化碳,会引入新的气体杂质。
(3)除去CaCl2溶液中的盐酸:加过量的碳酸钙,充分反应后过滤。一般不选氧化钙或氢氧化钙。
CaCO3+2HCl === CaCl2+H2O+CO2↑
第六单元 碳和碳的氧化物
课题3 二氧化碳和一氧化碳(第4课时)
1.关于一氧化碳和二氧化碳的叙述中,正确的是( )
A.都是无色有毒的气体
B.都能用排空气法收集
C.它们之间可以相互转化
D.都能溶于水,并能使紫色石蕊试液变红
C
2.将N2、CO、CO2的混合气体先通过足量石灰水,再通过足量灼热氧化铜,最后剩余的气体是( )
A.氮气
B.二氧化碳
C.一氧化碳
D.二氧化碳和氮气
D
知识点1 第六单元知识间的联系
写出有关反应的化学方程式
① ;
② ;
;
C+O2 === CO2
点燃
C+2CuO === 2Cu+CO2↑
高温
2C+O2 === 2CO
点燃
③ ; ;
④ ;⑤ ;
⑥ ;
CO2+H2O === H2CO3
H2CO3 === H2O+CO2↑
2CO+O2 === 2CO2
点燃
C+CO2 === 2CO
高温
CO+CuO === Cu+CO2
△
3CO+ Fe2O3 2Fe + 3CO2
====
高温
⑦ ;
⑧ ;
。
⑨ 。
CO2+Ca(OH)2 === CaCO3↓+H2O
CaCO3+2HCl === CaCl2+H2O+CO2↑
CaCO3+2HCl === CaCl2+H2O+CO2↑
CaCO3 === CaO+CO2↑
高温
注意:
CO2+H2O === H2CO3,
从CO2角度,即CO2 H2CO3;
从H2O角度,即H2O H2CO3。
CO2+Ca(OH)2 === CaCO3↓+H2O,
即有CO2→H2O和
CO2→CaCO3的转化关系。
【课堂练习1】
1.某同学在复习时总结了如下的物质关系“→”表示物质间存在转化关系,“—”表示两端的物质能发生反应)
(1)物质Y由三种元素组成,则物质Y是____________。
(2)写出H2O→X的化学方程式____________________________。
Ca(OH)2
2H2O=== 2H2↑+O2↑
通电
(3)CO2→CaCO3的化学方程式为__________________________________。
(4)请用“→”画出一条图中没有给出的转化关系。
CO2+Ca(OH)2 === CaCO3↓+H2O
CaCO3→CO2(CO2→H2O,CO2→O2)
O2
2.已知在常温下A为液体,B、C、F是气体;其中C是最轻的气体,F是造成温室效应的主要气体;G为黑色固体单质,H是白色不溶于水固体,它们之间的转化关系如图,回答下列问题:
H2O
H2
O2
CaCO3
CO2
CO
Cu
C
CuO
C
C
黑 C、CuO、Fe3O4、MnO2
红 Cu Fe2O3
通电 H2O
Cu
(1)写出有关物质的化学式:
C是_____;G是____;H是__________;I是______。
(2)写出下列化学方程式:
③ ;
⑤ ;
⑥ 。
H2
C
CaCO3
CO
CO2+Ca(OH)2 === CaCO3↓+H2O
C+2CuO === 2Cu+CO2↑
高温
CO+CuO === CO2+Cu
△
不增杂
不伤主
易分离
不增、不减、易分离
除杂
除去CO 中的CO2最合理的方法是
石灰水
CO2和CO
让混合气体通过澄清的石灰水
让混合气体通过通过灼热的碳层
一般不宜用水除去CO中的CO2,溶解于水中的CO2的量不多,且CO2与水反应生成的碳酸不稳定,易分解。
CO2 + Ca(OH)2 =CaCO3↓+ H2O
CO2+C 2CO
高温
CO
除去CO2 中的CO最合理的方法是____________
化学方程式________________________
通过灼热的氧化铜
不能通过点燃除去因为气体中如果含有大量的CO2的话,是无法点燃的,而且无法确定混入其中的O2恰好反应,带入新的杂质。
知识点2 气体的提纯
被提纯物质 杂质 方法或操作 化学方程式
二氧化碳 氧气
一氧化碳 二氧化碳
二氧化碳 一氧化碳
通过灼热
的铜网
CO2+Ca(OH)2 ===
CaCO3↓+H2O
通过足量的
澄清石灰水
通过灼热的
氧化铜
2Cu+O2 === 2CuO
△
CO+CuO === Cu+CO2
△
【课堂练习2】
1.除去CO2中混有少量O2的最佳方法是( )
A.点燃 B.通过灼热的铜网
C.通过澄清石灰水 D.通过灼热的木炭层
B
2.除去二氧化碳中混有的少量一氧化碳,可采用的方法是( )
A.通过澄清石灰水 B.用燃着的木条点燃
C.通过灼热木炭粉 D.通过灼热氧化铜
D
1.下列有关碳及其化合物的说法错误的是( )
A.二氧化碳的水溶液使石蕊显红色
B.干冰用于人工降雨
C.紧闭门窗用木炭烤火易使人中毒
D.金刚石导电性能良好
D
测评反馈
2.除去一氧化碳气体中混有的少量二氧化碳,可采用的方法是( )
A.把混合气体通过足量澄清的石灰水
B.把混合气体点燃
C.把混合气体通过灼热的氧化铜
D.把混合气体倾倒到另一个容器中
A
3.含碳元素的物质间发生转化:C→CO→CO2→H2CO3,其中碳元素化合价发生变化的是( )
A.② B.①② C.③ D.①③
① ② ③
B
4.有甲、乙、丙三种纯净物,甲为黑色固体,乙、丙为无色气体。点燃时,甲既能生成乙,也能生成丙,丙点燃也能生成乙。在以下关于这三种物质推断的叙述中,正确的是( )
A.甲是一种化合物 B.乙是一氧化碳
C.丙是一氧化碳 D.丙是二氧化碳
C
5.甲、乙、丙三种物质,在一定条件下可以通过一步化学
反应实现下列转化。(“→”表示反应生成,部分反应物、成物及反应条件省略),则甲、乙、丙可能依次是( )
A.H2O2、H2O、H2
B.CuO、Cu、O2
C.KClO3、O2、KCl
D.C、CO2、CO
D
1.推断中重要的物质转化关系
(1)组成相同的气体一般为CO和CO2;组成相同的液体为H2O和H2O2;它们化学性质差异的原因是分子构成不同。
名师点睛
(2)重要的转化关系列举
(3)二氧化碳转变成水:CO2+Ca(OH)2 === CaCO3↓+H2O。
课堂小结
C
CO
CO2
C +CO2 == 2CO
高温
2C + O2 == 2CO
点燃
C +CO2 == 2CO
高温
C + O2 == CO2
点燃
C + 2CuO == 2Cu + CO2↑
高温
C、CO和CO2之间的转化关系
2CO + O2 == 2CO2
点燃
CO + CuO == Cu + CO2
△
2.易错点(1)不能用在空气中灼烧的方法除去铜粉中的炭粉,因铜会与氧气反应生成氧化铜。
(2)不能用点燃的方法除去二氧化碳中的一氧化碳,会引入新的气体杂质。
(3)除去CaCl2溶液中的盐酸:加过量的碳酸钙,充分反应后过滤。一般不选氧化钙或氢氧化钙。
CaCO3+2HCl === CaCl2+H2O+CO2↑
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
