人教版化学九上第三单元课题3 元素(第1课时)课件(共32张PPT)
文档属性
| 名称 | 人教版化学九上第三单元课题3 元素(第1课时)课件(共32张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-07 00:00:00 | ||
图片预览








文档简介
(共32张PPT)
第三单元 构成物质的奥秘
课题3 元素(第1课时)
1.右图是硫原子结构示意图,硫原子的最外层电
子数是___,硫原子容易_____(“得”或“失”)
电子;硫离子的符号为_____;硫离子与硫原子的
化学性质______(填“相同”或“不同”)。
6
得
S2-
不同
2.“加碘食盐”“高钙牛奶”“含氟牙膏”等商品中的“碘、钙、氟”指的是( )
A.原子 B.分子 C.元素 D.离子
C
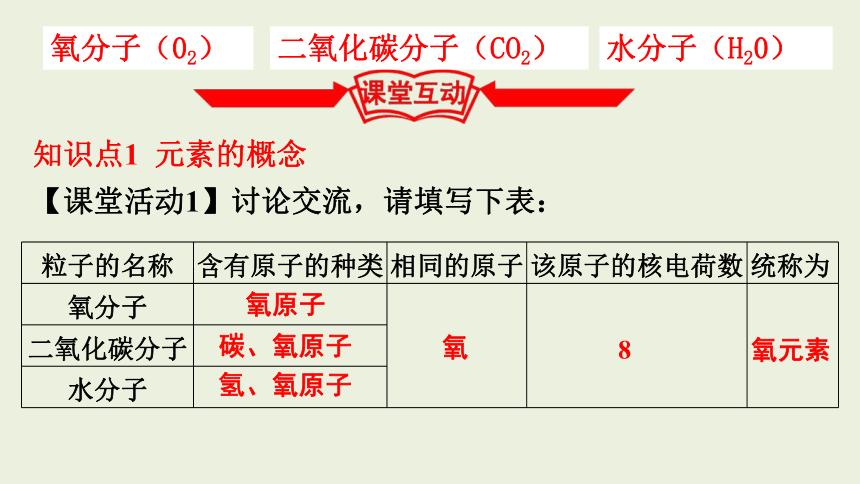
知识点1 元素的概念
【课堂活动1】讨论交流,请填写下表:
粒子的名称 含有原子的种类 相同的原子 该原子的核电荷数 统称为
氧分子
二氧化碳分子
水分子
氧原子
碳、氧原子
氢、氧原子
氧
8
氧元素
氧分子(02)
二氧化碳分子(CO2)
水分子(H20)
元素是具有相同核电荷数(即质子数)的一类原子的总称。★:元素的种类由核电荷数(即质子数) 决定
1.概念
⑴核电荷数(即质子数)决定元素的种类。
⑵元素是一个宏观概念,只讲种类,不讲个数。
注意:
⑶元素是原子的总称,原子是元素中的一种具体粒子。
探究点一 元素的概念
什么是元素?你认为什么决定了元素的种类 ?
1.元素是________________________的__________的总称。
注意:元素由_________________决定;不同元素之间的本质区别是_________(或__________)不同。
2.到目前发现的元素有______种,组成的物质有________种。
质子数(核电荷数)相同
一类原子
质子数或核电荷数
质子数
100多
几千万
核电荷数
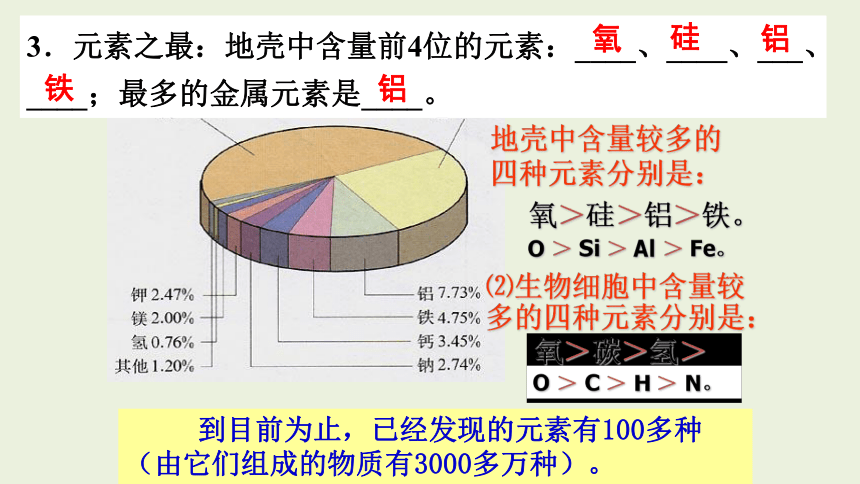
3.元素在自然界的分布
地壳中含量较多的四种元素分别是:
氧>硅>铝>铁。
O > Si > Al > Fe。
⑵生物细胞中含量较多的四种元素分别是:
氧>碳>氢>氮。
O > C > H > N。
到目前为止,已经发现的元素有100多种(由它们组成的物质有3000多万种)。
⑴地壳里各种元素的含量(质量分数)
3.元素之最:地壳中含量前4位的元素:____、____、___、____;最多的金属元素是____。
氧
硅
铝
铁
铝
③生物细胞中含量最多的元素是:
氧元素 O
①地壳中含量最多的元素是:
②地壳中含量最多的金属元素是:
氧元素 O
铝元素 Al
化学之最:
④空气中含量最多的元素是:
氮元素 N
小结:
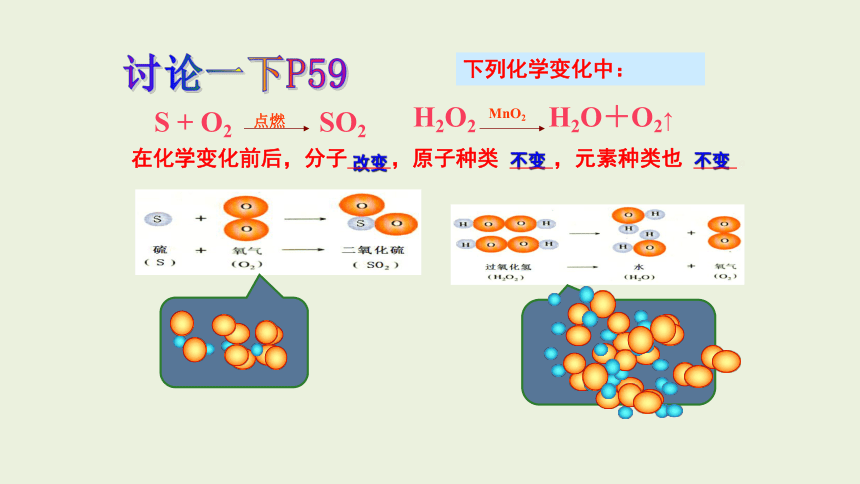
改变
不变
不变
H2O2 H2O+O2↑
MnO2
S + O2 SO2
点燃
在化学变化前后,分子 ,原子种类 ,元素种类也 。
下列化学变化中:
讨论一下P59
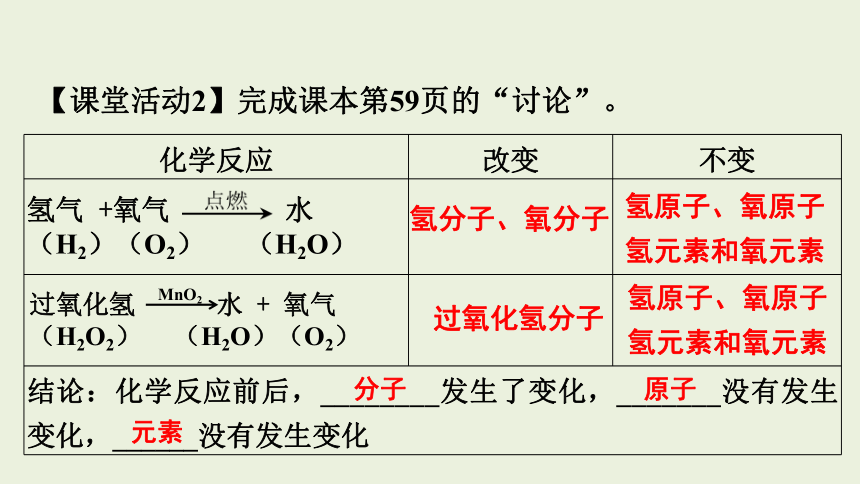
【课堂活动2】完成课本第59页的“讨论”。
化学反应 改变 不变
氢气 +氧气 水 (H2)(O2) (H2O)
过氧化氢 水 + 氧气(H2O2) (H2O)(O2)
结论:化学反应前后,________发生了变化,_______没有发生变化,______没有发生变化
氢分子、氧分子
氢原子、氧原子
氢元素和氧元素
过氧化氢分子
氢原子、氧原子
氢元素和氧元素
分子
原子
元素
MnO2
[小结]元素与原子的比较
元素 原子
定义 具有相同____________的__________的总称 原子是__________中的最小粒子
适用 范围 用于描述物质的________组成,如水由氢元素、氧元素组成 物质——元素 用于描述物质的________构成,如1个水分子由2个氢原子和1个氧原子构成,但不能说“一个水分子是由氢元素和氧元素所组成。” 分子——原子
核电荷数
一类原子
化学变化
宏观
微观
元素 原子
表示 意义 只讲种类,不讲个数,如:氢元素,不能说“几个氢元素” 既表示种类,又表示个数,能说“几个氢原子”
联系 元素是具有相同核电荷数的一类原子的总称,原子是体现元素性质的最小粒子
练习:
在酒精火焰上罩一个干冷的烧杯,发现烧杯内壁有水雾出现,迅速倒转烧杯,注入少量的澄清石灰水,振荡,石灰水变浑浊。这说明酒精在空气中燃烧生成了那些物质?请推测,酒精中含有哪些元素?
(氢、氧)
(碳、氧)
(氧)
(?)
酒精中一定含有碳和氢元素,可能含有氧元素。因为有氧气参与反应,氧气带进了氧元素。
化学变化前后,元素的种类不变!
C2H5OH+3O2 3H2O+2CO2
点燃
酒精+氧气 水+二氧化碳
点燃
【课堂练习1】
1.四氟化硅(SiF4)中氟元素与硅元素最本质的区别是( )
A.相对原子质量不同 B.中子数不同
C.名称不同 D.质子数不同
2.硝酸见光分解成水、二氧化氮和氧气,则硝酸中含有___种元素,理由是_____________________________。
D
3
化学反应前后元素的种类不变
比较下列名词有什么不同:
⑴氧气 ⑵氧 ⑶氧分子 ⑷氧原子
⑴氧气:能支持燃烧、供给呼吸的一种物质。
⑵氧:氧元素,所有氧原子的总称。
⑶氧分子:每两个氧原子构成的1个分子。
⑷氧原子:核电荷数(或质子数)为8的原子。
O2
O
O2
O
下列说法中正确的是:
1. 水(H2O)是由氢气和氧气组成的。
2. 水(H2O)是由两个氢原子和一个氧原子构成的。
3. 水(H2O)是由氢元素和氧元素组成的。
4. 水(H2O)是由水分子构成的。
×
√
×
√
练习:
5. 水分子(H2O)是由氢气和氧气组成的。
6. 水分子(H2O)是由氢元素和氧元素组成的。
7. 每个水分子(H2O)是由两个氢原子和一个氧原子构成的。
√
×
×
1. 水由氢元素和氧元素组成。
2. 水由水分子构成。
3. 水分子由氢原子和氧原子构成。
4. 一个水分子由两个氢原子和一个氧原子构成。
构成物质的粒子有分子、原子、离子。有些物质由分子构成,
(如氢气H2、氧气O2、二氧化碳CO2、水H2O、氧气O2、氮气N2等);
有些物质由原子构成(如Fe、Cu、Al、C、Si等),
有些物质由离子构成(如NaCl、KCl、KClO3、KMnO4等)。
由分子构成的:水和大多数气体(除稀有气体)等,
由原子直接构成的:金属如:Mg,Fe,Cu
知识点2 多种多样的物质及其组成。
[自学1]阅读课本第60页“图3-18”,回答下列问题:
1.从宏观看:物质由________组成;从微观看:构成物质的粒子有_____________________。
2.由分子直接构成的物质有:___________________等;
由原子直接构成的物质有:___________________等;
由离子直接构成的物质有:___________________等。
元素
分子、原子、离子
氧气、氢气、氨
铁、汞、金刚石
硫酸铜、氯化钠
CuSO4、NaCl
【课堂练习2】回答下列问题:
(1)原子、分子、离子都是构成物质的微观粒子,如:二氧化碳是由_______________(填具体粒子的名称,下同)构成的,氯化钠是由_________________构成的。
(2)右图中,用“元素”“原子”“分子”“离子”填空。A______,B_____,C______,D_____。
二氧化碳分子
钠离子和氯离子
元素
原子
分子
离子
宏观
从宏观角度讲物质是由元素组成的,可描述为“某物质是由某元素组成的”。
微观
从微观角度讲物质是由分子、原子、离子等粒子构成的,可描述为“某物质是由某种粒子(分子、原子、离子)构成的”;分子的构成用原子来描述,即“某分子是由某原子构成的” 。
[归纳提升] 组成与构成分别是从宏观和微观两个角度描述物质的,经常用到分子、原子、元素等概念。
知识点3 元素符号
【自学2】阅读课本第61页,了解元素符号、元素符号的书写和元素符号表示的意义,填写下列空白:
1.国际上统一用_________________________________来表示元素,如遇相同的情况,就附加一个_____________来区别。(第一个字母________,第二个字母_______)
2.元素符号表示的意义: _________,_________________。
元素拉丁文名称的第一个字母
小写字母
大写
小写
一种元素
该元素的一个原子
下图中氧元素符号表示什么 ?
2.元素符号表示的意义:
⑴表示一种元素(宏观)
⑵表示这种元素的一个原子(微观)
答:O 表示氧元素、表示一个氧原子。
元素符号都能表示两个意义。以元素符号Fe 为例
⑴(宏观)表示_______
⑵(微观)表示 _____________。某些符号还能表示第三个意义(金属元素或稀有气体或固态非金属),表示该元素的单质。如Fe 还能表示
⑶ _____________
铁元素
一个铁原子
铁这种物质(铁单质)
例 下列符号各表示哪些意义?
(1)O:___________________________________;
(2)2Cu:_________________________________;
(3)Fe:___________________________________。
氧元素、一个氧原子
[应用示例]
2个铜原子
铁元素、一个铁原子、铁这种物质
若元素符号前面有数字,则只有微观意义。
【课堂练习3】在下表里填写符合要求的符号或符号所表示的意义:
符号表示的意义 铜元素 2个 镁原子
化学符号 3Fe O2﹣ Al
Cu
2Mg
三个
铁原子
氧离子
铝元素、
一个铝原子
1.某药品说明书中标明:本品每克含碘150 mg、镁65 mg、锌1.5 mg、铜2 mg、锰1 mg,这里所标的“碘、镁、锌、铜、锰”是指( )
A.分子 B.原子 C.元素 D.无法确定
2.地壳中含量最多的元素是( )
A.氧 B.铝 C.硅 D.铁
C
A
测评反馈
3.化学反应前后一定发生变化的是( )
A.原子的种类 B.分子的种类
C.元素的种类 D.都有可能发生改变
B
4.下列关于物质的组成及结构的说法中,正确的是( )
A.汞是由银元素和水元素组成的
B.硫酸铜由硫酸铜离子构成
C.二氧化氮是由二氧化氮的分子构成的
D.铁是由铁分子构成的
C
5.碳-12、碳-13、碳-14都是碳元素的原子,它们的主要差别在于( )
A.电子数目不同
B.中子数不同
C.质子数目不同
D.化学性质不同
B
1.如何理解“宏观和微观”:“物质”“元素”都属于宏观范畴;“分子”“原子”“离子”“原子核”“质子”“中子”和“电子”都属于微观世界。若在元素符号的前面加上数字,它就失去了宏观意义,此时,只有微观意义。如“2H”只表示2个氢原子;“3C”表示3个碳原子。
2.如何理解化学反应元素种类不变:原子是化学变化中的最小粒子,原子不变即元素也不改变。
名师点睛
3.易错点
(1)元素概念的关键词:“相同核电荷数(或核内质子数)”“一类原子”。如“具有相同核电荷数的微粒属于同种元素”是错误的,如氢分子(H2)含有2个(1×2=2)质子,氦原子也是2个质子,但它们不属于同种元素。
(2)物质等描述时注意事项:物质由元素组成(不能说分子、原子、离子由元素组成);由离子构成的物质要说出阳离子和阴离子。如“水由氢元素和氧元素组成”,不能说“水分子由氢元素和氧元素组成”,应该说“水分子由氢原子和氧原子构成”;氯化钠由钠离子、氯离子构成。
第三单元 构成物质的奥秘
课题3 元素(第1课时)
1.右图是硫原子结构示意图,硫原子的最外层电
子数是___,硫原子容易_____(“得”或“失”)
电子;硫离子的符号为_____;硫离子与硫原子的
化学性质______(填“相同”或“不同”)。
6
得
S2-
不同
2.“加碘食盐”“高钙牛奶”“含氟牙膏”等商品中的“碘、钙、氟”指的是( )
A.原子 B.分子 C.元素 D.离子
C
知识点1 元素的概念
【课堂活动1】讨论交流,请填写下表:
粒子的名称 含有原子的种类 相同的原子 该原子的核电荷数 统称为
氧分子
二氧化碳分子
水分子
氧原子
碳、氧原子
氢、氧原子
氧
8
氧元素
氧分子(02)
二氧化碳分子(CO2)
水分子(H20)
元素是具有相同核电荷数(即质子数)的一类原子的总称。★:元素的种类由核电荷数(即质子数) 决定
1.概念
⑴核电荷数(即质子数)决定元素的种类。
⑵元素是一个宏观概念,只讲种类,不讲个数。
注意:
⑶元素是原子的总称,原子是元素中的一种具体粒子。
探究点一 元素的概念
什么是元素?你认为什么决定了元素的种类 ?
1.元素是________________________的__________的总称。
注意:元素由_________________决定;不同元素之间的本质区别是_________(或__________)不同。
2.到目前发现的元素有______种,组成的物质有________种。
质子数(核电荷数)相同
一类原子
质子数或核电荷数
质子数
100多
几千万
核电荷数
3.元素在自然界的分布
地壳中含量较多的四种元素分别是:
氧>硅>铝>铁。
O > Si > Al > Fe。
⑵生物细胞中含量较多的四种元素分别是:
氧>碳>氢>氮。
O > C > H > N。
到目前为止,已经发现的元素有100多种(由它们组成的物质有3000多万种)。
⑴地壳里各种元素的含量(质量分数)
3.元素之最:地壳中含量前4位的元素:____、____、___、____;最多的金属元素是____。
氧
硅
铝
铁
铝
③生物细胞中含量最多的元素是:
氧元素 O
①地壳中含量最多的元素是:
②地壳中含量最多的金属元素是:
氧元素 O
铝元素 Al
化学之最:
④空气中含量最多的元素是:
氮元素 N
小结:
改变
不变
不变
H2O2 H2O+O2↑
MnO2
S + O2 SO2
点燃
在化学变化前后,分子 ,原子种类 ,元素种类也 。
下列化学变化中:
讨论一下P59
【课堂活动2】完成课本第59页的“讨论”。
化学反应 改变 不变
氢气 +氧气 水 (H2)(O2) (H2O)
过氧化氢 水 + 氧气(H2O2) (H2O)(O2)
结论:化学反应前后,________发生了变化,_______没有发生变化,______没有发生变化
氢分子、氧分子
氢原子、氧原子
氢元素和氧元素
过氧化氢分子
氢原子、氧原子
氢元素和氧元素
分子
原子
元素
MnO2
[小结]元素与原子的比较
元素 原子
定义 具有相同____________的__________的总称 原子是__________中的最小粒子
适用 范围 用于描述物质的________组成,如水由氢元素、氧元素组成 物质——元素 用于描述物质的________构成,如1个水分子由2个氢原子和1个氧原子构成,但不能说“一个水分子是由氢元素和氧元素所组成。” 分子——原子
核电荷数
一类原子
化学变化
宏观
微观
元素 原子
表示 意义 只讲种类,不讲个数,如:氢元素,不能说“几个氢元素” 既表示种类,又表示个数,能说“几个氢原子”
联系 元素是具有相同核电荷数的一类原子的总称,原子是体现元素性质的最小粒子
练习:
在酒精火焰上罩一个干冷的烧杯,发现烧杯内壁有水雾出现,迅速倒转烧杯,注入少量的澄清石灰水,振荡,石灰水变浑浊。这说明酒精在空气中燃烧生成了那些物质?请推测,酒精中含有哪些元素?
(氢、氧)
(碳、氧)
(氧)
(?)
酒精中一定含有碳和氢元素,可能含有氧元素。因为有氧气参与反应,氧气带进了氧元素。
化学变化前后,元素的种类不变!
C2H5OH+3O2 3H2O+2CO2
点燃
酒精+氧气 水+二氧化碳
点燃
【课堂练习1】
1.四氟化硅(SiF4)中氟元素与硅元素最本质的区别是( )
A.相对原子质量不同 B.中子数不同
C.名称不同 D.质子数不同
2.硝酸见光分解成水、二氧化氮和氧气,则硝酸中含有___种元素,理由是_____________________________。
D
3
化学反应前后元素的种类不变
比较下列名词有什么不同:
⑴氧气 ⑵氧 ⑶氧分子 ⑷氧原子
⑴氧气:能支持燃烧、供给呼吸的一种物质。
⑵氧:氧元素,所有氧原子的总称。
⑶氧分子:每两个氧原子构成的1个分子。
⑷氧原子:核电荷数(或质子数)为8的原子。
O2
O
O2
O
下列说法中正确的是:
1. 水(H2O)是由氢气和氧气组成的。
2. 水(H2O)是由两个氢原子和一个氧原子构成的。
3. 水(H2O)是由氢元素和氧元素组成的。
4. 水(H2O)是由水分子构成的。
×
√
×
√
练习:
5. 水分子(H2O)是由氢气和氧气组成的。
6. 水分子(H2O)是由氢元素和氧元素组成的。
7. 每个水分子(H2O)是由两个氢原子和一个氧原子构成的。
√
×
×
1. 水由氢元素和氧元素组成。
2. 水由水分子构成。
3. 水分子由氢原子和氧原子构成。
4. 一个水分子由两个氢原子和一个氧原子构成。
构成物质的粒子有分子、原子、离子。有些物质由分子构成,
(如氢气H2、氧气O2、二氧化碳CO2、水H2O、氧气O2、氮气N2等);
有些物质由原子构成(如Fe、Cu、Al、C、Si等),
有些物质由离子构成(如NaCl、KCl、KClO3、KMnO4等)。
由分子构成的:水和大多数气体(除稀有气体)等,
由原子直接构成的:金属如:Mg,Fe,Cu
知识点2 多种多样的物质及其组成。
[自学1]阅读课本第60页“图3-18”,回答下列问题:
1.从宏观看:物质由________组成;从微观看:构成物质的粒子有_____________________。
2.由分子直接构成的物质有:___________________等;
由原子直接构成的物质有:___________________等;
由离子直接构成的物质有:___________________等。
元素
分子、原子、离子
氧气、氢气、氨
铁、汞、金刚石
硫酸铜、氯化钠
CuSO4、NaCl
【课堂练习2】回答下列问题:
(1)原子、分子、离子都是构成物质的微观粒子,如:二氧化碳是由_______________(填具体粒子的名称,下同)构成的,氯化钠是由_________________构成的。
(2)右图中,用“元素”“原子”“分子”“离子”填空。A______,B_____,C______,D_____。
二氧化碳分子
钠离子和氯离子
元素
原子
分子
离子
宏观
从宏观角度讲物质是由元素组成的,可描述为“某物质是由某元素组成的”。
微观
从微观角度讲物质是由分子、原子、离子等粒子构成的,可描述为“某物质是由某种粒子(分子、原子、离子)构成的”;分子的构成用原子来描述,即“某分子是由某原子构成的” 。
[归纳提升] 组成与构成分别是从宏观和微观两个角度描述物质的,经常用到分子、原子、元素等概念。
知识点3 元素符号
【自学2】阅读课本第61页,了解元素符号、元素符号的书写和元素符号表示的意义,填写下列空白:
1.国际上统一用_________________________________来表示元素,如遇相同的情况,就附加一个_____________来区别。(第一个字母________,第二个字母_______)
2.元素符号表示的意义: _________,_________________。
元素拉丁文名称的第一个字母
小写字母
大写
小写
一种元素
该元素的一个原子
下图中氧元素符号表示什么 ?
2.元素符号表示的意义:
⑴表示一种元素(宏观)
⑵表示这种元素的一个原子(微观)
答:O 表示氧元素、表示一个氧原子。
元素符号都能表示两个意义。以元素符号Fe 为例
⑴(宏观)表示_______
⑵(微观)表示 _____________。某些符号还能表示第三个意义(金属元素或稀有气体或固态非金属),表示该元素的单质。如Fe 还能表示
⑶ _____________
铁元素
一个铁原子
铁这种物质(铁单质)
例 下列符号各表示哪些意义?
(1)O:___________________________________;
(2)2Cu:_________________________________;
(3)Fe:___________________________________。
氧元素、一个氧原子
[应用示例]
2个铜原子
铁元素、一个铁原子、铁这种物质
若元素符号前面有数字,则只有微观意义。
【课堂练习3】在下表里填写符合要求的符号或符号所表示的意义:
符号表示的意义 铜元素 2个 镁原子
化学符号 3Fe O2﹣ Al
Cu
2Mg
三个
铁原子
氧离子
铝元素、
一个铝原子
1.某药品说明书中标明:本品每克含碘150 mg、镁65 mg、锌1.5 mg、铜2 mg、锰1 mg,这里所标的“碘、镁、锌、铜、锰”是指( )
A.分子 B.原子 C.元素 D.无法确定
2.地壳中含量最多的元素是( )
A.氧 B.铝 C.硅 D.铁
C
A
测评反馈
3.化学反应前后一定发生变化的是( )
A.原子的种类 B.分子的种类
C.元素的种类 D.都有可能发生改变
B
4.下列关于物质的组成及结构的说法中,正确的是( )
A.汞是由银元素和水元素组成的
B.硫酸铜由硫酸铜离子构成
C.二氧化氮是由二氧化氮的分子构成的
D.铁是由铁分子构成的
C
5.碳-12、碳-13、碳-14都是碳元素的原子,它们的主要差别在于( )
A.电子数目不同
B.中子数不同
C.质子数目不同
D.化学性质不同
B
1.如何理解“宏观和微观”:“物质”“元素”都属于宏观范畴;“分子”“原子”“离子”“原子核”“质子”“中子”和“电子”都属于微观世界。若在元素符号的前面加上数字,它就失去了宏观意义,此时,只有微观意义。如“2H”只表示2个氢原子;“3C”表示3个碳原子。
2.如何理解化学反应元素种类不变:原子是化学变化中的最小粒子,原子不变即元素也不改变。
名师点睛
3.易错点
(1)元素概念的关键词:“相同核电荷数(或核内质子数)”“一类原子”。如“具有相同核电荷数的微粒属于同种元素”是错误的,如氢分子(H2)含有2个(1×2=2)质子,氦原子也是2个质子,但它们不属于同种元素。
(2)物质等描述时注意事项:物质由元素组成(不能说分子、原子、离子由元素组成);由离子构成的物质要说出阳离子和阴离子。如“水由氢元素和氧元素组成”,不能说“水分子由氢元素和氧元素组成”,应该说“水分子由氢原子和氧原子构成”;氯化钠由钠离子、氯离子构成。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
