1.2.2有机化合物的分子式和结构的确定 课件(共27张ppt)化学人教版(2019)选择性必修3
文档属性
| 名称 | 1.2.2有机化合物的分子式和结构的确定 课件(共27张ppt)化学人教版(2019)选择性必修3 |  | |
| 格式 | pptx | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-10 15:31:13 | ||
图片预览






文档简介
(共27张PPT)
第一章 有机化合物的结构特点与研究方法
第二节 研究有机化合物的一般方法
第2课时 有机化合物的分子式和结构的确定
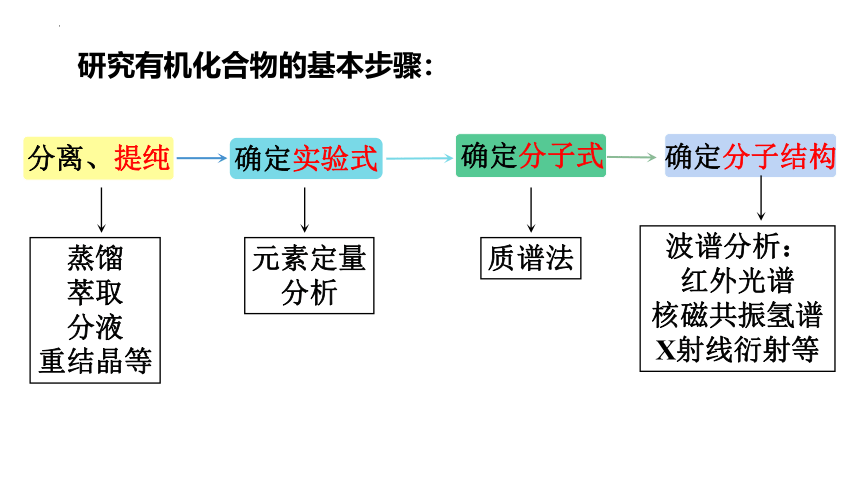
研究有机化合物的基本步骤:
蒸馏
萃取
分液
重结晶等
元素定量分析
质谱法
波谱分析:
红外光谱
核磁共振氢谱
X射线衍射等
分离、提纯
确定实验式
确定分子式
确定分子结构
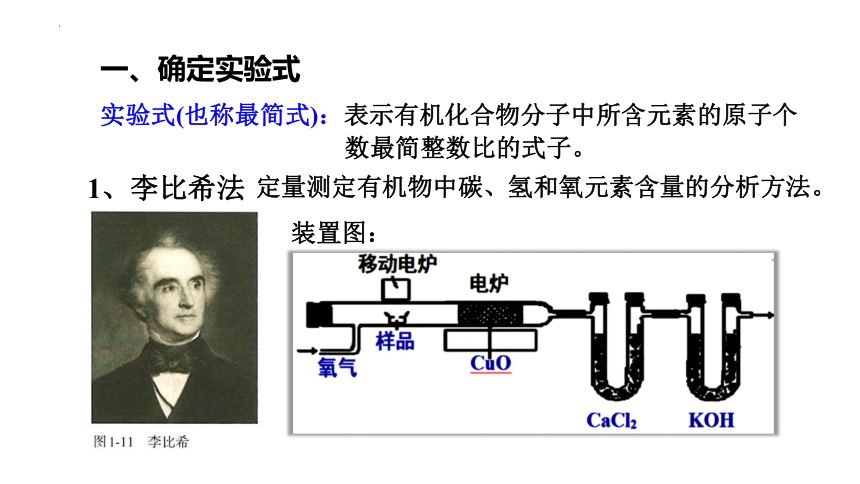
一、确定实验式
实验式(也称最简式):表示有机化合物分子中所含元素的原子个
数最简整数比的式子。
1、李比希法
定量测定有机物中碳、氢和氧元素含量的分析方法。
装置图:
计算反应前后装置
质量差
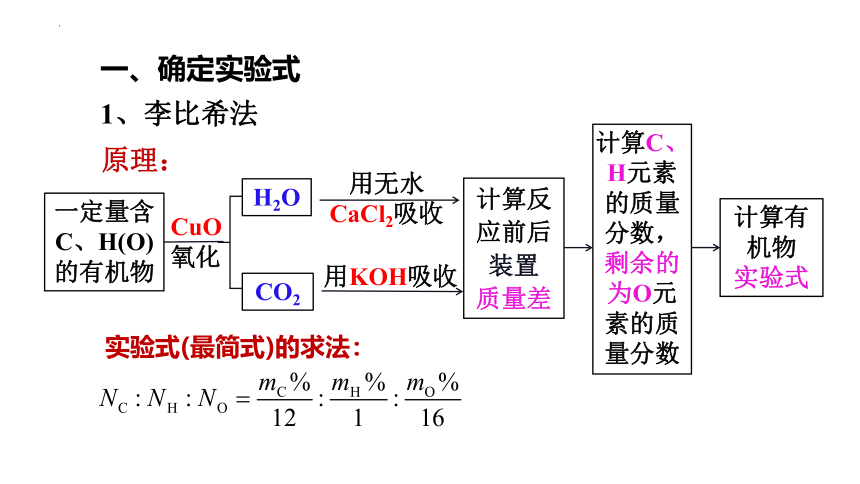
原理:
一、确定实验式
1、李比希法
一定量含C、H(O)的有机物
H2O
CO2
CuO
氧化
用KOH吸收
用无水CaCl2吸收
计算C、H元素的质量分数,剩余的为O元素的质量分数
计算有机物
实验式
实验式(最简式)的求法:
1、某有机化合物完全燃烧生成CO2和H2O,能说明该有机化合物中只C、H两种元素吗?
不能。若有机化合物含有C、H、O三种元素,该有机化合物完全燃烧也生成CO2和H2O。
先用浓硫酸(或无水CaCl2)吸收H2O,再用浓KOH(或碱石灰)吸收CO2。
2、定量测定CO2和H2O的顺序是什么?能否交换顺序?
论
讨
与
考
思
不能。因为KOH既可以吸收水又可以吸收二氧化碳。
练习1:某种含C、H、O三种元素的未知物A,经燃烧分析实验测得其中碳的质量分数为52.2%,氢的质量分数为13.1%。试求该未知物A的实验式。
解:(1)计算该有机化合物中氧元素的质量分数:
w(O)=100%-52.2%-13.1%=34.7%
∴实验式:C2H6O
(2)计算该有机化合物分子内各元素原子的个数比:
N(C):N(H):N(O) =
= 2:6:1
练习2:将5.8 g某有机物在足量O2中充分燃烧,并将其产物依次通过足量的无水CaCl2和KOH浓溶液,发现水CaCl2增重5.4 g , KOH浓溶液增重13.2 g。求其实验式。
解:
5.8g有机物中,含C:
含H:
含O:
N(C):N(H):N(O)
=3:6:1
∴实验式为 C3H6O
可以直接测出有机物中各元素原子的质量分数。
2、现代元素分析仪
现代化的元素分析仪
一、确定实验式
二、确定分子式
根据实验式确定它的分子式,还需要什么条件?
---确定相对分子质量
1、计算法
③相对密度法:根据气体A相对于气体B(已知)的相对密度d。MA=d×MB
②标准状况密度法:已知标准状况下气体的密度ρ,求算摩尔质量。M=ρ×22.4 L·mol-1
①定义法:M = m / n
分子式是实验式的整数倍
(1)标准状况下0.56g某气态烃的体积为448mL;
列式计算下列有机物的相对分子质量:
28
(4)3.2g某饱和一元醇与足量金属钠反应得到1.12L(标况)氢气。
(2)某卤代烃的蒸气密度是相同状况下甲烷密度的11.75倍;
(3)某气态烃在标准状况时的密度为1.25g/L;
16×11.75=188
1.25×22.4=28
2R—OH + 2Na → 2R—ONa + H2↑
32
商余法确定烃的分子式:
烃A:
Mr
÷12
=x ··· y
A的分子式为:CxHy
=x
A的分子式为:Cx-1H12
分别求出相对分子质量为42、58、72、92的烃的分子式。
42÷12=3 ··· 6
C3H6
58÷12=4 ··· 10
C4H10
72÷12=6
C5H12
92÷12=7 ··· 8
C7H8
2、仪器测定
—— 质谱法
最大的质荷比
有机物分子
确定相对分子质量
高能电子
流轰击
带正电荷的分子离子和碎片离子
磁场作用下先后到达检测仪
质谱图
质荷比=
电荷
相对分子质量
质谱图中最大的质荷比
=样品分子的相对分子质量
如图为某有机化合物的质谱图:
从图中可知,该有机物的相对分子质量为 ,
46
已知未知物A的实验式C2H6O,则该有机物的分子式是 。
C2H6O
某有机物的结构确定:
①测定实验式:某含C、H、O三种元素的有机物,经燃烧分析实验测定其碳的质量分数是64.86%,氢的质量分数是13.51%,则其实验式是 。
②确定分子式:下图是该有机物的质谱图,则其相对分子质量为 ,分子式为 。
设分子式为(C4H10O)n
则 74n=74
∴n=1
因此分子式为C4H10O
C4H10O
74
C4H10O
咖啡和茶类饮料中都含有兴奋剂咖啡因。经元素分析测定,咖啡因中各元素的质量分数是:碳49.5%,氢5.2%,氮28.9%,氧16.5%。
(1)咖啡因的实验式为 。
(2)质谱法测得咖啡因的相对分子质量为194,则咖啡因的分子式为 。
C4H5N2O
C8H10N4O2
n(C):n(H):n(N):n(O)= : : :
49.5%
12
5.2%
1
28.9%
14
16.5%
16
=4:5:2:1
设分子式为(C4H5N2O)n,
194
(12×4+5+14×2+16)
n = =2
所以咖啡因的分子式为C8H10N4O2
三、确定分子结构
确定有机物结构式的一般步骤是:
(1)根据分子式写出可能的同分异构体;
(2)利用该物质的性质推测可能含有的官能团,确定正确的结构。
例:未知物A的分子式为C2H6O,其结构可能是什么?
测定方法
化学方法:看是否与Na反应
物理方法:红外光谱法等
当化合物结构比较复杂时,若用化学方法,时间长、浪费试剂,因此科学上常常需要采取一些物理方法。与鉴定有机物结构有关的物理方法有红外光谱、核磁共振谱、X射线衍射等。
1、红外光谱
---测定有机化合物分子中化学键或官能团
(1)原理:不同官能团或化学键吸收频率不同,在红外光
谱图上将处于不同的位置。
(2)红外光谱图
左图是分子式为C2H6O的未知物A的红外光谱图,分子中有O—H(或—OH),可确定A的结构简式为 。
CH3CH2OH
有机物Y的分子式为C4H8O2,其红外光谱如图所示,则该有机物可能的结构简式为( )
A.CH3COOCH2CH3
B.OHCCH2CH2OCH3
C.HCOOCH2CH2CH3
D.(CH3)2CHCOOH
A
2、核磁共振氢谱(NMR)
核磁共振仪
(1)原理:
氢原子核具有磁性。处于不同化学环境中的
氢原子因产生共振时吸收的频率不同,在谱图上
出现的位置也不同,具有不同的化学位移(用δ表
示),且吸收峰的面积与氢原子数成正比。
---测定有机化合物分子中氢原子的类型和相对数目
(2)核磁共振氢谱:
吸收峰数目=等效氢的种数
峰强度(峰面积或峰高)之比=
不同等效氢的个数之比
典例分析
未知物A的核磁共振氢谱
二甲醚的核磁共振氢谱
未知物A(分子式为C2H6O)的核磁共振氢谱图如左上图所示,由此可以判断A的分子中有3种处于不同化学环境的氢原子,个数比为3:2:1。
二甲醚(CH3OCH3)分子的核磁共振氢谱图如右上图所示,图中只有一个峰,由此可以判断二甲醚分子中6个氢原子的化学环境相同。
1、丙醇有两种:
右图是其中一种物质的核磁共振氢谱,则与该谱图对应的物质的名称为:_______
CH3CH2CH2OH 1-丙醇
CH3CH(OH)CH3 2-丙醇
2-丙醇
2、下列有机物在H’-NMR上只给出一组峰的是( )
A、HCHO B、CH3OH
C、HCOOH D、CH3COOCH3
A
3、在核磁共振氢谱中出现两组峰,且峰面积之比为3∶2的化合物是( )
D
3、X射线衍射
---有机化合物晶体结构的测定
原理:X射线是一种波长很短(约10-10m)的电磁波,它
和晶体中的原子相互作用可以产生衍射图 。
根据原子坐标,可以计算原子间的距离,判断哪些原子之间存在化学键,确定键长和键角,得出分子的空间结构。
单晶衍射图
1. 下列说法不正确的是( )
A.通过质谱法可以确认有机化合物的相对分子质量
B.甲苯分子的核磁共振氢谱中有4个不同的吸收峰
C.红外光谱可以帮助确定许多有机物的结构
D.某有机物完全燃烧只生成CO2和H2O,两者物质的量之比为1:2,则该有机物一定为甲烷
D
2. 乙酸和甲酸甲酯互为同分异构体,其结构式分别为,
通过下列方法或检测仪得出的信息或信号完全相同的是( )
A.李比希元素分析法 B.红外光谱仪
C.核磁共振仪 D.质谱仪
A
3. 已知某有机物A的红外光谱和核磁共振氢谱如图所示,下列说法中不正确的是 ( )
A.由红外光谱可知,该有机物分子中至少有三种不同的化学键
B.由核磁共振氢谱可知,该有机物分子中有三种不同的氢原子
C.仅由核磁共振氢谱无法得知其分子中的氢原子总数
D.若A的分子式为C3H8O,则其结构简式可能为
D
4. 有机物X是一种重要的有机合成中间体,用于制造塑料、涂料和黏合剂等高聚物。为研究X的组成与结构,进行如下实验:
(1)将10.0 g X在足量O2中充分燃烧,并将其产物依次通过足量的无水CaCl2和KOH浓溶液,发现无水CaCl2增重7.2 g,KOH浓溶液增重22.0 g。有机物X的实验式为___________。
(2)有机物X的质谱图如图所示,则有机
物X的相对分子质量为_________。
(3)经红外光谱测定,有机物X中含有醛基;
有机物X的核磁共振氢谱图上有2组吸收峰,
峰面积之比为3∶1。则有机物X的结构简式为________________。
C5H8O2
(CH3)2C(CHO)2
100
第一章 有机化合物的结构特点与研究方法
第二节 研究有机化合物的一般方法
第2课时 有机化合物的分子式和结构的确定
研究有机化合物的基本步骤:
蒸馏
萃取
分液
重结晶等
元素定量分析
质谱法
波谱分析:
红外光谱
核磁共振氢谱
X射线衍射等
分离、提纯
确定实验式
确定分子式
确定分子结构
一、确定实验式
实验式(也称最简式):表示有机化合物分子中所含元素的原子个
数最简整数比的式子。
1、李比希法
定量测定有机物中碳、氢和氧元素含量的分析方法。
装置图:
计算反应前后装置
质量差
原理:
一、确定实验式
1、李比希法
一定量含C、H(O)的有机物
H2O
CO2
CuO
氧化
用KOH吸收
用无水CaCl2吸收
计算C、H元素的质量分数,剩余的为O元素的质量分数
计算有机物
实验式
实验式(最简式)的求法:
1、某有机化合物完全燃烧生成CO2和H2O,能说明该有机化合物中只C、H两种元素吗?
不能。若有机化合物含有C、H、O三种元素,该有机化合物完全燃烧也生成CO2和H2O。
先用浓硫酸(或无水CaCl2)吸收H2O,再用浓KOH(或碱石灰)吸收CO2。
2、定量测定CO2和H2O的顺序是什么?能否交换顺序?
论
讨
与
考
思
不能。因为KOH既可以吸收水又可以吸收二氧化碳。
练习1:某种含C、H、O三种元素的未知物A,经燃烧分析实验测得其中碳的质量分数为52.2%,氢的质量分数为13.1%。试求该未知物A的实验式。
解:(1)计算该有机化合物中氧元素的质量分数:
w(O)=100%-52.2%-13.1%=34.7%
∴实验式:C2H6O
(2)计算该有机化合物分子内各元素原子的个数比:
N(C):N(H):N(O) =
= 2:6:1
练习2:将5.8 g某有机物在足量O2中充分燃烧,并将其产物依次通过足量的无水CaCl2和KOH浓溶液,发现水CaCl2增重5.4 g , KOH浓溶液增重13.2 g。求其实验式。
解:
5.8g有机物中,含C:
含H:
含O:
N(C):N(H):N(O)
=3:6:1
∴实验式为 C3H6O
可以直接测出有机物中各元素原子的质量分数。
2、现代元素分析仪
现代化的元素分析仪
一、确定实验式
二、确定分子式
根据实验式确定它的分子式,还需要什么条件?
---确定相对分子质量
1、计算法
③相对密度法:根据气体A相对于气体B(已知)的相对密度d。MA=d×MB
②标准状况密度法:已知标准状况下气体的密度ρ,求算摩尔质量。M=ρ×22.4 L·mol-1
①定义法:M = m / n
分子式是实验式的整数倍
(1)标准状况下0.56g某气态烃的体积为448mL;
列式计算下列有机物的相对分子质量:
28
(4)3.2g某饱和一元醇与足量金属钠反应得到1.12L(标况)氢气。
(2)某卤代烃的蒸气密度是相同状况下甲烷密度的11.75倍;
(3)某气态烃在标准状况时的密度为1.25g/L;
16×11.75=188
1.25×22.4=28
2R—OH + 2Na → 2R—ONa + H2↑
32
商余法确定烃的分子式:
烃A:
Mr
÷12
=x ··· y
A的分子式为:CxHy
=x
A的分子式为:Cx-1H12
分别求出相对分子质量为42、58、72、92的烃的分子式。
42÷12=3 ··· 6
C3H6
58÷12=4 ··· 10
C4H10
72÷12=6
C5H12
92÷12=7 ··· 8
C7H8
2、仪器测定
—— 质谱法
最大的质荷比
有机物分子
确定相对分子质量
高能电子
流轰击
带正电荷的分子离子和碎片离子
磁场作用下先后到达检测仪
质谱图
质荷比=
电荷
相对分子质量
质谱图中最大的质荷比
=样品分子的相对分子质量
如图为某有机化合物的质谱图:
从图中可知,该有机物的相对分子质量为 ,
46
已知未知物A的实验式C2H6O,则该有机物的分子式是 。
C2H6O
某有机物的结构确定:
①测定实验式:某含C、H、O三种元素的有机物,经燃烧分析实验测定其碳的质量分数是64.86%,氢的质量分数是13.51%,则其实验式是 。
②确定分子式:下图是该有机物的质谱图,则其相对分子质量为 ,分子式为 。
设分子式为(C4H10O)n
则 74n=74
∴n=1
因此分子式为C4H10O
C4H10O
74
C4H10O
咖啡和茶类饮料中都含有兴奋剂咖啡因。经元素分析测定,咖啡因中各元素的质量分数是:碳49.5%,氢5.2%,氮28.9%,氧16.5%。
(1)咖啡因的实验式为 。
(2)质谱法测得咖啡因的相对分子质量为194,则咖啡因的分子式为 。
C4H5N2O
C8H10N4O2
n(C):n(H):n(N):n(O)= : : :
49.5%
12
5.2%
1
28.9%
14
16.5%
16
=4:5:2:1
设分子式为(C4H5N2O)n,
194
(12×4+5+14×2+16)
n = =2
所以咖啡因的分子式为C8H10N4O2
三、确定分子结构
确定有机物结构式的一般步骤是:
(1)根据分子式写出可能的同分异构体;
(2)利用该物质的性质推测可能含有的官能团,确定正确的结构。
例:未知物A的分子式为C2H6O,其结构可能是什么?
测定方法
化学方法:看是否与Na反应
物理方法:红外光谱法等
当化合物结构比较复杂时,若用化学方法,时间长、浪费试剂,因此科学上常常需要采取一些物理方法。与鉴定有机物结构有关的物理方法有红外光谱、核磁共振谱、X射线衍射等。
1、红外光谱
---测定有机化合物分子中化学键或官能团
(1)原理:不同官能团或化学键吸收频率不同,在红外光
谱图上将处于不同的位置。
(2)红外光谱图
左图是分子式为C2H6O的未知物A的红外光谱图,分子中有O—H(或—OH),可确定A的结构简式为 。
CH3CH2OH
有机物Y的分子式为C4H8O2,其红外光谱如图所示,则该有机物可能的结构简式为( )
A.CH3COOCH2CH3
B.OHCCH2CH2OCH3
C.HCOOCH2CH2CH3
D.(CH3)2CHCOOH
A
2、核磁共振氢谱(NMR)
核磁共振仪
(1)原理:
氢原子核具有磁性。处于不同化学环境中的
氢原子因产生共振时吸收的频率不同,在谱图上
出现的位置也不同,具有不同的化学位移(用δ表
示),且吸收峰的面积与氢原子数成正比。
---测定有机化合物分子中氢原子的类型和相对数目
(2)核磁共振氢谱:
吸收峰数目=等效氢的种数
峰强度(峰面积或峰高)之比=
不同等效氢的个数之比
典例分析
未知物A的核磁共振氢谱
二甲醚的核磁共振氢谱
未知物A(分子式为C2H6O)的核磁共振氢谱图如左上图所示,由此可以判断A的分子中有3种处于不同化学环境的氢原子,个数比为3:2:1。
二甲醚(CH3OCH3)分子的核磁共振氢谱图如右上图所示,图中只有一个峰,由此可以判断二甲醚分子中6个氢原子的化学环境相同。
1、丙醇有两种:
右图是其中一种物质的核磁共振氢谱,则与该谱图对应的物质的名称为:_______
CH3CH2CH2OH 1-丙醇
CH3CH(OH)CH3 2-丙醇
2-丙醇
2、下列有机物在H’-NMR上只给出一组峰的是( )
A、HCHO B、CH3OH
C、HCOOH D、CH3COOCH3
A
3、在核磁共振氢谱中出现两组峰,且峰面积之比为3∶2的化合物是( )
D
3、X射线衍射
---有机化合物晶体结构的测定
原理:X射线是一种波长很短(约10-10m)的电磁波,它
和晶体中的原子相互作用可以产生衍射图 。
根据原子坐标,可以计算原子间的距离,判断哪些原子之间存在化学键,确定键长和键角,得出分子的空间结构。
单晶衍射图
1. 下列说法不正确的是( )
A.通过质谱法可以确认有机化合物的相对分子质量
B.甲苯分子的核磁共振氢谱中有4个不同的吸收峰
C.红外光谱可以帮助确定许多有机物的结构
D.某有机物完全燃烧只生成CO2和H2O,两者物质的量之比为1:2,则该有机物一定为甲烷
D
2. 乙酸和甲酸甲酯互为同分异构体,其结构式分别为,
通过下列方法或检测仪得出的信息或信号完全相同的是( )
A.李比希元素分析法 B.红外光谱仪
C.核磁共振仪 D.质谱仪
A
3. 已知某有机物A的红外光谱和核磁共振氢谱如图所示,下列说法中不正确的是 ( )
A.由红外光谱可知,该有机物分子中至少有三种不同的化学键
B.由核磁共振氢谱可知,该有机物分子中有三种不同的氢原子
C.仅由核磁共振氢谱无法得知其分子中的氢原子总数
D.若A的分子式为C3H8O,则其结构简式可能为
D
4. 有机物X是一种重要的有机合成中间体,用于制造塑料、涂料和黏合剂等高聚物。为研究X的组成与结构,进行如下实验:
(1)将10.0 g X在足量O2中充分燃烧,并将其产物依次通过足量的无水CaCl2和KOH浓溶液,发现无水CaCl2增重7.2 g,KOH浓溶液增重22.0 g。有机物X的实验式为___________。
(2)有机物X的质谱图如图所示,则有机
物X的相对分子质量为_________。
(3)经红外光谱测定,有机物X中含有醛基;
有机物X的核磁共振氢谱图上有2组吸收峰,
峰面积之比为3∶1。则有机物X的结构简式为________________。
C5H8O2
(CH3)2C(CHO)2
100
