浙教版九上 2.2金属的化学性质 随堂练习(含解析)
文档属性
| 名称 | 浙教版九上 2.2金属的化学性质 随堂练习(含解析) |

|
|
| 格式 | doc | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-09-13 00:00:00 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
浙教版九上 2.2金属的化学性质 随堂练习
一、单选题
1.早在1637年,我国的科学技术著作《天工开物》已记载了冶炼铅的方法,其主要反应的化学方程式是。该反应属于( ) www-2-1-cnjy-com
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
2.秀秀通过实验探究某种金属R的活动性强弱,并根据实验现象编制检索表如图,根据检索表可知,金属R的活动性强弱排序正确的是( )
A.Fe>Ag>R B.Fe>R>Ag C.R>Fe>Ag D.Ag>R>Fe
3.食品干燥剂是指能除去潮湿物质中水分的物质。食品抗氧化剂是一种延缓食品氧化变质、提高食品稳定性和延长贮存期的食品添加剂,下列物质可用作食品双吸剂的是( )
A.铜粉 B.铁粉
C.生石灰 D.氢氧化钠固体
4.向一定质量AgNO3和Cu(NO3)2的混合溶液中加入n,溶液质量与加入Zn的质量关系如图所示。下列说法正确的是( ) 21·世纪*教育网
A.a点溶液中含有两种溶质
B.c点溶液中的溶质为Zn(NO3)2和Cu(NO3)2
C.取b点的沉淀物,滴加稀盐酸有气泡产生
D.d点沉淀物有Ag、Cu和Zn
5.在柠檬中插入两种不同的金属可以制成水果电池。相同条件下,两种金属的活动性差异越大,水果电池的电压也越大。下列柠檬电池中电压最大的是( ) 21cnjy.com
A. B.
C. D.
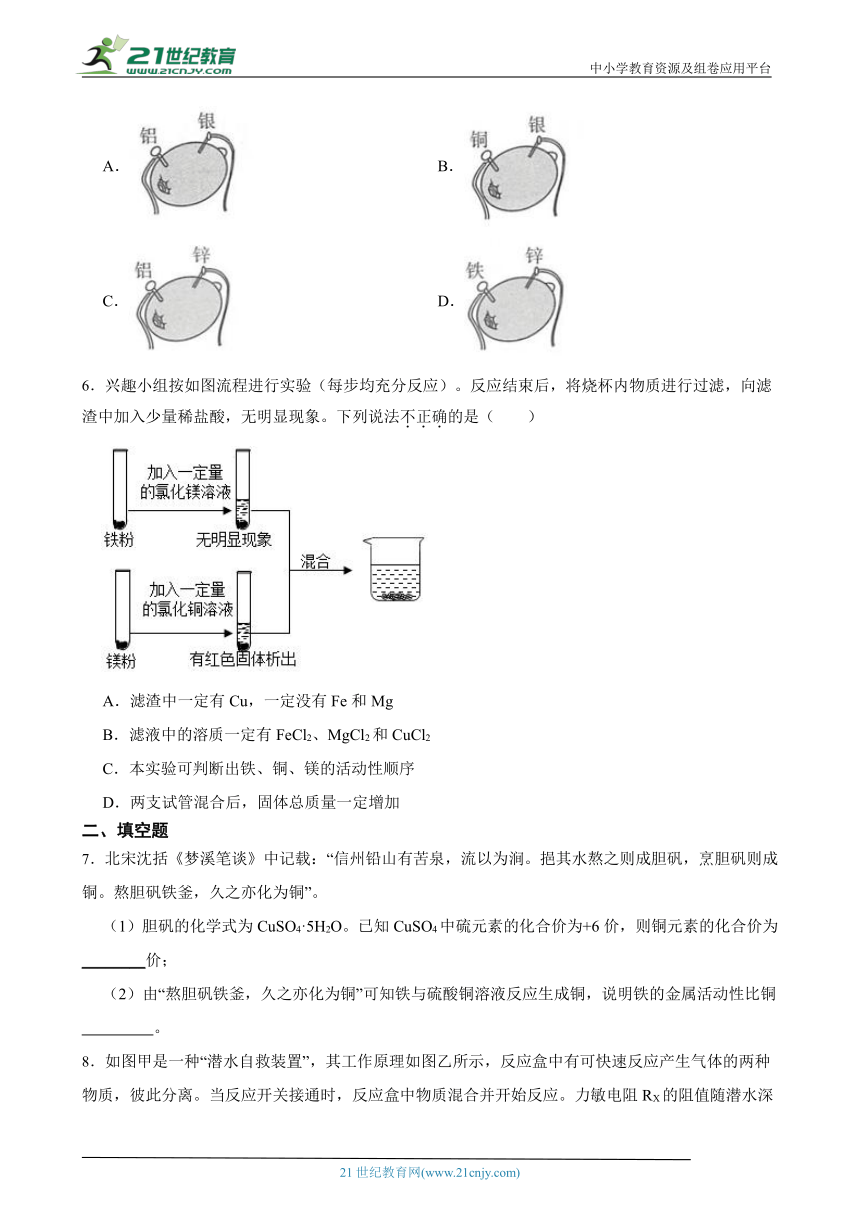
6.兴趣小组按如图流程进行实验(每步均充分反应)。反应结束后,将烧杯内物质进行过滤,向滤渣中加入少量稀盐酸,无明显现象。下列说法不正确的是( ) 21教育名师原创作品
A.滤渣中一定有Cu,一定没有Fe和Mg
B.滤液中的溶质一定有FeCl2、MgCl2和CuCl2
C.本实验可判断出铁、铜、镁的活动性顺序
D.两支试管混合后,固体总质量一定增加
二、填空题
7.北宋沈括《梦溪笔谈》中记载:“信州铅山有苦泉,流以为涧。挹其水熬之则成胆矾,烹胆矾则成铜。熬胆矾铁釜,久之亦化为铜”。
(1)胆矾的化学式为CuSO4·5H2O。已知CuSO4中硫元素的化合价为+6价,则铜元素的化合价为 ________价;
(2)由“熬胆矾铁釜,久之亦化为铜”可知铁与硫酸铜溶液反应生成铜,说明铁的金属活动性比铜
。【来源:21·世纪·教育·网】
8.如图甲是一种“潜水自救装置”,其工作原理如图乙所示,反应盒中有可快速反应产生气体的两种物质,彼此分离。当反应开关接通时,反应盒中物质混合并开始反应。力敏电阻RX的阻值随潜水深度的改变而改变,当达到设定的最大安全深度时,电磁铁吸引衔铁,充气开关接通,气囊快速充气上浮,将潜水运动员拉回到水面。其中U为电源电压,R0为定值电阻。
(1)下列放入A中的物质组合,产生气体速度最快的是 。
A.稀盐酸和铁粉 B.稀盐酸和镁粉 C.稀盐酸和铜粉
(2)请计算HCl中氯元素的质量分数 (保留一位小数)
(3)为实现以上功能,所选RX的阻值应随压力增大而 。(填“增大”或“减小”)
9.我国古代有青铜器的高超熔铸技艺,青铜是铜锡合金,锡的加入可明显提高铜的强度和抗腐蚀性,锡是由锡石冶炼而来。我国古代曾用“湿法炼铜"火法炼铜”。“湿法炼铜"原理:曾青(硫酸铜溶液)得铁则化为铜;“火法炼铜”是用辉铜矿(主要成分Cu2S)炼铜,其原理是:Cu2S与氧气在高温条件下反应生成铜和二氧化硫。 www.21-cn-jy.com
(1)用来冶炼锡的锡石的主要成分SnO2属于 (选填"氧化物""酸"碱"或"盐")。
(2)本材料中,“湿法炼铜"属于 反应(填写反应的基本类型)﹔“火法炼铜”的化学方程式为 。 21*cnjy*com
三、综合说理题
10.铝在空气中久置会慢慢失去光泽,将足量久置在空气中的铝片放入一定量的稀硫酸中, 其放出氢气质量与时间的关系如图所示 (反应时温度变化忽略不计)。查资料得知:
①其他条件相同时,反应物接触面积越大,反应物的浓度越高,反应速度越快;
②反应速率越快,相同时间内生成物的质量越大。请根据上述资料和所学知识解释0-t4各时间段内氢气的质量变化情况。
11.暖宝宝又叫暖贴,在寒冷的冬季外出时,贴于肩部、腹部或关节部位,对防止冻伤驱寒有很好的效果。它不用火、电、水或其他能源,撕开外袋即可发热,并可保持8-18小时左右(平均温度52℃)。
资料一:暖宝宝使用双层包装。外层是常规不透气外袋,内层是由微孔透气膜制成的无纺布袋,里面装有发热材料。
资料二:暖宝宝发热材料主要是铁粉、活性炭、蛭石、水、食盐等。蛭石薄膜状,是当今世界首屈一指的超级保温材料。活性炭有强吸附性,它的疏松结构中储有水蒸气。
资料三:日常生活中,铁质物品在盐溶液中更容易生锈。
注意事项:⒈暖宝宝须妥善保存,避免外袋破损。
⒉不可将暖宝宝直接贴于皮肤表面。
综合上述信息并运用所学知识,解释暖宝宝发热的工作原理,及注意事项。
12.在天平的两个托盘上各放一只烧杯,烧杯中都盛有质量和质量分数相等的稀盐酸,此时天平保持平衡,如果在烧杯中分别同时投入相同质量的足量的锌粉和镁粉。在整个反应过程中天平指针将会如何偏转呢?请判断指针发生偏转的情况并分析原因。
答案解析部分
1.C
置换反应指的是一种单质与另一种化合物反应生成另一种单质和化合物。
通过化学方程式分析反应物和生成物中均有单质和化合物,故其为置换反应。
A.化合反应是多种物质生成一种物质;
B.分解反应一种物质生成多种物质;
D.复分解反应指两种化合物互相交换成分,生成另外两种化合物的反应,叫做复分解反应。
故答案为:C
2.B
常见金属的活动性顺序为钾钙钠镁铝锌铁锡铅(氢)铜汞银铂金;排在氢之前的都能与稀盐酸反应。
由图表可知,2不能与盐酸反应,而铁能与盐酸反应,故R小于铁;又由于R能置换铜,而金属银不行,故R大于银;
故答案为:B
3.B
双吸剂的要求是指能除去潮湿物质中水分的物质,还能延缓食品氧化变质、提高食品稳定性和延长贮存期的食品添加剂。2·1·c·n·j·y
CD.生石灰和氢氧化钠固体都能吸水,但是无法与氧气反应,所以不符合题意;
A.铜粉自然氧化,故不符合题意;
B.铁粉既能吸水,又能与氧气反应;
故答案为:B
4.D
活泼性强胡金属可以把活泼性弱的金属从它的盐溶液中置换出来。且活泼性相差越大,越容易被置换出来。ab段是锌与硝酸银的反应,反应后生成了硝酸锌和银单质。bc段是硝酸铜和锌反应,反应生成了铜和硝酸锌。
2-1-c-n-j-y
A.a点时硝酸银与锌反应过程中,所以硝酸银还有剩余,所以该点胡溶质应该有三种,反应生成胡硝酸锌,没反应完胡硝酸银以及还没开始反应的硝酸铜,所以A错误。
B.c点时,锌与硝酸银,硝酸铜都恰好完全反应完,所以溶质只有反应生成的硝酸锌,所以B错误。
C.b点时,锌与硝酸银恰好完全反应,与硝酸铜还未开始反应,所以沉淀物只有反应生成的银,银活泼性比H弱,加稀盐酸不能反应。故C错误。
D.d点时,锌与硝酸银以及硝酸铜都已经反应完,且锌过量,所以沉淀物有银,铜,锌。故D正确。
5.A
初中科学常考金属活动性顺序为钾 钙 钠 镁 铝 锌 铁 锡 铅 铜 汞 银 铂 金
由上述金属活动性顺序表可知,金属活动性差异最大的是铝和银,故选A.
故答案为:A
6.B
本题主要考查金属的活动性顺序对置换反应进行先后的影响。
由加入稀盐酸无现象可知滤渣中一定有铜,无其他金属;则滤液中一定有氯化镁,氯化亚铜,可能有氯化铜。
A.加入稀盐酸无现象可知滤渣中一定有铜,无其他金属;
【出处:21教育名师】
B.有上述分析可知氯化铜可能还没反应完,故可能有氯化铜;
C.根据第一次时的反应现象即可知三者的活动性,活动性强的金属置换活动性弱的金属;
D.不管是铁置换出铜还是镁置换出铜,由其相对原子质量可知,质量一定增大;
故答案为:B
7.(1)+2
(2)强
化学式各元素的化合价总价为零,以及考查了金属的活动性顺序。
(1)氧元素为-2价,故铜元素为+2价;
(2)活泼性强的金属可置换活泼性弱的金属, 故铁的金属活动性比铜强;
故答案为:(1)+2 ;(2)强21*cnjy*com
8.(1)B
(2)97.3%
(3)减小
(1)根据金属活动性顺序可知,金属活动性Mg>Fe>H>Cu,所以Mg和盐酸产生氢气的速率最快,Fe次之,Cu不与盐酸反应,故答案选择B。
(2)HCl中氯元素的质量分数=。
(3)随着水深度的增加,力敏电阻Rx受到的压力增大。当达到设定的最大安全深度时,电磁铁吸引衔铁,充气开关接通,说明随着深度的增加,电磁铁磁性增强,控制电路的电流增大,在电源电压不变时,Rx的阻值减小,所以答案为“减小”。【来源:21cnj*y.co*m】
9.(1)氧化物
(2)置换;Cu2S+O2=2Cu+SO2
酸的概念:电离时产生的阳离子全部都是氢离子的化合物;碱的概念:电离时产生的阴离子全部都是氢氧根离子的化合物;
21教育网
(1) SnO2属于氧化物,只含有两种元素,其中一种是氧元素的化合物成为氧化物;
(2)置换反应是单质和化合物反应生成新单质和新化合物的反应,所以本材料中,“湿法炼铜"属于置换反应,化学方程式为Cu2S+O2=2Cu+SO2 ;
故答案为:(1) 氧化物 (2)置换、Cu2S+O2=2Cu+SO2【版权所有:21教育】
10.0~t1是氧化铝跟稀硫酸反应,无氢气生成Al2O3+3H2SO4=Al2(SO4)3+3H2O
t1~t2是单质铝与稀硫酸反应2Al+3H2SO4=Al2(SO4)3+3H2↑,此阶段随反应时间增加,氢气的质量不断增加;
t2~t3是随着反应进行硫酸浓度逐渐减小,铝片逐渐减少,反应速率减小,产生氢气速率逐渐减小,但产生的氢气总质量继续增加;
t3~t4是硫酸反应完全,不再产生氢气,氢气的质量不再变化。
根据铝表面有氧化铝膜,加入稀硫酸时,先氧化铝与硫酸反应,此时无气体产生,然后铝再与硫酸反应,产生氢气,且随反应的进行,硫酸的浓度减小,反应速率减慢,最终硫酸过量,反应停止分析。
11.①铁粉接触氧气和水,发生缓慢氧化,缓慢氧化放出热量
②氧气通过内袋透气膜进入里面与材料接触,发生反应。透气膜的透氧速率可以控制放热的时间和温度。
③活性炭粉吸附水蒸气,疏松结构使铁粉与水和氧气的接触面积增大。④食盐加快氧化速度。
⑤蛭石保温,温度能够持续更长时间。
⑥产品在使用前不能发生反应,所以外袋不透气,使里面的材料不接触空气。
⑦暖宝宝产生的热量使平均温度达到52℃,远高于人体正常体温。示例:打开暖宝宝外袋后,内袋暴露在空气中,氧气通过透气膜进入里面与材料接触。透气膜的透氧速率可以控制放热的时间和温度。活性炭粉吸附水蒸气,它的疏松结构使铁粉与水和氧气的接触面积增大。铁粉接触氧气和水,发生缓慢氧化,产生热量。材料中的食盐加快了铁缓慢氧化速度。蛭石是超级保温材料,使温度能够持续8-18小时。21·cn·jy·com
产品在使用前不能发生反应,所以外袋不透气,使里面的材料不接触空气而氧化。暖宝宝产生的热量使平均温度达到52℃,远高于人体正常体温,所以不能直接贴于皮肤表面,以免烫伤。
根据铁粉与氧气和水发生缓慢氧化放热, 透气膜的透氧速率可以控制放热的时间和温度,活性炭可增加药品的接触面积,食盐可加快反应速率,蛭石保温及使用暖宝宝要避免烫伤及药品漏气失效分析。
12.现象:开始时指针偏向锌粉一侧,完全反应后指针指向分度盘中央。
原理:①Zn+2HCl==ZnCl2+H2↑;Mg+2HCl==MgCl2+H2↑
②Mg的金属活动性比Zn强,与相同的盐酸反应时,Mg比Zn更剧烈。
③足量的Mg和Zn与等量的酸充分反应时,生成的氢气质量相等
分析:⑴反应开始时,由于Mg比Zn活泼,相同条件下,Mg与盐酸反应更剧烈,产生氢气更快,放Mg粉的烧杯中剩余物的质量小于锌粉一侧,因此反应开始时指针偏向锌粉一侧。
⑵完全反应后,由于足量的Mg和Zn与等量的酸充分反应时,生成的氢气质量相等,因此两烧杯中剩余物质量也相等,天平指针指向分度盘中央。21世纪教育网版权所有
根据镁的活动性比锌活泼,产生气体快及利用方程式计算等量酸恰好完全反应时最终产生氢气相等分析,再由天平增重质量=加入质量-氢气质量判断天平平衡情况。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
浙教版九上 2.2金属的化学性质 随堂练习
一、单选题
1.早在1637年,我国的科学技术著作《天工开物》已记载了冶炼铅的方法,其主要反应的化学方程式是。该反应属于( ) www-2-1-cnjy-com
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
2.秀秀通过实验探究某种金属R的活动性强弱,并根据实验现象编制检索表如图,根据检索表可知,金属R的活动性强弱排序正确的是( )
A.Fe>Ag>R B.Fe>R>Ag C.R>Fe>Ag D.Ag>R>Fe
3.食品干燥剂是指能除去潮湿物质中水分的物质。食品抗氧化剂是一种延缓食品氧化变质、提高食品稳定性和延长贮存期的食品添加剂,下列物质可用作食品双吸剂的是( )
A.铜粉 B.铁粉
C.生石灰 D.氢氧化钠固体
4.向一定质量AgNO3和Cu(NO3)2的混合溶液中加入n,溶液质量与加入Zn的质量关系如图所示。下列说法正确的是( ) 21·世纪*教育网
A.a点溶液中含有两种溶质
B.c点溶液中的溶质为Zn(NO3)2和Cu(NO3)2
C.取b点的沉淀物,滴加稀盐酸有气泡产生
D.d点沉淀物有Ag、Cu和Zn
5.在柠檬中插入两种不同的金属可以制成水果电池。相同条件下,两种金属的活动性差异越大,水果电池的电压也越大。下列柠檬电池中电压最大的是( ) 21cnjy.com
A. B.
C. D.
6.兴趣小组按如图流程进行实验(每步均充分反应)。反应结束后,将烧杯内物质进行过滤,向滤渣中加入少量稀盐酸,无明显现象。下列说法不正确的是( ) 21教育名师原创作品
A.滤渣中一定有Cu,一定没有Fe和Mg
B.滤液中的溶质一定有FeCl2、MgCl2和CuCl2
C.本实验可判断出铁、铜、镁的活动性顺序
D.两支试管混合后,固体总质量一定增加
二、填空题
7.北宋沈括《梦溪笔谈》中记载:“信州铅山有苦泉,流以为涧。挹其水熬之则成胆矾,烹胆矾则成铜。熬胆矾铁釜,久之亦化为铜”。
(1)胆矾的化学式为CuSO4·5H2O。已知CuSO4中硫元素的化合价为+6价,则铜元素的化合价为 ________价;
(2)由“熬胆矾铁釜,久之亦化为铜”可知铁与硫酸铜溶液反应生成铜,说明铁的金属活动性比铜
。【来源:21·世纪·教育·网】
8.如图甲是一种“潜水自救装置”,其工作原理如图乙所示,反应盒中有可快速反应产生气体的两种物质,彼此分离。当反应开关接通时,反应盒中物质混合并开始反应。力敏电阻RX的阻值随潜水深度的改变而改变,当达到设定的最大安全深度时,电磁铁吸引衔铁,充气开关接通,气囊快速充气上浮,将潜水运动员拉回到水面。其中U为电源电压,R0为定值电阻。
(1)下列放入A中的物质组合,产生气体速度最快的是 。
A.稀盐酸和铁粉 B.稀盐酸和镁粉 C.稀盐酸和铜粉
(2)请计算HCl中氯元素的质量分数 (保留一位小数)
(3)为实现以上功能,所选RX的阻值应随压力增大而 。(填“增大”或“减小”)
9.我国古代有青铜器的高超熔铸技艺,青铜是铜锡合金,锡的加入可明显提高铜的强度和抗腐蚀性,锡是由锡石冶炼而来。我国古代曾用“湿法炼铜"火法炼铜”。“湿法炼铜"原理:曾青(硫酸铜溶液)得铁则化为铜;“火法炼铜”是用辉铜矿(主要成分Cu2S)炼铜,其原理是:Cu2S与氧气在高温条件下反应生成铜和二氧化硫。 www.21-cn-jy.com
(1)用来冶炼锡的锡石的主要成分SnO2属于 (选填"氧化物""酸"碱"或"盐")。
(2)本材料中,“湿法炼铜"属于 反应(填写反应的基本类型)﹔“火法炼铜”的化学方程式为 。 21*cnjy*com
三、综合说理题
10.铝在空气中久置会慢慢失去光泽,将足量久置在空气中的铝片放入一定量的稀硫酸中, 其放出氢气质量与时间的关系如图所示 (反应时温度变化忽略不计)。查资料得知:
①其他条件相同时,反应物接触面积越大,反应物的浓度越高,反应速度越快;
②反应速率越快,相同时间内生成物的质量越大。请根据上述资料和所学知识解释0-t4各时间段内氢气的质量变化情况。
11.暖宝宝又叫暖贴,在寒冷的冬季外出时,贴于肩部、腹部或关节部位,对防止冻伤驱寒有很好的效果。它不用火、电、水或其他能源,撕开外袋即可发热,并可保持8-18小时左右(平均温度52℃)。
资料一:暖宝宝使用双层包装。外层是常规不透气外袋,内层是由微孔透气膜制成的无纺布袋,里面装有发热材料。
资料二:暖宝宝发热材料主要是铁粉、活性炭、蛭石、水、食盐等。蛭石薄膜状,是当今世界首屈一指的超级保温材料。活性炭有强吸附性,它的疏松结构中储有水蒸气。
资料三:日常生活中,铁质物品在盐溶液中更容易生锈。
注意事项:⒈暖宝宝须妥善保存,避免外袋破损。
⒉不可将暖宝宝直接贴于皮肤表面。
综合上述信息并运用所学知识,解释暖宝宝发热的工作原理,及注意事项。
12.在天平的两个托盘上各放一只烧杯,烧杯中都盛有质量和质量分数相等的稀盐酸,此时天平保持平衡,如果在烧杯中分别同时投入相同质量的足量的锌粉和镁粉。在整个反应过程中天平指针将会如何偏转呢?请判断指针发生偏转的情况并分析原因。
答案解析部分
1.C
置换反应指的是一种单质与另一种化合物反应生成另一种单质和化合物。
通过化学方程式分析反应物和生成物中均有单质和化合物,故其为置换反应。
A.化合反应是多种物质生成一种物质;
B.分解反应一种物质生成多种物质;
D.复分解反应指两种化合物互相交换成分,生成另外两种化合物的反应,叫做复分解反应。
故答案为:C
2.B
常见金属的活动性顺序为钾钙钠镁铝锌铁锡铅(氢)铜汞银铂金;排在氢之前的都能与稀盐酸反应。
由图表可知,2不能与盐酸反应,而铁能与盐酸反应,故R小于铁;又由于R能置换铜,而金属银不行,故R大于银;
故答案为:B
3.B
双吸剂的要求是指能除去潮湿物质中水分的物质,还能延缓食品氧化变质、提高食品稳定性和延长贮存期的食品添加剂。2·1·c·n·j·y
CD.生石灰和氢氧化钠固体都能吸水,但是无法与氧气反应,所以不符合题意;
A.铜粉自然氧化,故不符合题意;
B.铁粉既能吸水,又能与氧气反应;
故答案为:B
4.D
活泼性强胡金属可以把活泼性弱的金属从它的盐溶液中置换出来。且活泼性相差越大,越容易被置换出来。ab段是锌与硝酸银的反应,反应后生成了硝酸锌和银单质。bc段是硝酸铜和锌反应,反应生成了铜和硝酸锌。
2-1-c-n-j-y
A.a点时硝酸银与锌反应过程中,所以硝酸银还有剩余,所以该点胡溶质应该有三种,反应生成胡硝酸锌,没反应完胡硝酸银以及还没开始反应的硝酸铜,所以A错误。
B.c点时,锌与硝酸银,硝酸铜都恰好完全反应完,所以溶质只有反应生成的硝酸锌,所以B错误。
C.b点时,锌与硝酸银恰好完全反应,与硝酸铜还未开始反应,所以沉淀物只有反应生成的银,银活泼性比H弱,加稀盐酸不能反应。故C错误。
D.d点时,锌与硝酸银以及硝酸铜都已经反应完,且锌过量,所以沉淀物有银,铜,锌。故D正确。
5.A
初中科学常考金属活动性顺序为钾 钙 钠 镁 铝 锌 铁 锡 铅 铜 汞 银 铂 金
由上述金属活动性顺序表可知,金属活动性差异最大的是铝和银,故选A.
故答案为:A
6.B
本题主要考查金属的活动性顺序对置换反应进行先后的影响。
由加入稀盐酸无现象可知滤渣中一定有铜,无其他金属;则滤液中一定有氯化镁,氯化亚铜,可能有氯化铜。
A.加入稀盐酸无现象可知滤渣中一定有铜,无其他金属;
【出处:21教育名师】
B.有上述分析可知氯化铜可能还没反应完,故可能有氯化铜;
C.根据第一次时的反应现象即可知三者的活动性,活动性强的金属置换活动性弱的金属;
D.不管是铁置换出铜还是镁置换出铜,由其相对原子质量可知,质量一定增大;
故答案为:B
7.(1)+2
(2)强
化学式各元素的化合价总价为零,以及考查了金属的活动性顺序。
(1)氧元素为-2价,故铜元素为+2价;
(2)活泼性强的金属可置换活泼性弱的金属, 故铁的金属活动性比铜强;
故答案为:(1)+2 ;(2)强21*cnjy*com
8.(1)B
(2)97.3%
(3)减小
(1)根据金属活动性顺序可知,金属活动性Mg>Fe>H>Cu,所以Mg和盐酸产生氢气的速率最快,Fe次之,Cu不与盐酸反应,故答案选择B。
(2)HCl中氯元素的质量分数=。
(3)随着水深度的增加,力敏电阻Rx受到的压力增大。当达到设定的最大安全深度时,电磁铁吸引衔铁,充气开关接通,说明随着深度的增加,电磁铁磁性增强,控制电路的电流增大,在电源电压不变时,Rx的阻值减小,所以答案为“减小”。【来源:21cnj*y.co*m】
9.(1)氧化物
(2)置换;Cu2S+O2=2Cu+SO2
酸的概念:电离时产生的阳离子全部都是氢离子的化合物;碱的概念:电离时产生的阴离子全部都是氢氧根离子的化合物;
21教育网
(1) SnO2属于氧化物,只含有两种元素,其中一种是氧元素的化合物成为氧化物;
(2)置换反应是单质和化合物反应生成新单质和新化合物的反应,所以本材料中,“湿法炼铜"属于置换反应,化学方程式为Cu2S+O2=2Cu+SO2 ;
故答案为:(1) 氧化物 (2)置换、Cu2S+O2=2Cu+SO2【版权所有:21教育】
10.0~t1是氧化铝跟稀硫酸反应,无氢气生成Al2O3+3H2SO4=Al2(SO4)3+3H2O
t1~t2是单质铝与稀硫酸反应2Al+3H2SO4=Al2(SO4)3+3H2↑,此阶段随反应时间增加,氢气的质量不断增加;
t2~t3是随着反应进行硫酸浓度逐渐减小,铝片逐渐减少,反应速率减小,产生氢气速率逐渐减小,但产生的氢气总质量继续增加;
t3~t4是硫酸反应完全,不再产生氢气,氢气的质量不再变化。
根据铝表面有氧化铝膜,加入稀硫酸时,先氧化铝与硫酸反应,此时无气体产生,然后铝再与硫酸反应,产生氢气,且随反应的进行,硫酸的浓度减小,反应速率减慢,最终硫酸过量,反应停止分析。
11.①铁粉接触氧气和水,发生缓慢氧化,缓慢氧化放出热量
②氧气通过内袋透气膜进入里面与材料接触,发生反应。透气膜的透氧速率可以控制放热的时间和温度。
③活性炭粉吸附水蒸气,疏松结构使铁粉与水和氧气的接触面积增大。④食盐加快氧化速度。
⑤蛭石保温,温度能够持续更长时间。
⑥产品在使用前不能发生反应,所以外袋不透气,使里面的材料不接触空气。
⑦暖宝宝产生的热量使平均温度达到52℃,远高于人体正常体温。示例:打开暖宝宝外袋后,内袋暴露在空气中,氧气通过透气膜进入里面与材料接触。透气膜的透氧速率可以控制放热的时间和温度。活性炭粉吸附水蒸气,它的疏松结构使铁粉与水和氧气的接触面积增大。铁粉接触氧气和水,发生缓慢氧化,产生热量。材料中的食盐加快了铁缓慢氧化速度。蛭石是超级保温材料,使温度能够持续8-18小时。21·cn·jy·com
产品在使用前不能发生反应,所以外袋不透气,使里面的材料不接触空气而氧化。暖宝宝产生的热量使平均温度达到52℃,远高于人体正常体温,所以不能直接贴于皮肤表面,以免烫伤。
根据铁粉与氧气和水发生缓慢氧化放热, 透气膜的透氧速率可以控制放热的时间和温度,活性炭可增加药品的接触面积,食盐可加快反应速率,蛭石保温及使用暖宝宝要避免烫伤及药品漏气失效分析。
12.现象:开始时指针偏向锌粉一侧,完全反应后指针指向分度盘中央。
原理:①Zn+2HCl==ZnCl2+H2↑;Mg+2HCl==MgCl2+H2↑
②Mg的金属活动性比Zn强,与相同的盐酸反应时,Mg比Zn更剧烈。
③足量的Mg和Zn与等量的酸充分反应时,生成的氢气质量相等
分析:⑴反应开始时,由于Mg比Zn活泼,相同条件下,Mg与盐酸反应更剧烈,产生氢气更快,放Mg粉的烧杯中剩余物的质量小于锌粉一侧,因此反应开始时指针偏向锌粉一侧。
⑵完全反应后,由于足量的Mg和Zn与等量的酸充分反应时,生成的氢气质量相等,因此两烧杯中剩余物质量也相等,天平指针指向分度盘中央。21世纪教育网版权所有
根据镁的活动性比锌活泼,产生气体快及利用方程式计算等量酸恰好完全反应时最终产生氢气相等分析,再由天平增重质量=加入质量-氢气质量判断天平平衡情况。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
