人教版九年级化学 第十一单元 (二)酸、碱、盐化学性质的应用——反应后溶液中溶质成分的探究课件(共19张PPT)
文档属性
| 名称 | 人教版九年级化学 第十一单元 (二)酸、碱、盐化学性质的应用——反应后溶液中溶质成分的探究课件(共19张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 432.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-10 00:00:00 | ||
图片预览




文档简介
(共19张PPT)
酸、碱、盐专题复习
(二)酸、碱、盐化学性质的应用——反应后溶液中溶质成分的探究
目录
01
知识点精讲
02
课堂检测
步 骤 说 明 举例[以Na2CO3和Ca(OH)2的反应为例]
写化学方程式 要正确书写化学方程式
CaCO3↓+2NaOH
知识点 反应后溶液中溶质成分的猜想
步 骤 说 明 举例[以Na2CO3和Ca(OH)2的反应为例]
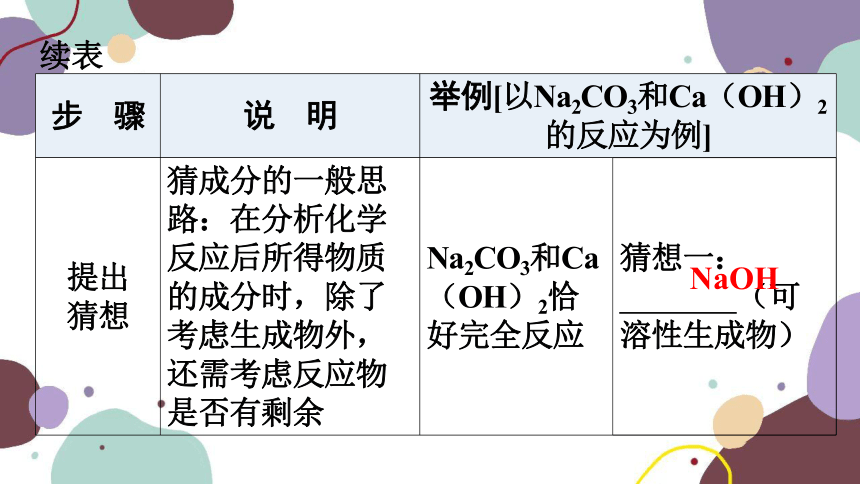
提出 猜想 猜成分的一般思路:在分析化学反应后所得物质的成分时,除了考虑生成物外,还需考虑反应物是否有剩余 Na2CO3和Ca(OH)2恰好完全反应 猜想一: NaOH (可溶性生成物)
NaOH
续表
步 骤 说 明 举例[以Na2CO3和Ca(OH)2的反应为例]
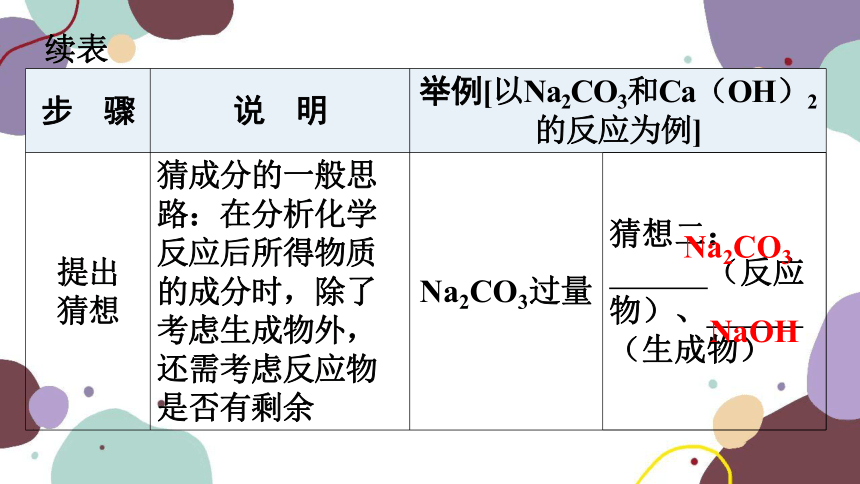
提出 猜想 猜成分的一般思路:在分析化学反应后所得物质的成分时,除了考虑生成物外,还需考虑反应物是否有剩余 Na2CO3过量 猜想二: Na2CO (反应物)、 NaO (生成物)
Na2CO3
NaOH
续表
步 骤 说 明 举例[以Na2CO3和Ca(OH)2的反应为例]
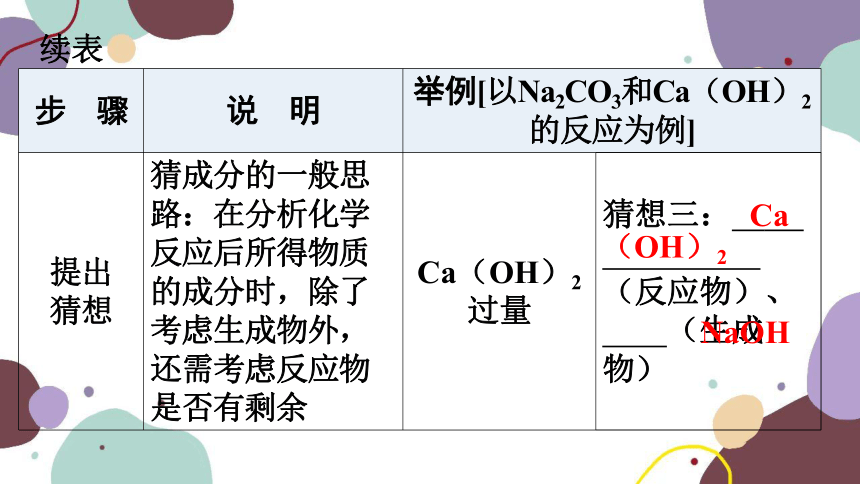
提出 猜想 猜成分的一般思路:在分析化学反应后所得物质的成分时,除了考虑生成物外,还需考虑反应物是否有剩余 Ca(OH)2过量 猜想三: Ca(OH)2 (反应物)、 NaO (生成物)
Ca
(OH)2
NaOH
续表
步 骤 说 明 举例[以Na2CO3和Ca(OH)2的反应为例]
验证 猜想 在验证所得成分时,不需要验证生成物的存在与否,可以利用反应物的性质验证是否有过量的反应物 取少量反应后的滤液于试管中,加入适量Na2CO3溶液,若产生白色沉淀,则猜想 三 正确;若无明显变化,则另取少量反应后滤液于试管中加适量Ca(OH)2,若产生白色沉淀,则猜想 二 正确;若仍无明显变化,则猜想 一 正确
三
二
一
续表
【归纳】(1)反应后溶液的溶质中,生成物一定存在,不参加反应的物质一定存在,反应物可能存在。
(2)反应后溶液的溶质中的生成物一定是可溶性的生成物。反应生成的气体、沉淀不在溶液中,不需考虑;反应生成的水是溶剂,也不需要考虑。
课堂练习
1. 为确定实验室制取CO2后溶液中溶质的成分,可加入适量的( A )
A. CuO B. AgNO3溶液
C. 酚酞溶液 D. Cu
A
2. 化学兴趣小组的同学用大理石和稀盐酸制取二氧化碳,得到反应后的溶液,如果想要验证溶液中溶质的成分,下列试剂不能选用的是( D )
A. 紫色石蕊溶液 B. pH试纸
C. 碳酸钾溶液 D. 硝酸银溶液
D
思路点拨 验证成分时,一定存在的物质不需要验证,选择试剂时,要防止试剂与待验证成分和一定存在的物质产生相同现象而对检验过程造成干扰。
1. 向盛有NaOH和Na2CO3两种溶液的烧杯中加入一定量的稀硫酸,看到产生大量气泡。则停止冒气泡后,下列有关烧杯中溶质成分的推断,错误的是( D )
A. 可能只有Na2SO4
B. 可能是Na2SO4和Na2CO3
C. 可能是Na2SO4和H2SO4
D. 可能是Na2SO4、Na2CO3和NaOH
D
2. 某兴趣小组用氢氧化钠溶液与稀盐酸做中和反应的实验,待反应发生一段时间后,为检验所得溶液中的溶质成分,同学们分别加入四种不同物质并绘制图像,下列图像中不能与其他三个图像得到同一结论的是( C )
C
3. 学习小组同学用如图Z-2-1所示的实验探究完碱的化学性质后,将甲、乙、丙中的无色溶液均倒入洁净的废液缸,发现废液明显变浑浊且呈红色。同学们很好奇,于是接着进行了下列的拓展学习与探究。
图Z-2-1
H2O
小气球逐
渐变大
(2)废液呈红色,说明废液显 碱 性。废液变浑浊,是因为倾倒前丙中的溶液含有 Ca(OH)2 (填化学式)。
碱
Ca(OH)2
【拓展问题】使废液变成红色的物质是什么?
【作出猜想】猜想一:只有Na2CO3;猜想二:只有NaOH;猜想三:NaOH和Ca(OH)2;猜想四:NaOH和Na2CO3。
你认为以上猜想中,不合理的是猜想 一 。
一
【查阅资料】CaCl2溶液呈中性。
【验证猜想】静置一段时间后,取少量废液缸中的上层红色清液于试管中,加入过量CaCl2溶液,有白色沉淀生成。静置后,发现试管中的上层清液仍为红色,由此证明了猜想 四 成立。
四
谢 谢!
酸、碱、盐专题复习
(二)酸、碱、盐化学性质的应用——反应后溶液中溶质成分的探究
目录
01
知识点精讲
02
课堂检测
步 骤 说 明 举例[以Na2CO3和Ca(OH)2的反应为例]
写化学方程式 要正确书写化学方程式
CaCO3↓+2NaOH
知识点 反应后溶液中溶质成分的猜想
步 骤 说 明 举例[以Na2CO3和Ca(OH)2的反应为例]
提出 猜想 猜成分的一般思路:在分析化学反应后所得物质的成分时,除了考虑生成物外,还需考虑反应物是否有剩余 Na2CO3和Ca(OH)2恰好完全反应 猜想一: NaOH (可溶性生成物)
NaOH
续表
步 骤 说 明 举例[以Na2CO3和Ca(OH)2的反应为例]
提出 猜想 猜成分的一般思路:在分析化学反应后所得物质的成分时,除了考虑生成物外,还需考虑反应物是否有剩余 Na2CO3过量 猜想二: Na2CO (反应物)、 NaO (生成物)
Na2CO3
NaOH
续表
步 骤 说 明 举例[以Na2CO3和Ca(OH)2的反应为例]
提出 猜想 猜成分的一般思路:在分析化学反应后所得物质的成分时,除了考虑生成物外,还需考虑反应物是否有剩余 Ca(OH)2过量 猜想三: Ca(OH)2 (反应物)、 NaO (生成物)
Ca
(OH)2
NaOH
续表
步 骤 说 明 举例[以Na2CO3和Ca(OH)2的反应为例]
验证 猜想 在验证所得成分时,不需要验证生成物的存在与否,可以利用反应物的性质验证是否有过量的反应物 取少量反应后的滤液于试管中,加入适量Na2CO3溶液,若产生白色沉淀,则猜想 三 正确;若无明显变化,则另取少量反应后滤液于试管中加适量Ca(OH)2,若产生白色沉淀,则猜想 二 正确;若仍无明显变化,则猜想 一 正确
三
二
一
续表
【归纳】(1)反应后溶液的溶质中,生成物一定存在,不参加反应的物质一定存在,反应物可能存在。
(2)反应后溶液的溶质中的生成物一定是可溶性的生成物。反应生成的气体、沉淀不在溶液中,不需考虑;反应生成的水是溶剂,也不需要考虑。
课堂练习
1. 为确定实验室制取CO2后溶液中溶质的成分,可加入适量的( A )
A. CuO B. AgNO3溶液
C. 酚酞溶液 D. Cu
A
2. 化学兴趣小组的同学用大理石和稀盐酸制取二氧化碳,得到反应后的溶液,如果想要验证溶液中溶质的成分,下列试剂不能选用的是( D )
A. 紫色石蕊溶液 B. pH试纸
C. 碳酸钾溶液 D. 硝酸银溶液
D
思路点拨 验证成分时,一定存在的物质不需要验证,选择试剂时,要防止试剂与待验证成分和一定存在的物质产生相同现象而对检验过程造成干扰。
1. 向盛有NaOH和Na2CO3两种溶液的烧杯中加入一定量的稀硫酸,看到产生大量气泡。则停止冒气泡后,下列有关烧杯中溶质成分的推断,错误的是( D )
A. 可能只有Na2SO4
B. 可能是Na2SO4和Na2CO3
C. 可能是Na2SO4和H2SO4
D. 可能是Na2SO4、Na2CO3和NaOH
D
2. 某兴趣小组用氢氧化钠溶液与稀盐酸做中和反应的实验,待反应发生一段时间后,为检验所得溶液中的溶质成分,同学们分别加入四种不同物质并绘制图像,下列图像中不能与其他三个图像得到同一结论的是( C )
C
3. 学习小组同学用如图Z-2-1所示的实验探究完碱的化学性质后,将甲、乙、丙中的无色溶液均倒入洁净的废液缸,发现废液明显变浑浊且呈红色。同学们很好奇,于是接着进行了下列的拓展学习与探究。
图Z-2-1
H2O
小气球逐
渐变大
(2)废液呈红色,说明废液显 碱 性。废液变浑浊,是因为倾倒前丙中的溶液含有 Ca(OH)2 (填化学式)。
碱
Ca(OH)2
【拓展问题】使废液变成红色的物质是什么?
【作出猜想】猜想一:只有Na2CO3;猜想二:只有NaOH;猜想三:NaOH和Ca(OH)2;猜想四:NaOH和Na2CO3。
你认为以上猜想中,不合理的是猜想 一 。
一
【查阅资料】CaCl2溶液呈中性。
【验证猜想】静置一段时间后,取少量废液缸中的上层红色清液于试管中,加入过量CaCl2溶液,有白色沉淀生成。静置后,发现试管中的上层清液仍为红色,由此证明了猜想 四 成立。
四
谢 谢!
同课章节目录
