7.2.2烃 乙炔与苯 课件(共21张ppt)化学人教版(2019)必修第二册
文档属性
| 名称 | 7.2.2烃 乙炔与苯 课件(共21张ppt)化学人教版(2019)必修第二册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 19.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-11 00:00:00 | ||
图片预览





文档简介
(共21张PPT)
第七章 有机化合物
第二节 乙烯与有机高分子材料
课时2 烃
学习目标:知道烃的概念及分类,了解烷烃、烯烃、炔烃、芳香烃的组成、结构及其性质特点。
一、烃的概念和分类
1.概念
仅含C和H两种元素的有机物,称为碳氢化合物,也称为烃。
下列物质属于烃的是:
H2S、 C2H2、 CH3Cl、 C2H5OH、 CH4、 H2、 金刚石、 CH3COOH、 CO2、 C2H4
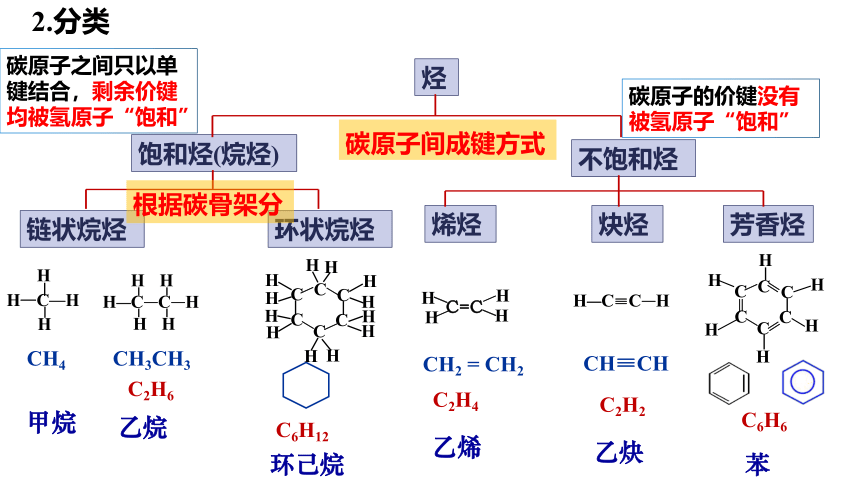
2.分类
烃
饱和烃(烷烃)
不饱和烃
链状烷烃
环状烷烃
烯烃
炔烃
芳香烃
H—C—C—H
H
H
H
H
H—C—H
H
H
H—C≡C—H
C
H
H
H
H
—
C
C
C
C
C
—
—
—
H
H
H
H
H
H
H
H
—
—
C=C
H
—
—
H
H
H
‖
C
H
—
C
C
C
C
C
—
H
H
H
H
H
‖
‖
CH2 = CH2
CH≡CH
CH4
C2H6
CH3CH3
C2H4
C2H2
C6H6
C6H12
甲烷
乙烷
环己烷
乙烯
乙炔
苯
碳原子间成键方式
根据碳骨架分
碳原子之间只以单键结合,剩余价键均被氢原子“饱和”
碳原子的价键没有被氢原子“饱和”
烃 结构特点 分子通式 不饱和度
烷烃
环烷烃
单烯烃
单炔烃
苯及苯的同系物
仅含“C-C”链状
只含一个“C= C”链状
只含一个苯环的芳香烃
仅含“C—C”环状
只含一个含“C≡ C”链状
CnH2n+2(n≥1)
CnH2n (n≥2)
CnH2n -6(n≥6)
CnH2n (n≥3)
CnH2n -2(n≥2)
1
1
2
——
烃分子中结合的氢原子数少于相同碳原子链烷烃中的氢原子数,就具有一定的不饱和度。每少2个H原子,算为1个不饱和度。
4
【归纳整理】
1. 烃有不同的分类方法,下列说法正确的是( )
① 按烃分子中碳的成键方式分: 饱和烃、 不饱和烃
② 按烃分子中碳骨架的形状分: 链状烃、 环状烃
③ 根据不饱和烃中不饱和键的类型分: 烯烃、炔烃、芳香烃等
④ 可划分为烃、环状烃、烯烃
A.①③④ B.①②③ C.①②④ D.②③④
B
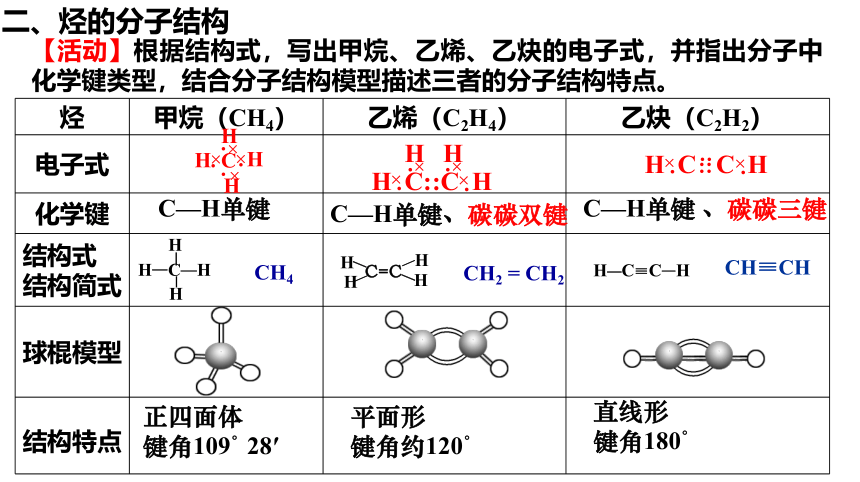
烃 甲烷(CH4) 乙烯(C2H4) 乙炔(C2H2)
电子式
化学键
结构式 结构简式
球棍模型
结构特点
.
×
.
×
H
C
H
H
.
×
.
×
H
H
H
.×
H C::C H
.×
.×
.×
H C C H
.×
.×
::
:
H—C—H
H
H
—
—
C=C
H
—
—
H
H
H
H—C≡C—H
CH2 = CH2
CH4
CH≡CH
C—H单键
C—H单键、碳碳双键
C—H单键 、碳碳三键
平面形
键角约120°
直线形
键角180°
正四面体
键角109°28′
二、烃的分子结构
【活动】根据结构式,写出甲烷、乙烯、乙炔的电子式,并指出分子中化学键类型,结合分子结构模型描述三者的分子结构特点。
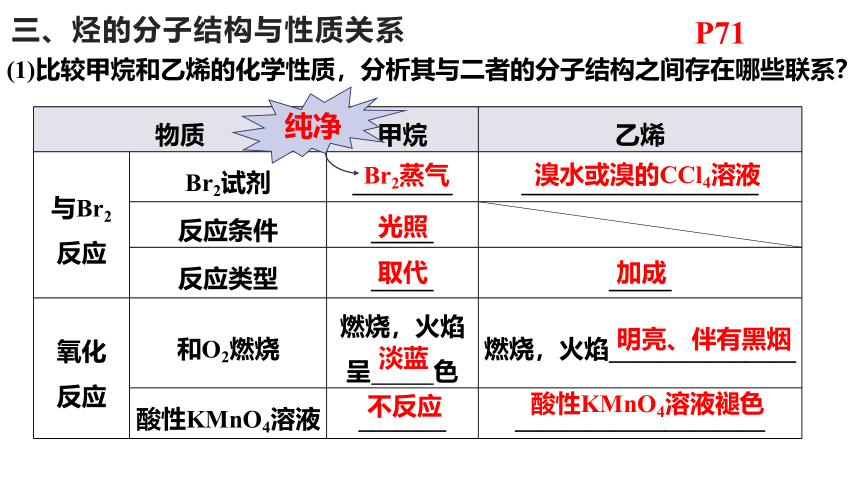
三、烃的分子结构与性质关系
(1)比较甲烷和乙烯的化学性质,分析其与二者的分子结构之间存在哪些联系?
物质 甲烷 乙烯
与Br2 反应 Br2试剂 ________ ___________________
反应条件 _____
反应类型 _____ _____
氧化 反应 和O2燃烧 燃烧,火焰 呈 色 燃烧,火焰_______________
酸性KMnO4溶液 _______ ____________________
Br2蒸气
溴水或溴的CCl4溶液
光照
取代
加成
淡蓝
明亮、伴有黑烟
不反应
酸性KMnO4溶液褪色
纯净
P71
(1)比较甲烷和乙烯的化学性质,分析其与二者的分子结构之间存在哪些联系?
性质和结构关系 CH4分子中的碳原子为 结构,所成的键为 ,性质 ,主要发生 反应 CH2==CH2分子中的碳原子为_ 结构,所成的键为 ,其中一个键容易断裂,性质活泼,主要发生 、 反应
饱和
单键
稳定
取代
不饱和
碳碳双键
加成反应
氧化
结论:烷烃、烯烃、均可燃烧;其中烷烃易取代,而烯烃,易加成。 烯烃能与酸性高锰酸钾溶液发生氧化反应。
(2) 乙炔是甲烷或乙烯的同系物吗?为什么?
不是,结构不相似,在分子组成上也不相差一个或若干个CH2原子团。
三、烃的分子结构与性质关系
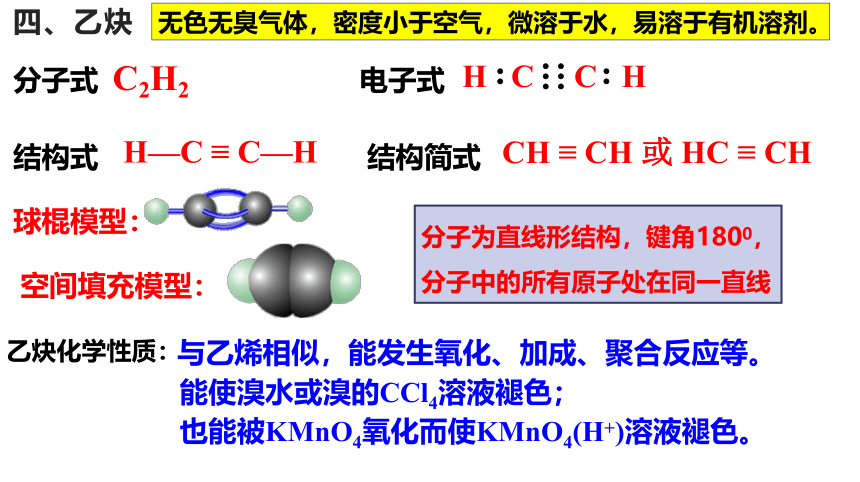
四、乙炔
分子式 电子式
结构式 结构简式
球棍模型:
空间填充模型:
C2H2
H C C H
H—C ≡ C—H
CH ≡ CH 或 HC ≡ CH
分子为直线形结构,键角1800,分子中的所有原子处在同一直线
无色无臭气体,密度小于空气,微溶于水,易溶于有机溶剂。
乙炔化学性质:
与乙烯相似,能发生氧化、加成、聚合反应等。
能使溴水或溴的CCl4溶液褪色;
也能被KMnO4氧化而使KMnO4(H+)溶液褪色。
化学性质
(1)氧化反应:燃烧,使酸性高锰酸钾褪色。
(2)加成反应:与H2、Br2、HX等
(3)加聚反应
2C2H2 + 5O2 4CO2 + 2H2O
现象:明亮火焰,且伴有浓烈的黑烟
四、乙炔
H—C C—H
Br
Br
H—C C—H+Br—Br
能使溴水或溴的四氯化碳溶液褪色
nCH CH
CH=CH
n
催化剂
聚乙炔:导电塑料
2. 下列关于乙烷、乙烯、乙炔的说法正确的个数( )
①它们不是同系物,也不具有相似的性质
②乙烷是饱和烃,乙烯、乙炔是不饱和烃
③乙烯、乙炔能使溴水褪色,乙烷不能使溴水褪色
④它们都能燃烧,乙炔燃烧火焰应该最明亮,有浓烟
⑤它们都能使酸性KMnO4溶液褪色
A.2个 B.3个 C.4个 D.5个
C
√
√
√
×
√
1.写出乙炔分别与氢气、氯气、氯化氢发生加成反应的化学方程式。
CH≡CH + HCl CH2═CHCl
催化剂
1.芳香族化合物:分子中含有苯环的有机物。
分子式 结构式 结构简式 空间填充模型 空间形状
或
五、苯
科学史话
2.苯的组成与结构
凯库勒式
结构特点:
1.具有平面正六边形结构,所有原子(十二原子)均在同一平面上。
2.苯环中所有碳碳键等同,是一种介于单键和双键之间的独特的键。
3.苯中的6个碳原子是等效的,6 个氢原子也是等效的。
苯:无色液体,有毒、有气味,密度小于水,难溶于水。
(苯是最简单的芳香烃)
平面正六边形
C6H6
思考:根据苯的成键方式和结构推测其可能有哪些化学性质?
①氧化反应:
点燃
2C6H6 + 15O2 12CO2 + 6H2O
浓烈黑烟
苯不能使酸性KMnO4溶液褪色,也不与溴水反应。
③加成反应:
Ni
+ 3H2
②取代反应:
+ Br2
FeBr3
反应物:苯和液溴(不能用溴水)
Br
+ HBr
4.苯的化学性质
思考:可否用酸性KMnO4溶液区分苯(密度小于水)和四氯化碳(密度大于水)?
(鉴别甲烷、乙烯和苯)
预测:将苯通入溴水中会有什么现象?
小结:苯环具有特殊的稳定性,易取代,能加成,难氧化。
3、根据烷烃通式,结合乙烯、乙炔与乙烷的球棍模型分析得出环烷烃、烯烃、炔烃的分子组成通式各是什么?
链状烷烃的分子组成通式为CnH2n+2
烯烃的分子组成通式为CnH2n(n≥2)
环烷烃的分子组成通式为CnH2n (n≥3)
炔烃的分子组成通式为CnH2n-2(n≥2)
单
单
(只含一个碳碳双键)
(只含一个碳碳三键)
七、苯的同系物
分子结构中只含一个苯环,与苯分子组成相差一个或若干个CH2原子团的同一系列有机物。
分子通式:CnH2n-6(n≥6)
C7H8
C8H10
C6H6
(一)分子结构特点:均只含一个苯环,支链为烷烃基。
苯的同系物可看作是苯分子结构中氢原子被链烷基取代后的产物。
思考:有机物 是苯的同系物吗?
萘 属稠环芳香烃
思考:以下三种物质是何种关系?
CH3
CH3
CH3
2. 苯乙烯是一种重要的有机化工原料,其结构简式为 它不可能具有的性质是( )
A. 易溶于水,不易溶于有机溶剂
B. 在空气中燃烧产生黑烟
C. 它能使溴的四氯化碳溶液褪色,也能使酸性高锰酸钾溶液褪色
D. 能发生加成反应
A
烃 乙烯(C2H4) 乙炔(C2H2) 苯(C6H6)
球棍模型
结构简式
碳碳键
结构特点
化学 性质
CH2 = CH2
双键
三键
平面型
键角:120°
氧化反应
加成反应
加聚反应
CH ≡ CH
或 HC ≡ CH
直线型
键角:180°
氧化反应
加成反应
加聚反应
介于单键和双键之间特殊的化学键
平面正六边形键角:120°
氧化反应
取代反应
加成反应
所有原子共直线
所有原子共平面
所有原子共平面
小结
原子间成键方式
空间构型
四面体形
平面形
直线形
平面形
键角
一定共面原子
109°28′
约120°
180°
120°
3个
6个
4个(共线)
12个
对称轴上原子是共线
有机物共面共线问题
1、代表物(结构不同的基团母体)的空间构型
1.在①丙烯、②氯乙烯、③苯、④甲苯⑤1,3 丁二烯( )五种有机化合物中,分子内所有原子均可在同一平面的是( )
A.①② B.②③⑤ C.③④ D.②④⑤
B
2. 下列有机分子中,所有原子不可能处于同一平面的是( )
D
3. 下列关于CH3—CH=CH—C≡C—CF3分子的结构叙述正确的是( )
A、6个碳原子有可能都在一条直线上
B、6个碳原子不可能都在一条直线上
C、6个碳原子一定都在同一平面上
D、6个碳原子不可能都在同一平面上
BC
第七章 有机化合物
第二节 乙烯与有机高分子材料
课时2 烃
学习目标:知道烃的概念及分类,了解烷烃、烯烃、炔烃、芳香烃的组成、结构及其性质特点。
一、烃的概念和分类
1.概念
仅含C和H两种元素的有机物,称为碳氢化合物,也称为烃。
下列物质属于烃的是:
H2S、 C2H2、 CH3Cl、 C2H5OH、 CH4、 H2、 金刚石、 CH3COOH、 CO2、 C2H4
2.分类
烃
饱和烃(烷烃)
不饱和烃
链状烷烃
环状烷烃
烯烃
炔烃
芳香烃
H—C—C—H
H
H
H
H
H—C—H
H
H
H—C≡C—H
C
H
H
H
H
—
C
C
C
C
C
—
—
—
H
H
H
H
H
H
H
H
—
—
C=C
H
—
—
H
H
H
‖
C
H
—
C
C
C
C
C
—
H
H
H
H
H
‖
‖
CH2 = CH2
CH≡CH
CH4
C2H6
CH3CH3
C2H4
C2H2
C6H6
C6H12
甲烷
乙烷
环己烷
乙烯
乙炔
苯
碳原子间成键方式
根据碳骨架分
碳原子之间只以单键结合,剩余价键均被氢原子“饱和”
碳原子的价键没有被氢原子“饱和”
烃 结构特点 分子通式 不饱和度
烷烃
环烷烃
单烯烃
单炔烃
苯及苯的同系物
仅含“C-C”链状
只含一个“C= C”链状
只含一个苯环的芳香烃
仅含“C—C”环状
只含一个含“C≡ C”链状
CnH2n+2(n≥1)
CnH2n (n≥2)
CnH2n -6(n≥6)
CnH2n (n≥3)
CnH2n -2(n≥2)
1
1
2
——
烃分子中结合的氢原子数少于相同碳原子链烷烃中的氢原子数,就具有一定的不饱和度。每少2个H原子,算为1个不饱和度。
4
【归纳整理】
1. 烃有不同的分类方法,下列说法正确的是( )
① 按烃分子中碳的成键方式分: 饱和烃、 不饱和烃
② 按烃分子中碳骨架的形状分: 链状烃、 环状烃
③ 根据不饱和烃中不饱和键的类型分: 烯烃、炔烃、芳香烃等
④ 可划分为烃、环状烃、烯烃
A.①③④ B.①②③ C.①②④ D.②③④
B
烃 甲烷(CH4) 乙烯(C2H4) 乙炔(C2H2)
电子式
化学键
结构式 结构简式
球棍模型
结构特点
.
×
.
×
H
C
H
H
.
×
.
×
H
H
H
.×
H C::C H
.×
.×
.×
H C C H
.×
.×
::
:
H—C—H
H
H
—
—
C=C
H
—
—
H
H
H
H—C≡C—H
CH2 = CH2
CH4
CH≡CH
C—H单键
C—H单键、碳碳双键
C—H单键 、碳碳三键
平面形
键角约120°
直线形
键角180°
正四面体
键角109°28′
二、烃的分子结构
【活动】根据结构式,写出甲烷、乙烯、乙炔的电子式,并指出分子中化学键类型,结合分子结构模型描述三者的分子结构特点。
三、烃的分子结构与性质关系
(1)比较甲烷和乙烯的化学性质,分析其与二者的分子结构之间存在哪些联系?
物质 甲烷 乙烯
与Br2 反应 Br2试剂 ________ ___________________
反应条件 _____
反应类型 _____ _____
氧化 反应 和O2燃烧 燃烧,火焰 呈 色 燃烧,火焰_______________
酸性KMnO4溶液 _______ ____________________
Br2蒸气
溴水或溴的CCl4溶液
光照
取代
加成
淡蓝
明亮、伴有黑烟
不反应
酸性KMnO4溶液褪色
纯净
P71
(1)比较甲烷和乙烯的化学性质,分析其与二者的分子结构之间存在哪些联系?
性质和结构关系 CH4分子中的碳原子为 结构,所成的键为 ,性质 ,主要发生 反应 CH2==CH2分子中的碳原子为_ 结构,所成的键为 ,其中一个键容易断裂,性质活泼,主要发生 、 反应
饱和
单键
稳定
取代
不饱和
碳碳双键
加成反应
氧化
结论:烷烃、烯烃、均可燃烧;其中烷烃易取代,而烯烃,易加成。 烯烃能与酸性高锰酸钾溶液发生氧化反应。
(2) 乙炔是甲烷或乙烯的同系物吗?为什么?
不是,结构不相似,在分子组成上也不相差一个或若干个CH2原子团。
三、烃的分子结构与性质关系
四、乙炔
分子式 电子式
结构式 结构简式
球棍模型:
空间填充模型:
C2H2
H C C H
H—C ≡ C—H
CH ≡ CH 或 HC ≡ CH
分子为直线形结构,键角1800,分子中的所有原子处在同一直线
无色无臭气体,密度小于空气,微溶于水,易溶于有机溶剂。
乙炔化学性质:
与乙烯相似,能发生氧化、加成、聚合反应等。
能使溴水或溴的CCl4溶液褪色;
也能被KMnO4氧化而使KMnO4(H+)溶液褪色。
化学性质
(1)氧化反应:燃烧,使酸性高锰酸钾褪色。
(2)加成反应:与H2、Br2、HX等
(3)加聚反应
2C2H2 + 5O2 4CO2 + 2H2O
现象:明亮火焰,且伴有浓烈的黑烟
四、乙炔
H—C C—H
Br
Br
H—C C—H+Br—Br
能使溴水或溴的四氯化碳溶液褪色
nCH CH
CH=CH
n
催化剂
聚乙炔:导电塑料
2. 下列关于乙烷、乙烯、乙炔的说法正确的个数( )
①它们不是同系物,也不具有相似的性质
②乙烷是饱和烃,乙烯、乙炔是不饱和烃
③乙烯、乙炔能使溴水褪色,乙烷不能使溴水褪色
④它们都能燃烧,乙炔燃烧火焰应该最明亮,有浓烟
⑤它们都能使酸性KMnO4溶液褪色
A.2个 B.3个 C.4个 D.5个
C
√
√
√
×
√
1.写出乙炔分别与氢气、氯气、氯化氢发生加成反应的化学方程式。
CH≡CH + HCl CH2═CHCl
催化剂
1.芳香族化合物:分子中含有苯环的有机物。
分子式 结构式 结构简式 空间填充模型 空间形状
或
五、苯
科学史话
2.苯的组成与结构
凯库勒式
结构特点:
1.具有平面正六边形结构,所有原子(十二原子)均在同一平面上。
2.苯环中所有碳碳键等同,是一种介于单键和双键之间的独特的键。
3.苯中的6个碳原子是等效的,6 个氢原子也是等效的。
苯:无色液体,有毒、有气味,密度小于水,难溶于水。
(苯是最简单的芳香烃)
平面正六边形
C6H6
思考:根据苯的成键方式和结构推测其可能有哪些化学性质?
①氧化反应:
点燃
2C6H6 + 15O2 12CO2 + 6H2O
浓烈黑烟
苯不能使酸性KMnO4溶液褪色,也不与溴水反应。
③加成反应:
Ni
+ 3H2
②取代反应:
+ Br2
FeBr3
反应物:苯和液溴(不能用溴水)
Br
+ HBr
4.苯的化学性质
思考:可否用酸性KMnO4溶液区分苯(密度小于水)和四氯化碳(密度大于水)?
(鉴别甲烷、乙烯和苯)
预测:将苯通入溴水中会有什么现象?
小结:苯环具有特殊的稳定性,易取代,能加成,难氧化。
3、根据烷烃通式,结合乙烯、乙炔与乙烷的球棍模型分析得出环烷烃、烯烃、炔烃的分子组成通式各是什么?
链状烷烃的分子组成通式为CnH2n+2
烯烃的分子组成通式为CnH2n(n≥2)
环烷烃的分子组成通式为CnH2n (n≥3)
炔烃的分子组成通式为CnH2n-2(n≥2)
单
单
(只含一个碳碳双键)
(只含一个碳碳三键)
七、苯的同系物
分子结构中只含一个苯环,与苯分子组成相差一个或若干个CH2原子团的同一系列有机物。
分子通式:CnH2n-6(n≥6)
C7H8
C8H10
C6H6
(一)分子结构特点:均只含一个苯环,支链为烷烃基。
苯的同系物可看作是苯分子结构中氢原子被链烷基取代后的产物。
思考:有机物 是苯的同系物吗?
萘 属稠环芳香烃
思考:以下三种物质是何种关系?
CH3
CH3
CH3
2. 苯乙烯是一种重要的有机化工原料,其结构简式为 它不可能具有的性质是( )
A. 易溶于水,不易溶于有机溶剂
B. 在空气中燃烧产生黑烟
C. 它能使溴的四氯化碳溶液褪色,也能使酸性高锰酸钾溶液褪色
D. 能发生加成反应
A
烃 乙烯(C2H4) 乙炔(C2H2) 苯(C6H6)
球棍模型
结构简式
碳碳键
结构特点
化学 性质
CH2 = CH2
双键
三键
平面型
键角:120°
氧化反应
加成反应
加聚反应
CH ≡ CH
或 HC ≡ CH
直线型
键角:180°
氧化反应
加成反应
加聚反应
介于单键和双键之间特殊的化学键
平面正六边形键角:120°
氧化反应
取代反应
加成反应
所有原子共直线
所有原子共平面
所有原子共平面
小结
原子间成键方式
空间构型
四面体形
平面形
直线形
平面形
键角
一定共面原子
109°28′
约120°
180°
120°
3个
6个
4个(共线)
12个
对称轴上原子是共线
有机物共面共线问题
1、代表物(结构不同的基团母体)的空间构型
1.在①丙烯、②氯乙烯、③苯、④甲苯⑤1,3 丁二烯( )五种有机化合物中,分子内所有原子均可在同一平面的是( )
A.①② B.②③⑤ C.③④ D.②④⑤
B
2. 下列有机分子中,所有原子不可能处于同一平面的是( )
D
3. 下列关于CH3—CH=CH—C≡C—CF3分子的结构叙述正确的是( )
A、6个碳原子有可能都在一条直线上
B、6个碳原子不可能都在一条直线上
C、6个碳原子一定都在同一平面上
D、6个碳原子不可能都在同一平面上
BC
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
