第八章化学与可持续发展测试(含解析)2022-2023学年高一下学期化学人教版(2019)必修第二册
文档属性
| 名称 | 第八章化学与可持续发展测试(含解析)2022-2023学年高一下学期化学人教版(2019)必修第二册 |

|
|
| 格式 | docx | ||
| 文件大小 | 103.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-11 00:00:00 | ||
图片预览




文档简介
第八章 化学与可持续发展 测试
一、单选题
1.下列制备物质的转化关系不合理的是
A.制:
B.制:
C.制NaOH:海水NaCl溶液NaOH
D.制Mg:海水溶液
2.化学与人类生产、生活、科研密切相关,下列有关说法不正确的是
A.工业上电解熔融Al2O3冶炼Al
B.维生素C常用作抗氧化剂,说明它具有还原性
C.糖类、蛋白质和油脂都属于营养物质,都能发生水解反应
D.工业生产玻璃、水泥,均需用石灰石作原料
3.下列说法正确的是
A.分馏石油可以得到汽油、柴油、植物油和润滑油
B.棉花和蚕丝的主要成分都是纤维素
C.水煤气可用来合成液态烃及甲醇等含氧有机物
D.糖类、油脂、蛋白质都属于有机高分子化合物
4.化学与人类生产、生活及社会可持续发展密切相关,下列说法正确的是
A.春晚直播间高清摄像头镜片的主要成分是单质硅
B.嫦娥五号采样返回器带回的月壤含有MgO·FeO·SiO2,该物质属于氧化物
C.燃煤“气化”、“脱硫”、“钙基固硫”等措施有利于减少SO2排放和酸雨形成
D.臭氧/生物活性炭技术可用于饮用水的深度处理,该原理利用了活性炭的还原性
5.下列物质中,可用作食品抗氧化剂的是
A.抗坏血酸 B.硫酸钙 C.三聚氰胺 D.碳酸镁
6.下列有关叙述错误的是( )
A.石油裂化是为了获得更多的汽油,裂解是为了获得气态烃
B.煤经过干馏可得到焦炭、煤焦油和焦炉气
C.甲烷、汽油、酒精都是烃类,都可作燃料
D.甲醛的水溶液俗称福尔马林,可杀菌防腐,但不可用于食品保鲜
7.习近平主席在十九大报告中指出,坚持人与自然和谐共生。必须树立和践行绿水青山就是金山银山的理念,坚持节约资源和保护环境的基本国策。下列说法错误的是
A.酸雨是指pH小于7的雨水
B.汽车尾气已成为许多城市空气的主要污染源
C.可以用生石灰作为脱硫剂以减少工业废气SO2的排放
D.二氧化硫、二氧化氮和可吸入颗粒物是大气主要污染物
8.下列有关化学用品的安全使用(或措施)正确的是
A.在实验室发现钠着火时,立即用水浇灭
B.装运乙醇的包装箱上应贴上易燃液体的危险品标志图标
C.为了预防新冠肺炎,在家中关闭门窗用大量的95%的酒精进行环境消毒
D.食品添加剂为各种各样的化学物质,所以国家应立法杜绝使用食品添加剂
9.下列物质不属于“城市空气质量日报”报道的是
A.氮氧化物 B.二氧化碳 C.PM2.5 D.二氧化硫
10.下列关于煤、石油、天然气等资源的说法中正确的是
A.石油裂解得到的汽油是纯净物
B.石油产品都可用于聚合反应
C.天然气是一种清洁的化工原料
D.水煤气是通过煤的液化得到的气体燃料
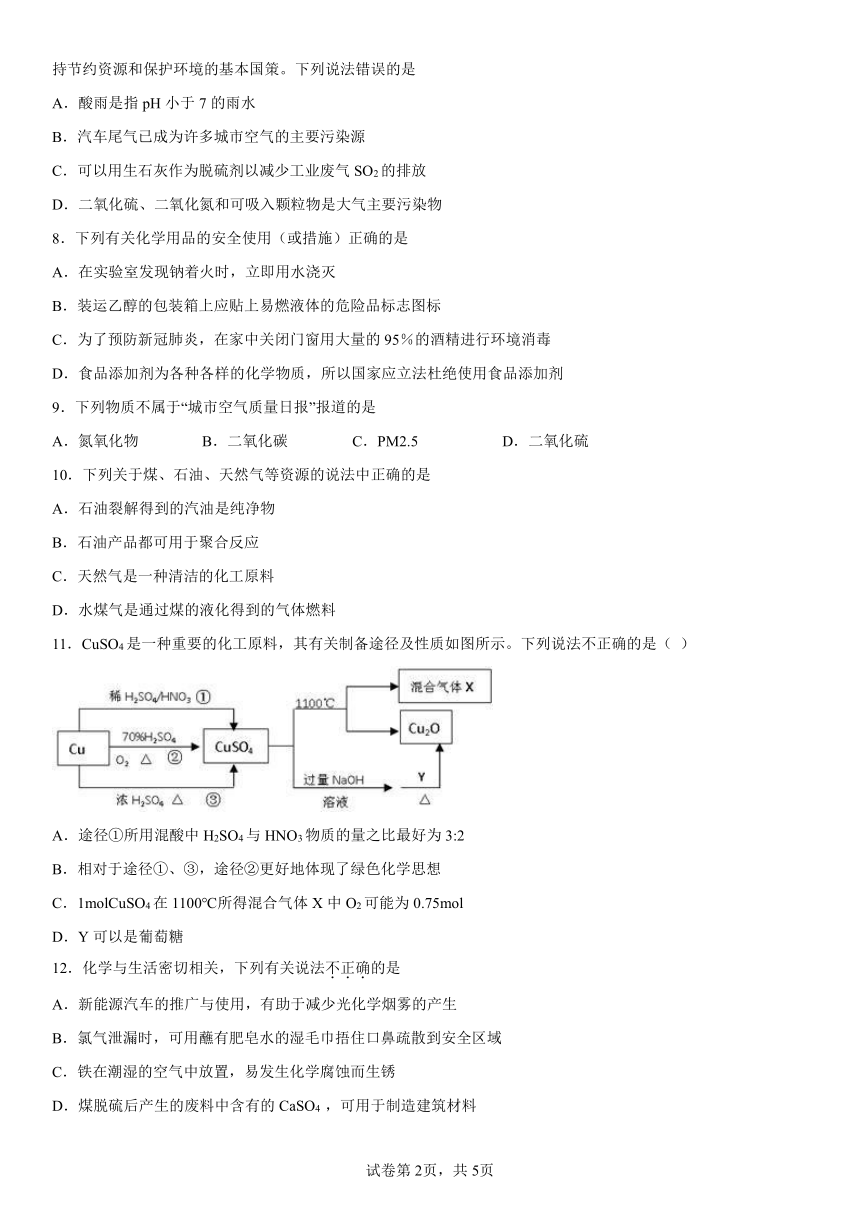
11.CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是( )
A.途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2
B.相对于途径①、③,途径②更好地体现了绿色化学思想
C.1molCuSO4在1100℃所得混合气体X中O2可能为0.75mol
D.Y可以是葡萄糖
12.化学与生活密切相关,下列有关说法不正确的是
A.新能源汽车的推广与使用,有助于减少光化学烟雾的产生
B.氯气泄漏时,可用蘸有肥皂水的湿毛巾捂住口鼻疏散到安全区域
C.铁在潮湿的空气中放置,易发生化学腐蚀而生锈
D.煤脱硫后产生的废料中含有的CaSO4 ,可用于制造建筑材料
二、填空题
13.金属元素的原子结构决定了金属元素的性质、在自然界中的存在形式及冶炼方法。
(1)金属的冶炼一般有下列方法:
a.焦炭法
b.水煤气(氢气和一氧化碳)法
c.活泼金属置换法
d.电解法
请从上述四种方法中选择相应的字母填入表中空格:
高炉炼铁 湿法炼铜 铝热法炼铬 工业上冶炼铝
______ ______ ______ ______
写出Al与Cr2O3反应的化学方程式:__________。
(2)铜在地壳中的含量远低于铝,但人类利用铜的历史远早于铝,这与古代发生的森林大火有一定的关系,因为人类在大火之后的灰烬中会发现红色发亮的物质。现在人们认识到,这种物质就是孔雀石[主要成分为Cu2(OH)2CO3,热稳定性差]在大火中转化而生成的铜,写出大火中与铜元素有关的三个化学方程式:______。
14.海洋是一座巨大的化学资源宝库,从中可以提取多种化学物质。从淡化海水中提取溴是海水综合利用的重要途径,其流程如下:
完成下列填空:
(1)过程II中物质X可以选SO2吸收溴,写出该反应的化学方程式__________。
(2)过程I、II要达到的目的是______________。
(3)写出过程III反应的离子方程式___________。
(4)若过程II中物质X选Na2CO3吸收溴,发生如下反应:3Br2 +6Na2CO3 +3H2O == 5NaBr +NaBrO3 +6NaHCO3
①反应中被氧化与被还原的溴的物质的量之比为_______________。
②反应中消耗3 mol Br2转移电子的物质的量为__________。
③在含有NaBr、NaBrO3的混合溶液中加入适量的稀硫酸酸化即可得到溴,写出该反应的离子方程式__________。
15.下表是某食品包装上的说明,表中列出了部分配料。
品名 好吃你就多吃点
部分配料 ① 奶粉 ②白砂糖③ 乳酸钙 ④ 山梨酸钾
生产日期 标于包装封口处
配料中,富含蛋白质的是_______,属于糖类的是______,属于营养强化剂的是___,属于防腐剂的是______。
16.太原市家用燃料的更新经历了以下几个过程:
请回答下列问题。
(1)为了使煤充分燃烧,可采取的措施是____。
(2)煤的气化可产生管道煤气,其主要反应是碳与水蒸气在高温下生成两种常见的可燃性气体,这两种气体是_______________。
(3)液化石油气的主要成分是丙烷(C3H8),丙烷完全燃烧的化学反应方程式是______________。
(4)天然气作燃料比煤更清洁的原因是____(答一条即可)。
17.为了防治酸雨,减少煤燃烧时向大气排放的SO2,工业上采用生石灰和含硫的煤混合使用以“固硫”(避免硫的化合物进入大气),最后生成石膏。试回答:
(1)整个“固硫”反应所涉及的反应类型包括:①化合反应②分解反应 ③置换反应 ④复分解反应 ⑤氧化还原反应 ⑥非氧化还原反应 ⑦离子反应 ⑧非离子反应(分子反应)。其中正确的是( )。
A.①⑤⑥⑦ B.①②③⑤⑧ C.①⑤⑥⑧ D.②④⑤⑦
(2)第一步“固硫”反应的化学方程式中所需气态物质的化学计量数为( )
A.1 B.2 C.3 D.4
(3)比较此法与石灰石粉末与含硫煤混合法哪个更好些________(A.生石灰 B.石灰石),原因是________。
(4)你认为减少酸雨产生可采取的措施是( )。
①少用煤作燃料 ②把工厂的烟囱造高 ③先将燃料煤脱硫 ④在土壤中加石灰防止酸化 ⑤开发新能源,避免含S、N的氧化物大量排放
A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤
18.揭秘港珠澳大桥中的超级材料。
(1)在建设中,广泛采用了氟碳涂料和凤铝的建材幕墙、门窗产品。凤铝属于___(填“金属”或“合成”)材料。
(2)凤铝的硬度比纯铝的硬度___(填“大”或“小”)。
(3)在建设中广泛使用了Al、Zn、Cu利用它们完成如下实验:
①将未打磨的铝片放入ZnSO4溶液中,没有明显现象。
②将打磨过的铝片放入ZnSO4溶液中,铝片表面有明显变化。
③将打磨过的锌片放入CuSO4溶液中,锌片表面变红。
实验①中无现象是因为铝片表面有一层致密的___(填化学式)薄膜;实验②中发生反应的化学方程式为___;实验③中锌片足量,充分反应后溶液变为___色。
19.在农业生产中是否应该继续施用化肥和农药的小组辩论中,正方小明和反方小刚分别叙述了自己的观点:
(1)下面事实不能支持小明观点的是___________(填字母)。
A.可以解决快速增长的人口吃饭问题
B.可以促进农作物生长,杀灭害虫,形成良性的生态循环
C.合成农药用量少、见效快
D.降低了农业生产成本,可以促进农业机械化、规模化发展
(2)持反方观点的小刚从生态系统、害虫的抗药性及食品中化肥、农药的残留等方面进行了驳斥,下列两例事实是小刚对滥用杀虫剂造成的恶性循环的论证:事实1.在远离施药地的南极,在海鸟和鱼体内都检测出了某些农药成分。事实2.喜马拉雅山的积雪中也发现了某些农药成分。这些事实说明____(填序号)。
①农药、化肥被考察队或登山者带到南极或高山上
②农药、化肥的滥用已影响到全球的生态循环
③农药、化肥成分可以在生态链中富集,导致生物链系统发生变化
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
【详解】A.氮气和氢气生成NH3,氨和空气的混合气通入灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮。生成的一氧化氮利用反应后残余的氧气继续氧化为二氧化氮,随后将二氧化氮通入水中制取硝酸,转化关系合理,故A不符合题意;
B.S通过和氧气生成SO2,SO2在催化剂条件下生成SO3,SO3通入水中得到,转化关系合理,故B不符合题意;
C.海水提纯可获得NaCl溶液,电解NaCl溶液可制备NaOH,转化关系合理,故C不符合题意;
D.电解饱和氯化镁溶液,在阳极处产生氯气,阴极处产生氢气和氢氧化镁,因此不能用这种方法获得镁,转化关系不合理,故D符合题意;
故答案选D。
2.C
【详解】A.铝是活泼的金属,工业上电解熔融Al2O3冶炼Al,同时生成氧气,故A正确;
B.维生素C具有还原性,常用作抗氧化剂,故B正确;
C.单糖不能发生水解,如葡萄糖、果糖等,故C错误;
D.工业生产玻璃原料为纯碱、石灰石和石英,工业生产水泥的原料为黏土和石灰石,故D正确;
故选C。
3.C
【详解】A.石油分馏得到汽油、柴油、润滑油等烷烃、环烷烃,植物油属于酯类不能通过石油分馏得到,故A错误;
B.棉花主要成分是纤维素,蚕丝的主要成分是蛋白质,故B错误;
C.水煤气的主要成分为CO、氢气,可在一定条件下合成烃、甲醇等,故C正确;
D.糖类中只有多糖属于高分子化合物,单糖、二糖以及油脂均不属于有机高分子化合物,故D错误;
故选:C。
4.C
【详解】A.春晚直播间高清摄像头镜片的主要成分是硅酸钠,A错误;
B.月壤含有MgO·FeO·SiO2,该物质含有4种元素,不属于氧化物,B错误;
C.燃煤“气化”是将煤转化为可燃性的气体()的过程;“脱硫”、“钙基固硫”是在燃煤过程中加入碳酸钙,在燃烧过程中将SO2转化为的过程,三者均有利于减少SO2排放和酸雨形成,C正确;
D.活性炭具有吸附性,臭氧/生物活性炭技术可用于饮用水的深度处理,该原理利用了活性炭的吸附性,D错误;
故答案为:C。
5.A
【详解】抗坏血酸又称为维生素C,具有还原性,可用作食品抗氧化剂,故选A。
6.C
【详解】A.石油裂化的目的是为了获得轻质油,裂解的目的是为了获得乙烯等短链的不饱和烃,裂解的目的是为了获得乙烯等短链的不饱和烃,A正确;
B.煤干馏是在隔绝空气条件下对煤加强热使煤分解,可以得到焦炭、煤焦油、焦炉气、粗氨水等重要化工原料,B正确;
C.酒精含有碳氢氧元素,不属于烃类化合物,C错误;
D.甲醛的水溶液俗称福尔马林,具有杀菌、防腐性能,甲醛有毒,不能用于食品保鲜,D正确;
故合理选项是C。
7.A
【详解】A.酸雨是pH小于5.6的雨水,A错误;
B.汽车尾气中的氮氧化物,可引起光化学烟雾,是许多城市空气的主要污染源,B正确;
C.二氧化硫为酸性氧化物,可与生石灰发生反应生成亚硫酸钙,从而可减少工业废气SO2的排放,C正确;
D.大气污染物包括一氧化碳、二氧化硫、氮氧化物和可吸入颗粒物、臭氧等,D正确;
故选A。
8.B
【详解】A.金属Na容易与H2O反应产生可燃性气体H2,所以在实验室发现钠着火时,不能用水浇灭,而应该使用沙子灭火,A错误;
B.乙醇是可燃性液体,故装运乙醇的包装箱上应贴上易燃液体的危险品标志图标,B正确;
C.为了预防新冠肺炎,在家中关闭门窗用大量的75%的酒精进行环境消毒,C错误;
D.食品添加剂具有以下三个特征:一是为加入到食品中的物质,因此,它一般不单独作为食品来食用;二是既包括人工合成的物质,也包括天然物质;三是加入到食品中的目的是为改善食品品质和色、香、味以及为防腐、保鲜和加工工艺的需要,所以合理使用食品添加剂有助于改善食品品质、丰富食品营养成分,并且要控制在一定量的范围内,不能超标,否则会对人体健康产生一定的危害,D错误;
故合理选项是B。
9.B
【详解】城市空气质量日报目前计入空气污染指数的项目包括二氧化硫、一氧化碳、二氧化氮等氮氧化物、可吸入颗粒物PM2.5和臭氧等,不包括二氧化碳;故选B。
10.C
【详解】A.石油分馏得到的汽油是混合物,故A错误;
B.石油分馏产品主要为烷烃、环烷烃等,不能发生聚合反应,故B错误;
C.天然气的主要成分为甲烷,燃烧充分,生成物为二氧化碳和水,为清洁的化石燃料,故C正确;
D.水煤气是通过煤高温下与水蒸气反应得到的气体燃料,水煤气不是通过煤的液化得到的,通过煤的气化可得到水煤气,故D错误;
答案选C。
11.C
【详解】A、根据反应式3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O可知,硫酸与硝酸的物质的量之比是3︰2,选项A正确;
B、途径①③中均生成大气污染物,而②没有,所以选项B正确;
C、1mol硫酸铜可以生成0.5mol氧化亚铜,转移1mol电子,所以生成0.25mol氧气,选项C不正确;
D、醛基能被新制的氢氧化铜悬浊液氧化,生成氧化亚铜,葡萄糖含有醛基,D正确;
所以正确的答案选C。
12.C
【详解】A. 新能源汽车的推广与使用,减少汽油的使用,有助于减少光化学烟雾的产生,故A正确;
B. 肥皂水显碱性,因此氯气泄漏时,可用蘸有肥皂水的湿毛巾捂住口鼻疏散到安全区域,故B正确;
C. 铁在潮湿的空气中放置,易发生电化学腐蚀而生锈,故C错误;
D.在煤中添加石灰石作为脱硫剂,反应后生成CaSO3,进一步氧化为CaSO4,可制得石膏,用作建筑材料,故D正确。
答案选C。
13.(1) a c c d 2Al+Cr2O3Al2O3+2Cr
(2)Cu2(OH)2CO32CuO+H2O+CO2↑、2CuO+C2Cu+CO2↑、CuO+COCu+CO2
【解析】略
14. SO2+Br2+2H2O=H2SO4+2HBr 富集溴元素 Cl2+2Br=Br2+2Cl- 1:5 5mol 5Br-+BrO+6H+ =3Br2+3H2O
【分析】淡化海水加入硫酸酸化,再通入氯气,置换出溴,利用空气吹出溴,并用Na2CO3吸收溴,得到含溴离子的溶液,再通入氯气将溴离子氧化,得到溴的浓溶液,据此分析。
【详解】(1)过程II中物质X可以选SO2吸收溴,溴与含二氧化硫的水溶液反应生成氢溴酸和硫酸,反应的化学方程式为SO2+Br2+2H2O=H2SO4+2HBr;
(2)过程I、II由稀的溴溶液到得到浓的溴溶液,要达到的目的是富集溴元素;
(3)过程III利用氯气将溴离子氧化生成溴单质,反应的离子方程式为Cl2+2Br=Br2+2Cl-;
(4) ①根据反应3Br2 +6Na2CO3 +3H2O =5NaBr +NaBrO3 +6NaHCO3可知,NaBr为还原产物,NaBrO3为氧化产物,故反应中被氧化与被还原的溴的物质的量之比为1:5;
②反应3Br2 +6Na2CO3 +3H2O =5NaBr +NaBrO3 +6NaHCO3中溴由0价变为-1价和由0价变为+5价,根据反应方程式可知,若消耗3 mol Br2转移电子的物质的量为5mol;
③在含有NaBr、NaBrO3的混合溶液中加入适量的稀硫酸酸化即可得到溴,该反应的离子方程式为5Br-+BrO+6H+ =3Br2+3H2O。
15. ① ② ③ ④
【详解】以上配料中,奶粉富含大量蛋白质;白砂糖属于糖类;乳酸钙属于营养强化剂;在食品中常添加山梨酸钾作防腐剂;
故答案为:①;②;③;④。
16. 将煤粉碎 CO、H2 C3H8+5O23CO2+4H2O 减少了粉尘污染
【详解】(1)为了使煤充分燃烧,需要加快化学反应速率,可采取的措施是将煤粉碎。
(2)碳与水蒸气在高温下生成两种常见的可燃性气体,根据原子守恒,这两种气体是CO和氢气。
(3)丙烷完全燃烧生成CO2和水,化学反应方程式为C3H8+5O23CO2+4H2O。
(4)天然气作燃料比煤更清洁的原因是减少了粉尘污染。
17. C A A 此法节约煤,成本低 C
【详解】(1)在含硫的煤中加生石灰“固硫”的反应是CaO+SO2=CaSO3、2CaSO3+O2=2CaSO4,可见所涉及到的反应类型有化合反应、氧化还原反应、非氧化还原反应和非离子反应,答案选C。
(2)第一步“固硫”反应的化学方程式为CaO+SO2=CaSO3,气态物质的化学计量数为1,答案选A。
(3)石灰石分解成CaO需要消耗很高的能量,浪费煤,使生产成本提高,故使用生石灰更好,答案选A。
(4)①少用煤作燃料,可减少SO2的排放,减少酸雨;②把工厂的烟囱造高,不能减少酸雨;③先将燃料煤脱硫,可减少SO2的排放,减少酸雨;④在土壤中加石灰虽可中和酸雨造成的酸性,但不会减少酸雨;⑤开发新能源,避免含S、N的氧化物大量排放,减少酸雨;能减少酸雨的措施有①③⑤,答案选C。
18.(1)金属
(2)大
(3) Al2O3 2Al+3ZnSO4=Al2(SO4)3+3Zn 无
【分析】(1)
金属材料分为纯金属和合金,凤铝是铝合金,属于金属材料;
(2)
合金的硬度一般比纯金属的大;
(3)
金属铝性质活泼,在空气中被氧气氧化,表面生成一层致密的Al2O3薄膜;将打磨过的铝片放入ZnSO4溶液中,Al的金属活动性大于Zn,可以将Zn置换出来,方程式为2Al+3ZnSO4=Al2(SO4)3+3Zn;Zn的金属活动性大于Cu,Zn可以将Cu置换出来,Zn+CuSO4=ZnSO4+Cu,Zn过量可以将Cu2+完全置换出来,反应后溶液无色。
19.(1)B
(2)②③
【解析】略
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列制备物质的转化关系不合理的是
A.制:
B.制:
C.制NaOH:海水NaCl溶液NaOH
D.制Mg:海水溶液
2.化学与人类生产、生活、科研密切相关,下列有关说法不正确的是
A.工业上电解熔融Al2O3冶炼Al
B.维生素C常用作抗氧化剂,说明它具有还原性
C.糖类、蛋白质和油脂都属于营养物质,都能发生水解反应
D.工业生产玻璃、水泥,均需用石灰石作原料
3.下列说法正确的是
A.分馏石油可以得到汽油、柴油、植物油和润滑油
B.棉花和蚕丝的主要成分都是纤维素
C.水煤气可用来合成液态烃及甲醇等含氧有机物
D.糖类、油脂、蛋白质都属于有机高分子化合物
4.化学与人类生产、生活及社会可持续发展密切相关,下列说法正确的是
A.春晚直播间高清摄像头镜片的主要成分是单质硅
B.嫦娥五号采样返回器带回的月壤含有MgO·FeO·SiO2,该物质属于氧化物
C.燃煤“气化”、“脱硫”、“钙基固硫”等措施有利于减少SO2排放和酸雨形成
D.臭氧/生物活性炭技术可用于饮用水的深度处理,该原理利用了活性炭的还原性
5.下列物质中,可用作食品抗氧化剂的是
A.抗坏血酸 B.硫酸钙 C.三聚氰胺 D.碳酸镁
6.下列有关叙述错误的是( )
A.石油裂化是为了获得更多的汽油,裂解是为了获得气态烃
B.煤经过干馏可得到焦炭、煤焦油和焦炉气
C.甲烷、汽油、酒精都是烃类,都可作燃料
D.甲醛的水溶液俗称福尔马林,可杀菌防腐,但不可用于食品保鲜
7.习近平主席在十九大报告中指出,坚持人与自然和谐共生。必须树立和践行绿水青山就是金山银山的理念,坚持节约资源和保护环境的基本国策。下列说法错误的是
A.酸雨是指pH小于7的雨水
B.汽车尾气已成为许多城市空气的主要污染源
C.可以用生石灰作为脱硫剂以减少工业废气SO2的排放
D.二氧化硫、二氧化氮和可吸入颗粒物是大气主要污染物
8.下列有关化学用品的安全使用(或措施)正确的是
A.在实验室发现钠着火时,立即用水浇灭
B.装运乙醇的包装箱上应贴上易燃液体的危险品标志图标
C.为了预防新冠肺炎,在家中关闭门窗用大量的95%的酒精进行环境消毒
D.食品添加剂为各种各样的化学物质,所以国家应立法杜绝使用食品添加剂
9.下列物质不属于“城市空气质量日报”报道的是
A.氮氧化物 B.二氧化碳 C.PM2.5 D.二氧化硫
10.下列关于煤、石油、天然气等资源的说法中正确的是
A.石油裂解得到的汽油是纯净物
B.石油产品都可用于聚合反应
C.天然气是一种清洁的化工原料
D.水煤气是通过煤的液化得到的气体燃料
11.CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是( )
A.途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2
B.相对于途径①、③,途径②更好地体现了绿色化学思想
C.1molCuSO4在1100℃所得混合气体X中O2可能为0.75mol
D.Y可以是葡萄糖
12.化学与生活密切相关,下列有关说法不正确的是
A.新能源汽车的推广与使用,有助于减少光化学烟雾的产生
B.氯气泄漏时,可用蘸有肥皂水的湿毛巾捂住口鼻疏散到安全区域
C.铁在潮湿的空气中放置,易发生化学腐蚀而生锈
D.煤脱硫后产生的废料中含有的CaSO4 ,可用于制造建筑材料
二、填空题
13.金属元素的原子结构决定了金属元素的性质、在自然界中的存在形式及冶炼方法。
(1)金属的冶炼一般有下列方法:
a.焦炭法
b.水煤气(氢气和一氧化碳)法
c.活泼金属置换法
d.电解法
请从上述四种方法中选择相应的字母填入表中空格:
高炉炼铁 湿法炼铜 铝热法炼铬 工业上冶炼铝
______ ______ ______ ______
写出Al与Cr2O3反应的化学方程式:__________。
(2)铜在地壳中的含量远低于铝,但人类利用铜的历史远早于铝,这与古代发生的森林大火有一定的关系,因为人类在大火之后的灰烬中会发现红色发亮的物质。现在人们认识到,这种物质就是孔雀石[主要成分为Cu2(OH)2CO3,热稳定性差]在大火中转化而生成的铜,写出大火中与铜元素有关的三个化学方程式:______。
14.海洋是一座巨大的化学资源宝库,从中可以提取多种化学物质。从淡化海水中提取溴是海水综合利用的重要途径,其流程如下:
完成下列填空:
(1)过程II中物质X可以选SO2吸收溴,写出该反应的化学方程式__________。
(2)过程I、II要达到的目的是______________。
(3)写出过程III反应的离子方程式___________。
(4)若过程II中物质X选Na2CO3吸收溴,发生如下反应:3Br2 +6Na2CO3 +3H2O == 5NaBr +NaBrO3 +6NaHCO3
①反应中被氧化与被还原的溴的物质的量之比为_______________。
②反应中消耗3 mol Br2转移电子的物质的量为__________。
③在含有NaBr、NaBrO3的混合溶液中加入适量的稀硫酸酸化即可得到溴,写出该反应的离子方程式__________。
15.下表是某食品包装上的说明,表中列出了部分配料。
品名 好吃你就多吃点
部分配料 ① 奶粉 ②白砂糖③ 乳酸钙 ④ 山梨酸钾
生产日期 标于包装封口处
配料中,富含蛋白质的是_______,属于糖类的是______,属于营养强化剂的是___,属于防腐剂的是______。
16.太原市家用燃料的更新经历了以下几个过程:
请回答下列问题。
(1)为了使煤充分燃烧,可采取的措施是____。
(2)煤的气化可产生管道煤气,其主要反应是碳与水蒸气在高温下生成两种常见的可燃性气体,这两种气体是_______________。
(3)液化石油气的主要成分是丙烷(C3H8),丙烷完全燃烧的化学反应方程式是______________。
(4)天然气作燃料比煤更清洁的原因是____(答一条即可)。
17.为了防治酸雨,减少煤燃烧时向大气排放的SO2,工业上采用生石灰和含硫的煤混合使用以“固硫”(避免硫的化合物进入大气),最后生成石膏。试回答:
(1)整个“固硫”反应所涉及的反应类型包括:①化合反应②分解反应 ③置换反应 ④复分解反应 ⑤氧化还原反应 ⑥非氧化还原反应 ⑦离子反应 ⑧非离子反应(分子反应)。其中正确的是( )。
A.①⑤⑥⑦ B.①②③⑤⑧ C.①⑤⑥⑧ D.②④⑤⑦
(2)第一步“固硫”反应的化学方程式中所需气态物质的化学计量数为( )
A.1 B.2 C.3 D.4
(3)比较此法与石灰石粉末与含硫煤混合法哪个更好些________(A.生石灰 B.石灰石),原因是________。
(4)你认为减少酸雨产生可采取的措施是( )。
①少用煤作燃料 ②把工厂的烟囱造高 ③先将燃料煤脱硫 ④在土壤中加石灰防止酸化 ⑤开发新能源,避免含S、N的氧化物大量排放
A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤
18.揭秘港珠澳大桥中的超级材料。
(1)在建设中,广泛采用了氟碳涂料和凤铝的建材幕墙、门窗产品。凤铝属于___(填“金属”或“合成”)材料。
(2)凤铝的硬度比纯铝的硬度___(填“大”或“小”)。
(3)在建设中广泛使用了Al、Zn、Cu利用它们完成如下实验:
①将未打磨的铝片放入ZnSO4溶液中,没有明显现象。
②将打磨过的铝片放入ZnSO4溶液中,铝片表面有明显变化。
③将打磨过的锌片放入CuSO4溶液中,锌片表面变红。
实验①中无现象是因为铝片表面有一层致密的___(填化学式)薄膜;实验②中发生反应的化学方程式为___;实验③中锌片足量,充分反应后溶液变为___色。
19.在农业生产中是否应该继续施用化肥和农药的小组辩论中,正方小明和反方小刚分别叙述了自己的观点:
(1)下面事实不能支持小明观点的是___________(填字母)。
A.可以解决快速增长的人口吃饭问题
B.可以促进农作物生长,杀灭害虫,形成良性的生态循环
C.合成农药用量少、见效快
D.降低了农业生产成本,可以促进农业机械化、规模化发展
(2)持反方观点的小刚从生态系统、害虫的抗药性及食品中化肥、农药的残留等方面进行了驳斥,下列两例事实是小刚对滥用杀虫剂造成的恶性循环的论证:事实1.在远离施药地的南极,在海鸟和鱼体内都检测出了某些农药成分。事实2.喜马拉雅山的积雪中也发现了某些农药成分。这些事实说明____(填序号)。
①农药、化肥被考察队或登山者带到南极或高山上
②农药、化肥的滥用已影响到全球的生态循环
③农药、化肥成分可以在生态链中富集,导致生物链系统发生变化
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
【详解】A.氮气和氢气生成NH3,氨和空气的混合气通入灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮。生成的一氧化氮利用反应后残余的氧气继续氧化为二氧化氮,随后将二氧化氮通入水中制取硝酸,转化关系合理,故A不符合题意;
B.S通过和氧气生成SO2,SO2在催化剂条件下生成SO3,SO3通入水中得到,转化关系合理,故B不符合题意;
C.海水提纯可获得NaCl溶液,电解NaCl溶液可制备NaOH,转化关系合理,故C不符合题意;
D.电解饱和氯化镁溶液,在阳极处产生氯气,阴极处产生氢气和氢氧化镁,因此不能用这种方法获得镁,转化关系不合理,故D符合题意;
故答案选D。
2.C
【详解】A.铝是活泼的金属,工业上电解熔融Al2O3冶炼Al,同时生成氧气,故A正确;
B.维生素C具有还原性,常用作抗氧化剂,故B正确;
C.单糖不能发生水解,如葡萄糖、果糖等,故C错误;
D.工业生产玻璃原料为纯碱、石灰石和石英,工业生产水泥的原料为黏土和石灰石,故D正确;
故选C。
3.C
【详解】A.石油分馏得到汽油、柴油、润滑油等烷烃、环烷烃,植物油属于酯类不能通过石油分馏得到,故A错误;
B.棉花主要成分是纤维素,蚕丝的主要成分是蛋白质,故B错误;
C.水煤气的主要成分为CO、氢气,可在一定条件下合成烃、甲醇等,故C正确;
D.糖类中只有多糖属于高分子化合物,单糖、二糖以及油脂均不属于有机高分子化合物,故D错误;
故选:C。
4.C
【详解】A.春晚直播间高清摄像头镜片的主要成分是硅酸钠,A错误;
B.月壤含有MgO·FeO·SiO2,该物质含有4种元素,不属于氧化物,B错误;
C.燃煤“气化”是将煤转化为可燃性的气体()的过程;“脱硫”、“钙基固硫”是在燃煤过程中加入碳酸钙,在燃烧过程中将SO2转化为的过程,三者均有利于减少SO2排放和酸雨形成,C正确;
D.活性炭具有吸附性,臭氧/生物活性炭技术可用于饮用水的深度处理,该原理利用了活性炭的吸附性,D错误;
故答案为:C。
5.A
【详解】抗坏血酸又称为维生素C,具有还原性,可用作食品抗氧化剂,故选A。
6.C
【详解】A.石油裂化的目的是为了获得轻质油,裂解的目的是为了获得乙烯等短链的不饱和烃,裂解的目的是为了获得乙烯等短链的不饱和烃,A正确;
B.煤干馏是在隔绝空气条件下对煤加强热使煤分解,可以得到焦炭、煤焦油、焦炉气、粗氨水等重要化工原料,B正确;
C.酒精含有碳氢氧元素,不属于烃类化合物,C错误;
D.甲醛的水溶液俗称福尔马林,具有杀菌、防腐性能,甲醛有毒,不能用于食品保鲜,D正确;
故合理选项是C。
7.A
【详解】A.酸雨是pH小于5.6的雨水,A错误;
B.汽车尾气中的氮氧化物,可引起光化学烟雾,是许多城市空气的主要污染源,B正确;
C.二氧化硫为酸性氧化物,可与生石灰发生反应生成亚硫酸钙,从而可减少工业废气SO2的排放,C正确;
D.大气污染物包括一氧化碳、二氧化硫、氮氧化物和可吸入颗粒物、臭氧等,D正确;
故选A。
8.B
【详解】A.金属Na容易与H2O反应产生可燃性气体H2,所以在实验室发现钠着火时,不能用水浇灭,而应该使用沙子灭火,A错误;
B.乙醇是可燃性液体,故装运乙醇的包装箱上应贴上易燃液体的危险品标志图标,B正确;
C.为了预防新冠肺炎,在家中关闭门窗用大量的75%的酒精进行环境消毒,C错误;
D.食品添加剂具有以下三个特征:一是为加入到食品中的物质,因此,它一般不单独作为食品来食用;二是既包括人工合成的物质,也包括天然物质;三是加入到食品中的目的是为改善食品品质和色、香、味以及为防腐、保鲜和加工工艺的需要,所以合理使用食品添加剂有助于改善食品品质、丰富食品营养成分,并且要控制在一定量的范围内,不能超标,否则会对人体健康产生一定的危害,D错误;
故合理选项是B。
9.B
【详解】城市空气质量日报目前计入空气污染指数的项目包括二氧化硫、一氧化碳、二氧化氮等氮氧化物、可吸入颗粒物PM2.5和臭氧等,不包括二氧化碳;故选B。
10.C
【详解】A.石油分馏得到的汽油是混合物,故A错误;
B.石油分馏产品主要为烷烃、环烷烃等,不能发生聚合反应,故B错误;
C.天然气的主要成分为甲烷,燃烧充分,生成物为二氧化碳和水,为清洁的化石燃料,故C正确;
D.水煤气是通过煤高温下与水蒸气反应得到的气体燃料,水煤气不是通过煤的液化得到的,通过煤的气化可得到水煤气,故D错误;
答案选C。
11.C
【详解】A、根据反应式3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O可知,硫酸与硝酸的物质的量之比是3︰2,选项A正确;
B、途径①③中均生成大气污染物,而②没有,所以选项B正确;
C、1mol硫酸铜可以生成0.5mol氧化亚铜,转移1mol电子,所以生成0.25mol氧气,选项C不正确;
D、醛基能被新制的氢氧化铜悬浊液氧化,生成氧化亚铜,葡萄糖含有醛基,D正确;
所以正确的答案选C。
12.C
【详解】A. 新能源汽车的推广与使用,减少汽油的使用,有助于减少光化学烟雾的产生,故A正确;
B. 肥皂水显碱性,因此氯气泄漏时,可用蘸有肥皂水的湿毛巾捂住口鼻疏散到安全区域,故B正确;
C. 铁在潮湿的空气中放置,易发生电化学腐蚀而生锈,故C错误;
D.在煤中添加石灰石作为脱硫剂,反应后生成CaSO3,进一步氧化为CaSO4,可制得石膏,用作建筑材料,故D正确。
答案选C。
13.(1) a c c d 2Al+Cr2O3Al2O3+2Cr
(2)Cu2(OH)2CO32CuO+H2O+CO2↑、2CuO+C2Cu+CO2↑、CuO+COCu+CO2
【解析】略
14. SO2+Br2+2H2O=H2SO4+2HBr 富集溴元素 Cl2+2Br=Br2+2Cl- 1:5 5mol 5Br-+BrO+6H+ =3Br2+3H2O
【分析】淡化海水加入硫酸酸化,再通入氯气,置换出溴,利用空气吹出溴,并用Na2CO3吸收溴,得到含溴离子的溶液,再通入氯气将溴离子氧化,得到溴的浓溶液,据此分析。
【详解】(1)过程II中物质X可以选SO2吸收溴,溴与含二氧化硫的水溶液反应生成氢溴酸和硫酸,反应的化学方程式为SO2+Br2+2H2O=H2SO4+2HBr;
(2)过程I、II由稀的溴溶液到得到浓的溴溶液,要达到的目的是富集溴元素;
(3)过程III利用氯气将溴离子氧化生成溴单质,反应的离子方程式为Cl2+2Br=Br2+2Cl-;
(4) ①根据反应3Br2 +6Na2CO3 +3H2O =5NaBr +NaBrO3 +6NaHCO3可知,NaBr为还原产物,NaBrO3为氧化产物,故反应中被氧化与被还原的溴的物质的量之比为1:5;
②反应3Br2 +6Na2CO3 +3H2O =5NaBr +NaBrO3 +6NaHCO3中溴由0价变为-1价和由0价变为+5价,根据反应方程式可知,若消耗3 mol Br2转移电子的物质的量为5mol;
③在含有NaBr、NaBrO3的混合溶液中加入适量的稀硫酸酸化即可得到溴,该反应的离子方程式为5Br-+BrO+6H+ =3Br2+3H2O。
15. ① ② ③ ④
【详解】以上配料中,奶粉富含大量蛋白质;白砂糖属于糖类;乳酸钙属于营养强化剂;在食品中常添加山梨酸钾作防腐剂;
故答案为:①;②;③;④。
16. 将煤粉碎 CO、H2 C3H8+5O23CO2+4H2O 减少了粉尘污染
【详解】(1)为了使煤充分燃烧,需要加快化学反应速率,可采取的措施是将煤粉碎。
(2)碳与水蒸气在高温下生成两种常见的可燃性气体,根据原子守恒,这两种气体是CO和氢气。
(3)丙烷完全燃烧生成CO2和水,化学反应方程式为C3H8+5O23CO2+4H2O。
(4)天然气作燃料比煤更清洁的原因是减少了粉尘污染。
17. C A A 此法节约煤,成本低 C
【详解】(1)在含硫的煤中加生石灰“固硫”的反应是CaO+SO2=CaSO3、2CaSO3+O2=2CaSO4,可见所涉及到的反应类型有化合反应、氧化还原反应、非氧化还原反应和非离子反应,答案选C。
(2)第一步“固硫”反应的化学方程式为CaO+SO2=CaSO3,气态物质的化学计量数为1,答案选A。
(3)石灰石分解成CaO需要消耗很高的能量,浪费煤,使生产成本提高,故使用生石灰更好,答案选A。
(4)①少用煤作燃料,可减少SO2的排放,减少酸雨;②把工厂的烟囱造高,不能减少酸雨;③先将燃料煤脱硫,可减少SO2的排放,减少酸雨;④在土壤中加石灰虽可中和酸雨造成的酸性,但不会减少酸雨;⑤开发新能源,避免含S、N的氧化物大量排放,减少酸雨;能减少酸雨的措施有①③⑤,答案选C。
18.(1)金属
(2)大
(3) Al2O3 2Al+3ZnSO4=Al2(SO4)3+3Zn 无
【分析】(1)
金属材料分为纯金属和合金,凤铝是铝合金,属于金属材料;
(2)
合金的硬度一般比纯金属的大;
(3)
金属铝性质活泼,在空气中被氧气氧化,表面生成一层致密的Al2O3薄膜;将打磨过的铝片放入ZnSO4溶液中,Al的金属活动性大于Zn,可以将Zn置换出来,方程式为2Al+3ZnSO4=Al2(SO4)3+3Zn;Zn的金属活动性大于Cu,Zn可以将Cu置换出来,Zn+CuSO4=ZnSO4+Cu,Zn过量可以将Cu2+完全置换出来,反应后溶液无色。
19.(1)B
(2)②③
【解析】略
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
