第一章《有机化合物的结构特点与研究方法》测试(含解析)2022-2023学年下学期高二化学人教版(2019)选择性必修3
文档属性
| 名称 | 第一章《有机化合物的结构特点与研究方法》测试(含解析)2022-2023学年下学期高二化学人教版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 338.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-13 00:00:00 | ||
图片预览




文档简介
第一章《有机化合物的结构特点与研究方法》测试
一、单选题
1.研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→确定分子式→确定结构式以下用于研究有机物的方法错误的是
A.核磁共振氢谱的研究有助于确定有机物分子中氢原子的类型和数目比
B.蒸馏常用于分离提纯液态有机混合物
C.燃烧法是确定有机物成分的有效方法之一
D.红外光谱通常用于分析有机物的相对分子质量
2.分子式为C7H16,且有一个支链的有机物有(不考虑立体异构)
A.1种 B.2种 C.3种 D.4种
3.主链上有5个碳原子,分子中总共含有3个甲基的烷烃分子有
A.2种 B.3种 C.4种 D.5种
4.催化剂RuO2/Al-MgF2耐HF的腐蚀,如图所示可应用于氟化工行业中的氯循环。下列说法不正确的是
A.若Ru的价电子排布式为4d75s1,则该元素位于Ⅷ族
B.上述转化过程中涉及的有机反应类型有加成反应、消去反应
C.可通过液化分离出HCl中大多数的HF
D.上述循环中有水生成
5.下列说法正确的是
A.蛋白质、纤维素和油脂水解的最终产物都含有电解质
B.煤中含有煤焦油等有机物,可以通过分馏的方法从煤焦油中获得苯和二甲苯等物质
C.紫外光谱仪,红外光谱仪以及质谱仪都可用于研究有机物结构
D.石油工业中通过对轻质油进行裂化得到乙烯等气体
6.NM—3是处于临床试验阶段的小分子抗癌药物,分子结构如图。下列说法正确的是
A.该有机物的化学式为C12H12O6
B.该有机物含有三种官能团
C.该物质不属于芳香化合物
D.该有机物可属于羧酸类
7.下列化学用语错误的是
A. 的结构示意图为
B.二氧化硅的分子式为
C.中子数为8的氮原子可表示为
D.HClO的结构式为H-O-Cl
8.下列说法错误的是
A.利用红外光谱实验可确定青蒿素分子中含有的部分基团
B.超分子具有分子识别和自组装的特征
C.金刚石晶体中碳原子个数与C—C键键数之比为1:4
D.等离子体是由电子、阳离子和电中性的粒子组成的
9.有机化合物E( )是制备新型缓解过敏药物的原料。下列说法正确的是
A.E的分子式为C13H11N2OCl,每个分子中含有两个苯环
B.E分子的官能团中含有酰胺基,分子的不饱和度为9
C.每个E分子含有1个手性碳原子和7个双键
D.E可以发生水解、氧化、加成、消去等反应
10.下列关于蒸馏操作有关说法正确的是
A.温度计的水银球应插入到液面以下
B.蒸馏过程中,加入沸石(或碎瓷片)的目的是防止暴沸
C.冷凝管进出水的方向是上进下出
D.用烧杯接收蒸馏出来的液体
11.芬必得是一种高效的消炎药物,主要成分为布洛芬,布洛芬的结构简式如图所示。下列有关布洛芬的说法正确的是
A.分子式为 B.不能使酸性高锰酸钾溶液褪色
C.可以发生加成反应和取代反应 D.苯环上的一氯代物有4种
二、填空题
12.有0.1 mol某有机物A和0.25 mol氧气在一密闭容器中充分燃烧,所得产物通过浓硫酸时使其增重5.4g,再通过足量灼热的氧化铜粉末,固体质量减轻1.6g,最后再通过足量过氧化钠粉末,固体质量增加了8.4g。试通过分析计算(要写出分析计算过程):
(1)该有机物A的分子式______。
(2)若0.1 mol含羟基的有机物B与有机物A的最简式相同,且在0.2 mol氧气中能完全然烧,试确定B的结构简式______。
13.某种烃A的蒸气折合成标况下的密度是3.214g/L,已知该烃的碳氢质量比为5∶1,求:
(1)该烃的相对分子质量:________;
(2)确定该烃的分子式:____________;
(3)如果该烃的一氯取代物有4种,写出该烃的结构简式:__________;
(4)烃A可由另一种烃B通过加成反应而制得,则烃B的可能的是(任写一种可能的结构简式):_____________。
14.(1)写出下列基团的名称:
—C═C— ─C≡C─ ─CH3 ─CH2CH3或─C2H5
_____ _____ _____ _____
(2)有下列机物,请将它所对应的类别用序号填入下列表格中:
(1)CH3CH2CH3 ①酯
(2)CH2=CH—CH3 ②羧酸
(3)CH3COOCH3 ③醛
(4)CH3-CHO ④醇
(5)CH3-OH ⑤烯烃
(6)CH3CH2COOH ⑥烷烃
物质编号 所属类别编号 物质编号 所属类别编号
(1) _____ (4)
(2) (5)
(3) (6)
15.按要求回答下列问题:
(1)乙烷的结构式为____。
(2)丙烷的结构简式为_____。
(3)分子中含有30个氢原子的饱和链状烷烃的分子式为____。
(4)相对分子质量为58的饱和链状烷烃的结构有____种,分别写出它们的结构简式:_____。
(5)分子式为C5H12的直链烷烃的习惯命名为____,其一氯代物只有一种的同分异构体的结构简式为___。
16.最近,我国一留美化学家参与合成了一种新型炸药,它跟三硝基甘油一样抗打击、抗震,但一经引爆就发生激烈爆炸,据信是迄今最烈性的非核爆炸品。该炸药的化学式为C8N8O16,同种元素的原子在分子中是毫无区别的。
(1)画出它的结构式_________。
(2)写出它的爆炸反应方程式________。
(3)该物质为何是迄今最烈性的非核爆炸品______________。
17.含碳元素的物质是化学世界中最庞大的家族。回答下列问题:
(1)碳在形成化合物时,其键型以共价键为主,中的化学键从形成的过程来看属于___________(填“”或“”)键,从其极性来看属于___________(填“极性”或“非极性”)键。
(2)和分子中属于非极性分子的是___________;与互为等电子体的阳离子是___________;与互为等电子体的阴离子是___________。
(3)有机物中含氧官能团的名称为___________,其中含有___________个手性碳原子。
(4)甲醇与乙烷的相对分子质量和范德华力均相近,但是二者的沸点相差很大,造成该差异的原因是___________。
18.现有下列8种有机物,请按要求作答:
① ② ③ ④ ⑤
(1)按官能团分类,其中属于羧酸的有___________(填序号,下同),属于醇的有___________。
(2)④中所含官能团的名称是___________,③中所含官能团为___________(填符号)。
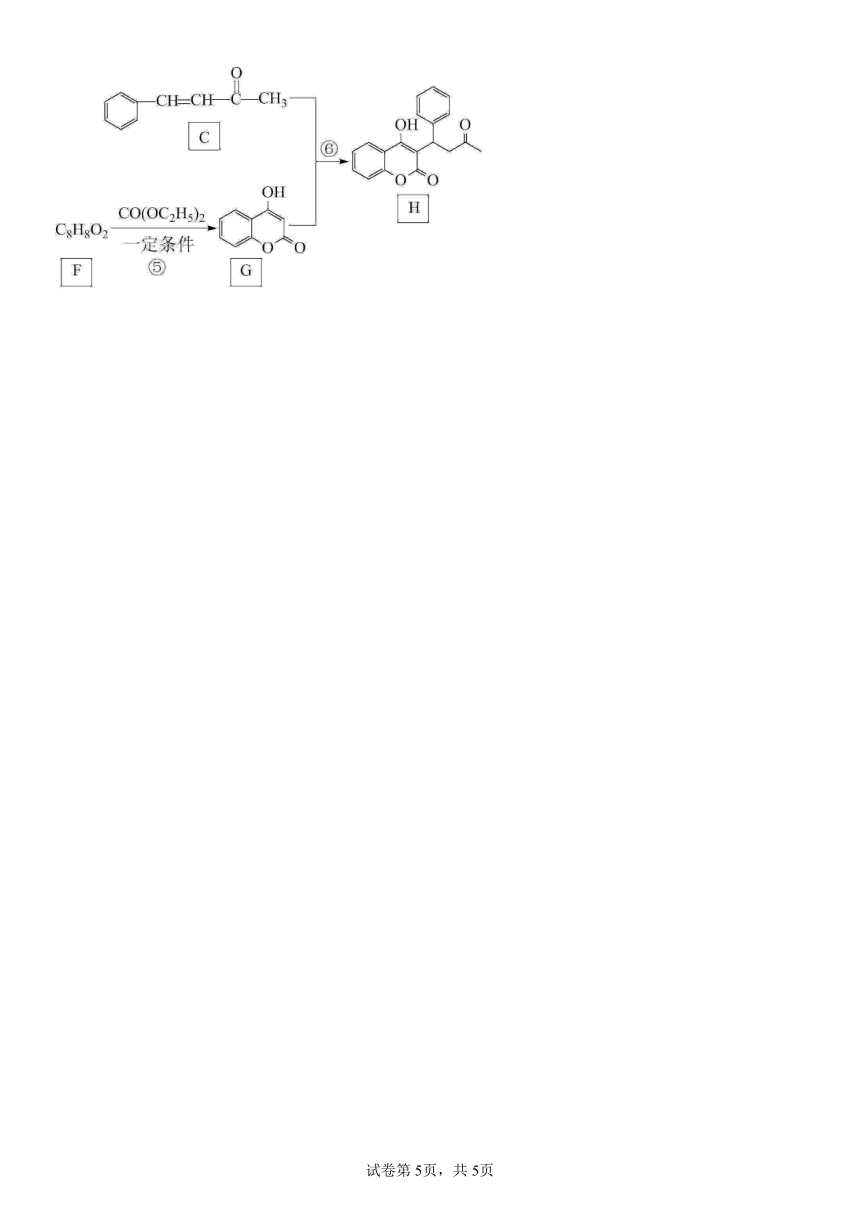
19.G与C生成H属于_______
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
【详解】A.从核磁共振氢谱图上可以推知有机物分子中有几种不同类型的氢原子以及其数目,A项正确;
B.蒸馏是利用互溶液态混合物中各组分的沸点不同而进行分离的方法,B项正确;
C.通过燃烧,能将有机物转化为简单无机物,并做定量测定,从而测定有机物成分,C项正确;
D.红外光谱是确定有机物分子中的化学键和官能团,不能确定有机物的相对分子质量,D项错误;
故答案为D。
2.C
【详解】分子式为C7H16,且有一个支链的有机物有、、共3种,故答案为:C。
3.B
【详解】烷烃主链上有5个碳原子,且分子中有3个甲基,其中主链上已经含有2个甲基,则侧链含有1个甲基,可以为1个甲基或1个乙基,该烷烃主链的碳架为:,当侧链为1个甲基时,甲基可以在1、2号C,存在2种结构;当侧链为乙基时,乙基只能在2号C,有1种结构,所以满足条件的烷烃的结构简式有3种,答案选B。
4.B
【详解】A.Ru为44号元素,若Ru的价电子排布式为4d75s1,则该元素位于Ⅷ族,A正确;
B. 反应中生成不饱和键,为消去反应;由图可知,没有加成反应,B错误;
C.氟化氢和氯化氢沸点差别较大,可通过液化分离出HCl中大多数的HF,C正确;
D.由图可知,氯化氢和氧气在催化剂作用下生成氯气,根据质量守恒可知,循环中有水生成,D正确;
故选B。
5.C
【详解】A. 蛋白质水解后生成的氨基酸是电解质、纤维素水解后的葡萄糖是非电解质、油脂水解后高级脂肪酸或高级脂肪酸钠是电解质,A错误;
B. 煤中没有煤焦油,煤干馏后生成煤焦油,B错误;
C. 紫外光谱仪可用于测定共轭二烯烃,红外光谱仪可测定某些基团或官能团、质谱仪能确定被测物质的分子量和结构,C正确;
D. 石油工业中通过对轻质油进行裂解得到乙烯、丙烯、丁二烯等气体,D错误;
答案选C。
6.D
【详解】A. 根据有机物结构简式可知该有机物的化学式为C12H10O6,A错误;
B. 该有机物含有4种官能团,分别是羧基、酯基、碳碳双键和酚羟基,B错误;
C. 分子中含有苯环,该物质属于芳香化合物,C错误;
D. 分子中含有羧基,该有机物可属于羧酸类,D正确。
答案选D。
7.B
【详解】A.核外有10个电子,结构示意图为,A正确;
B.二氧化硅是由原子构成的,没有分子,二氧化硅的化学式为,B错误;
C.氮原子质子数为7,中子数为8,质量数为15,可表示为,C正确;
D.HClO的结构式H-O-Cl,D正确;
故答案选B。
8.C
【详解】A.在有机物分子中,组成化学键或官能团的原子处于不断振动的状态,其振动频率与红外光的振动频率相当,利用红外光谱实验可确定青蒿素分子中含有的部分基团,故A正确;
B.超分子是两种或两种以上分子依靠分子间相互作用结合在一起,组成复杂的、有组织的聚集体,具有分子识别与自组装的特征,B正确;
C.在金刚石晶体中,每个碳原子形成4个C-C键,每两个碳原子形成一个C-C键,则每个碳原子形成的共价键平均为,所以在金刚石晶体中,碳原子与C-C键数之比为1:2,C错误;
D.等离子体是电子、阳离子和电中性粒子组成的整体上呈电中性的气态物质,D正确;
故答案选:C。
9.B
【详解】A.E的分子式为C13H11N2OCl,每个分子中仅含有一个苯环,A项错误;
B.每个碳碳双键不饱和度为1,每个碳氮双键不饱和度为1,每个碳氧双键不饱和度为1,环状结构不饱和度为1,苯环不饱和度为4,E分子的不饱和度共计为9,B项正确;
C.E分子中无手性碳原子,苯环的碳原子之间是一种介于碳碳单键和碳碳双键之间的特殊的键,不存在碳碳双键,故共有4个双键,C项错误;
D.E分子中的氯原子与苯环直接连接,不能发生消去反应,D项错误;
答案选B。
10.B
【详解】A.蒸馏操作中温度计的水银球应放在支管口处,故A错误;
B.蒸馏过程中,加入沸石(或碎瓷片)的目的是防止暴沸,故B正确;
C.冷凝管进出水的方向是下进上出,故C错误;
D.蒸馏时用锥形瓶接收蒸馏出来的液体,故D错误;
故选B。
11.C
【详解】A.布洛芬的不饱和度为5,碳原子数为13,氧原子数为2,则氢原子数为,则布洛芬的分子式为,A错误;
B.与苯环相连的碳原子上有氢原子,可以被酸性高锰酸钾溶液氧化,B错误;
C.含有苯环,可以发生加成反应;含有羧基,可以发生酯化反应(取代反应),C正确;
D.苯环上有两个处于对位的取代基,结构对称,所以苯环上只有两种不同化学环境的氢原子,则苯环上的一氯代物有2种,D错误;
故选C。
12. C3H6O3 HOCH2CHO
【分析】“浓硫酸时使其增重5.4g”,则表明反应生成水5.4g,n(H2O)==0.3mol;“通过足量灼热的氧化铜粉末,固体质量减轻1.6g”,发生反应为CO+CuO=Cu+CO2,由此可求出n(CO)==0.1mol;“通过足量过氧化钠粉末,固体质量增加了8.4g”,可将反应简化为Na2O2+CO=Na2CO3,由此得出生成的n(CO2)==0.3mol,其中有0.1molCO2来自CO与CuO的反应,据此分析解答。
【详解】(1)由以上分析,可以得出,0.1molA+0.25molO2=0.3molH2O+0.1molCO+0.2molCO2,从而得出反应方程式为A+2.5O2=3H2O+CO+2CO2,依据质量守恒原理,可得出A的分子式为C3H6O3。答案为:C3H6O3;
(2)由A的分子式C3H6O3,可确定其最简式为CH2O,由此假设B的分子式(CH2O)n,因为0.1 molB在0.2mol氧气中能完全然烧,所以0.1n=0.2,n=2,B的分子式为C2H4O2。由于B分子中含有-OH,所以其结构简式为HOCH2CHO。答案为:HOCH2CHO。
【点睛】此题的易错点主要集中在对“最后再通过足量过氧化钠粉末,固体质量增加了8.4g”的理解。也就是前面还原CuO反应生成的CO2有没有与Na2O2发生反应,因为我们无法将前面反应生成的气体与原混合气进行分离,所以计算得到的CO2的物质的量,应包括还原CuO生成的CO2的物质的量。
13. 72 C5H12 (CH3)2CHCH2 CH3 CH2=C(CH3)CH2 CH3 、(CH3)2CHCH=CH2 、(CH3)2C=CHCH3
【详解】(1)烃A的蒸气折合成标况下的密度是3.214g·L-1,所以A的摩尔质量是3.214g·L-1×22.4L·mol-1=72g·mol-1,该烃的相对分子质量为72。
(2)该烃的碳氢质量比为5∶1,该烃分子中碳、氢原子个数之比是:=5︰12,则该烃最简式是C5H12,该烃的分子式为(C5H12)x,则72x=72,解得x=1,则该烃的分子式为C5H12。
(3)该烃的一氯取代物有4种,说明分子中氢原子有4种,所以结构简式为(CH3)2CHCH2 CH3。
(4)烯烃加氢即得到烷烃,则烷烃分子中相邻碳原子上各去1个氢原子,即形成烯烃,所以B的结构简式可能是 CH2=C(CH3)CH2 CH3 、(CH3)2CHCH=CH2 、(CH3)2C=CHCH3。
14. 双键 三键 甲基 乙基
物质编号 所属类别编号 物质编号 所属类别编号
(1) ⑥ (4) ③
(2) ⑤ (5) ④
(3) ① (6) ②
【详解】(1)由有机物基团的结构简式可得基团的名称分别为:碳碳双键、碳碳三键 、甲基、乙基(2)CH3CH2CH3类别为烷烃;CH2=CH—CH3中的官能团为碳碳双键,类别为烯烃; CH3COOCH3的官能团为酯键,类别为酯;CH3-CHO的官能团为醛基,类别为醛;CH3-OH的官能团为羟基,类别为醇;CH3CH2COOH的官能团为羧基,类别为羧酸;故答案为
物质编号 所属类别编号 物质编号 所属类别编号
(1) ⑥ (4) ③
(2) ⑤ (5) ④
(3) ① (6) ②
15.(1)
(2)CH3CH2CH3
(3)C14H30
(4) 2 CH3CH2CH2CH3、
(5) 正戊烷 C(CH3)4
【解析】(1)
乙烷的分子式为,其结构式为;
(2)
丙烷的分子式为,其结构简式为;
(3)
由烷烃的分子通式(n为正整数)可知,,,其分子式为;
(4)
由烷烃的分子通式可知,,,的同分异构体有2种,分别为和;
(5)
分子式为的直链烷烃的习惯命名为正戊烷, 其一氯代物只有一种的同分异构体则其分子中只有一种化学环境的氢原子,其结构简式为C(CH3)4。
16. 八硝基环辛四烯: C8(NO2)8= 8CO2+4N2 ①八硝基立方烷分解得到的两种气体都是最稳定的化合物;②立方烷的碳架键角只有90℃,大大小于109928'(或答:是张力很大的环),因而八硝基立方烷是一种高能化合物,分解时将释放大量能量;③八硝基立方烷分解产物完全是气体,体积膨胀将引起激烈爆炸
【解析】略
17.(1) 极性
(2) 、
(3) 羧基 1
(4)甲醇分子间存在氢键,因此其沸点远高于乙烷
【解析】(1)
甲烷中碳原子的sp3杂化轨道与氢原子的s轨道以头碰头的方式形成4个碳氢共价键,该共价键为σ键;碳氢键是由不同种原子形成的共价键,为极性共价键。
(2)
甲烷中心原子C的价电子对数为4+(4-14)=4,采取sp3杂化,空间构型为正四面体,正负电荷重心重合,为非极性分子,二氧化碳中心原子C的价电子对数为2+(4-22)=2,采取sp杂化,空间构型为直线型,正负电荷重心重合,为非极性分子;甲烷分子中原子数为5、价电子总数为8,二氧化碳分子中原子数为3、价电子总数为16,利用同主族变换和左右移位法可得,与CH4互为等电子体的阳离子是,与CO2互为等电子体的阴离子是。
(3)
由有机物的结构可知,有机物中含氧官能团为羧基;手性碳原子是指人们将连有四个不同基团的碳原子形象地称为手性碳原子,由有机物的结构可知,其中含1个手性碳原子。
(4)
甲醇分子间存在氢键,但乙烷分子间不存在氢键,因此虽然两者相对分子质量和范德华力均相近,但甲醇的沸点高于乙烷。
18. ⑤ ① 酯基
【详解】(1)①中官能团为羟基,属于醇;②中官能团为碳碳双键,属于烯烃;③中官能团为溴原子,属于卤代烃;④中官能团为酯基,属于酯;⑤中官能团为羧基,属于羧酸。因而按官能团分类,其中属于羧酸的有⑤,属于醇的有①。故答案:⑤;①。
(2)④中所含官能团的名称为酯基,③中所含官能团为。故答案:酯基;。
19.加成反应
【详解】含有双键或三键的有机物与其他物质发生反应时,双键或三键中的一个断裂,在不饱和碳原子两端分别接上其他原子的反应称为加成反应,由G、C、H的结构可看出,G与C生成H属于加成反应。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→确定分子式→确定结构式以下用于研究有机物的方法错误的是
A.核磁共振氢谱的研究有助于确定有机物分子中氢原子的类型和数目比
B.蒸馏常用于分离提纯液态有机混合物
C.燃烧法是确定有机物成分的有效方法之一
D.红外光谱通常用于分析有机物的相对分子质量
2.分子式为C7H16,且有一个支链的有机物有(不考虑立体异构)
A.1种 B.2种 C.3种 D.4种
3.主链上有5个碳原子,分子中总共含有3个甲基的烷烃分子有
A.2种 B.3种 C.4种 D.5种
4.催化剂RuO2/Al-MgF2耐HF的腐蚀,如图所示可应用于氟化工行业中的氯循环。下列说法不正确的是
A.若Ru的价电子排布式为4d75s1,则该元素位于Ⅷ族
B.上述转化过程中涉及的有机反应类型有加成反应、消去反应
C.可通过液化分离出HCl中大多数的HF
D.上述循环中有水生成
5.下列说法正确的是
A.蛋白质、纤维素和油脂水解的最终产物都含有电解质
B.煤中含有煤焦油等有机物,可以通过分馏的方法从煤焦油中获得苯和二甲苯等物质
C.紫外光谱仪,红外光谱仪以及质谱仪都可用于研究有机物结构
D.石油工业中通过对轻质油进行裂化得到乙烯等气体
6.NM—3是处于临床试验阶段的小分子抗癌药物,分子结构如图。下列说法正确的是
A.该有机物的化学式为C12H12O6
B.该有机物含有三种官能团
C.该物质不属于芳香化合物
D.该有机物可属于羧酸类
7.下列化学用语错误的是
A. 的结构示意图为
B.二氧化硅的分子式为
C.中子数为8的氮原子可表示为
D.HClO的结构式为H-O-Cl
8.下列说法错误的是
A.利用红外光谱实验可确定青蒿素分子中含有的部分基团
B.超分子具有分子识别和自组装的特征
C.金刚石晶体中碳原子个数与C—C键键数之比为1:4
D.等离子体是由电子、阳离子和电中性的粒子组成的
9.有机化合物E( )是制备新型缓解过敏药物的原料。下列说法正确的是
A.E的分子式为C13H11N2OCl,每个分子中含有两个苯环
B.E分子的官能团中含有酰胺基,分子的不饱和度为9
C.每个E分子含有1个手性碳原子和7个双键
D.E可以发生水解、氧化、加成、消去等反应
10.下列关于蒸馏操作有关说法正确的是
A.温度计的水银球应插入到液面以下
B.蒸馏过程中,加入沸石(或碎瓷片)的目的是防止暴沸
C.冷凝管进出水的方向是上进下出
D.用烧杯接收蒸馏出来的液体
11.芬必得是一种高效的消炎药物,主要成分为布洛芬,布洛芬的结构简式如图所示。下列有关布洛芬的说法正确的是
A.分子式为 B.不能使酸性高锰酸钾溶液褪色
C.可以发生加成反应和取代反应 D.苯环上的一氯代物有4种
二、填空题
12.有0.1 mol某有机物A和0.25 mol氧气在一密闭容器中充分燃烧,所得产物通过浓硫酸时使其增重5.4g,再通过足量灼热的氧化铜粉末,固体质量减轻1.6g,最后再通过足量过氧化钠粉末,固体质量增加了8.4g。试通过分析计算(要写出分析计算过程):
(1)该有机物A的分子式______。
(2)若0.1 mol含羟基的有机物B与有机物A的最简式相同,且在0.2 mol氧气中能完全然烧,试确定B的结构简式______。
13.某种烃A的蒸气折合成标况下的密度是3.214g/L,已知该烃的碳氢质量比为5∶1,求:
(1)该烃的相对分子质量:________;
(2)确定该烃的分子式:____________;
(3)如果该烃的一氯取代物有4种,写出该烃的结构简式:__________;
(4)烃A可由另一种烃B通过加成反应而制得,则烃B的可能的是(任写一种可能的结构简式):_____________。
14.(1)写出下列基团的名称:
—C═C— ─C≡C─ ─CH3 ─CH2CH3或─C2H5
_____ _____ _____ _____
(2)有下列机物,请将它所对应的类别用序号填入下列表格中:
(1)CH3CH2CH3 ①酯
(2)CH2=CH—CH3 ②羧酸
(3)CH3COOCH3 ③醛
(4)CH3-CHO ④醇
(5)CH3-OH ⑤烯烃
(6)CH3CH2COOH ⑥烷烃
物质编号 所属类别编号 物质编号 所属类别编号
(1) _____ (4)
(2) (5)
(3) (6)
15.按要求回答下列问题:
(1)乙烷的结构式为____。
(2)丙烷的结构简式为_____。
(3)分子中含有30个氢原子的饱和链状烷烃的分子式为____。
(4)相对分子质量为58的饱和链状烷烃的结构有____种,分别写出它们的结构简式:_____。
(5)分子式为C5H12的直链烷烃的习惯命名为____,其一氯代物只有一种的同分异构体的结构简式为___。
16.最近,我国一留美化学家参与合成了一种新型炸药,它跟三硝基甘油一样抗打击、抗震,但一经引爆就发生激烈爆炸,据信是迄今最烈性的非核爆炸品。该炸药的化学式为C8N8O16,同种元素的原子在分子中是毫无区别的。
(1)画出它的结构式_________。
(2)写出它的爆炸反应方程式________。
(3)该物质为何是迄今最烈性的非核爆炸品______________。
17.含碳元素的物质是化学世界中最庞大的家族。回答下列问题:
(1)碳在形成化合物时,其键型以共价键为主,中的化学键从形成的过程来看属于___________(填“”或“”)键,从其极性来看属于___________(填“极性”或“非极性”)键。
(2)和分子中属于非极性分子的是___________;与互为等电子体的阳离子是___________;与互为等电子体的阴离子是___________。
(3)有机物中含氧官能团的名称为___________,其中含有___________个手性碳原子。
(4)甲醇与乙烷的相对分子质量和范德华力均相近,但是二者的沸点相差很大,造成该差异的原因是___________。
18.现有下列8种有机物,请按要求作答:
① ② ③ ④ ⑤
(1)按官能团分类,其中属于羧酸的有___________(填序号,下同),属于醇的有___________。
(2)④中所含官能团的名称是___________,③中所含官能团为___________(填符号)。
19.G与C生成H属于_______
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
【详解】A.从核磁共振氢谱图上可以推知有机物分子中有几种不同类型的氢原子以及其数目,A项正确;
B.蒸馏是利用互溶液态混合物中各组分的沸点不同而进行分离的方法,B项正确;
C.通过燃烧,能将有机物转化为简单无机物,并做定量测定,从而测定有机物成分,C项正确;
D.红外光谱是确定有机物分子中的化学键和官能团,不能确定有机物的相对分子质量,D项错误;
故答案为D。
2.C
【详解】分子式为C7H16,且有一个支链的有机物有、、共3种,故答案为:C。
3.B
【详解】烷烃主链上有5个碳原子,且分子中有3个甲基,其中主链上已经含有2个甲基,则侧链含有1个甲基,可以为1个甲基或1个乙基,该烷烃主链的碳架为:,当侧链为1个甲基时,甲基可以在1、2号C,存在2种结构;当侧链为乙基时,乙基只能在2号C,有1种结构,所以满足条件的烷烃的结构简式有3种,答案选B。
4.B
【详解】A.Ru为44号元素,若Ru的价电子排布式为4d75s1,则该元素位于Ⅷ族,A正确;
B. 反应中生成不饱和键,为消去反应;由图可知,没有加成反应,B错误;
C.氟化氢和氯化氢沸点差别较大,可通过液化分离出HCl中大多数的HF,C正确;
D.由图可知,氯化氢和氧气在催化剂作用下生成氯气,根据质量守恒可知,循环中有水生成,D正确;
故选B。
5.C
【详解】A. 蛋白质水解后生成的氨基酸是电解质、纤维素水解后的葡萄糖是非电解质、油脂水解后高级脂肪酸或高级脂肪酸钠是电解质,A错误;
B. 煤中没有煤焦油,煤干馏后生成煤焦油,B错误;
C. 紫外光谱仪可用于测定共轭二烯烃,红外光谱仪可测定某些基团或官能团、质谱仪能确定被测物质的分子量和结构,C正确;
D. 石油工业中通过对轻质油进行裂解得到乙烯、丙烯、丁二烯等气体,D错误;
答案选C。
6.D
【详解】A. 根据有机物结构简式可知该有机物的化学式为C12H10O6,A错误;
B. 该有机物含有4种官能团,分别是羧基、酯基、碳碳双键和酚羟基,B错误;
C. 分子中含有苯环,该物质属于芳香化合物,C错误;
D. 分子中含有羧基,该有机物可属于羧酸类,D正确。
答案选D。
7.B
【详解】A.核外有10个电子,结构示意图为,A正确;
B.二氧化硅是由原子构成的,没有分子,二氧化硅的化学式为,B错误;
C.氮原子质子数为7,中子数为8,质量数为15,可表示为,C正确;
D.HClO的结构式H-O-Cl,D正确;
故答案选B。
8.C
【详解】A.在有机物分子中,组成化学键或官能团的原子处于不断振动的状态,其振动频率与红外光的振动频率相当,利用红外光谱实验可确定青蒿素分子中含有的部分基团,故A正确;
B.超分子是两种或两种以上分子依靠分子间相互作用结合在一起,组成复杂的、有组织的聚集体,具有分子识别与自组装的特征,B正确;
C.在金刚石晶体中,每个碳原子形成4个C-C键,每两个碳原子形成一个C-C键,则每个碳原子形成的共价键平均为,所以在金刚石晶体中,碳原子与C-C键数之比为1:2,C错误;
D.等离子体是电子、阳离子和电中性粒子组成的整体上呈电中性的气态物质,D正确;
故答案选:C。
9.B
【详解】A.E的分子式为C13H11N2OCl,每个分子中仅含有一个苯环,A项错误;
B.每个碳碳双键不饱和度为1,每个碳氮双键不饱和度为1,每个碳氧双键不饱和度为1,环状结构不饱和度为1,苯环不饱和度为4,E分子的不饱和度共计为9,B项正确;
C.E分子中无手性碳原子,苯环的碳原子之间是一种介于碳碳单键和碳碳双键之间的特殊的键,不存在碳碳双键,故共有4个双键,C项错误;
D.E分子中的氯原子与苯环直接连接,不能发生消去反应,D项错误;
答案选B。
10.B
【详解】A.蒸馏操作中温度计的水银球应放在支管口处,故A错误;
B.蒸馏过程中,加入沸石(或碎瓷片)的目的是防止暴沸,故B正确;
C.冷凝管进出水的方向是下进上出,故C错误;
D.蒸馏时用锥形瓶接收蒸馏出来的液体,故D错误;
故选B。
11.C
【详解】A.布洛芬的不饱和度为5,碳原子数为13,氧原子数为2,则氢原子数为,则布洛芬的分子式为,A错误;
B.与苯环相连的碳原子上有氢原子,可以被酸性高锰酸钾溶液氧化,B错误;
C.含有苯环,可以发生加成反应;含有羧基,可以发生酯化反应(取代反应),C正确;
D.苯环上有两个处于对位的取代基,结构对称,所以苯环上只有两种不同化学环境的氢原子,则苯环上的一氯代物有2种,D错误;
故选C。
12. C3H6O3 HOCH2CHO
【分析】“浓硫酸时使其增重5.4g”,则表明反应生成水5.4g,n(H2O)==0.3mol;“通过足量灼热的氧化铜粉末,固体质量减轻1.6g”,发生反应为CO+CuO=Cu+CO2,由此可求出n(CO)==0.1mol;“通过足量过氧化钠粉末,固体质量增加了8.4g”,可将反应简化为Na2O2+CO=Na2CO3,由此得出生成的n(CO2)==0.3mol,其中有0.1molCO2来自CO与CuO的反应,据此分析解答。
【详解】(1)由以上分析,可以得出,0.1molA+0.25molO2=0.3molH2O+0.1molCO+0.2molCO2,从而得出反应方程式为A+2.5O2=3H2O+CO+2CO2,依据质量守恒原理,可得出A的分子式为C3H6O3。答案为:C3H6O3;
(2)由A的分子式C3H6O3,可确定其最简式为CH2O,由此假设B的分子式(CH2O)n,因为0.1 molB在0.2mol氧气中能完全然烧,所以0.1n=0.2,n=2,B的分子式为C2H4O2。由于B分子中含有-OH,所以其结构简式为HOCH2CHO。答案为:HOCH2CHO。
【点睛】此题的易错点主要集中在对“最后再通过足量过氧化钠粉末,固体质量增加了8.4g”的理解。也就是前面还原CuO反应生成的CO2有没有与Na2O2发生反应,因为我们无法将前面反应生成的气体与原混合气进行分离,所以计算得到的CO2的物质的量,应包括还原CuO生成的CO2的物质的量。
13. 72 C5H12 (CH3)2CHCH2 CH3 CH2=C(CH3)CH2 CH3 、(CH3)2CHCH=CH2 、(CH3)2C=CHCH3
【详解】(1)烃A的蒸气折合成标况下的密度是3.214g·L-1,所以A的摩尔质量是3.214g·L-1×22.4L·mol-1=72g·mol-1,该烃的相对分子质量为72。
(2)该烃的碳氢质量比为5∶1,该烃分子中碳、氢原子个数之比是:=5︰12,则该烃最简式是C5H12,该烃的分子式为(C5H12)x,则72x=72,解得x=1,则该烃的分子式为C5H12。
(3)该烃的一氯取代物有4种,说明分子中氢原子有4种,所以结构简式为(CH3)2CHCH2 CH3。
(4)烯烃加氢即得到烷烃,则烷烃分子中相邻碳原子上各去1个氢原子,即形成烯烃,所以B的结构简式可能是 CH2=C(CH3)CH2 CH3 、(CH3)2CHCH=CH2 、(CH3)2C=CHCH3。
14. 双键 三键 甲基 乙基
物质编号 所属类别编号 物质编号 所属类别编号
(1) ⑥ (4) ③
(2) ⑤ (5) ④
(3) ① (6) ②
【详解】(1)由有机物基团的结构简式可得基团的名称分别为:碳碳双键、碳碳三键 、甲基、乙基(2)CH3CH2CH3类别为烷烃;CH2=CH—CH3中的官能团为碳碳双键,类别为烯烃; CH3COOCH3的官能团为酯键,类别为酯;CH3-CHO的官能团为醛基,类别为醛;CH3-OH的官能团为羟基,类别为醇;CH3CH2COOH的官能团为羧基,类别为羧酸;故答案为
物质编号 所属类别编号 物质编号 所属类别编号
(1) ⑥ (4) ③
(2) ⑤ (5) ④
(3) ① (6) ②
15.(1)
(2)CH3CH2CH3
(3)C14H30
(4) 2 CH3CH2CH2CH3、
(5) 正戊烷 C(CH3)4
【解析】(1)
乙烷的分子式为,其结构式为;
(2)
丙烷的分子式为,其结构简式为;
(3)
由烷烃的分子通式(n为正整数)可知,,,其分子式为;
(4)
由烷烃的分子通式可知,,,的同分异构体有2种,分别为和;
(5)
分子式为的直链烷烃的习惯命名为正戊烷, 其一氯代物只有一种的同分异构体则其分子中只有一种化学环境的氢原子,其结构简式为C(CH3)4。
16. 八硝基环辛四烯: C8(NO2)8= 8CO2+4N2 ①八硝基立方烷分解得到的两种气体都是最稳定的化合物;②立方烷的碳架键角只有90℃,大大小于109928'(或答:是张力很大的环),因而八硝基立方烷是一种高能化合物,分解时将释放大量能量;③八硝基立方烷分解产物完全是气体,体积膨胀将引起激烈爆炸
【解析】略
17.(1) 极性
(2) 、
(3) 羧基 1
(4)甲醇分子间存在氢键,因此其沸点远高于乙烷
【解析】(1)
甲烷中碳原子的sp3杂化轨道与氢原子的s轨道以头碰头的方式形成4个碳氢共价键,该共价键为σ键;碳氢键是由不同种原子形成的共价键,为极性共价键。
(2)
甲烷中心原子C的价电子对数为4+(4-14)=4,采取sp3杂化,空间构型为正四面体,正负电荷重心重合,为非极性分子,二氧化碳中心原子C的价电子对数为2+(4-22)=2,采取sp杂化,空间构型为直线型,正负电荷重心重合,为非极性分子;甲烷分子中原子数为5、价电子总数为8,二氧化碳分子中原子数为3、价电子总数为16,利用同主族变换和左右移位法可得,与CH4互为等电子体的阳离子是,与CO2互为等电子体的阴离子是。
(3)
由有机物的结构可知,有机物中含氧官能团为羧基;手性碳原子是指人们将连有四个不同基团的碳原子形象地称为手性碳原子,由有机物的结构可知,其中含1个手性碳原子。
(4)
甲醇分子间存在氢键,但乙烷分子间不存在氢键,因此虽然两者相对分子质量和范德华力均相近,但甲醇的沸点高于乙烷。
18. ⑤ ① 酯基
【详解】(1)①中官能团为羟基,属于醇;②中官能团为碳碳双键,属于烯烃;③中官能团为溴原子,属于卤代烃;④中官能团为酯基,属于酯;⑤中官能团为羧基,属于羧酸。因而按官能团分类,其中属于羧酸的有⑤,属于醇的有①。故答案:⑤;①。
(2)④中所含官能团的名称为酯基,③中所含官能团为。故答案:酯基;。
19.加成反应
【详解】含有双键或三键的有机物与其他物质发生反应时,双键或三键中的一个断裂,在不饱和碳原子两端分别接上其他原子的反应称为加成反应,由G、C、H的结构可看出,G与C生成H属于加成反应。
答案第1页,共2页
答案第1页,共2页
