7.2物质溶解的量同步练习(含答案)---2022-2023学年九年级化学科粤版(2012)下册
文档属性
| 名称 | 7.2物质溶解的量同步练习(含答案)---2022-2023学年九年级化学科粤版(2012)下册 | 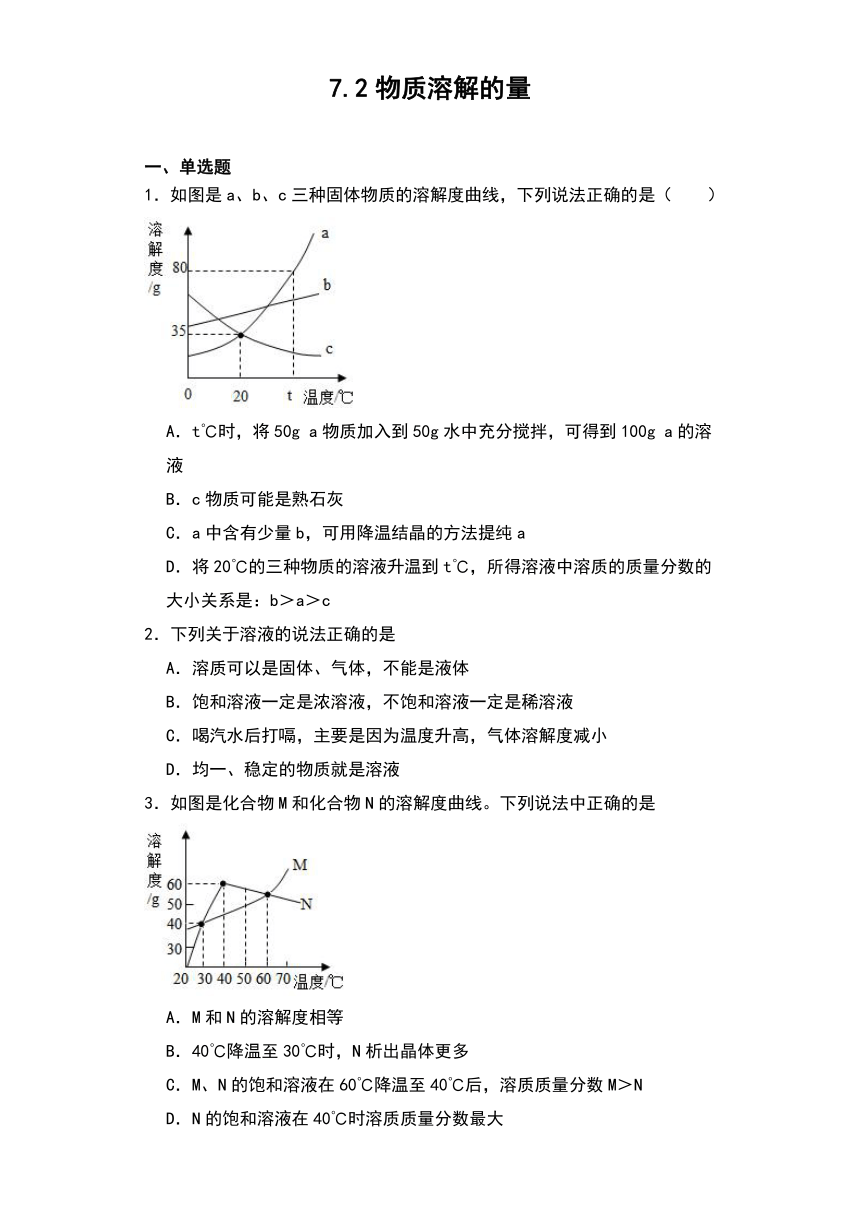 | |
| 格式 | docx | ||
| 文件大小 | 73.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-14 22:40:38 | ||
图片预览



文档简介
7.2物质溶解的量
一、单选题
1.如图是a、b、c三种固体物质的溶解度曲线,下列说法正确的是( )
A.t℃时,将50g a物质加入到50g水中充分搅拌,可得到100g a的溶液
B.c物质可能是熟石灰
C.a中含有少量b,可用降温结晶的方法提纯a
D.将20℃的三种物质的溶液升温到t℃,所得溶液中溶质的质量分数的大小关系是:b>a>c
2.下列关于溶液的说法正确的是
A.溶质可以是固体、气体,不能是液体
B.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液
C.喝汽水后打嗝,主要是因为温度升高,气体溶解度减小
D.均一、稳定的物质就是溶液
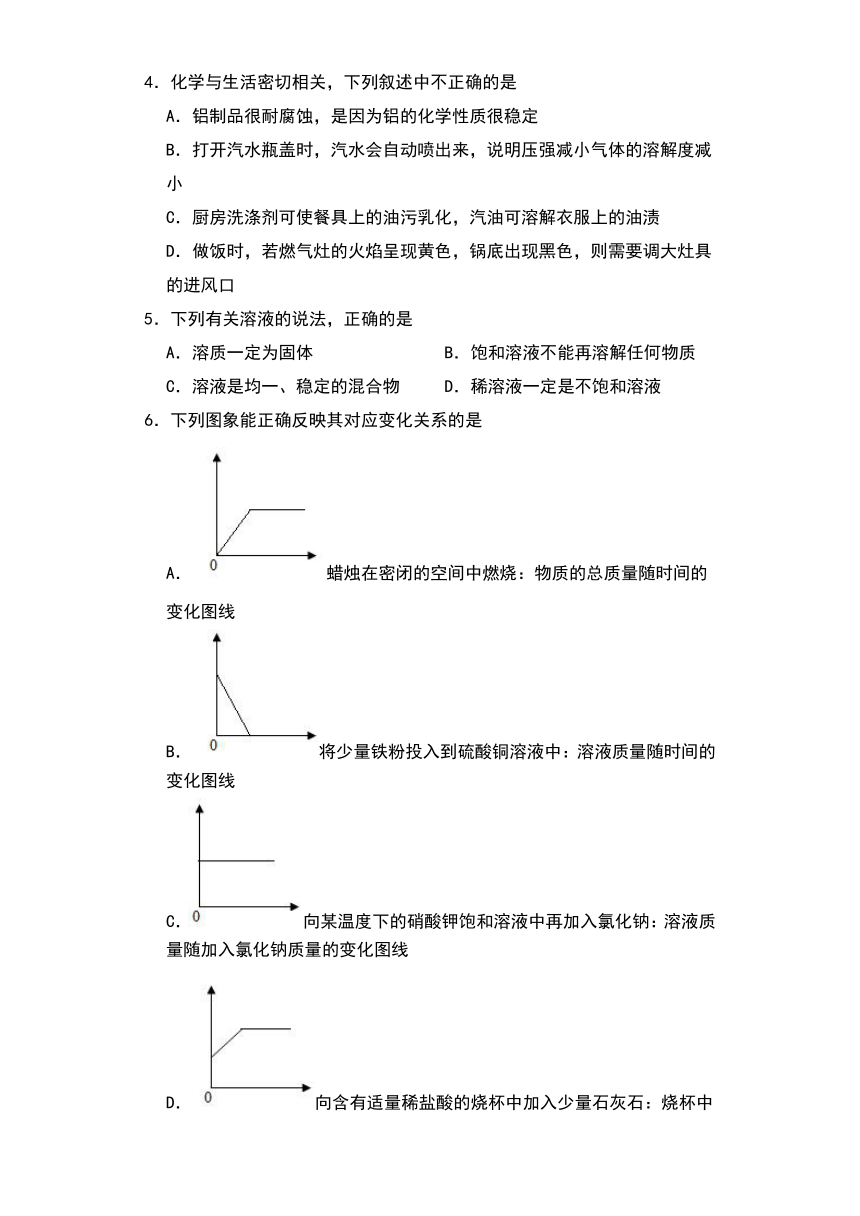
3.如图是化合物M和化合物N的溶解度曲线。下列说法中正确的是
A.M和N的溶解度相等
B.40℃降温至30℃时,N析出晶体更多
C.M、N的饱和溶液在60℃降温至40℃后,溶质质量分数M>N
D.N的饱和溶液在40℃时溶质质量分数最大
4.化学与生活密切相关,下列叙述中不正确的是
A.铝制品很耐腐蚀,是因为铝的化学性质很稳定
B.打开汽水瓶盖时,汽水会自动喷出来,说明压强减小气体的溶解度减小
C.厨房洗涤剂可使餐具上的油污乳化,汽油可溶解衣服上的油渍
D.做饭时,若燃气灶的火焰呈现黄色,锅底出现黑色,则需要调大灶具的进风口
5.下列有关溶液的说法,正确的是
A.溶质一定为固体 B.饱和溶液不能再溶解任何物质
C.溶液是均一、稳定的混合物 D.稀溶液一定是不饱和溶液
6.下列图象能正确反映其对应变化关系的是
A.蜡烛在密闭的空间中燃烧:物质的总质量随时间的变化图线
B.将少量铁粉投入到硫酸铜溶液中:溶液质量随时间的变化图线
C.向某温度下的硝酸钾饱和溶液中再加入氯化钠:溶液质量随加入氯化钠质量的变化图线
D.向含有适量稀盐酸的烧杯中加入少量石灰石:烧杯中物质质量随时间的变化图线
7.有关溶液说法正确的是
A.溶液一定是无色透明的
B.饱和溶液是不能继续溶解溶质的溶液
C.溶液是均一稳定的混合物
D.不饱和溶液一定是稀溶液
8.下列生活中的现象,溶质的溶解度无变化的是
A.揭开啤酒瓶盖,有大量气泡溢出
B.烧水时,沸腾前有较多小气泡
C.加足量白糖,热糖水比凉糖水甜
D.食盐加入水中无明显变化,搅拌后完全溶解
9.水是重要的溶剂。下列有关水和溶液的说法正确的是
A.凡是均一、稳定的液体都属于溶液
B.通过沉淀、过滤、吸附、灭菌等净化后,水的硬度能有效降低
C.要把接近饱和的石灰水溶液变为饱和溶液可蒸发水分或降低温度
D.氯化钾在20℃时的溶解度为34g,那么20℃时50g水中最多能溶解17gKCl
10.下列说法错误的是
A.喝汽水常常打隔,说明气体溶解度与温度有关
B.钢是很纯的铁,所以钢的性能比铁优良
C.浓溶液加水稀释变为稀溶液的过程中,溶质质量不改变
D.海水晒盐析出晶体后的母液是氯化钠的饱和溶液
11.甲、乙两种物质的溶解度曲线如图所示。下列说法正确的是( )
A.甲的溶解度大于乙的溶解度
B.t1℃时,甲、乙两种物质的溶液中,溶质的质量分数相等
C.t2℃时,甲的饱和溶液溶质质量分数为30%
D.t1℃时,甲、乙的饱和溶液分别恒温蒸发20g水,析出晶体的质量相等
12.下列关于溶液的叙述错误的是( )
A.溶液一定是混合物
B.碘酒是一种溶液,其中溶剂是酒精
C.一定温度下,某物质的饱和溶液不能再溶解其他任何物质
D.固态氢氧化钠溶于水溶液温度升高
13.下列关于溶液的说法正确的是( )
A.泥水中,泥是溶质,水是溶剂
B.氢氧化钠在溶解过程中,会放出热量,使溶液温度升高
C.配制溶液时,搅拌可以增大固体物质的溶解度
D.生活中常用蒸馏的方法降低水的硬度
14.下图为甲、乙(均不含结晶水)两种物质的溶解度曲线,根据如图的溶解度曲线,判断下列叙述正确的是
A.将t1℃甲、乙两种物质的溶液升温到t2℃,均变成不饱和溶液,所得溶液中溶质质量分数相等
B.t1℃等质量的甲、乙溶液蒸发等质量的水,甲析出的晶体比乙多
C.甲中混有少量乙时,可以用蒸发溶剂的方法获得较纯净的甲
D.t2℃等质量的甲、乙的溶液降低温度到t1℃后,所得溶液的质量可能相等
15.某固体物质的溶解度曲线如图所示,则下列说法中不正确的是( )
A.图中 B 点的意义:表示该物质在 t3 ℃时,每200g 溶剂和 2S1 g 溶质形成不饱和溶液
B.若 A 点的溶液在保持温度不变的情况下加 50 克水,A 点的溶解度将变小
C.t2 ℃时,A 点溶液中溶质的质量分数一定比M点溶液中的大
D.从该物质的饱和溶液中得到大量的该固体应该采用降温结晶
二、填空题
16.水是生命之源,人类的生产、生活离不开水。
(1)活性炭能除去河水中有颜色、有异味物质,这是利用活性炭的 性,生活中将自来水用 方法,既可降低水的硬度,又可以杀菌。
(2)如图是电解水的简易装置,试管l中收集的气体是 。
(3)高铁酸钾(化学式为K2FeO4)是新型净水剂,K2FeO4中Fe元素的化合价为 。
(4)根据下表回答相关问题。
温度(℃) 0 20 40 60 80 100
溶解度 (g/100g 水) KNO3 13.3 31.6 63.9 110.0 169.0 246.0
NaCl 35.7 36.0 36.6 37.3 38.4 39.8
①上表中两种物质的溶解度相等的温度范围是在 ℃;
②20℃时,将20g NaCl放入50g水中,充分搅拌,所得溶液的质量是 ,要进一步降低该溶液的溶质质量分数,可进行的操作是 。
17.用学过的化学知识说明或解释下列问题:
(1)滴有洗涤剂的水能更好去除油污,是由于洗涤剂有 作用。
(2)蒸馏时蒸馏瓶中沸石的作用是防止 。
(3)蒸发食盐水时玻璃棒需不断搅拌是防止 。
(4)煮水在沸腾前水中常有气泡冒出的原因是气体溶解度随 。
(5)倾倒液体时,试剂瓶标签向手心是为了防止 。
(6)铁粉可作双吸剂是因为可以除去包装袋中的 (填两种常见物质的化学式)。
(7)山林救火在火势蔓延前方砍掉树木达到灭火目的的原理是 。
18.甲、乙、丙三种物质的溶解度线如图所示,请回答问题。
(1)当温度为t2℃时,p点的意义 ,甲、乙、丙三种物质形成饱和溶液的溶质质量分数的关系为 。
(2)t3℃时,甲的饱和溶液中溶质与溶液的质量比是 (填最简比)。
(3)若将丙的饱和溶液从t3℃降温到t1℃时,一定会发生改变的是 。
A 溶解度 B 溶剂质量 C 溶质质量 D 溶质质量分数
19.KNO3和KCl的溶解度曲线如图所示:
(1)t3℃时,KCl的溶解度为 ;
(2)硝酸钾的饱和溶液中提纯全部的硝酸钾,采用的方法是 (选填“蒸发结晶”或“降温结晶”);
(3)现有t2℃时,有相同质量的KNO3和KCl的饱和溶液。不考虑水的蒸发,下列关系一定成立的是 。
A t2℃时,两溶液中溶质的质量分数相等
B 分别降温到t1℃,析出KNO3的质量大于析出KCl的质量
C 分别升温至t3℃,所得溶液中溶质的质量分数相等
D 保持t2℃不变,分别加入等质量的水,混匀后所得溶液中溶质的质量分数相等
20.某物质R在20℃时的溶解度是34g,50℃时的溶解度是52g。现有20℃时盛有150g水的烧杯甲,通过如图所示的操作,分别得到相应的溶液A—E。请回答下列问题:
(1)溶液A属于 (填“饱和”或“不饱和”)溶液。
(2)溶液B中溶质和溶剂的质量比为 (填最简整数比)。
(3)已知溶液C恰好饱和,步骤③中的m的值为 。
(4)上述溶液中,溶质质量分数一定相等的是 (填字母)。
三、实验题
21.图1是甲、乙两种固体物质的溶解度曲线,请结合图1、图2回答问题.
(1) ℃时,甲物质与乙物质的溶解度相等.
(2)使甲物质从60℃的饱和溶液中结晶析出的最好方法是 .
(3)80℃时,将等质量的甲、乙两种物质分别加入盛有100g水的烧杯中充分溶解,观察到的现象如图2所示. (填A或B)烧杯中的溶液一定达到饱和状态,溶质的质量分数为 .要使A烧杯中剩余的固体继续溶解可采用的一种方法是 .
参考答案:
1.C2.C3.D4.A5.C6.D7.C8.D9.D10.B11.D12.C13.B14.D15.B
16.(1)吸附 煮沸
(2)氢气(H2)
(3)+6
(4)20~40℃ 68g 加水或降温
17.乳化 暴沸 液体局部受热过高造成液体飞溅 温度的升高而减小 残留液流下腐蚀标签 H2O、O2 隔离可燃物
18.t2°C时,甲乙物质溶解度相等 甲=乙>丙 4:9 A
19.40.0g 蒸发结晶 ABCD
20.不饱和 1:3 28 CD
21.40 降温 A 23.1% 加溶剂(或降温)
一、单选题
1.如图是a、b、c三种固体物质的溶解度曲线,下列说法正确的是( )
A.t℃时,将50g a物质加入到50g水中充分搅拌,可得到100g a的溶液
B.c物质可能是熟石灰
C.a中含有少量b,可用降温结晶的方法提纯a
D.将20℃的三种物质的溶液升温到t℃,所得溶液中溶质的质量分数的大小关系是:b>a>c
2.下列关于溶液的说法正确的是
A.溶质可以是固体、气体,不能是液体
B.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液
C.喝汽水后打嗝,主要是因为温度升高,气体溶解度减小
D.均一、稳定的物质就是溶液
3.如图是化合物M和化合物N的溶解度曲线。下列说法中正确的是
A.M和N的溶解度相等
B.40℃降温至30℃时,N析出晶体更多
C.M、N的饱和溶液在60℃降温至40℃后,溶质质量分数M>N
D.N的饱和溶液在40℃时溶质质量分数最大
4.化学与生活密切相关,下列叙述中不正确的是
A.铝制品很耐腐蚀,是因为铝的化学性质很稳定
B.打开汽水瓶盖时,汽水会自动喷出来,说明压强减小气体的溶解度减小
C.厨房洗涤剂可使餐具上的油污乳化,汽油可溶解衣服上的油渍
D.做饭时,若燃气灶的火焰呈现黄色,锅底出现黑色,则需要调大灶具的进风口
5.下列有关溶液的说法,正确的是
A.溶质一定为固体 B.饱和溶液不能再溶解任何物质
C.溶液是均一、稳定的混合物 D.稀溶液一定是不饱和溶液
6.下列图象能正确反映其对应变化关系的是
A.蜡烛在密闭的空间中燃烧:物质的总质量随时间的变化图线
B.将少量铁粉投入到硫酸铜溶液中:溶液质量随时间的变化图线
C.向某温度下的硝酸钾饱和溶液中再加入氯化钠:溶液质量随加入氯化钠质量的变化图线
D.向含有适量稀盐酸的烧杯中加入少量石灰石:烧杯中物质质量随时间的变化图线
7.有关溶液说法正确的是
A.溶液一定是无色透明的
B.饱和溶液是不能继续溶解溶质的溶液
C.溶液是均一稳定的混合物
D.不饱和溶液一定是稀溶液
8.下列生活中的现象,溶质的溶解度无变化的是
A.揭开啤酒瓶盖,有大量气泡溢出
B.烧水时,沸腾前有较多小气泡
C.加足量白糖,热糖水比凉糖水甜
D.食盐加入水中无明显变化,搅拌后完全溶解
9.水是重要的溶剂。下列有关水和溶液的说法正确的是
A.凡是均一、稳定的液体都属于溶液
B.通过沉淀、过滤、吸附、灭菌等净化后,水的硬度能有效降低
C.要把接近饱和的石灰水溶液变为饱和溶液可蒸发水分或降低温度
D.氯化钾在20℃时的溶解度为34g,那么20℃时50g水中最多能溶解17gKCl
10.下列说法错误的是
A.喝汽水常常打隔,说明气体溶解度与温度有关
B.钢是很纯的铁,所以钢的性能比铁优良
C.浓溶液加水稀释变为稀溶液的过程中,溶质质量不改变
D.海水晒盐析出晶体后的母液是氯化钠的饱和溶液
11.甲、乙两种物质的溶解度曲线如图所示。下列说法正确的是( )
A.甲的溶解度大于乙的溶解度
B.t1℃时,甲、乙两种物质的溶液中,溶质的质量分数相等
C.t2℃时,甲的饱和溶液溶质质量分数为30%
D.t1℃时,甲、乙的饱和溶液分别恒温蒸发20g水,析出晶体的质量相等
12.下列关于溶液的叙述错误的是( )
A.溶液一定是混合物
B.碘酒是一种溶液,其中溶剂是酒精
C.一定温度下,某物质的饱和溶液不能再溶解其他任何物质
D.固态氢氧化钠溶于水溶液温度升高
13.下列关于溶液的说法正确的是( )
A.泥水中,泥是溶质,水是溶剂
B.氢氧化钠在溶解过程中,会放出热量,使溶液温度升高
C.配制溶液时,搅拌可以增大固体物质的溶解度
D.生活中常用蒸馏的方法降低水的硬度
14.下图为甲、乙(均不含结晶水)两种物质的溶解度曲线,根据如图的溶解度曲线,判断下列叙述正确的是
A.将t1℃甲、乙两种物质的溶液升温到t2℃,均变成不饱和溶液,所得溶液中溶质质量分数相等
B.t1℃等质量的甲、乙溶液蒸发等质量的水,甲析出的晶体比乙多
C.甲中混有少量乙时,可以用蒸发溶剂的方法获得较纯净的甲
D.t2℃等质量的甲、乙的溶液降低温度到t1℃后,所得溶液的质量可能相等
15.某固体物质的溶解度曲线如图所示,则下列说法中不正确的是( )
A.图中 B 点的意义:表示该物质在 t3 ℃时,每200g 溶剂和 2S1 g 溶质形成不饱和溶液
B.若 A 点的溶液在保持温度不变的情况下加 50 克水,A 点的溶解度将变小
C.t2 ℃时,A 点溶液中溶质的质量分数一定比M点溶液中的大
D.从该物质的饱和溶液中得到大量的该固体应该采用降温结晶
二、填空题
16.水是生命之源,人类的生产、生活离不开水。
(1)活性炭能除去河水中有颜色、有异味物质,这是利用活性炭的 性,生活中将自来水用 方法,既可降低水的硬度,又可以杀菌。
(2)如图是电解水的简易装置,试管l中收集的气体是 。
(3)高铁酸钾(化学式为K2FeO4)是新型净水剂,K2FeO4中Fe元素的化合价为 。
(4)根据下表回答相关问题。
温度(℃) 0 20 40 60 80 100
溶解度 (g/100g 水) KNO3 13.3 31.6 63.9 110.0 169.0 246.0
NaCl 35.7 36.0 36.6 37.3 38.4 39.8
①上表中两种物质的溶解度相等的温度范围是在 ℃;
②20℃时,将20g NaCl放入50g水中,充分搅拌,所得溶液的质量是 ,要进一步降低该溶液的溶质质量分数,可进行的操作是 。
17.用学过的化学知识说明或解释下列问题:
(1)滴有洗涤剂的水能更好去除油污,是由于洗涤剂有 作用。
(2)蒸馏时蒸馏瓶中沸石的作用是防止 。
(3)蒸发食盐水时玻璃棒需不断搅拌是防止 。
(4)煮水在沸腾前水中常有气泡冒出的原因是气体溶解度随 。
(5)倾倒液体时,试剂瓶标签向手心是为了防止 。
(6)铁粉可作双吸剂是因为可以除去包装袋中的 (填两种常见物质的化学式)。
(7)山林救火在火势蔓延前方砍掉树木达到灭火目的的原理是 。
18.甲、乙、丙三种物质的溶解度线如图所示,请回答问题。
(1)当温度为t2℃时,p点的意义 ,甲、乙、丙三种物质形成饱和溶液的溶质质量分数的关系为 。
(2)t3℃时,甲的饱和溶液中溶质与溶液的质量比是 (填最简比)。
(3)若将丙的饱和溶液从t3℃降温到t1℃时,一定会发生改变的是 。
A 溶解度 B 溶剂质量 C 溶质质量 D 溶质质量分数
19.KNO3和KCl的溶解度曲线如图所示:
(1)t3℃时,KCl的溶解度为 ;
(2)硝酸钾的饱和溶液中提纯全部的硝酸钾,采用的方法是 (选填“蒸发结晶”或“降温结晶”);
(3)现有t2℃时,有相同质量的KNO3和KCl的饱和溶液。不考虑水的蒸发,下列关系一定成立的是 。
A t2℃时,两溶液中溶质的质量分数相等
B 分别降温到t1℃,析出KNO3的质量大于析出KCl的质量
C 分别升温至t3℃,所得溶液中溶质的质量分数相等
D 保持t2℃不变,分别加入等质量的水,混匀后所得溶液中溶质的质量分数相等
20.某物质R在20℃时的溶解度是34g,50℃时的溶解度是52g。现有20℃时盛有150g水的烧杯甲,通过如图所示的操作,分别得到相应的溶液A—E。请回答下列问题:
(1)溶液A属于 (填“饱和”或“不饱和”)溶液。
(2)溶液B中溶质和溶剂的质量比为 (填最简整数比)。
(3)已知溶液C恰好饱和,步骤③中的m的值为 。
(4)上述溶液中,溶质质量分数一定相等的是 (填字母)。
三、实验题
21.图1是甲、乙两种固体物质的溶解度曲线,请结合图1、图2回答问题.
(1) ℃时,甲物质与乙物质的溶解度相等.
(2)使甲物质从60℃的饱和溶液中结晶析出的最好方法是 .
(3)80℃时,将等质量的甲、乙两种物质分别加入盛有100g水的烧杯中充分溶解,观察到的现象如图2所示. (填A或B)烧杯中的溶液一定达到饱和状态,溶质的质量分数为 .要使A烧杯中剩余的固体继续溶解可采用的一种方法是 .
参考答案:
1.C2.C3.D4.A5.C6.D7.C8.D9.D10.B11.D12.C13.B14.D15.B
16.(1)吸附 煮沸
(2)氢气(H2)
(3)+6
(4)20~40℃ 68g 加水或降温
17.乳化 暴沸 液体局部受热过高造成液体飞溅 温度的升高而减小 残留液流下腐蚀标签 H2O、O2 隔离可燃物
18.t2°C时,甲乙物质溶解度相等 甲=乙>丙 4:9 A
19.40.0g 蒸发结晶 ABCD
20.不饱和 1:3 28 CD
21.40 降温 A 23.1% 加溶剂(或降温)
