4.2.1元素性质的周期性变化规律 课件(共25张PPT) 2023-2024学年高一上学期化学人教版(2019)必修第一册
文档属性
| 名称 | 4.2.1元素性质的周期性变化规律 课件(共25张PPT) 2023-2024学年高一上学期化学人教版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-14 00:00:00 | ||
图片预览






文档简介
(共25张PPT)
第四章 物质结构 元素周期律
第二节 元素周期律
第一课时 元素性质的周期性变化规律
01
原子核外电子排布
02
03
学
习
目
标
找出核外电子排布特点:呈周期性的变化 。
元素的性质
根据核外电子排布的变化特点,理解元素的性质:原子半径、主要化合价的递变性。
元素周期律
理解元素周期律的实质,并能应用解决有关问题
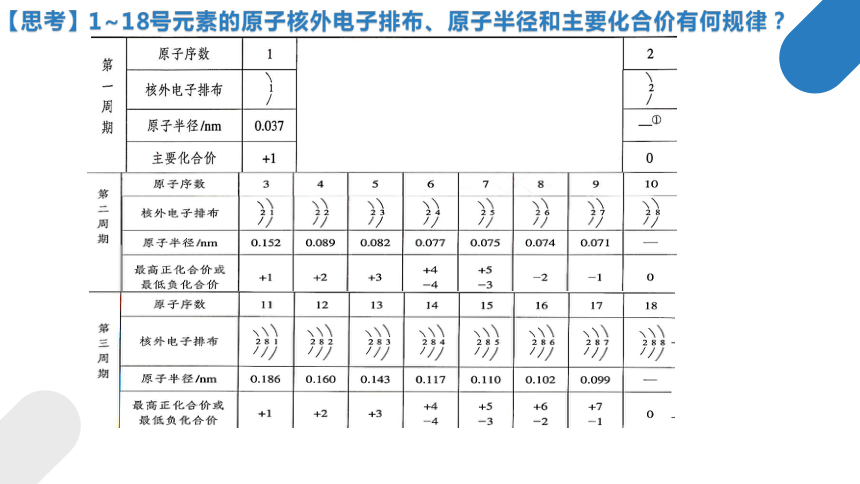
【思考】1~18号元素的原子核外电子排布、原子半径和主要化合价有何规律?
一、元素性质的周期性变化规律
1. 元素原子结构的周期性变化
周期序数 原子序数 电子层数 最外层电子数
一 1~2 1 1 → 2
二 3~10
三 11~18
2
3
1 →8
1 →8
由1到8
规律:
同周期,从左到右,随着原子序数的递增,元素原子的最外层电子排布呈现 的周期性变化(第一周期除外)
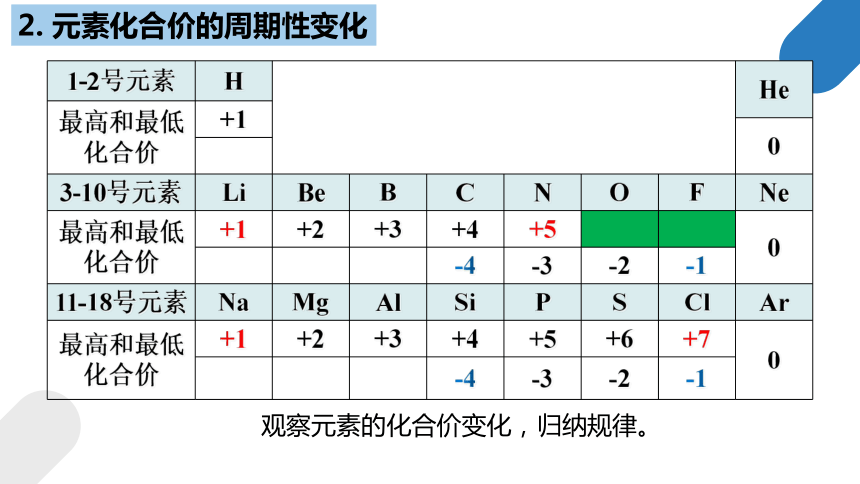
2. 元素化合价的周期性变化
观察元素的化合价变化,归纳规律。
1-2号元素 H He
最高和最低 化合价 +1
0
3-10号元素 Li Be B C N O F Ne
最高和最低 化合价 +1 +2 +3 +4 +5 0
-4 -3 -2 -1
11-18号元素 Na Mg Al Si P S Cl Ar
最高和最低 化合价 +1 +2 +3 +4 +5 +6 +7 0
-4 -3 -2 -1
原子序数 最高或最低化合价的变化
1~2
3~10
11~18
规律:同周期,从左到右,随着原子序数的递增,元素的最高正化合价呈现由 (第二周期 ),最低负化合价呈现由 的周期性变化。
2 . 元素化合价的周期性变化
+1 → 0
+1 → +5
-4 → -1 → 0
+1 → +7
-4 → -1 → 0
+1 → +7
+1 → +5
-4 → -1
元素的主要化合价:指最高正价和最低负价
分析表4-5(p-105)
①元素的最高正价=最外层电子数(O、F无正价)
②元素的最低负价=最外层电子数-8(金属无负价)
③稀有气体元素化合价为0
2 . 元素化合价的周期性变化
g
测量依据不同
3. 元素原子半径的周期性变化
观察原子的半径变化,归纳规律。
规律:同周期,从左到右,随着原子序数的递增,原子半径逐渐减小
同主族,从上到下,随着原子序数的增大,原子半径逐渐增大
原子序数 原子半径的变化
1~2
3~10
11~18
3. 元素原子半径的周期性变化
逐渐减小
逐渐减小
【思考】对于电子层数相同(同周期)的原子,为什么核电荷数越多,原子半径越小?
原因:核电荷数越多,原子对核外电子的引力越大,原子半径越小。
【归纳整理】微粒半径大小比较方法:
同种元素:
价高径小
不同元素
电子层数不同:
层多径大
电子层数相同:
序大径小
微粒半径
如:r(Fe)>r(Fe2+)>r(Fe3+) 、r(Cl-)>r(Cl)
如:r(S)>r(C)>r(H)
如:r(Na)>r(Mg)>r(Al)
如:r(N3-)>r(O2-)>r(Al3+)
1.请画出O2-、F-、Na+、Mg2+四种离子核外电子排布,并比较离子半径:
①核外电子排布:
②离子半径:
[学以致用]
课堂练习
1. 下列各组元素中,按原子半径依次增大的顺序排列的是( )
A. Na、Mg、Al B. Cl、S、P
C. Na、N、F D. I、Br、Cl
2. 下列化合物中,阳离子与阴离子半径比最小的是( )
A. NaF B. LiI C. CsF D. LiF
B
B
3. 下列各组元素性质的递变错误的是( )
A.Li、Be、B原子最外层电子数依次增多
B.P、S、Cl元素的最高正化合价依次升高
C.B、C、N、O、F原子半径依次增大
D.Be、Mg、Ca、Sr、Ba的失电子能力依次增强
C
二、第三周期元素性质的递变性规律
【探究一】:探究钠、镁、铝金属性强弱
实验操作 实验现象 实验结论
加热前,镁条表面附着了少量 ,加热至沸腾后,有较多的 ,溶液变为 色 镁与冷水几乎不反应,能与热水反应,反应的化学方程式为
无色气泡
无色气泡冒出
红
Na Mg Al
与水(或酸) 反应的现象 与冷水剧烈反应,放出大量的热,并产生气体 与冷水几乎不反应,与沸水缓慢反应,与酸剧烈反应 与沸水反应很慢,与酸反应较快
剧烈程度 随着核电荷数增大,与水(或酸)反应越来越________
最高价氧化物对应水化物的碱性强弱 NaOH 强碱 Mg(OH)2 中强碱 Al(OH)3
结论 ① 最高价氧化物对应的水化物的碱性:__________________ ② 金属性:__________________
缓慢
NaOH>Mg(OH)2>Al(OH)3
Na>Mg>Al
两性氢氧化物
【探究一】探究钠、镁、铝金属性强弱
【探究二】探究钠、铝的金属性强弱
AlCl3溶液
氨水
HCl溶液
NaOH溶液
Al3+ + 3NH3·H2O = Al(OH)3↓+ 3NH4+
Al(OH)3 + 3HCl = AlCl3 + 3H2O
Al(OH)3+NaOH = NaAlO2 + 2H2O
白色絮状沉淀
体现Na的金属性比Al的金属性强
Na Mg Al Si P S Cl
电子层数相同,核电荷数增大,半径减小
最外层电子数依次递增,失电子能力减弱,得电子能力增强
金属性减弱,非金属性增强
二、第三周期元素性质的递变性规律
判断金属性强弱的标准是什么?
如何证明Si、P、S、Cl的非金属性逐渐增强呢?
元素金属性和非金属性的周期性变化
1、元素金属性和非金属性的判断标准
(1)直接
判据
金属性
元素的原子失电子 的能力
非金属性
元素的原子得电子的能力
(2)间接判据
金属性
非金属性
a、元素的单质与水或与酸反应置换出氢气的难易。
越容易,元素的金属性就越强。
b、元素最高正价氧化物对应的水化物的碱性强弱。
碱性越强,元素的金属性就越强。
a、元素的单质与氢气生成气态氢化物的难易和气态氢化物的稳定性。
越容易,越稳定则元素的非金属性就越强。
b、元素最高正价氧化物对应的水化物酸性强弱
酸性越强,元素的非金属性就越强
【思考】如何证明Si、P、S、Cl的非金属性逐渐增强呢?
非金属元素 Si P S Cl
最高价氧化物对应的水化物(含氧酸)的酸性强弱 H2SiO3(硅酸) 酸 H3PO4(磷酸) 酸 H2SO4(硫酸) 酸 HClO4(高氯酸)
酸
最高价氧化物对应的水化物(含氧酸)的酸性强弱: 。
非金属性由弱到强的顺序为
弱
强
强
H2SiO3Si中强
元素 单质与氢气的化合条件 氢化物化学式 氢化物稳定性 结论
Si 高温下少量反应 SiH4 很不稳定 非金属性由弱到强的顺序为
P 磷蒸气,困难 PH3 不稳定
S 加热反应 H2S 较不稳定
Cl 光照或点燃 HCl 稳定
Si【思考】如何证明Si、P、S、Cl的非金属性逐渐增强呢?
二、第三周期元素性质的递变性规律
同一周期元素,电子层数相同,从左到右,核电荷数依次 ,最外层电子数逐渐 ,原子半径逐渐 ,越容易 电子形成稳定结构,非金属性逐渐 ,金属性逐渐 。
增多
增多
减小
得到
增强
减弱
类比:其他周期主族元素,一般情况下也会得出类似的结论
三、元素周期律
1. 定义:元素的性质随着原子序数的递增而呈周期性的变化。
2. 实质:元素原子的核外电子排布的周期性变化。
即元素原子核外电子排布的周期性变化决定了元素性质的周期性变化。
巩固练习
1. X、Y、Z 为同周期的三种元素。已知它们最高价氧化物的水化物的酸性由强到弱的顺序为HXO4 > H2YO4 > H3ZO4,则下列判断正确的是( )
A. 非金属性:X < Y < Z
B. 原子半径:X > Y > Z
C. 气态氢化物的稳定性:X > Y > Z
D. 原子最外层电子数:X < Y < Z
C
2. 下列事实不能用元素周期律解释的只有( )
A. 碱性:KOH>NaOH B. 相对原子质量:Ar>K
C. 酸性:HClO4>H2SO4 D. 元素的金属性:Mg>Al
B
3. 如图为周期表中短周期的一部分。已知a原子的最外层电子数是电子总数的三分之一,下列说法中正确的是( )
A. a的最高价氧化物对应水化物有两性
B. b与d组成的化合物不能与水反应
C. c的单质能与强碱反应生成两种盐
D. 非金属性:c>d>b>a
C
第四章 物质结构 元素周期律
第二节 元素周期律
第一课时 元素性质的周期性变化规律
01
原子核外电子排布
02
03
学
习
目
标
找出核外电子排布特点:呈周期性的变化 。
元素的性质
根据核外电子排布的变化特点,理解元素的性质:原子半径、主要化合价的递变性。
元素周期律
理解元素周期律的实质,并能应用解决有关问题
【思考】1~18号元素的原子核外电子排布、原子半径和主要化合价有何规律?
一、元素性质的周期性变化规律
1. 元素原子结构的周期性变化
周期序数 原子序数 电子层数 最外层电子数
一 1~2 1 1 → 2
二 3~10
三 11~18
2
3
1 →8
1 →8
由1到8
规律:
同周期,从左到右,随着原子序数的递增,元素原子的最外层电子排布呈现 的周期性变化(第一周期除外)
2. 元素化合价的周期性变化
观察元素的化合价变化,归纳规律。
1-2号元素 H He
最高和最低 化合价 +1
0
3-10号元素 Li Be B C N O F Ne
最高和最低 化合价 +1 +2 +3 +4 +5 0
-4 -3 -2 -1
11-18号元素 Na Mg Al Si P S Cl Ar
最高和最低 化合价 +1 +2 +3 +4 +5 +6 +7 0
-4 -3 -2 -1
原子序数 最高或最低化合价的变化
1~2
3~10
11~18
规律:同周期,从左到右,随着原子序数的递增,元素的最高正化合价呈现由 (第二周期 ),最低负化合价呈现由 的周期性变化。
2 . 元素化合价的周期性变化
+1 → 0
+1 → +5
-4 → -1 → 0
+1 → +7
-4 → -1 → 0
+1 → +7
+1 → +5
-4 → -1
元素的主要化合价:指最高正价和最低负价
分析表4-5(p-105)
①元素的最高正价=最外层电子数(O、F无正价)
②元素的最低负价=最外层电子数-8(金属无负价)
③稀有气体元素化合价为0
2 . 元素化合价的周期性变化
g
测量依据不同
3. 元素原子半径的周期性变化
观察原子的半径变化,归纳规律。
规律:同周期,从左到右,随着原子序数的递增,原子半径逐渐减小
同主族,从上到下,随着原子序数的增大,原子半径逐渐增大
原子序数 原子半径的变化
1~2
3~10
11~18
3. 元素原子半径的周期性变化
逐渐减小
逐渐减小
【思考】对于电子层数相同(同周期)的原子,为什么核电荷数越多,原子半径越小?
原因:核电荷数越多,原子对核外电子的引力越大,原子半径越小。
【归纳整理】微粒半径大小比较方法:
同种元素:
价高径小
不同元素
电子层数不同:
层多径大
电子层数相同:
序大径小
微粒半径
如:r(Fe)>r(Fe2+)>r(Fe3+) 、r(Cl-)>r(Cl)
如:r(S)>r(C)>r(H)
如:r(Na)>r(Mg)>r(Al)
如:r(N3-)>r(O2-)>r(Al3+)
1.请画出O2-、F-、Na+、Mg2+四种离子核外电子排布,并比较离子半径:
①核外电子排布:
②离子半径:
[学以致用]
课堂练习
1. 下列各组元素中,按原子半径依次增大的顺序排列的是( )
A. Na、Mg、Al B. Cl、S、P
C. Na、N、F D. I、Br、Cl
2. 下列化合物中,阳离子与阴离子半径比最小的是( )
A. NaF B. LiI C. CsF D. LiF
B
B
3. 下列各组元素性质的递变错误的是( )
A.Li、Be、B原子最外层电子数依次增多
B.P、S、Cl元素的最高正化合价依次升高
C.B、C、N、O、F原子半径依次增大
D.Be、Mg、Ca、Sr、Ba的失电子能力依次增强
C
二、第三周期元素性质的递变性规律
【探究一】:探究钠、镁、铝金属性强弱
实验操作 实验现象 实验结论
加热前,镁条表面附着了少量 ,加热至沸腾后,有较多的 ,溶液变为 色 镁与冷水几乎不反应,能与热水反应,反应的化学方程式为
无色气泡
无色气泡冒出
红
Na Mg Al
与水(或酸) 反应的现象 与冷水剧烈反应,放出大量的热,并产生气体 与冷水几乎不反应,与沸水缓慢反应,与酸剧烈反应 与沸水反应很慢,与酸反应较快
剧烈程度 随着核电荷数增大,与水(或酸)反应越来越________
最高价氧化物对应水化物的碱性强弱 NaOH 强碱 Mg(OH)2 中强碱 Al(OH)3
结论 ① 最高价氧化物对应的水化物的碱性:__________________ ② 金属性:__________________
缓慢
NaOH>Mg(OH)2>Al(OH)3
Na>Mg>Al
两性氢氧化物
【探究一】探究钠、镁、铝金属性强弱
【探究二】探究钠、铝的金属性强弱
AlCl3溶液
氨水
HCl溶液
NaOH溶液
Al3+ + 3NH3·H2O = Al(OH)3↓+ 3NH4+
Al(OH)3 + 3HCl = AlCl3 + 3H2O
Al(OH)3+NaOH = NaAlO2 + 2H2O
白色絮状沉淀
体现Na的金属性比Al的金属性强
Na Mg Al Si P S Cl
电子层数相同,核电荷数增大,半径减小
最外层电子数依次递增,失电子能力减弱,得电子能力增强
金属性减弱,非金属性增强
二、第三周期元素性质的递变性规律
判断金属性强弱的标准是什么?
如何证明Si、P、S、Cl的非金属性逐渐增强呢?
元素金属性和非金属性的周期性变化
1、元素金属性和非金属性的判断标准
(1)直接
判据
金属性
元素的原子失电子 的能力
非金属性
元素的原子得电子的能力
(2)间接判据
金属性
非金属性
a、元素的单质与水或与酸反应置换出氢气的难易。
越容易,元素的金属性就越强。
b、元素最高正价氧化物对应的水化物的碱性强弱。
碱性越强,元素的金属性就越强。
a、元素的单质与氢气生成气态氢化物的难易和气态氢化物的稳定性。
越容易,越稳定则元素的非金属性就越强。
b、元素最高正价氧化物对应的水化物酸性强弱
酸性越强,元素的非金属性就越强
【思考】如何证明Si、P、S、Cl的非金属性逐渐增强呢?
非金属元素 Si P S Cl
最高价氧化物对应的水化物(含氧酸)的酸性强弱 H2SiO3(硅酸) 酸 H3PO4(磷酸) 酸 H2SO4(硫酸) 酸 HClO4(高氯酸)
酸
最高价氧化物对应的水化物(含氧酸)的酸性强弱: 。
非金属性由弱到强的顺序为
弱
强
强
H2SiO3
元素 单质与氢气的化合条件 氢化物化学式 氢化物稳定性 结论
Si 高温下少量反应 SiH4 很不稳定 非金属性由弱到强的顺序为
P 磷蒸气,困难 PH3 不稳定
S 加热反应 H2S 较不稳定
Cl 光照或点燃 HCl 稳定
Si
二、第三周期元素性质的递变性规律
同一周期元素,电子层数相同,从左到右,核电荷数依次 ,最外层电子数逐渐 ,原子半径逐渐 ,越容易 电子形成稳定结构,非金属性逐渐 ,金属性逐渐 。
增多
增多
减小
得到
增强
减弱
类比:其他周期主族元素,一般情况下也会得出类似的结论
三、元素周期律
1. 定义:元素的性质随着原子序数的递增而呈周期性的变化。
2. 实质:元素原子的核外电子排布的周期性变化。
即元素原子核外电子排布的周期性变化决定了元素性质的周期性变化。
巩固练习
1. X、Y、Z 为同周期的三种元素。已知它们最高价氧化物的水化物的酸性由强到弱的顺序为HXO4 > H2YO4 > H3ZO4,则下列判断正确的是( )
A. 非金属性:X < Y < Z
B. 原子半径:X > Y > Z
C. 气态氢化物的稳定性:X > Y > Z
D. 原子最外层电子数:X < Y < Z
C
2. 下列事实不能用元素周期律解释的只有( )
A. 碱性:KOH>NaOH B. 相对原子质量:Ar>K
C. 酸性:HClO4>H2SO4 D. 元素的金属性:Mg>Al
B
3. 如图为周期表中短周期的一部分。已知a原子的最外层电子数是电子总数的三分之一,下列说法中正确的是( )
A. a的最高价氧化物对应水化物有两性
B. b与d组成的化合物不能与水反应
C. c的单质能与强碱反应生成两种盐
D. 非金属性:c>d>b>a
C
