第3章有机合成及其应用合成高分子化合物测试卷(含解析)2022-2023学年下学期高二化学鲁科版(2019)选择性必修3
文档属性
| 名称 | 第3章有机合成及其应用合成高分子化合物测试卷(含解析)2022-2023学年下学期高二化学鲁科版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 594.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-16 00:00:00 | ||
图片预览



文档简介
第3章 有机合成及其应用 合成高分子化合物 测试卷
一、单选题
1.分枝酸可用于生化研究,其结构简式为,下列关于分枝酸的说法正确的是
A.分子中含有3种官能团
B.1 mol分枝酸最多可与3mol NaOH发生中和反应
C.在一定条件下可与乙醇、乙酸反应,且反应类型相同
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且褪色原理相同
2.化学分析的手段通常有定性分析、定量分析、仪器分析等,现代化学中仪器分析是研究物质结构的基本方法和实验手段。下列仪器分析手段的运用科学可行的是
A.光谱分析:利用原子光谱上的特征谱线来鉴定元素
B.质谱分析:利用质荷比来测定分子立体结构
C.红外光谱分析:利用分子吸收与化学键振动频率相同的红外线来测定晶体类型
D.X衍射图谱分析:利用X射线透过物质时记录的分立斑点或谱线来测定有机化合物中氢原子的种类和数目
3.化学与生产、生活密切相关。下列说法错误的是
A.用红外光谱实验确定青蒿素分子中的官能团
B.水库的钢闸门与电源正极连接可实现电化学保护
C.智能手机常用的锂离子电池属于二次电池
D.以铁粉为主要成分制成双吸剂放入食品包装袋,可以延长食物的保质期
4.德国卡尔 肖莱马是有机化学的奠基人和杰出的有机化学理论家.他的主要贡献是对脂肪烃的系统研究并解决了烷烃的异构理论.根据下表中烃的分子式排列规律,判断空格中烃的同分异构体数目是( )
1 2 3 4 5 6 7 8
CH4 C2H4 C3H8 C4H8 C6H12 C7H16 C8H16
A.3 B.4 C.5 D.6
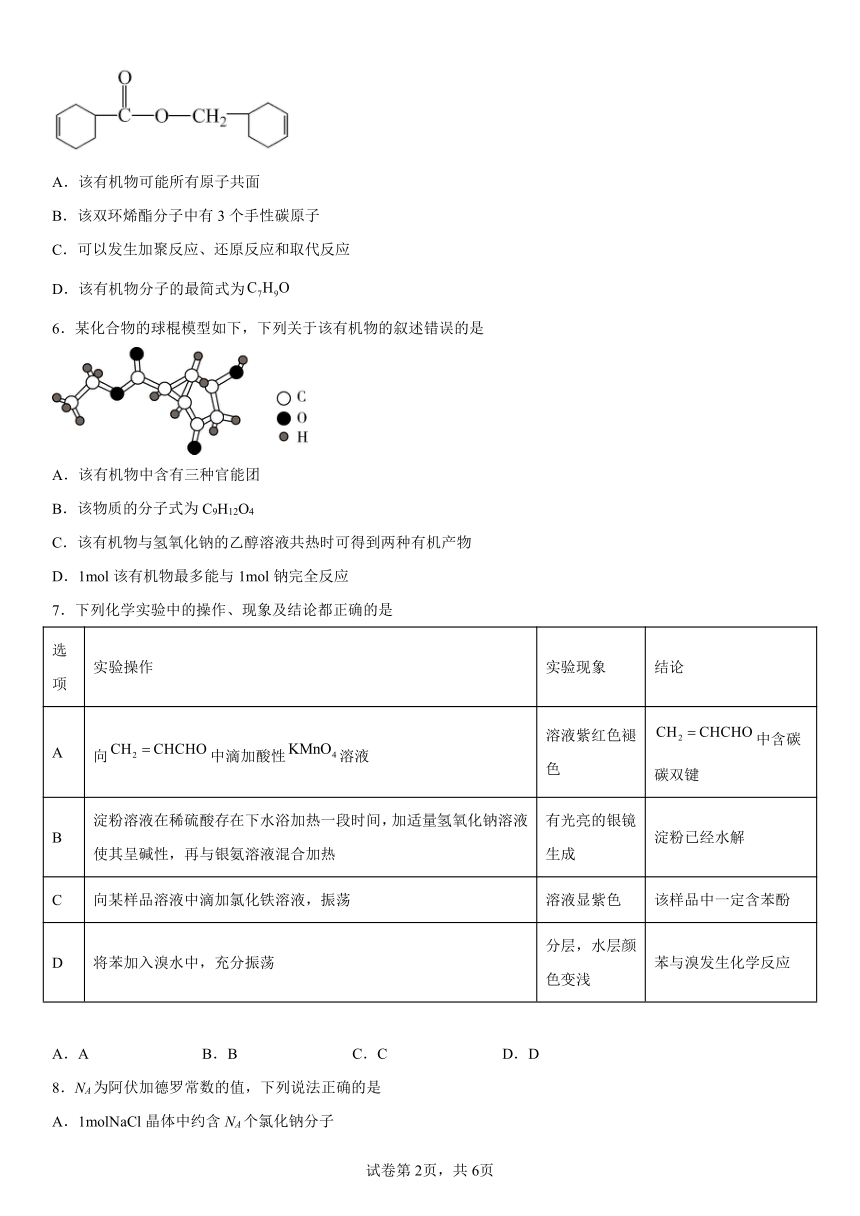
5.手性碳是指连接四个不同的原子或基团的碳原子。北京冬奥会在2022年2月举行,绿色环保是主要理念。在场馆建设中用到的一种耐腐、耐高温的表面涂料是以某双环烯酯为原料制得,该双环烯酯的结构如图所示。下列说法正确的是
A.该有机物可能所有原子共面
B.该双环烯酯分子中有3个手性碳原子
C.可以发生加聚反应、还原反应和取代反应
D.该有机物分子的最简式为
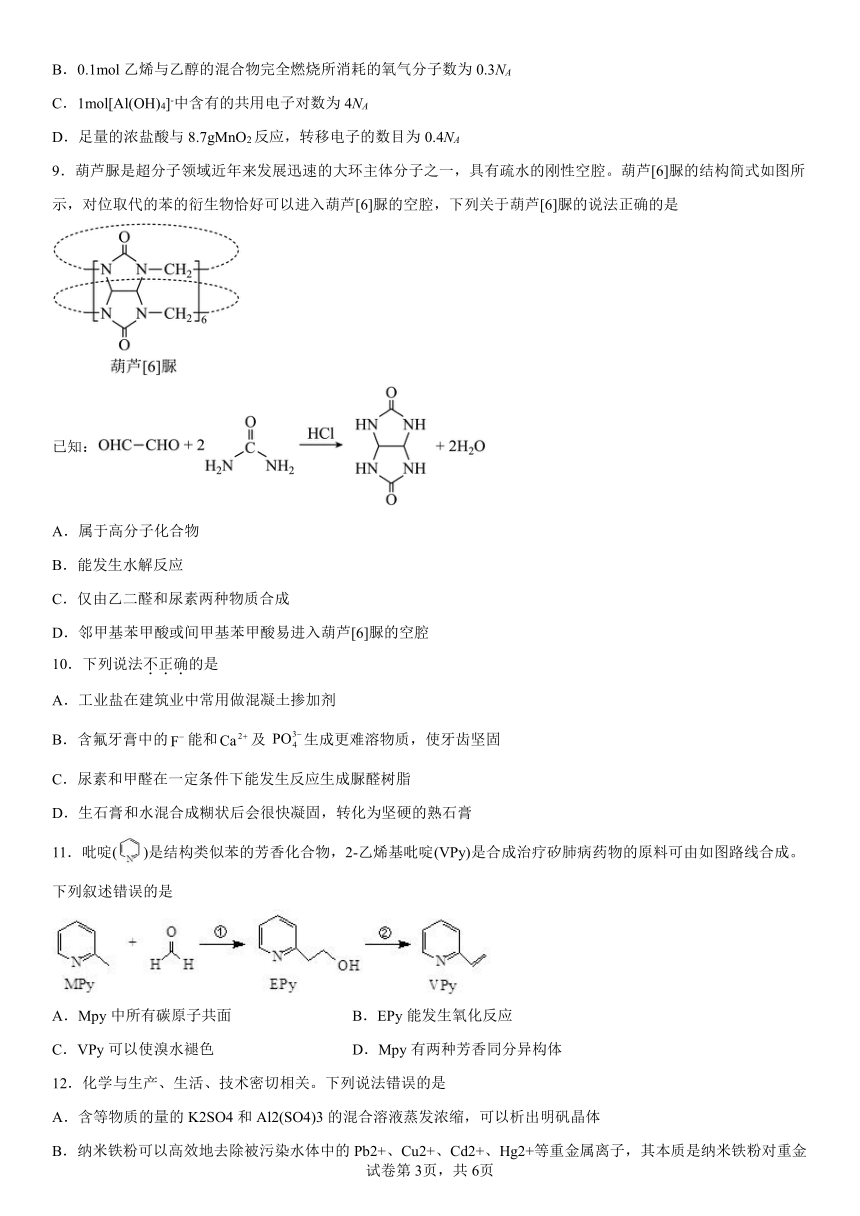
6.某化合物的球棍模型如下,下列关于该有机物的叙述错误的是
A.该有机物中含有三种官能团
B.该物质的分子式为C9H12O4
C.该有机物与氢氧化钠的乙醇溶液共热时可得到两种有机产物
D.1mol该有机物最多能与1mol钠完全反应
7.下列化学实验中的操作、现象及结论都正确的是
选项 实验操作 实验现象 结论
A 向中滴加酸性溶液 溶液紫红色褪色 中含碳碳双键
B 淀粉溶液在稀硫酸存在下水浴加热一段时间,加适量氢氧化钠溶液使其呈碱性,再与银氨溶液混合加热 有光亮的银镜生成 淀粉已经水解
C 向某样品溶液中滴加氯化铁溶液,振荡 溶液显紫色 该样品中一定含苯酚
D 将苯加入溴水中,充分振荡 分层,水层颜色变浅 苯与溴发生化学反应
A.A B.B C.C D.D
8.NA为阿伏加德罗常数的值,下列说法正确的是
A.1molNaCl晶体中约含NA个氯化钠分子
B.0.1mol乙烯与乙醇的混合物完全燃烧所消耗的氧气分子数为0.3NA
C.1mol[Al(OH)4]-中含有的共用电子对数为4NA
D.足量的浓盐酸与8.7gMnO2反应,转移电子的数目为0.4NA
9.葫芦脲是超分子领域近年来发展迅速的大环主体分子之一,具有疏水的刚性空腔。葫芦[6]脲的结构简式如图所示,对位取代的苯的衍生物恰好可以进入葫芦[6]脲的空腔,下列关于葫芦[6]脲的说法正确的是
已知:
A.属于高分子化合物
B.能发生水解反应
C.仅由乙二醛和尿素两种物质合成
D.邻甲基苯甲酸或间甲基苯甲酸易进入葫芦[6]脲的空腔
10.下列说法不正确的是
A.工业盐在建筑业中常用做混凝土掺加剂
B.含氟牙膏中的能和及生成更难溶物质,使牙齿坚固
C.尿素和甲醛在一定条件下能发生反应生成脲醛树脂
D.生石膏和水混合成糊状后会很快凝固,转化为坚硬的熟石膏
11.吡啶()是结构类似苯的芳香化合物,2-乙烯基吡啶(VPy)是合成治疗矽肺病药物的原料可由如图路线合成。下列叙述错误的是
A.Mpy中所有碳原子共面 B.EPy能发生氧化反应
C.VPy可以使溴水褪色 D.Mpy有两种芳香同分异构体
12.化学与生产、生活、技术密切相关。下列说法错误的是
A.含等物质的量的K2SO4和Al2(SO4)3的混合溶液蒸发浓缩,可以析出明矾晶体
B.纳米铁粉可以高效地去除被污染水体中的Pb2+、Cu2+、Cd2+、Hg2+等重金属离子,其本质是纳米铁粉对重金属离子较强的物理吸附
C.可在元素周期表过渡元素中寻找催化剂和耐高温、耐腐蚀的合金材料
D.涤纶、醇酸树脂、环氧树脂、酚醛树脂等高分子化合物都是缩聚反应制得的
二、填空题
13.(1)有下列几组物质,请将序号填入下列空格内:
A、CH2=CH-COOH和油酸(C17H33COOH) B、12C60和石墨
C、和
D、35Cl和37Cl E、乙醇和乙二醇
①互为同位素的是__________;
②互为同系物的是______________;
③互为同素异形体的是______;
④互为同分异构体的是__________;
(2)请写出下列反应的化学方程式:
①由丙烯制取聚丙烯:_____________________________________
②丙氨酸缩聚形成多肽:___________________________________
③淀粉水解:_____________________________________________
④丙醛与新制的氢氧化铜悬浊液反应:_______________________
14.高分子化合物I为重要的化工原料。其合成路线如下:
己如: ①:②R—Br R—CN R—COOH
参照上述合成路线,写出由1,3—丁二烯和乙烯为起始原料制备化合物的合成路线_______(无机试剂任选)。
15.根据下面五种有机物回答问题:
(1)其中属于苯的同系物的是____(填序号,下同);等质量的五种物质完全燃烧后消耗氧气最多的是______。
(2)①中所含官能团的名称为_____。
(3)④可由某烯烃与1个H2通过加成反应制得,则烯烃可能的结构有______种(不考虑立体异构)。
(4)⑤的同分异构体中,核磁共振氢谱只有一组峰的结构简式为_____。
16.碳化钙(CaC2)是重要的基本化工原料,工业上主要用于生产乙炔,进而用于生产其他有机物。以碳化钙为原料生产聚1,3-丁二烯()的合成路线如下图所示。回答下列问题:
(l)写出碳化钙生成乙炔的化学方程式:______________。
(2)A的结构简式为______________;①和②的反应类型分别为_______、_______。
(3)若聚1,3-丁二烯的平均相对分子质量为27000,则n=______________。
(4)三分子乙炔在一定条件下可聚合成环状分子,该分子的结构简式可表示为______________。
(5)以丙炔和溴苯为原料(无机试剂任选),设计制备正丙苯的合成路线:____________________________。
17.某烃A 0.2 mol 在氧气中完全燃烧后,生成CO2和H2O分别为2 mol、1.4 mol。试回答:
(1)烃A的分子式为___________。
(2)现有苯的同系物甲、乙、丙,分子式都与烃A相同 。
①甲不能被KMnO4的酸性溶液氧化成芳香酸,它的结构简式___________ ;
②乙能被KMnO4的酸性溶液氧化成芳香酸且分子结构中只含有一个烷基,则乙可能的结构有___________种;如乙能被KMnO4的酸性溶液氧化成C8H6O4 ,则乙可能的结构有___________种;
③丙的苯环上的一溴代物只有一种,则丙可能的结构有___________种。
18.近年来,乳酸[]成为人们的研究热点之一,乳酸可由淀粉为原料,通过生物发酵法制备。
请回答下列有关问题:
(1)淀粉遇到单质碘呈_______色。
(2)葡萄糖是自然界中分布最广的单糖,写出葡萄糖的结构简式_______。
(3)在一定条件下,下列物质能与葡萄糖发生反应的是_______。
A.乙醇 B.NaOH溶液 C.悬浊液 D.
(4)乳酸在一定条件下可发生多种反应。
①乳酸发生消去反应的产物可使的溶液褪色,写出乳酸发生消去反应的化学方程式_______。
②乳酸在一定条件下反应可生成六元环状化合物,写出该六元环状化合物的结构简式_______。
③乳酸在一定条件下反应可生成高分子聚合物(聚乳酸),写出该反应的化学方程式_______。
(5)1mol乳酸分别与足量的Na、NaOH、反应时,消耗三种物质的物质的量之比为_______。
19.某含苯环的烃A,其相对分子质量为104,碳的质量分数为。
(1)A的分子式为___________。
(2)A与溴的四氯化碳溶液反应的化学方程式为___________。
(3)已知:。请写出A与稀、冷的溶液在碱性条件下反应的化学方程式___________。
(4)一定条件下,A与氢气完全反应,写出此化合物的结构简式___________。
(5)在一定条件下,由A聚合得到的高分子化合物的结构简式为___________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
【详解】A. 该有机物中含有羧基、羟基、醚键三种官能团,A正确;
B.醚键、醇羟基与氢氧化钠不能反应,羧基可以与氢氧化钠反应,1 mol分枝酸最多可与2mol NaOH发生中和反应,B错误;
C.结构中含有羟基、羧基,在一定条件下可与乙醇、乙酸反应,发生酯化反应,应类型相同,C正确;
D.分支酸含有碳碳双键,与溴单质能发生加成反应,与酸性高锰酸钾溶液反应,属于氧化反应,反应原理不同,D错误;
故选C。
2.A
【详解】A.光谱分析:利用原子光谱上的特征谱线来鉴定元素,A项正确;
B.质谱分析:利用质荷比来测定有机物相对分子质量,B项错误;
C.红外光谱分析:利用有机化合物分子中不同基团的特征吸收频率不同来初步判断有机化合物中有哪些基团,C项错误;
D.X衍射图谱分析:利用X射线透过物质时记录的分立斑点或谱线来测定晶体类型和结构,D项错误;
答案选A。
3.B
【详解】A.用红外光谱实验确定青蒿素分子中的官能团,A正确;
B.水库的钢闸门与电源负极连接可实现电化学保护,为外加电源的阴极保护法,B错误;
C.锂离子电池是充电电池,属于二次电池,C正确;
D.铁粉具有还原性,能作抗氧化剂,可以延长食物的保质期,D正确;
故选B。
4.A
【详解】从1到8,物质的分子中C原子个数递增,因此物质5的分子中应含有5个碳原子;各物质的分子构成中H原子符合1与2、3与4、7与8的H原子个数相等,则可推断5与6的分子构成中H原子个数相等,即物质5的分子中含有12个H原子;综合以上分析,物质5的化学式为C5H12,同分异构体有正、异、新3种。
故选A。
5.C
【详解】A.有机物结构中碳环除去双键位置以外,其余位置都是烷基结构,都属于空间折线形结构,原子不共面,描述错误,不符题意;
B.结构中标识“1、2”的两个碳原子为手性碳原子,不是三个手性碳原子,描述错误,不符题意;
C.碳碳双键可以发生加聚反应、还原反应、酯基可以发生水解取代反应,描述正确,符合题意;
D.该有机物分子式应为C14H18O2,描述错误,不符题意;
综上,本题选C。
6.C
【分析】由球棍模型可得结构简式为;
【详解】A.该有机物中含有酯基、羟基、羰基共三种官能团,故A正确;
B.由球棍模型可知分子中含有9个C原子、12个H原子、4个O原子,则有机物的分子式C9H12O4,故B正确;
C.含有醇羟基,应在浓硫酸作用下发生消去反应,故C错误;
D.该有机物含有1个醇羟基,1mol该有机物最多能与1mol钠完全反应,故D正确;
故选:C。
7.B
【详解】A.醛基也能使酸性高锰酸钾溶液褪色,A错误;
B.淀粉在酸性条件下水解,得到的产物在碱性条件下与银氨溶液反应,B正确;
C.含酚羟基的物质均能使三氯化铁溶液显紫色,不一定是苯酚,C错误;
D.苯和溴水不反应,发生的是萃取,为物理变化,D错误;
故选B。
8.B
【详解】A.NaCl属于离子化合物,由Na+和Cl-构成,不含有氯化钠分子,A不正确;
B.乙醇的分子式可写成C2H4 H2O,与C2H4的耗氧量相同,1mol乙烯燃烧消耗氧气3mol,则0.1mol乙烯与乙醇的混合物完全燃烧所消耗的氧气分子数为0.3NA,B正确;
C.1个[Al(OH)4]-中含有7个共价键和1个配位键,所以1mol[Al(OH)4]-中含有的共用电子对数为8NA,C不正确;
D.MnO2与浓盐酸反应制氯气,存在如下关系式:MnO2—2e-,足量的浓盐酸与8.7gMnO2(0.1mol)反应,转移电子的数目为0.2NA,D不正确;
故选B。
9.B
【详解】A.由结构简式可知,葫芦[6]脲的相对分子质量小于一万,不属于高分子化合物,故A错误;
B.由结构简式可知,葫芦[6]脲分子中含有酰胺基,一定条件下可以发生水解反应,故B正确;
C.由结构简式可知,葫芦[6]脲由乙二醛、尿素和甲醛三种物质合成,故C错误;
D.由题给信息可知,对位取代的苯的衍生物恰好可以进入葫芦[6]脲的空腔,则邻甲基苯甲酸或间甲基苯甲酸不能进入葫芦[6]脲的空腔,故D错误;
故选B。
10.D
【详解】A.亚硝酸钠(NaNO3)俗称工业盐,在建筑工业中常用作混凝土掺加剂,以促进混凝土凝固,故A正确;
B.牙膏当中添加氟化物,其中的能与牙齿表层的羟基磷灰石[Ca5(PO4)3(OH)]发生反应生成溶解度更小的氟磷灰石[Ca5(PO4)3F],从而抵抗酸对牙齿的侵蚀,故B正确;
C.尿素()中与氮原子相连的氢原子可以像苯酚中苯环上的氢原子那样与甲醛发生反应,生成交联脲醛树脂,故C正确;
D.熟石膏与水混合成糊状后会很快凝固,转化为坚硬的生石膏,利用石膏的这一性质,医疗上可用来制作石膏绷带,故D错误。
故选D。
11.D
【详解】A.Mpy结构中碳碳双键交替存在,仅有一个甲基且与双键上的碳原子相连,故Mpy中所有碳原子共面,A项正确;
B.EPy的结构简式中含有碳碳双键和羟基,故能发生氧化反应,B项正确;
C.VPy的结构简式中含有碳碳双键,能和溴发生加成反应使溴水褪色,C项正确;
D.Mpy的分子式为C6H7N,同分异构体中含有苯环,则取代基只能是氨基,只有一种同分异构体,D项错误;
答案选D。
12.B
【详解】A.明矾的化学式为KAl(SO4)2·12H2O,K2SO4和Al2(SO4)3为等物质的量,因此蒸发浓缩后,可以析出明矾晶体,故A说法正确;
B.铁单质能与Cu2+、Pb2+、Hg2+等离子发生置换反应得到金属单质,治理污染,利用Fe的还原性,与吸附性无关,故B说法错误;
C.在元素周期表的过渡元素中寻找催化剂、耐高温、耐腐蚀的合金材料,如钒、钛、锰等,故C说法正确;
D.涤纶、尼龙、醇酸树脂、环氧树脂、酚醛树脂等均为人工合成高分子化合物,都是缩聚反应制得的,故D说法正确;
故选B。
13. D A B C CH3CH2CHO+NaOH+2Cu(OH)2Cu2O↓+CH3CH2COONa+3H2O
【详解】分析:(1)有相同质子数,不同中子数的原子或同一元素的不同核素互为同位素;结构相似、分子组成相差若干个“CH2”原子团的有机化合物互相称为同系物;相同元素组成,不同形态的单质互为同素异形体;具有相同分子式而结构不同的化合物互为同分异构体;
(2)①丙烯含有碳碳双键,可发生加聚反应生成聚丙烯;
②丙氨酸含有羧基和氨基,可发生缩聚反应;
③淀粉水解生成葡萄糖;
④丙醛与新制的氢氧化铜悬浊液在加热条件下发生反应生成丙酸钠、水和氧化亚铜。
详解:(1)A.CH2=CH-COOH和油酸(C17H33COOH)结构相似、分子组成相差15个“CH2”原子团,故互为同系物;
B.12C60和石墨都是由碳元素组成的不同单质,故互为同素异形体;
C.和分子式相同,但结构不同,故互为同分异构体;
D、35Cl和37Cl质子数相同,中子数不同,故互为同位素;
E、乙醇和乙二醇都属于醇类。则
①互为同位素的是35Cl和37Cl,答案为:D;
②互为同系物的是CH2=CH-COOH和油酸(C17H33COOH),答案为:A;
③互为同素异形体的是12C60和石墨,答案为:B;
④互为同分异构体的是和,答案为:C;
(2)①丙烯含有碳碳双键,可发生加聚反应生成聚丙烯,反应的方程式为;
②丙氨酸含有羧基和氨基,可发生缩聚反应,反应的方程式为;
③淀粉在酸性环境下水解的最终产物是葡萄糖,化学方程式为;
④丙醛与新制的氢氧化铜悬浊液在加热条件下发生反应生成丙酸钠、水和氧化亚铜,方程式为CH3CH2CHO+NaOH+2Cu(OH)2Cu2O↓+CH3CH2COONa+3H2O。
点睛:本题考查同位素、同素异形体、同分异构体、同系物的概念以及化学反应方程式书写,题目难度不大。对于同位素、同素异形体、同系物和同分异构体这四组概念,学习时应着重从其定义、对象、化学式、结构和性质等方面进行比较,抓住各自的不同点,注意从本质上理解和掌握。
14.
【详解】由已知①+=和②R-BrR-CNR-COOH可得,1,3-丁二烯与乙烯反应生成;与溴单质加成生成;与HCN取代生成;在酸性条件下水解生成;所以由1,3-丁二烯和乙烯为起始原料制备化合物的合成路线为:
故答案为:
15. ② ④ 酯基、羟基、醛基 3
【分析】(1)根据同系物的概念,结合苯同系物特点判断;质量相同时,物质分子中H元素含量越高,其完全燃烧消耗氧气就越多;
(2)根据物质分子结构,结合各种官能团的结构分析判断;
(3)根据烯烃加成反应特点,判断碳碳双键可能的位置,以确定其同分异构体种类数目;
(4)结合同分异构体的概念及H原子种类数目判断物质结构。
【详解】(1)由于同系物是结构相似,在分子组成上相差一个或若干个CH2原子团的物质,苯的同系物分子式通式是CnH2n-6,其同系物中应该含有苯环,支链为饱和烷基。在上述物质中是苯的同系物,故合理选项是②;
由于12 g C完全燃烧消耗1 mol O2;4 g H完全燃烧消耗1 mol O2;所以等质量的物质完全燃烧,物质中H元素的含量越高,完全燃烧消耗的氧气就越多。在上述五种物质中,④表示的烷烃达到结合H原子的最大数目,H元素含量最高,故其完全燃烧消耗氧气最大,故合理选项是④;
(2)①表示的物质中含氧官能团有-COO-、-OH、 -CHO,它们的名称分别是酯基、羟基、醛基;
(3)烯烃与H2发生加成反应时,断裂碳碳双键中较活泼的一个碳碳键,然后在这两个C原子上个结合1个H原子,形成烷烃,因此若是烯烃与氢气加成产物,则碳碳双键可能的位置为:。碳碳双键有几种不同位置,就存在几种同分异构体,因此其可能的同分异构体有三种;
(4)⑤表示的物质是 ,该物质是烯烃,分子式是C6H12,其同分异构体若核磁共振氢谱只有一组峰,说明分子中只有一种位置的H原子,则物质应该具有对称结构,其结构简式为。
【点睛】本题考查了物质的命名、同系物的判断、烯烃的加成规律、有机物燃烧消耗氧气与物质组成的关系及同分异构体的判断。掌握有关概念、物质的结构与反应特点是正确解答的关键。要从对称角度分析判断碳碳双键可能的位置,以确定其结构的不同,判断同分异构体种类数目。
16. CaC2+2H2O=Ca(OH)2+CH≡CH↑ CH3C≡CCH3 取代反应 消去反应 500
【分析】根据流程图,D为CH2=CH-CH=CH2,C为含有4个碳原子的卤代烃,则A、B均含有4个碳原子;因此NaC≡CNa与CH3Cl发生取代反应生成A,A为CH3C≡CCH3,A与氢气加成反应生成B,B能够与溴发生加成反应,则B为CH3CH=CHCH3,C为CH3CHBrCHBrCH3,C发生消去反应生成D(CH2=CH-CH=CH2)。
【详解】(l)碳化钙与水生成乙炔的化学方程式为CaC2+2H2O=Ca(OH)2+CH≡CH↑,故答案为CaC2+2H2O=Ca(OH)2+CH≡CH↑;
(2)根据上述分析,A为CH3C≡CCH3,反应①为NaC≡CNa与CH3Cl发生的取代反应,反应②为CH3CHBrCHBrCH3在氢氧化钠醇溶液中发生的消去反应,故答案为CH3C≡CCH3;取代反应;消去反应;
(3)若聚1,3-丁二烯的平均相对分子质量为27000,则n==500,故答案为500;
(4)三分子乙炔在一定条件下可聚合成环状分子,该分子的结构简式可表示为,故答案为;
(5)以丙炔和溴苯为原料合成正丙苯,正丙苯的结构简式为,根据题干流程图的提示,需要合成CH3C≡CNa,CH3C≡CNa与溴苯发生取代反应即可得到,与足量氢气加成即可,因此合成路线为,故答案为。
【点睛】本题考查了有机合成与推断,难度中等。解答本题的关键是根据流程图,采用逆向思维的方法分析判断各物质的结构简式。本题的易错点(5),要注意充分利用题干流程图的信息进行思考。
17. 3 9 3
【分析】设烃A的分子式为,0.2molA完全燃烧生成和分别为2mol、1.4mol,则个;个,即A的分子式为。
【详解】(1)烃A的分子式为,故填;
(2)根据题意甲、乙、丙均为A的同分异构体;
①甲不能被酸性高锰酸钾氧化,所以其与苯环相连的C原子上无H,其结构为,故填;
②若乙中只有一个烷基,则苯环上的取代基只有一个,且能被高锰酸钾氧化,其结构有、、,共计3种;如乙被氧化成,说明苯环上有两个取代基,且与苯环相连的C原子上有H原子,其结构有、、、、、、、、,共9种,故填3、9;
③丙的苯环上的一溴代物只有1种,说明苯环上的取代基处于对称位置,其结构有、、共3种,故填3。
18.(1)蓝
(2)CH2OH(CHOH)4CHO
(3)ACD
(4) CH2=CHCOOH+H2O n+(n-1)H2O
(5)2:1:1
【解析】(1)
淀粉遇到碘单质,淀粉呈蓝色;
(2)
葡萄糖为多羟基醛,其结构简式为CH2OH(CHOH)4CHO;
(3)
A.葡萄糖含羟基,一定条件下能与乙醇反应生成醚类物质,A正确;
B.葡萄糖与NaOH不反应,B不正确;
C.葡萄糖中含有醛基,可与Cu(OH)2发生氧化反应,C正确;
D.葡萄糖中含有羟基,可与CH3COOH发生酯化反应,D正确;
答案选ACD;
(4)
①乳酸中含有羟基,且与羟基相连的碳的邻位碳上有H,能发生醇的消去反应,则乳酸发生消去反应的方程式为CH2=CHCOOH+H2O;
②2个乳酸发生酯化反应可生成六元环状化合物,则结构简式为;
③乳酸中含有羟基、羧基,多个分子间发生缩聚反应可生成高分子化合物聚乳酸,反应的方程式为n+(n-1)H2O;
(5)
乳酸中含有羟基、羧基,羟基、羧基均能和钠反应,1mol乳酸消耗2molNa;只有羧基能与氢氧化钠反应,1mol乳酸消耗1molNaOH;只有羧基能与碳酸氢钠反应,1mol乳酸消耗1molNaHCO3;故1mol乳酸消耗三者物质的量之比为2:1:1。
19.
【分析】某含苯环的烃A,其相对分子质量为104,碳的质量分数为,则该分子中C原子的个数为=8,则H原子个数为=8,所以A的分子式为,结合问题中A可以发生的反应,可知A的结构简式为:。
【详解】(1)由上述分析可知,A的分子式为:,故填;
(2)A与溴的四氯化碳溶液发生加成反应,反应的化学方程式为,故填 ;
(3)由可知, 与稀、冷的溶液在碱性条件下反应的化学方程式为:,
故填;
(4)一定条件下, 与氢气完全反应,苯环与碳碳双键均与氢气发生加成反应,生成的化合物的结构简式为 ,故填 ;
含有碳碳双键,可发生加聚反应生成聚苯乙烯,高分子化合物结构简式为 ,故填 。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.分枝酸可用于生化研究,其结构简式为,下列关于分枝酸的说法正确的是
A.分子中含有3种官能团
B.1 mol分枝酸最多可与3mol NaOH发生中和反应
C.在一定条件下可与乙醇、乙酸反应,且反应类型相同
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且褪色原理相同
2.化学分析的手段通常有定性分析、定量分析、仪器分析等,现代化学中仪器分析是研究物质结构的基本方法和实验手段。下列仪器分析手段的运用科学可行的是
A.光谱分析:利用原子光谱上的特征谱线来鉴定元素
B.质谱分析:利用质荷比来测定分子立体结构
C.红外光谱分析:利用分子吸收与化学键振动频率相同的红外线来测定晶体类型
D.X衍射图谱分析:利用X射线透过物质时记录的分立斑点或谱线来测定有机化合物中氢原子的种类和数目
3.化学与生产、生活密切相关。下列说法错误的是
A.用红外光谱实验确定青蒿素分子中的官能团
B.水库的钢闸门与电源正极连接可实现电化学保护
C.智能手机常用的锂离子电池属于二次电池
D.以铁粉为主要成分制成双吸剂放入食品包装袋,可以延长食物的保质期
4.德国卡尔 肖莱马是有机化学的奠基人和杰出的有机化学理论家.他的主要贡献是对脂肪烃的系统研究并解决了烷烃的异构理论.根据下表中烃的分子式排列规律,判断空格中烃的同分异构体数目是( )
1 2 3 4 5 6 7 8
CH4 C2H4 C3H8 C4H8 C6H12 C7H16 C8H16
A.3 B.4 C.5 D.6
5.手性碳是指连接四个不同的原子或基团的碳原子。北京冬奥会在2022年2月举行,绿色环保是主要理念。在场馆建设中用到的一种耐腐、耐高温的表面涂料是以某双环烯酯为原料制得,该双环烯酯的结构如图所示。下列说法正确的是
A.该有机物可能所有原子共面
B.该双环烯酯分子中有3个手性碳原子
C.可以发生加聚反应、还原反应和取代反应
D.该有机物分子的最简式为
6.某化合物的球棍模型如下,下列关于该有机物的叙述错误的是
A.该有机物中含有三种官能团
B.该物质的分子式为C9H12O4
C.该有机物与氢氧化钠的乙醇溶液共热时可得到两种有机产物
D.1mol该有机物最多能与1mol钠完全反应
7.下列化学实验中的操作、现象及结论都正确的是
选项 实验操作 实验现象 结论
A 向中滴加酸性溶液 溶液紫红色褪色 中含碳碳双键
B 淀粉溶液在稀硫酸存在下水浴加热一段时间,加适量氢氧化钠溶液使其呈碱性,再与银氨溶液混合加热 有光亮的银镜生成 淀粉已经水解
C 向某样品溶液中滴加氯化铁溶液,振荡 溶液显紫色 该样品中一定含苯酚
D 将苯加入溴水中,充分振荡 分层,水层颜色变浅 苯与溴发生化学反应
A.A B.B C.C D.D
8.NA为阿伏加德罗常数的值,下列说法正确的是
A.1molNaCl晶体中约含NA个氯化钠分子
B.0.1mol乙烯与乙醇的混合物完全燃烧所消耗的氧气分子数为0.3NA
C.1mol[Al(OH)4]-中含有的共用电子对数为4NA
D.足量的浓盐酸与8.7gMnO2反应,转移电子的数目为0.4NA
9.葫芦脲是超分子领域近年来发展迅速的大环主体分子之一,具有疏水的刚性空腔。葫芦[6]脲的结构简式如图所示,对位取代的苯的衍生物恰好可以进入葫芦[6]脲的空腔,下列关于葫芦[6]脲的说法正确的是
已知:
A.属于高分子化合物
B.能发生水解反应
C.仅由乙二醛和尿素两种物质合成
D.邻甲基苯甲酸或间甲基苯甲酸易进入葫芦[6]脲的空腔
10.下列说法不正确的是
A.工业盐在建筑业中常用做混凝土掺加剂
B.含氟牙膏中的能和及生成更难溶物质,使牙齿坚固
C.尿素和甲醛在一定条件下能发生反应生成脲醛树脂
D.生石膏和水混合成糊状后会很快凝固,转化为坚硬的熟石膏
11.吡啶()是结构类似苯的芳香化合物,2-乙烯基吡啶(VPy)是合成治疗矽肺病药物的原料可由如图路线合成。下列叙述错误的是
A.Mpy中所有碳原子共面 B.EPy能发生氧化反应
C.VPy可以使溴水褪色 D.Mpy有两种芳香同分异构体
12.化学与生产、生活、技术密切相关。下列说法错误的是
A.含等物质的量的K2SO4和Al2(SO4)3的混合溶液蒸发浓缩,可以析出明矾晶体
B.纳米铁粉可以高效地去除被污染水体中的Pb2+、Cu2+、Cd2+、Hg2+等重金属离子,其本质是纳米铁粉对重金属离子较强的物理吸附
C.可在元素周期表过渡元素中寻找催化剂和耐高温、耐腐蚀的合金材料
D.涤纶、醇酸树脂、环氧树脂、酚醛树脂等高分子化合物都是缩聚反应制得的
二、填空题
13.(1)有下列几组物质,请将序号填入下列空格内:
A、CH2=CH-COOH和油酸(C17H33COOH) B、12C60和石墨
C、和
D、35Cl和37Cl E、乙醇和乙二醇
①互为同位素的是__________;
②互为同系物的是______________;
③互为同素异形体的是______;
④互为同分异构体的是__________;
(2)请写出下列反应的化学方程式:
①由丙烯制取聚丙烯:_____________________________________
②丙氨酸缩聚形成多肽:___________________________________
③淀粉水解:_____________________________________________
④丙醛与新制的氢氧化铜悬浊液反应:_______________________
14.高分子化合物I为重要的化工原料。其合成路线如下:
己如: ①:②R—Br R—CN R—COOH
参照上述合成路线,写出由1,3—丁二烯和乙烯为起始原料制备化合物的合成路线_______(无机试剂任选)。
15.根据下面五种有机物回答问题:
(1)其中属于苯的同系物的是____(填序号,下同);等质量的五种物质完全燃烧后消耗氧气最多的是______。
(2)①中所含官能团的名称为_____。
(3)④可由某烯烃与1个H2通过加成反应制得,则烯烃可能的结构有______种(不考虑立体异构)。
(4)⑤的同分异构体中,核磁共振氢谱只有一组峰的结构简式为_____。
16.碳化钙(CaC2)是重要的基本化工原料,工业上主要用于生产乙炔,进而用于生产其他有机物。以碳化钙为原料生产聚1,3-丁二烯()的合成路线如下图所示。回答下列问题:
(l)写出碳化钙生成乙炔的化学方程式:______________。
(2)A的结构简式为______________;①和②的反应类型分别为_______、_______。
(3)若聚1,3-丁二烯的平均相对分子质量为27000,则n=______________。
(4)三分子乙炔在一定条件下可聚合成环状分子,该分子的结构简式可表示为______________。
(5)以丙炔和溴苯为原料(无机试剂任选),设计制备正丙苯的合成路线:____________________________。
17.某烃A 0.2 mol 在氧气中完全燃烧后,生成CO2和H2O分别为2 mol、1.4 mol。试回答:
(1)烃A的分子式为___________。
(2)现有苯的同系物甲、乙、丙,分子式都与烃A相同 。
①甲不能被KMnO4的酸性溶液氧化成芳香酸,它的结构简式___________ ;
②乙能被KMnO4的酸性溶液氧化成芳香酸且分子结构中只含有一个烷基,则乙可能的结构有___________种;如乙能被KMnO4的酸性溶液氧化成C8H6O4 ,则乙可能的结构有___________种;
③丙的苯环上的一溴代物只有一种,则丙可能的结构有___________种。
18.近年来,乳酸[]成为人们的研究热点之一,乳酸可由淀粉为原料,通过生物发酵法制备。
请回答下列有关问题:
(1)淀粉遇到单质碘呈_______色。
(2)葡萄糖是自然界中分布最广的单糖,写出葡萄糖的结构简式_______。
(3)在一定条件下,下列物质能与葡萄糖发生反应的是_______。
A.乙醇 B.NaOH溶液 C.悬浊液 D.
(4)乳酸在一定条件下可发生多种反应。
①乳酸发生消去反应的产物可使的溶液褪色,写出乳酸发生消去反应的化学方程式_______。
②乳酸在一定条件下反应可生成六元环状化合物,写出该六元环状化合物的结构简式_______。
③乳酸在一定条件下反应可生成高分子聚合物(聚乳酸),写出该反应的化学方程式_______。
(5)1mol乳酸分别与足量的Na、NaOH、反应时,消耗三种物质的物质的量之比为_______。
19.某含苯环的烃A,其相对分子质量为104,碳的质量分数为。
(1)A的分子式为___________。
(2)A与溴的四氯化碳溶液反应的化学方程式为___________。
(3)已知:。请写出A与稀、冷的溶液在碱性条件下反应的化学方程式___________。
(4)一定条件下,A与氢气完全反应,写出此化合物的结构简式___________。
(5)在一定条件下,由A聚合得到的高分子化合物的结构简式为___________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
【详解】A. 该有机物中含有羧基、羟基、醚键三种官能团,A正确;
B.醚键、醇羟基与氢氧化钠不能反应,羧基可以与氢氧化钠反应,1 mol分枝酸最多可与2mol NaOH发生中和反应,B错误;
C.结构中含有羟基、羧基,在一定条件下可与乙醇、乙酸反应,发生酯化反应,应类型相同,C正确;
D.分支酸含有碳碳双键,与溴单质能发生加成反应,与酸性高锰酸钾溶液反应,属于氧化反应,反应原理不同,D错误;
故选C。
2.A
【详解】A.光谱分析:利用原子光谱上的特征谱线来鉴定元素,A项正确;
B.质谱分析:利用质荷比来测定有机物相对分子质量,B项错误;
C.红外光谱分析:利用有机化合物分子中不同基团的特征吸收频率不同来初步判断有机化合物中有哪些基团,C项错误;
D.X衍射图谱分析:利用X射线透过物质时记录的分立斑点或谱线来测定晶体类型和结构,D项错误;
答案选A。
3.B
【详解】A.用红外光谱实验确定青蒿素分子中的官能团,A正确;
B.水库的钢闸门与电源负极连接可实现电化学保护,为外加电源的阴极保护法,B错误;
C.锂离子电池是充电电池,属于二次电池,C正确;
D.铁粉具有还原性,能作抗氧化剂,可以延长食物的保质期,D正确;
故选B。
4.A
【详解】从1到8,物质的分子中C原子个数递增,因此物质5的分子中应含有5个碳原子;各物质的分子构成中H原子符合1与2、3与4、7与8的H原子个数相等,则可推断5与6的分子构成中H原子个数相等,即物质5的分子中含有12个H原子;综合以上分析,物质5的化学式为C5H12,同分异构体有正、异、新3种。
故选A。
5.C
【详解】A.有机物结构中碳环除去双键位置以外,其余位置都是烷基结构,都属于空间折线形结构,原子不共面,描述错误,不符题意;
B.结构中标识“1、2”的两个碳原子为手性碳原子,不是三个手性碳原子,描述错误,不符题意;
C.碳碳双键可以发生加聚反应、还原反应、酯基可以发生水解取代反应,描述正确,符合题意;
D.该有机物分子式应为C14H18O2,描述错误,不符题意;
综上,本题选C。
6.C
【分析】由球棍模型可得结构简式为;
【详解】A.该有机物中含有酯基、羟基、羰基共三种官能团,故A正确;
B.由球棍模型可知分子中含有9个C原子、12个H原子、4个O原子,则有机物的分子式C9H12O4,故B正确;
C.含有醇羟基,应在浓硫酸作用下发生消去反应,故C错误;
D.该有机物含有1个醇羟基,1mol该有机物最多能与1mol钠完全反应,故D正确;
故选:C。
7.B
【详解】A.醛基也能使酸性高锰酸钾溶液褪色,A错误;
B.淀粉在酸性条件下水解,得到的产物在碱性条件下与银氨溶液反应,B正确;
C.含酚羟基的物质均能使三氯化铁溶液显紫色,不一定是苯酚,C错误;
D.苯和溴水不反应,发生的是萃取,为物理变化,D错误;
故选B。
8.B
【详解】A.NaCl属于离子化合物,由Na+和Cl-构成,不含有氯化钠分子,A不正确;
B.乙醇的分子式可写成C2H4 H2O,与C2H4的耗氧量相同,1mol乙烯燃烧消耗氧气3mol,则0.1mol乙烯与乙醇的混合物完全燃烧所消耗的氧气分子数为0.3NA,B正确;
C.1个[Al(OH)4]-中含有7个共价键和1个配位键,所以1mol[Al(OH)4]-中含有的共用电子对数为8NA,C不正确;
D.MnO2与浓盐酸反应制氯气,存在如下关系式:MnO2—2e-,足量的浓盐酸与8.7gMnO2(0.1mol)反应,转移电子的数目为0.2NA,D不正确;
故选B。
9.B
【详解】A.由结构简式可知,葫芦[6]脲的相对分子质量小于一万,不属于高分子化合物,故A错误;
B.由结构简式可知,葫芦[6]脲分子中含有酰胺基,一定条件下可以发生水解反应,故B正确;
C.由结构简式可知,葫芦[6]脲由乙二醛、尿素和甲醛三种物质合成,故C错误;
D.由题给信息可知,对位取代的苯的衍生物恰好可以进入葫芦[6]脲的空腔,则邻甲基苯甲酸或间甲基苯甲酸不能进入葫芦[6]脲的空腔,故D错误;
故选B。
10.D
【详解】A.亚硝酸钠(NaNO3)俗称工业盐,在建筑工业中常用作混凝土掺加剂,以促进混凝土凝固,故A正确;
B.牙膏当中添加氟化物,其中的能与牙齿表层的羟基磷灰石[Ca5(PO4)3(OH)]发生反应生成溶解度更小的氟磷灰石[Ca5(PO4)3F],从而抵抗酸对牙齿的侵蚀,故B正确;
C.尿素()中与氮原子相连的氢原子可以像苯酚中苯环上的氢原子那样与甲醛发生反应,生成交联脲醛树脂,故C正确;
D.熟石膏与水混合成糊状后会很快凝固,转化为坚硬的生石膏,利用石膏的这一性质,医疗上可用来制作石膏绷带,故D错误。
故选D。
11.D
【详解】A.Mpy结构中碳碳双键交替存在,仅有一个甲基且与双键上的碳原子相连,故Mpy中所有碳原子共面,A项正确;
B.EPy的结构简式中含有碳碳双键和羟基,故能发生氧化反应,B项正确;
C.VPy的结构简式中含有碳碳双键,能和溴发生加成反应使溴水褪色,C项正确;
D.Mpy的分子式为C6H7N,同分异构体中含有苯环,则取代基只能是氨基,只有一种同分异构体,D项错误;
答案选D。
12.B
【详解】A.明矾的化学式为KAl(SO4)2·12H2O,K2SO4和Al2(SO4)3为等物质的量,因此蒸发浓缩后,可以析出明矾晶体,故A说法正确;
B.铁单质能与Cu2+、Pb2+、Hg2+等离子发生置换反应得到金属单质,治理污染,利用Fe的还原性,与吸附性无关,故B说法错误;
C.在元素周期表的过渡元素中寻找催化剂、耐高温、耐腐蚀的合金材料,如钒、钛、锰等,故C说法正确;
D.涤纶、尼龙、醇酸树脂、环氧树脂、酚醛树脂等均为人工合成高分子化合物,都是缩聚反应制得的,故D说法正确;
故选B。
13. D A B C CH3CH2CHO+NaOH+2Cu(OH)2Cu2O↓+CH3CH2COONa+3H2O
【详解】分析:(1)有相同质子数,不同中子数的原子或同一元素的不同核素互为同位素;结构相似、分子组成相差若干个“CH2”原子团的有机化合物互相称为同系物;相同元素组成,不同形态的单质互为同素异形体;具有相同分子式而结构不同的化合物互为同分异构体;
(2)①丙烯含有碳碳双键,可发生加聚反应生成聚丙烯;
②丙氨酸含有羧基和氨基,可发生缩聚反应;
③淀粉水解生成葡萄糖;
④丙醛与新制的氢氧化铜悬浊液在加热条件下发生反应生成丙酸钠、水和氧化亚铜。
详解:(1)A.CH2=CH-COOH和油酸(C17H33COOH)结构相似、分子组成相差15个“CH2”原子团,故互为同系物;
B.12C60和石墨都是由碳元素组成的不同单质,故互为同素异形体;
C.和分子式相同,但结构不同,故互为同分异构体;
D、35Cl和37Cl质子数相同,中子数不同,故互为同位素;
E、乙醇和乙二醇都属于醇类。则
①互为同位素的是35Cl和37Cl,答案为:D;
②互为同系物的是CH2=CH-COOH和油酸(C17H33COOH),答案为:A;
③互为同素异形体的是12C60和石墨,答案为:B;
④互为同分异构体的是和,答案为:C;
(2)①丙烯含有碳碳双键,可发生加聚反应生成聚丙烯,反应的方程式为;
②丙氨酸含有羧基和氨基,可发生缩聚反应,反应的方程式为;
③淀粉在酸性环境下水解的最终产物是葡萄糖,化学方程式为;
④丙醛与新制的氢氧化铜悬浊液在加热条件下发生反应生成丙酸钠、水和氧化亚铜,方程式为CH3CH2CHO+NaOH+2Cu(OH)2Cu2O↓+CH3CH2COONa+3H2O。
点睛:本题考查同位素、同素异形体、同分异构体、同系物的概念以及化学反应方程式书写,题目难度不大。对于同位素、同素异形体、同系物和同分异构体这四组概念,学习时应着重从其定义、对象、化学式、结构和性质等方面进行比较,抓住各自的不同点,注意从本质上理解和掌握。
14.
【详解】由已知①+=和②R-BrR-CNR-COOH可得,1,3-丁二烯与乙烯反应生成;与溴单质加成生成;与HCN取代生成;在酸性条件下水解生成;所以由1,3-丁二烯和乙烯为起始原料制备化合物的合成路线为:
故答案为:
15. ② ④ 酯基、羟基、醛基 3
【分析】(1)根据同系物的概念,结合苯同系物特点判断;质量相同时,物质分子中H元素含量越高,其完全燃烧消耗氧气就越多;
(2)根据物质分子结构,结合各种官能团的结构分析判断;
(3)根据烯烃加成反应特点,判断碳碳双键可能的位置,以确定其同分异构体种类数目;
(4)结合同分异构体的概念及H原子种类数目判断物质结构。
【详解】(1)由于同系物是结构相似,在分子组成上相差一个或若干个CH2原子团的物质,苯的同系物分子式通式是CnH2n-6,其同系物中应该含有苯环,支链为饱和烷基。在上述物质中是苯的同系物,故合理选项是②;
由于12 g C完全燃烧消耗1 mol O2;4 g H完全燃烧消耗1 mol O2;所以等质量的物质完全燃烧,物质中H元素的含量越高,完全燃烧消耗的氧气就越多。在上述五种物质中,④表示的烷烃达到结合H原子的最大数目,H元素含量最高,故其完全燃烧消耗氧气最大,故合理选项是④;
(2)①表示的物质中含氧官能团有-COO-、-OH、 -CHO,它们的名称分别是酯基、羟基、醛基;
(3)烯烃与H2发生加成反应时,断裂碳碳双键中较活泼的一个碳碳键,然后在这两个C原子上个结合1个H原子,形成烷烃,因此若是烯烃与氢气加成产物,则碳碳双键可能的位置为:。碳碳双键有几种不同位置,就存在几种同分异构体,因此其可能的同分异构体有三种;
(4)⑤表示的物质是 ,该物质是烯烃,分子式是C6H12,其同分异构体若核磁共振氢谱只有一组峰,说明分子中只有一种位置的H原子,则物质应该具有对称结构,其结构简式为。
【点睛】本题考查了物质的命名、同系物的判断、烯烃的加成规律、有机物燃烧消耗氧气与物质组成的关系及同分异构体的判断。掌握有关概念、物质的结构与反应特点是正确解答的关键。要从对称角度分析判断碳碳双键可能的位置,以确定其结构的不同,判断同分异构体种类数目。
16. CaC2+2H2O=Ca(OH)2+CH≡CH↑ CH3C≡CCH3 取代反应 消去反应 500
【分析】根据流程图,D为CH2=CH-CH=CH2,C为含有4个碳原子的卤代烃,则A、B均含有4个碳原子;因此NaC≡CNa与CH3Cl发生取代反应生成A,A为CH3C≡CCH3,A与氢气加成反应生成B,B能够与溴发生加成反应,则B为CH3CH=CHCH3,C为CH3CHBrCHBrCH3,C发生消去反应生成D(CH2=CH-CH=CH2)。
【详解】(l)碳化钙与水生成乙炔的化学方程式为CaC2+2H2O=Ca(OH)2+CH≡CH↑,故答案为CaC2+2H2O=Ca(OH)2+CH≡CH↑;
(2)根据上述分析,A为CH3C≡CCH3,反应①为NaC≡CNa与CH3Cl发生的取代反应,反应②为CH3CHBrCHBrCH3在氢氧化钠醇溶液中发生的消去反应,故答案为CH3C≡CCH3;取代反应;消去反应;
(3)若聚1,3-丁二烯的平均相对分子质量为27000,则n==500,故答案为500;
(4)三分子乙炔在一定条件下可聚合成环状分子,该分子的结构简式可表示为,故答案为;
(5)以丙炔和溴苯为原料合成正丙苯,正丙苯的结构简式为,根据题干流程图的提示,需要合成CH3C≡CNa,CH3C≡CNa与溴苯发生取代反应即可得到,与足量氢气加成即可,因此合成路线为,故答案为。
【点睛】本题考查了有机合成与推断,难度中等。解答本题的关键是根据流程图,采用逆向思维的方法分析判断各物质的结构简式。本题的易错点(5),要注意充分利用题干流程图的信息进行思考。
17. 3 9 3
【分析】设烃A的分子式为,0.2molA完全燃烧生成和分别为2mol、1.4mol,则个;个,即A的分子式为。
【详解】(1)烃A的分子式为,故填;
(2)根据题意甲、乙、丙均为A的同分异构体;
①甲不能被酸性高锰酸钾氧化,所以其与苯环相连的C原子上无H,其结构为,故填;
②若乙中只有一个烷基,则苯环上的取代基只有一个,且能被高锰酸钾氧化,其结构有、、,共计3种;如乙被氧化成,说明苯环上有两个取代基,且与苯环相连的C原子上有H原子,其结构有、、、、、、、、,共9种,故填3、9;
③丙的苯环上的一溴代物只有1种,说明苯环上的取代基处于对称位置,其结构有、、共3种,故填3。
18.(1)蓝
(2)CH2OH(CHOH)4CHO
(3)ACD
(4) CH2=CHCOOH+H2O n+(n-1)H2O
(5)2:1:1
【解析】(1)
淀粉遇到碘单质,淀粉呈蓝色;
(2)
葡萄糖为多羟基醛,其结构简式为CH2OH(CHOH)4CHO;
(3)
A.葡萄糖含羟基,一定条件下能与乙醇反应生成醚类物质,A正确;
B.葡萄糖与NaOH不反应,B不正确;
C.葡萄糖中含有醛基,可与Cu(OH)2发生氧化反应,C正确;
D.葡萄糖中含有羟基,可与CH3COOH发生酯化反应,D正确;
答案选ACD;
(4)
①乳酸中含有羟基,且与羟基相连的碳的邻位碳上有H,能发生醇的消去反应,则乳酸发生消去反应的方程式为CH2=CHCOOH+H2O;
②2个乳酸发生酯化反应可生成六元环状化合物,则结构简式为;
③乳酸中含有羟基、羧基,多个分子间发生缩聚反应可生成高分子化合物聚乳酸,反应的方程式为n+(n-1)H2O;
(5)
乳酸中含有羟基、羧基,羟基、羧基均能和钠反应,1mol乳酸消耗2molNa;只有羧基能与氢氧化钠反应,1mol乳酸消耗1molNaOH;只有羧基能与碳酸氢钠反应,1mol乳酸消耗1molNaHCO3;故1mol乳酸消耗三者物质的量之比为2:1:1。
19.
【分析】某含苯环的烃A,其相对分子质量为104,碳的质量分数为,则该分子中C原子的个数为=8,则H原子个数为=8,所以A的分子式为,结合问题中A可以发生的反应,可知A的结构简式为:。
【详解】(1)由上述分析可知,A的分子式为:,故填;
(2)A与溴的四氯化碳溶液发生加成反应,反应的化学方程式为,故填 ;
(3)由可知, 与稀、冷的溶液在碱性条件下反应的化学方程式为:,
故填;
(4)一定条件下, 与氢气完全反应,苯环与碳碳双键均与氢气发生加成反应,生成的化合物的结构简式为 ,故填 ;
含有碳碳双键,可发生加聚反应生成聚苯乙烯,高分子化合物结构简式为 ,故填 。
答案第1页,共2页
答案第1页,共2页
