2.1.1烷烃的结构和性质 课件(共26张PPT) 高二下学期化学人教版(2019)选择性必修3
文档属性
| 名称 | 2.1.1烷烃的结构和性质 课件(共26张PPT) 高二下学期化学人教版(2019)选择性必修3 |  | |
| 格式 | pptx | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-16 11:10:43 | ||
图片预览





文档简介
(共26张PPT)
第二章 烃
第一节 烷烃
第1课时 烷烃的结构和性质
【教学目标】:
1.了解烷烃的物理性质
2.掌握烷烃的结构特点和主要化学性质
【教学重点难点】:
1.烷烃的结构特点和主要化学性质;
2.烷烃同分异构体的书写
天然气
液化石油气
汽油、柴油
凡士林
石蜡
生活中常见的烷烃
1.烷烃的存在
主要成分都是烷烃。
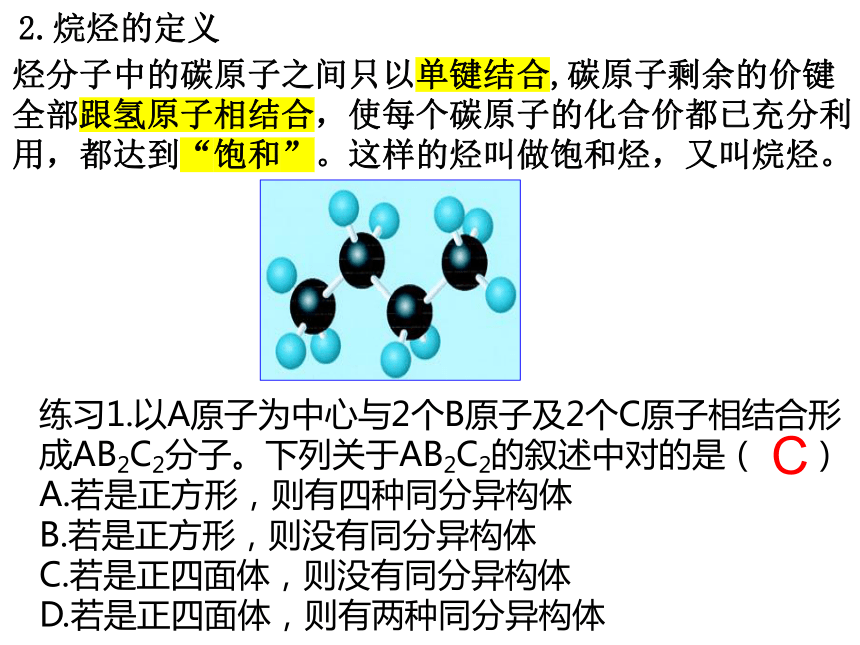
烃分子中的碳原子之间只以单键结合,碳原子剩余的价键全部跟氢原子相结合,使每个碳原子的化合价都已充分利用,都达到“饱和”。这样的烃叫做饱和烃,又叫烷烃。
2.烷烃的定义
练习1.以A原子为中心与2个B原子及2个C原子相结合形成AB2C2分子。下列关于AB2C2的叙述中对的是( )
A.若是正方形,则有四种同分异构体
B.若是正方形,则没有同分异构体
C.若是正四面体,则没有同分异构体
D.若是正四面体,则有两种同分异构体
C
一、烷烃的结构和性质
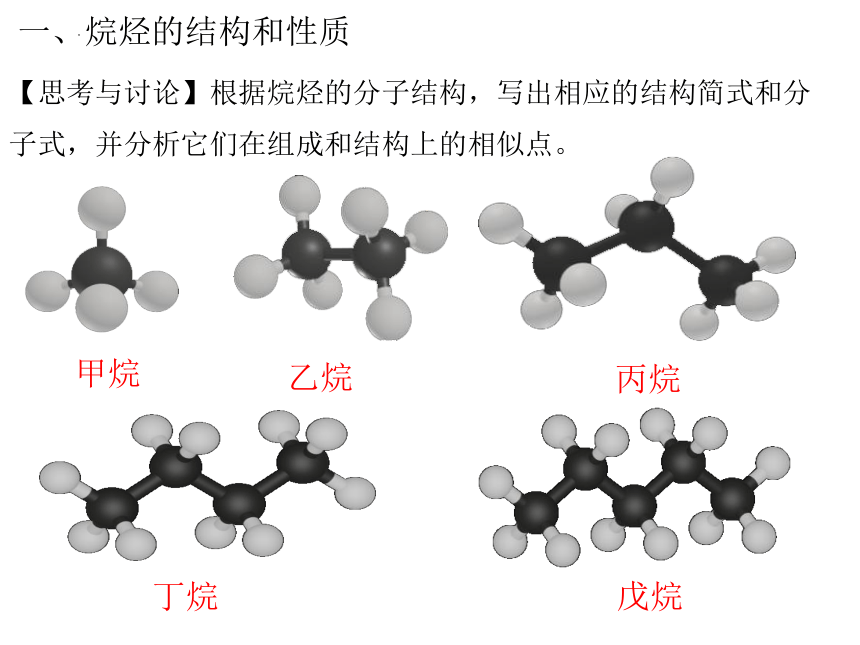
【思考与讨论】根据烷烃的分子结构,写出相应的结构简式和分子式,并分析它们在组成和结构上的相似点。
甲烷
乙烷
丙烷
丁烷
戊烷
CH4
CH3CH3
CH3CH2CH3
CH3CH2CH2CH3
CH3CH2CH2CH2CH3
CH4
C2H6
C3H8
C4H10
C5H12
sp3
sp3
sp3
sp3
sp3
σ键
σ键
σ键
σ键
σ键
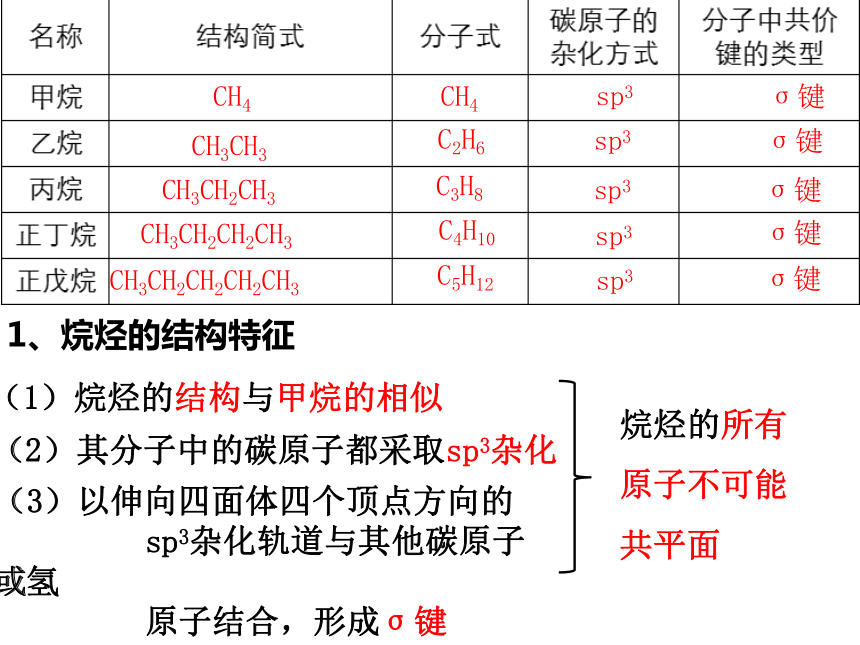
1、烷烃的结构特征
(1)烷烃的结构与甲烷的相似
(2)其分子中的碳原子都采取sp3杂化
(3)以伸向四面体四个顶点方向的
sp3杂化轨道与其他碳原子或氢
原子结合,形成σ键
(4)烷烃分子中的共价键全部是单键
分子中的碳原子并非直线状排列,
而是锯齿状。
烷烃的所有原子不可能共平面
①空气中燃烧(可燃性)氧化反应
②能在光照下与氯气发生取代反应
2、甲烷的性质
(1)物理性质:无色、无臭的气体,难溶于水,
密度比空气的小
(2)化学性质:比较稳定,常温下不能被酸性
高锰酸钾溶液氧化。也不与强酸、强碱及溴的
四氯化碳溶液反应。
练习4:25℃时某气态烃与O2混合充入密闭容器中,点燃后恢复至25℃,此时容器内压强为原来的1/3,再经NaOH溶液处理,容器内几乎成为真空。该烃为( )
A.CH4 B.C2H6 C.C3H8 D.C4H10
A
练习5:两气态烃以任意比混和,在105℃时1L该混和烃与9L氧气混和,充分燃烧后恢复到原状态,所得的气体仍是10L。下列混和烃中不符合此条件的是( )
A、CH4 C2H4 B、CH4 C3H4
C、C2H4 C3H4 D、C2H2 C3H6
D
(1)氧化反应(烷烃的特征反应) :
1.气态烃燃烧后,若>100℃ , V= y /4-1
①y=4,V前=V后 ②y<4,V前>V后 ③y>4,V前2.气态烃燃烧后,若< 100℃,V前> V后, V=1+ y /4
拓展:烃的燃烧规律-----耗氧方面
例1:等物质的量的下列烃完全燃烧时耗氧量最大的是
①甲烷 ②2-甲基丁烷 ③2-甲基-1-丁烯
④苯 ⑤己烷 ⑥1-己烯
例2:等质量的下列烃完全燃烧时耗氧量最大的是
A.CH4 B. C3H8 C.C2H4 D. C6H6
例3:下列各组物质中只要总质量一定,不论以何种比例混和,完全燃烧生成CO2和水的质量也总是定值的是 A.丙烷和丙稀B.乙烯和丙烷 C.乙烯和丁烯D.甲烷和乙烷
3.最简式相同时,只要总质量一定,任意比例混和,完全燃烧生成的二氧化碳和水的量保持不变。
1.等物质的量的烃完全燃烧时,x+y/4的值越大耗氧越多
2.等质量的烃完全燃烧时,y/x值越大耗氧越多
练习6:等质量的下列各组混合物完全燃烧生成CO2的质量由大到小是 。
①C2H6、C3H8 ②C3H4、C3H6 ③C3H6、C2H4 ④C4H10、C3H8 ⑤C2H2、C3H4
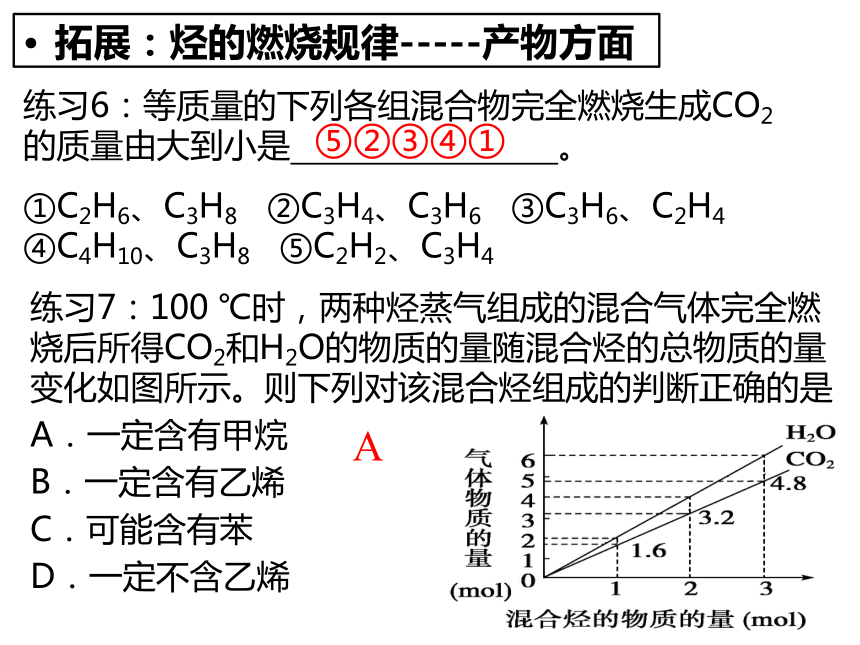
练习7:100 ℃时,两种烃蒸气组成的混合气体完全燃烧后所得CO2和H2O的物质的量随混合烃的总物质的量变化如图所示。则下列对该混合烃组成的判断正确的是
A.一定含有甲烷
B.一定含有乙烯
C.可能含有苯
D.一定不含乙烯
A
拓展:烃的燃烧规律-----产物方面
⑤②③④①
甲烷与氯气取代现象:气体的黄绿色变淡、瓶壁上出现油状液滴、量筒内液面上升。
(2)取代反应(烷烃的特征反应) :
烷烃取代反应特点:
① 连锁反应:逐步取代,同时进行,混合物,不适合制备
② 定量特点:1molX2取代1mol氢原子
③ 反应条件:纯净卤素,光照
甲烷与氯气反应的四种主要生成物的性质
化学式 CH3Cl CH2Cl2 CHCl3 CCl4
名称
溶解性 常温状态 用途 一氯甲烷
二氯甲烷
三氯甲烷
四氯化碳
都不溶于水
气态
液态
重要的有机溶剂
氯仿
四氯甲烷
练习8:若要使0.5molCH4完全和Cl2发生取代反应,并生成相同物质的量的四种取代物,则需要Cl2的物质的量为( )
A.2.5mol B.2mol C.1.25mol D .0.5mol
C
CH4 C + 2H2
甲烷高温下可分解成碳和氢气;长链烷烃高温下可
分解成短链烷烃和烯烃,这在石油化工上称为石油的裂化。
【拓展】分解反应
C4H10 C2H4+C2H6
△
C4H10 CH4+C3H6
△
C16H34 C8H16 +C8H18
催化剂
高温
C8H18 C4H10 +C4H8
催化剂
高温
高温
石油的裂化
石油的裂解
思考与讨论:
(1)根据甲烷的性质推测烷烃可能具有的性质,
填写下表。
颜色 溶解性 可燃性 与酸性高锰酸钾溶液 与溴的四氯化碳溶液 与强酸、强碱溶液 与氯气(在光照下)
无色
难溶
于水
空气中
可以燃烧
不反应
取代反应
不反应
不反应
(2)根据甲烷的燃烧反应,写出汽油的成分之一辛烷(C8H18)完全燃烧的化学方程式。
2C8H18+25O2 16CO2+18H2O
点燃
(3)根据甲烷与氯气的反应,写出乙烷与氯气反应生成一氯乙烷的化学方程式。指出该反应的反应类型,并从化学键和官能团的角度分析反应中有机化合物的变化。
+
Cl—Cl
光
C
C
H
H
H
H
H
H
C
C
Cl
H
H
H
H
H
Cl
H
+
取代反应:
(4)乙烷与氯气在光照下反应,可能生成哪些产物?
请写出它们的结构简式。
①CH3CH2Cl
②CH3CHCl2、CH2ClCH2Cl
③CH3CCl3、 CH2ClCHCl2
④CH2ClCCl3、CHCl2CHCl2
⑤CHCl2CCl3
⑥CCl3CCl3。
【方法导引】替代法
(1)概念:结构相似,在分子组成上相差一个或
若干个CH2原子团的化合物。
3、同系物
(2)实例:CH4、C2H6、C3H8、C17H36互为同系物。
几点说明:同系物一定具有不同的碳原子数(或分子式)。
同系物一定具有不同的相对分子质量(相差14 n)。
同
两种物质属于同一类物质,官能团的种类
和数目一样。
似
差
两种物质结构相似,碳骨架的链接方式相同。
两种物质分子组成上相差一个或多个CH2原子团
(3)理解
练习2、下列哪组是同系物( )
A.CH3CH2CH2CH3与CH3CH(CH3)CH3
B.CH3CH3与CH3CH(CH3)CH3
C.CH2=CH2与
B
HO
OH
HO
CH3
D.
与
练习2:下列说法正确的是( )
A.所有的烷烃,彼此都是同系物
B.两种化合物的组成元素相同,各元素的质量分数也相同,二者一定是同分异构体
C.相对分子质量相同的几种化合物一定是同分异构体
D.每个碳原子的化合价都已饱和,碳原子之间只以单键相结合形成的链烃一定是烷烃
D
名 称 结构简式 常温下状态 熔点 /℃ 沸点 / ℃ 相对 密度 水溶性
甲烷 CH4 气 -182 -161 0.466 不溶
乙烷 CH3CH3 气 -183.3 -88.6 0.572 不溶
丙烷 CH3CH2CH3 气 -187.6 -42.1 0.585 不溶
丁烷 CH3(CH2)2CH3 气 -138.4 -0.5 0.5788 不溶
戊烷 CH3(CH2)3CH3 液 -130 36.1 0.6262 不溶
十七烷 CH3(CH2)15CH3 固 22 301.8 0.7780 不溶
二十四烷 CH3(CH2)22CH3 固 54 391.3 0.7991 不溶
4、烷烃的物理性质
①聚集状态:常温常压下,C1~C4气态;C5~C16液态;C17以上固态。
②熔、沸点:↑
烷烃中随M增加,范德华力增大,熔沸点升高。
在烷烃的同分异构体中,支链越多,沸点越低。
新戊烷常温下为气态
③相对密度:
难溶于水,密度均小于水,并逐渐增加,
④溶解性:
烷烃都难溶于水,易溶于有机溶剂。
练习3:下列烷烃沸点最高的是( )
A.CH3CH2CH3 B.CH3CH2CH2CH3
C.CH3(CH2)3CH3 D.(CH3)2CHCH2CH3
C
课堂小结
结
全单键
化
性
物
性
构
烷烃的结构与甲烷的相似
碳原子sp3杂化,σ键
烷烃的结构与性质
取代反应:氯气光照
稳定,不与三强反应
氧化反应:可燃性
碳数增加熔沸点升高
碳数增加密度增大
碳数增加气液固态。
【2019·浙江4月选考 · C项判断正误】等物质的量的甲烷与氯气反应的产物是CH3Cl( )
ⅹ
【2017·全国卷Ⅱ · D项判断正误】甲烷与氯气在光照下反应后的混合气体能使湿润的石蕊试纸变红,说明生成的一氯甲烷具有酸性( )
ⅹ
【2015·上海卷】卤代烃的制备有多种方法,下列卤代烃不适合由相应的烃经卤代反应制得的是 ( )
C
【2018·全国卷Ⅱ】实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。光照下反应一段时间后,下列装置示意图中能正确反映实验现象的是( )
D
【2013·海南卷,双选】下列烃在光照下与氯气反应,只生成一种一氯代物的有( )
A.2-甲基丙烷 B.环戊烷
C.2,2-二甲基丁烷 D.2,2-二甲基丙烷
BD
(1)烷烃分子中的所有共价键全部是σ键。 ( )
(2)汽油、煤油、石蜡中的主要成分为烷烃。 ( )
(3)烷烃的化学性质稳定,不能发生氧化反应。( )
(4)乙烷的熔、沸点比丙烷的高。( )
练习1.判断正误(对的在括号内打“√”,错的在括号内打“×”)
√
√
×
×
(5)烷烃能使酸性KMnO4溶液褪色。 ( )
(6)烷烃在一定条件下与卤素单质反应生成卤代烃( )
(7)符合CnH2n+2的烃一定为烷烃。 ( )
(8)制取1-氯乙烷时可用乙烷和氯气反应。( )
×
×
√
√
练习2.下列关于烷烃性质的叙述中,不正确的是( )
A.烷烃同系物随相对分子质量增大,熔点、沸点逐渐升高,常温下的状态由气态递变到液态,相对分子质量大的则为固态
B.烷烃同系物的密度随相对分子质量增大逐渐增大
C.烷烃跟卤素单质在光照条件下能发生取代反应
D.烷烃同系物都能使溴水、酸性KMnO4溶液褪色
D
练习3、下列说法不正确的是( )
C
练习4、下列说法正确的是( )
A.随着碳原子数的增加,链状烷烃中碳的质量分数逐渐增大,无限趋近
B.链状烷烃分子中每个碳原子都是sp2杂化,能形成4个共价键
C.碳碳间以单键结合,碳原子剩余价键全部与氢原子结合的烃一定符合通式CnH2n+2
D.正戊烷分子中所有碳原子均在一条直线上
A
第二章 烃
第一节 烷烃
第1课时 烷烃的结构和性质
【教学目标】:
1.了解烷烃的物理性质
2.掌握烷烃的结构特点和主要化学性质
【教学重点难点】:
1.烷烃的结构特点和主要化学性质;
2.烷烃同分异构体的书写
天然气
液化石油气
汽油、柴油
凡士林
石蜡
生活中常见的烷烃
1.烷烃的存在
主要成分都是烷烃。
烃分子中的碳原子之间只以单键结合,碳原子剩余的价键全部跟氢原子相结合,使每个碳原子的化合价都已充分利用,都达到“饱和”。这样的烃叫做饱和烃,又叫烷烃。
2.烷烃的定义
练习1.以A原子为中心与2个B原子及2个C原子相结合形成AB2C2分子。下列关于AB2C2的叙述中对的是( )
A.若是正方形,则有四种同分异构体
B.若是正方形,则没有同分异构体
C.若是正四面体,则没有同分异构体
D.若是正四面体,则有两种同分异构体
C
一、烷烃的结构和性质
【思考与讨论】根据烷烃的分子结构,写出相应的结构简式和分子式,并分析它们在组成和结构上的相似点。
甲烷
乙烷
丙烷
丁烷
戊烷
CH4
CH3CH3
CH3CH2CH3
CH3CH2CH2CH3
CH3CH2CH2CH2CH3
CH4
C2H6
C3H8
C4H10
C5H12
sp3
sp3
sp3
sp3
sp3
σ键
σ键
σ键
σ键
σ键
1、烷烃的结构特征
(1)烷烃的结构与甲烷的相似
(2)其分子中的碳原子都采取sp3杂化
(3)以伸向四面体四个顶点方向的
sp3杂化轨道与其他碳原子或氢
原子结合,形成σ键
(4)烷烃分子中的共价键全部是单键
分子中的碳原子并非直线状排列,
而是锯齿状。
烷烃的所有原子不可能共平面
①空气中燃烧(可燃性)氧化反应
②能在光照下与氯气发生取代反应
2、甲烷的性质
(1)物理性质:无色、无臭的气体,难溶于水,
密度比空气的小
(2)化学性质:比较稳定,常温下不能被酸性
高锰酸钾溶液氧化。也不与强酸、强碱及溴的
四氯化碳溶液反应。
练习4:25℃时某气态烃与O2混合充入密闭容器中,点燃后恢复至25℃,此时容器内压强为原来的1/3,再经NaOH溶液处理,容器内几乎成为真空。该烃为( )
A.CH4 B.C2H6 C.C3H8 D.C4H10
A
练习5:两气态烃以任意比混和,在105℃时1L该混和烃与9L氧气混和,充分燃烧后恢复到原状态,所得的气体仍是10L。下列混和烃中不符合此条件的是( )
A、CH4 C2H4 B、CH4 C3H4
C、C2H4 C3H4 D、C2H2 C3H6
D
(1)氧化反应(烷烃的特征反应) :
1.气态烃燃烧后,若>100℃ , V= y /4-1
①y=4,V前=V后 ②y<4,V前>V后 ③y>4,V前
拓展:烃的燃烧规律-----耗氧方面
例1:等物质的量的下列烃完全燃烧时耗氧量最大的是
①甲烷 ②2-甲基丁烷 ③2-甲基-1-丁烯
④苯 ⑤己烷 ⑥1-己烯
例2:等质量的下列烃完全燃烧时耗氧量最大的是
A.CH4 B. C3H8 C.C2H4 D. C6H6
例3:下列各组物质中只要总质量一定,不论以何种比例混和,完全燃烧生成CO2和水的质量也总是定值的是 A.丙烷和丙稀B.乙烯和丙烷 C.乙烯和丁烯D.甲烷和乙烷
3.最简式相同时,只要总质量一定,任意比例混和,完全燃烧生成的二氧化碳和水的量保持不变。
1.等物质的量的烃完全燃烧时,x+y/4的值越大耗氧越多
2.等质量的烃完全燃烧时,y/x值越大耗氧越多
练习6:等质量的下列各组混合物完全燃烧生成CO2的质量由大到小是 。
①C2H6、C3H8 ②C3H4、C3H6 ③C3H6、C2H4 ④C4H10、C3H8 ⑤C2H2、C3H4
练习7:100 ℃时,两种烃蒸气组成的混合气体完全燃烧后所得CO2和H2O的物质的量随混合烃的总物质的量变化如图所示。则下列对该混合烃组成的判断正确的是
A.一定含有甲烷
B.一定含有乙烯
C.可能含有苯
D.一定不含乙烯
A
拓展:烃的燃烧规律-----产物方面
⑤②③④①
甲烷与氯气取代现象:气体的黄绿色变淡、瓶壁上出现油状液滴、量筒内液面上升。
(2)取代反应(烷烃的特征反应) :
烷烃取代反应特点:
① 连锁反应:逐步取代,同时进行,混合物,不适合制备
② 定量特点:1molX2取代1mol氢原子
③ 反应条件:纯净卤素,光照
甲烷与氯气反应的四种主要生成物的性质
化学式 CH3Cl CH2Cl2 CHCl3 CCl4
名称
溶解性 常温状态 用途 一氯甲烷
二氯甲烷
三氯甲烷
四氯化碳
都不溶于水
气态
液态
重要的有机溶剂
氯仿
四氯甲烷
练习8:若要使0.5molCH4完全和Cl2发生取代反应,并生成相同物质的量的四种取代物,则需要Cl2的物质的量为( )
A.2.5mol B.2mol C.1.25mol D .0.5mol
C
CH4 C + 2H2
甲烷高温下可分解成碳和氢气;长链烷烃高温下可
分解成短链烷烃和烯烃,这在石油化工上称为石油的裂化。
【拓展】分解反应
C4H10 C2H4+C2H6
△
C4H10 CH4+C3H6
△
C16H34 C8H16 +C8H18
催化剂
高温
C8H18 C4H10 +C4H8
催化剂
高温
高温
石油的裂化
石油的裂解
思考与讨论:
(1)根据甲烷的性质推测烷烃可能具有的性质,
填写下表。
颜色 溶解性 可燃性 与酸性高锰酸钾溶液 与溴的四氯化碳溶液 与强酸、强碱溶液 与氯气(在光照下)
无色
难溶
于水
空气中
可以燃烧
不反应
取代反应
不反应
不反应
(2)根据甲烷的燃烧反应,写出汽油的成分之一辛烷(C8H18)完全燃烧的化学方程式。
2C8H18+25O2 16CO2+18H2O
点燃
(3)根据甲烷与氯气的反应,写出乙烷与氯气反应生成一氯乙烷的化学方程式。指出该反应的反应类型,并从化学键和官能团的角度分析反应中有机化合物的变化。
+
Cl—Cl
光
C
C
H
H
H
H
H
H
C
C
Cl
H
H
H
H
H
Cl
H
+
取代反应:
(4)乙烷与氯气在光照下反应,可能生成哪些产物?
请写出它们的结构简式。
①CH3CH2Cl
②CH3CHCl2、CH2ClCH2Cl
③CH3CCl3、 CH2ClCHCl2
④CH2ClCCl3、CHCl2CHCl2
⑤CHCl2CCl3
⑥CCl3CCl3。
【方法导引】替代法
(1)概念:结构相似,在分子组成上相差一个或
若干个CH2原子团的化合物。
3、同系物
(2)实例:CH4、C2H6、C3H8、C17H36互为同系物。
几点说明:同系物一定具有不同的碳原子数(或分子式)。
同系物一定具有不同的相对分子质量(相差14 n)。
同
两种物质属于同一类物质,官能团的种类
和数目一样。
似
差
两种物质结构相似,碳骨架的链接方式相同。
两种物质分子组成上相差一个或多个CH2原子团
(3)理解
练习2、下列哪组是同系物( )
A.CH3CH2CH2CH3与CH3CH(CH3)CH3
B.CH3CH3与CH3CH(CH3)CH3
C.CH2=CH2与
B
HO
OH
HO
CH3
D.
与
练习2:下列说法正确的是( )
A.所有的烷烃,彼此都是同系物
B.两种化合物的组成元素相同,各元素的质量分数也相同,二者一定是同分异构体
C.相对分子质量相同的几种化合物一定是同分异构体
D.每个碳原子的化合价都已饱和,碳原子之间只以单键相结合形成的链烃一定是烷烃
D
名 称 结构简式 常温下状态 熔点 /℃ 沸点 / ℃ 相对 密度 水溶性
甲烷 CH4 气 -182 -161 0.466 不溶
乙烷 CH3CH3 气 -183.3 -88.6 0.572 不溶
丙烷 CH3CH2CH3 气 -187.6 -42.1 0.585 不溶
丁烷 CH3(CH2)2CH3 气 -138.4 -0.5 0.5788 不溶
戊烷 CH3(CH2)3CH3 液 -130 36.1 0.6262 不溶
十七烷 CH3(CH2)15CH3 固 22 301.8 0.7780 不溶
二十四烷 CH3(CH2)22CH3 固 54 391.3 0.7991 不溶
4、烷烃的物理性质
①聚集状态:常温常压下,C1~C4气态;C5~C16液态;C17以上固态。
②熔、沸点:↑
烷烃中随M增加,范德华力增大,熔沸点升高。
在烷烃的同分异构体中,支链越多,沸点越低。
新戊烷常温下为气态
③相对密度:
难溶于水,密度均小于水,并逐渐增加,
④溶解性:
烷烃都难溶于水,易溶于有机溶剂。
练习3:下列烷烃沸点最高的是( )
A.CH3CH2CH3 B.CH3CH2CH2CH3
C.CH3(CH2)3CH3 D.(CH3)2CHCH2CH3
C
课堂小结
结
全单键
化
性
物
性
构
烷烃的结构与甲烷的相似
碳原子sp3杂化,σ键
烷烃的结构与性质
取代反应:氯气光照
稳定,不与三强反应
氧化反应:可燃性
碳数增加熔沸点升高
碳数增加密度增大
碳数增加气液固态。
【2019·浙江4月选考 · C项判断正误】等物质的量的甲烷与氯气反应的产物是CH3Cl( )
ⅹ
【2017·全国卷Ⅱ · D项判断正误】甲烷与氯气在光照下反应后的混合气体能使湿润的石蕊试纸变红,说明生成的一氯甲烷具有酸性( )
ⅹ
【2015·上海卷】卤代烃的制备有多种方法,下列卤代烃不适合由相应的烃经卤代反应制得的是 ( )
C
【2018·全国卷Ⅱ】实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。光照下反应一段时间后,下列装置示意图中能正确反映实验现象的是( )
D
【2013·海南卷,双选】下列烃在光照下与氯气反应,只生成一种一氯代物的有( )
A.2-甲基丙烷 B.环戊烷
C.2,2-二甲基丁烷 D.2,2-二甲基丙烷
BD
(1)烷烃分子中的所有共价键全部是σ键。 ( )
(2)汽油、煤油、石蜡中的主要成分为烷烃。 ( )
(3)烷烃的化学性质稳定,不能发生氧化反应。( )
(4)乙烷的熔、沸点比丙烷的高。( )
练习1.判断正误(对的在括号内打“√”,错的在括号内打“×”)
√
√
×
×
(5)烷烃能使酸性KMnO4溶液褪色。 ( )
(6)烷烃在一定条件下与卤素单质反应生成卤代烃( )
(7)符合CnH2n+2的烃一定为烷烃。 ( )
(8)制取1-氯乙烷时可用乙烷和氯气反应。( )
×
×
√
√
练习2.下列关于烷烃性质的叙述中,不正确的是( )
A.烷烃同系物随相对分子质量增大,熔点、沸点逐渐升高,常温下的状态由气态递变到液态,相对分子质量大的则为固态
B.烷烃同系物的密度随相对分子质量增大逐渐增大
C.烷烃跟卤素单质在光照条件下能发生取代反应
D.烷烃同系物都能使溴水、酸性KMnO4溶液褪色
D
练习3、下列说法不正确的是( )
C
练习4、下列说法正确的是( )
A.随着碳原子数的增加,链状烷烃中碳的质量分数逐渐增大,无限趋近
B.链状烷烃分子中每个碳原子都是sp2杂化,能形成4个共价键
C.碳碳间以单键结合,碳原子剩余价键全部与氢原子结合的烃一定符合通式CnH2n+2
D.正戊烷分子中所有碳原子均在一条直线上
A
