3.4.2羧酸衍生物——酯 课件(共56张ppt)化学人教版(2019)选择性必修3
文档属性
| 名称 | 3.4.2羧酸衍生物——酯 课件(共56张ppt)化学人教版(2019)选择性必修3 |
|
|
| 格式 | pptx | ||
| 文件大小 | 4.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-16 00:00:00 | ||
图片预览







文档简介
(共56张PPT)
第三章 烃的衍生物
第四节 羧酸 羧酸衍生物
第二课时 羧酸衍生物——酯
羧酸
羧酸衍生物
羧酸衍生物:
羧酸分子中羧基上的羟基被其他原子或原子团取代得到的产物。
如:乙酸分子中羧基上的羟基被乙氧基(—OCH2CH3)取代后生成的乙酸乙酯,被氨基(—NH2)取代后生成的乙酰胺。
R-C-
O
=
酰基
R-C-OR
O
=
酯
R-C-X
O
=
酰卤
R-C-NH2
O
=
酰胺
羧酸衍生物
自然界中的有机酯
乙酸异戊酯
戊酸戊酯
丁酸乙酯
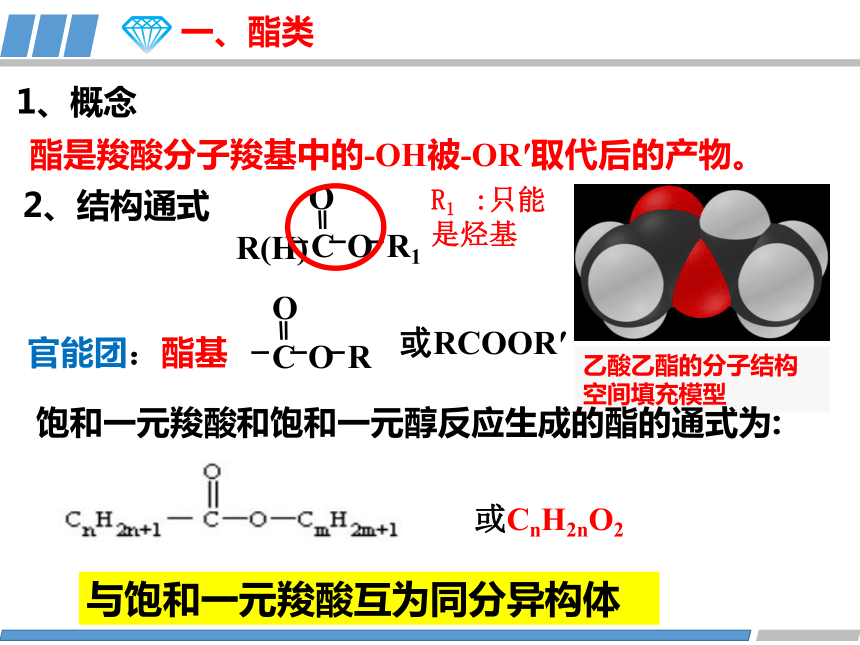
1、概念
酯是羧酸分子羧基中的-OH被-OR′取代后的产物。
2、结构通式
R1 :只能是烃基
R(H)
C
O
R1
O
乙酸乙酯的分子结构空间填充模型
官能团:酯基
C
O
R
O
或RCOOR′
饱和一元羧酸和饱和一元醇反应生成的酯的通式为:
或CnH2nO2
与饱和一元羧酸互为同分异构体
一、酯类
羧酸(或无机含氧酸)+ 醇 酯 + 水
乙酸 乙醇 乙酸乙酯
某酸 某醇 某酸某酯
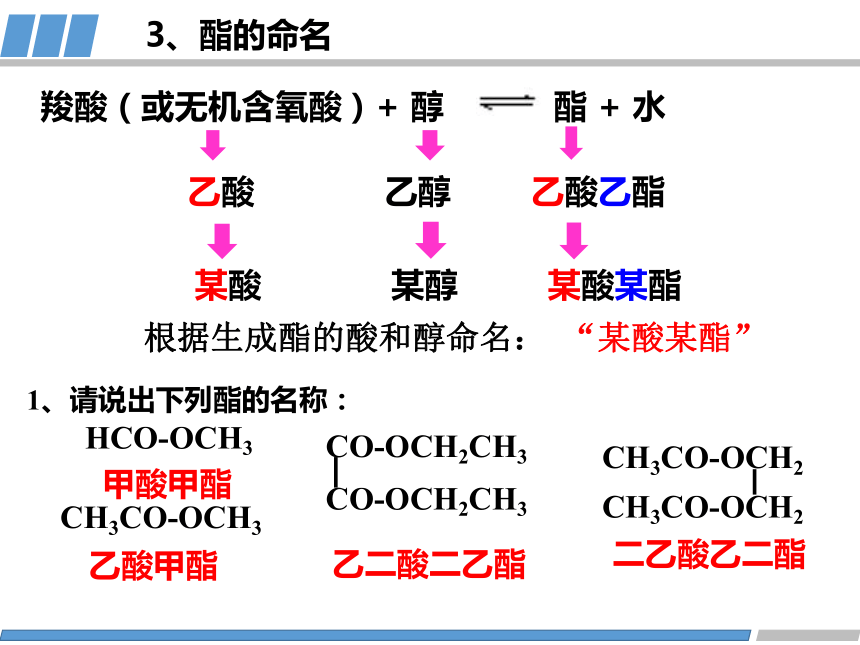
1、请说出下列酯的名称:
HCO-OCH3
CH3CO-OCH3
CO-OCH2CH3
CO-OCH2CH3
CH3CO-OCH2
CH3CO-OCH2
甲酸甲酯
乙酸甲酯
乙二酸二乙酯
二乙酸乙二酯
3、酯的命名
根据生成酯的酸和醇命名: “某酸某酯”
(1)(CH3)2CHCOOCH3
(2)HCOOCH(CH3)2
异丁酸甲酯
甲酸异丙酯
丙酸乙酯
(3)CH3CH2COOCH2CH3
写出下列物质的名称:
(4)CH3CH2O—NO2
硝酸乙酯
苯甲酸甲酯
甲酸苯甲酯
COOCH3
(5)
(6)
CH2OOCH
练一练
作溶剂
作制备饮料和糖果和糕点的酯类香料
物理性质
存在
用途
密度一般比水小
难溶于水,易溶于有机溶剂
许多酯也是常用的有机溶剂。
酯类广泛存在于自然界
低级酯是有芳香气味的液体,存在于各种水果和花草中
4、物理性质
5、酯的化学性质
CH3COOC2H5 +H2O
浓硫酸
△
CH3COOH + C2H5OH
(1)根据该反应的特点,预测乙酸乙酯可能发生的化学反应。
CH3COOC2H5 +H2O
△
CH3COOH + C2H5OH
浓硫酸
(2)请同学们思考如何提高乙酸乙酯的水解速率?
升温、增大反应物浓度、催化剂(无机酸、碱、盐等无机物)
(3)如何比较水解速率的大小?
酯层消失的时间差异
相同时间内酯层的消失量
请你设计实验,绘制实验表格,探讨乙酸乙酯在中性、酸性和碱性溶液中的水解速率
已知:①乙酸乙酯在常温下水解速率很慢
②乙酸乙酯的沸点为76.5—77.5℃
可供选择的试剂:
已染色的乙酸乙酯、蒸馏水、稀硫酸、30%NaOH、酚酞
科学探究1:
①酸碱性对酯的水解的影响:
实验分组 实验操作 现象 结论
1
2 3 1.在3支试管中各加人2 mL乙酸乙酯,再分别加入5ml的稀硫酸、蒸馏水和含有酚酞的NaOH溶液.
2.水浴加热,记录酯层消失和酯香味消失的时间.
几乎无变化
酯层变薄
酯层消失
水解速率
(由快到慢):
碱性溶液
>酸性溶液
>中性溶液
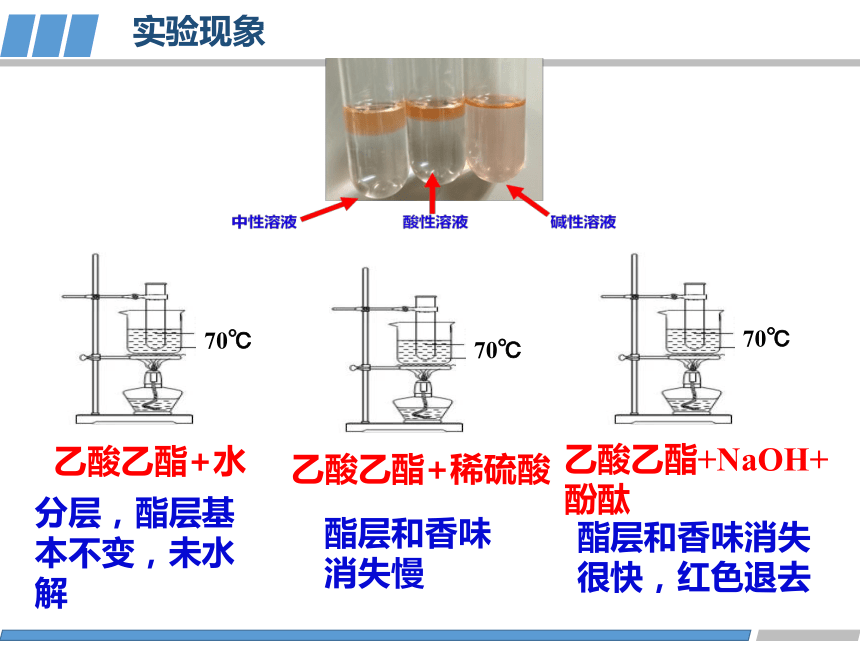
乙酸乙酯+水
70℃
乙酸乙酯+稀硫酸
70℃
乙酸乙酯+NaOH+酚酞
70℃
分层,酯层基本不变,未水解
酯层和香味消失慢
酯层和香味消失很快,红色退去
实验现象
思考与讨论(用化学方程式解释):
1、为什么乙酸乙酯在酸性溶液中的水解速率大于中性溶液的水解速率?
CH3COOC2H5 +H2O
稀硫酸
△
CH3COOH + C2H5OH
无机酸作催化剂,加快反应速率
2、为什么乙酸乙酯在碱性溶液中能够水解完全(请同学们从平衡移动的角度进行分析)?
△
CH3COOC2H5 +NaOH
CH3COONa + C2H5OH
无机碱不仅起催化作用,而且能与水解生成的羧酸发生中和反应,使平衡右移,水解程度增大,直至完全。酯在碱性条件下的水解不可逆。
上述反应的实质是什么?
在酸或碱存在条件下,酯能发生水解反应生成相应的羧酸和醇,酯的水解反应是酯化反应的逆反应。其中在酸性条件下水解是可逆反应,但在碱性条件下,水解是不可逆的。
CH3COOC2H5+H2O CH3COOH+C2H5OH
稀硫酸
△
CH3COOC2H5+NaOH CH3COONa+C2H5OH
△
酸性水解可逆
生成了羧酸盐,使水解反应不可逆,用“→”,也属于取代反应
酯的水解:(取代反应)
稀硫酸
△
CH3C—O—C2H5+H2O CH3COOH+C2H5OH
=
O
酯水解时怎样断键?
酯水解时断酰氧键!
酸还羟基醇还氢
总结:
深度思考
RCOOR' +H2O
水解不完全
稀硫酸
△
RCOOH+R'OH
RCOOR'+NaOH→
水解完全
RCOONa+R' OH
△
请你设计实验,绘制实验表格,探讨乙酸乙酯在不同温度下的水解速率
实验 步骤 a. 分别取2ml乙酸乙酯放入2支试管中,然后向试管中分别加入5ml含酚酞的5mL30%NaOH
b. 振荡均匀后,把2支试管分别放入常温、70~80 ℃的水浴里
实验现象
实验结论
②温度对酯的水解的影响:
温度高的试管酯层消失得更快
温度越高,乙酸乙酯的水解速率越大
科学探究2:
⑴酯在碱性条件下水解速率最快,其次是酸性条件,中性条件下几乎不水解; 在强碱的溶液中酯水解趋于完全。
⑵温度越高,酯水解程度越大。
(水解反应是吸热反应)
酯的水解规律:
归纳小结
某羧酸酯的分子式为C18H26O5,1mol 该酯完全水解可得到 1mol 羧酸和 2mol 乙醇,该羧酸的分子式为
A .C14H18O5 B.C14H16O4 C .C16H22O5 D.C16H20O5
练习
A
酯水解反应和酯化反应的比较
酯化反应 水解
反应关系 CH3COOH+C2H5OH CH3COOC2H5+H2O 催化剂 浓H2SO4 稀H2SO4或NaOH溶液
催化剂的其他作用 吸水,提高乙酸和乙醇的转化率 NaOH中和酯水解生成的乙酸,提高酯的水解率
加热方式 酒精灯火焰加热 热水浴加热
反应类型 酯化反应,取代反应 水解反应,取代反应
RCOOH + HOR′ RCOOR′ + H2O
酯化
水解
1mol下列有机物在 NaOH 溶液中完全水解,所需 NaOH 的量是多少?
CH3COCH3
O
‖
水解后生成乙酸和甲醇,只有乙酸和 NaOH 反应,所以需要 1mol NaOH
水解后生成苯酚和丙酸,所以需要 2mol NaOH ;
同理 则可知第三个需要 3mol NaOH
例题
拓展:有机物在碱性环境下的水解
条件:NaOH溶液,△
(1)R-X
RCOO
(2)
(3)RCOOR'
(4)
X
1mol下列有机物在 NaOH 溶液中完全水解,所需 NaOH 的量是多少?
1mol
2mol
1mol
2mol
卤代烃的水解
酯的水解
酸碱中和(羧酸、酚)
有机物在碱性环境下的水解
以下物质1mol最多能消耗多少molNaOH
CH3COO
COOH
CH2OOCCH3
CH2COOC2H5
CH3COO
Br
CH2Br
3mol
2mol
5mol
1、写出下列酯在酸和碱条件下水解的反应方程式。
HCOOCH3
练习
2. 1mol有机物
与足量NaOH 溶液充分反应,消耗NaOH 的物质的量为( )
A.5mol B.4mol C.3mol D.2mol
COOCH3
CH3COO
COOH
A
练习
4.现有分子式为C3H6O2的四种有机物A、B、C、D,且分子内均含有甲基,把它们分别进行下列实验以鉴别之,其实验记录如下:
NaOH溶液 银氨溶液 新制Cu(OH)2 金属钠
A 中和反应 —— 溶解 产生氢气
B —— 有银镜 产生红色沉淀 产生氢气
C 水解反应 有银镜 产生红色沉淀 ——
D 水解反应 —— —— ——
则A、B、C、D的结构简式分别为:
A: B:
C: D:
CH3CH2COOH
CH3CH(OH)CHO
HCOOCH2CH3
CH3COOCH3
练习
5. 一环酯化合物,结构简式如下:
试推断:
1.该环酯化合物在酸性条件下水解的产物是什么? 写出其结构简式;
2.写出此水解产物与金属钠反应的化学方程式;
3.此水解产物是否可能与FeCl3溶液发生变色反应?
C-OH
OH
HO-CH2
O
-------
-------
练习
化学与生活
地沟油,泛指在生活中存在的各类劣质油,如回收的食用油、反复使用的炸油等,其主要成分是油脂。地沟油最大来源为城市大型饭店下水道的隔油池。长期食用可能会引发癌症,对人体的危害极大。
1.概念
是由多种高级脂肪酸和甘油反应生成的酯,属于酯类。(甘油三酯)
常见的形成油脂的高级脂肪酸有:
硬脂酸: 软脂酸:
油酸: 亚油酸:
C17H35COOH
C15H31COOH
C17H33COOH
2.结构
油脂不属于高分子化合物。
二、油脂
C17H31COOH
⑵按高级脂肪酸的种类分:
单甘油酯:R1、R2、R3都相同;
混甘油酯:R1、R2、R3不都同;
天然油脂大多数为混甘油酯。
3.分类
⑴按状态分:油:常温下呈液态;(植物油)
脂肪:常温下呈固体。(动物脂肪)
1、液态的油脂烃基中含有不饱和键,能使溴水褪色。
2、单甘油酯是纯净物,但是混合甘油酯并不一定是混合物,但要注意植物油和动物油都是混合物。
CH2
O
C
O
R1
CH
O
C
O
R2
CH2
O
C
O
R3
“脂”和” “酯” 的异同
脂 酯
联系 区别 形成酯的醇
形成酯的酸
内 涵
都属于酯
一定为甘油
任何醇或酚
高级脂肪酸
任何含氧酸
专指油脂
包含油脂
CH3C-O-C2H5
O
1、下列物质属于油脂的是 ( )
④润滑油 ⑤花生油 ⑥石蜡 ⑦煤焦油
A.①② B.④⑤
C.①⑤ D.①③
C
课堂检测
(1)密度比水的密度小,为0.9~ 0.95g/cm3;
(2)有明显的油腻感;
(3)不溶于水,易溶于有机溶剂,是一种良好的有机溶剂;
(4)当高级脂肪酸中烯烃基多时大多为液态的油;当高级脂肪酸中烷烃基多时,大多为固态的脂肪。
4、油脂的物理性质
写出硬脂酸、油酸分别与丙三醇反应的化学方程式:
浓硫酸
△
+3H2O
C17H33COOH +
CH2OH
CHOH
CH2OH
浓硫酸
△
+3H2O
3
3
硬脂酸甘油酯
油酸甘油酯
练一练
C
CH2
O
C17H35
O
C
O
O
C
CH2
O
C17H35
CH
O
C17H35
C
CH2
O
C17H33
O
C
O
O
C
CH2
O
C17H33
CH
O
C17H33
C17H35COOH +
CH2OH
CHOH
CH2OH
硬脂酸
丙三醇——甘油
油酸
丙三醇——甘油
(1)水解反应
在酸、碱等催化剂的作用下油脂可以发生水解反应
稀硫酸
△
CH2
O
C
O
C17H35
CH
O
C
O
C17H35
CH2
O
C
O
C17H35
硬脂酸甘油酯
+3H2O
硬脂酸
甘油
油脂+3水
3高级脂肪酸+甘油
稀硫酸
△
5.油脂的化学性质
3
C17H35COOH +
CH2OH
CHOH
CH2OH
CH2
O
C
O
C17H35
CH
O
C
O
C17H35
CH2
O
C
O
C17H35
硬脂酸甘油酯
+3NaOH
硬脂酸钠
甘油
△
油脂+3氢氧化钠
3高级脂肪酸钠+甘油
△
油脂在碱性溶液中水解生成高级脂肪酸盐和甘油
生成肥皂
皂化反应
(1)水解反应
在碱的作用下油脂可以发生水解反应
3
C17H35COONa +
CH2OH
CHOH
CH2OH
手工皂
皂化反应:油脂在碱性条件下的水解反应。
在皂化锅中加入油脂和NaOH溶液,充分搅拌并加热,油脂层逐渐减少,最后液体分层消失,皂化反应完成;加入NaCl细颗粒,在液体上方析出高级脂肪酸钠固体,用纱布过滤,干燥,加入添加剂,成型后即可得到肥皂。
脂肪、植物油
氢氧化钠
加热
高级脂肪酸钠、甘油、水
氯化钠
搅拌、静置
高级脂肪酸钠
甘油、食盐溶液
上层:
下层:
加填充剂(松香、硅酸钠等)
压滤、干燥成型
成品肥皂
甘油
蒸馏
皂化
盐析
加入食盐的目的是发生盐析,可降低高级脂肪酸钠的溶解度,发生聚沉,使其分层析出。
制造肥皂的简单流程
(2)油脂的氢化(硬化)
人造脂肪(硬化油)
人造脂肪(硬化油)具有不易氧化变质、便于储存和运输等优势,可用作制肥皂和人造奶油的原料。
CH2
O
C
O
C17H33
CH
O
C
O
C17H33
CH2
O
C
O
C17H33
油酸甘油酯
+3 H2
硬脂酸甘油酯
△
催化剂
CH2
O
C
O
C17H35
CH
O
C
O
C17H35
CH2
O
C
O
C17H35
油脂对人体的作用
油脂
提供热能
提供人体必需脂肪酸
溶解维生素
增加饱腹感
保护内脏器官
储备热能
细胞膜、神经和脑组织的成分
小结
常言道:“一白遮百丑”,几乎所有女士都希望自己的肌肤能够更白一点,最近几年烟酰胺火遍了全网,作为美白爱好者护肤宝库里必备的一款护肤品,它的美白功效一直以来都广受好评。烟酰胺的结构简式如图 。
化学与生活
蛋白质一级结构中的肽键,在化学上也叫酰胺键,酰胺也是羧酸的衍生物。酰胺具有怎样的性质呢?在学习酰胺之前,下面先简单介绍一下胺
…
C=O
H—N
H—C—R1
C=O
H—N
H—C—R2
C=O
H—N
H—C—R3
C=O
H—N
H—C—R4
…
蛋白质的结构示意图
蛋白质的三级结构
蛋白质的二级结构
蛋白质的四级结构
三、酰胺
烃基取代氨分子中的氢原子而形成的化合物
一般可写作:
官能团:
氨基(—NH2)
1.胺
胺也可看作是烃分子中的氢原子被氨基所替代得到的化合物
R-NH2
甲胺(CH3NH2)
苯胺
这个氨基可以是被取代的氨基(—NRR',R和R'可以是氢原子或烃基)
用途:胺的用途很广,是重要的化工原料。例如,甲胺和苯胺都是合成医药、农药和染料等的重要原料。
(1)结构
胺类化合物具有碱性可与强酸反应生成有机铵盐,如苯胺与盐酸反应的化学方程式为
(2)主要化学性质
CH3—NH2+HCl CH3—NH3Cl
(CH3)2NH+HCl (CH3)2NH2Cl
(CH3)3N+HCl (CH3)3NHCl
有机胺类都具有碱性,可与强酸反应生成有机铵盐
NH2
NH3Cl
+HCl
苯胺
苯胺盐酸盐
故通式表示为
其中
叫做酰胺基
酰胺基的结构简式为
R、R′可以是H或烃基。
叫做酰基
定义:酰胺是羧酸分子中羟基被氨基所替代得到的化合物。
结构:其结构一般表示为
(1)结构
2.酰胺
乙酰胺
苯甲酰胺
N,N-二甲基甲酰胺
CH3—C—NH2
O
—C—NH2
O
H—C—N(CH3)2
O
(2)常见酰胺的结构简式
酰胺键,与酯基类似,在酸或碱存在并加热的条件下可以发生水解反应。请写出下列化学方程式
O
CH3—C—OC2H5+H2O
CH3—C—NH2+H2O
O
R—C—NH2+H2O RCOOH+NH3
O
催化剂
△
O
CH3—C—OC2H5+H2O CH3—C—OH+C2H5OH
O
稀硫酸
△
δ+
δ-
δ+
δ-
CH3—C—NH2+H2O CH3COOH+NH3
O
催化剂
△
思考与讨论:
乙酰胺水解时分别加入HCl、NaOH,写出其化学方程式?
酰胺在酸或碱存在并加热的条件下可以发生水解反应。如RCONH2与盐酸和氢氧化钠的反应
①与HCl溶液反应:
②与NaOH溶液反应:
水解时加入碱,生成的酸就会变成盐,同时有氨气逸出。
(3)酰胺的化学性质
思考:尿素的水解产物是什么?
NH2—C—NH2+2H2O H2CO3+2NH3
O
催化剂
△
×
CO2+H2O
NH2—C—NH2+H2O CO2+2NH3
O
催化剂
△
【思考与讨论】洗涤丝绸质衣物,能否选用肥皂或洗衣粉进行清洗?为什么最好用洗发水进行清洗?
丝绸本质上是蛋白质,里面含有肽键,即酰胺键。肥皂或洗衣粉水溶液呈碱性,在碱性条件下,酰胺键会水解。所以洗涤丝绸,不能用肥皂或洗衣粉,最好用洗发水。
【例】写出苯甲酰胺加入HCl、NaOH水解时的化学方程式。
—C—NH2 +H2O —COOH+NH3
O
催化剂
△
—C—NH2+HCl +H2O —COOH+NH4Cl
O
△
—C—NH2+NaOH —COONa+NH3↑
O
△
(3)应用
酰胺常被用作溶剂和化工原料。例如,N,N 二甲基甲酰胺是良好的溶剂,可以溶解很多有机化合物和无机化合物,是生产多种化学纤维的溶剂,也用于合成农药、医药等。
注意:—NH2和—CONH2都是亲水基团,与水分子能形成氢键,故低级胺、酰胺都能溶于水。
氨、胺、酰胺和铵盐的比较。
氨 胺 酰胺 铵盐
组成元素
结构特点
化学性质
用途
N、H
C、N、H
C、O、N、H
N、H等
NH3
三角锥形
含有氨基
R-NH2
含有NH4+
含有酰胺基
具有碱性,与酸反应生成铵盐
具有碱性,与酸反应生成盐
在酸或碱存在并加热下可发生水解反应
受热易分解,
与碱共热
产生氨气
制冷剂,
生产硝酸和尿素
合成医药、
农药和染料
溶剂和化工原料
生产化肥、和炸药
归纳小结
反应条件与反应类型的关系
(1)NaOH溶液,△
卤代烃的水解
酯的水解
酸碱中和(羧酸、酚)
(2)浓硫酸,△
醇的消去
醇的分子间脱水成醚(取代反应)
酯化反应(取代反应)
磺化反应(取代反应)
小结
几种衍生物之间的关系
溴乙烷
乙烯
乙醇
乙醛
乙酸
乙酸乙酯
①
②
③
④
⑤
⑥
⑦
⑧
⑨
⑩
11
用化学方程式表示上述变化过程
课堂小结
第三章 烃的衍生物
第四节 羧酸 羧酸衍生物
第二课时 羧酸衍生物——酯
羧酸
羧酸衍生物
羧酸衍生物:
羧酸分子中羧基上的羟基被其他原子或原子团取代得到的产物。
如:乙酸分子中羧基上的羟基被乙氧基(—OCH2CH3)取代后生成的乙酸乙酯,被氨基(—NH2)取代后生成的乙酰胺。
R-C-
O
=
酰基
R-C-OR
O
=
酯
R-C-X
O
=
酰卤
R-C-NH2
O
=
酰胺
羧酸衍生物
自然界中的有机酯
乙酸异戊酯
戊酸戊酯
丁酸乙酯
1、概念
酯是羧酸分子羧基中的-OH被-OR′取代后的产物。
2、结构通式
R1 :只能是烃基
R(H)
C
O
R1
O
乙酸乙酯的分子结构空间填充模型
官能团:酯基
C
O
R
O
或RCOOR′
饱和一元羧酸和饱和一元醇反应生成的酯的通式为:
或CnH2nO2
与饱和一元羧酸互为同分异构体
一、酯类
羧酸(或无机含氧酸)+ 醇 酯 + 水
乙酸 乙醇 乙酸乙酯
某酸 某醇 某酸某酯
1、请说出下列酯的名称:
HCO-OCH3
CH3CO-OCH3
CO-OCH2CH3
CO-OCH2CH3
CH3CO-OCH2
CH3CO-OCH2
甲酸甲酯
乙酸甲酯
乙二酸二乙酯
二乙酸乙二酯
3、酯的命名
根据生成酯的酸和醇命名: “某酸某酯”
(1)(CH3)2CHCOOCH3
(2)HCOOCH(CH3)2
异丁酸甲酯
甲酸异丙酯
丙酸乙酯
(3)CH3CH2COOCH2CH3
写出下列物质的名称:
(4)CH3CH2O—NO2
硝酸乙酯
苯甲酸甲酯
甲酸苯甲酯
COOCH3
(5)
(6)
CH2OOCH
练一练
作溶剂
作制备饮料和糖果和糕点的酯类香料
物理性质
存在
用途
密度一般比水小
难溶于水,易溶于有机溶剂
许多酯也是常用的有机溶剂。
酯类广泛存在于自然界
低级酯是有芳香气味的液体,存在于各种水果和花草中
4、物理性质
5、酯的化学性质
CH3COOC2H5 +H2O
浓硫酸
△
CH3COOH + C2H5OH
(1)根据该反应的特点,预测乙酸乙酯可能发生的化学反应。
CH3COOC2H5 +H2O
△
CH3COOH + C2H5OH
浓硫酸
(2)请同学们思考如何提高乙酸乙酯的水解速率?
升温、增大反应物浓度、催化剂(无机酸、碱、盐等无机物)
(3)如何比较水解速率的大小?
酯层消失的时间差异
相同时间内酯层的消失量
请你设计实验,绘制实验表格,探讨乙酸乙酯在中性、酸性和碱性溶液中的水解速率
已知:①乙酸乙酯在常温下水解速率很慢
②乙酸乙酯的沸点为76.5—77.5℃
可供选择的试剂:
已染色的乙酸乙酯、蒸馏水、稀硫酸、30%NaOH、酚酞
科学探究1:
①酸碱性对酯的水解的影响:
实验分组 实验操作 现象 结论
1
2 3 1.在3支试管中各加人2 mL乙酸乙酯,再分别加入5ml的稀硫酸、蒸馏水和含有酚酞的NaOH溶液.
2.水浴加热,记录酯层消失和酯香味消失的时间.
几乎无变化
酯层变薄
酯层消失
水解速率
(由快到慢):
碱性溶液
>酸性溶液
>中性溶液
乙酸乙酯+水
70℃
乙酸乙酯+稀硫酸
70℃
乙酸乙酯+NaOH+酚酞
70℃
分层,酯层基本不变,未水解
酯层和香味消失慢
酯层和香味消失很快,红色退去
实验现象
思考与讨论(用化学方程式解释):
1、为什么乙酸乙酯在酸性溶液中的水解速率大于中性溶液的水解速率?
CH3COOC2H5 +H2O
稀硫酸
△
CH3COOH + C2H5OH
无机酸作催化剂,加快反应速率
2、为什么乙酸乙酯在碱性溶液中能够水解完全(请同学们从平衡移动的角度进行分析)?
△
CH3COOC2H5 +NaOH
CH3COONa + C2H5OH
无机碱不仅起催化作用,而且能与水解生成的羧酸发生中和反应,使平衡右移,水解程度增大,直至完全。酯在碱性条件下的水解不可逆。
上述反应的实质是什么?
在酸或碱存在条件下,酯能发生水解反应生成相应的羧酸和醇,酯的水解反应是酯化反应的逆反应。其中在酸性条件下水解是可逆反应,但在碱性条件下,水解是不可逆的。
CH3COOC2H5+H2O CH3COOH+C2H5OH
稀硫酸
△
CH3COOC2H5+NaOH CH3COONa+C2H5OH
△
酸性水解可逆
生成了羧酸盐,使水解反应不可逆,用“→”,也属于取代反应
酯的水解:(取代反应)
稀硫酸
△
CH3C—O—C2H5+H2O CH3COOH+C2H5OH
=
O
酯水解时怎样断键?
酯水解时断酰氧键!
酸还羟基醇还氢
总结:
深度思考
RCOOR' +H2O
水解不完全
稀硫酸
△
RCOOH+R'OH
RCOOR'+NaOH→
水解完全
RCOONa+R' OH
△
请你设计实验,绘制实验表格,探讨乙酸乙酯在不同温度下的水解速率
实验 步骤 a. 分别取2ml乙酸乙酯放入2支试管中,然后向试管中分别加入5ml含酚酞的5mL30%NaOH
b. 振荡均匀后,把2支试管分别放入常温、70~80 ℃的水浴里
实验现象
实验结论
②温度对酯的水解的影响:
温度高的试管酯层消失得更快
温度越高,乙酸乙酯的水解速率越大
科学探究2:
⑴酯在碱性条件下水解速率最快,其次是酸性条件,中性条件下几乎不水解; 在强碱的溶液中酯水解趋于完全。
⑵温度越高,酯水解程度越大。
(水解反应是吸热反应)
酯的水解规律:
归纳小结
某羧酸酯的分子式为C18H26O5,1mol 该酯完全水解可得到 1mol 羧酸和 2mol 乙醇,该羧酸的分子式为
A .C14H18O5 B.C14H16O4 C .C16H22O5 D.C16H20O5
练习
A
酯水解反应和酯化反应的比较
酯化反应 水解
反应关系 CH3COOH+C2H5OH CH3COOC2H5+H2O 催化剂 浓H2SO4 稀H2SO4或NaOH溶液
催化剂的其他作用 吸水,提高乙酸和乙醇的转化率 NaOH中和酯水解生成的乙酸,提高酯的水解率
加热方式 酒精灯火焰加热 热水浴加热
反应类型 酯化反应,取代反应 水解反应,取代反应
RCOOH + HOR′ RCOOR′ + H2O
酯化
水解
1mol下列有机物在 NaOH 溶液中完全水解,所需 NaOH 的量是多少?
CH3COCH3
O
‖
水解后生成乙酸和甲醇,只有乙酸和 NaOH 反应,所以需要 1mol NaOH
水解后生成苯酚和丙酸,所以需要 2mol NaOH ;
同理 则可知第三个需要 3mol NaOH
例题
拓展:有机物在碱性环境下的水解
条件:NaOH溶液,△
(1)R-X
RCOO
(2)
(3)RCOOR'
(4)
X
1mol下列有机物在 NaOH 溶液中完全水解,所需 NaOH 的量是多少?
1mol
2mol
1mol
2mol
卤代烃的水解
酯的水解
酸碱中和(羧酸、酚)
有机物在碱性环境下的水解
以下物质1mol最多能消耗多少molNaOH
CH3COO
COOH
CH2OOCCH3
CH2COOC2H5
CH3COO
Br
CH2Br
3mol
2mol
5mol
1、写出下列酯在酸和碱条件下水解的反应方程式。
HCOOCH3
练习
2. 1mol有机物
与足量NaOH 溶液充分反应,消耗NaOH 的物质的量为( )
A.5mol B.4mol C.3mol D.2mol
COOCH3
CH3COO
COOH
A
练习
4.现有分子式为C3H6O2的四种有机物A、B、C、D,且分子内均含有甲基,把它们分别进行下列实验以鉴别之,其实验记录如下:
NaOH溶液 银氨溶液 新制Cu(OH)2 金属钠
A 中和反应 —— 溶解 产生氢气
B —— 有银镜 产生红色沉淀 产生氢气
C 水解反应 有银镜 产生红色沉淀 ——
D 水解反应 —— —— ——
则A、B、C、D的结构简式分别为:
A: B:
C: D:
CH3CH2COOH
CH3CH(OH)CHO
HCOOCH2CH3
CH3COOCH3
练习
5. 一环酯化合物,结构简式如下:
试推断:
1.该环酯化合物在酸性条件下水解的产物是什么? 写出其结构简式;
2.写出此水解产物与金属钠反应的化学方程式;
3.此水解产物是否可能与FeCl3溶液发生变色反应?
C-OH
OH
HO-CH2
O
-------
-------
练习
化学与生活
地沟油,泛指在生活中存在的各类劣质油,如回收的食用油、反复使用的炸油等,其主要成分是油脂。地沟油最大来源为城市大型饭店下水道的隔油池。长期食用可能会引发癌症,对人体的危害极大。
1.概念
是由多种高级脂肪酸和甘油反应生成的酯,属于酯类。(甘油三酯)
常见的形成油脂的高级脂肪酸有:
硬脂酸: 软脂酸:
油酸: 亚油酸:
C17H35COOH
C15H31COOH
C17H33COOH
2.结构
油脂不属于高分子化合物。
二、油脂
C17H31COOH
⑵按高级脂肪酸的种类分:
单甘油酯:R1、R2、R3都相同;
混甘油酯:R1、R2、R3不都同;
天然油脂大多数为混甘油酯。
3.分类
⑴按状态分:油:常温下呈液态;(植物油)
脂肪:常温下呈固体。(动物脂肪)
1、液态的油脂烃基中含有不饱和键,能使溴水褪色。
2、单甘油酯是纯净物,但是混合甘油酯并不一定是混合物,但要注意植物油和动物油都是混合物。
CH2
O
C
O
R1
CH
O
C
O
R2
CH2
O
C
O
R3
“脂”和” “酯” 的异同
脂 酯
联系 区别 形成酯的醇
形成酯的酸
内 涵
都属于酯
一定为甘油
任何醇或酚
高级脂肪酸
任何含氧酸
专指油脂
包含油脂
CH3C-O-C2H5
O
1、下列物质属于油脂的是 ( )
④润滑油 ⑤花生油 ⑥石蜡 ⑦煤焦油
A.①② B.④⑤
C.①⑤ D.①③
C
课堂检测
(1)密度比水的密度小,为0.9~ 0.95g/cm3;
(2)有明显的油腻感;
(3)不溶于水,易溶于有机溶剂,是一种良好的有机溶剂;
(4)当高级脂肪酸中烯烃基多时大多为液态的油;当高级脂肪酸中烷烃基多时,大多为固态的脂肪。
4、油脂的物理性质
写出硬脂酸、油酸分别与丙三醇反应的化学方程式:
浓硫酸
△
+3H2O
C17H33COOH +
CH2OH
CHOH
CH2OH
浓硫酸
△
+3H2O
3
3
硬脂酸甘油酯
油酸甘油酯
练一练
C
CH2
O
C17H35
O
C
O
O
C
CH2
O
C17H35
CH
O
C17H35
C
CH2
O
C17H33
O
C
O
O
C
CH2
O
C17H33
CH
O
C17H33
C17H35COOH +
CH2OH
CHOH
CH2OH
硬脂酸
丙三醇——甘油
油酸
丙三醇——甘油
(1)水解反应
在酸、碱等催化剂的作用下油脂可以发生水解反应
稀硫酸
△
CH2
O
C
O
C17H35
CH
O
C
O
C17H35
CH2
O
C
O
C17H35
硬脂酸甘油酯
+3H2O
硬脂酸
甘油
油脂+3水
3高级脂肪酸+甘油
稀硫酸
△
5.油脂的化学性质
3
C17H35COOH +
CH2OH
CHOH
CH2OH
CH2
O
C
O
C17H35
CH
O
C
O
C17H35
CH2
O
C
O
C17H35
硬脂酸甘油酯
+3NaOH
硬脂酸钠
甘油
△
油脂+3氢氧化钠
3高级脂肪酸钠+甘油
△
油脂在碱性溶液中水解生成高级脂肪酸盐和甘油
生成肥皂
皂化反应
(1)水解反应
在碱的作用下油脂可以发生水解反应
3
C17H35COONa +
CH2OH
CHOH
CH2OH
手工皂
皂化反应:油脂在碱性条件下的水解反应。
在皂化锅中加入油脂和NaOH溶液,充分搅拌并加热,油脂层逐渐减少,最后液体分层消失,皂化反应完成;加入NaCl细颗粒,在液体上方析出高级脂肪酸钠固体,用纱布过滤,干燥,加入添加剂,成型后即可得到肥皂。
脂肪、植物油
氢氧化钠
加热
高级脂肪酸钠、甘油、水
氯化钠
搅拌、静置
高级脂肪酸钠
甘油、食盐溶液
上层:
下层:
加填充剂(松香、硅酸钠等)
压滤、干燥成型
成品肥皂
甘油
蒸馏
皂化
盐析
加入食盐的目的是发生盐析,可降低高级脂肪酸钠的溶解度,发生聚沉,使其分层析出。
制造肥皂的简单流程
(2)油脂的氢化(硬化)
人造脂肪(硬化油)
人造脂肪(硬化油)具有不易氧化变质、便于储存和运输等优势,可用作制肥皂和人造奶油的原料。
CH2
O
C
O
C17H33
CH
O
C
O
C17H33
CH2
O
C
O
C17H33
油酸甘油酯
+3 H2
硬脂酸甘油酯
△
催化剂
CH2
O
C
O
C17H35
CH
O
C
O
C17H35
CH2
O
C
O
C17H35
油脂对人体的作用
油脂
提供热能
提供人体必需脂肪酸
溶解维生素
增加饱腹感
保护内脏器官
储备热能
细胞膜、神经和脑组织的成分
小结
常言道:“一白遮百丑”,几乎所有女士都希望自己的肌肤能够更白一点,最近几年烟酰胺火遍了全网,作为美白爱好者护肤宝库里必备的一款护肤品,它的美白功效一直以来都广受好评。烟酰胺的结构简式如图 。
化学与生活
蛋白质一级结构中的肽键,在化学上也叫酰胺键,酰胺也是羧酸的衍生物。酰胺具有怎样的性质呢?在学习酰胺之前,下面先简单介绍一下胺
…
C=O
H—N
H—C—R1
C=O
H—N
H—C—R2
C=O
H—N
H—C—R3
C=O
H—N
H—C—R4
…
蛋白质的结构示意图
蛋白质的三级结构
蛋白质的二级结构
蛋白质的四级结构
三、酰胺
烃基取代氨分子中的氢原子而形成的化合物
一般可写作:
官能团:
氨基(—NH2)
1.胺
胺也可看作是烃分子中的氢原子被氨基所替代得到的化合物
R-NH2
甲胺(CH3NH2)
苯胺
这个氨基可以是被取代的氨基(—NRR',R和R'可以是氢原子或烃基)
用途:胺的用途很广,是重要的化工原料。例如,甲胺和苯胺都是合成医药、农药和染料等的重要原料。
(1)结构
胺类化合物具有碱性可与强酸反应生成有机铵盐,如苯胺与盐酸反应的化学方程式为
(2)主要化学性质
CH3—NH2+HCl CH3—NH3Cl
(CH3)2NH+HCl (CH3)2NH2Cl
(CH3)3N+HCl (CH3)3NHCl
有机胺类都具有碱性,可与强酸反应生成有机铵盐
NH2
NH3Cl
+HCl
苯胺
苯胺盐酸盐
故通式表示为
其中
叫做酰胺基
酰胺基的结构简式为
R、R′可以是H或烃基。
叫做酰基
定义:酰胺是羧酸分子中羟基被氨基所替代得到的化合物。
结构:其结构一般表示为
(1)结构
2.酰胺
乙酰胺
苯甲酰胺
N,N-二甲基甲酰胺
CH3—C—NH2
O
—C—NH2
O
H—C—N(CH3)2
O
(2)常见酰胺的结构简式
酰胺键,与酯基类似,在酸或碱存在并加热的条件下可以发生水解反应。请写出下列化学方程式
O
CH3—C—OC2H5+H2O
CH3—C—NH2+H2O
O
R—C—NH2+H2O RCOOH+NH3
O
催化剂
△
O
CH3—C—OC2H5+H2O CH3—C—OH+C2H5OH
O
稀硫酸
△
δ+
δ-
δ+
δ-
CH3—C—NH2+H2O CH3COOH+NH3
O
催化剂
△
思考与讨论:
乙酰胺水解时分别加入HCl、NaOH,写出其化学方程式?
酰胺在酸或碱存在并加热的条件下可以发生水解反应。如RCONH2与盐酸和氢氧化钠的反应
①与HCl溶液反应:
②与NaOH溶液反应:
水解时加入碱,生成的酸就会变成盐,同时有氨气逸出。
(3)酰胺的化学性质
思考:尿素的水解产物是什么?
NH2—C—NH2+2H2O H2CO3+2NH3
O
催化剂
△
×
CO2+H2O
NH2—C—NH2+H2O CO2+2NH3
O
催化剂
△
【思考与讨论】洗涤丝绸质衣物,能否选用肥皂或洗衣粉进行清洗?为什么最好用洗发水进行清洗?
丝绸本质上是蛋白质,里面含有肽键,即酰胺键。肥皂或洗衣粉水溶液呈碱性,在碱性条件下,酰胺键会水解。所以洗涤丝绸,不能用肥皂或洗衣粉,最好用洗发水。
【例】写出苯甲酰胺加入HCl、NaOH水解时的化学方程式。
—C—NH2 +H2O —COOH+NH3
O
催化剂
△
—C—NH2+HCl +H2O —COOH+NH4Cl
O
△
—C—NH2+NaOH —COONa+NH3↑
O
△
(3)应用
酰胺常被用作溶剂和化工原料。例如,N,N 二甲基甲酰胺是良好的溶剂,可以溶解很多有机化合物和无机化合物,是生产多种化学纤维的溶剂,也用于合成农药、医药等。
注意:—NH2和—CONH2都是亲水基团,与水分子能形成氢键,故低级胺、酰胺都能溶于水。
氨、胺、酰胺和铵盐的比较。
氨 胺 酰胺 铵盐
组成元素
结构特点
化学性质
用途
N、H
C、N、H
C、O、N、H
N、H等
NH3
三角锥形
含有氨基
R-NH2
含有NH4+
含有酰胺基
具有碱性,与酸反应生成铵盐
具有碱性,与酸反应生成盐
在酸或碱存在并加热下可发生水解反应
受热易分解,
与碱共热
产生氨气
制冷剂,
生产硝酸和尿素
合成医药、
农药和染料
溶剂和化工原料
生产化肥、和炸药
归纳小结
反应条件与反应类型的关系
(1)NaOH溶液,△
卤代烃的水解
酯的水解
酸碱中和(羧酸、酚)
(2)浓硫酸,△
醇的消去
醇的分子间脱水成醚(取代反应)
酯化反应(取代反应)
磺化反应(取代反应)
小结
几种衍生物之间的关系
溴乙烷
乙烯
乙醇
乙醛
乙酸
乙酸乙酯
①
②
③
④
⑤
⑥
⑦
⑧
⑨
⑩
11
用化学方程式表示上述变化过程
课堂小结
