化学沪教版九上练习:4.3 化学方程式的书写与应用(含解析)
文档属性
| 名称 | 化学沪教版九上练习:4.3 化学方程式的书写与应用(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-18 00:00:00 | ||
图片预览




文档简介
第3节 化学方程式的书写与应用
一、选择题
1.从化学方程式中不能获得的信息是( )
A.反应条件
B.化学反应的快慢
C.哪些物质是反应物,哪些物质是生成物
D.反应物和生成物的质量关系
2.化学方程式可读作( )
A.镁加氧气等于氧化镁
B.2个镁加1个氧气等于2个氧化镁
C.镁和氧气在点燃条件下生成氧化镁
D.镁加氧气点燃等于氧化镁
3.液氨可用作汽车的清洁燃料,其燃烧时的化学方程式为,下列从化学方程式中获取的信息错误的是( )
A.该反应前后,分子数目发生改变
B.4 g氨气与3 g氧气完全反应,可以生成2 g氮气与6 g水
C.在反应前后,各原子的数目都没有改变
D.生成氮气与水的质量比为14:27
4.四位同学正在讨论某一个化学方程式表示的意义。下列四个化学方程式中,同时符合这四位同学所描述的是( )
A.
B.
C.
D.
5.下列化学方程式书写正确的是( )
A.
B.
C.
D.
6.在反应A+3B2C+3D中,已知A和B的相对分子质量之比为7:8,当
2.8 gA与一定量B恰好完全反应后,生成3.6 gD,则C的质量为( )
A.9.6 g
B.8.8 g
C.6.8 g
D.4.4 g
二、填空题
7.丁烷是石油液化气的主要成分之一,也是市售打火机的燃料,其化学式为,试写出丁烷完全燃烧的化学方程式:________________________________。
三、计算题
8.湿法炼铜为我国首创。早在西汉时期,就有从胆矾水溶液中置换出铜的记载,其反应的化学方程式为。若采用此法炼制128 t铜,需要消耗铁的质量是多少?
四、综合题
9. 2021年1月29日12时47分,我国在酒泉卫星发射中心用长征四号丙运载火箭,成功将遥感三十一号02组卫星发射升空,卫星顺利进入预定轨道。偏二甲肼()是一种常用的火箭推进剂,其燃烧的化学方程式为,写出该化学方程式所提供的3条信息:
(1)________________________________;
(2)________________________________;
(3)________________________________。
10.某同学写了以下化学方程式:
A.
B.
C.
D.
E.
根据化学方程式错误的不同,将其序号填入以下相应的空白处:
(1)未配平的是________;
(2)化学式写错的是________;
(3)“”使用不当的是________;
(4)未注明反应条件的是________;
(5)反应条件写错的是________。
11.我国科学家成功研发出一种新型铂单原子催化剂,能将二氧化碳高效转化为甲醇(),该反应的微观过程如图所示:
(1)该反应的化学方程式为________________________________;反应前后化合价发生改变的元素有________。
(2)甲醇不仅是化学工业的基础原料,还是一种清洁的液体燃料。写出甲醇在空气中完全燃烧的化学方程式:________________________________。
(3)若该转化技术广泛应用,则其对人类社会的重要意义是________________________________。
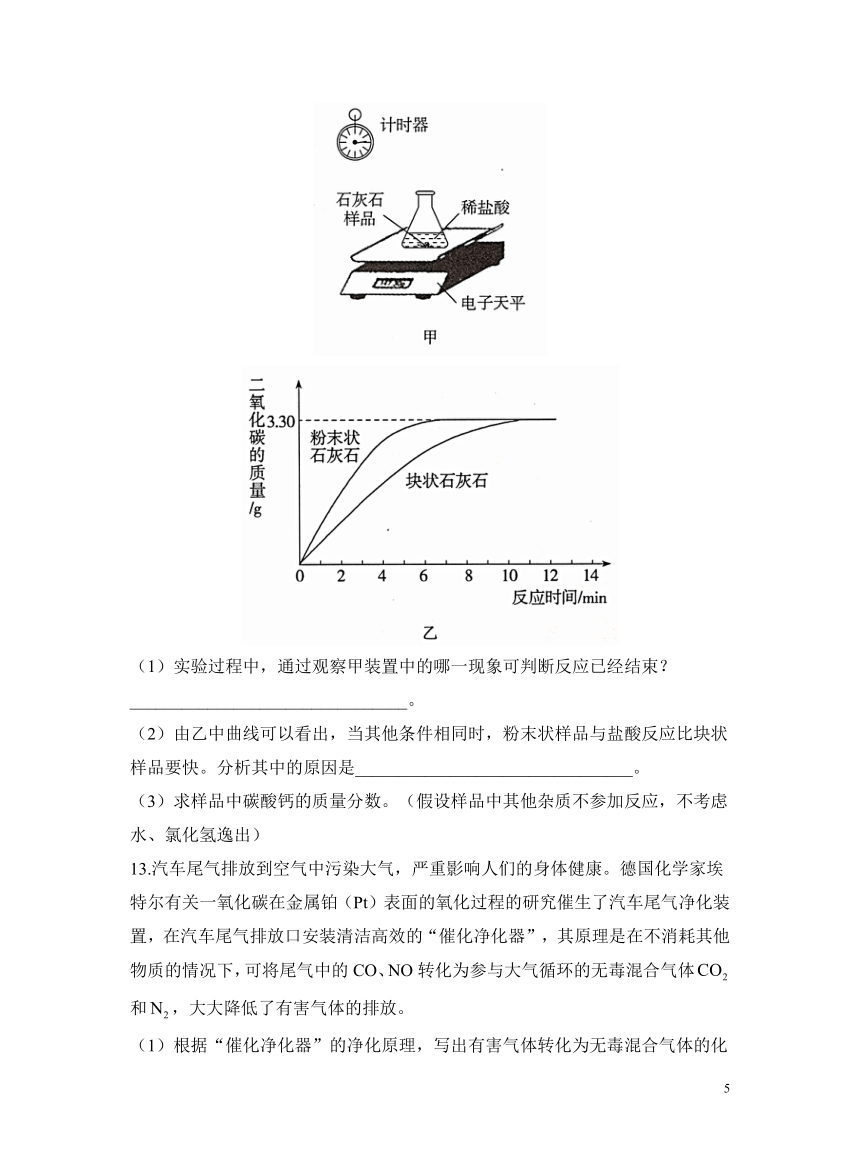
12.某学习小组将采集到的块状石灰石样品用水冲洗后晾干,称取20.00克样品平均分成两份,一份粉碎成粉末,另一份不变。分别与足量相同质量分数的稀盐酸反应,经数据处理得到释放出二氧化碳的质量与反应时间的关系(如乙所示)。
(1)实验过程中,通过观察甲装置中的哪一现象可判断反应已经结束?________________________________。
(2)由乙中曲线可以看出,当其他条件相同时,粉末状样品与盐酸反应比块状样品要快。分析其中的原因是________________________________。
(3)求样品中碳酸钙的质量分数。(假设样品中其他杂质不参加反应,不考虑水、氯化氢逸出)
13.汽车尾气排放到空气中污染大气,严重影响人们的身体健康。德国化学家埃特尔有关一氧化碳在金属铂(Pt)表面的氧化过程的研究催生了汽车尾气净化装置,在汽车尾气排放口安装清洁高效的“催化净化器”,其原理是在不消耗其他物质的情况下,可将尾气中的CO、NO转化为参与大气循环的无毒混合气体和,大大降低了有害气体的排放。
(1)根据“催化净化器”的净化原理,写出有害气体转化为无毒混合气体的化学方程式:________________________________。
(2)如果转化过程中生成176 g,试计算理论上转化CO、NO的质量分别为多少?
14.碳酸氢钠是小苏打的主要成分。在医疗上,它是治疗胃酸(主要成分是盐酸)过多的药剂之一,反应的化学方程式:,化学实验小组取27 g小苏打样品(含有少量不与HCl反应的杂质)进行测定实验。现将小苏打样品平均分为3份,分别进行3次实验。实验数据如表。
实验次数 第一次 第二次 第三次
小苏打样品的质量/g 9 9 9
加入稀盐酸的质量/g 50 100 150
生成气体的质量/g 2.2 4.4 4.4
(1)第________次实验中和HCl恰好完全反应。
(2)计算27 g小苏打样品中碳酸氢钠的质量。(写出计算过程,结果精确到
0.1 g)
参考答案
一、选择题
1.答案:B
解析:由化学方程式可以获得反应发生的条件;由化学方程式无法确定反应的快慢;化学方程式中,“”左边的是反应物,右边的是生成物;由化学方程式可以计算出反应物和生成物的质量关系。
2.答案:C
解析:化学方程式中,“+”读作“和”“与”“跟”,“”读作“生成”,题给化学方程式可读作镁和氧气在点燃条件下生成氧化镁。
3.答案:B
解析:题给反应前后,分子数目发生改变,A说法正确;68 g与96 g完全反应生成56 g和108 g,B说法不正确;在反应前后,各原子的数目都没有改变,C说法正确;生成氮气与水的质量比为(2×28):(6×18)=14:27,D说法正确。
4.答案:C
解析:A中微观粒子个数比是1:1:1,物质的质量比为32:32:64=1:1:2;B中反应不属于化合反应,微观粒子个数比是1:2:1:2,物质的质量比为16:64:44:36=4:16:11:9;C符合题意;D中反应各物质的质量比为3:4:7。
5.答案:B
解析:A项,铁在氧气中燃烧生成四氧化三铁,正确的化学方程式为;B项,该化学方程式书写正确;C项,该化学方程式中反应条件及氧化镁的化学式书写错误,正确的化学方程式应为;D项,该化学方程式没有配平且氢气后面没有标注气体符号,正确的化学方程式应为。
6.答案:B
解析:设参加反应的B的质量为x,A、B的相对分子质量分别为7a、8a。
当2.8 gA与9.6 gB恰好完全反应后,生成3.6 gD,同时生成C的质量为2.8 g+
9.6 g-3.6 g=8.8 g。
二、填空题
7.答案:
解析:反应物为丁烷与氧气,生成物是二氧化碳与水,反应条件为点燃,按照化学方程式的书写步骤进行书写即可。
三、计算题
8.答案:解:设需要消耗铁的质量为x。
答:需要消耗铁的质量为112 t。
解析:根据铁与硫酸铜反应的化学方程式,由铜的质量可以计算需要消耗铁的质量。
四、综合题
9.答案:(1)偏二甲肼在点燃条件下与氧气反应生成氮气、二氧化碳和水
(2)在点燃的条件下,每60份质量的偏二甲肼与128份质量的氧气反应生成28份质量的氮气、88份质量的二氧化碳及72份质量的水
(3)在点燃的条件下,1个偏二甲肼分子与4个氧分子反应生成1个氮分子、2个二氧化碳分子及4个水分子(合理即可)
解析:化学方程式可表示反应条件,可表示反应物、生成物之间的质量比,可表示反应物、生成物之间的粒子个数比等。
10.答案:(1)B
(2)A
(3)D
(4)E
(5)C
解析:A中镁燃烧生成MgO;B中反应前后原子的数目不相等,没有配平;C中的反应条件标注错误,过氧化氢应在二氧化锰的催化作用下制取氧气;D中气体符号标注不正确,应标注生成物,不能标注反应物;E中没有标注反应条件,硫在点燃的条件下与氧气反应。
11.答案(1) C、H
(2)
(3)低碳减排,有利于缓解温室效应(或其他合理答案)
解析:(1)根据反应的微观示意图,可写出题给反应的化学方程式为,碳元素由+4价变为-2价,氢元素由0价变为+1价,反应前后化合价发生改变的元素有C、H。(2)甲醇在空气中完全燃烧生成了二氧化碳和水,反应的化学方程式为。(3)若该转化技术广泛应用,其对人类社会的重要意义是低碳减排,有利于缓解温室效应,同时也能节约其他能源等。
12.答案:(1)电子天平的示数不再发生变化
(2)粉末状的石灰石与稀盐酸的接触面积大,反应速率快;而块状的石灰石与稀盐酸的接触面积小,反应速率慢
(3)解:设每份样品中碳酸钙的质量为x。
称取20.00 g样品平均分成两份,每份的质量为20.00 g÷2=10.00 g
样品中碳酸钙的质量分数为
答:样品中碳酸钙的质量分数为75.0%。
解析:(1)甲装置中电子天平的示数不再发生变化时,说明反应已经结束。(2)粉末状的石灰石与稀盐酸的接触面积大,反应速率快;而块状的石灰石与稀盐酸的接触面积小,反应速率慢。(3)结合图像可知,完全反应生成二氧化碳的质量为3.30 g,根据碳酸钙与盐酸反应的化学方程式,由二氧化碳的质量可以计算碳酸钙的质量,从而可以计算样品中碳酸钙的质量分数。
13.答案:(1)
(2)解:设理论上转化CO、NO的质量分别为x、y。
答:理论上转化CO、NO的质量分别为112 g、120 g。
解析:(1)CO与NO在催化剂的作用下反应生成与,根据化学方程式的书写步骤进行书写即可。(2)根据CO与NO在催化剂的作用下反应生成与的化学方程式,由生成的质量,可以分别计算出CO、NO的质量。
14.答案:(1)二
(2)解:设9 g小苏打样品中碳酸氢钠的质量为x。
则27 g小苏打样品中碳酸氢钠的质量为8.4 g×3=25.2 g
答:27 g小苏打样品中碳酸氢钠的质量为25.2 g。
解析:(1)分析表中数据可知,第一次9 g碳酸氢钠样品与50 g盐酸反应生成2.2 g二氧化碳,第二次9g碳酸氢钠样品与100 g盐酸反应生成4.4 g二氧化碳,第三次9 g碳酸氢钠样品与150 g盐酸反应也生成4.4 g二氧化碳,说明9 g碳酸氢钠样品与100 g盐酸恰好反应生成4.4 g二氧化碳,所以第二次实验中碳酸氢钠与盐酸恰好完全反应。(2)根据碳酸氢钠与盐酸反应的化学方程式及二氧化碳的质量可以计算9 g小苏打样品中碳酸氢钠的质量,从而可以计算27 g小苏打样品中碳酸氢钠的质量。
1
一、选择题
1.从化学方程式中不能获得的信息是( )
A.反应条件
B.化学反应的快慢
C.哪些物质是反应物,哪些物质是生成物
D.反应物和生成物的质量关系
2.化学方程式可读作( )
A.镁加氧气等于氧化镁
B.2个镁加1个氧气等于2个氧化镁
C.镁和氧气在点燃条件下生成氧化镁
D.镁加氧气点燃等于氧化镁
3.液氨可用作汽车的清洁燃料,其燃烧时的化学方程式为,下列从化学方程式中获取的信息错误的是( )
A.该反应前后,分子数目发生改变
B.4 g氨气与3 g氧气完全反应,可以生成2 g氮气与6 g水
C.在反应前后,各原子的数目都没有改变
D.生成氮气与水的质量比为14:27
4.四位同学正在讨论某一个化学方程式表示的意义。下列四个化学方程式中,同时符合这四位同学所描述的是( )
A.
B.
C.
D.
5.下列化学方程式书写正确的是( )
A.
B.
C.
D.
6.在反应A+3B2C+3D中,已知A和B的相对分子质量之比为7:8,当
2.8 gA与一定量B恰好完全反应后,生成3.6 gD,则C的质量为( )
A.9.6 g
B.8.8 g
C.6.8 g
D.4.4 g
二、填空题
7.丁烷是石油液化气的主要成分之一,也是市售打火机的燃料,其化学式为,试写出丁烷完全燃烧的化学方程式:________________________________。
三、计算题
8.湿法炼铜为我国首创。早在西汉时期,就有从胆矾水溶液中置换出铜的记载,其反应的化学方程式为。若采用此法炼制128 t铜,需要消耗铁的质量是多少?
四、综合题
9. 2021年1月29日12时47分,我国在酒泉卫星发射中心用长征四号丙运载火箭,成功将遥感三十一号02组卫星发射升空,卫星顺利进入预定轨道。偏二甲肼()是一种常用的火箭推进剂,其燃烧的化学方程式为,写出该化学方程式所提供的3条信息:
(1)________________________________;
(2)________________________________;
(3)________________________________。
10.某同学写了以下化学方程式:
A.
B.
C.
D.
E.
根据化学方程式错误的不同,将其序号填入以下相应的空白处:
(1)未配平的是________;
(2)化学式写错的是________;
(3)“”使用不当的是________;
(4)未注明反应条件的是________;
(5)反应条件写错的是________。
11.我国科学家成功研发出一种新型铂单原子催化剂,能将二氧化碳高效转化为甲醇(),该反应的微观过程如图所示:
(1)该反应的化学方程式为________________________________;反应前后化合价发生改变的元素有________。
(2)甲醇不仅是化学工业的基础原料,还是一种清洁的液体燃料。写出甲醇在空气中完全燃烧的化学方程式:________________________________。
(3)若该转化技术广泛应用,则其对人类社会的重要意义是________________________________。
12.某学习小组将采集到的块状石灰石样品用水冲洗后晾干,称取20.00克样品平均分成两份,一份粉碎成粉末,另一份不变。分别与足量相同质量分数的稀盐酸反应,经数据处理得到释放出二氧化碳的质量与反应时间的关系(如乙所示)。
(1)实验过程中,通过观察甲装置中的哪一现象可判断反应已经结束?________________________________。
(2)由乙中曲线可以看出,当其他条件相同时,粉末状样品与盐酸反应比块状样品要快。分析其中的原因是________________________________。
(3)求样品中碳酸钙的质量分数。(假设样品中其他杂质不参加反应,不考虑水、氯化氢逸出)
13.汽车尾气排放到空气中污染大气,严重影响人们的身体健康。德国化学家埃特尔有关一氧化碳在金属铂(Pt)表面的氧化过程的研究催生了汽车尾气净化装置,在汽车尾气排放口安装清洁高效的“催化净化器”,其原理是在不消耗其他物质的情况下,可将尾气中的CO、NO转化为参与大气循环的无毒混合气体和,大大降低了有害气体的排放。
(1)根据“催化净化器”的净化原理,写出有害气体转化为无毒混合气体的化学方程式:________________________________。
(2)如果转化过程中生成176 g,试计算理论上转化CO、NO的质量分别为多少?
14.碳酸氢钠是小苏打的主要成分。在医疗上,它是治疗胃酸(主要成分是盐酸)过多的药剂之一,反应的化学方程式:,化学实验小组取27 g小苏打样品(含有少量不与HCl反应的杂质)进行测定实验。现将小苏打样品平均分为3份,分别进行3次实验。实验数据如表。
实验次数 第一次 第二次 第三次
小苏打样品的质量/g 9 9 9
加入稀盐酸的质量/g 50 100 150
生成气体的质量/g 2.2 4.4 4.4
(1)第________次实验中和HCl恰好完全反应。
(2)计算27 g小苏打样品中碳酸氢钠的质量。(写出计算过程,结果精确到
0.1 g)
参考答案
一、选择题
1.答案:B
解析:由化学方程式可以获得反应发生的条件;由化学方程式无法确定反应的快慢;化学方程式中,“”左边的是反应物,右边的是生成物;由化学方程式可以计算出反应物和生成物的质量关系。
2.答案:C
解析:化学方程式中,“+”读作“和”“与”“跟”,“”读作“生成”,题给化学方程式可读作镁和氧气在点燃条件下生成氧化镁。
3.答案:B
解析:题给反应前后,分子数目发生改变,A说法正确;68 g与96 g完全反应生成56 g和108 g,B说法不正确;在反应前后,各原子的数目都没有改变,C说法正确;生成氮气与水的质量比为(2×28):(6×18)=14:27,D说法正确。
4.答案:C
解析:A中微观粒子个数比是1:1:1,物质的质量比为32:32:64=1:1:2;B中反应不属于化合反应,微观粒子个数比是1:2:1:2,物质的质量比为16:64:44:36=4:16:11:9;C符合题意;D中反应各物质的质量比为3:4:7。
5.答案:B
解析:A项,铁在氧气中燃烧生成四氧化三铁,正确的化学方程式为;B项,该化学方程式书写正确;C项,该化学方程式中反应条件及氧化镁的化学式书写错误,正确的化学方程式应为;D项,该化学方程式没有配平且氢气后面没有标注气体符号,正确的化学方程式应为。
6.答案:B
解析:设参加反应的B的质量为x,A、B的相对分子质量分别为7a、8a。
当2.8 gA与9.6 gB恰好完全反应后,生成3.6 gD,同时生成C的质量为2.8 g+
9.6 g-3.6 g=8.8 g。
二、填空题
7.答案:
解析:反应物为丁烷与氧气,生成物是二氧化碳与水,反应条件为点燃,按照化学方程式的书写步骤进行书写即可。
三、计算题
8.答案:解:设需要消耗铁的质量为x。
答:需要消耗铁的质量为112 t。
解析:根据铁与硫酸铜反应的化学方程式,由铜的质量可以计算需要消耗铁的质量。
四、综合题
9.答案:(1)偏二甲肼在点燃条件下与氧气反应生成氮气、二氧化碳和水
(2)在点燃的条件下,每60份质量的偏二甲肼与128份质量的氧气反应生成28份质量的氮气、88份质量的二氧化碳及72份质量的水
(3)在点燃的条件下,1个偏二甲肼分子与4个氧分子反应生成1个氮分子、2个二氧化碳分子及4个水分子(合理即可)
解析:化学方程式可表示反应条件,可表示反应物、生成物之间的质量比,可表示反应物、生成物之间的粒子个数比等。
10.答案:(1)B
(2)A
(3)D
(4)E
(5)C
解析:A中镁燃烧生成MgO;B中反应前后原子的数目不相等,没有配平;C中的反应条件标注错误,过氧化氢应在二氧化锰的催化作用下制取氧气;D中气体符号标注不正确,应标注生成物,不能标注反应物;E中没有标注反应条件,硫在点燃的条件下与氧气反应。
11.答案(1) C、H
(2)
(3)低碳减排,有利于缓解温室效应(或其他合理答案)
解析:(1)根据反应的微观示意图,可写出题给反应的化学方程式为,碳元素由+4价变为-2价,氢元素由0价变为+1价,反应前后化合价发生改变的元素有C、H。(2)甲醇在空气中完全燃烧生成了二氧化碳和水,反应的化学方程式为。(3)若该转化技术广泛应用,其对人类社会的重要意义是低碳减排,有利于缓解温室效应,同时也能节约其他能源等。
12.答案:(1)电子天平的示数不再发生变化
(2)粉末状的石灰石与稀盐酸的接触面积大,反应速率快;而块状的石灰石与稀盐酸的接触面积小,反应速率慢
(3)解:设每份样品中碳酸钙的质量为x。
称取20.00 g样品平均分成两份,每份的质量为20.00 g÷2=10.00 g
样品中碳酸钙的质量分数为
答:样品中碳酸钙的质量分数为75.0%。
解析:(1)甲装置中电子天平的示数不再发生变化时,说明反应已经结束。(2)粉末状的石灰石与稀盐酸的接触面积大,反应速率快;而块状的石灰石与稀盐酸的接触面积小,反应速率慢。(3)结合图像可知,完全反应生成二氧化碳的质量为3.30 g,根据碳酸钙与盐酸反应的化学方程式,由二氧化碳的质量可以计算碳酸钙的质量,从而可以计算样品中碳酸钙的质量分数。
13.答案:(1)
(2)解:设理论上转化CO、NO的质量分别为x、y。
答:理论上转化CO、NO的质量分别为112 g、120 g。
解析:(1)CO与NO在催化剂的作用下反应生成与,根据化学方程式的书写步骤进行书写即可。(2)根据CO与NO在催化剂的作用下反应生成与的化学方程式,由生成的质量,可以分别计算出CO、NO的质量。
14.答案:(1)二
(2)解:设9 g小苏打样品中碳酸氢钠的质量为x。
则27 g小苏打样品中碳酸氢钠的质量为8.4 g×3=25.2 g
答:27 g小苏打样品中碳酸氢钠的质量为25.2 g。
解析:(1)分析表中数据可知,第一次9 g碳酸氢钠样品与50 g盐酸反应生成2.2 g二氧化碳,第二次9g碳酸氢钠样品与100 g盐酸反应生成4.4 g二氧化碳,第三次9 g碳酸氢钠样品与150 g盐酸反应也生成4.4 g二氧化碳,说明9 g碳酸氢钠样品与100 g盐酸恰好反应生成4.4 g二氧化碳,所以第二次实验中碳酸氢钠与盐酸恰好完全反应。(2)根据碳酸氢钠与盐酸反应的化学方程式及二氧化碳的质量可以计算9 g小苏打样品中碳酸氢钠的质量,从而可以计算27 g小苏打样品中碳酸氢钠的质量。
1
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
