化学(沪教版)九年级上册综合练习:4.2 化学反应中的质量关系(含解析)
文档属性
| 名称 | 化学(沪教版)九年级上册综合练习:4.2 化学反应中的质量关系(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 88.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-18 00:00:00 | ||
图片预览



文档简介
4.2 化学反应中的质量关系
一、单选题
1.下列说法错误的是
A.化学反应前后,物质的种类一定发生改变
B.化学反应前后,分子的种类一定发生改变
C.化学反应前后,原子的数目一定不发生改变
D.化学反应前后,原子团一定发生改变
2.自然科学的发展使我们的生活变得丰富多彩。通过化学的学习,你觉得下列情况中不可能实现的是
A.通过化学反应使水直接变成汽油 B.用肥皂水区分硬水和软水
C.用人工的方法合成结晶牛胰岛素 D.通过分离液态空气法得到氧气
3.在反应A+B→C+D中,若15 A与10 B完全反应没有剩余,则生成的C和D的质量总和为
A.15 g B.10 g C.25 g D.5 g
4.某物质在氧气中燃烧只生成和。下列说法正确的是
A.该物质一定是混合物 B.该物质一定含有碳元素和氢元素
C.该物质是由和组成的 D.该物质一定不含氧元素
5.据报道,美国宇航局的专家发明了“月球制氧机”,这种“月球制氧机”利用聚焦太阳能产生的高温使月球土壤发生化学反应制取氧气,据此可推测月球土壤中一定含有
A.氧元素 B.氧气 C.水 D.氯酸钾
6.下列叙述完全符合质量守恒定律的是
A.水结成冰前后,质量保持不变
B.50 mL水和50 mL乙醇混合后总体积小于100 mL
C.在100 g30%过氧化氢溶液中,含有30 g过氧化氢和70 g水
D.1.2 g碳与3.2 g氧气恰好完全反应可生成4.4 g二氧化碳
7.在一密闭容器中,有甲、乙、丙、丁四种物质,在一定的条件下,充分反应,测得反应前后各物质质量如下表 :
物质 甲 乙 丙 丁
反应前的质量/g 4 1 42 10
反应后的质量/g 待测 20 6 31
关于此反应,下列认识正确的是
A.该变化的基本反应类型一定是化合反应 B.参加反应的甲、丙的质量比为1:9
C.乙、丁的相对分子质量比一定为10:9 D.甲反应后的质量为8 g
8.某化合物完全燃烧,需要4.8 g氧气,同时只生成4.4 g二氧化碳和2.7 g 水,则该化合物中
A.只含有碳、氢两种元素 B.只含有碳、氧两种元素
C.含有碳、氢、氧三种元素 D.无法确定
9.在化学反应A+B=C+D中,fgA与B反应生成m gC和n gD,则参加反应的B的质量是多少g?
A.m+n B.m-n C.m+n+f D.m+n-f
10.下列现象不能用质量守恒定律解释的是
A.木材燃烧,余下灰烬的质量小于原木材质量
B.铜丝在火焰上灼烧,灼烧后的“铜丝”质量增加
C.加热高锰酸钾,剩余固体质量减少
D.将一定质量的水冷凝后结成冰,质量不变
11.下列关于化学反应的说法中,正确的是
A.反应前后质量守恒、体积守恒、分子数目守恒
B.反应物的质量总和等于生成物的质量总和
C.反应前后原子数目没有变,原子质量有变化
D.反应后生成了新物质,不是生成了新元素
12.化学反应前后必定改变的是
A.原子的种类 B.分子的种类 C.原子的质量 D.原子的数目
13.下列各组物质,在敞口容器里发生反应,容器内物质的总质量在反应前后不变的是
A.镁条放入盐酸中 B.高锰酸钾固体受热分解
C.硫酸铜溶液加入氢氧化钠溶液 D.在空气中加热铜粉
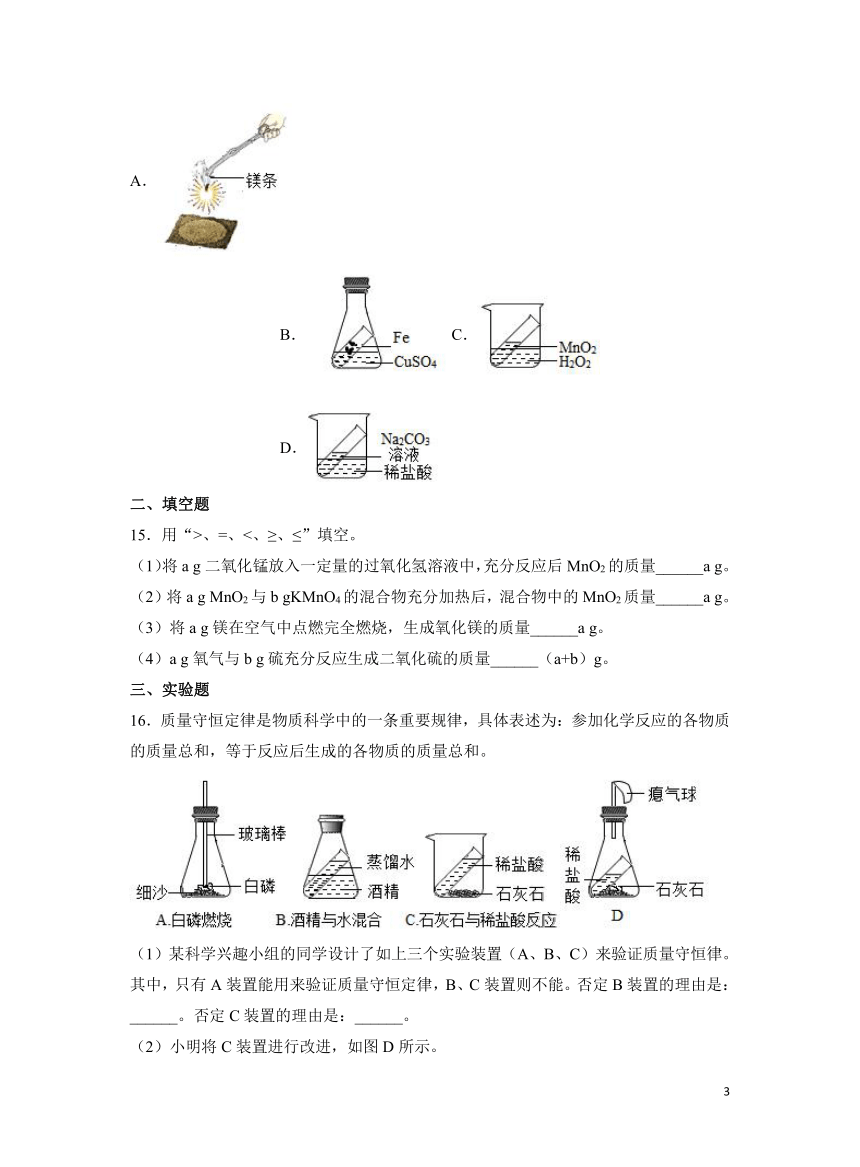
14.下列实验能够直接用于验证质量守恒定律的是
A. B.C. D.
二、填空题
15.用“>、=、<、≥、≤”填空。
(1)将a g二氧化锰放入一定量的过氧化氢溶液中,充分反应后MnO2的质量______a g。
(2)将a g MnO2与b gKMnO4的混合物充分加热后,混合物中的MnO2质量______a g。
(3)将a g镁在空气中点燃完全燃烧,生成氧化镁的质量______a g。
(4)a g氧气与b g硫充分反应生成二氧化硫的质量______(a+b)g。
三、实验题
16.质量守恒定律是物质科学中的一条重要规律,具体表述为:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
(1)某科学兴趣小组的同学设计了如上三个实验装置(A、B、C)来验证质量守恒律。其中,只有A装置能用来验证质量守恒定律,B、C装置则不能。否定B装置的理由是:______。否定C装置的理由是:______。
(2)小明将C装置进行改进,如图D所示。
①此实验气球的作用是:______。
②此实验的现象是______。
③待完全反应后,将装置D置于天平上称量,所得数据较反应前的小。若整个操作过程无差错,则造成上述实验误差的原因是______。
参考答案
一、单选题
1.【答案】D
【详解】
A.化学变化中有新物质生成,所以化学反应前后,物质的种类一定发生改变,选项正确;
B.化学变化中有新物质生成,即有新分子生成,所以化学反应前后,分子的种类一定发生改变,选项正确;
C.原子是化学变化中的最小粒子,所以化学反应前后,原子的数目一定不发生改变,选项正确;
D.化学反应前后,原子团不一定发生改变,选项错误。
故选D。
2.【答案】A
【详解】
A.由质量守恒定律,反应前后元素种类不变,水中不含碳元素,不能通过化学反应使水直接变成汽油,故选项说法错误;
B.硬水和软水的区别在于所含的钙镁离子的多少,可用肥皂水来区分硬水和软水,加入肥皂水,若产生泡沫较多,则是软水,若产生泡沫较少,则是硬水,故选项说法正确;
C.我国已经成功合成结晶牛胰岛素,可以用人工的方法合成结晶牛胰岛素,故选项说法正确;
D.氧气和氮气的沸点不同,通过分离液态空气法得到氧气,故选项说法正确。
故选:A。
3.【答案】C
【详解】
据质量守恒定律,在化学反应中,参加反应的各物质的质量总和等于反应后生成各物质的质量总和,所以生成C和D的质量总和为15 g+10 g=25 g;
故选:C。
4.【答案】B
【分析】
根据质量守恒定律,化学反应前后元素的种类不变,某物质在氧气中燃烧,反应物有两种,其中氧气只含有氧元素,产物只有水和二氧化碳,共含有碳、氢、氧三种元素,氧元素可能来自氧气,也可能来自某物质,不能确定;但氧气中无碳、氢元素,即某物质中一定含有碳、氢两种元素,故准确结论是:该物质中一定含C、H,可能含有O。
【详解】
A.该物质不一定是混合物,例如甲烷燃烧生成二氧化碳和水,错误;
B.该物质一定含有碳元素和氢元素,正确;
C.该物质燃烧生成 CO2 和 H2O ,不是含有二氧化碳和水,错误;
D.该物质可能含氧元素,错误。
故选B。
5.【答案】A
【详解】
A.氧气是由氧元素组成的,根据质量守恒定律,反应前后元素的种类不变,要制氧气原料中必须含有氧元素,故A正确;
B.制氧气可能用物理方法,也可能用化学方法,如用化学方法的话,原料中不一定含氧气,故B错误;
C.水中含有氧元素,可用来制氧气,但含有氧元素的物质均有可能,不一定是水,故C错误;
D.氯酸钾中含有氧元素,能用来制氧气,但含有氧元素的物质均有可能,不一定是氯酸钾,故D错误。
故选:A。
6.【答案】D
【详解】
A.水结成冰前后,质量保持不变,为水的三态变化,为物理变化,不能用质量守恒定律解释;
B.50 mL水和50 mL乙醇混合后总体积小于100 mL,无新物质生成,为物理变化,不能用质量守恒定律解释;
C.在100 g过氧化氢溶液中,含有30 g过氧化氢和70 g水,无新物质生成,不适用质量守恒定律;
D.1.2 g碳与3.2 g氧气恰好完全反应可生成4.4 g二氧化碳,生成物质量=反应物质量之和,符合质量守恒定律。故选D。
【点睛】
质量守恒定律只能解释化学变化,而A、B、C三项中都没有发生化学变化,只是发生了物理变化,因此。质量守恒定律只适合于任何的化学变化。
7.【答案】B
【详解】
A.根据质量守恒定律可知:反应前各物质的质量总和=反应后生成各物质的质量总和,所以待测值=4+1+42+10-20-6-31=0;根据反应中反应物质量会减少,生成物质量会增加,可以判断反应物为:甲和丙,而生成物为乙和丁,反应物为两种不是化合反应,故错误;
B.参加反应的甲、丙的质量比为:(4 g-0 g):(42 g-6 g)=4:36 g=1:9,故正确;
C.根据化学方程式的意义可以知道,参加反应中各物质的质量总和等于跟物质的相对分子质量与其化学计量数的积的比值,由于不知道反应中乙和丁的化学计量数,所以无从判断反应中乙和丁的相对分子质量的比,故错误;
D.根据A的解答可以知道,反应后甲的质量为0,故错误。
故选B。
【点睛】
质量守恒定律是指参加化学反应的各物质的质量总和,等于反应后生成各物质的质量总和。从微观来说,该定律成立的原因是:“在化学反应前后,原子的种类、数目和质量三不变”。
8.【答案】C
【分析】
根据质量守恒定律,由生成物可以初步确定该物质中含有碳元素和氢元素,由生成的二氧化碳和水中碳、氢元素的质量和与该物质的质量进行对比,从而确定该物质的组成元素。
【详解】
中含有碳元素的质量为:,水中含有氢元素的质量为:,生成物二氧化碳和水中所含碳、氢元素的质量和为,某化合物的质量为,,该物质中含氧元素的质量为:,则该物质中一定含有碳、氢、氧三种元素。
故选C。
9.【答案】D
【详解】
已知化学反应A+B=C+D 中,若f gA与一定量的B恰好完全反应,生成m gC和n gD;根据质量守恒定律可知参加反应的B的质量为m g+n g-f g=(m+n-f)g。
故选:D 。
10.【答案】D
【详解】
A.木材燃烧,余下灰烬的质量小于原木材质量,是因为生成的二氧化碳逸散到了空气中,该选项遵循质量守恒定律;
B.铜丝在火焰上灼烧,灼烧后的“铜丝”质量增加,是因为铜和空气中的氧气反应生成了氧化铜,该选项遵循质量守恒定律;
C.加热高锰酸钾,剩余固体质量减少,是因为反应生成的氧气逸出,该选项遵循质量守恒定律;
D.水冷凝后结成冰的过程没有发生化学变化,不能用质量守恒定律解释。
故选:D。
11.【答案】D
【详解】
A.化学反应前后质量守恒,但体积和分子数目不一定守恒,选项不正确;
B.参加化学反应的物质质量总和等于生成物的质量总和,选项不正确;
C.化学反应前后原子数目没有变,原子质量也没有变化,选择不正确;
D.化学反应前后元素种类不变,反应后生成了新物质,不是生成了新元素,选项正确。
故选D。
12.【答案】B
【详解】
化学反应的过程,就是参加反应的各物质的原子重新组合生成其他物质的过程。在化学反应中 ,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变。
A.化学变化前后原子的种类不改变。不选A;
B.化学变化后生成了新物质,分子的种类一定改变。所以选择B;
C.化学变化前后原子的质量不改变。不选C;
D.化学变化前后原子的数目不改变。不选D。
综上所述:选择B。
13.【答案】C
【详解】
A.镁条放入盐酸中,生成氢气逸出,容器内质量变化,不符合题意;
B.高锰酸钾加热生成氧气逸出,容器内质量变化,不符合题意;
C.硫酸铜溶液和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,没有生成气体,容器内质量不变,符合题意;
D.在空气中加热铜粉,铜和氧气反应生成氧化铜,固体质量增加,容器内质量变化,不符合题意。
故选:C。
14.【答案】B
【详解】
A.有气体参加反应,反应后生成的氧化镁比镁条重,不能直接用于验证质量守恒定律;
B.Fe和CuSO4反应,生成FeSO4和Cu,能用于验证质量守恒定律;
C.过氧化氢分解生成氧气,不能用于验证质量守恒定律;
D.稀盐酸和Na2CO3反应有气体生成,反应后烧杯质量减小,不能用于验证质量守恒定律。
故选:B。
二、填空题
15.【答案】
(1)=
(2)>
(3)>
(4)≤
【分析】
(1)二氧化锰在该反应中做催化剂,催化剂在化学反应前后的质量不变,将a g MnO2放入一定量的过氧化氢溶液中,充分反应后MnO2的质量仍为a g,故填:=;
(2)高锰酸钾受热分解生成锰酸钾、二氧化锰、氧气,故将a g MnO2与b g KMnO4的混合物充分加热后,固体剩余物中MnO2的质量大于a g,故填:>
(3)镁在氧气中燃烧生成氧化镁,根据质量守恒定律可知,将a g镁在空气中点燃完全燃烧,生成氧化镁的质量大于a g,故填:>;
(4)a g硫与b g氧气充分反应,可能二者都完全反应,也可能一种有剩余,故a g氧气与b g硫充分反应生成二氧化硫的质量小于或等于(a+b)g,故填:≤。
【点睛】
三、实验题
16.【答案】
(1)物理变化不适用质量守恒定律 反应生成的二氧化碳气体逸散到空气中
(2)防止生成气体逸出,还可防止橡皮塞冲出,平衡气压 有大量气泡产生,气球胀大 膨胀的气球产生了浮力
【分析】
(1)由质量守恒定律的定义可知,只有化学变化才符合质量守恒定律,B中酒精溶于水属于物理变化,不能用来验证质量守恒定律,C中石灰石与盐酸反应生成氯化钙、水和二氧化碳,反应生成的二氧化碳气体逸散到空气中,天平不平衡,不能用来直接验证质量守恒,故填:物理变化不适用质量守恒定律;石灰石和稀盐酸反应生成二氧化碳,反应生成的二氧化碳气体逸散到空气中;
(2)①此实验气球的作用是防止生成气体逸出,还可防止橡皮塞冲出,平衡气压,故填:防止生成气体逸出,还可防止橡皮塞冲出,平衡气压;
②石灰石与盐酸反应生成氯化钙、水和二氧化碳,有气体放出,所以可观察到的现象是锥形瓶内有大量气泡产生,气球胀大,故填:有大量气泡产生,气球胀大;
③由于气球体积变大后,受到的浮力增大,所以会导致天平称量反应后物质质量的读数偏小,故填:膨胀的气球产生了浮力。
1
一、单选题
1.下列说法错误的是
A.化学反应前后,物质的种类一定发生改变
B.化学反应前后,分子的种类一定发生改变
C.化学反应前后,原子的数目一定不发生改变
D.化学反应前后,原子团一定发生改变
2.自然科学的发展使我们的生活变得丰富多彩。通过化学的学习,你觉得下列情况中不可能实现的是
A.通过化学反应使水直接变成汽油 B.用肥皂水区分硬水和软水
C.用人工的方法合成结晶牛胰岛素 D.通过分离液态空气法得到氧气
3.在反应A+B→C+D中,若15 A与10 B完全反应没有剩余,则生成的C和D的质量总和为
A.15 g B.10 g C.25 g D.5 g
4.某物质在氧气中燃烧只生成和。下列说法正确的是
A.该物质一定是混合物 B.该物质一定含有碳元素和氢元素
C.该物质是由和组成的 D.该物质一定不含氧元素
5.据报道,美国宇航局的专家发明了“月球制氧机”,这种“月球制氧机”利用聚焦太阳能产生的高温使月球土壤发生化学反应制取氧气,据此可推测月球土壤中一定含有
A.氧元素 B.氧气 C.水 D.氯酸钾
6.下列叙述完全符合质量守恒定律的是
A.水结成冰前后,质量保持不变
B.50 mL水和50 mL乙醇混合后总体积小于100 mL
C.在100 g30%过氧化氢溶液中,含有30 g过氧化氢和70 g水
D.1.2 g碳与3.2 g氧气恰好完全反应可生成4.4 g二氧化碳
7.在一密闭容器中,有甲、乙、丙、丁四种物质,在一定的条件下,充分反应,测得反应前后各物质质量如下表 :
物质 甲 乙 丙 丁
反应前的质量/g 4 1 42 10
反应后的质量/g 待测 20 6 31
关于此反应,下列认识正确的是
A.该变化的基本反应类型一定是化合反应 B.参加反应的甲、丙的质量比为1:9
C.乙、丁的相对分子质量比一定为10:9 D.甲反应后的质量为8 g
8.某化合物完全燃烧,需要4.8 g氧气,同时只生成4.4 g二氧化碳和2.7 g 水,则该化合物中
A.只含有碳、氢两种元素 B.只含有碳、氧两种元素
C.含有碳、氢、氧三种元素 D.无法确定
9.在化学反应A+B=C+D中,fgA与B反应生成m gC和n gD,则参加反应的B的质量是多少g?
A.m+n B.m-n C.m+n+f D.m+n-f
10.下列现象不能用质量守恒定律解释的是
A.木材燃烧,余下灰烬的质量小于原木材质量
B.铜丝在火焰上灼烧,灼烧后的“铜丝”质量增加
C.加热高锰酸钾,剩余固体质量减少
D.将一定质量的水冷凝后结成冰,质量不变
11.下列关于化学反应的说法中,正确的是
A.反应前后质量守恒、体积守恒、分子数目守恒
B.反应物的质量总和等于生成物的质量总和
C.反应前后原子数目没有变,原子质量有变化
D.反应后生成了新物质,不是生成了新元素
12.化学反应前后必定改变的是
A.原子的种类 B.分子的种类 C.原子的质量 D.原子的数目
13.下列各组物质,在敞口容器里发生反应,容器内物质的总质量在反应前后不变的是
A.镁条放入盐酸中 B.高锰酸钾固体受热分解
C.硫酸铜溶液加入氢氧化钠溶液 D.在空气中加热铜粉
14.下列实验能够直接用于验证质量守恒定律的是
A. B.C. D.
二、填空题
15.用“>、=、<、≥、≤”填空。
(1)将a g二氧化锰放入一定量的过氧化氢溶液中,充分反应后MnO2的质量______a g。
(2)将a g MnO2与b gKMnO4的混合物充分加热后,混合物中的MnO2质量______a g。
(3)将a g镁在空气中点燃完全燃烧,生成氧化镁的质量______a g。
(4)a g氧气与b g硫充分反应生成二氧化硫的质量______(a+b)g。
三、实验题
16.质量守恒定律是物质科学中的一条重要规律,具体表述为:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
(1)某科学兴趣小组的同学设计了如上三个实验装置(A、B、C)来验证质量守恒律。其中,只有A装置能用来验证质量守恒定律,B、C装置则不能。否定B装置的理由是:______。否定C装置的理由是:______。
(2)小明将C装置进行改进,如图D所示。
①此实验气球的作用是:______。
②此实验的现象是______。
③待完全反应后,将装置D置于天平上称量,所得数据较反应前的小。若整个操作过程无差错,则造成上述实验误差的原因是______。
参考答案
一、单选题
1.【答案】D
【详解】
A.化学变化中有新物质生成,所以化学反应前后,物质的种类一定发生改变,选项正确;
B.化学变化中有新物质生成,即有新分子生成,所以化学反应前后,分子的种类一定发生改变,选项正确;
C.原子是化学变化中的最小粒子,所以化学反应前后,原子的数目一定不发生改变,选项正确;
D.化学反应前后,原子团不一定发生改变,选项错误。
故选D。
2.【答案】A
【详解】
A.由质量守恒定律,反应前后元素种类不变,水中不含碳元素,不能通过化学反应使水直接变成汽油,故选项说法错误;
B.硬水和软水的区别在于所含的钙镁离子的多少,可用肥皂水来区分硬水和软水,加入肥皂水,若产生泡沫较多,则是软水,若产生泡沫较少,则是硬水,故选项说法正确;
C.我国已经成功合成结晶牛胰岛素,可以用人工的方法合成结晶牛胰岛素,故选项说法正确;
D.氧气和氮气的沸点不同,通过分离液态空气法得到氧气,故选项说法正确。
故选:A。
3.【答案】C
【详解】
据质量守恒定律,在化学反应中,参加反应的各物质的质量总和等于反应后生成各物质的质量总和,所以生成C和D的质量总和为15 g+10 g=25 g;
故选:C。
4.【答案】B
【分析】
根据质量守恒定律,化学反应前后元素的种类不变,某物质在氧气中燃烧,反应物有两种,其中氧气只含有氧元素,产物只有水和二氧化碳,共含有碳、氢、氧三种元素,氧元素可能来自氧气,也可能来自某物质,不能确定;但氧气中无碳、氢元素,即某物质中一定含有碳、氢两种元素,故准确结论是:该物质中一定含C、H,可能含有O。
【详解】
A.该物质不一定是混合物,例如甲烷燃烧生成二氧化碳和水,错误;
B.该物质一定含有碳元素和氢元素,正确;
C.该物质燃烧生成 CO2 和 H2O ,不是含有二氧化碳和水,错误;
D.该物质可能含氧元素,错误。
故选B。
5.【答案】A
【详解】
A.氧气是由氧元素组成的,根据质量守恒定律,反应前后元素的种类不变,要制氧气原料中必须含有氧元素,故A正确;
B.制氧气可能用物理方法,也可能用化学方法,如用化学方法的话,原料中不一定含氧气,故B错误;
C.水中含有氧元素,可用来制氧气,但含有氧元素的物质均有可能,不一定是水,故C错误;
D.氯酸钾中含有氧元素,能用来制氧气,但含有氧元素的物质均有可能,不一定是氯酸钾,故D错误。
故选:A。
6.【答案】D
【详解】
A.水结成冰前后,质量保持不变,为水的三态变化,为物理变化,不能用质量守恒定律解释;
B.50 mL水和50 mL乙醇混合后总体积小于100 mL,无新物质生成,为物理变化,不能用质量守恒定律解释;
C.在100 g过氧化氢溶液中,含有30 g过氧化氢和70 g水,无新物质生成,不适用质量守恒定律;
D.1.2 g碳与3.2 g氧气恰好完全反应可生成4.4 g二氧化碳,生成物质量=反应物质量之和,符合质量守恒定律。故选D。
【点睛】
质量守恒定律只能解释化学变化,而A、B、C三项中都没有发生化学变化,只是发生了物理变化,因此。质量守恒定律只适合于任何的化学变化。
7.【答案】B
【详解】
A.根据质量守恒定律可知:反应前各物质的质量总和=反应后生成各物质的质量总和,所以待测值=4+1+42+10-20-6-31=0;根据反应中反应物质量会减少,生成物质量会增加,可以判断反应物为:甲和丙,而生成物为乙和丁,反应物为两种不是化合反应,故错误;
B.参加反应的甲、丙的质量比为:(4 g-0 g):(42 g-6 g)=4:36 g=1:9,故正确;
C.根据化学方程式的意义可以知道,参加反应中各物质的质量总和等于跟物质的相对分子质量与其化学计量数的积的比值,由于不知道反应中乙和丁的化学计量数,所以无从判断反应中乙和丁的相对分子质量的比,故错误;
D.根据A的解答可以知道,反应后甲的质量为0,故错误。
故选B。
【点睛】
质量守恒定律是指参加化学反应的各物质的质量总和,等于反应后生成各物质的质量总和。从微观来说,该定律成立的原因是:“在化学反应前后,原子的种类、数目和质量三不变”。
8.【答案】C
【分析】
根据质量守恒定律,由生成物可以初步确定该物质中含有碳元素和氢元素,由生成的二氧化碳和水中碳、氢元素的质量和与该物质的质量进行对比,从而确定该物质的组成元素。
【详解】
中含有碳元素的质量为:,水中含有氢元素的质量为:,生成物二氧化碳和水中所含碳、氢元素的质量和为,某化合物的质量为,,该物质中含氧元素的质量为:,则该物质中一定含有碳、氢、氧三种元素。
故选C。
9.【答案】D
【详解】
已知化学反应A+B=C+D 中,若f gA与一定量的B恰好完全反应,生成m gC和n gD;根据质量守恒定律可知参加反应的B的质量为m g+n g-f g=(m+n-f)g。
故选:D 。
10.【答案】D
【详解】
A.木材燃烧,余下灰烬的质量小于原木材质量,是因为生成的二氧化碳逸散到了空气中,该选项遵循质量守恒定律;
B.铜丝在火焰上灼烧,灼烧后的“铜丝”质量增加,是因为铜和空气中的氧气反应生成了氧化铜,该选项遵循质量守恒定律;
C.加热高锰酸钾,剩余固体质量减少,是因为反应生成的氧气逸出,该选项遵循质量守恒定律;
D.水冷凝后结成冰的过程没有发生化学变化,不能用质量守恒定律解释。
故选:D。
11.【答案】D
【详解】
A.化学反应前后质量守恒,但体积和分子数目不一定守恒,选项不正确;
B.参加化学反应的物质质量总和等于生成物的质量总和,选项不正确;
C.化学反应前后原子数目没有变,原子质量也没有变化,选择不正确;
D.化学反应前后元素种类不变,反应后生成了新物质,不是生成了新元素,选项正确。
故选D。
12.【答案】B
【详解】
化学反应的过程,就是参加反应的各物质的原子重新组合生成其他物质的过程。在化学反应中 ,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变。
A.化学变化前后原子的种类不改变。不选A;
B.化学变化后生成了新物质,分子的种类一定改变。所以选择B;
C.化学变化前后原子的质量不改变。不选C;
D.化学变化前后原子的数目不改变。不选D。
综上所述:选择B。
13.【答案】C
【详解】
A.镁条放入盐酸中,生成氢气逸出,容器内质量变化,不符合题意;
B.高锰酸钾加热生成氧气逸出,容器内质量变化,不符合题意;
C.硫酸铜溶液和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,没有生成气体,容器内质量不变,符合题意;
D.在空气中加热铜粉,铜和氧气反应生成氧化铜,固体质量增加,容器内质量变化,不符合题意。
故选:C。
14.【答案】B
【详解】
A.有气体参加反应,反应后生成的氧化镁比镁条重,不能直接用于验证质量守恒定律;
B.Fe和CuSO4反应,生成FeSO4和Cu,能用于验证质量守恒定律;
C.过氧化氢分解生成氧气,不能用于验证质量守恒定律;
D.稀盐酸和Na2CO3反应有气体生成,反应后烧杯质量减小,不能用于验证质量守恒定律。
故选:B。
二、填空题
15.【答案】
(1)=
(2)>
(3)>
(4)≤
【分析】
(1)二氧化锰在该反应中做催化剂,催化剂在化学反应前后的质量不变,将a g MnO2放入一定量的过氧化氢溶液中,充分反应后MnO2的质量仍为a g,故填:=;
(2)高锰酸钾受热分解生成锰酸钾、二氧化锰、氧气,故将a g MnO2与b g KMnO4的混合物充分加热后,固体剩余物中MnO2的质量大于a g,故填:>
(3)镁在氧气中燃烧生成氧化镁,根据质量守恒定律可知,将a g镁在空气中点燃完全燃烧,生成氧化镁的质量大于a g,故填:>;
(4)a g硫与b g氧气充分反应,可能二者都完全反应,也可能一种有剩余,故a g氧气与b g硫充分反应生成二氧化硫的质量小于或等于(a+b)g,故填:≤。
【点睛】
三、实验题
16.【答案】
(1)物理变化不适用质量守恒定律 反应生成的二氧化碳气体逸散到空气中
(2)防止生成气体逸出,还可防止橡皮塞冲出,平衡气压 有大量气泡产生,气球胀大 膨胀的气球产生了浮力
【分析】
(1)由质量守恒定律的定义可知,只有化学变化才符合质量守恒定律,B中酒精溶于水属于物理变化,不能用来验证质量守恒定律,C中石灰石与盐酸反应生成氯化钙、水和二氧化碳,反应生成的二氧化碳气体逸散到空气中,天平不平衡,不能用来直接验证质量守恒,故填:物理变化不适用质量守恒定律;石灰石和稀盐酸反应生成二氧化碳,反应生成的二氧化碳气体逸散到空气中;
(2)①此实验气球的作用是防止生成气体逸出,还可防止橡皮塞冲出,平衡气压,故填:防止生成气体逸出,还可防止橡皮塞冲出,平衡气压;
②石灰石与盐酸反应生成氯化钙、水和二氧化碳,有气体放出,所以可观察到的现象是锥形瓶内有大量气泡产生,气球胀大,故填:有大量气泡产生,气球胀大;
③由于气球体积变大后,受到的浮力增大,所以会导致天平称量反应后物质质量的读数偏小,故填:膨胀的气球产生了浮力。
1
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
