1.1.2分散系及其分类 课件(共30张ppt)化学人教版(2019)必修第一册
文档属性
| 名称 | 1.1.2分散系及其分类 课件(共30张ppt)化学人教版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 8.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-19 00:00:00 | ||
图片预览









文档简介
(共30张PPT)
第2课时 分散系及其分类
第一章 物质及其变化
第一节 物质的分类及转化
一种或几种物质分散到另一种物质里,形成的均一、稳定的混合物。
固体小颗粒分散到液体里形成的不均一、不稳定的混合物。
小液滴分散到液体里形成的不均一、不稳定的混合物。
【旧知回顾】
溶液:
悬浊液:
乳浊液:
1、分散系:把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系。分散质:分散剂:被分散成粒子的物质另一种物质二、分散系及其分类
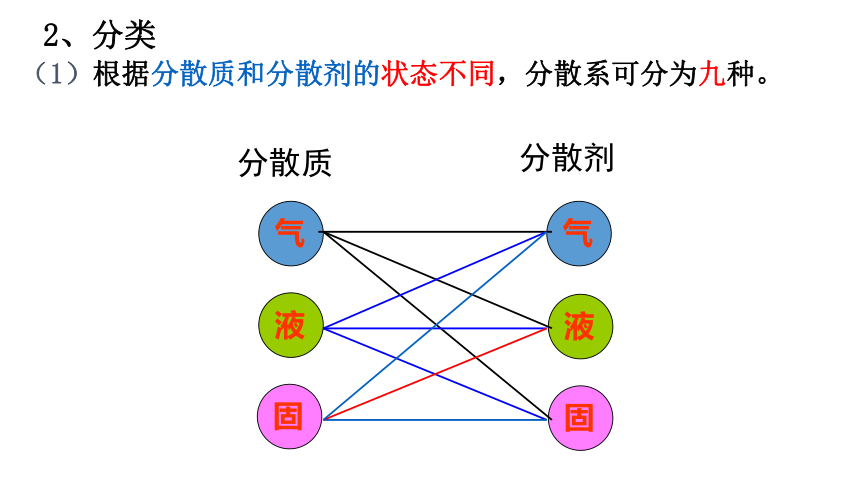
(1)根据分散质和分散剂的状态不同,分散系可分为九种。
分散质
分散剂
气
液
固
气
液
固
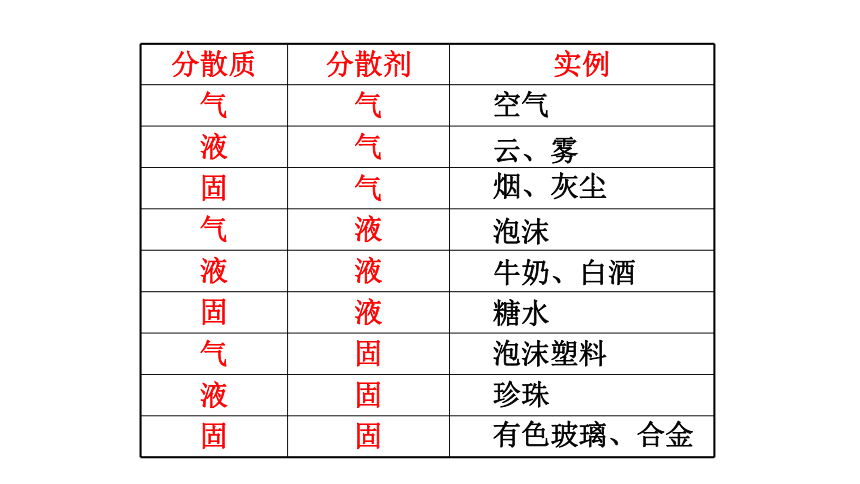
2、分类
分散质 分散剂 实例
气 气
液 气
固 气
气 液
液 液
固 液
气 固
液 固
固 固
空气
云、雾
烟、灰尘
牛奶、白酒
泡沫
有色玻璃、合金
珍珠
泡沫塑料
糖水
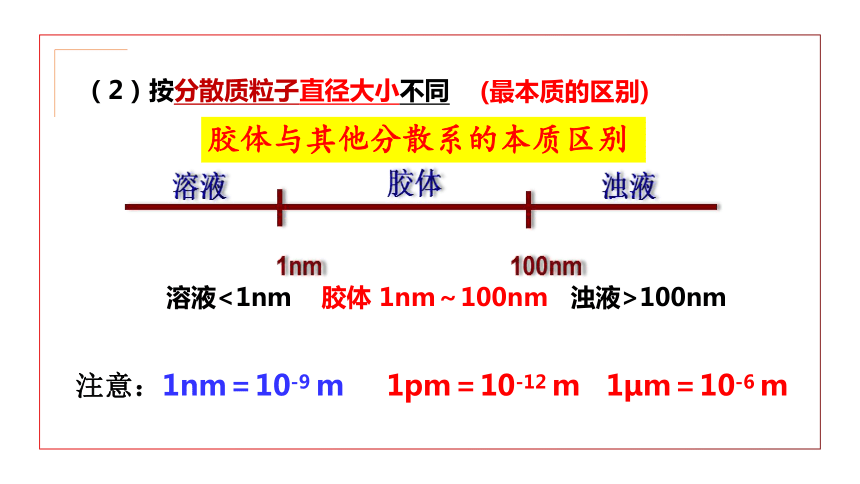
溶液<1nm 胶体 1nm~100nm 浊液>100nm
(2)按分散质粒子直径大小不同
(最本质的区别)
注意:1nm=10-9 m 1pm=10-12 m 1μm=10-6 m
胶体与其他分散系的本质区别
3、胶体:分散质粒子的直径为1nm-100nm的分散系。胶体的分类气溶胶、液溶胶、固溶胶气 溶 胶
晨雾
烟
白云
牛奶
豆浆
果冻
液溶胶
固 溶 胶
烟水晶
有色玻璃
1. 下列分散系中,分散质粒子直径最大的是( )
A.氢氧化铜悬浊液 B.淀粉溶液
C.食盐水 D.牛奶
2. 根据气象台报道,沿海一些城市经常出现大雾天气,致使高速公路关闭航班停飞。雾属于下列分散系中的( )
A.溶液 B.悬浊液
C.乳浊液 D.胶体
A
D
【练习】
分散系
胶 体
浊 液
溶 液
悬
浊
液
乳
浊
液
气
溶
胶
液
溶
胶
固
溶
胶
【实验探究】Fe(OH)3胶体的制备及性质
操作
步骤
1.取40ml的蒸馏水,并煮沸
原理:
2.向沸水中滴加5-6滴饱和FeCl3溶液
3.继续煮沸至溶液呈红褐色,停止加热。
FeCl3 + 3H2O Fe(OH)3(胶体)+3HCl
Fe(OH)3 胶体的制备
Ⅰ.不能过度加热,以免出现Fe(OH)3胶体沉聚。
Ⅱ.不能用玻璃搅拌,防止生成Fe(OH)3沉淀。
注意:
△
将饱和FeCl3溶液分别滴入下列液体中,能形成胶体的是 ( )
A.冷水 B.沸水
C.NaOH浓溶液 D.NaCl浓溶液
B
【练习】
P8 【实验1-1】
用激光笔光束分别照射置于暗处的CuSO4溶液和Fe(OH)3胶体,观察有何现象?
有一条光亮的通路
无光亮的通路
胶体能发生丁达尔效应,而溶液不能。
Fe(OH)3胶体
CuSO4溶液
“丁达尔效应”
【结论】
胶粒对光线散射,
光波分散传播形成。
【胶体与溶液的鉴别方法】
丁达尔效应
胶体的性质
树林中的丁达尔效应
电影院中的丁达尔效应
溶液 胶体 浊液
分散质粒子大小 <1nm 1nm~100nm >100nm
稳定性、均一性 均一、稳定 均一、较稳定 不均一不稳定
丁达尔效应 无 有 无
透过滤纸情况 通过 通过 不能
1、溶液、胶体、浊液的本质区别是粒子的直径大小
2、区别溶液和胶体的简便方法是丁达尔效应
3、胶体的性质:丁达尔效应
归纳总结
完成下表:
过滤后的现象
Fe(OH)3胶体
泥 水
胶体透过滤纸,且没有得到滤渣,过滤后溶液还是红褐色
得到滤渣,过滤后溶液是透明的
实验证明:浊液的分散质粒子大于
胶体的分散质的粒子。
采用半透膜提纯胶体:
把10ml淀粉胶体5mlNaCl溶液混合成的液体,加入用半透膜制成的袋内,将此袋浸入蒸馏水中,2min后,用两只试管各取烧杯中的液体5ml,向其中一支试管里滴加少量AgCl溶液,向另一支试管里滴加少量碘水,观察两支试管中有什么变化?
可以用半透膜分离和提纯胶体和溶液形成的混合体系。
分散系 分散质粒子大小 主要 特征 能否通过半透膜 能否通过滤纸
举例
溶液
胶体
浊液
>100 nm
<1 nm
1~100 nm
不稳定
不均一
稳定
均一
介稳定
均一
泥浆水
NaCl溶液
能
不能
能
豆浆、牛奶
墨水、血液
能
不能
不能
浊液、溶液、胶体三种分散系的区别
2. 胶体的运动学性质——布朗运动
1827年,英国植物学家布朗把花粉悬浮在水里,用显微镜观察,发现花粉的小颗粒在作不停的、无秩序的运动,这种现象叫做布朗运动。
胶体粒子在分散剂分子的撞击下做无规则运动,是胶体具有介稳性的次要原因。
注意:凭借肉眼可以看到的微粒的运动不是补朗运动,如:尘土飞扬、红墨水扩散等。
思考
胶体为什么具有介稳性?
主要原因 胶体粒子可以通过吸附离子而带有电荷,同种胶粒带同种电荷,而同种电荷会相互排斥,所以胶体难聚沉。
次要原因 胶体粒子在不停的做布朗运动
3、胶体的电学性质----电泳现象
在外加电场作用下,胶体粒子在分散剂里向电极(阴极或阳极)做定向移动的现象,叫做电泳。
结论:胶体粒子带电。
规律:金属氧化物、金属氢氧化物的胶体粒子带正电荷,非金属氧化物、金属硫化物、土壤、血液、硅酸胶体粒子带负电荷。
带电原因:胶粒具有较大表面积能吸附带电微粒。(应用:作净水剂)
——胶体稳定的主要原因
胶粒带电,吸附离子;
同种胶粒吸附同种离子,相互排斥。
应用:用于高压除尘、疾病检测等。
4、胶体的介稳性和凝聚现象
向胶体中加入少量电解质溶液时,由于加入的阳离子(或阴离子)中和了胶体粒子所带的电荷,使胶体粒子聚集成为较大的颗粒,从而形成沉淀从分散剂里析出,这个过程叫做聚沉,如:石膏或卤水点豆腐、 FeCl3溶液用于伤口止血等。
胶体凝聚的方法:
(1)加热 (2)加电解质溶液
(3)加带相反电荷的胶体(4)搅拌
五、常见胶体及其应用:
1、常见胶体
烟、云、雾 、有色玻璃、淀粉溶液、蓝黑墨水、豆浆、牛奶、血液、黄河水、大气中的飘尘、工厂废气中固体悬物、矿山开采的粉尘、纺织厂或食品厂弥漫于空气中的有机纤维或颗粒、纳米材料等。
胶体的分类
液溶胶
气溶胶
固溶胶
淀粉溶液、豆浆、蓝黑墨水、
牛奶、血液、黄河水
大气中的飘尘、工厂废气中固体悬物、
纺织厂食品厂弥漫于空气中的有机纤维
或颗粒,矿山开采的粉尘、烟、云、雾 .
有色玻璃
一些纳米材料
2、胶体的应用
(1)石膏或卤水点豆腐、制造果冻
(2)明矾净水原理
(3)江河入海处形成沙洲三角洲
(4)使用蓝色墨水的钢笔抽黑色墨水容易堵塞
(5)喝豆浆放糖不放盐
(6)FeCl3溶液用于伤口止血。
(7)冶金厂大量烟尘用高压电除去。
(8)土壤胶体中离子吸附和交换过程,保肥作用。
……
第2课时 分散系及其分类
第一章 物质及其变化
第一节 物质的分类及转化
一种或几种物质分散到另一种物质里,形成的均一、稳定的混合物。
固体小颗粒分散到液体里形成的不均一、不稳定的混合物。
小液滴分散到液体里形成的不均一、不稳定的混合物。
【旧知回顾】
溶液:
悬浊液:
乳浊液:
1、分散系:把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系。分散质:分散剂:被分散成粒子的物质另一种物质二、分散系及其分类
(1)根据分散质和分散剂的状态不同,分散系可分为九种。
分散质
分散剂
气
液
固
气
液
固
2、分类
分散质 分散剂 实例
气 气
液 气
固 气
气 液
液 液
固 液
气 固
液 固
固 固
空气
云、雾
烟、灰尘
牛奶、白酒
泡沫
有色玻璃、合金
珍珠
泡沫塑料
糖水
溶液<1nm 胶体 1nm~100nm 浊液>100nm
(2)按分散质粒子直径大小不同
(最本质的区别)
注意:1nm=10-9 m 1pm=10-12 m 1μm=10-6 m
胶体与其他分散系的本质区别
3、胶体:分散质粒子的直径为1nm-100nm的分散系。胶体的分类气溶胶、液溶胶、固溶胶气 溶 胶
晨雾
烟
白云
牛奶
豆浆
果冻
液溶胶
固 溶 胶
烟水晶
有色玻璃
1. 下列分散系中,分散质粒子直径最大的是( )
A.氢氧化铜悬浊液 B.淀粉溶液
C.食盐水 D.牛奶
2. 根据气象台报道,沿海一些城市经常出现大雾天气,致使高速公路关闭航班停飞。雾属于下列分散系中的( )
A.溶液 B.悬浊液
C.乳浊液 D.胶体
A
D
【练习】
分散系
胶 体
浊 液
溶 液
悬
浊
液
乳
浊
液
气
溶
胶
液
溶
胶
固
溶
胶
【实验探究】Fe(OH)3胶体的制备及性质
操作
步骤
1.取40ml的蒸馏水,并煮沸
原理:
2.向沸水中滴加5-6滴饱和FeCl3溶液
3.继续煮沸至溶液呈红褐色,停止加热。
FeCl3 + 3H2O Fe(OH)3(胶体)+3HCl
Fe(OH)3 胶体的制备
Ⅰ.不能过度加热,以免出现Fe(OH)3胶体沉聚。
Ⅱ.不能用玻璃搅拌,防止生成Fe(OH)3沉淀。
注意:
△
将饱和FeCl3溶液分别滴入下列液体中,能形成胶体的是 ( )
A.冷水 B.沸水
C.NaOH浓溶液 D.NaCl浓溶液
B
【练习】
P8 【实验1-1】
用激光笔光束分别照射置于暗处的CuSO4溶液和Fe(OH)3胶体,观察有何现象?
有一条光亮的通路
无光亮的通路
胶体能发生丁达尔效应,而溶液不能。
Fe(OH)3胶体
CuSO4溶液
“丁达尔效应”
【结论】
胶粒对光线散射,
光波分散传播形成。
【胶体与溶液的鉴别方法】
丁达尔效应
胶体的性质
树林中的丁达尔效应
电影院中的丁达尔效应
溶液 胶体 浊液
分散质粒子大小 <1nm 1nm~100nm >100nm
稳定性、均一性 均一、稳定 均一、较稳定 不均一不稳定
丁达尔效应 无 有 无
透过滤纸情况 通过 通过 不能
1、溶液、胶体、浊液的本质区别是粒子的直径大小
2、区别溶液和胶体的简便方法是丁达尔效应
3、胶体的性质:丁达尔效应
归纳总结
完成下表:
过滤后的现象
Fe(OH)3胶体
泥 水
胶体透过滤纸,且没有得到滤渣,过滤后溶液还是红褐色
得到滤渣,过滤后溶液是透明的
实验证明:浊液的分散质粒子大于
胶体的分散质的粒子。
采用半透膜提纯胶体:
把10ml淀粉胶体5mlNaCl溶液混合成的液体,加入用半透膜制成的袋内,将此袋浸入蒸馏水中,2min后,用两只试管各取烧杯中的液体5ml,向其中一支试管里滴加少量AgCl溶液,向另一支试管里滴加少量碘水,观察两支试管中有什么变化?
可以用半透膜分离和提纯胶体和溶液形成的混合体系。
分散系 分散质粒子大小 主要 特征 能否通过半透膜 能否通过滤纸
举例
溶液
胶体
浊液
>100 nm
<1 nm
1~100 nm
不稳定
不均一
稳定
均一
介稳定
均一
泥浆水
NaCl溶液
能
不能
能
豆浆、牛奶
墨水、血液
能
不能
不能
浊液、溶液、胶体三种分散系的区别
2. 胶体的运动学性质——布朗运动
1827年,英国植物学家布朗把花粉悬浮在水里,用显微镜观察,发现花粉的小颗粒在作不停的、无秩序的运动,这种现象叫做布朗运动。
胶体粒子在分散剂分子的撞击下做无规则运动,是胶体具有介稳性的次要原因。
注意:凭借肉眼可以看到的微粒的运动不是补朗运动,如:尘土飞扬、红墨水扩散等。
思考
胶体为什么具有介稳性?
主要原因 胶体粒子可以通过吸附离子而带有电荷,同种胶粒带同种电荷,而同种电荷会相互排斥,所以胶体难聚沉。
次要原因 胶体粒子在不停的做布朗运动
3、胶体的电学性质----电泳现象
在外加电场作用下,胶体粒子在分散剂里向电极(阴极或阳极)做定向移动的现象,叫做电泳。
结论:胶体粒子带电。
规律:金属氧化物、金属氢氧化物的胶体粒子带正电荷,非金属氧化物、金属硫化物、土壤、血液、硅酸胶体粒子带负电荷。
带电原因:胶粒具有较大表面积能吸附带电微粒。(应用:作净水剂)
——胶体稳定的主要原因
胶粒带电,吸附离子;
同种胶粒吸附同种离子,相互排斥。
应用:用于高压除尘、疾病检测等。
4、胶体的介稳性和凝聚现象
向胶体中加入少量电解质溶液时,由于加入的阳离子(或阴离子)中和了胶体粒子所带的电荷,使胶体粒子聚集成为较大的颗粒,从而形成沉淀从分散剂里析出,这个过程叫做聚沉,如:石膏或卤水点豆腐、 FeCl3溶液用于伤口止血等。
胶体凝聚的方法:
(1)加热 (2)加电解质溶液
(3)加带相反电荷的胶体(4)搅拌
五、常见胶体及其应用:
1、常见胶体
烟、云、雾 、有色玻璃、淀粉溶液、蓝黑墨水、豆浆、牛奶、血液、黄河水、大气中的飘尘、工厂废气中固体悬物、矿山开采的粉尘、纺织厂或食品厂弥漫于空气中的有机纤维或颗粒、纳米材料等。
胶体的分类
液溶胶
气溶胶
固溶胶
淀粉溶液、豆浆、蓝黑墨水、
牛奶、血液、黄河水
大气中的飘尘、工厂废气中固体悬物、
纺织厂食品厂弥漫于空气中的有机纤维
或颗粒,矿山开采的粉尘、烟、云、雾 .
有色玻璃
一些纳米材料
2、胶体的应用
(1)石膏或卤水点豆腐、制造果冻
(2)明矾净水原理
(3)江河入海处形成沙洲三角洲
(4)使用蓝色墨水的钢笔抽黑色墨水容易堵塞
(5)喝豆浆放糖不放盐
(6)FeCl3溶液用于伤口止血。
(7)冶金厂大量烟尘用高压电除去。
(8)土壤胶体中离子吸附和交换过程,保肥作用。
……
