1.3.2氧化剂和还原剂 课件(共19张ppt)化学人教版(2019)必修第一册
文档属性
| 名称 | 1.3.2氧化剂和还原剂 课件(共19张ppt)化学人教版(2019)必修第一册 |  | |
| 格式 | pptx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-19 14:52:40 | ||
图片预览


文档简介
(共19张PPT)
人教版必修第一册
第一章 物质及其变化
第三节 氧化还原反应
第2课时 氧化剂和还原剂
网
科
学
1、氧化还原反应的本质是 ( )
A、得氧失氧 B、化合价升降
C、有无新物质生成 D、电子转移
D
练一练练一练
2、下列反应中属于氧化还原反应的是( )
A、2HCl + CaCO3 = CaCl2 + H2O + CO2↑
B、H2O + CaO = Ca(OH)2
C、CaCO3 = CaO + CO2 ↑
D、2CO + O2 = 2CO2
点燃
D
人教版必修第一册
高温
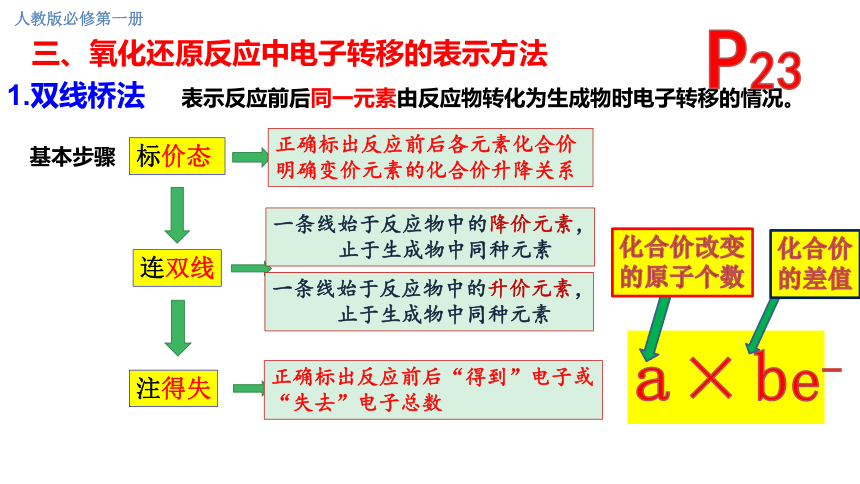
a × be-
标价态
正确标出反应前后各元素化合价
明确变价元素的化合价升降关系
连双线
一条线始于反应物中的降价元素,
止于生成物中同种元素
一条线始于反应物中的升价元素,
止于生成物中同种元素
注得失
正确标出反应前后“得到”电子或“失去”电子总数
三、氧化还原反应中电子转移的表示方法
1.双线桥法
表示反应前后同一元素由反应物转化为生成物时电子转移的情况。
基本步骤
人教版必修第一册
化合价改变
的原子个数
化合价
的差值
P23
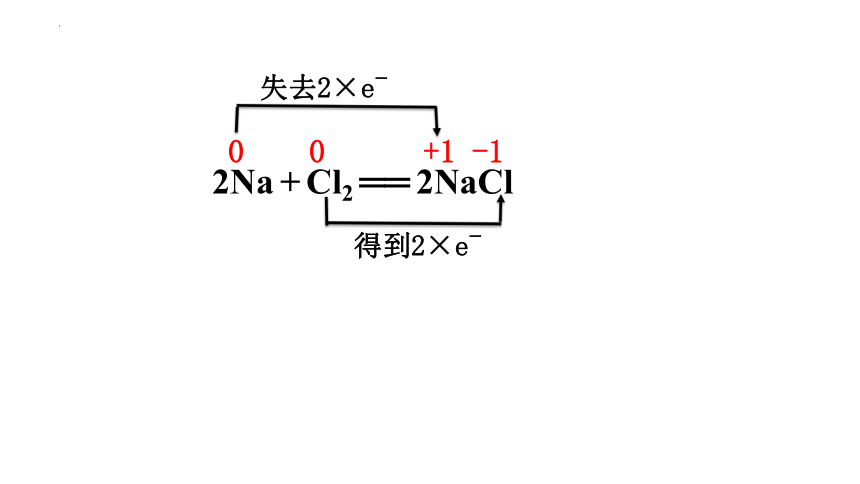
2Na + Cl2 ══ 2NaCl
点 燃
0 0 +1 -1
失去2×e-
得到2×e-
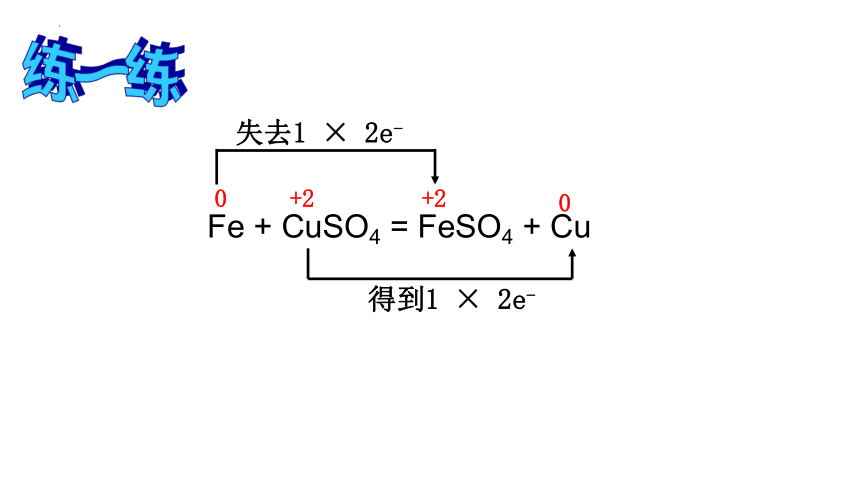
练一练
用双线桥法标出以下反应的电子转移情况:
Fe + CuSO4 = FeSO4 + Cu
0
+2
+2
0
失去1 × 2e-
得到1 × 2e-
H2O + C == H2 + CO
+1 0 0 +2
得到2×e-
失去1 × 2e-
2.单线桥法 表示反应过程中不同元素原子间的电子转移情况。
标价态
基本步骤
正确标出反应前后各元素化合价
明确变价元素的化合价升降关系
连单线
箭头由失电子的原子指向得电子的原子
注数目
正确标出反应中转移的电子总数
注意:不需要标明“得到”或“失去
人教版必修第一册
P25
2Na + Cl2 ══ 2NaCl
点 燃
0 0 +1 -1
2e-
用单线桥表示下列氧化还原反应的电子转移情况
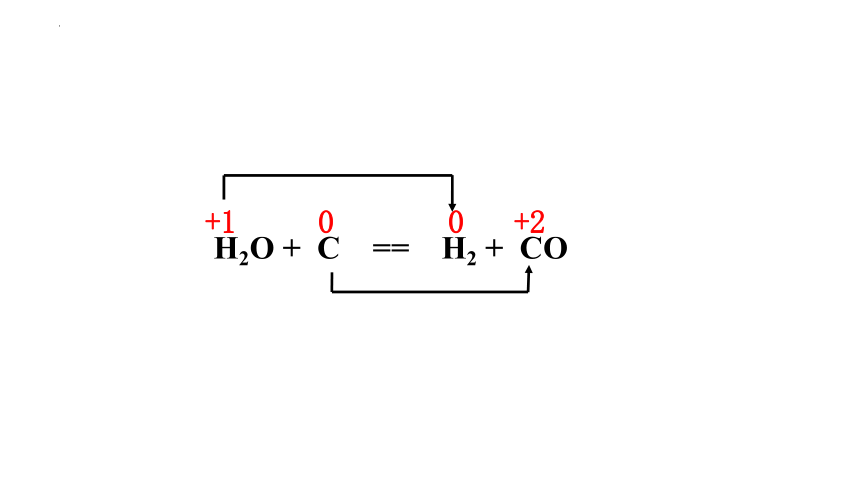
H2O + C == H2 + CO
Zn + 2HCl == ZnCl2 + H2↑
+1 0 0 +2
2e-
0 +1 +2 0
2e-
还原剂
氧化产物
CuO + H2 = Cu + H2O
+2
0
0
+1
化合价降低,得到2e-,
被还原,发生还原反应
化合价升高,失去2e-,
被氧化,发生氧化反应
还原产物
氧化剂:元素化合价降低的反应物。
还原剂:元素化合价升高的反应物。
人教版必修第一册
四、氧化剂和还原剂
氧化剂
氧化产物:还原剂发生氧化反应后的生成物。
还原产物:氧化剂发生还原反应后的生成物。
氧化剂有氧化性,还原剂有还原性。
氧化性:氧化剂>氧化产物
还原性:还原剂>还原产物
口诀:升失氧 ,降得还 ;若问剂,恰相反。
P25
反应物
性质
特征
本质
反应
反应产物
氧化剂
具有氧化性
得电子
化合价降低
发生还原反应(被还原)
还原产物
还原剂
具有还原性
失电子
化合价升高
发生氧化反应
(被氧化)
氧化产物
氧化还原反应中各概念之间的关系
人教版必修第一册
口诀:升失氧 ,降得还 ;若问剂,恰相反。
① 2H2 + O2 = 2H2O
② 2HgO = 2Hg + O2↑
③ WO3 + 3H2 = W+ 3H2O
指出下列反应中氧化剂、还原剂
点燃
高温
氧化剂
还原剂
氧化剂
还原剂
判断依据:看化合价的升降变化
【练习】
氧化剂
还原剂
人教版必修第一册
口诀:升失氧 ,降得还 ;若问剂,恰相反。
常见氧化剂:O2、Cl2;HNO3、浓H2SO4、KMnO4、FeCl3 等
常见还原剂:Al、 Zn、 Fe; C、 H2、CO、KI等
人教版必修第一册
P26
氧化还原反应是一类重要的化学反应,广泛存在生产和生活中
金属的冶炼
绿色植物的光合作用
正影响
正影响
氧化还原反应是一类重要的化学反应,广泛存在生产和生活中
易燃物的自燃
食物的腐败
钢铁的锈蚀
负影响
负影响
负影响
氧化还原反应的意义
氧化还原反应在生产、生活中着广泛的应用。有利也有害,我们应该学会科学、合理地运用化学知识,趋利避害,造福人类。
人教版必修第一册
目前,汽车尾气系统中均安装了催化转化器。在催化转化器中,汽车尾气中的CO和NO在催化剂的作用下发生反应,生成CO2和N2。
思考·讨论
(1)请写出上述反应的化学方程式
该化学反应式的反应物有哪些?
该化学反应式的生成物有哪些?
CO和NO
CO2和N2
2NO + 2CO —— N2 + 2CO2
催化剂
思考·讨论
(2)请分析上述反应是否为氧化还原反应。如果是,请指出反应中的氧化剂和还原剂。
如何判断是否是氧化还原反应?
“升失氧”还原剂
“得降还”氧化剂
有电子转移
有化合价变化
2NO + 2CO —— N2 + 2CO2
催化剂
失去电子,化合价升高,被氧化
得到电子,化合价降低,被还原
氧化剂
还原剂
思考·讨论
(3)催化转化器中发生的反应对减少汽车尾气污染有什么作用?
因此在汽车上安装催化转化器可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)相互反应生成无毒害物质,减少汽车尾气污染。
催化转化器中会发生什么反应?
2NO + 2CO —— N2 + 2CO2
催化剂
NO和CO是有毒有害物质,产物N2和CO2 是无毒无害物质
人教版必修第一册
第一章 物质及其变化
第三节 氧化还原反应
第2课时 氧化剂和还原剂
网
科
学
1、氧化还原反应的本质是 ( )
A、得氧失氧 B、化合价升降
C、有无新物质生成 D、电子转移
D
练一练练一练
2、下列反应中属于氧化还原反应的是( )
A、2HCl + CaCO3 = CaCl2 + H2O + CO2↑
B、H2O + CaO = Ca(OH)2
C、CaCO3 = CaO + CO2 ↑
D、2CO + O2 = 2CO2
点燃
D
人教版必修第一册
高温
a × be-
标价态
正确标出反应前后各元素化合价
明确变价元素的化合价升降关系
连双线
一条线始于反应物中的降价元素,
止于生成物中同种元素
一条线始于反应物中的升价元素,
止于生成物中同种元素
注得失
正确标出反应前后“得到”电子或“失去”电子总数
三、氧化还原反应中电子转移的表示方法
1.双线桥法
表示反应前后同一元素由反应物转化为生成物时电子转移的情况。
基本步骤
人教版必修第一册
化合价改变
的原子个数
化合价
的差值
P23
2Na + Cl2 ══ 2NaCl
点 燃
0 0 +1 -1
失去2×e-
得到2×e-
练一练
用双线桥法标出以下反应的电子转移情况:
Fe + CuSO4 = FeSO4 + Cu
0
+2
+2
0
失去1 × 2e-
得到1 × 2e-
H2O + C == H2 + CO
+1 0 0 +2
得到2×e-
失去1 × 2e-
2.单线桥法 表示反应过程中不同元素原子间的电子转移情况。
标价态
基本步骤
正确标出反应前后各元素化合价
明确变价元素的化合价升降关系
连单线
箭头由失电子的原子指向得电子的原子
注数目
正确标出反应中转移的电子总数
注意:不需要标明“得到”或“失去
人教版必修第一册
P25
2Na + Cl2 ══ 2NaCl
点 燃
0 0 +1 -1
2e-
用单线桥表示下列氧化还原反应的电子转移情况
H2O + C == H2 + CO
Zn + 2HCl == ZnCl2 + H2↑
+1 0 0 +2
2e-
0 +1 +2 0
2e-
还原剂
氧化产物
CuO + H2 = Cu + H2O
+2
0
0
+1
化合价降低,得到2e-,
被还原,发生还原反应
化合价升高,失去2e-,
被氧化,发生氧化反应
还原产物
氧化剂:元素化合价降低的反应物。
还原剂:元素化合价升高的反应物。
人教版必修第一册
四、氧化剂和还原剂
氧化剂
氧化产物:还原剂发生氧化反应后的生成物。
还原产物:氧化剂发生还原反应后的生成物。
氧化剂有氧化性,还原剂有还原性。
氧化性:氧化剂>氧化产物
还原性:还原剂>还原产物
口诀:升失氧 ,降得还 ;若问剂,恰相反。
P25
反应物
性质
特征
本质
反应
反应产物
氧化剂
具有氧化性
得电子
化合价降低
发生还原反应(被还原)
还原产物
还原剂
具有还原性
失电子
化合价升高
发生氧化反应
(被氧化)
氧化产物
氧化还原反应中各概念之间的关系
人教版必修第一册
口诀:升失氧 ,降得还 ;若问剂,恰相反。
① 2H2 + O2 = 2H2O
② 2HgO = 2Hg + O2↑
③ WO3 + 3H2 = W+ 3H2O
指出下列反应中氧化剂、还原剂
点燃
高温
氧化剂
还原剂
氧化剂
还原剂
判断依据:看化合价的升降变化
【练习】
氧化剂
还原剂
人教版必修第一册
口诀:升失氧 ,降得还 ;若问剂,恰相反。
常见氧化剂:O2、Cl2;HNO3、浓H2SO4、KMnO4、FeCl3 等
常见还原剂:Al、 Zn、 Fe; C、 H2、CO、KI等
人教版必修第一册
P26
氧化还原反应是一类重要的化学反应,广泛存在生产和生活中
金属的冶炼
绿色植物的光合作用
正影响
正影响
氧化还原反应是一类重要的化学反应,广泛存在生产和生活中
易燃物的自燃
食物的腐败
钢铁的锈蚀
负影响
负影响
负影响
氧化还原反应的意义
氧化还原反应在生产、生活中着广泛的应用。有利也有害,我们应该学会科学、合理地运用化学知识,趋利避害,造福人类。
人教版必修第一册
目前,汽车尾气系统中均安装了催化转化器。在催化转化器中,汽车尾气中的CO和NO在催化剂的作用下发生反应,生成CO2和N2。
思考·讨论
(1)请写出上述反应的化学方程式
该化学反应式的反应物有哪些?
该化学反应式的生成物有哪些?
CO和NO
CO2和N2
2NO + 2CO —— N2 + 2CO2
催化剂
思考·讨论
(2)请分析上述反应是否为氧化还原反应。如果是,请指出反应中的氧化剂和还原剂。
如何判断是否是氧化还原反应?
“升失氧”还原剂
“得降还”氧化剂
有电子转移
有化合价变化
2NO + 2CO —— N2 + 2CO2
催化剂
失去电子,化合价升高,被氧化
得到电子,化合价降低,被还原
氧化剂
还原剂
思考·讨论
(3)催化转化器中发生的反应对减少汽车尾气污染有什么作用?
因此在汽车上安装催化转化器可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)相互反应生成无毒害物质,减少汽车尾气污染。
催化转化器中会发生什么反应?
2NO + 2CO —— N2 + 2CO2
催化剂
NO和CO是有毒有害物质,产物N2和CO2 是无毒无害物质
