初中化学科粤版九上5.3 二氧化碳的性质和制法 课件(共26张PPT)
文档属性
| 名称 | 初中化学科粤版九上5.3 二氧化碳的性质和制法 课件(共26张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-20 00:00:00 | ||
图片预览





文档简介
(共26张PPT)
5.3 二氧化碳的性质和制法
1.了解大自然中CO2的循环及含量变化对环境的影响,认
识保护自然平衡、人与自然和谐相处的重要性。
2.初步学习在实验室制取CO2的方法。
3.培养分析、加工图片信息的能力。
4.知道CO2的主要性质和用途。
学习目标
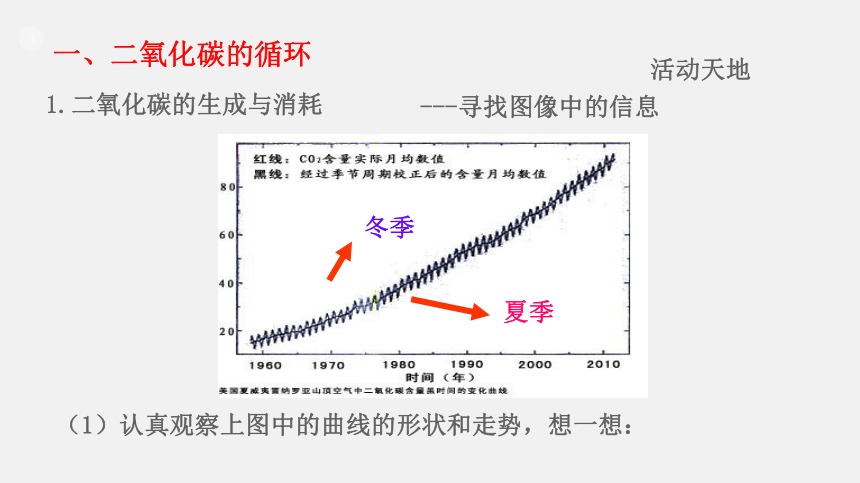
夏季
冬季
---寻找图像中的信息
(1)认真观察上图中的曲线的形状和走势,想一想:
活动天地
一、二氧化碳的循环
1.二氧化碳的生成与消耗
①在同一年度内,大气中二氧化碳的含量是怎样变化的?
②是不是每一年度都在重复这样的变化规律呢?原因是什么呢?
③在不同年度,空气中二氧化碳含量的变化呈现了怎样的趋势?
④你还能从这幅图中获得哪些信息?
长时间的连续观测表明:
同一年度内,大气中二氧化碳的含量是冬季高于夏季,而且这种变化规律每年都在发生,这主要是因为冬季植物的 光合作用减弱,生活取暖燃烧化石燃料,产生大量二氧化 碳的缘故。
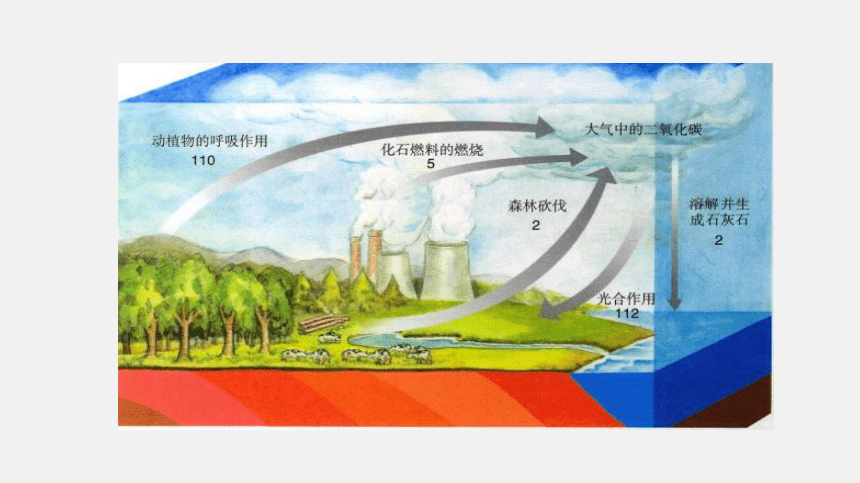
二氧化碳的生成和消耗
(2)分析上图,讨论以下问题。
①产生二氧化碳的主要途径有哪些 共有多少种
②自然界中消耗二氧化碳的主要途径有哪些 共有多少种
③产生的二氧化碳与消耗的二氧化碳相等吗
④从图中可以看出,二氧化碳主要以哪种途径被消耗
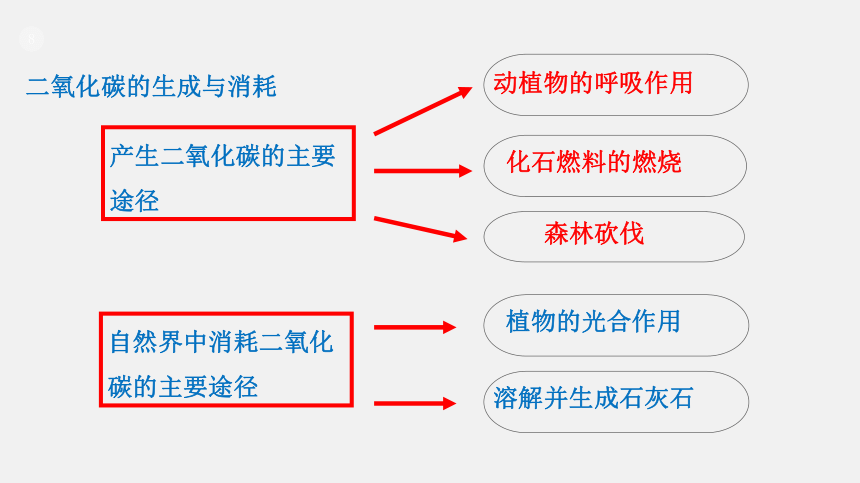
产生二氧化碳的主要途径
自然界中消耗二氧化碳的主要途径
动植物的呼吸作用
化石燃料的燃烧
森林砍伐
溶解并生成石灰石
植物的光合作用
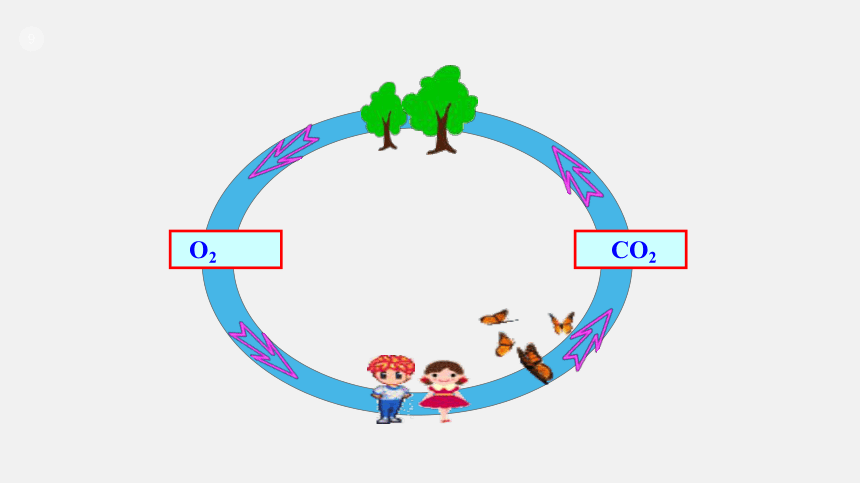
二氧化碳的生成与消耗
CO2
O2
2.大气中CO2含量增加对自然环境的影响
(1)大气中CO2含量增加对自然环境有何影响?
观点1.科学家普遍认为,大气中二氧化碳含量的增加导致全球变暖,引起“温室效应”,从而使两极冰川融化,海平面升高,海水上涨,许多沿海城市、岛屿或低洼地区将面临被海水淹没的危险。
观点2.一些科学家认为目前没有任何确切证据说明CO2含量的增加与天气的变化有直接的关系。
观点3.也有科学家认为地球演化过程中的另一个“冰期”即将到来,二氧化碳含量增加导致的全球变暖对延缓“冰期”的到来具有积极作用。
(2)以上观点你支持哪一点?如何减少二氧化碳的排放量
减少二氧化碳排放量的措施:
①减少煤、石油、天然气等化石燃料的使用;
②开发利用太阳能、地热能、风能、氢能等清洁能源;
③大力植树造林,严禁乱砍滥伐。
多识一点
节能减排:节约能源、降低能源消耗、减少污染物排放。
低碳生活:把生活作息时所耗用的能量要尽量减少,从而减低二氧低碳的排放量。
我已经知道:
二氧化碳既不能 ,也不 ,这属于它的 性质。
化学
燃烧
支持燃烧
(1)常用药品及反应原理:在实验室里,二氧化碳常用稀盐酸和大理石或石灰石反应制得,化学方程式如下:
二、二氧化碳的性质
CaCO3 + 2HCl ==== CaCl2 + H2O + CO2↑
碳酸钙 盐酸 氯化钙 水 二氧化碳
1.二氧化碳的制取
CO2的物理性质
通常情况下,二氧化碳是一种无色无味的气体,它还有固态和液态。在一定温度和压强条件下可以实现以下转化:
加 压
降 温
加 压
降 温
固态二氧化碳
俗称“干冰”,易升华,常作“制冷剂”
液态二氧化碳
无色
CO 2(气体)
无 色、无味
向一个收集满二氧化碳气体的塑料瓶中加入约二分之一体积的水,立即旋紧瓶盖,振荡,观察现象。
CO2的溶解性如何?
我想知道:
实验1
证明CO2能否溶于水。
一个装有蒸馏水的塑料瓶、一个装满CO2的塑料瓶
塑料瓶变瘪了
实验目的:
实验用品:
实验方案:
实验现象:
实验结论:
二氧化碳能溶于水
你知道了吗?
当你打开一碳酸饮料时是否可看到下图的现象 结合所学知识,你能解释产生这种现象的原因吗?
这是因为CO2能溶于水,通常1 L水约溶解1 L CO2,压强越大它在水中的溶解量越多。生产汽水等碳酸饮料时是将CO2在加压的情况将它压入饮料瓶中的,当打开饮料瓶时,压强减小,它在水中溶解量也会减少,所以会看到许多气泡从瓶口冒出。
我还想知道:
CO2的密度如何?
实验2
实验目的:
实验用品:
实验方案:
实验现象:
实验结论:
探究CO2的密度与空气密度大小。
一只大烧杯、一个铁皮架、两只相同大小的蜡烛、火柴、一个装满CO2的集气瓶
下层蜡烛先熄灭,上层蜡烛后熄灭
二氧化碳的密度比空气的密度大。
在大烧杯中放置一个铁皮架,架上固定两支点燃的蜡烛,将一瓶二氧化碳慢慢倒入烧杯中
在印度尼西亚的爪哇岛,有一个奇怪的山谷,当有人带着狗走进峡谷时,人能顺利经过,但狗却昏死过去,当人弯腰救狗时,人也会昏倒,于是人们便称此谷为“鬼谷”,这个鬼是什么呢?
我能解谜:
CO2
我来总结:
CO2的物理性质
1.CO2通常是一种无色无味的气体,它还有固态和液态。
2.CO2能溶于水。
3.CO2密度比空气大。
CO2的化学性质
活动探究1:CO2溶于水是物理变化还是化学变化?
实验操作 实验现象 实验结论
一种新物质使石蕊变色
二氧化碳不能使 石蕊变色
水不能使石蕊变色
不变色
不变色
变 红
知识储备:
石蕊是一种色素,紫色的石蕊试剂遇酸时变成红色。
研究证实:二氧化碳能与水反应生成碳酸,碳酸使紫色 石蕊试剂变红
CO2 + H2O ===== H2CO3(碳酸)
新物质是
???
酸
且碳酸不稳定,易分解成二氧化碳和水:
H2CO3 == H2O + CO2
活动探究2:澄清石灰水检验CO2的原理。
实验方案
实验现象
实验结论
澄清石灰水变浑浊
CO2与石灰水反应生成白色沉淀:
向澄清石灰水中通入CO2
我来总结:
CO2的化学性质
1.既不能燃烧,也不能支持燃烧;不能供给呼吸。
2.与水反应生成碳酸:
CO2 + H2O === H2CO3
3.与石灰水反应生成白色沉淀碳酸钙:
碳酸不稳定易分解:
H2CO3 == H2O + CO2
1.CO2在下列变化中只发生物理变化的是( )
A.溶于水中 B.溶于石灰水中
C.进行光合作用 D.制成干冰
2.鉴别氢气、氧气和二氧化碳三种气体最简便的方法是( )
A.分别通入澄清石灰水
B.测定三种气体的密度
C.用燃着的木条放在集气瓶口
D.试验三种气体的溶解性
D
C
练一练:
5.3 二氧化碳的性质和制法
1.了解大自然中CO2的循环及含量变化对环境的影响,认
识保护自然平衡、人与自然和谐相处的重要性。
2.初步学习在实验室制取CO2的方法。
3.培养分析、加工图片信息的能力。
4.知道CO2的主要性质和用途。
学习目标
夏季
冬季
---寻找图像中的信息
(1)认真观察上图中的曲线的形状和走势,想一想:
活动天地
一、二氧化碳的循环
1.二氧化碳的生成与消耗
①在同一年度内,大气中二氧化碳的含量是怎样变化的?
②是不是每一年度都在重复这样的变化规律呢?原因是什么呢?
③在不同年度,空气中二氧化碳含量的变化呈现了怎样的趋势?
④你还能从这幅图中获得哪些信息?
长时间的连续观测表明:
同一年度内,大气中二氧化碳的含量是冬季高于夏季,而且这种变化规律每年都在发生,这主要是因为冬季植物的 光合作用减弱,生活取暖燃烧化石燃料,产生大量二氧化 碳的缘故。
二氧化碳的生成和消耗
(2)分析上图,讨论以下问题。
①产生二氧化碳的主要途径有哪些 共有多少种
②自然界中消耗二氧化碳的主要途径有哪些 共有多少种
③产生的二氧化碳与消耗的二氧化碳相等吗
④从图中可以看出,二氧化碳主要以哪种途径被消耗
产生二氧化碳的主要途径
自然界中消耗二氧化碳的主要途径
动植物的呼吸作用
化石燃料的燃烧
森林砍伐
溶解并生成石灰石
植物的光合作用
二氧化碳的生成与消耗
CO2
O2
2.大气中CO2含量增加对自然环境的影响
(1)大气中CO2含量增加对自然环境有何影响?
观点1.科学家普遍认为,大气中二氧化碳含量的增加导致全球变暖,引起“温室效应”,从而使两极冰川融化,海平面升高,海水上涨,许多沿海城市、岛屿或低洼地区将面临被海水淹没的危险。
观点2.一些科学家认为目前没有任何确切证据说明CO2含量的增加与天气的变化有直接的关系。
观点3.也有科学家认为地球演化过程中的另一个“冰期”即将到来,二氧化碳含量增加导致的全球变暖对延缓“冰期”的到来具有积极作用。
(2)以上观点你支持哪一点?如何减少二氧化碳的排放量
减少二氧化碳排放量的措施:
①减少煤、石油、天然气等化石燃料的使用;
②开发利用太阳能、地热能、风能、氢能等清洁能源;
③大力植树造林,严禁乱砍滥伐。
多识一点
节能减排:节约能源、降低能源消耗、减少污染物排放。
低碳生活:把生活作息时所耗用的能量要尽量减少,从而减低二氧低碳的排放量。
我已经知道:
二氧化碳既不能 ,也不 ,这属于它的 性质。
化学
燃烧
支持燃烧
(1)常用药品及反应原理:在实验室里,二氧化碳常用稀盐酸和大理石或石灰石反应制得,化学方程式如下:
二、二氧化碳的性质
CaCO3 + 2HCl ==== CaCl2 + H2O + CO2↑
碳酸钙 盐酸 氯化钙 水 二氧化碳
1.二氧化碳的制取
CO2的物理性质
通常情况下,二氧化碳是一种无色无味的气体,它还有固态和液态。在一定温度和压强条件下可以实现以下转化:
加 压
降 温
加 压
降 温
固态二氧化碳
俗称“干冰”,易升华,常作“制冷剂”
液态二氧化碳
无色
CO 2(气体)
无 色、无味
向一个收集满二氧化碳气体的塑料瓶中加入约二分之一体积的水,立即旋紧瓶盖,振荡,观察现象。
CO2的溶解性如何?
我想知道:
实验1
证明CO2能否溶于水。
一个装有蒸馏水的塑料瓶、一个装满CO2的塑料瓶
塑料瓶变瘪了
实验目的:
实验用品:
实验方案:
实验现象:
实验结论:
二氧化碳能溶于水
你知道了吗?
当你打开一碳酸饮料时是否可看到下图的现象 结合所学知识,你能解释产生这种现象的原因吗?
这是因为CO2能溶于水,通常1 L水约溶解1 L CO2,压强越大它在水中的溶解量越多。生产汽水等碳酸饮料时是将CO2在加压的情况将它压入饮料瓶中的,当打开饮料瓶时,压强减小,它在水中溶解量也会减少,所以会看到许多气泡从瓶口冒出。
我还想知道:
CO2的密度如何?
实验2
实验目的:
实验用品:
实验方案:
实验现象:
实验结论:
探究CO2的密度与空气密度大小。
一只大烧杯、一个铁皮架、两只相同大小的蜡烛、火柴、一个装满CO2的集气瓶
下层蜡烛先熄灭,上层蜡烛后熄灭
二氧化碳的密度比空气的密度大。
在大烧杯中放置一个铁皮架,架上固定两支点燃的蜡烛,将一瓶二氧化碳慢慢倒入烧杯中
在印度尼西亚的爪哇岛,有一个奇怪的山谷,当有人带着狗走进峡谷时,人能顺利经过,但狗却昏死过去,当人弯腰救狗时,人也会昏倒,于是人们便称此谷为“鬼谷”,这个鬼是什么呢?
我能解谜:
CO2
我来总结:
CO2的物理性质
1.CO2通常是一种无色无味的气体,它还有固态和液态。
2.CO2能溶于水。
3.CO2密度比空气大。
CO2的化学性质
活动探究1:CO2溶于水是物理变化还是化学变化?
实验操作 实验现象 实验结论
一种新物质使石蕊变色
二氧化碳不能使 石蕊变色
水不能使石蕊变色
不变色
不变色
变 红
知识储备:
石蕊是一种色素,紫色的石蕊试剂遇酸时变成红色。
研究证实:二氧化碳能与水反应生成碳酸,碳酸使紫色 石蕊试剂变红
CO2 + H2O ===== H2CO3(碳酸)
新物质是
???
酸
且碳酸不稳定,易分解成二氧化碳和水:
H2CO3 == H2O + CO2
活动探究2:澄清石灰水检验CO2的原理。
实验方案
实验现象
实验结论
澄清石灰水变浑浊
CO2与石灰水反应生成白色沉淀:
向澄清石灰水中通入CO2
我来总结:
CO2的化学性质
1.既不能燃烧,也不能支持燃烧;不能供给呼吸。
2.与水反应生成碳酸:
CO2 + H2O === H2CO3
3.与石灰水反应生成白色沉淀碳酸钙:
碳酸不稳定易分解:
H2CO3 == H2O + CO2
1.CO2在下列变化中只发生物理变化的是( )
A.溶于水中 B.溶于石灰水中
C.进行光合作用 D.制成干冰
2.鉴别氢气、氧气和二氧化碳三种气体最简便的方法是( )
A.分别通入澄清石灰水
B.测定三种气体的密度
C.用燃着的木条放在集气瓶口
D.试验三种气体的溶解性
D
C
练一练:
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
