浙江省杭州市滨江区2022-2023学年八年级下学期期末教学质量调研科学试题(word版,含答案)
文档属性
| 名称 | 浙江省杭州市滨江区2022-2023学年八年级下学期期末教学质量调研科学试题(word版,含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 619.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-07-23 00:00:00 | ||
图片预览




文档简介
2022学年第二学期期末教学质量检测
八年级科学
考生须知:
1.本试卷满分160分,考试时间120分钟。
2.答题前,必须在答题纸指定位置填写学校、班级、姓名、座位号。
3.必须在答题卷对应答题位置上答题,写在其他地方无效。答题方式详见答题纸上的说明。
4.不能使用计算器,全卷g=10N/kg。
本卷可能用到的相对原子质量:C﹕12 H﹕1 O﹕16 S﹕32 N﹕14 Fe﹕56 Cl﹕35.5 Ca﹕40
试题卷
一、选择题(本题有20小题,每小题3分,共60分,请选出一个符合题意的正确选项)
1.16O和18O是氧元素的两种同位素原子,则由 16O构成的氧分子和由18O构成的氧分子,不同的是( )
A.质子数 B.中子数 C.电子数 D.氧原子个数
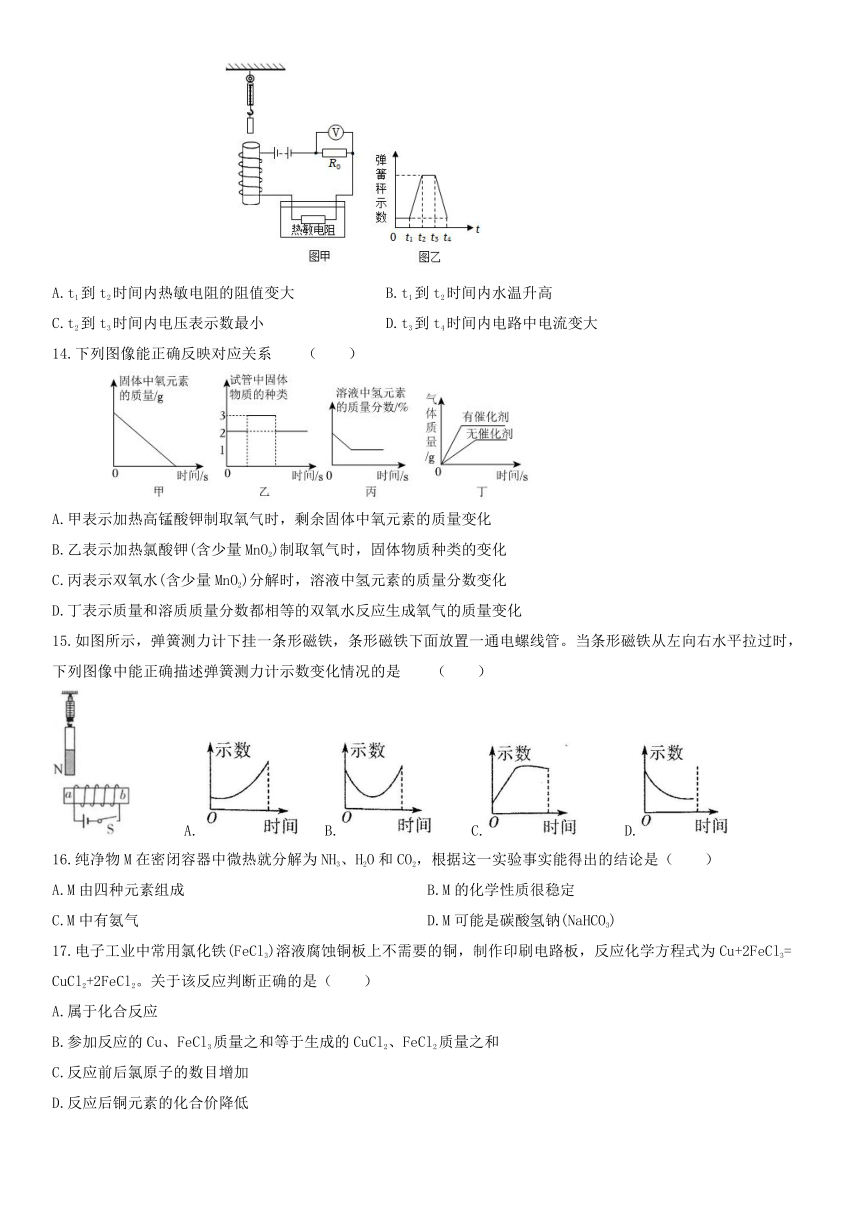
2.下列图示不属于模型的是( )
A.足球烯 B.电路图 C.质量体积关系图 D.有毒标志
3.下列有关叶片及其蒸腾作用的叙述,正确的是 ( )
A.叶片的上下表皮由一层绿色的表皮细胞组成 B.气孔是由保卫细胞控制其开闭
C.植物吸收的水分有少量通过蒸腾作用散失 D.蒸腾作用散失的水主要靠筛管运输
4.如图是条形磁体的磁感线分布,图中的E、F、P、Q四点,磁场最强的是 ( )
A.E点 B.F点 C.P点 D.Q点
5.下列关于土壤非生命物质探究的实验中,操作正确的是 ( )
A.加热土壤 B.过滤土壤浸出液 C.称量土壤 D.蒸发土壤浸出液
6.世界上各种物质都是由一些最基本的元素组成的。下列说法不正确的是 ( )
A.元素在地壳中的分布是不均匀的,地壳中最多的金属元素是铝
B.海水中有大量的氯化钠,因此海水中含量最高的是氯元素
C.放射性元素对人体有害,但利用放射性可以检查和治疗一些疾病
D.人体内也含有一些有害元素,如镉、汞、铅等,这与食物、水体及大气的污染有关
7.2022年北京冬奥会上,我国滑雪运动员所用的滑雪杖材质为铝合金。如图是铝在元素周期表中的相关信息,其中不能直接体现的信息是 ( )
A.原子序数 B.金属元素 C.中子数 D.相对原子质量
8.请据图分析,下列说法正确的是 ( )
A.图甲表示血液流经人体肌肉组织细胞后,氧气含量的变化
B.图乙表示菜豆种子萌发及幼苗长成植物体的过程中,有机物含量的变化
C.图丙中A点显示此时某绿色植物没有进行光合作用和呼吸作用
D.图丁曲线A→B段表示肺完成一次吸气过程
9.在杭州市余杭区仁和街道新桥村有一棵千年树龄的古银杏树,它的“树心”已经朽烂,变成了一棵“空心树”。可是,这棵古树在当地政府和村民的保护下还是枝繁叶茂、生命力旺盛。由此推断,朽烂掉的“树心”是这棵树的( )
A.全部韧皮部 B.全部木质部 C.全部树皮 D.部分木质部
10.下列有关物质燃烧时观察到的现象的叙述中,正确的是 ( )
A.硫在氧气中燃烧,发出淡蓝色的火焰,生成有刺激性气味的气体
B.木炭在氧气中燃烧,发出白光,生成能使澄清石灰水变浑浊的气体
C.红磷在氧气中燃烧,放出大量热,产生大量白雾
D.铁丝在氧气中燃烧,火星四射,生成氧化铁
11.2020年2月4日,中国工程院院土李兰娟的研究团队发现:达芦那韦(化学式为C27H37N3O7S)能显著抑制新冠肺炎病毒复制。下列有关说法错误的是 ( )
A.达芦那韦由五种元素组成 B.达芦那韦由分子构成
C.一个达芦那韦分子由75个原子构成 D.达芦那韦中C和H两种元素的质量比为27﹕37
12.小滨对一些科学符号中数字的含义有如下的理解,其中正确的是 ( )
A.CO2:可表示二氧化碳气体中有2个氧原子 B.CO32-:可表示一个碳酸根离子带2个单位负电荷
C.2C:可表示两种碳单质 D.Al3+:一个铝原子带三个单位的正电荷
13.小滨利用“热敏电阻的阻值会随温度的升高而减小”的性质,设计了判断水温变化的装置,其工作原理如图甲所示,电源、热敏电阻、电磁铁、定值电阻R0由导线连接成一个串联电路,在线圈的上方固定一个弹簧测力计,其下端挂一铁块。实验时把热敏电阻放入盛水的烧杯中,水温的变化会引起弹簧测力计示数发生变化:如图乙所示为某次实验中弹簧测力计读数随时间变化的图像。下列说法正确的是( )
A.t1到t2时间内热敏电阻的阻值变大 B.t1到t2时间内水温升高
C.t2到t3时间内电压表示数最小 D.t3到t4时间内电路中电流变大
14.下列图像能正确反映对应关系 ( )
A.甲表示加热高锰酸钾制取氧气时,剩余固体中氧元素的质量变化
B.乙表示加热氯酸钾(含少量MnO2)制取氧气时,固体物质种类的变化
C.丙表示双氧水(含少量MnO2)分解时,溶液中氢元素的质量分数变化
D.丁表示质量和溶质质量分数都相等的双氧水反应生成氧气的质量变化
15.如图所示,弹簧测力计下挂一条形磁铁,条形磁铁下面放置一通电螺线管。当条形磁铁从左向右水平拉过时,下列图像中能正确描述弹簧测力计示数变化情况的是 ( )
A. B. C. D.
16.纯净物M在密闭容器中微热就分解为NH3、H2O和CO2,根据这一实验事实能得出的结论是( )
A.M由四种元素组成 B.M的化学性质很稳定
C.M中有氨气 D.M可能是碳酸氢钠(NaHCO3)
17.电子工业中常用氯化铁(FeCl3)溶液腐蚀铜板上不需要的铜,制作印刷电路板,反应化学方程式为Cu+2FeCl3=
CuCl2+2FeCl2。关于该反应判断正确的是( )
A.属于化合反应
B.参加反应的Cu、FeCl3质量之和等于生成的CuCl2、FeCl2质量之和
C.反应前后氯原子的数目增加
D.反应后铜元素的化合价降低
18.对下列实验中出现的异常现象分析合理的是 ( )
选项 异常现象 分析
A 制取CO2气体时,始终收集不到CO2 收集CO2的集气瓶没盖玻璃片
B 利用排水法收集氧气,但是O2不纯 通入氧气前集气瓶内水没有装满
C 细铁丝在氧气中燃烧时,集气瓶瓶底炸裂 由于引燃的火柴太长了
D 测定空气中氧气含量时,进入集气瓶中的水过少 红磷过量
19.小江家的家庭电路如图所示,小江闭合开关S,电灯正常发光。分别将台灯与洗衣机插入P、Q插座,都闭合开关,发现它们不能工作。于是小江只拔下台灯的插头,用测电笔检测P插座,左右两孔都能使测电笔的氛管发光,则小江家电路出现的故障可能是 ( )
A.进户零线断路 B.AB间断路 C.进户火线断路 D.BC间断路
20.逻辑推理是科学学习中常用的思维方法,下列推理合理的是( )
A.因为离子是带电的粒子,所以带电的粒子就是离子
B.因为单质中只含一种元素,所以只含一种元素的物质就是单质
C.因为化合物含有多种元素,所以含多种元素的物质一定都是化合物
D.因为水电解只得到氢气和氧气,所以水一定由氢、氧两种元素组成
二、简答题(本题有9小题,共34分)
21.(5分)用化学用语填空:①碘单质化学式为 ;②氦气的化学式为 ;
③4个铵根离子 ;④n个硫酸根离子 ;⑤将“神舟十号”飞船送入太空的是“长征二号”F运载火箭,火箭工作中发生的反应为C2H8N2+2R=3N2+4H2O+2CO2,其中R的化学式是 。
22.(3分)下列常见物质:①氧气;②二氧化碳;③铁;④汞(水银);⑤水;⑥氯化钠。其中由原子直接构成的有
,由分子构成的有 ,由离子构成的有 (填序号)。
23.(3分)家庭电路中,触电是人直接接触 造成的。安全用电原则是:不接触 ,
不靠近 。
24.(4分)如图是探究“怎样产生感应电流”的实验装置。ab是一根导体,通过导线、开关连接在灵敏电流计的两接线柱上。
(1)本实验中,如果 ,我们就认为有感应电流产生。
(2)闭合开关后,假设导线不动,磁铁左右水平运动,电路 感应电流(选填“有”或“无”)。
(3)闭合开关后,假设磁铁不动,导体向纸面里外方向运动,电路 感应电流(选填“有”或“无”)。
25.(4分)追寻科学家的足迹,一起了解氧气的发现史。(汞蒸气和汞的化合物均有毒性)
(1)1773年,舍勒用加热分解硝酸钾、氧化汞、碳酸银等物质都能制得氧气。从物质组成角度分析:加热上述物质均可制得氧气的原因是 。
(2)之后,法国化学家拉瓦锡用如图装置,把少量的汞放入如图所示的曲颈瓶中,连续加热12天后,发现银白色的液态汞变成了红色的粉末,容器中空气的体积大约减少了五分之一。随后他又将产生的红色粉末收集于另一容器中并加强热,发现又生成了汞和另一种气体。这种气体的体积恰好等于之前曲颈瓶中空气减小的体积。
拉瓦锡通过定量研究的方法发现了空气中的氧气和氮气。该实验中选择使用汞的优点有 。(可多选)
A.实验过程中没有污染 B.在汞槽中起到液封的作用
C.生成的化合物加热分解又能得到汞和氧气 D.能将密闭装置内空气中的氧气几乎耗尽
26.(6分)“杂交水稻之父”袁隆平院士经过多年的努力,利用野生稻培育出了具有许多优良性状的“超级杂交水稻”,并研究出能在盐碱地上种植的“海水稻”。
(1)“超级杂交水稻”的茎不能明显增粗是因为其茎中没有 (填茎的结构名称)。
(2)耐盐碱水稻根毛细胞的细胞液浓度 (选填“小于”、“等于”或“大于”)所生长的土壤溶液浓度时,根毛细胞吸水,吸收的水大部分用于 作用。
27.(2分)下表是教材中元素周期表的一部分,除标出的元素外,表中的数字编号①—④各表示一种元素。请回答问题。
(1)数字编号②表示的元素是 (填符号)。
(2)③代表的元素与Mg元素形成的化合物的化学式为 。
28.(3分)小滨对教材中“探究二氧化碳性质”的相关实验装置进行了如图的改进。当通入二氧化碳一段时间后,可观察到试管A内溶液的颜色呈 色,试管B中出现的现象是 ,烧杯C中 (选填“上面”或“下面”)的蜡烛先熄灭。
29.(4分)氮氧化物(如NO2、NO等)进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾。因此必须对含有氮氧化物的废气进行处理。
(1)用氢氧化钠溶液可吸收废气中的氮氧化物。反应的化学方程式为:NO2+NO+2NaOH=2NaNO2+H2O,产物NaNO2中N元素的化合价为 ;已知“HNO2”读作“亚硝酸”,则NaNO2的名称为 。
(2)汽车尾气中含有NO和CO,消除这两种物质对大气污染的方法是安装催化转化器,使它们发生反应生成N2和CO2,该反应的化学方程式为 。
三、实验探究题(本题有4小题,共34分)
30.(8分)小滨偶然发现月季茎折断后仍能成活(如图甲),想探究月季茎折断后什么情况下还能成活?他将生理状况相似的20株月季分成五组,进行如下表所示的处理。(处理方法和位置如图乙、丙所示,云母片能阻断物质的运输。)
组别 处理方法
1 不做处理
2 在B处韧皮部环割一圈
3 在B处韧皮部环割半圈
4 在A处木质部切断并插入云母片(不影响韧皮部功能)
5 在B处木质部切断并插入云母片(不影响韧皮部功能)
(1)第1组不做处理是为了作为 。
(2)结合以上信息判断,一段时间后月季植株一定死亡的实验组有 (填组别)。
(3)为探究月季折断程度是否影响月季的存活,应增加一组(第6组)实验的处理方法是
,并与第5组形成对照。
(4)经以上6组实验可以得出折断的月季是否仍能存活与月季折断的程度和 有关。
31.(10分)实验室常用下列装置来制取氧气:
(1)请写出以下实验器材的名称:a ,b 。用双氧水和二氧化锰来制取干燥的氧气时,可选用的发生和收集装置是 (填序号)。
(2)将产生的氧气分别通入G、H装置,通过实验现象说明可燃物的燃烧必备的一个条件是 。
(3)实验室常用氯化铵固体与碱石灰固体共热来制取氨气,它们发生反应的化学方程式是:2NH4Cl+Ca(OH)2CaCl2
+2NH3↑+2H2O。常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水。根据以上信息,请你判断制取并收集氨气时应选择的装置是 (填序号)。
32.(8分)某科学小组为探究绿色植物在维持碳——氧平衡中的作用,设计了如图一所示的密闭透明的实验装置(此实验忽略温度等因素对装置内气体体积等的影响):将图一装置放在室外培养24小时,连接氧气检测仪,测得装置内一昼夜氧气浓度的变化曲线如图二。请据图分析作答:
(1)分析图一和图二可知:随着时间推移,红墨水滴的位置在一天中 时移动到最右端(填数字);判断该植物在24小时后积累了有机物,依据是曲线中A点低于 点(填图中字母);
(2)请写出在图二AF段中,该植物一直进行的生理活动是 (选填“光合作用”或“呼吸作用”);
(3)若用图一装置继续探究光合作用是否需要水分,则对该绿色植物进行的处理是
。
33.(8分)在“探究电磁铁磁性强弱与电流大小关系”的实验中,小明用绝缘细线将电磁铁M悬挂在铁架台上,并保持它与软铁块P的距离不变。以下是他的部分实验步骤:
①断开开关S,按图组装实验电路,将滑动变阻器的滑片置于最右端。用已调零的电子测力计测出软铁块P对测力计的压力F0并记录在表格中;
②闭合开关S,调节滑动变阻器的滑片到适当位置,读出电流表的示数I和电子测力计的示数F,并将I、F的数据记录在表格中;
③仿照步骤②再进行两次实验。
(1)实验中小明是通过 来判定电磁铁磁性强弱的。
(2)闭合开关S后,电磁铁下端的磁极为 (选填“N”或“S”)极。
(3)由表中数据可以得出的实验结论是: 。
(4)本实验中,滑动变阻器除了保护电路的作用外,还起到 的作用。
四、分析计算题(本题有4小题,共32分)
34.(6分)我国科研团队通过电催化结合生物合成的方式,实现了二氧化碳合成葡萄糖和脂肪酸。第1步是将二氧化碳还原到一氧化碳,第2步是一氧化碳转化为高纯的乙酸,第3步是在乙酸中加入经过基因编辑之后的酵母进行发酵,最后得到葡萄糖和脂肪酸。如图所示是1、2两步过程,请回答下列问题。
(1)两步反应前后,物质的总质量不改变,请从微观上解释: ;
(2)二氧化碳和一氧化碳化学性质不同的根本原因是 ;
(3)请写出乙酸中碳、氢、氧元素质量比 。
35.(8分)为了检测实验室中石灰石样品中碳酸钙的含量,某同学用溶质质量分数相同的盐酸与样品进行了四组实验测定(样品中的杂质不溶于水,且不与盐酸反应),测得数据如表。试回答:
甲 乙 丙 丁
所取石灰石质量/g 10.0 10.0 10.0 10.0
加入盐酸质量/g 20.0 30.0 45.0 50.0
剩余固体质量/g 6.0 4.0 2.0 2.0
(1)石灰石样品中碳酸钙的质量分数是 ;
(2)各组充分反应后,盐酸有剩余的实验组别是 ;
(3)实验所用稀盐酸的溶质质量分数是多少 (写出计算过程)
36.(8分)纯电动汽车是一种采用蓄电池作为唯一动力源的汽车,电池的安全性主要体现在对其温度的控制上,当某组电池温度过高时,立即启动制冷系统进行降温,图甲是小滨设计的模拟控温装置示意图,电磁继电器与热敏电阻Rt、滑动变阻器RP串联接在电压为6V的电源两端。当电磁铁线圈(电阻不计)中的电流I大于或等于25mA时,衔铁被吸合,热敏电阻置于温度监测区域,其阻值Rt与温度t的关系如图乙所示,滑动变阻器的最大阻值为200Ω。
(1)图甲中应将b端与 端相连;
(2)若设置电池温度为60℃时启动制冷系统,则滑动变阻器阻值应为多少?
(3)若要提高启动温度,RP接入电路的阻值应该怎么调节?并简要说明理由。
37.(10分)在杭州亚运村西北侧的“世纪变”,成立了全省首个“电力能源碳中和技术示范基地”。这座变电站获得了权威机构颁发的《碳中和证书》,节能减碳成效已经获得认可,以上措施可缓解的环境问题是 。如图甲是小滨验证该问题的实验装置,在 (填“阳光”或“黑暗”)下一段时间后,可观察到水柱向 (填“左”或“右”)移动。
此外,根据研究发现海洋吸收二氧化碳有三种方式(图乙)。
图甲 图乙
(1)自然溶解:大气中的二氧化碳能不断地溶解到海水中。研究表明,海水温度越低,单位体积溶解的二氧化碳越多。一年四季中,单位体积海水中溶解二氧化碳最多的是 季。
(2)植物固碳:近海滩涂上的红树林、海洋浮游植物等通过光合作用吸收二氧化碳,最终这些碳元素随着植物残体沉积到海底。植物固碳只能发生在海洋的浅层,超过一定深度不能发生,其原因是
。
(3)碳酸盐泵:贝壳类、珊瑚等海洋生物将碳元素以碳酸钙的形式沉积起来。某地贝壳堤储存了约4亿吨贝壳,其中95%为碳酸钙,则该地贝壳堤固定了 亿吨碳元素?
2022学年第二学期期末教学质量检测参考答案
一、选择题(本题有20小题,每小题3分,共60分,请选出一个符合题意的正确选项)
题号 1 2 3 4 5 6 7 8 9 10
答案 B D B A D B C D D B
题号 11 12 13 14 15 16 17 18 19 20
答案 D B B B A A B B B D
二、简答题(本题有9小题,共34分)
21.(5分)①I2;②He;③4NH4+;④nSO42-;⑤N2O4。
22.(3分)③④;①②⑤;⑥。
23.(3分)火线;低压带电体;高压带电体。
24.(4分)(1)灵敏电流计指针发生偏转;(2)有;(3)无。
25.(4分)(1)这些物质中都含有氧元素;(2)BCD。
26.(4分)(1)形成层;(2)蒸腾作用。
27.(2分)(1)Li;(2)MgO。
28.(3分)红;澄清石灰水变浑浊;下面。
29.(4分)(1)+3;亚硝酸钠;(2)。
三、实验探究题(本题有4小题,共34分)
30.(8分)(1)对照;(2)2、5;(3)在B处将部分木质部切断并插入云母片(不影响韧皮部功能);(4)折断的位置。
31.(10分)(1)铁架台;长颈漏斗;BE;(2)温度达到可燃物的着火点;(3)AD。
32.(8分)(1)18;F;(2)呼吸作用;(3)将一个叶片割断主叶脉,导管被切断,这样叶片前部分就得不到从根运输来的水分,叶片后部分就能得到水分。因此,叶片前后两部分就形成以水为唯一变量的对照实验。
33.(8分)(1)电子测力计示数;(2)N;(3)线圈匝数一定时,通过电磁铁的电流越大,电磁铁磁性越强;(4)改变电流大小。
四、分析计算题(本题有4小题,共32分)
37.(10分)温室效应;阳光;左;(1)冬;(2)海洋超过一定深度,光照弱,植物光合作用弱,无法维持生长;(3)0.456亿。
八年级科学
考生须知:
1.本试卷满分160分,考试时间120分钟。
2.答题前,必须在答题纸指定位置填写学校、班级、姓名、座位号。
3.必须在答题卷对应答题位置上答题,写在其他地方无效。答题方式详见答题纸上的说明。
4.不能使用计算器,全卷g=10N/kg。
本卷可能用到的相对原子质量:C﹕12 H﹕1 O﹕16 S﹕32 N﹕14 Fe﹕56 Cl﹕35.5 Ca﹕40
试题卷
一、选择题(本题有20小题,每小题3分,共60分,请选出一个符合题意的正确选项)
1.16O和18O是氧元素的两种同位素原子,则由 16O构成的氧分子和由18O构成的氧分子,不同的是( )
A.质子数 B.中子数 C.电子数 D.氧原子个数
2.下列图示不属于模型的是( )
A.足球烯 B.电路图 C.质量体积关系图 D.有毒标志
3.下列有关叶片及其蒸腾作用的叙述,正确的是 ( )
A.叶片的上下表皮由一层绿色的表皮细胞组成 B.气孔是由保卫细胞控制其开闭
C.植物吸收的水分有少量通过蒸腾作用散失 D.蒸腾作用散失的水主要靠筛管运输
4.如图是条形磁体的磁感线分布,图中的E、F、P、Q四点,磁场最强的是 ( )
A.E点 B.F点 C.P点 D.Q点
5.下列关于土壤非生命物质探究的实验中,操作正确的是 ( )
A.加热土壤 B.过滤土壤浸出液 C.称量土壤 D.蒸发土壤浸出液
6.世界上各种物质都是由一些最基本的元素组成的。下列说法不正确的是 ( )
A.元素在地壳中的分布是不均匀的,地壳中最多的金属元素是铝
B.海水中有大量的氯化钠,因此海水中含量最高的是氯元素
C.放射性元素对人体有害,但利用放射性可以检查和治疗一些疾病
D.人体内也含有一些有害元素,如镉、汞、铅等,这与食物、水体及大气的污染有关
7.2022年北京冬奥会上,我国滑雪运动员所用的滑雪杖材质为铝合金。如图是铝在元素周期表中的相关信息,其中不能直接体现的信息是 ( )
A.原子序数 B.金属元素 C.中子数 D.相对原子质量
8.请据图分析,下列说法正确的是 ( )
A.图甲表示血液流经人体肌肉组织细胞后,氧气含量的变化
B.图乙表示菜豆种子萌发及幼苗长成植物体的过程中,有机物含量的变化
C.图丙中A点显示此时某绿色植物没有进行光合作用和呼吸作用
D.图丁曲线A→B段表示肺完成一次吸气过程
9.在杭州市余杭区仁和街道新桥村有一棵千年树龄的古银杏树,它的“树心”已经朽烂,变成了一棵“空心树”。可是,这棵古树在当地政府和村民的保护下还是枝繁叶茂、生命力旺盛。由此推断,朽烂掉的“树心”是这棵树的( )
A.全部韧皮部 B.全部木质部 C.全部树皮 D.部分木质部
10.下列有关物质燃烧时观察到的现象的叙述中,正确的是 ( )
A.硫在氧气中燃烧,发出淡蓝色的火焰,生成有刺激性气味的气体
B.木炭在氧气中燃烧,发出白光,生成能使澄清石灰水变浑浊的气体
C.红磷在氧气中燃烧,放出大量热,产生大量白雾
D.铁丝在氧气中燃烧,火星四射,生成氧化铁
11.2020年2月4日,中国工程院院土李兰娟的研究团队发现:达芦那韦(化学式为C27H37N3O7S)能显著抑制新冠肺炎病毒复制。下列有关说法错误的是 ( )
A.达芦那韦由五种元素组成 B.达芦那韦由分子构成
C.一个达芦那韦分子由75个原子构成 D.达芦那韦中C和H两种元素的质量比为27﹕37
12.小滨对一些科学符号中数字的含义有如下的理解,其中正确的是 ( )
A.CO2:可表示二氧化碳气体中有2个氧原子 B.CO32-:可表示一个碳酸根离子带2个单位负电荷
C.2C:可表示两种碳单质 D.Al3+:一个铝原子带三个单位的正电荷
13.小滨利用“热敏电阻的阻值会随温度的升高而减小”的性质,设计了判断水温变化的装置,其工作原理如图甲所示,电源、热敏电阻、电磁铁、定值电阻R0由导线连接成一个串联电路,在线圈的上方固定一个弹簧测力计,其下端挂一铁块。实验时把热敏电阻放入盛水的烧杯中,水温的变化会引起弹簧测力计示数发生变化:如图乙所示为某次实验中弹簧测力计读数随时间变化的图像。下列说法正确的是( )
A.t1到t2时间内热敏电阻的阻值变大 B.t1到t2时间内水温升高
C.t2到t3时间内电压表示数最小 D.t3到t4时间内电路中电流变大
14.下列图像能正确反映对应关系 ( )
A.甲表示加热高锰酸钾制取氧气时,剩余固体中氧元素的质量变化
B.乙表示加热氯酸钾(含少量MnO2)制取氧气时,固体物质种类的变化
C.丙表示双氧水(含少量MnO2)分解时,溶液中氢元素的质量分数变化
D.丁表示质量和溶质质量分数都相等的双氧水反应生成氧气的质量变化
15.如图所示,弹簧测力计下挂一条形磁铁,条形磁铁下面放置一通电螺线管。当条形磁铁从左向右水平拉过时,下列图像中能正确描述弹簧测力计示数变化情况的是 ( )
A. B. C. D.
16.纯净物M在密闭容器中微热就分解为NH3、H2O和CO2,根据这一实验事实能得出的结论是( )
A.M由四种元素组成 B.M的化学性质很稳定
C.M中有氨气 D.M可能是碳酸氢钠(NaHCO3)
17.电子工业中常用氯化铁(FeCl3)溶液腐蚀铜板上不需要的铜,制作印刷电路板,反应化学方程式为Cu+2FeCl3=
CuCl2+2FeCl2。关于该反应判断正确的是( )
A.属于化合反应
B.参加反应的Cu、FeCl3质量之和等于生成的CuCl2、FeCl2质量之和
C.反应前后氯原子的数目增加
D.反应后铜元素的化合价降低
18.对下列实验中出现的异常现象分析合理的是 ( )
选项 异常现象 分析
A 制取CO2气体时,始终收集不到CO2 收集CO2的集气瓶没盖玻璃片
B 利用排水法收集氧气,但是O2不纯 通入氧气前集气瓶内水没有装满
C 细铁丝在氧气中燃烧时,集气瓶瓶底炸裂 由于引燃的火柴太长了
D 测定空气中氧气含量时,进入集气瓶中的水过少 红磷过量
19.小江家的家庭电路如图所示,小江闭合开关S,电灯正常发光。分别将台灯与洗衣机插入P、Q插座,都闭合开关,发现它们不能工作。于是小江只拔下台灯的插头,用测电笔检测P插座,左右两孔都能使测电笔的氛管发光,则小江家电路出现的故障可能是 ( )
A.进户零线断路 B.AB间断路 C.进户火线断路 D.BC间断路
20.逻辑推理是科学学习中常用的思维方法,下列推理合理的是( )
A.因为离子是带电的粒子,所以带电的粒子就是离子
B.因为单质中只含一种元素,所以只含一种元素的物质就是单质
C.因为化合物含有多种元素,所以含多种元素的物质一定都是化合物
D.因为水电解只得到氢气和氧气,所以水一定由氢、氧两种元素组成
二、简答题(本题有9小题,共34分)
21.(5分)用化学用语填空:①碘单质化学式为 ;②氦气的化学式为 ;
③4个铵根离子 ;④n个硫酸根离子 ;⑤将“神舟十号”飞船送入太空的是“长征二号”F运载火箭,火箭工作中发生的反应为C2H8N2+2R=3N2+4H2O+2CO2,其中R的化学式是 。
22.(3分)下列常见物质:①氧气;②二氧化碳;③铁;④汞(水银);⑤水;⑥氯化钠。其中由原子直接构成的有
,由分子构成的有 ,由离子构成的有 (填序号)。
23.(3分)家庭电路中,触电是人直接接触 造成的。安全用电原则是:不接触 ,
不靠近 。
24.(4分)如图是探究“怎样产生感应电流”的实验装置。ab是一根导体,通过导线、开关连接在灵敏电流计的两接线柱上。
(1)本实验中,如果 ,我们就认为有感应电流产生。
(2)闭合开关后,假设导线不动,磁铁左右水平运动,电路 感应电流(选填“有”或“无”)。
(3)闭合开关后,假设磁铁不动,导体向纸面里外方向运动,电路 感应电流(选填“有”或“无”)。
25.(4分)追寻科学家的足迹,一起了解氧气的发现史。(汞蒸气和汞的化合物均有毒性)
(1)1773年,舍勒用加热分解硝酸钾、氧化汞、碳酸银等物质都能制得氧气。从物质组成角度分析:加热上述物质均可制得氧气的原因是 。
(2)之后,法国化学家拉瓦锡用如图装置,把少量的汞放入如图所示的曲颈瓶中,连续加热12天后,发现银白色的液态汞变成了红色的粉末,容器中空气的体积大约减少了五分之一。随后他又将产生的红色粉末收集于另一容器中并加强热,发现又生成了汞和另一种气体。这种气体的体积恰好等于之前曲颈瓶中空气减小的体积。
拉瓦锡通过定量研究的方法发现了空气中的氧气和氮气。该实验中选择使用汞的优点有 。(可多选)
A.实验过程中没有污染 B.在汞槽中起到液封的作用
C.生成的化合物加热分解又能得到汞和氧气 D.能将密闭装置内空气中的氧气几乎耗尽
26.(6分)“杂交水稻之父”袁隆平院士经过多年的努力,利用野生稻培育出了具有许多优良性状的“超级杂交水稻”,并研究出能在盐碱地上种植的“海水稻”。
(1)“超级杂交水稻”的茎不能明显增粗是因为其茎中没有 (填茎的结构名称)。
(2)耐盐碱水稻根毛细胞的细胞液浓度 (选填“小于”、“等于”或“大于”)所生长的土壤溶液浓度时,根毛细胞吸水,吸收的水大部分用于 作用。
27.(2分)下表是教材中元素周期表的一部分,除标出的元素外,表中的数字编号①—④各表示一种元素。请回答问题。
(1)数字编号②表示的元素是 (填符号)。
(2)③代表的元素与Mg元素形成的化合物的化学式为 。
28.(3分)小滨对教材中“探究二氧化碳性质”的相关实验装置进行了如图的改进。当通入二氧化碳一段时间后,可观察到试管A内溶液的颜色呈 色,试管B中出现的现象是 ,烧杯C中 (选填“上面”或“下面”)的蜡烛先熄灭。
29.(4分)氮氧化物(如NO2、NO等)进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾。因此必须对含有氮氧化物的废气进行处理。
(1)用氢氧化钠溶液可吸收废气中的氮氧化物。反应的化学方程式为:NO2+NO+2NaOH=2NaNO2+H2O,产物NaNO2中N元素的化合价为 ;已知“HNO2”读作“亚硝酸”,则NaNO2的名称为 。
(2)汽车尾气中含有NO和CO,消除这两种物质对大气污染的方法是安装催化转化器,使它们发生反应生成N2和CO2,该反应的化学方程式为 。
三、实验探究题(本题有4小题,共34分)
30.(8分)小滨偶然发现月季茎折断后仍能成活(如图甲),想探究月季茎折断后什么情况下还能成活?他将生理状况相似的20株月季分成五组,进行如下表所示的处理。(处理方法和位置如图乙、丙所示,云母片能阻断物质的运输。)
组别 处理方法
1 不做处理
2 在B处韧皮部环割一圈
3 在B处韧皮部环割半圈
4 在A处木质部切断并插入云母片(不影响韧皮部功能)
5 在B处木质部切断并插入云母片(不影响韧皮部功能)
(1)第1组不做处理是为了作为 。
(2)结合以上信息判断,一段时间后月季植株一定死亡的实验组有 (填组别)。
(3)为探究月季折断程度是否影响月季的存活,应增加一组(第6组)实验的处理方法是
,并与第5组形成对照。
(4)经以上6组实验可以得出折断的月季是否仍能存活与月季折断的程度和 有关。
31.(10分)实验室常用下列装置来制取氧气:
(1)请写出以下实验器材的名称:a ,b 。用双氧水和二氧化锰来制取干燥的氧气时,可选用的发生和收集装置是 (填序号)。
(2)将产生的氧气分别通入G、H装置,通过实验现象说明可燃物的燃烧必备的一个条件是 。
(3)实验室常用氯化铵固体与碱石灰固体共热来制取氨气,它们发生反应的化学方程式是:2NH4Cl+Ca(OH)2CaCl2
+2NH3↑+2H2O。常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水。根据以上信息,请你判断制取并收集氨气时应选择的装置是 (填序号)。
32.(8分)某科学小组为探究绿色植物在维持碳——氧平衡中的作用,设计了如图一所示的密闭透明的实验装置(此实验忽略温度等因素对装置内气体体积等的影响):将图一装置放在室外培养24小时,连接氧气检测仪,测得装置内一昼夜氧气浓度的变化曲线如图二。请据图分析作答:
(1)分析图一和图二可知:随着时间推移,红墨水滴的位置在一天中 时移动到最右端(填数字);判断该植物在24小时后积累了有机物,依据是曲线中A点低于 点(填图中字母);
(2)请写出在图二AF段中,该植物一直进行的生理活动是 (选填“光合作用”或“呼吸作用”);
(3)若用图一装置继续探究光合作用是否需要水分,则对该绿色植物进行的处理是
。
33.(8分)在“探究电磁铁磁性强弱与电流大小关系”的实验中,小明用绝缘细线将电磁铁M悬挂在铁架台上,并保持它与软铁块P的距离不变。以下是他的部分实验步骤:
①断开开关S,按图组装实验电路,将滑动变阻器的滑片置于最右端。用已调零的电子测力计测出软铁块P对测力计的压力F0并记录在表格中;
②闭合开关S,调节滑动变阻器的滑片到适当位置,读出电流表的示数I和电子测力计的示数F,并将I、F的数据记录在表格中;
③仿照步骤②再进行两次实验。
(1)实验中小明是通过 来判定电磁铁磁性强弱的。
(2)闭合开关S后,电磁铁下端的磁极为 (选填“N”或“S”)极。
(3)由表中数据可以得出的实验结论是: 。
(4)本实验中,滑动变阻器除了保护电路的作用外,还起到 的作用。
四、分析计算题(本题有4小题,共32分)
34.(6分)我国科研团队通过电催化结合生物合成的方式,实现了二氧化碳合成葡萄糖和脂肪酸。第1步是将二氧化碳还原到一氧化碳,第2步是一氧化碳转化为高纯的乙酸,第3步是在乙酸中加入经过基因编辑之后的酵母进行发酵,最后得到葡萄糖和脂肪酸。如图所示是1、2两步过程,请回答下列问题。
(1)两步反应前后,物质的总质量不改变,请从微观上解释: ;
(2)二氧化碳和一氧化碳化学性质不同的根本原因是 ;
(3)请写出乙酸中碳、氢、氧元素质量比 。
35.(8分)为了检测实验室中石灰石样品中碳酸钙的含量,某同学用溶质质量分数相同的盐酸与样品进行了四组实验测定(样品中的杂质不溶于水,且不与盐酸反应),测得数据如表。试回答:
甲 乙 丙 丁
所取石灰石质量/g 10.0 10.0 10.0 10.0
加入盐酸质量/g 20.0 30.0 45.0 50.0
剩余固体质量/g 6.0 4.0 2.0 2.0
(1)石灰石样品中碳酸钙的质量分数是 ;
(2)各组充分反应后,盐酸有剩余的实验组别是 ;
(3)实验所用稀盐酸的溶质质量分数是多少 (写出计算过程)
36.(8分)纯电动汽车是一种采用蓄电池作为唯一动力源的汽车,电池的安全性主要体现在对其温度的控制上,当某组电池温度过高时,立即启动制冷系统进行降温,图甲是小滨设计的模拟控温装置示意图,电磁继电器与热敏电阻Rt、滑动变阻器RP串联接在电压为6V的电源两端。当电磁铁线圈(电阻不计)中的电流I大于或等于25mA时,衔铁被吸合,热敏电阻置于温度监测区域,其阻值Rt与温度t的关系如图乙所示,滑动变阻器的最大阻值为200Ω。
(1)图甲中应将b端与 端相连;
(2)若设置电池温度为60℃时启动制冷系统,则滑动变阻器阻值应为多少?
(3)若要提高启动温度,RP接入电路的阻值应该怎么调节?并简要说明理由。
37.(10分)在杭州亚运村西北侧的“世纪变”,成立了全省首个“电力能源碳中和技术示范基地”。这座变电站获得了权威机构颁发的《碳中和证书》,节能减碳成效已经获得认可,以上措施可缓解的环境问题是 。如图甲是小滨验证该问题的实验装置,在 (填“阳光”或“黑暗”)下一段时间后,可观察到水柱向 (填“左”或“右”)移动。
此外,根据研究发现海洋吸收二氧化碳有三种方式(图乙)。
图甲 图乙
(1)自然溶解:大气中的二氧化碳能不断地溶解到海水中。研究表明,海水温度越低,单位体积溶解的二氧化碳越多。一年四季中,单位体积海水中溶解二氧化碳最多的是 季。
(2)植物固碳:近海滩涂上的红树林、海洋浮游植物等通过光合作用吸收二氧化碳,最终这些碳元素随着植物残体沉积到海底。植物固碳只能发生在海洋的浅层,超过一定深度不能发生,其原因是
。
(3)碳酸盐泵:贝壳类、珊瑚等海洋生物将碳元素以碳酸钙的形式沉积起来。某地贝壳堤储存了约4亿吨贝壳,其中95%为碳酸钙,则该地贝壳堤固定了 亿吨碳元素?
2022学年第二学期期末教学质量检测参考答案
一、选择题(本题有20小题,每小题3分,共60分,请选出一个符合题意的正确选项)
题号 1 2 3 4 5 6 7 8 9 10
答案 B D B A D B C D D B
题号 11 12 13 14 15 16 17 18 19 20
答案 D B B B A A B B B D
二、简答题(本题有9小题,共34分)
21.(5分)①I2;②He;③4NH4+;④nSO42-;⑤N2O4。
22.(3分)③④;①②⑤;⑥。
23.(3分)火线;低压带电体;高压带电体。
24.(4分)(1)灵敏电流计指针发生偏转;(2)有;(3)无。
25.(4分)(1)这些物质中都含有氧元素;(2)BCD。
26.(4分)(1)形成层;(2)蒸腾作用。
27.(2分)(1)Li;(2)MgO。
28.(3分)红;澄清石灰水变浑浊;下面。
29.(4分)(1)+3;亚硝酸钠;(2)。
三、实验探究题(本题有4小题,共34分)
30.(8分)(1)对照;(2)2、5;(3)在B处将部分木质部切断并插入云母片(不影响韧皮部功能);(4)折断的位置。
31.(10分)(1)铁架台;长颈漏斗;BE;(2)温度达到可燃物的着火点;(3)AD。
32.(8分)(1)18;F;(2)呼吸作用;(3)将一个叶片割断主叶脉,导管被切断,这样叶片前部分就得不到从根运输来的水分,叶片后部分就能得到水分。因此,叶片前后两部分就形成以水为唯一变量的对照实验。
33.(8分)(1)电子测力计示数;(2)N;(3)线圈匝数一定时,通过电磁铁的电流越大,电磁铁磁性越强;(4)改变电流大小。
四、分析计算题(本题有4小题,共32分)
37.(10分)温室效应;阳光;左;(1)冬;(2)海洋超过一定深度,光照弱,植物光合作用弱,无法维持生长;(3)0.456亿。
同课章节目录
