3.5 有机合成(解析版)
图片预览




文档简介
中小学教育资源及组卷应用平台
第三章 第五节 有机合成
【学习目标】
1.掌握烃及烃的衍生物性质及官能团相互转化的一些方法。
2.了解有机合成的基本过程和基本原则,根据合成路线图学会推断有机物的结构,根据信息能设计有机化合物的合成路线。
【素养目标】
1.通过有机物的结构推测有机物的转化路径,培养学生“宏观辨识与微观探析”的学科素养。
2、通过建立有机物合成推断的思维模型,培养学生“证据推理与模型认知”的学科素养。
必备知识与关键能力
知识点一:有机合成的主要任务
1.有机合成的概念
有机合成指利用简单、易得的原料,通过有机反应生成具有特定结构和功能的有机化合物的过程。
2.有机合成的任务
有机合成的任务包括目标化合物分子骨架的构建和官能团的转化。
3.有机合成遵循的原则
(1)起始原料要廉价、易得、低毒、低污染。
(2)尽量选择步骤最少的合成路线,使得反应过程中副反应少、产率高。
(3)符合“绿色化学”的要求,操作简单、条件温和、能耗低、易实现、原料利用率高、污染少,尽量实现零排放。
(4)按照一定的反应顺序和规律引入官能团,不能臆造不存在的反应事实。在引入官能团的过程中,要注意先后顺序,以及对先引入的官能团的保护。
4.有机合成中碳骨架的构建
(1)碳链增长的反应
加聚反应;缩聚反应;酯化反应;利用题目所给信息反应,如卤代烃的取代反应,醛、酮的加成反应……
①炔烃、烯烃、醛、酮与HCN加成:
②醛酮的羟醛缩合(其中至少一种含有α H):
③卤代烃与NaCN、CH3CH2ONa、CH3CCNa等的取代反应:RCl+NaCNRCN+NaCl。
④聚合反应
a.加聚反应(烯烃、二烯烃、乙炔等):
b.缩聚反应:酯化反应类型(如乙二醇与乙二酸反应)、氨基酸缩合类型(如甘氨酸缩合)、甲醛与苯酚(酚醛树脂)。
⑤酯化反应:CH3CH2OH+CH3COOHCH3COOCH2CH3+H2O。
(2)碳链减短的反应
①氧化反应,包括烯烃、炔烃的部分氧化,苯的同系物氧化成苯甲酸等。
②水解反应,主要包括酯的水解、蛋白质的水解和多糖的水解。如RCOOR′+H2ORCOOH+R′—OH。
③烷烃发生裂化或裂解反应:C16H34C8H18+C8H16;C8H18C4H10+C4H8。
④脱羧反应:R—COONa+NaOHR—H+Na2CO3。
①烷烃的裂化反应;
②利用题目所给信息反应,如烯烃、炔烃的氧化反应,羧酸及其盐的脱羧反应……
(3)常见由链成环的方法
①二元醇成环 如:HOCH2CH2OH +H2O
②羟基酸酯化成环 如:
③氨基酸成环 如:H2NCH2CH2COOH
④二元羧酸成环 如:HOOCCH2CH2COOH
⑤双烯合成 如:
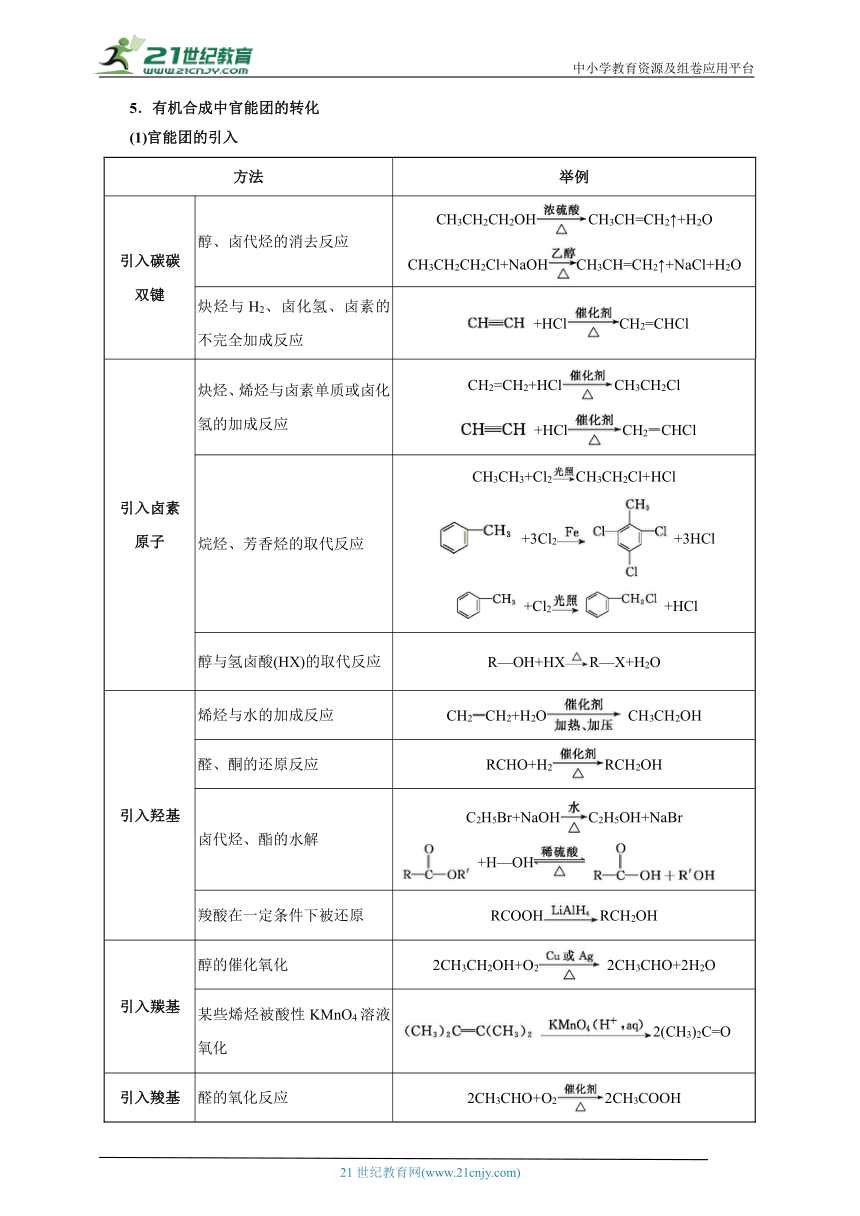
5.有机合成中官能团的转化
(1)官能团的引入
方法 举例
引入碳碳 双键 醇、卤代烃的消去反应 CH3CH2CH2OHCH3CH=CH2↑+H2O CH3CH2CH2Cl+NaOHCH3CH=CH2↑+NaCl+H2O
炔烃与H2、卤化氢、卤素的不完全加成反应 +HClCH2=CHCl
引入卤素 原子 炔烃、烯烃与卤素单质或卤化氢的加成反应 CH2=CH2+HClCH3CH2Cl +HClCH2CHCl
烷烃、芳香烃的取代反应 CH3CH3+Cl2CH3CH2Cl+HCl +3Cl2+3HCl +Cl2+HCl
醇与氢卤酸(HX)的取代反应 R—OH+HXR—X+H2O
引入羟基 烯烃与水的加成反应 CH2CH2+H2O CH3CH2OH
醛、酮的还原反应 RCHO+H2RCH2OH
卤代烃、酯的水解 C2H5Br+NaOHC2H5OH+NaBr +H—OH
羧酸在一定条件下被还原 RCOOHRCH2OH
引入羰基 醇的催化氧化 2CH3CH2OH+O2 2CH3CHO+2H2O
某些烯烃被酸性KMnO4溶液氧化 2(CH3)2C=O
引入羧基 醛的氧化反应 2CH3CHO+O22CH3COOH
某些烯烃被酸性KMnO4溶液氧化 CH3CHCHCH32CH3COOH
酯的水解 CH3COOC2H5+H2OCH3COOH+C2H5OH
(2)官能团的消除
①通过加成反应可以消除或。如:CH2=CH2+H2CH3CH3
②通过消去反应、氧化反应或酯化反应可消除—OH。如:CH3CH2OHCH2=CH2↑+H2O
2CH3CH2OH+O22CH3CHO+2H2O
CH3CH2OH+CH3COOHCH3COOCH2CH3+H2O
③通过氧化反应或加成反应可消除—CHO。如:2CH3CHO+O22CH3COOH
④通过水解反应消除酯基、肽键、卤素原子。
(3)官能团的改变
①利用官能团的衍生关系进行衍变,如R—CH2OHR—CHOR—COOH;
②通过某种化学途径使一个官能团变为两个,如
CH3CH2OHCH2==CH2Cl—CH2—CH2ClHO—CH2—CH2—OH;
③通过某种手段改变官能团的位置,如
。
6.官能团的保护与恢复
(1)碳碳双键:在氧化其他基团前可以利用其与HCl等的加成反应将其保护起来,待氧化后再利用消去反应转变为碳碳双键。
HOCH2CH==CHCH2OHHOCH2CH2CHClCH2OH
HOOC—CH==CH—COOH。
(2)酚羟基:在氧化其他基团前可以用NaOH溶液或CH3I保护。
(3)醛基:在氧化其他基团前可以用乙醇(或乙二醇)加成保护。
①
②
(4)氨基:在氧化其他基团前可以用醋酸酐将氨基转化为酰胺,然后再水解转化为氨基。
(5)醇羟基、羧基可以成酯保护。
典例1.下列说法不正确的是( )
A.有机合成的思路就是通过有机反应构建目标化合物的分子构架,并引入或转化成所需的官能团
B.有机合成过程可以简单表示为基础原料→中间体→目标化合物
C.逆合成分析法可以简单表示为目标化合物→中间体→基础原料
D.为减少污染,有机合成不能使用辅助原料,不能有副产物
【答案】D
【解析】有机合成中可以使用辅助原料,也可以产生副产物,D项错误。
典例2.有机化合物分子中能引入卤素原子的反应是( )
A.消去反应 B.酯化反应 C.水解反应 D.取代反应
【答案】D
【解析】消去反应主要是消去原子或原子团,形成双键,A项错误;酯化反应是羧酸与醇生成酯和水的而反应,不可能引入卤素原子,B项错误;酯的水解反应能引入羟基和羧基,但不能引入卤素原子,C项错误;烷烃或芳香烃的取代反应均可引入卤素原子,D项正确。
典例3.某同学设计了由乙醇合成乙二醇的路线,如下图所示。下列说法正确的是( )
A.X可以发生取代反应
B.等物质的量的乙醇、X完全燃烧,消耗氧气的量相同
C.步骤②需要在氢氧化钠的醇溶液中反应
D.步骤①的反应类型是水解反应
【答案】B
【解析】乙醇在步骤①发生消去反应生成乙烯,乙烯与溴单质发生加成反应生成1,2 二溴乙烷,1,2 二溴乙烷在步骤②发生水解反应生成乙二醇。X为乙烯,含有碳碳双键,能够发生加成反应,故A错误;乙醇燃烧耗氧部分为C2H4,因此等物质的量的乙醇、乙烯完全燃烧,消耗氧气的量相同,故B正确;步骤②为1,2 二溴乙烷水解生成乙二醇,反应条件为氢氧化钠水溶液、加热,故C错误;步骤①为乙醇发生消去反应生成乙烯,故D错误。
知识点二:有机合成的路线和设计实施
1.有机合成过程
有机合成的过程是利用简单的试剂作为基础原料,通过有机反应链上官能团或一段碳链,得到一个中间体;在此基础上利用中间体上的官能团,加上辅助原料,进行第二步反应,合成第二个中间体,经过多步反应,按照目标化合物的要求,合成具有一定碳原子数目、一定结构的目标化合物。
有机合成过程示意图
2.有机合成路线设计思路
(1)设计有机合成路线时,首先要正确判断需合成的有机物的类别,它含有哪些官能团,与哪些知识信息有关。
(2)其次是根据现有的原料、信息和有关反应规律,尽可能合理地把目标化合物分成若干片段,或寻找官能团的引入、转换、保护方法,或设法将各片段拼凑衍变,尽快找出合成目标化合物的关键。
(3)最后将正向推导和逆向推导得出的若干个合成路线加以综合比较,选择最佳的合成方案。
3.有机合成推断方法
(1)正合成分析法
即从某种原料分子开始,对比目标分子与原料分子的结构(碳骨架及官能团),对该原料分子进行碳骨架的构建和官能团的引入(或者官能团的转化),从而设计出合理的合成路线。如利用乙烯为原料合成乙酸乙酯,可采用正推法:
(2)逆合成分析法
即从目标分子着手,分析目标分子的结构,然后由目标分子逆推出原料分子,并进行合成路线的设计。
逆合成分析示意图
①逆推法合成乙二酸二乙酯
②逆推法合成对苯甲酸苯甲酯
通过对苯甲酸苯甲酯()的结构分析可知合成该有机化合物的是苯甲酸与苯甲醇,继续逆推可得原料分子为甲苯,如图所示:
③综合推理法
设计有机合成路线时,用正合成分析法不能得到目标产物,而用逆合成分析法也得不到起始原料时,往往结合这两种思维模式,采用从两边向中间“挤压”的方式,使问题得到解决。
知识点三:常见的有机合成路线
(1)一元合成路线
R—CH===CH2卤代烃一元醇→一元醛→一元羧酸→酯
(2)二元合成路线
CH2===CH2XCH2—CH2X二元醇→二元醛→二元羧酸→
(3)芳香化合物合成路线
典例4.卤代烃与金属镁在无水乙醚中反应,可制得格林试剂RMgX,它可与醛、酮等羰基化合物加成:
所得产物经水解可以得到醇,这是某些复杂醇的合成方法之一。现欲合成(CH3)3C—OH,下列所选用的卤代烃和羰基化合物的组合正确的是( )
A.乙醛和氯乙烷 B.甲醛和1 溴丙烷
C.甲醛和2 溴丙烷 D.丙酮和一氯甲烷
【答案】D
【解析】由题给信息可知产物中与—OH相连的碳原子是羰基碳原子,要合成,需要丙酮和一氯甲烷。
典例5.山梨酸是一种高效安全的防腐保鲜剂,其合成路线如图所示,下列说法正确的是( )
A.反应1属于缩聚反应
B.反应2每生成1 mol山梨酸需要消耗1 mol水
C.可用酸性高锰酸钾溶液检验山梨酸中是否含有巴豆醛
D.山梨酸与K2CO3溶液反应可生成水溶性更好的山梨酸钾
【答案】D
【解析】反应1中没有小分子副产物生成,不属于缩聚反应,A错误;反应2每生成1 mol 山梨酸理论上不需要消耗水,原因是一个酯基水解消耗1个水分子,但同时分子内因消去反应又生成一个水分子,B错误;山梨酸、巴豆醛分子结构中均含有碳碳双键,二者均能与酸性高锰酸钾溶液反应,不能检验,C错误;山梨酸钾是可溶性钾盐,其水溶性更好,山梨酸的酸性大于碳酸,故山梨酸与K2CO3溶液反应可生成水溶性更好的山梨酸钾,D正确。
核心价值与学科素养
【知识结构化】 有机物之间的相互转化
【思维建模】 有机合成题的解题思路
典例6.β-苯基丙烯醛(如构简式如丁所示)可用于水果保鲜或食用香料,合成路线如图。下列说法正确的是( )
A.甲与乙互为同系物
B.反应①为加成反应,反应②为消去反应
C.1 mol丙与足量金属钠反应放出2 g H2
D.1 mol丁可被1 mol新制Cu(OH)2完全氧化
【答案】B
【解析】A.甲与乙结构不相似,不是互为同系物,故A错误;B.反应①苯甲醛中的醛基发生加成反应,反应②中羟基与邻碳上氢发生消去反应,故B正确;C.1 mol丙与足量金属钠反应放出1 g H2,故C错误;D.1 mol丁含1 mol醛基,可被2 mol新制Cu(OH)2完全氧化,故D错误;故选B。
典例7.我国自主研发的对二甲苯的绿色合成路线取得新进展,其合成示意图如下:
下列说法错误的是( )
A.过程i发生了加成反应
B.利用相同的原理以及相同的原料,也能合成间二甲苯
C.中间产物M的结构简式为
D.该合成路线理论上碳原子的利用率为100%,且最终得到的有机产物只能用蒸馏的方法进行分离
【答案】D
【解析】过程i是异戊二烯和丙醛发生加成反应生成中间产物M,故A正确;异戊二烯和丙醛发生加成反应有2种加成方式,可以合成对二甲苯和间二甲苯,但是不能合成邻二甲苯,故B正确;由M的球棍模型可知,甲基的邻位有一个双键,所以中间产物M的结构简式为:,故C正确;根据合成示意图可知:该合成路线分2步,第一步为加成反应,第二步为脱水反应,两步的碳原子利用率均为100%,最终得到的产物为对二甲苯和水,用分液的方法可将二者分离,不需要蒸馏,故D错误。
【跟踪练习】 基础过关
1. 在有机合成中,常需要将官能团消除或增加,且要求过程科学、简捷,下列相关过程不合理的是( )
A.乙烯乙二醇:CH2CH2
B.乙醇溴乙烷:CH3CH2OHCH2CH2CH3CH2Br
C.乙醛乙烯:CH3CHOCH3CH2OHCH2CH2
D.乙醇乙酸:CH3CH2OHCH3CHOCH3COOH
【答案】B
【解析】乙醇可以与氢溴酸发生取代反应生成溴乙烷,不需要先消去,再加成。
2. 甲基丙烯酸甲酯旧法合成的反应是(CH3)2C===O+HCN―→(CH3)2C(OH)CN,(CH3)2C(OH)CN+CH3OH+H2SO4―→CH2===C(CH3)COOCH3+NH4HSO4。20世纪90年代新法合成的反应是CH3C≡CH+CO+CH3OHCH2===C(CH3)COOCH3,与旧法比较,新法的优点是( )
A.原料无爆炸危险 B.原料都是无毒物质
C.没有副产物,原料利用率高 D.条件较简单
【答案】C
【解析】新法有CO、CH3OH参与,CO、CH3OH有毒且可燃,有爆炸危险,所以A、B两项错误;新法需要催化剂而旧法不用,所以D项错误;比较两种合成方法,新法的优点是没有副产物,原料利用率高,所以C项正确。
3. 下列说法不正确的是( )
A.可发生消去反应引入碳碳双键
B.可发生催化氧化反应引入羧基
C.CH3CH2Br可发生取代反应引入羟基
D.与CH2===CH2可发生加成反应引入环
【答案】B
【解析】上无氢原子,故不能发生催化氧化反应生成羧酸,B不正确。
4. 某石油化工产品X的转化关系如图所示,下列判断错误的是( )
A.X→Y是加成反应
B.乙酸→W是酯化反应,也是取代反应
C.Y能与钠反应产生氢气
D.W能与NaOH溶液反应,但不能与稀硫酸反应
【答案】D
【解析】X为石油化工产品,并结合图示转化关系可推知X为CH2==CH2,Y为C2H5OH,Z为CH3CHO,W为乙酸乙酯。乙酸乙酯与NaOH溶液和稀硫酸均能发生水解反应,D项不正确。
5. 已知醇在一定条件下经分子间脱水可以生成醚,以乙醇、浓硫酸、溴水、氢氧化钠的水溶液为主要原料合成。最佳合成路线中依次涉及的反应类型是( )
①氧化 ②还原 ③取代 ④加成 ⑤消去 ⑥中和 ⑦水解 ⑧酯化 ⑨加聚
A.⑤④⑥⑧ B.⑤④⑦③
C.②⑤④⑧ D.②④⑥⑧
【答案】B
【解析】 合成的最佳路线为:CH3CH2OH CH2===CH2
能力达成
6. (1)由环己醇制取己二酸己二酯,最简单的流程途径顺序正确的是 (填序号)。
已知:RCH2CH2R'RCHO+RCHO
①取代反应 ②加成反应 ③氧化反应 ④还原反应 ⑤消去反应 ⑥酯化反应 ⑦中和反应 ⑧缩聚反应
A.③②⑤⑥ B.⑤③④⑥ C.⑤②③⑥ D.⑤③④⑦
(2)写出制取己二酸己二酯最后一步反应的化学方程式: 。
(3)写出由环己醇制取1,2-环己二醇的流程图。
。
【答案】(1)B
(2)++2H2O
(3)
【解析】采用逆推法分析可得该制备过程的流程为:
已知:①环己烯可以通过1,3-丁二烯与乙烯发生环化加成反应得到:
+(也可表示为+||)。
②实验证明,下列反应中反应物分子的环外双键比环内双键更容易被氧化。
现仅以1,3-丁二烯为有机原料,无机试剂任选,按下列途径合成甲基环己烷:
1,3-丁二烯ABD
请按要求填空:
(1)A的结构简式为 ;B的结构简式为 。
(2)写出下列反应的化学方程式和反应类型。
反应④: ;对应反应类型为 。
反应⑤: ;对应反应类型为 。
【答案】(1)
(2)+H2O 消去反应
+H2 加成反应
【解析】由合成途径和信息①可推知,A是由两分子1,3-丁二烯经下列反应制得的:+;而由C的分子式C7H14O和信息②可知,B是A的氧化产物,其结构简式为;C是B的加成产物,其结构简式为。要得到,可先使C消去—OH得到D,化学方程式为+H2O,再由D发生加成反应得到甲基环己烷:+H2。
化妆品中防腐剂的作用主要是抑制微生物的生长和繁殖,保持化妆品的性质稳定,使其开盖使用后不 易变质,延长保存时间。用甲苯生产一种常用的化妆品防腐剂,其生产过程如图(反应条件没有全部注明)。
AB
回答下列问题:
(1)有机化合物A的结构简式为 。
(2)在合成路线中,设计第③步与第⑥步反应的目的是 。
(3)写出反应⑤的化学方程式: 。
(4)写出由生成C7H5O3Na的化学方程式: 。
(5)下列有关说法正确的是 (填字母)。
a.莽草酸、对羟基苯甲酸都属于芳香族化合物
b.1 mol莽草酸与NaOH溶液反应,最多消耗4 mol NaOH
c.二者均可以发生酯化、氧化、加成等反应
d.利用FeCl3溶液可区别莽草酸和对羟基苯甲酸
(6)写出同时符合下列要求的的所有同分异构体的结构简式: 。
a.含苯环;
b.可与FeCl3溶液发生显色反应;
c.苯环上的一氯代物有两种;
d.能发生银镜反应,不能发生水解反应。
【答案】(1) (2)保护酚羟基,防止其被氧化
(3)+C2H5OH+H2O
(4)+NaHCO3+H2O+CO2↑
(5)cd (6)、
【解析】(1)由可知,与氯气发生甲基对位取代,A的结构简式为。
(2)第③步反应是CH3I与酚羟基反应生成醚键,第⑥步反应是醚键与HI反应又重新生成酚羟基,目的是保护酚羟基,防止其在第④步中被氧化。
(3)反应⑤是羧酸与醇的酯化反应。
(4)由生成C7H5O3Na,说明只有—COOH参加反应而酚羟基没有参加反应,可选用NaHCO3溶液,因为NaOH、Na2CO3均能与酚羟基反应。
(5)a项,莽草酸中无苯环,错误;b项,1 mol莽草酸与NaOH溶液反应,最多消耗1 mol NaOH,错误。(6)根据题意可知,满足条件的同分异构体的结构中有—CHO和酚羟基,且根据分子中氧原子个数可判断其结构中有两个酚羟基;苯环上的一氯代物有两种,说明是对称结构。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
第三章 第五节 有机合成
【学习目标】
1.掌握烃及烃的衍生物性质及官能团相互转化的一些方法。
2.了解有机合成的基本过程和基本原则,根据合成路线图学会推断有机物的结构,根据信息能设计有机化合物的合成路线。
【素养目标】
1.通过有机物的结构推测有机物的转化路径,培养学生“宏观辨识与微观探析”的学科素养。
2、通过建立有机物合成推断的思维模型,培养学生“证据推理与模型认知”的学科素养。
必备知识与关键能力
知识点一:有机合成的主要任务
1.有机合成的概念
有机合成指利用简单、易得的原料,通过有机反应生成具有特定结构和功能的有机化合物的过程。
2.有机合成的任务
有机合成的任务包括目标化合物分子骨架的构建和官能团的转化。
3.有机合成遵循的原则
(1)起始原料要廉价、易得、低毒、低污染。
(2)尽量选择步骤最少的合成路线,使得反应过程中副反应少、产率高。
(3)符合“绿色化学”的要求,操作简单、条件温和、能耗低、易实现、原料利用率高、污染少,尽量实现零排放。
(4)按照一定的反应顺序和规律引入官能团,不能臆造不存在的反应事实。在引入官能团的过程中,要注意先后顺序,以及对先引入的官能团的保护。
4.有机合成中碳骨架的构建
(1)碳链增长的反应
加聚反应;缩聚反应;酯化反应;利用题目所给信息反应,如卤代烃的取代反应,醛、酮的加成反应……
①炔烃、烯烃、醛、酮与HCN加成:
②醛酮的羟醛缩合(其中至少一种含有α H):
③卤代烃与NaCN、CH3CH2ONa、CH3CCNa等的取代反应:RCl+NaCNRCN+NaCl。
④聚合反应
a.加聚反应(烯烃、二烯烃、乙炔等):
b.缩聚反应:酯化反应类型(如乙二醇与乙二酸反应)、氨基酸缩合类型(如甘氨酸缩合)、甲醛与苯酚(酚醛树脂)。
⑤酯化反应:CH3CH2OH+CH3COOHCH3COOCH2CH3+H2O。
(2)碳链减短的反应
①氧化反应,包括烯烃、炔烃的部分氧化,苯的同系物氧化成苯甲酸等。
②水解反应,主要包括酯的水解、蛋白质的水解和多糖的水解。如RCOOR′+H2ORCOOH+R′—OH。
③烷烃发生裂化或裂解反应:C16H34C8H18+C8H16;C8H18C4H10+C4H8。
④脱羧反应:R—COONa+NaOHR—H+Na2CO3。
①烷烃的裂化反应;
②利用题目所给信息反应,如烯烃、炔烃的氧化反应,羧酸及其盐的脱羧反应……
(3)常见由链成环的方法
①二元醇成环 如:HOCH2CH2OH +H2O
②羟基酸酯化成环 如:
③氨基酸成环 如:H2NCH2CH2COOH
④二元羧酸成环 如:HOOCCH2CH2COOH
⑤双烯合成 如:
5.有机合成中官能团的转化
(1)官能团的引入
方法 举例
引入碳碳 双键 醇、卤代烃的消去反应 CH3CH2CH2OHCH3CH=CH2↑+H2O CH3CH2CH2Cl+NaOHCH3CH=CH2↑+NaCl+H2O
炔烃与H2、卤化氢、卤素的不完全加成反应 +HClCH2=CHCl
引入卤素 原子 炔烃、烯烃与卤素单质或卤化氢的加成反应 CH2=CH2+HClCH3CH2Cl +HClCH2CHCl
烷烃、芳香烃的取代反应 CH3CH3+Cl2CH3CH2Cl+HCl +3Cl2+3HCl +Cl2+HCl
醇与氢卤酸(HX)的取代反应 R—OH+HXR—X+H2O
引入羟基 烯烃与水的加成反应 CH2CH2+H2O CH3CH2OH
醛、酮的还原反应 RCHO+H2RCH2OH
卤代烃、酯的水解 C2H5Br+NaOHC2H5OH+NaBr +H—OH
羧酸在一定条件下被还原 RCOOHRCH2OH
引入羰基 醇的催化氧化 2CH3CH2OH+O2 2CH3CHO+2H2O
某些烯烃被酸性KMnO4溶液氧化 2(CH3)2C=O
引入羧基 醛的氧化反应 2CH3CHO+O22CH3COOH
某些烯烃被酸性KMnO4溶液氧化 CH3CHCHCH32CH3COOH
酯的水解 CH3COOC2H5+H2OCH3COOH+C2H5OH
(2)官能团的消除
①通过加成反应可以消除或。如:CH2=CH2+H2CH3CH3
②通过消去反应、氧化反应或酯化反应可消除—OH。如:CH3CH2OHCH2=CH2↑+H2O
2CH3CH2OH+O22CH3CHO+2H2O
CH3CH2OH+CH3COOHCH3COOCH2CH3+H2O
③通过氧化反应或加成反应可消除—CHO。如:2CH3CHO+O22CH3COOH
④通过水解反应消除酯基、肽键、卤素原子。
(3)官能团的改变
①利用官能团的衍生关系进行衍变,如R—CH2OHR—CHOR—COOH;
②通过某种化学途径使一个官能团变为两个,如
CH3CH2OHCH2==CH2Cl—CH2—CH2ClHO—CH2—CH2—OH;
③通过某种手段改变官能团的位置,如
。
6.官能团的保护与恢复
(1)碳碳双键:在氧化其他基团前可以利用其与HCl等的加成反应将其保护起来,待氧化后再利用消去反应转变为碳碳双键。
HOCH2CH==CHCH2OHHOCH2CH2CHClCH2OH
HOOC—CH==CH—COOH。
(2)酚羟基:在氧化其他基团前可以用NaOH溶液或CH3I保护。
(3)醛基:在氧化其他基团前可以用乙醇(或乙二醇)加成保护。
①
②
(4)氨基:在氧化其他基团前可以用醋酸酐将氨基转化为酰胺,然后再水解转化为氨基。
(5)醇羟基、羧基可以成酯保护。
典例1.下列说法不正确的是( )
A.有机合成的思路就是通过有机反应构建目标化合物的分子构架,并引入或转化成所需的官能团
B.有机合成过程可以简单表示为基础原料→中间体→目标化合物
C.逆合成分析法可以简单表示为目标化合物→中间体→基础原料
D.为减少污染,有机合成不能使用辅助原料,不能有副产物
【答案】D
【解析】有机合成中可以使用辅助原料,也可以产生副产物,D项错误。
典例2.有机化合物分子中能引入卤素原子的反应是( )
A.消去反应 B.酯化反应 C.水解反应 D.取代反应
【答案】D
【解析】消去反应主要是消去原子或原子团,形成双键,A项错误;酯化反应是羧酸与醇生成酯和水的而反应,不可能引入卤素原子,B项错误;酯的水解反应能引入羟基和羧基,但不能引入卤素原子,C项错误;烷烃或芳香烃的取代反应均可引入卤素原子,D项正确。
典例3.某同学设计了由乙醇合成乙二醇的路线,如下图所示。下列说法正确的是( )
A.X可以发生取代反应
B.等物质的量的乙醇、X完全燃烧,消耗氧气的量相同
C.步骤②需要在氢氧化钠的醇溶液中反应
D.步骤①的反应类型是水解反应
【答案】B
【解析】乙醇在步骤①发生消去反应生成乙烯,乙烯与溴单质发生加成反应生成1,2 二溴乙烷,1,2 二溴乙烷在步骤②发生水解反应生成乙二醇。X为乙烯,含有碳碳双键,能够发生加成反应,故A错误;乙醇燃烧耗氧部分为C2H4,因此等物质的量的乙醇、乙烯完全燃烧,消耗氧气的量相同,故B正确;步骤②为1,2 二溴乙烷水解生成乙二醇,反应条件为氢氧化钠水溶液、加热,故C错误;步骤①为乙醇发生消去反应生成乙烯,故D错误。
知识点二:有机合成的路线和设计实施
1.有机合成过程
有机合成的过程是利用简单的试剂作为基础原料,通过有机反应链上官能团或一段碳链,得到一个中间体;在此基础上利用中间体上的官能团,加上辅助原料,进行第二步反应,合成第二个中间体,经过多步反应,按照目标化合物的要求,合成具有一定碳原子数目、一定结构的目标化合物。
有机合成过程示意图
2.有机合成路线设计思路
(1)设计有机合成路线时,首先要正确判断需合成的有机物的类别,它含有哪些官能团,与哪些知识信息有关。
(2)其次是根据现有的原料、信息和有关反应规律,尽可能合理地把目标化合物分成若干片段,或寻找官能团的引入、转换、保护方法,或设法将各片段拼凑衍变,尽快找出合成目标化合物的关键。
(3)最后将正向推导和逆向推导得出的若干个合成路线加以综合比较,选择最佳的合成方案。
3.有机合成推断方法
(1)正合成分析法
即从某种原料分子开始,对比目标分子与原料分子的结构(碳骨架及官能团),对该原料分子进行碳骨架的构建和官能团的引入(或者官能团的转化),从而设计出合理的合成路线。如利用乙烯为原料合成乙酸乙酯,可采用正推法:
(2)逆合成分析法
即从目标分子着手,分析目标分子的结构,然后由目标分子逆推出原料分子,并进行合成路线的设计。
逆合成分析示意图
①逆推法合成乙二酸二乙酯
②逆推法合成对苯甲酸苯甲酯
通过对苯甲酸苯甲酯()的结构分析可知合成该有机化合物的是苯甲酸与苯甲醇,继续逆推可得原料分子为甲苯,如图所示:
③综合推理法
设计有机合成路线时,用正合成分析法不能得到目标产物,而用逆合成分析法也得不到起始原料时,往往结合这两种思维模式,采用从两边向中间“挤压”的方式,使问题得到解决。
知识点三:常见的有机合成路线
(1)一元合成路线
R—CH===CH2卤代烃一元醇→一元醛→一元羧酸→酯
(2)二元合成路线
CH2===CH2XCH2—CH2X二元醇→二元醛→二元羧酸→
(3)芳香化合物合成路线
典例4.卤代烃与金属镁在无水乙醚中反应,可制得格林试剂RMgX,它可与醛、酮等羰基化合物加成:
所得产物经水解可以得到醇,这是某些复杂醇的合成方法之一。现欲合成(CH3)3C—OH,下列所选用的卤代烃和羰基化合物的组合正确的是( )
A.乙醛和氯乙烷 B.甲醛和1 溴丙烷
C.甲醛和2 溴丙烷 D.丙酮和一氯甲烷
【答案】D
【解析】由题给信息可知产物中与—OH相连的碳原子是羰基碳原子,要合成,需要丙酮和一氯甲烷。
典例5.山梨酸是一种高效安全的防腐保鲜剂,其合成路线如图所示,下列说法正确的是( )
A.反应1属于缩聚反应
B.反应2每生成1 mol山梨酸需要消耗1 mol水
C.可用酸性高锰酸钾溶液检验山梨酸中是否含有巴豆醛
D.山梨酸与K2CO3溶液反应可生成水溶性更好的山梨酸钾
【答案】D
【解析】反应1中没有小分子副产物生成,不属于缩聚反应,A错误;反应2每生成1 mol 山梨酸理论上不需要消耗水,原因是一个酯基水解消耗1个水分子,但同时分子内因消去反应又生成一个水分子,B错误;山梨酸、巴豆醛分子结构中均含有碳碳双键,二者均能与酸性高锰酸钾溶液反应,不能检验,C错误;山梨酸钾是可溶性钾盐,其水溶性更好,山梨酸的酸性大于碳酸,故山梨酸与K2CO3溶液反应可生成水溶性更好的山梨酸钾,D正确。
核心价值与学科素养
【知识结构化】 有机物之间的相互转化
【思维建模】 有机合成题的解题思路
典例6.β-苯基丙烯醛(如构简式如丁所示)可用于水果保鲜或食用香料,合成路线如图。下列说法正确的是( )
A.甲与乙互为同系物
B.反应①为加成反应,反应②为消去反应
C.1 mol丙与足量金属钠反应放出2 g H2
D.1 mol丁可被1 mol新制Cu(OH)2完全氧化
【答案】B
【解析】A.甲与乙结构不相似,不是互为同系物,故A错误;B.反应①苯甲醛中的醛基发生加成反应,反应②中羟基与邻碳上氢发生消去反应,故B正确;C.1 mol丙与足量金属钠反应放出1 g H2,故C错误;D.1 mol丁含1 mol醛基,可被2 mol新制Cu(OH)2完全氧化,故D错误;故选B。
典例7.我国自主研发的对二甲苯的绿色合成路线取得新进展,其合成示意图如下:
下列说法错误的是( )
A.过程i发生了加成反应
B.利用相同的原理以及相同的原料,也能合成间二甲苯
C.中间产物M的结构简式为
D.该合成路线理论上碳原子的利用率为100%,且最终得到的有机产物只能用蒸馏的方法进行分离
【答案】D
【解析】过程i是异戊二烯和丙醛发生加成反应生成中间产物M,故A正确;异戊二烯和丙醛发生加成反应有2种加成方式,可以合成对二甲苯和间二甲苯,但是不能合成邻二甲苯,故B正确;由M的球棍模型可知,甲基的邻位有一个双键,所以中间产物M的结构简式为:,故C正确;根据合成示意图可知:该合成路线分2步,第一步为加成反应,第二步为脱水反应,两步的碳原子利用率均为100%,最终得到的产物为对二甲苯和水,用分液的方法可将二者分离,不需要蒸馏,故D错误。
【跟踪练习】 基础过关
1. 在有机合成中,常需要将官能团消除或增加,且要求过程科学、简捷,下列相关过程不合理的是( )
A.乙烯乙二醇:CH2CH2
B.乙醇溴乙烷:CH3CH2OHCH2CH2CH3CH2Br
C.乙醛乙烯:CH3CHOCH3CH2OHCH2CH2
D.乙醇乙酸:CH3CH2OHCH3CHOCH3COOH
【答案】B
【解析】乙醇可以与氢溴酸发生取代反应生成溴乙烷,不需要先消去,再加成。
2. 甲基丙烯酸甲酯旧法合成的反应是(CH3)2C===O+HCN―→(CH3)2C(OH)CN,(CH3)2C(OH)CN+CH3OH+H2SO4―→CH2===C(CH3)COOCH3+NH4HSO4。20世纪90年代新法合成的反应是CH3C≡CH+CO+CH3OHCH2===C(CH3)COOCH3,与旧法比较,新法的优点是( )
A.原料无爆炸危险 B.原料都是无毒物质
C.没有副产物,原料利用率高 D.条件较简单
【答案】C
【解析】新法有CO、CH3OH参与,CO、CH3OH有毒且可燃,有爆炸危险,所以A、B两项错误;新法需要催化剂而旧法不用,所以D项错误;比较两种合成方法,新法的优点是没有副产物,原料利用率高,所以C项正确。
3. 下列说法不正确的是( )
A.可发生消去反应引入碳碳双键
B.可发生催化氧化反应引入羧基
C.CH3CH2Br可发生取代反应引入羟基
D.与CH2===CH2可发生加成反应引入环
【答案】B
【解析】上无氢原子,故不能发生催化氧化反应生成羧酸,B不正确。
4. 某石油化工产品X的转化关系如图所示,下列判断错误的是( )
A.X→Y是加成反应
B.乙酸→W是酯化反应,也是取代反应
C.Y能与钠反应产生氢气
D.W能与NaOH溶液反应,但不能与稀硫酸反应
【答案】D
【解析】X为石油化工产品,并结合图示转化关系可推知X为CH2==CH2,Y为C2H5OH,Z为CH3CHO,W为乙酸乙酯。乙酸乙酯与NaOH溶液和稀硫酸均能发生水解反应,D项不正确。
5. 已知醇在一定条件下经分子间脱水可以生成醚,以乙醇、浓硫酸、溴水、氢氧化钠的水溶液为主要原料合成。最佳合成路线中依次涉及的反应类型是( )
①氧化 ②还原 ③取代 ④加成 ⑤消去 ⑥中和 ⑦水解 ⑧酯化 ⑨加聚
A.⑤④⑥⑧ B.⑤④⑦③
C.②⑤④⑧ D.②④⑥⑧
【答案】B
【解析】 合成的最佳路线为:CH3CH2OH CH2===CH2
能力达成
6. (1)由环己醇制取己二酸己二酯,最简单的流程途径顺序正确的是 (填序号)。
已知:RCH2CH2R'RCHO+RCHO
①取代反应 ②加成反应 ③氧化反应 ④还原反应 ⑤消去反应 ⑥酯化反应 ⑦中和反应 ⑧缩聚反应
A.③②⑤⑥ B.⑤③④⑥ C.⑤②③⑥ D.⑤③④⑦
(2)写出制取己二酸己二酯最后一步反应的化学方程式: 。
(3)写出由环己醇制取1,2-环己二醇的流程图。
。
【答案】(1)B
(2)++2H2O
(3)
【解析】采用逆推法分析可得该制备过程的流程为:
已知:①环己烯可以通过1,3-丁二烯与乙烯发生环化加成反应得到:
+(也可表示为+||)。
②实验证明,下列反应中反应物分子的环外双键比环内双键更容易被氧化。
现仅以1,3-丁二烯为有机原料,无机试剂任选,按下列途径合成甲基环己烷:
1,3-丁二烯ABD
请按要求填空:
(1)A的结构简式为 ;B的结构简式为 。
(2)写出下列反应的化学方程式和反应类型。
反应④: ;对应反应类型为 。
反应⑤: ;对应反应类型为 。
【答案】(1)
(2)+H2O 消去反应
+H2 加成反应
【解析】由合成途径和信息①可推知,A是由两分子1,3-丁二烯经下列反应制得的:+;而由C的分子式C7H14O和信息②可知,B是A的氧化产物,其结构简式为;C是B的加成产物,其结构简式为。要得到,可先使C消去—OH得到D,化学方程式为+H2O,再由D发生加成反应得到甲基环己烷:+H2。
化妆品中防腐剂的作用主要是抑制微生物的生长和繁殖,保持化妆品的性质稳定,使其开盖使用后不 易变质,延长保存时间。用甲苯生产一种常用的化妆品防腐剂,其生产过程如图(反应条件没有全部注明)。
AB
回答下列问题:
(1)有机化合物A的结构简式为 。
(2)在合成路线中,设计第③步与第⑥步反应的目的是 。
(3)写出反应⑤的化学方程式: 。
(4)写出由生成C7H5O3Na的化学方程式: 。
(5)下列有关说法正确的是 (填字母)。
a.莽草酸、对羟基苯甲酸都属于芳香族化合物
b.1 mol莽草酸与NaOH溶液反应,最多消耗4 mol NaOH
c.二者均可以发生酯化、氧化、加成等反应
d.利用FeCl3溶液可区别莽草酸和对羟基苯甲酸
(6)写出同时符合下列要求的的所有同分异构体的结构简式: 。
a.含苯环;
b.可与FeCl3溶液发生显色反应;
c.苯环上的一氯代物有两种;
d.能发生银镜反应,不能发生水解反应。
【答案】(1) (2)保护酚羟基,防止其被氧化
(3)+C2H5OH+H2O
(4)+NaHCO3+H2O+CO2↑
(5)cd (6)、
【解析】(1)由可知,与氯气发生甲基对位取代,A的结构简式为。
(2)第③步反应是CH3I与酚羟基反应生成醚键,第⑥步反应是醚键与HI反应又重新生成酚羟基,目的是保护酚羟基,防止其在第④步中被氧化。
(3)反应⑤是羧酸与醇的酯化反应。
(4)由生成C7H5O3Na,说明只有—COOH参加反应而酚羟基没有参加反应,可选用NaHCO3溶液,因为NaOH、Na2CO3均能与酚羟基反应。
(5)a项,莽草酸中无苯环,错误;b项,1 mol莽草酸与NaOH溶液反应,最多消耗1 mol NaOH,错误。(6)根据题意可知,满足条件的同分异构体的结构中有—CHO和酚羟基,且根据分子中氧原子个数可判断其结构中有两个酚羟基;苯环上的一氯代物有两种,说明是对称结构。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
