8.1 自然资源的开发利用(第2课时 海水资源的开发利用)(解析版)-2022-2023学年高一化学同步素养目标精品讲义(人教版2019必修第二册)
文档属性
| 名称 | 8.1 自然资源的开发利用(第2课时 海水资源的开发利用)(解析版)-2022-2023学年高一化学同步素养目标精品讲义(人教版2019必修第二册) |  | |
| 格式 | docx | ||
| 文件大小 | 781.5KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-24 16:33:48 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
第八章 第一节 化学与可持续发展
第2课时 海水资源的开发利用
【学习目标】
1.能够说出海水中富含的元素,了解目前海水中可以提取哪些资源,知道开发、利用海洋资源的重要性。
2.通过了解海水淡化、海水制盐的方法,进一步加深对物质分离和提纯方法的理解。
3.以海水提镁、海水提溴为例,用化学视角找到物质转化、元素富集的途径,从而认识化学在自然资源开发和利用过程中的作用和贡献。
4.通过海水提溴工艺流程图的绘制和分析,形成工业提取物质的一般思路和方法。
【素养目标】
1.通过对海水提镁、海水提溴工艺的分析,培养学生“证据推理和模型认知”的学科素养。
2.通过学习海水中的资源开发及利用,认识化学在自然资源开发和利用过程中的作用和贡献。培养学生“科学精神和社会责任”的学科素养。
必备知识与关键能力
知识点一:海水水资源的利用
1.海水水资源利用,主要包括海水淡化和直接利用海水进行循环冷却等。
2.海水淡化:通过从海水中提取淡水或从海水中把盐分离出去,都可以达到淡化海水的目的。海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等。其中蒸馏法的历史最久,技术和工艺也比较成熟,但成本较高。
3.海水的蒸馏
(1)原理
(2)注意事项
①烧瓶需垫石棉网加热。
②烧瓶所盛液体不能超过烧瓶容量的,也不能少于。
③需向烧瓶中加几粒沸石或几片碎瓷片,以防液体暴沸。
④冷凝器里的冷却水要从冷凝器的下口进、上口出。
典例1. 下列关于海水的知识不正确的是( )
A.海水资源的利用包括海水水资源利用和化学资源利用
B.海水既苦又涩,不能直接利用
C.海水中某些金属元素总储量很大,但富集程度却很低
D.海水淡化应同化工生产结合,同能源技术结合
【答案】B
【解析】海水可直接利用,如冲厕、作冷却水等。
典例2. 若实现海水淡化供应饮用水,下列方法在原理上完全不可行的是( )
A.加明矾使海水中盐分沉淀而淡化
B.利用太阳能使海水蒸馏淡化
C.将海水电解,然后让两极气体燃烧得到饮用水
D.将海水通过离子交换树脂,以除去所含离子
【答案】A
【解析】明矾具有净水作用,可使海水中的悬浮物形成沉淀而除去,但不能使海水中盐分沉淀。
知识点二:海水的化学资源开发利用
1.海水中的化学资源
(1)海水中的化学元素
海水中含量最多的为O、H两种元素,还有Cl、Na、Mg、S、Ca、K、Br、C、Sr、B、F等11种元素。其他为微量元素,如Au。
(2)海水中化学资源的利用
2.海水制盐
海水粗盐精盐。
典例3.海水是一个巨大的化学资源宝库,下列有关海水综合利用的说法正确的是( )
A.海水中含有钾元素,只需经过物理变化就可以得到钾单质
B.海水蒸发制海盐的过程中只发生了化学变化
C.从海水中可以得到NaCl,电解熔融NaCl可制备Cl2
D.利用潮汐发电是将化学能转化为电能
【答案】C
【解析】海水中的钾元素是以化合态形式存在,要求化合态转化为游离态,一定发生氧化还原反应,A不正确;海水蒸发制海盐,是发生了物理变化,B错误;电解熔融NaCl可以制得Na和Cl2,C正确;潮汐发电是将机械能转化为电能,因此D也不正确。
3.海水提溴
海水提溴的常用方法是空气吹出法。
(1)主要流程
(2)主要反应
Cl2+2Br-===Br2+2Cl-(氧化)
Br2+SO2+2H2O===2HBr+H2SO4(富集)
Cl2+2Br-===Br2+2Cl-(提取)
典例4. 海水提溴过程中将Br-氧化成Br2,可向其中加入氧化剂,合适的是( )
A.酸性KMnO4溶液 B.氯水 C.FeCl3溶液 D.碘水
【答案】B
【解析】Fe3+和I2的氧化性都不如Br2的强,C、D不正确;酸性KMnO4溶液能氧化Br-,但KMnO4价格比较贵,不适合工业生产用。
典例5. 从海水中可以提取溴,但得到的液溴中常常有少量氯气,除去氯气应该采用的方法是( )
A.加入适量的Na2CO3溶液
B.通入溴蒸气
C.加入适量的NaOH溶液
D.加入适量的NaBr溶液
【答案】D
【解析】Na2CO3溶液和NaOH溶液都能与溴反应,不能用于除杂。
4.海带提碘
(1)海带中含有碘元素的检验
①关键反应的反应原理:2H++2I-+H2O2===I2+2H2O。
②实验步骤及证明方法:
(2)海带中提碘
①工艺流程:海带→浸泡→氧化→过滤→提纯→碘单质。
②主要的化学反应原理:Cl2+2KI===2KCl+I2。
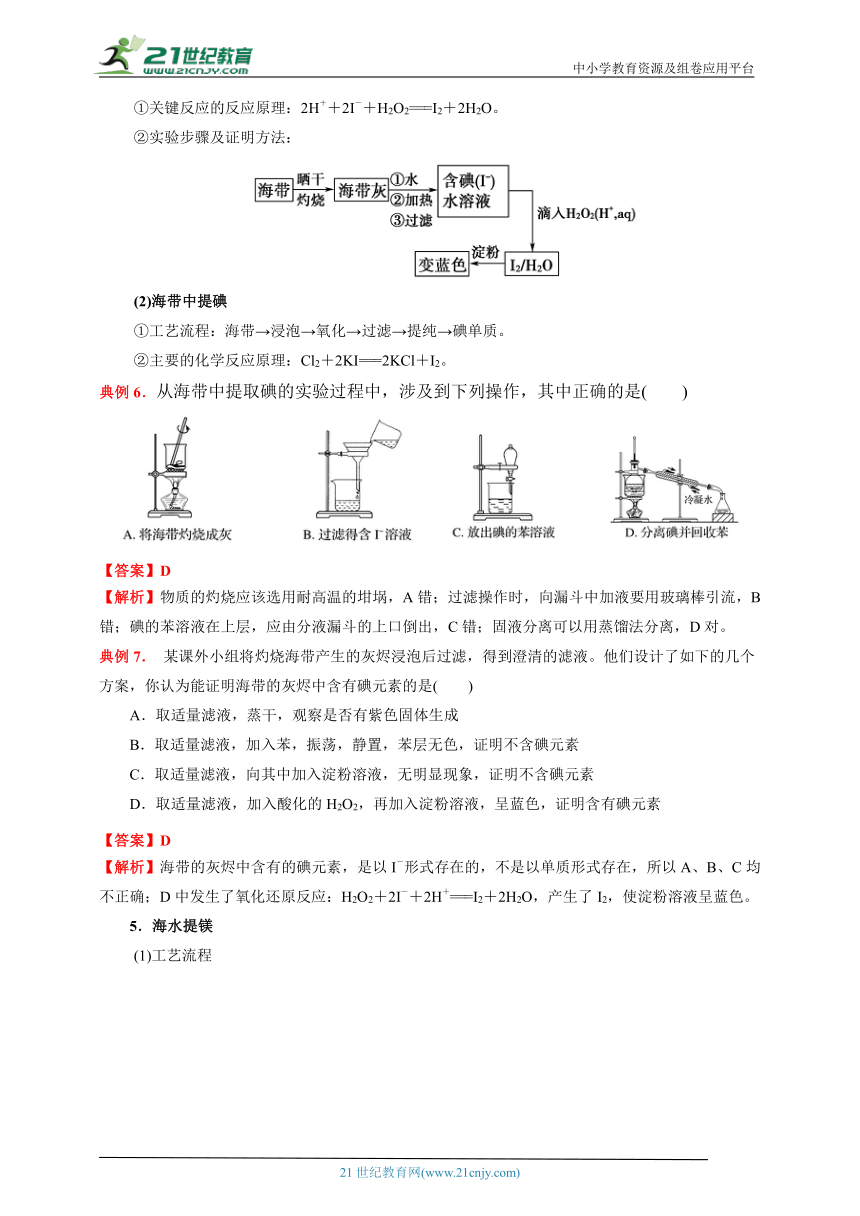
典例6.从海带中提取碘的实验过程中,涉及到下列操作,其中正确的是( )
【答案】D
【解析】物质的灼烧应该选用耐高温的坩埚,A错;过滤操作时,向漏斗中加液要用玻璃棒引流,B错;碘的苯溶液在上层,应由分液漏斗的上口倒出,C错;固液分离可以用蒸馏法分离,D对。
典例7. 某课外小组将灼烧海带产生的灰烬浸泡后过滤,得到澄清的滤液。他们设计了如下的几个方案,你认为能证明海带的灰烬中含有碘元素的是( )
A.取适量滤液,蒸干,观察是否有紫色固体生成
B.取适量滤液,加入苯,振荡,静置,苯层无色,证明不含碘元素
C.取适量滤液,向其中加入淀粉溶液,无明显现象,证明不含碘元素
D.取适量滤液,加入酸化的H2O2,再加入淀粉溶液,呈蓝色,证明含有碘元素
【答案】D
【解析】海带的灰烬中含有的碘元素,是以I-形式存在的,不是以单质形式存在,所以A、B、C均不正确;D中发生了氧化还原反应:H2O2+2I-+2H+===I2+2H2O,产生了I2,使淀粉溶液呈蓝色。
5.海水提镁
(1)工艺流程
(2)主要的化学反应原理
CaCO3CaO+CO2↑
CaO+H2O===Ca(OH)2
Ca(OH)2+MgCl2===Mg(OH)2↓+CaCl2
Mg(OH)2+2HCl===MgCl2+2H2O
MgCl2·6H2OMgCl2+6H2O;
MgCl2(熔融)Mg+Cl2↑
典例8.下表是氧化镁和氯化镁的熔、沸点数据:
物质 氧化镁 氯化镁
熔点/℃ 2 852 714
沸点/℃ 3 600 1 412
请参考以上数据分析,从海水中提取镁,正确的方法是( )
A.海水Mg(OH)2Mg
B.海水MgCl2溶液―→MgCl2晶体Mg
C.海水Mg(OH)2MgOMg
D.海水Mg(OH)2MgCl2溶液MgCl2(熔融)Mg
【答案】D
【解析】本题要求学生既要知道镁是由电解熔融的MgCl2得到,还要知道实际生产中从海水提取MgCl2的途径及原料的合理使用(用石灰乳而不用NaOH)。
6.新能源的开发
(1)从海水中提取铀和重水,铀和重水是核能开发的重要原料。
(2)潮汐能、波浪能是待开发的新型能源。
核心价值与学科素养
【知识结构化】
【跟踪练习】 基础过关
检验海带中碘元素的实验中,发生如下反应:2H++2I-+H2O2===I2+2H2O,下列对该反应的叙述中不正确的是( )
A.I2为氧化产物
B.H2O2既作氧化剂又作还原剂
C.氧化性强弱顺序为H2O2>I2
D.生成1 mol I2时转移2 mol电子
【答案】B
【解析】2I-+H2O2+2H+===I失2×e-2+2H2O得2×e-,该反应中I2为氧化产物,H2O2作氧化剂,根据氧化性由强到弱的顺序为氧化剂>氧化产物,所以氧化性H2O2>I2;反应中每生成1 mol I2,转移2 mol电子。
从海水中提取金属镁的生产步骤有:①浓缩结晶 ②加熟石灰 ③加盐酸 ④过滤 ⑤熔融电解,正确的操作顺序是( )
A.①②③④⑤ B.⑤④③①②
C.②④③①⑤ D.③④②①⑤
【答案】C
【解析】海水中含有Mg2+,加入Ca(OH)2可生成Mg(OH)2沉淀:Mg2++2OH-===Mg(OH)2↓,过滤可得到Mg(OH)2固体。再将Mg(OH)2转化为MgCl2,MgCl2熔点低,电解熔融MgCl2可得金属镁:MgCl2(熔融)Mg+Cl2↑。
从淡化海水中提取溴的流程如下图所示,下列有关说法错误的是( )
A.X为SO2气体,也可将SO2换成Na2SO3
B.设备Y为蒸馏塔
C.在提取溴的过程中一定有Br-被氧化
D.工业上,每获得1 mol Br2,需要消耗Cl2体积最多为44.8 L(标准状况)
【答案】C
【解析】 D 因为溴离子要经过二次氧化,因此工业上每获得1 molBr2,需要消耗Cl2的体积最少为44.8 L(标准状态下),错误。
碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间的转化关系如图所示。
下列说法中不正确的是( )
A.用淀粉 KI试纸和食醋检验加碘盐时淀粉 KI试纸会变蓝
B.足量Cl2能使湿润的、已变蓝的淀粉 KI试纸褪色,原因可能是5Cl2+I2+6H2O===2HIO3+10HCl
C.由图可知氧化性的强弱顺序为Cl2>I2>IO
D.途径Ⅱ中若生成1 mol I2,则反应中转移的电子数为10NA
【答案】C
【解析】加碘盐中含有IO,在酸性条件下可被I-还原生成I2, A正确;根据图示转化关系可知B正确;根据途径Ⅰ可知氧化性Cl2>I2,根据途径Ⅱ可知氧化性IO>I2,根据途径Ⅲ可知氧化性Cl2>IO,C错误;根据关系式2IO~I2~10e-,D正确。
从淡化海水中提取溴的流程如下:
下列有关说法不正确的是( )
A.X试剂可用Na2SO3饱和溶液
B.步骤Ⅲ的离子反应:2Br-+Cl2===2Cl-+Br2
C.工业上每获得1 mol Br2,需要消耗Cl2 44.8 L
D.步骤Ⅳ包含萃取、分液和蒸馏
【答案】C
【解析】Na2SO3+Br2+H2O===Na2SO4+2HBr,A正确;步骤Ⅲ利用氯的非金属性比溴强,可以利用置换反应制取Br2,B正确;反应Ⅰ和反应Ⅲ均使用到Cl2,故制取1 mol Br2消耗2 mol氯气,但未标明氯气所处的温度和压强,C错误;从浓溴水中提取溴,可利用有机溶剂(如苯)萃取溴,然后分液得到溴的有机溶液,再经蒸馏可得到纯净的溴,D正确。
能力达成
海水是可以综合利用的。从海水中提取食盐和溴的过程如下:
(1)请写出一种海水淡化的方法:_____________________________________。
(2)步骤Ⅰ获取Br2的离子方程式为___________________________________。
(3)步骤Ⅱ用SO2水溶液吸收Br2,使溴蒸气转化为氢溴酸以达到富集的目的。其反应的化学方程式为Br2+SO2+2H2O===H2SO4+2HBr,在该反应中,还原剂是________________(填化学式)。若反应中生成4 mol HBr,则消耗________mol SO2。
【答案】 (1)蒸馏法 (2)Cl2+2Br-===Br2+2Cl- (3)SO2 2
【解析】海水淡化的方法有蒸馏法、电渗析法、离子交换法等。海水淡化后得到NaCl,电解其熔融态可生成Na和Cl2,利用生成的Cl2氧化浓缩海水中的Br-得到Br2,离子反应方程式为Cl2+2Br-===Br2+2Cl-,然后通入空气,吹出Br2,再用SO2吸收Br2,发生反应的化学方程式为Br2+SO2+2H2O===H2SO4+2HBr,该反应中氧化剂为Br2,还原剂为SO2,反应中每生成4 mol HBr,则消耗2 mol SO2,最后再向含HBr的溶液中通入适量Cl2,蒸馏得到Br2。
海洋植物如海带、海藻中含有丰富的碘元素。碘元素以碘离子的形式存在。实验室从海藻中提取碘的流程如下:
(1)指出从海藻中提取I2的实验操作名称:①________________,③________________,
②的离子方程式______________________________________________。
(2)提取碘的过程中,可供选择的有机溶剂是( )
A.甲苯、酒精 B.四氯化碳、苯
C.汽油、乙酸 D.汽油、甘油
(3)为使海藻中I-转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器。还缺少的仪器是 。
(4)从含碘的有机溶剂中提取碘,还要经过蒸馏,指出下列蒸馏装置中的错误之处_______________________________________________________________。
(5)进行蒸馏操作时,使用水浴加热的原因是________,最后晶态碘在________中。
【答案】(1)过滤 萃取 2I-+Cl2===I2+2Cl- (2)B (3)分液漏斗,普通漏斗
(4)见解析 (5)萃取剂沸点较低,I2易升华 烧瓶
【解析】(1)为了从悬浊液中分离I-,应用过滤;从I2的水溶液中把它提取出来,应用萃取。(2)A中酒精,C中乙酸,D中甘油,都是易溶于水的物质,所以不能用于萃取碘。(3)萃取分液所必需的仪器是分液漏斗,过滤时所需仪器必有普通漏斗。(4)蒸馏的三点错误:①没有石棉网;②温度计插入液面以下;③冷凝管进、出水方向颠倒。(5)酒精、乙酸、甘油均不能做为I2的萃取剂。
镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下:
(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用________,要使MgSO4完全转化为沉淀,加入试剂的量应为________________。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是_______________________________。
(3)试剂②选用________;写出其反应的离子方程式________________________________。
(4)无水MgCl2在熔融状态下,通电后产生镁和氯气,该反应的化学方程式为___________________。
【答案】(1)石灰乳 过量 (2)过滤 (3)盐酸 Mg(OH)2+2H+===Mg2++2H2O
(4)MgCl2(熔融)Mg+Cl2↑
【解析】(1)工业上常加入廉价的石灰乳使海水中的MgSO4转化为Mg(OH)2;为使MgSO4完全转化为Mg(OH)2,应加入过量石灰乳。(2)加入石灰乳产生Mg(OH)2,通过过滤将Mg(OH)2分离出来。(3)用盐酸溶解Mg(OH)2,反应的离子方程式为Mg(OH)2+2H+===Mg2++2H2O(4)工业上电解熔融MgCl2制取Mg,反应的化学方程式为MgCl2(熔融)Mg+Cl2↑
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
第八章 第一节 化学与可持续发展
第2课时 海水资源的开发利用
【学习目标】
1.能够说出海水中富含的元素,了解目前海水中可以提取哪些资源,知道开发、利用海洋资源的重要性。
2.通过了解海水淡化、海水制盐的方法,进一步加深对物质分离和提纯方法的理解。
3.以海水提镁、海水提溴为例,用化学视角找到物质转化、元素富集的途径,从而认识化学在自然资源开发和利用过程中的作用和贡献。
4.通过海水提溴工艺流程图的绘制和分析,形成工业提取物质的一般思路和方法。
【素养目标】
1.通过对海水提镁、海水提溴工艺的分析,培养学生“证据推理和模型认知”的学科素养。
2.通过学习海水中的资源开发及利用,认识化学在自然资源开发和利用过程中的作用和贡献。培养学生“科学精神和社会责任”的学科素养。
必备知识与关键能力
知识点一:海水水资源的利用
1.海水水资源利用,主要包括海水淡化和直接利用海水进行循环冷却等。
2.海水淡化:通过从海水中提取淡水或从海水中把盐分离出去,都可以达到淡化海水的目的。海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等。其中蒸馏法的历史最久,技术和工艺也比较成熟,但成本较高。
3.海水的蒸馏
(1)原理
(2)注意事项
①烧瓶需垫石棉网加热。
②烧瓶所盛液体不能超过烧瓶容量的,也不能少于。
③需向烧瓶中加几粒沸石或几片碎瓷片,以防液体暴沸。
④冷凝器里的冷却水要从冷凝器的下口进、上口出。
典例1. 下列关于海水的知识不正确的是( )
A.海水资源的利用包括海水水资源利用和化学资源利用
B.海水既苦又涩,不能直接利用
C.海水中某些金属元素总储量很大,但富集程度却很低
D.海水淡化应同化工生产结合,同能源技术结合
【答案】B
【解析】海水可直接利用,如冲厕、作冷却水等。
典例2. 若实现海水淡化供应饮用水,下列方法在原理上完全不可行的是( )
A.加明矾使海水中盐分沉淀而淡化
B.利用太阳能使海水蒸馏淡化
C.将海水电解,然后让两极气体燃烧得到饮用水
D.将海水通过离子交换树脂,以除去所含离子
【答案】A
【解析】明矾具有净水作用,可使海水中的悬浮物形成沉淀而除去,但不能使海水中盐分沉淀。
知识点二:海水的化学资源开发利用
1.海水中的化学资源
(1)海水中的化学元素
海水中含量最多的为O、H两种元素,还有Cl、Na、Mg、S、Ca、K、Br、C、Sr、B、F等11种元素。其他为微量元素,如Au。
(2)海水中化学资源的利用
2.海水制盐
海水粗盐精盐。
典例3.海水是一个巨大的化学资源宝库,下列有关海水综合利用的说法正确的是( )
A.海水中含有钾元素,只需经过物理变化就可以得到钾单质
B.海水蒸发制海盐的过程中只发生了化学变化
C.从海水中可以得到NaCl,电解熔融NaCl可制备Cl2
D.利用潮汐发电是将化学能转化为电能
【答案】C
【解析】海水中的钾元素是以化合态形式存在,要求化合态转化为游离态,一定发生氧化还原反应,A不正确;海水蒸发制海盐,是发生了物理变化,B错误;电解熔融NaCl可以制得Na和Cl2,C正确;潮汐发电是将机械能转化为电能,因此D也不正确。
3.海水提溴
海水提溴的常用方法是空气吹出法。
(1)主要流程
(2)主要反应
Cl2+2Br-===Br2+2Cl-(氧化)
Br2+SO2+2H2O===2HBr+H2SO4(富集)
Cl2+2Br-===Br2+2Cl-(提取)
典例4. 海水提溴过程中将Br-氧化成Br2,可向其中加入氧化剂,合适的是( )
A.酸性KMnO4溶液 B.氯水 C.FeCl3溶液 D.碘水
【答案】B
【解析】Fe3+和I2的氧化性都不如Br2的强,C、D不正确;酸性KMnO4溶液能氧化Br-,但KMnO4价格比较贵,不适合工业生产用。
典例5. 从海水中可以提取溴,但得到的液溴中常常有少量氯气,除去氯气应该采用的方法是( )
A.加入适量的Na2CO3溶液
B.通入溴蒸气
C.加入适量的NaOH溶液
D.加入适量的NaBr溶液
【答案】D
【解析】Na2CO3溶液和NaOH溶液都能与溴反应,不能用于除杂。
4.海带提碘
(1)海带中含有碘元素的检验
①关键反应的反应原理:2H++2I-+H2O2===I2+2H2O。
②实验步骤及证明方法:
(2)海带中提碘
①工艺流程:海带→浸泡→氧化→过滤→提纯→碘单质。
②主要的化学反应原理:Cl2+2KI===2KCl+I2。
典例6.从海带中提取碘的实验过程中,涉及到下列操作,其中正确的是( )
【答案】D
【解析】物质的灼烧应该选用耐高温的坩埚,A错;过滤操作时,向漏斗中加液要用玻璃棒引流,B错;碘的苯溶液在上层,应由分液漏斗的上口倒出,C错;固液分离可以用蒸馏法分离,D对。
典例7. 某课外小组将灼烧海带产生的灰烬浸泡后过滤,得到澄清的滤液。他们设计了如下的几个方案,你认为能证明海带的灰烬中含有碘元素的是( )
A.取适量滤液,蒸干,观察是否有紫色固体生成
B.取适量滤液,加入苯,振荡,静置,苯层无色,证明不含碘元素
C.取适量滤液,向其中加入淀粉溶液,无明显现象,证明不含碘元素
D.取适量滤液,加入酸化的H2O2,再加入淀粉溶液,呈蓝色,证明含有碘元素
【答案】D
【解析】海带的灰烬中含有的碘元素,是以I-形式存在的,不是以单质形式存在,所以A、B、C均不正确;D中发生了氧化还原反应:H2O2+2I-+2H+===I2+2H2O,产生了I2,使淀粉溶液呈蓝色。
5.海水提镁
(1)工艺流程
(2)主要的化学反应原理
CaCO3CaO+CO2↑
CaO+H2O===Ca(OH)2
Ca(OH)2+MgCl2===Mg(OH)2↓+CaCl2
Mg(OH)2+2HCl===MgCl2+2H2O
MgCl2·6H2OMgCl2+6H2O;
MgCl2(熔融)Mg+Cl2↑
典例8.下表是氧化镁和氯化镁的熔、沸点数据:
物质 氧化镁 氯化镁
熔点/℃ 2 852 714
沸点/℃ 3 600 1 412
请参考以上数据分析,从海水中提取镁,正确的方法是( )
A.海水Mg(OH)2Mg
B.海水MgCl2溶液―→MgCl2晶体Mg
C.海水Mg(OH)2MgOMg
D.海水Mg(OH)2MgCl2溶液MgCl2(熔融)Mg
【答案】D
【解析】本题要求学生既要知道镁是由电解熔融的MgCl2得到,还要知道实际生产中从海水提取MgCl2的途径及原料的合理使用(用石灰乳而不用NaOH)。
6.新能源的开发
(1)从海水中提取铀和重水,铀和重水是核能开发的重要原料。
(2)潮汐能、波浪能是待开发的新型能源。
核心价值与学科素养
【知识结构化】
【跟踪练习】 基础过关
检验海带中碘元素的实验中,发生如下反应:2H++2I-+H2O2===I2+2H2O,下列对该反应的叙述中不正确的是( )
A.I2为氧化产物
B.H2O2既作氧化剂又作还原剂
C.氧化性强弱顺序为H2O2>I2
D.生成1 mol I2时转移2 mol电子
【答案】B
【解析】2I-+H2O2+2H+===I失2×e-2+2H2O得2×e-,该反应中I2为氧化产物,H2O2作氧化剂,根据氧化性由强到弱的顺序为氧化剂>氧化产物,所以氧化性H2O2>I2;反应中每生成1 mol I2,转移2 mol电子。
从海水中提取金属镁的生产步骤有:①浓缩结晶 ②加熟石灰 ③加盐酸 ④过滤 ⑤熔融电解,正确的操作顺序是( )
A.①②③④⑤ B.⑤④③①②
C.②④③①⑤ D.③④②①⑤
【答案】C
【解析】海水中含有Mg2+,加入Ca(OH)2可生成Mg(OH)2沉淀:Mg2++2OH-===Mg(OH)2↓,过滤可得到Mg(OH)2固体。再将Mg(OH)2转化为MgCl2,MgCl2熔点低,电解熔融MgCl2可得金属镁:MgCl2(熔融)Mg+Cl2↑。
从淡化海水中提取溴的流程如下图所示,下列有关说法错误的是( )
A.X为SO2气体,也可将SO2换成Na2SO3
B.设备Y为蒸馏塔
C.在提取溴的过程中一定有Br-被氧化
D.工业上,每获得1 mol Br2,需要消耗Cl2体积最多为44.8 L(标准状况)
【答案】C
【解析】 D 因为溴离子要经过二次氧化,因此工业上每获得1 molBr2,需要消耗Cl2的体积最少为44.8 L(标准状态下),错误。
碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间的转化关系如图所示。
下列说法中不正确的是( )
A.用淀粉 KI试纸和食醋检验加碘盐时淀粉 KI试纸会变蓝
B.足量Cl2能使湿润的、已变蓝的淀粉 KI试纸褪色,原因可能是5Cl2+I2+6H2O===2HIO3+10HCl
C.由图可知氧化性的强弱顺序为Cl2>I2>IO
D.途径Ⅱ中若生成1 mol I2,则反应中转移的电子数为10NA
【答案】C
【解析】加碘盐中含有IO,在酸性条件下可被I-还原生成I2, A正确;根据图示转化关系可知B正确;根据途径Ⅰ可知氧化性Cl2>I2,根据途径Ⅱ可知氧化性IO>I2,根据途径Ⅲ可知氧化性Cl2>IO,C错误;根据关系式2IO~I2~10e-,D正确。
从淡化海水中提取溴的流程如下:
下列有关说法不正确的是( )
A.X试剂可用Na2SO3饱和溶液
B.步骤Ⅲ的离子反应:2Br-+Cl2===2Cl-+Br2
C.工业上每获得1 mol Br2,需要消耗Cl2 44.8 L
D.步骤Ⅳ包含萃取、分液和蒸馏
【答案】C
【解析】Na2SO3+Br2+H2O===Na2SO4+2HBr,A正确;步骤Ⅲ利用氯的非金属性比溴强,可以利用置换反应制取Br2,B正确;反应Ⅰ和反应Ⅲ均使用到Cl2,故制取1 mol Br2消耗2 mol氯气,但未标明氯气所处的温度和压强,C错误;从浓溴水中提取溴,可利用有机溶剂(如苯)萃取溴,然后分液得到溴的有机溶液,再经蒸馏可得到纯净的溴,D正确。
能力达成
海水是可以综合利用的。从海水中提取食盐和溴的过程如下:
(1)请写出一种海水淡化的方法:_____________________________________。
(2)步骤Ⅰ获取Br2的离子方程式为___________________________________。
(3)步骤Ⅱ用SO2水溶液吸收Br2,使溴蒸气转化为氢溴酸以达到富集的目的。其反应的化学方程式为Br2+SO2+2H2O===H2SO4+2HBr,在该反应中,还原剂是________________(填化学式)。若反应中生成4 mol HBr,则消耗________mol SO2。
【答案】 (1)蒸馏法 (2)Cl2+2Br-===Br2+2Cl- (3)SO2 2
【解析】海水淡化的方法有蒸馏法、电渗析法、离子交换法等。海水淡化后得到NaCl,电解其熔融态可生成Na和Cl2,利用生成的Cl2氧化浓缩海水中的Br-得到Br2,离子反应方程式为Cl2+2Br-===Br2+2Cl-,然后通入空气,吹出Br2,再用SO2吸收Br2,发生反应的化学方程式为Br2+SO2+2H2O===H2SO4+2HBr,该反应中氧化剂为Br2,还原剂为SO2,反应中每生成4 mol HBr,则消耗2 mol SO2,最后再向含HBr的溶液中通入适量Cl2,蒸馏得到Br2。
海洋植物如海带、海藻中含有丰富的碘元素。碘元素以碘离子的形式存在。实验室从海藻中提取碘的流程如下:
(1)指出从海藻中提取I2的实验操作名称:①________________,③________________,
②的离子方程式______________________________________________。
(2)提取碘的过程中,可供选择的有机溶剂是( )
A.甲苯、酒精 B.四氯化碳、苯
C.汽油、乙酸 D.汽油、甘油
(3)为使海藻中I-转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器。还缺少的仪器是 。
(4)从含碘的有机溶剂中提取碘,还要经过蒸馏,指出下列蒸馏装置中的错误之处_______________________________________________________________。
(5)进行蒸馏操作时,使用水浴加热的原因是________,最后晶态碘在________中。
【答案】(1)过滤 萃取 2I-+Cl2===I2+2Cl- (2)B (3)分液漏斗,普通漏斗
(4)见解析 (5)萃取剂沸点较低,I2易升华 烧瓶
【解析】(1)为了从悬浊液中分离I-,应用过滤;从I2的水溶液中把它提取出来,应用萃取。(2)A中酒精,C中乙酸,D中甘油,都是易溶于水的物质,所以不能用于萃取碘。(3)萃取分液所必需的仪器是分液漏斗,过滤时所需仪器必有普通漏斗。(4)蒸馏的三点错误:①没有石棉网;②温度计插入液面以下;③冷凝管进、出水方向颠倒。(5)酒精、乙酸、甘油均不能做为I2的萃取剂。
镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下:
(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用________,要使MgSO4完全转化为沉淀,加入试剂的量应为________________。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是_______________________________。
(3)试剂②选用________;写出其反应的离子方程式________________________________。
(4)无水MgCl2在熔融状态下,通电后产生镁和氯气,该反应的化学方程式为___________________。
【答案】(1)石灰乳 过量 (2)过滤 (3)盐酸 Mg(OH)2+2H+===Mg2++2H2O
(4)MgCl2(熔融)Mg+Cl2↑
【解析】(1)工业上常加入廉价的石灰乳使海水中的MgSO4转化为Mg(OH)2;为使MgSO4完全转化为Mg(OH)2,应加入过量石灰乳。(2)加入石灰乳产生Mg(OH)2,通过过滤将Mg(OH)2分离出来。(3)用盐酸溶解Mg(OH)2,反应的离子方程式为Mg(OH)2+2H+===Mg2++2H2O(4)工业上电解熔融MgCl2制取Mg,反应的化学方程式为MgCl2(熔融)Mg+Cl2↑
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
