质量守恒定律应用学案
图片预览

文档简介
《质量守恒定律的应用》专题学案(拓展课)
主编:刘振中 学生: 班级: 日期:
一、微观导读——质量守恒定律的实质
二、考点解读:质量守恒定律的应用
【考点1】.质量守恒定律的实质
1.在下列各项中,化学反应前后,肯定没有发生改变的是( )
①原子的数目 ②分子的数目 ③元素的种类
④物质的总质量 ⑤物质的种类 ⑥原子的种类
A.①③④⑤ B.①③④⑥ C.①④⑥ D.①③⑤
2.下列现象可用质量守恒定律解释的是( )
A.10g水受热变成10g水蒸气
B.5g蔗糖溶于95g水中所得糖水的总质量为100g
C.铁钉生锈后,其固体的总质量增加
D.足量的硫在10L氧气中燃烧生成10L二氧化硫
【考点2】.求某个反应物或生成物的质量
1.在化学反应A+B==C+D中,15gA和足量的B充分
反应,生成12gC和16gD,则消耗B的质量是 。
2.在化学反应A+B==C+D中,5gA ( http: / / www.21cnjy.com )和足量的10gB恰好完全反应生成8gC,若用2.5gA和足量的B反应,可生成D的质量是 。
3.若24.5g氯酸钾和2g二氧化锰的混合 ( http: / / www.21cnjy.com )物加热到质量不再减少为止,得到剩余固体的质量为16.9g,则反应生成氧气的质量为 ,同时生成氯化钾的质量为 。
【考点3】.推知反应物或生成物的组成
1.已知某化合物X燃烧时所发生的化学方程式为:
X+2O2CO2+2H2O,据此推知X的化学式( )
A.CH4 B.C2H4 C.C6H6 D.C2H2
2.为了能及时发现煤气泄漏,常在煤气中加入少量有特殊气味的乙硫醇,乙硫醇燃烧的化学方程式为:2X+9O24CO2+6H2O+2SO2。则乙硫醇(X)的化学式是( )
A.C2H3SH B.CH3SH C.C2H5SH D.C2H5OH
3.硝化甘油(C3H5N3O9)可用于治疗心绞疼,因为它在人体内会被缓慢氧化生成A气体,化学方程式为:4C3H5N3O9+5O212A+12CO2+10H2O,则A的化学式为( )
A.NO B. NO2 C.N2 D.N2O
4.工业上常用乙炔燃烧产生的高温火焰来切割金属。若用R表示乙炔的化学式,其燃烧的化学方程式为:2R+5O24CO2+2H2O,则R的化学式为( )
A.C2H2 B. C2H4 C. C2H6 D. C2H5OH
5.某物质在空气中燃烧后,生成二氧化碳和水,则该化合物的组成中( )
A.只含碳元素和氢元素
B.一定含碳、氢元素,可能含氧元素
C.只含碳元素和氧元素
D.一定含碳、氢、氧三种元素
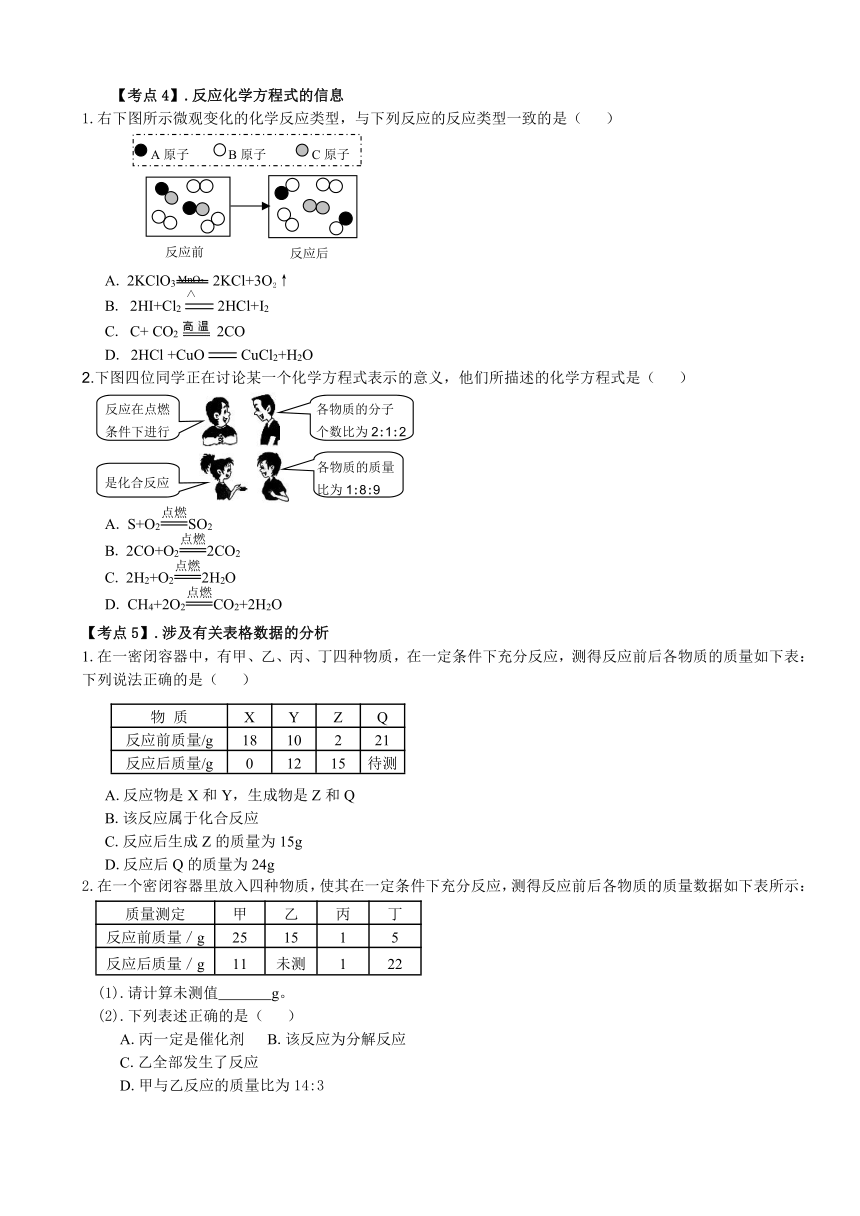
【考点4】.反应化学方程式的信息
1.右下图所示微观变化的化学反应类型,与下列反应的反应类型一致的是( )
A. 2KClO3 2KCl+3O2↑
B. 2HI+Cl22HCl+I2
C. C+ CO2 2CO
D. 2HCl +CuOCuCl2+H2O
2.下图四位同学正在讨论某一个化学方程式表示的意义,他们所描述的化学方程式是( )
A. S+O2SO2
B. 2CO+O22CO2
C. 2H2+O22H2O
D. CH4+2O2CO2+2H2O
【考点5】.涉及有关表格数据的分析
1.在一密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:下列说法正确的是( )
A.反应物是X和Y,生成物是Z和Q
B.该反应属于化合反应
C.反应后生成Z的质量为15g
D.反应后Q的质量为24g
2.在一个密闭容器里放入四种物质,使其在一定条件下充分反应,测得反应前后各物质的质量数据如下表所示:
(1).请计算未测值 g。
(2).下列表述正确的是( )
A.丙一定是催化剂 B.该反应为分解反应
C.乙全部发生了反应
D.甲与乙反应的质量比为14:3
3.一个密闭容器中有四种物质,在一定条件下发生反应,测得反应前后各物质的质量如(下表)所示。下列推理正确的是( )
A. Y一定是该反应的催化剂
B.该反应属于化合反应
C.反应后Q的质量为10g
D.该反应中消耗X与Q的质量之比为4:11
4.在一个密闭容器中放入甲、乙、丙、丁四种物质充分反应,在一段时间后,测得有关数据如下,则下列说法中,不正确的是( )
A.反应后物质甲的质量为13g
B.乙是反应物
C.反应中乙、丁的质量比为5:4
D.物质丙可能是该反应的催化剂
【考点6】.涉及有关微观图型的赏析
1.如图是密闭体系中,某个化学反应前、后各种物质的微观模拟图,图中“○”“●”表示两种不同元素的原子。根据
图示回答:
(1)该化学反应中,参加反应的 和 与反应后生成的 各粒子间的个数比为 。
(2)该反应所属的基本反应类型是 反应。
(3)该反应中的生成物 (填“可能”或“不可能”)属于氧化物。
2.右图是密闭体系中某反应的微观示意图,“○”和
“●”表示不同原子。
(1)反应后方框内应再填入
1个 微粒(选填序号)。
A. B. C.
(2)该反应所属的基本反应类型是 反应。
(3)写出符合该微观示意图的一个具体反应化学方程式 。
3.如下图所示:2个甲分子反应生成1个丙分子和3个乙分子。下列判断不正确的是( )
A.该反应的基本反应类型为分解反应
B.参加反应的甲物质属于化合物
C.该化学反应中原子的种类发生了改变
D.依质量守恒定律,1个乙分子含有2个A原子
4.“三效催化转换器”可将汽车尾气中的有毒气体处理为无污染的气体,下图为该反应的微观示意图(未配平)。下列说法不正确的是( )
A.该反应中共有三种元素
B.乙和丙中所含元素种类相同
C.甲和丁中同种元素化合价不相同
D.化学方程式中乙、丁的化学计量数均为1
5.已知某两种物质在光照条件下能发生化学反应,其微观示意图如下,则下列说法正确的是( )
A.图示中的反应物都是单质
B.图示中共有4种分子
C.该反应属于分解反应
D.该图示不符合质量守恒定律
五个一定不变:物质的总质量、元素种类(宏观)
原子的种类、原子的数目、原子的质量(实质)
两个一定改变:物质种类(宏观)、分子种类(微观)
一个可能改变:分子个数(微观)
H
H
H
O
O
H
H
O
O
通电
H
+
H
H
H
O
H
H
O
水分子 氧原子 氢原子 氧分子 氢分子
H
质量守恒定律的关键词: 变化, 关系。
反应化学方程式:2H2O2H2↑+ O2↑
通电
A原子 B原子 C原子
反应前
反应后
MnO2
△
各物质的分子
个数比为2:1:2
各物质的质量
比为1:8:9
反应在点燃
条件下进行
是化合反应
点燃
点燃
点燃
点燃
物 质 X Y Z Q
反应前质量/g 18 10 2 21
反应后质量/g 0 12 15 待测
质量测定 甲 乙 丙 丁
反应前质量/g 25 15 1 5
反应后质量/g 11 未测 1 22
物 质 X Y Z Q
反应前质量/g 4 10 1 21
反应后质量/g 0 10 15 待测
物 质 甲 乙 丙 丁
反应前质量/g 18 1 2 32
反应后质量/g 26 2 12
反应前
反应后
+
3乙+
+
甲 甲
丙
表示A原子
表示B原子
b.收集气体 c.检查装置气密性 d.验满 e.清洗仪器、整理桌面
表示B原子
+
催化剂
+
+
甲 乙 丙 丁
黄
蓝
蓝
黑
蓝
黑
蓝
蓝
黄
黄
(说明:一种小球代表一种原子)
主编:刘振中 学生: 班级: 日期:
一、微观导读——质量守恒定律的实质
二、考点解读:质量守恒定律的应用
【考点1】.质量守恒定律的实质
1.在下列各项中,化学反应前后,肯定没有发生改变的是( )
①原子的数目 ②分子的数目 ③元素的种类
④物质的总质量 ⑤物质的种类 ⑥原子的种类
A.①③④⑤ B.①③④⑥ C.①④⑥ D.①③⑤
2.下列现象可用质量守恒定律解释的是( )
A.10g水受热变成10g水蒸气
B.5g蔗糖溶于95g水中所得糖水的总质量为100g
C.铁钉生锈后,其固体的总质量增加
D.足量的硫在10L氧气中燃烧生成10L二氧化硫
【考点2】.求某个反应物或生成物的质量
1.在化学反应A+B==C+D中,15gA和足量的B充分
反应,生成12gC和16gD,则消耗B的质量是 。
2.在化学反应A+B==C+D中,5gA ( http: / / www.21cnjy.com )和足量的10gB恰好完全反应生成8gC,若用2.5gA和足量的B反应,可生成D的质量是 。
3.若24.5g氯酸钾和2g二氧化锰的混合 ( http: / / www.21cnjy.com )物加热到质量不再减少为止,得到剩余固体的质量为16.9g,则反应生成氧气的质量为 ,同时生成氯化钾的质量为 。
【考点3】.推知反应物或生成物的组成
1.已知某化合物X燃烧时所发生的化学方程式为:
X+2O2CO2+2H2O,据此推知X的化学式( )
A.CH4 B.C2H4 C.C6H6 D.C2H2
2.为了能及时发现煤气泄漏,常在煤气中加入少量有特殊气味的乙硫醇,乙硫醇燃烧的化学方程式为:2X+9O24CO2+6H2O+2SO2。则乙硫醇(X)的化学式是( )
A.C2H3SH B.CH3SH C.C2H5SH D.C2H5OH
3.硝化甘油(C3H5N3O9)可用于治疗心绞疼,因为它在人体内会被缓慢氧化生成A气体,化学方程式为:4C3H5N3O9+5O212A+12CO2+10H2O,则A的化学式为( )
A.NO B. NO2 C.N2 D.N2O
4.工业上常用乙炔燃烧产生的高温火焰来切割金属。若用R表示乙炔的化学式,其燃烧的化学方程式为:2R+5O24CO2+2H2O,则R的化学式为( )
A.C2H2 B. C2H4 C. C2H6 D. C2H5OH
5.某物质在空气中燃烧后,生成二氧化碳和水,则该化合物的组成中( )
A.只含碳元素和氢元素
B.一定含碳、氢元素,可能含氧元素
C.只含碳元素和氧元素
D.一定含碳、氢、氧三种元素
【考点4】.反应化学方程式的信息
1.右下图所示微观变化的化学反应类型,与下列反应的反应类型一致的是( )
A. 2KClO3 2KCl+3O2↑
B. 2HI+Cl22HCl+I2
C. C+ CO2 2CO
D. 2HCl +CuOCuCl2+H2O
2.下图四位同学正在讨论某一个化学方程式表示的意义,他们所描述的化学方程式是( )
A. S+O2SO2
B. 2CO+O22CO2
C. 2H2+O22H2O
D. CH4+2O2CO2+2H2O
【考点5】.涉及有关表格数据的分析
1.在一密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:下列说法正确的是( )
A.反应物是X和Y,生成物是Z和Q
B.该反应属于化合反应
C.反应后生成Z的质量为15g
D.反应后Q的质量为24g
2.在一个密闭容器里放入四种物质,使其在一定条件下充分反应,测得反应前后各物质的质量数据如下表所示:
(1).请计算未测值 g。
(2).下列表述正确的是( )
A.丙一定是催化剂 B.该反应为分解反应
C.乙全部发生了反应
D.甲与乙反应的质量比为14:3
3.一个密闭容器中有四种物质,在一定条件下发生反应,测得反应前后各物质的质量如(下表)所示。下列推理正确的是( )
A. Y一定是该反应的催化剂
B.该反应属于化合反应
C.反应后Q的质量为10g
D.该反应中消耗X与Q的质量之比为4:11
4.在一个密闭容器中放入甲、乙、丙、丁四种物质充分反应,在一段时间后,测得有关数据如下,则下列说法中,不正确的是( )
A.反应后物质甲的质量为13g
B.乙是反应物
C.反应中乙、丁的质量比为5:4
D.物质丙可能是该反应的催化剂
【考点6】.涉及有关微观图型的赏析
1.如图是密闭体系中,某个化学反应前、后各种物质的微观模拟图,图中“○”“●”表示两种不同元素的原子。根据
图示回答:
(1)该化学反应中,参加反应的 和 与反应后生成的 各粒子间的个数比为 。
(2)该反应所属的基本反应类型是 反应。
(3)该反应中的生成物 (填“可能”或“不可能”)属于氧化物。
2.右图是密闭体系中某反应的微观示意图,“○”和
“●”表示不同原子。
(1)反应后方框内应再填入
1个 微粒(选填序号)。
A. B. C.
(2)该反应所属的基本反应类型是 反应。
(3)写出符合该微观示意图的一个具体反应化学方程式 。
3.如下图所示:2个甲分子反应生成1个丙分子和3个乙分子。下列判断不正确的是( )
A.该反应的基本反应类型为分解反应
B.参加反应的甲物质属于化合物
C.该化学反应中原子的种类发生了改变
D.依质量守恒定律,1个乙分子含有2个A原子
4.“三效催化转换器”可将汽车尾气中的有毒气体处理为无污染的气体,下图为该反应的微观示意图(未配平)。下列说法不正确的是( )
A.该反应中共有三种元素
B.乙和丙中所含元素种类相同
C.甲和丁中同种元素化合价不相同
D.化学方程式中乙、丁的化学计量数均为1
5.已知某两种物质在光照条件下能发生化学反应,其微观示意图如下,则下列说法正确的是( )
A.图示中的反应物都是单质
B.图示中共有4种分子
C.该反应属于分解反应
D.该图示不符合质量守恒定律
五个一定不变:物质的总质量、元素种类(宏观)
原子的种类、原子的数目、原子的质量(实质)
两个一定改变:物质种类(宏观)、分子种类(微观)
一个可能改变:分子个数(微观)
H
H
H
O
O
H
H
O
O
通电
H
+
H
H
H
O
H
H
O
水分子 氧原子 氢原子 氧分子 氢分子
H
质量守恒定律的关键词: 变化, 关系。
反应化学方程式:2H2O2H2↑+ O2↑
通电
A原子 B原子 C原子
反应前
反应后
MnO2
△
各物质的分子
个数比为2:1:2
各物质的质量
比为1:8:9
反应在点燃
条件下进行
是化合反应
点燃
点燃
点燃
点燃
物 质 X Y Z Q
反应前质量/g 18 10 2 21
反应后质量/g 0 12 15 待测
质量测定 甲 乙 丙 丁
反应前质量/g 25 15 1 5
反应后质量/g 11 未测 1 22
物 质 X Y Z Q
反应前质量/g 4 10 1 21
反应后质量/g 0 10 15 待测
物 质 甲 乙 丙 丁
反应前质量/g 18 1 2 32
反应后质量/g 26 2 12
反应前
反应后
+
3乙+
+
甲 甲
丙
表示A原子
表示B原子
b.收集气体 c.检查装置气密性 d.验满 e.清洗仪器、整理桌面
表示B原子
+
催化剂
+
+
甲 乙 丙 丁
黄
蓝
蓝
黑
蓝
黑
蓝
蓝
黄
黄
(说明:一种小球代表一种原子)
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
