鲁教版(五四制)八年级课件:3.3 物质组成的表示 第2课时(共13张PPT)
文档属性
| 名称 | 鲁教版(五四制)八年级课件:3.3 物质组成的表示 第2课时(共13张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 211.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-27 00:00:00 | ||
图片预览



文档简介
(共13张PPT)
第3章 第3节 物质组成的表示
(第2课时)
鲁教版 化学
(八年级)
1
课堂导入
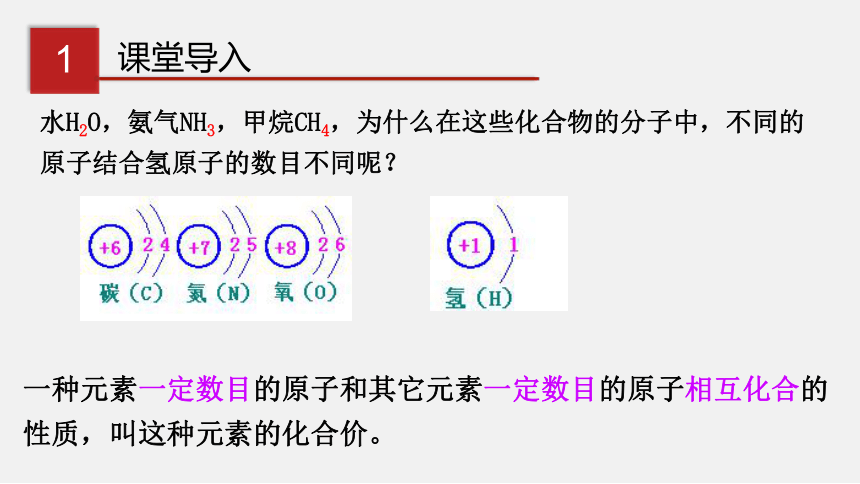
水H2O,氨气NH3,甲烷CH4,为什么在这些化合物的分子中,不同的原子结合氢原子的数目不同呢?
一种元素一定数目的原子和其它元素一定数目的原子相互化合的性质,叫这种元素的化合价。
Na
+11
8
1
2
Cl
+17
8
7
2
Na+
Cl-
+11
8
2
+17
8
8
2
Na+
Cl-
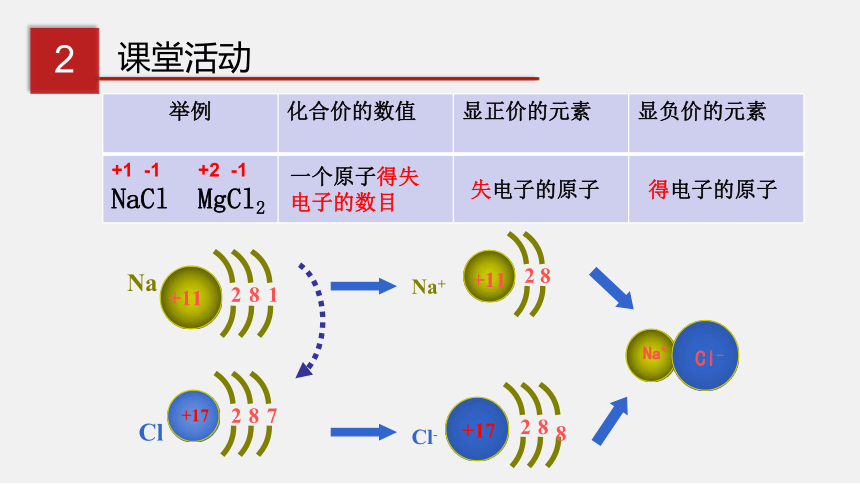
举例 化合价的数值 显正价的元素 显负价的元素
+1 -1 +2 -1 NaCl MgCl2
一个原子得失电子的数目
失电子的原子
得电子的原子
2
课堂活动
01
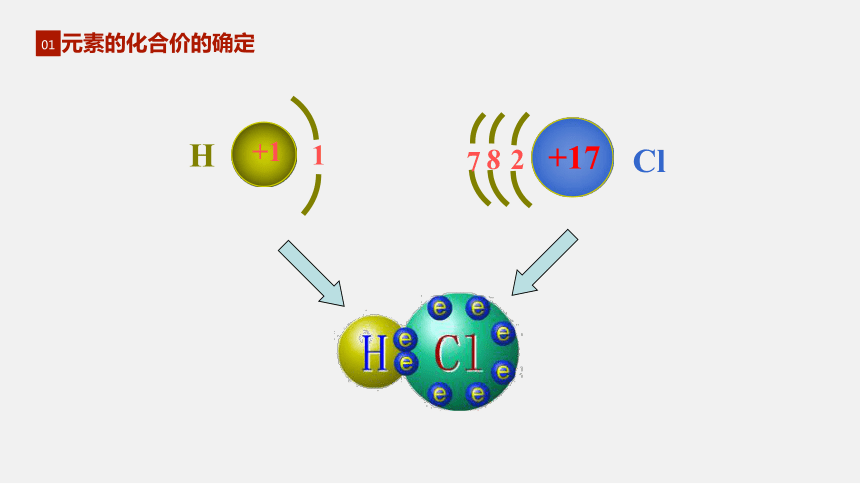
元素的化合价的确定
H
+1
1
Cl
+17
8
7
2
01
元素的化合价的确定
举例 化合价的数值 显正价的元素 显负价的元素
+1 -1 +2 -1 NaCl MgCl2 一个原子得失电子的数目 失电子的原子 得电子的原子
+1 -1 +1 -2 HCl H2O
一个原子跟其它原子共用电子对的数目
电子对偏离的原子
电子对偏向的原子
02
化合价的规律
1.在化合物中,氧元素通常显_____价;氢元素通常显______价。
2.化合物中,金属元素通常显____价,非金属元素显_____价。
+2 +4
3.一些元素在不同种物质中可显_____化合价。比如:CO CO2
4.在化合物中,各元素的正负化合价之和是 。
0 0
5.单质里,元素的化合价为_____。比如:H2 O2
-2
+1
正
负
不同
零
零
03
原子团
根的名称 根的符号 常见化合价
氢氧根 OH -1
硝酸根 NO3 -1
硫酸根 SO4 -2
碳酸根 CO3 -2
铵根 NH4 +1
某些原子作为一个整体参加化学反应,表现如同一个原子,它们叫做原子团,又叫根。
04
化合价的应用
1.根据化学式标出化合价
例1:标出Na2O中各元素的化合价
+1 -2
化合价的标法:位置——元素正上方,顺序——先正负,后数值,注意“1”不省略。
2.根据化学式计算某种元素的化合价。
例2:根据化学式KMnO4 计算Mn(锰元素)的化合价。
+1 –2
(+1)×1+x×1+(-2)×4=0
+7
04
化合价的应用
3.根据化合价书写化学式
例3:在化合物氧化铝中,铝元素的化合价是+3,氧元素的化合价是-2,写出氧化铝的化学式。
Al O
+3 -2
2 3
注意:1.书写其化学式时,一般把正价元素符号写在左边,负价元素符号写在右边,如NaCl、H2O 、MgCl2。
2.根据在化合物中,各元素的正负化合价之和为零检查化学式书写是否正确。
04
化合价的应用
注意事项:物质的组成是通过实验测得的,因此化学式的书写必须依据客观事实。只有确实知道有某种化合物存在,才可能根据元素化合价写出它的化学式,而不能随意写出实际上不存在的物质的化学式。
3
课堂小结
1.一种元素的原子能够跟其他元素的原子相互化合的比例,与这种元素的化合价有关。
2.在化合物中,元素的化合价由这种元素的一个原子得失电子或形成共用电子对决定的。
3.化合物中各元素的正负化合价的代数和为零。因此,可以根据化合价写出已知已知物质的化学式。
4
典例分析
考点:化合价
【典型例题1】根据下列化学式标出其中氮元素和硫元素的化合价
【典型例题2】在化合物氧化铁中,铁元素的化合价是+3,氧元素的化合价是-2,写出氧化铁的化学式。
NO2 NH3 HNO3(硝酸) SO2 Na2S
+4 –3 +5 +4 –2
Fe2O3
考点:化合价
【典型例题3】根据下列各组元素的化合价,试写出由它们组成的一种物质的化学式。
-1 Cl -2 O -1
OH
+1 Na
+2 Mg
NaCl
MgCl2
Na2O
MgO
Mg(OH)2
NaOH
第3章 第3节 物质组成的表示
(第2课时)
鲁教版 化学
(八年级)
1
课堂导入
水H2O,氨气NH3,甲烷CH4,为什么在这些化合物的分子中,不同的原子结合氢原子的数目不同呢?
一种元素一定数目的原子和其它元素一定数目的原子相互化合的性质,叫这种元素的化合价。
Na
+11
8
1
2
Cl
+17
8
7
2
Na+
Cl-
+11
8
2
+17
8
8
2
Na+
Cl-
举例 化合价的数值 显正价的元素 显负价的元素
+1 -1 +2 -1 NaCl MgCl2
一个原子得失电子的数目
失电子的原子
得电子的原子
2
课堂活动
01
元素的化合价的确定
H
+1
1
Cl
+17
8
7
2
01
元素的化合价的确定
举例 化合价的数值 显正价的元素 显负价的元素
+1 -1 +2 -1 NaCl MgCl2 一个原子得失电子的数目 失电子的原子 得电子的原子
+1 -1 +1 -2 HCl H2O
一个原子跟其它原子共用电子对的数目
电子对偏离的原子
电子对偏向的原子
02
化合价的规律
1.在化合物中,氧元素通常显_____价;氢元素通常显______价。
2.化合物中,金属元素通常显____价,非金属元素显_____价。
+2 +4
3.一些元素在不同种物质中可显_____化合价。比如:CO CO2
4.在化合物中,各元素的正负化合价之和是 。
0 0
5.单质里,元素的化合价为_____。比如:H2 O2
-2
+1
正
负
不同
零
零
03
原子团
根的名称 根的符号 常见化合价
氢氧根 OH -1
硝酸根 NO3 -1
硫酸根 SO4 -2
碳酸根 CO3 -2
铵根 NH4 +1
某些原子作为一个整体参加化学反应,表现如同一个原子,它们叫做原子团,又叫根。
04
化合价的应用
1.根据化学式标出化合价
例1:标出Na2O中各元素的化合价
+1 -2
化合价的标法:位置——元素正上方,顺序——先正负,后数值,注意“1”不省略。
2.根据化学式计算某种元素的化合价。
例2:根据化学式KMnO4 计算Mn(锰元素)的化合价。
+1 –2
(+1)×1+x×1+(-2)×4=0
+7
04
化合价的应用
3.根据化合价书写化学式
例3:在化合物氧化铝中,铝元素的化合价是+3,氧元素的化合价是-2,写出氧化铝的化学式。
Al O
+3 -2
2 3
注意:1.书写其化学式时,一般把正价元素符号写在左边,负价元素符号写在右边,如NaCl、H2O 、MgCl2。
2.根据在化合物中,各元素的正负化合价之和为零检查化学式书写是否正确。
04
化合价的应用
注意事项:物质的组成是通过实验测得的,因此化学式的书写必须依据客观事实。只有确实知道有某种化合物存在,才可能根据元素化合价写出它的化学式,而不能随意写出实际上不存在的物质的化学式。
3
课堂小结
1.一种元素的原子能够跟其他元素的原子相互化合的比例,与这种元素的化合价有关。
2.在化合物中,元素的化合价由这种元素的一个原子得失电子或形成共用电子对决定的。
3.化合物中各元素的正负化合价的代数和为零。因此,可以根据化合价写出已知已知物质的化学式。
4
典例分析
考点:化合价
【典型例题1】根据下列化学式标出其中氮元素和硫元素的化合价
【典型例题2】在化合物氧化铁中,铁元素的化合价是+3,氧元素的化合价是-2,写出氧化铁的化学式。
NO2 NH3 HNO3(硝酸) SO2 Na2S
+4 –3 +5 +4 –2
Fe2O3
考点:化合价
【典型例题3】根据下列各组元素的化合价,试写出由它们组成的一种物质的化学式。
-1 Cl -2 O -1
OH
+1 Na
+2 Mg
NaCl
MgCl2
Na2O
MgO
Mg(OH)2
NaOH
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
