鲁教版(五四制)八年级课件:3.3 物质组成的表示 第3课时(共14张PPT)
文档属性
| 名称 | 鲁教版(五四制)八年级课件:3.3 物质组成的表示 第3课时(共14张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 408.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-27 00:00:00 | ||
图片预览





文档简介
(共14张PPT)
中物理
第3章 第3节 物质组成的表示(第3课时)
鲁教版 化学
(八年级)
1
课堂导入
钠原子
镁原子
Mg
你怎样比较下列原子质量的大小?
相对原子质量: Na-23 Mg-24
2
课堂活动
化学式量:某物质化学式中各原子的相对质量的总和。
由分子构成的物质,其化学式量又叫做相对分子质量。
1×2+16×1=18
解:水的化学式量为:
例1:计算水(H2O)的化学式量
难点突破:要找准化学式中各种原子的个数。
01
化学式量
相对原子质量: C-12 O- 16 Ca-40 Cl-35.5 H- 1
变式训练1:计算下列物质的化学式量。
(1) Cl2
(2) CO2
(3) Ca(OH)2
35.5×2= 71
解:Cl2 的化学式量为:
12× 1+ 16×2 =44
解:CO2 的化学式量为:
40×1 + 16×2 + 1×2 = 74
解:Ca(OH)2的化学式量为:
或 40×1 +( 16 + 1)× 2 = 74
02
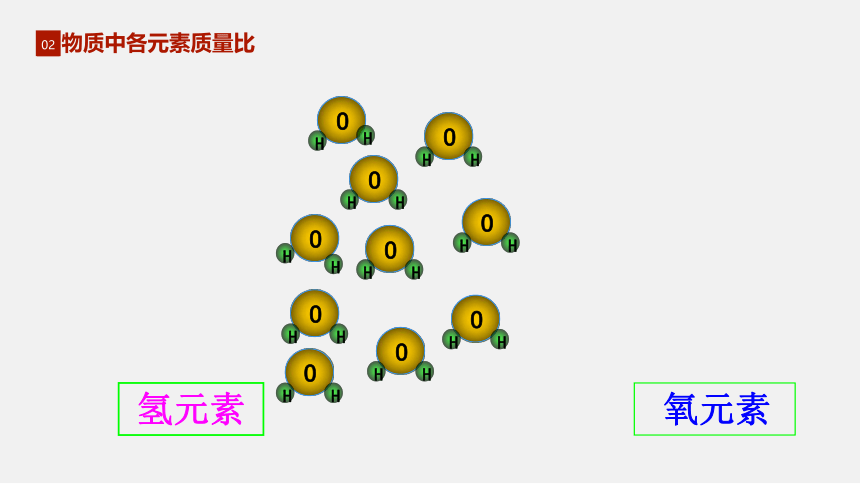
物质中各元素质量比
H2O
16
1
1
H原子的质量
O原子的质量
∶
1个H2O分子中
(1×2)∶ (16×1) = 1∶8
10个H2O分子中
(1×2×10)∶(16×1×10)= 1∶8
n个H2O分子中
(1×2×n)∶(16×1×n) = 1∶8
O
H
H
O
H
H
O
H
H
O
H
H
O
H
H
O
H
H
O
H
H
O
H
H
O
H
H
O
H
H
氢元素
氧元素
02
物质中各元素质量比
02
物质中各元素质量比
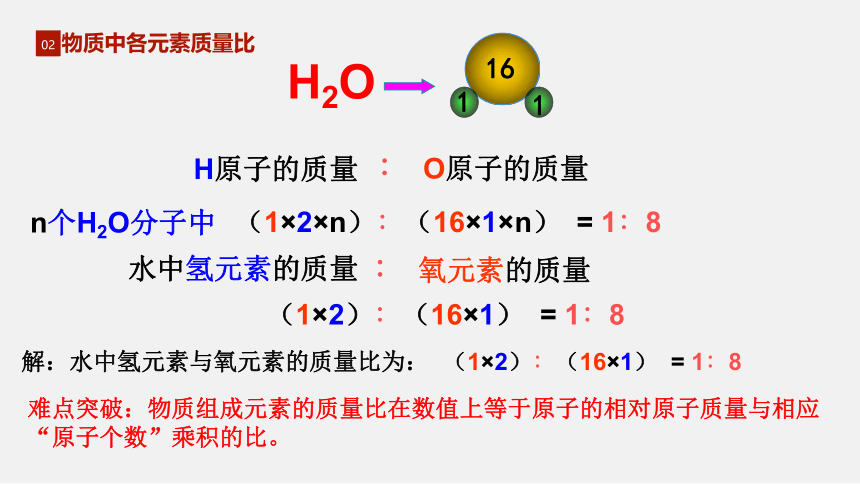
H2O
16
1
1
H原子的质量
O原子的质量
∶
n个H2O分子中
(1×2×n)∶(16×1×n) = 1∶8
(1×2)∶(16×1) = 1∶8
水中氢元素的质量
氧元素的质量
∶
(1×2)∶(16×1) = 1∶8
解:水中氢元素与氧元素的质量比为:
难点突破:物质组成元素的质量比在数值上等于原子的相对原子质量与相应“原子个数”乘积的比。
02
物质中各元素质量比
相对原子质量: C-12 O- 16 Ca-40 N-14 H- 1
变式训练2:计算下列物质中各元素的质量比。
(1) CO2
(2) CO(NH2)2
(12× 1):(16×2)= 3 ︰8
解:CO2 中碳、氧元素的质量比为:
(12× 1):(16×2):(14×2):(1×4)=3︰4︰7︰1
解:CO(NH2)2中碳、氧、氮、氢元素的质量比为:
02
物质中各元素质量比
【易错点】
1.如果题目中没规定元素的比例顺序,也要写出具体的元素比例顺序。
2.不要忘了括号。
3.计算结果一般要约成最简整数比。
03
物质中某元素的质量分数
物质中某元素的质量分数就是该元素的质量与物质的总质量之比。
已知水中氢元素与氧元素的质量比为(1×2)∶(16×1) = 1∶8,求水中氢元素质量分数。
H2O
16
1
1
解:水中氢元素质量分数为:
1
1+8
×100%
1×2
1×2 +16×1
×100%
≈11 %
≈11 %
解:水中氢元素质量分数为:
03
物质中某元素的质量分数
某元素的质量分数 =
该元素相对原子质量×原子个数
化合物的化学式量
× 100﹪
03
物质中某元素的质量分数
相对原子质量: C-12 O- 16 S-32 N-14 H- 1
变式训练3:分别计算下列物质中硫元素、氮元素的质量分数。
(1) SO2
(2) CO(NH2)2
解:SO2 中硫元素的质量分数为:
解:CO(NH2)2中氮元素的质量分数为:
32×1
32×1 +16×2
×100%=50%
14×1
12×1+16×2+14×2+1×4
×100% ≈46.7%
46.7%的含义:100克尿素中含氮元素46.7克。
3
课堂小结
物质组成的定量表示
化学式与相对原子质量
相对原子质量乘以原子个数
相加之和为化学式量
之比为各元素质量比
除以化学式量为元素的质量分数
4
典例分析
考点:物质组成的定量表示
【典型例题】“达菲”是治疗人类感染甲型流感的一种药物,而合成“达菲”的主要原料莽草酸(分子式C7H10O5)存在于我国盛产的八角茴香中。下列说法不正确的是( )
A.莽草酸中碳、氢、氧三种元素的质量比为42:5:40
B.莽草酸的相对分子质量为174
C.每个莽草酸分子中含有22个原子
D.莽草酸中碳元素的质量分数约为21%
D
中物理
第3章 第3节 物质组成的表示(第3课时)
鲁教版 化学
(八年级)
1
课堂导入
钠原子
镁原子
Mg
你怎样比较下列原子质量的大小?
相对原子质量: Na-23 Mg-24
2
课堂活动
化学式量:某物质化学式中各原子的相对质量的总和。
由分子构成的物质,其化学式量又叫做相对分子质量。
1×2+16×1=18
解:水的化学式量为:
例1:计算水(H2O)的化学式量
难点突破:要找准化学式中各种原子的个数。
01
化学式量
相对原子质量: C-12 O- 16 Ca-40 Cl-35.5 H- 1
变式训练1:计算下列物质的化学式量。
(1) Cl2
(2) CO2
(3) Ca(OH)2
35.5×2= 71
解:Cl2 的化学式量为:
12× 1+ 16×2 =44
解:CO2 的化学式量为:
40×1 + 16×2 + 1×2 = 74
解:Ca(OH)2的化学式量为:
或 40×1 +( 16 + 1)× 2 = 74
02
物质中各元素质量比
H2O
16
1
1
H原子的质量
O原子的质量
∶
1个H2O分子中
(1×2)∶ (16×1) = 1∶8
10个H2O分子中
(1×2×10)∶(16×1×10)= 1∶8
n个H2O分子中
(1×2×n)∶(16×1×n) = 1∶8
O
H
H
O
H
H
O
H
H
O
H
H
O
H
H
O
H
H
O
H
H
O
H
H
O
H
H
O
H
H
氢元素
氧元素
02
物质中各元素质量比
02
物质中各元素质量比
H2O
16
1
1
H原子的质量
O原子的质量
∶
n个H2O分子中
(1×2×n)∶(16×1×n) = 1∶8
(1×2)∶(16×1) = 1∶8
水中氢元素的质量
氧元素的质量
∶
(1×2)∶(16×1) = 1∶8
解:水中氢元素与氧元素的质量比为:
难点突破:物质组成元素的质量比在数值上等于原子的相对原子质量与相应“原子个数”乘积的比。
02
物质中各元素质量比
相对原子质量: C-12 O- 16 Ca-40 N-14 H- 1
变式训练2:计算下列物质中各元素的质量比。
(1) CO2
(2) CO(NH2)2
(12× 1):(16×2)= 3 ︰8
解:CO2 中碳、氧元素的质量比为:
(12× 1):(16×2):(14×2):(1×4)=3︰4︰7︰1
解:CO(NH2)2中碳、氧、氮、氢元素的质量比为:
02
物质中各元素质量比
【易错点】
1.如果题目中没规定元素的比例顺序,也要写出具体的元素比例顺序。
2.不要忘了括号。
3.计算结果一般要约成最简整数比。
03
物质中某元素的质量分数
物质中某元素的质量分数就是该元素的质量与物质的总质量之比。
已知水中氢元素与氧元素的质量比为(1×2)∶(16×1) = 1∶8,求水中氢元素质量分数。
H2O
16
1
1
解:水中氢元素质量分数为:
1
1+8
×100%
1×2
1×2 +16×1
×100%
≈11 %
≈11 %
解:水中氢元素质量分数为:
03
物质中某元素的质量分数
某元素的质量分数 =
该元素相对原子质量×原子个数
化合物的化学式量
× 100﹪
03
物质中某元素的质量分数
相对原子质量: C-12 O- 16 S-32 N-14 H- 1
变式训练3:分别计算下列物质中硫元素、氮元素的质量分数。
(1) SO2
(2) CO(NH2)2
解:SO2 中硫元素的质量分数为:
解:CO(NH2)2中氮元素的质量分数为:
32×1
32×1 +16×2
×100%=50%
14×1
12×1+16×2+14×2+1×4
×100% ≈46.7%
46.7%的含义:100克尿素中含氮元素46.7克。
3
课堂小结
物质组成的定量表示
化学式与相对原子质量
相对原子质量乘以原子个数
相加之和为化学式量
之比为各元素质量比
除以化学式量为元素的质量分数
4
典例分析
考点:物质组成的定量表示
【典型例题】“达菲”是治疗人类感染甲型流感的一种药物,而合成“达菲”的主要原料莽草酸(分子式C7H10O5)存在于我国盛产的八角茴香中。下列说法不正确的是( )
A.莽草酸中碳、氢、氧三种元素的质量比为42:5:40
B.莽草酸的相对分子质量为174
C.每个莽草酸分子中含有22个原子
D.莽草酸中碳元素的质量分数约为21%
D
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
