2023浙教版科学八年级上册暑假“胜人一筹”专题训练(八):物质的溶解性(2)【含解析】
文档属性
| 名称 | 2023浙教版科学八年级上册暑假“胜人一筹”专题训练(八):物质的溶解性(2)【含解析】 |

|
|
| 格式 | doc | ||
| 文件大小 | 194.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-07-28 00:00:00 | ||
图片预览


文档简介
物质的溶解性(2)
1.如图是一杯充分搅拌并久置后的糖水,图中甲、乙、丙三处溶液的溶质质量分数分别为a、b、c,其大小关系是( )
A.a>b>c B.a<b<c C.a<b=c D.a=b=c
2.许多科学知识在逻辑上存在如图所示关系,下列关于溶液说法正确的是( )
A.饱和溶液包含浓溶液
B.饱和溶液与稀溶液属于并列关系
C.饱和溶液与不饱和溶液属于交叉关系
D.不饱和溶液与稀溶液属于交叉关系
3.碳酸钠易溶于水,其溶解度如下表。在20℃时,将30克碳酸钠粉未加入100克水中,充分搅拌后,再逐渐升温到30℃,这一过程中( )
温度/摄氏度 10 20 30 40
溶解度/克 12.2 21.8 39.7 53.2
A.溶液从饱和溶液变为不饱和溶液 B.溶液一直是饱和溶液
C.溶液从不饱和溶液变为饱和溶液 D.溶渡一直是为不饱和溶液
4.在10℃时,A物质的溶解度为5g/100g水,则此温度下,A物质的饱和溶液里,下列质量比关系正确的是( )
A.m溶液:m溶质=1:20 B.m溶质:m溶液=1:20
C.m溶液:m溶剂=21:20 D.m溶剂:m溶质=19:1
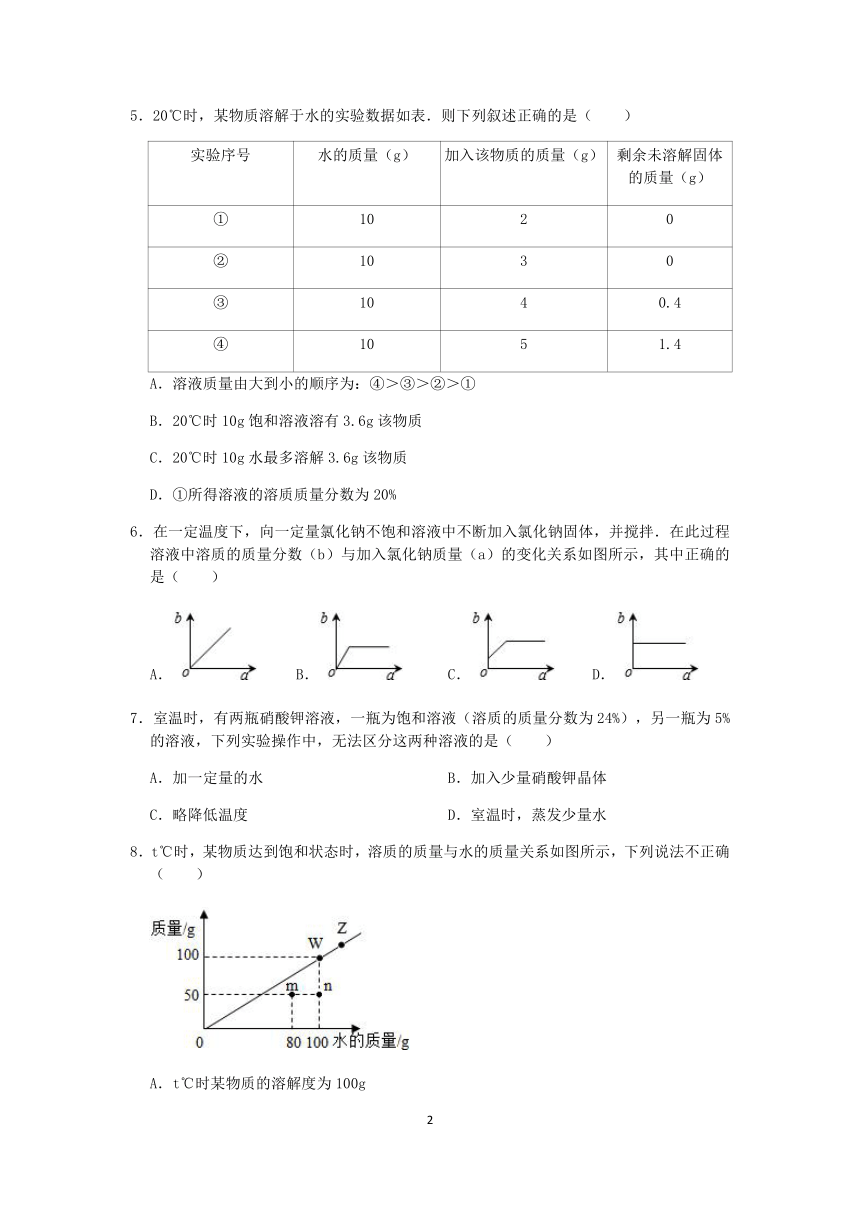
5.20℃时,某物质溶解于水的实验数据如表.则下列叙述正确的是( )
实验序号 水的质量(g) 加入该物质的质量(g) 剩余未溶解固体的质量(g)
① 10 2 0
② 10 3 0
③ 10 4 0.4
④ 10 5 1.4
A.溶液质量由大到小的顺序为:④>③>②>①
B.20℃时10g饱和溶液溶有3.6g该物质
C.20℃时10g水最多溶解3.6g该物质
D.①所得溶液的溶质质量分数为20%
6.在一定温度下,向一定量氯化钠不饱和溶液中不断加入氯化钠固体,并搅拌.在此过程溶液中溶质的质量分数(b)与加入氯化钠质量(a)的变化关系如图所示,其中正确的是( )
A. B. C. D.
7.室温时,有两瓶硝酸钾溶液,一瓶为饱和溶液(溶质的质量分数为24%),另一瓶为5%的溶液,下列实验操作中,无法区分这两种溶液的是( )
A.加一定量的水 B.加入少量硝酸钾晶体
C.略降低温度 D.室温时,蒸发少量水
8.t℃时,某物质达到饱和状态时,溶质的质量与水的质量关系如图所示,下列说法不正确( )
A.t℃时某物质的溶解度为100g
B.溶质的质量分数大小为:W>m>n
C.点Z向点W移动的一种方法是降低温度
D.点m向点W移动的一种方法是先加20g水再加入50g该溶质,充分溶解
9.某温度下,ag饱和硝酸钾溶液蒸干得bg硝酸钾,此温度下,硝酸钾的溶解度计算式如下,正确的是( )
A.100g B.g C.100g D.100g
10.已知20℃时硝酸钾的溶解度为31.6g,50℃时硝酸钾的溶解度为85.5g,且溶解度随温度升高而增大,某科学兴趣小组的同学在20℃时进行了如图实验,得到相应的溶液①~⑤,下列说法正确的是( )
A.保持温度不变,若在④中加入4.5g硝酸钾固体可得到饱和溶液
B.②③⑤中溶质的质量相等
C.①③④均为不饱和溶液
D.④→⑤可析出53.9g硝酸钾晶体
11.烧杯中盛有150g水,加入某种固体A,进行如图甲所示的实验操作,得到相应的溶液①~③,请回答下列问题:
(1)①的溶液中溶质质量分数为 。(精确到0.1%)
(2)固体A的溶解度曲线是图乙中的 。
(3)关于图甲中烧杯内的物质,以下几种说法正确的有 。
A.①、②、③中,只有③中上层清液是饱和溶液
B.若使②中的固体溶解,可采用加水或升温的方法
C.①和②的溶液中,溶质质量相等
D.①的溶液中溶质质量分数一定比③的上层清液中溶质质量分数小
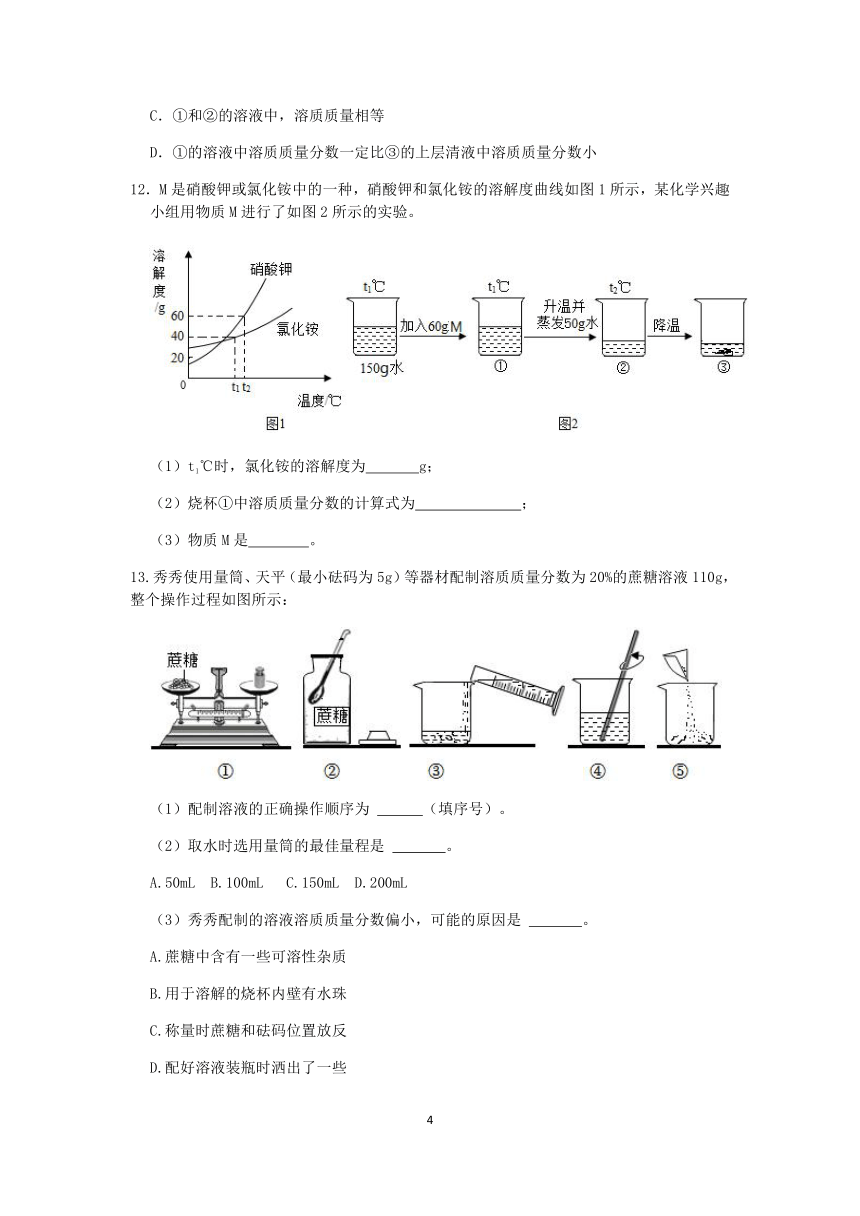
12.M是硝酸钾或氯化铵中的一种,硝酸钾和氯化铵的溶解度曲线如图1所示,某化学兴趣小组用物质M进行了如图2所示的实验。
(1)t1℃时,氯化铵的溶解度为 g;
(2)烧杯①中溶质质量分数的计算式为 ;
(3)物质M是 。
13.秀秀使用量筒、天平(最小砝码为5g)等器材配制溶质质量分数为20%的蔗糖溶液110g,整个操作过程如图所示:
(1)配制溶液的正确操作顺序为 (填序号)。
(2)取水时选用量筒的最佳量程是 。
A.50mL B.100mL C.150mL D.200mL
(3)秀秀配制的溶液溶质质量分数偏小,可能的原因是 。
A.蔗糖中含有一些可溶性杂质
B.用于溶解的烧杯内壁有水珠
C.称量时蔗糖和砝码位置放反
D.配好溶液装瓶时洒出了一些
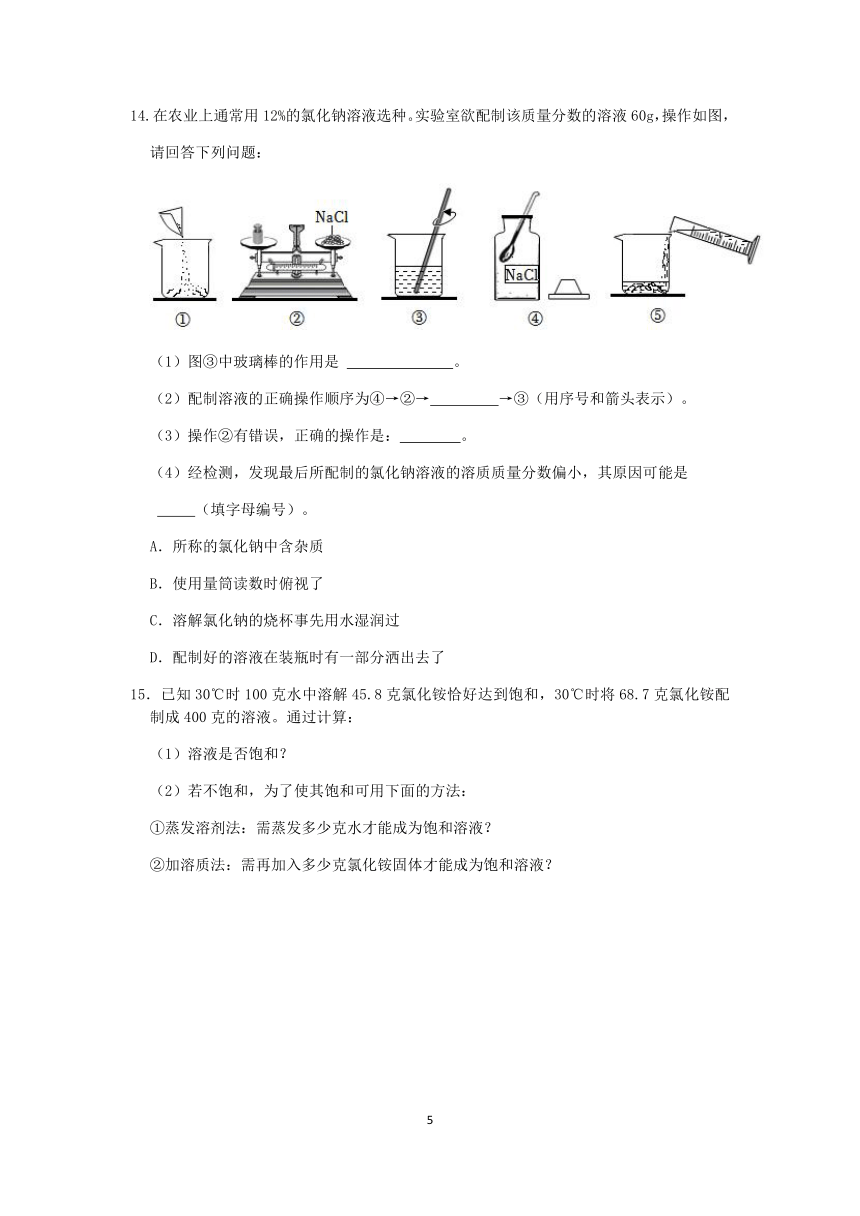
14.在农业上通常用12%的氯化钠溶液选种。实验室欲配制该质量分数的溶液60g,操作如图,
请回答下列问题:
(1)图③中玻璃棒的作用是 。
(2)配制溶液的正确操作顺序为④→②→ →③(用序号和箭头表示)。
(3)操作②有错误,正确的操作是: 。
(4)经检测,发现最后所配制的氯化钠溶液的溶质质量分数偏小,其原因可能是
(填字母编号)。
A.所称的氯化钠中含杂质
B.使用量筒读数时俯视了
C.溶解氯化钠的烧杯事先用水湿润过
D.配制好的溶液在装瓶时有一部分洒出去了
15.已知30℃时100克水中溶解45.8克氯化铵恰好达到饱和,30℃时将68.7克氯化铵配制成400克的溶液。通过计算:
(1)溶液是否饱和?
(2)若不饱和,为了使其饱和可用下面的方法:
①蒸发溶剂法:需蒸发多少克水才能成为饱和溶液?
②加溶质法:需再加入多少克氯化铵固体才能成为饱和溶液?
16.小强因感冒到医院看病,医生给他输液时,要用到生理盐水.如图所示是医生给他用的一瓶生理盐水标签,请根据标签给出的数据回答下列问题(设生理盐水的密度为1.0×103千克/米3):
(1)生理盐水属于 (选填“纯净物”或“混合物”)
(2)若以每分钟100滴(20滴约为1毫升)的速率给小李静脉输液,则输完这瓶生理盐水约需 分钟.
(3)输液过程中,小李想到了如下的几个问题,请通过计算帮助解决:这瓶生理盐水的溶质质量分数为多少?如果用质量分数为10%的氯化钠溶液来配制这样一瓶生理盐水,需要10%的氯化钠溶液多少克?
答案及解析
1.D
解:溶液具有均一性的特点。故图中甲、乙、丙三处溶液的溶质质量分数相同。
故选:D。
2.D
【解析】
A、浓稀溶液是溶液中所含溶质质量分数的大小,溶液是否饱和与溶液的浓稀没有必然联系,饱和溶液可能是浓溶液,也可能是稀溶液,两者之间是交叉关系,故选项说法错误。
B、浓稀溶液是溶液中所含溶质质量分数的大小,溶液是否饱和与溶液的浓稀没有必然联系,饱和溶液可能是浓溶液,也可能是稀溶液,两者之间是交叉关系,故选项说法错误。
C、在一定温度下、一定量的溶剂里,不能继续溶解这种溶质的溶液是饱和溶液,还能继续溶解这种溶质的溶液是不饱和溶液,饱和溶液与不饱和溶液属于并列关系,故选项说法错误。
D、浓稀溶液是溶液中所含溶质质量分数的大小,溶液是否饱和与溶液的浓稀没有必然联系,不饱和溶液可能是浓溶液,也可能是稀溶液,不饱和溶液与稀溶液之间是交叉关系,故选项说法正确。
3.A
【解析】
20℃时,碳酸钠的溶解度为21.8g,20℃时,将30克碳酸钠粉未加入100克水中,有碳酸钠不能继续溶解,所得溶液为饱和溶液;30℃,碳酸钠的溶解度为39.7g,该温度下100g水中最多能溶解碳酸钠39.7g,所得溶液为不饱和溶液,则这一过程中溶液从饱和溶液变为不饱和溶液。
4.C
解:在10℃时,A物质的溶解度为5g/100g水,含义是10℃时,100g水中最多能溶解A物质5g,溶液达到饱和状态,形成饱和溶液105g。
A、该温度下A物质的饱和溶液中溶液质量:溶质质量=105g:5g=21:1,故选项说法错误。
B、该温度下A物质的饱和溶液中溶质质量:溶液质量=5g:105g=1:21,故选项说法错误。
C、该温度下A物质的饱和溶液中溶液质量:溶剂质量=105g:100g=21:20,故选项说法正确。
D、该温度下A物质的饱和溶液中溶剂质量:溶质质量=100g:5g=20:1,故选项说法错误。
故选:C。
5.C
解:A、对比②③可见,20℃时,10g水中达到饱和,最多可以溶解3.6g该物质,所以③④都是饱和溶液,二者的质量相等,所以溶液质量由大到小的顺序为:④=③>②>①,故A错误;
B、根据实验③所得数据,20℃时10g水溶解13.6g﹣10g=3.6g该物质时溶液为饱和溶液,即20℃时10g饱和溶液溶有3.6g该物质的叙述是错误的;故B错误;
C、③、④溶液中同为10g水中溶解了3.6g某物质,所以20℃时10g水最多洛解3.6g该物质,故C正确;
D、①所得溶液是10g水中溶解了2g氯化钠制得,所得溶液的溶质质量分数为100%=16.7%.故D错误;
故选:C。
6.C
解:A、刚开始溶质的质量不为0,溶质质量分数不是一直增大,故错误;
B、刚开始溶质的质量等于了0,故错误;
C、刚开始是不饱和氯化钠溶液,溶质氯化钠的质量大于0;当不断加入氯化钠固体时,溶质的质量在不断增加,溶质的质量分数逐渐增大;当氯化钠不再溶解时,溶液饱和,溶质不变,溶质的质量分数也恒定不变,故正确。
D、溶质的质量分数是有变化的,故错误。
故选:C。
7.A
解:
A、各加入少量水振荡,没有现象。故此选项错误。
B、向硝酸钾的饱和溶液中各加入少量硝酸钾晶体,振荡。晶体不溶解。可区分开饱和溶液和不饱和溶液,故此选项正确。
C、硝酸钾的饱和溶液在降低温度时会有晶体析出,不饱和的不会析出晶体,故此选项正确。
D、蒸发少量水饱和的溶液会有晶体析出,不饱和的不会析出晶体,故此选项正确。
故选:A。
8.C
解:A、此图象是t℃时物质的溶解情况,以及t℃时的溶解度是100g,故说法正确;
B、图中四点的含义分别是m点:80g水中溶解50g溶质的不饱和溶液;n点:100g水中溶解50g溶质的不饱和溶液;W点是100g水中溶解100g溶质的饱和溶液,这一温度下的饱和溶液,所以质量分数W>m>n,故说法正确。
C、点Z向点W移动的一种方法是减少水的质量或减少溶质的质量,故说法错误;
D、点m向点W移动的一种方法是先加20g水再加入50g该溶质,使该物质在该温度下达到饱和状态,故说法正确;
故选:C。
9.C
解:设此温度下,硝酸钾的溶解度为x,则:
x
故选:C。
10.C
解:A、在50℃时,硝酸钾溶解度为85.5g,所以此时100g水最多溶解85.5g硝酸钾,此时总共加入硝酸钾质量为80g,之后又加入4.5g,此时硝酸钾质量为84.5g,未达到85.5g,所以此时没有达到饱和状态,选项A错误;
B、②中温度为20℃,此时硝酸钾最多溶解31.6g,而此时加入50g硝酸钾,所以溶解硝酸钾为31.6g,③温度升高至50℃,此时溶解硝酸钾最多为85.5g,加入硝酸钾一共50g,全部溶解,⑤又降温至20℃,此时最多溶解硝酸钾为31.6g,所以②和⑤溶质质量一样多,③的质量为50g,选项B错误;
C、①最多溶解硝酸钾为31.6g,此时为20g硝酸钾,形成不饱和溶液,③温度为50℃,最多溶解硝酸钾为85.5g,加入硝酸钾一共为50g,未到达饱和溶液,④此时温度为50℃,加入硝酸钾质量为80g,未达到85.5g,形成不饱和溶液,选项C正确;
D、⑤温度降至20℃,此时溶液最大溶解硝酸钾为31.6g,原先溶解硝酸钾为80g,此时析出硝酸钾质量=80g﹣31.6g=48.4g,选项D错误;
故选:C。
11.解:(1)①的溶液中溶质质量分数为100%≈16.7%;
(2)在t3℃时,50gA全部溶解,所以固体A的溶解度曲线是图乙中的a;
(3)t1℃时,A物质的溶解度是20g,①中溶质30g,溶剂150g,②中溶剂150g,溶质30g;t3℃时,A物质的溶解度是50g,③中溶质50g,溶剂100g。
A、①、②、③中,②的烧杯底部有固体剩余,所以②③中上层清液都是饱和溶液,故A错误;
B、A物质的溶解度随温度的升高而增大,所以若使②中的固体溶解,可采用加水或升温的方法,故B正确;
C、①和②的溶液中,溶质质量相等,故C正确;
D、③中溶质质量分数100%≈33.3%,所以①的溶液中溶质质量分数一定比③的上层清液中溶质质量分数小,故D正确。
故选:BCD。
故答案为:(1)16.7%;(2)a;(3)BCD。
12.解:(1)由溶解度曲线可知:t1℃时,氯化铵的溶解度为40g;故答案为:40;
(2)烧杯①中溶质质量分数的计算式为:;故答案为:;
(3)物质M是硝酸钾,因为在t1℃时,60gM全部溶于100g水中;故答案为:硝酸钾;
13.解:(1)配制溶液的正确操作顺序为②(取药品)①(称量)⑤(把药品转移到烧杯中)③(把水转移到烧杯中)④(溶解)。
故答案为:②①⑤③④。
(2)需要水的体积是(110g﹣110g×20%)÷1g/mL=88mL,取水时选用量筒的最佳量程是100mL,是因为100mL大于88mL并且与88mL最接近。
故答案为:B。
(3)A.蔗糖中含有一些可溶性杂质,导致蔗糖质量偏小,进一步导致质量分数偏小。
B.用于溶解的烧杯内壁有水珠,导致水的质量偏大,进一步导致质量分数偏小。
C.称量时蔗糖和砝码位置放反,导致称量的蔗糖质量偏小,进一步导致质量分数偏小。
D.配好溶液装瓶时洒出了一些,不影响质量分数。
故答案为:ABC。
14.解:(1)玻璃棒在溶解时,起到搅拌加快溶解的作用;
故答案为:搅拌,加快溶解。
(2)实验室配制溶液步骤为计算、称量、溶解,所以顺序为④→②→①→⑤→③;
故答案为:①→⑤。
(3)天平称量遵循左物右码原则,所以左边放氯化钠,右边放砝码;
故答案为:左边放氯化钠,右边放砝码。
(4)A、氯化钠含有杂质,称量氯化钠质量减小,造成溶液溶质质量分数减小,选项A符合题意;
B、俯视读数造成溶液体积减小,配制溶液溶质质量分数偏大,选项B不符合题意;
C、用水浸湿烧杯造成溶剂质量增大,造成溶液溶质质量分数减小,选项C符合题意;
D、配制好的溶液洒落不影响溶质质量分数,选项D不符合题意;
故选:AC。
15.解:(1)由于30℃时氯化铵的溶解度是45.8g,也就是100克水中最多可溶解45.8克的氯化铵,因此400克溶液中最多溶解的氯化铵的质量是125.7克。所以,在30℃时,把68.7g氯化铵配制成400克溶液,所得溶液是不饱和溶液;
(2)①由于30℃时氯化铵的溶解度是45.8g,也就是100克水中最多可溶解45.8克的氯化铵,则完全溶解68,7g氯化铵仅需150g水,所以需蒸发水的质量为400g﹣150g﹣68.7g=181.3g;
②由于30℃时氯化铵的溶解度是45.8g,也就是100克水中最多可溶解45.8克的氯化铵,400g溶液含有水的质量为:400g﹣68.7g=331.3g,该温度下的331.3g水中最多能溶解氯化铵的质量为:151.7g,还需要加入氯化铵的质量为:151.7g﹣68.7g=83.0g,溶液才能达到饱和;
故答案为:(1)所得溶液是不饱和溶液;(2)①需蒸发181.3克水才能成为饱和溶液;②需再加入83.0克氯化铵,溶液才能成为饱和溶液。
16.解:(1)生理盐水中含有氯化钠和水,属于混合物.故填:混合物.
(2)需要的时间为:500mL100分钟,故填:100;
(3)1.0×103千克/米3=1g/mL
由标签给出的数据可知这瓶生理盐水的溶质质量为4.5g,生理盐水的质量为500mL×1g/L=500g
这瓶生理盐水的溶质质量分数为0.9%;
如果用质量分数为10%的氯化钠溶液来配制这样一瓶生理盐水,设需要10%的氯化钠溶液为x
10%×x=4.5g
x=45g
故填:0.9%;45g
1.如图是一杯充分搅拌并久置后的糖水,图中甲、乙、丙三处溶液的溶质质量分数分别为a、b、c,其大小关系是( )
A.a>b>c B.a<b<c C.a<b=c D.a=b=c
2.许多科学知识在逻辑上存在如图所示关系,下列关于溶液说法正确的是( )
A.饱和溶液包含浓溶液
B.饱和溶液与稀溶液属于并列关系
C.饱和溶液与不饱和溶液属于交叉关系
D.不饱和溶液与稀溶液属于交叉关系
3.碳酸钠易溶于水,其溶解度如下表。在20℃时,将30克碳酸钠粉未加入100克水中,充分搅拌后,再逐渐升温到30℃,这一过程中( )
温度/摄氏度 10 20 30 40
溶解度/克 12.2 21.8 39.7 53.2
A.溶液从饱和溶液变为不饱和溶液 B.溶液一直是饱和溶液
C.溶液从不饱和溶液变为饱和溶液 D.溶渡一直是为不饱和溶液
4.在10℃时,A物质的溶解度为5g/100g水,则此温度下,A物质的饱和溶液里,下列质量比关系正确的是( )
A.m溶液:m溶质=1:20 B.m溶质:m溶液=1:20
C.m溶液:m溶剂=21:20 D.m溶剂:m溶质=19:1
5.20℃时,某物质溶解于水的实验数据如表.则下列叙述正确的是( )
实验序号 水的质量(g) 加入该物质的质量(g) 剩余未溶解固体的质量(g)
① 10 2 0
② 10 3 0
③ 10 4 0.4
④ 10 5 1.4
A.溶液质量由大到小的顺序为:④>③>②>①
B.20℃时10g饱和溶液溶有3.6g该物质
C.20℃时10g水最多溶解3.6g该物质
D.①所得溶液的溶质质量分数为20%
6.在一定温度下,向一定量氯化钠不饱和溶液中不断加入氯化钠固体,并搅拌.在此过程溶液中溶质的质量分数(b)与加入氯化钠质量(a)的变化关系如图所示,其中正确的是( )
A. B. C. D.
7.室温时,有两瓶硝酸钾溶液,一瓶为饱和溶液(溶质的质量分数为24%),另一瓶为5%的溶液,下列实验操作中,无法区分这两种溶液的是( )
A.加一定量的水 B.加入少量硝酸钾晶体
C.略降低温度 D.室温时,蒸发少量水
8.t℃时,某物质达到饱和状态时,溶质的质量与水的质量关系如图所示,下列说法不正确( )
A.t℃时某物质的溶解度为100g
B.溶质的质量分数大小为:W>m>n
C.点Z向点W移动的一种方法是降低温度
D.点m向点W移动的一种方法是先加20g水再加入50g该溶质,充分溶解
9.某温度下,ag饱和硝酸钾溶液蒸干得bg硝酸钾,此温度下,硝酸钾的溶解度计算式如下,正确的是( )
A.100g B.g C.100g D.100g
10.已知20℃时硝酸钾的溶解度为31.6g,50℃时硝酸钾的溶解度为85.5g,且溶解度随温度升高而增大,某科学兴趣小组的同学在20℃时进行了如图实验,得到相应的溶液①~⑤,下列说法正确的是( )
A.保持温度不变,若在④中加入4.5g硝酸钾固体可得到饱和溶液
B.②③⑤中溶质的质量相等
C.①③④均为不饱和溶液
D.④→⑤可析出53.9g硝酸钾晶体
11.烧杯中盛有150g水,加入某种固体A,进行如图甲所示的实验操作,得到相应的溶液①~③,请回答下列问题:
(1)①的溶液中溶质质量分数为 。(精确到0.1%)
(2)固体A的溶解度曲线是图乙中的 。
(3)关于图甲中烧杯内的物质,以下几种说法正确的有 。
A.①、②、③中,只有③中上层清液是饱和溶液
B.若使②中的固体溶解,可采用加水或升温的方法
C.①和②的溶液中,溶质质量相等
D.①的溶液中溶质质量分数一定比③的上层清液中溶质质量分数小
12.M是硝酸钾或氯化铵中的一种,硝酸钾和氯化铵的溶解度曲线如图1所示,某化学兴趣小组用物质M进行了如图2所示的实验。
(1)t1℃时,氯化铵的溶解度为 g;
(2)烧杯①中溶质质量分数的计算式为 ;
(3)物质M是 。
13.秀秀使用量筒、天平(最小砝码为5g)等器材配制溶质质量分数为20%的蔗糖溶液110g,整个操作过程如图所示:
(1)配制溶液的正确操作顺序为 (填序号)。
(2)取水时选用量筒的最佳量程是 。
A.50mL B.100mL C.150mL D.200mL
(3)秀秀配制的溶液溶质质量分数偏小,可能的原因是 。
A.蔗糖中含有一些可溶性杂质
B.用于溶解的烧杯内壁有水珠
C.称量时蔗糖和砝码位置放反
D.配好溶液装瓶时洒出了一些
14.在农业上通常用12%的氯化钠溶液选种。实验室欲配制该质量分数的溶液60g,操作如图,
请回答下列问题:
(1)图③中玻璃棒的作用是 。
(2)配制溶液的正确操作顺序为④→②→ →③(用序号和箭头表示)。
(3)操作②有错误,正确的操作是: 。
(4)经检测,发现最后所配制的氯化钠溶液的溶质质量分数偏小,其原因可能是
(填字母编号)。
A.所称的氯化钠中含杂质
B.使用量筒读数时俯视了
C.溶解氯化钠的烧杯事先用水湿润过
D.配制好的溶液在装瓶时有一部分洒出去了
15.已知30℃时100克水中溶解45.8克氯化铵恰好达到饱和,30℃时将68.7克氯化铵配制成400克的溶液。通过计算:
(1)溶液是否饱和?
(2)若不饱和,为了使其饱和可用下面的方法:
①蒸发溶剂法:需蒸发多少克水才能成为饱和溶液?
②加溶质法:需再加入多少克氯化铵固体才能成为饱和溶液?
16.小强因感冒到医院看病,医生给他输液时,要用到生理盐水.如图所示是医生给他用的一瓶生理盐水标签,请根据标签给出的数据回答下列问题(设生理盐水的密度为1.0×103千克/米3):
(1)生理盐水属于 (选填“纯净物”或“混合物”)
(2)若以每分钟100滴(20滴约为1毫升)的速率给小李静脉输液,则输完这瓶生理盐水约需 分钟.
(3)输液过程中,小李想到了如下的几个问题,请通过计算帮助解决:这瓶生理盐水的溶质质量分数为多少?如果用质量分数为10%的氯化钠溶液来配制这样一瓶生理盐水,需要10%的氯化钠溶液多少克?
答案及解析
1.D
解:溶液具有均一性的特点。故图中甲、乙、丙三处溶液的溶质质量分数相同。
故选:D。
2.D
【解析】
A、浓稀溶液是溶液中所含溶质质量分数的大小,溶液是否饱和与溶液的浓稀没有必然联系,饱和溶液可能是浓溶液,也可能是稀溶液,两者之间是交叉关系,故选项说法错误。
B、浓稀溶液是溶液中所含溶质质量分数的大小,溶液是否饱和与溶液的浓稀没有必然联系,饱和溶液可能是浓溶液,也可能是稀溶液,两者之间是交叉关系,故选项说法错误。
C、在一定温度下、一定量的溶剂里,不能继续溶解这种溶质的溶液是饱和溶液,还能继续溶解这种溶质的溶液是不饱和溶液,饱和溶液与不饱和溶液属于并列关系,故选项说法错误。
D、浓稀溶液是溶液中所含溶质质量分数的大小,溶液是否饱和与溶液的浓稀没有必然联系,不饱和溶液可能是浓溶液,也可能是稀溶液,不饱和溶液与稀溶液之间是交叉关系,故选项说法正确。
3.A
【解析】
20℃时,碳酸钠的溶解度为21.8g,20℃时,将30克碳酸钠粉未加入100克水中,有碳酸钠不能继续溶解,所得溶液为饱和溶液;30℃,碳酸钠的溶解度为39.7g,该温度下100g水中最多能溶解碳酸钠39.7g,所得溶液为不饱和溶液,则这一过程中溶液从饱和溶液变为不饱和溶液。
4.C
解:在10℃时,A物质的溶解度为5g/100g水,含义是10℃时,100g水中最多能溶解A物质5g,溶液达到饱和状态,形成饱和溶液105g。
A、该温度下A物质的饱和溶液中溶液质量:溶质质量=105g:5g=21:1,故选项说法错误。
B、该温度下A物质的饱和溶液中溶质质量:溶液质量=5g:105g=1:21,故选项说法错误。
C、该温度下A物质的饱和溶液中溶液质量:溶剂质量=105g:100g=21:20,故选项说法正确。
D、该温度下A物质的饱和溶液中溶剂质量:溶质质量=100g:5g=20:1,故选项说法错误。
故选:C。
5.C
解:A、对比②③可见,20℃时,10g水中达到饱和,最多可以溶解3.6g该物质,所以③④都是饱和溶液,二者的质量相等,所以溶液质量由大到小的顺序为:④=③>②>①,故A错误;
B、根据实验③所得数据,20℃时10g水溶解13.6g﹣10g=3.6g该物质时溶液为饱和溶液,即20℃时10g饱和溶液溶有3.6g该物质的叙述是错误的;故B错误;
C、③、④溶液中同为10g水中溶解了3.6g某物质,所以20℃时10g水最多洛解3.6g该物质,故C正确;
D、①所得溶液是10g水中溶解了2g氯化钠制得,所得溶液的溶质质量分数为100%=16.7%.故D错误;
故选:C。
6.C
解:A、刚开始溶质的质量不为0,溶质质量分数不是一直增大,故错误;
B、刚开始溶质的质量等于了0,故错误;
C、刚开始是不饱和氯化钠溶液,溶质氯化钠的质量大于0;当不断加入氯化钠固体时,溶质的质量在不断增加,溶质的质量分数逐渐增大;当氯化钠不再溶解时,溶液饱和,溶质不变,溶质的质量分数也恒定不变,故正确。
D、溶质的质量分数是有变化的,故错误。
故选:C。
7.A
解:
A、各加入少量水振荡,没有现象。故此选项错误。
B、向硝酸钾的饱和溶液中各加入少量硝酸钾晶体,振荡。晶体不溶解。可区分开饱和溶液和不饱和溶液,故此选项正确。
C、硝酸钾的饱和溶液在降低温度时会有晶体析出,不饱和的不会析出晶体,故此选项正确。
D、蒸发少量水饱和的溶液会有晶体析出,不饱和的不会析出晶体,故此选项正确。
故选:A。
8.C
解:A、此图象是t℃时物质的溶解情况,以及t℃时的溶解度是100g,故说法正确;
B、图中四点的含义分别是m点:80g水中溶解50g溶质的不饱和溶液;n点:100g水中溶解50g溶质的不饱和溶液;W点是100g水中溶解100g溶质的饱和溶液,这一温度下的饱和溶液,所以质量分数W>m>n,故说法正确。
C、点Z向点W移动的一种方法是减少水的质量或减少溶质的质量,故说法错误;
D、点m向点W移动的一种方法是先加20g水再加入50g该溶质,使该物质在该温度下达到饱和状态,故说法正确;
故选:C。
9.C
解:设此温度下,硝酸钾的溶解度为x,则:
x
故选:C。
10.C
解:A、在50℃时,硝酸钾溶解度为85.5g,所以此时100g水最多溶解85.5g硝酸钾,此时总共加入硝酸钾质量为80g,之后又加入4.5g,此时硝酸钾质量为84.5g,未达到85.5g,所以此时没有达到饱和状态,选项A错误;
B、②中温度为20℃,此时硝酸钾最多溶解31.6g,而此时加入50g硝酸钾,所以溶解硝酸钾为31.6g,③温度升高至50℃,此时溶解硝酸钾最多为85.5g,加入硝酸钾一共50g,全部溶解,⑤又降温至20℃,此时最多溶解硝酸钾为31.6g,所以②和⑤溶质质量一样多,③的质量为50g,选项B错误;
C、①最多溶解硝酸钾为31.6g,此时为20g硝酸钾,形成不饱和溶液,③温度为50℃,最多溶解硝酸钾为85.5g,加入硝酸钾一共为50g,未到达饱和溶液,④此时温度为50℃,加入硝酸钾质量为80g,未达到85.5g,形成不饱和溶液,选项C正确;
D、⑤温度降至20℃,此时溶液最大溶解硝酸钾为31.6g,原先溶解硝酸钾为80g,此时析出硝酸钾质量=80g﹣31.6g=48.4g,选项D错误;
故选:C。
11.解:(1)①的溶液中溶质质量分数为100%≈16.7%;
(2)在t3℃时,50gA全部溶解,所以固体A的溶解度曲线是图乙中的a;
(3)t1℃时,A物质的溶解度是20g,①中溶质30g,溶剂150g,②中溶剂150g,溶质30g;t3℃时,A物质的溶解度是50g,③中溶质50g,溶剂100g。
A、①、②、③中,②的烧杯底部有固体剩余,所以②③中上层清液都是饱和溶液,故A错误;
B、A物质的溶解度随温度的升高而增大,所以若使②中的固体溶解,可采用加水或升温的方法,故B正确;
C、①和②的溶液中,溶质质量相等,故C正确;
D、③中溶质质量分数100%≈33.3%,所以①的溶液中溶质质量分数一定比③的上层清液中溶质质量分数小,故D正确。
故选:BCD。
故答案为:(1)16.7%;(2)a;(3)BCD。
12.解:(1)由溶解度曲线可知:t1℃时,氯化铵的溶解度为40g;故答案为:40;
(2)烧杯①中溶质质量分数的计算式为:;故答案为:;
(3)物质M是硝酸钾,因为在t1℃时,60gM全部溶于100g水中;故答案为:硝酸钾;
13.解:(1)配制溶液的正确操作顺序为②(取药品)①(称量)⑤(把药品转移到烧杯中)③(把水转移到烧杯中)④(溶解)。
故答案为:②①⑤③④。
(2)需要水的体积是(110g﹣110g×20%)÷1g/mL=88mL,取水时选用量筒的最佳量程是100mL,是因为100mL大于88mL并且与88mL最接近。
故答案为:B。
(3)A.蔗糖中含有一些可溶性杂质,导致蔗糖质量偏小,进一步导致质量分数偏小。
B.用于溶解的烧杯内壁有水珠,导致水的质量偏大,进一步导致质量分数偏小。
C.称量时蔗糖和砝码位置放反,导致称量的蔗糖质量偏小,进一步导致质量分数偏小。
D.配好溶液装瓶时洒出了一些,不影响质量分数。
故答案为:ABC。
14.解:(1)玻璃棒在溶解时,起到搅拌加快溶解的作用;
故答案为:搅拌,加快溶解。
(2)实验室配制溶液步骤为计算、称量、溶解,所以顺序为④→②→①→⑤→③;
故答案为:①→⑤。
(3)天平称量遵循左物右码原则,所以左边放氯化钠,右边放砝码;
故答案为:左边放氯化钠,右边放砝码。
(4)A、氯化钠含有杂质,称量氯化钠质量减小,造成溶液溶质质量分数减小,选项A符合题意;
B、俯视读数造成溶液体积减小,配制溶液溶质质量分数偏大,选项B不符合题意;
C、用水浸湿烧杯造成溶剂质量增大,造成溶液溶质质量分数减小,选项C符合题意;
D、配制好的溶液洒落不影响溶质质量分数,选项D不符合题意;
故选:AC。
15.解:(1)由于30℃时氯化铵的溶解度是45.8g,也就是100克水中最多可溶解45.8克的氯化铵,因此400克溶液中最多溶解的氯化铵的质量是125.7克。所以,在30℃时,把68.7g氯化铵配制成400克溶液,所得溶液是不饱和溶液;
(2)①由于30℃时氯化铵的溶解度是45.8g,也就是100克水中最多可溶解45.8克的氯化铵,则完全溶解68,7g氯化铵仅需150g水,所以需蒸发水的质量为400g﹣150g﹣68.7g=181.3g;
②由于30℃时氯化铵的溶解度是45.8g,也就是100克水中最多可溶解45.8克的氯化铵,400g溶液含有水的质量为:400g﹣68.7g=331.3g,该温度下的331.3g水中最多能溶解氯化铵的质量为:151.7g,还需要加入氯化铵的质量为:151.7g﹣68.7g=83.0g,溶液才能达到饱和;
故答案为:(1)所得溶液是不饱和溶液;(2)①需蒸发181.3克水才能成为饱和溶液;②需再加入83.0克氯化铵,溶液才能成为饱和溶液。
16.解:(1)生理盐水中含有氯化钠和水,属于混合物.故填:混合物.
(2)需要的时间为:500mL100分钟,故填:100;
(3)1.0×103千克/米3=1g/mL
由标签给出的数据可知这瓶生理盐水的溶质质量为4.5g,生理盐水的质量为500mL×1g/L=500g
这瓶生理盐水的溶质质量分数为0.9%;
如果用质量分数为10%的氯化钠溶液来配制这样一瓶生理盐水,设需要10%的氯化钠溶液为x
10%×x=4.5g
x=45g
故填:0.9%;45g
同课章节目录
