化学人教版(2019)必修第一册3.1铁及其化合物(共16张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册3.1铁及其化合物(共16张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-07-28 00:00:00 | ||
图片预览


文档简介
(共16张PPT)
铁及其化合物
将硫酸亚铁配成溶液喷于叶片上,可改善黄化效果。
硫酸亚铁容易变质
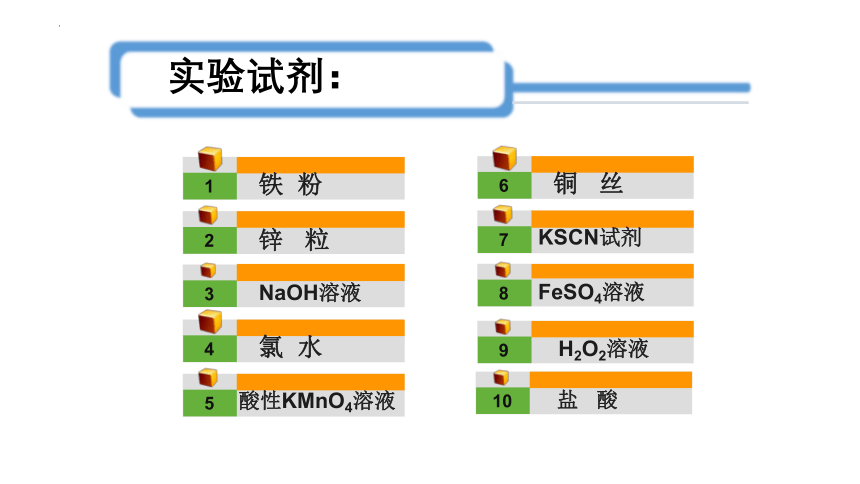
实验试剂:
1
铁 粉
2
锌 粒
3
NaOH溶液
4
氯 水
5
酸性KMnO4溶液
9
H2O2溶液
6
铜 丝
7
KSCN试剂
8
FeSO4溶液
10
盐 酸
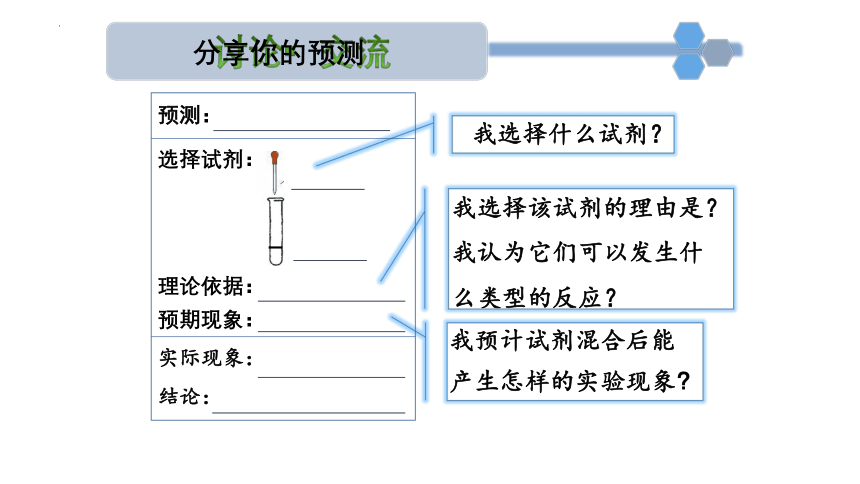
我选择什么试剂?
我选择该试剂的理由是?
我认为它们可以发生什么类型的反应?
我预计试剂混合后能产生怎样的实验现象?
讨论 交流
预测:
选择试剂:
理论依据:
预期现象:
实际现象:
结论:
分享你的预测
预测:
选择试剂:
理论依据:
预期现象:
实际现象:
结论:
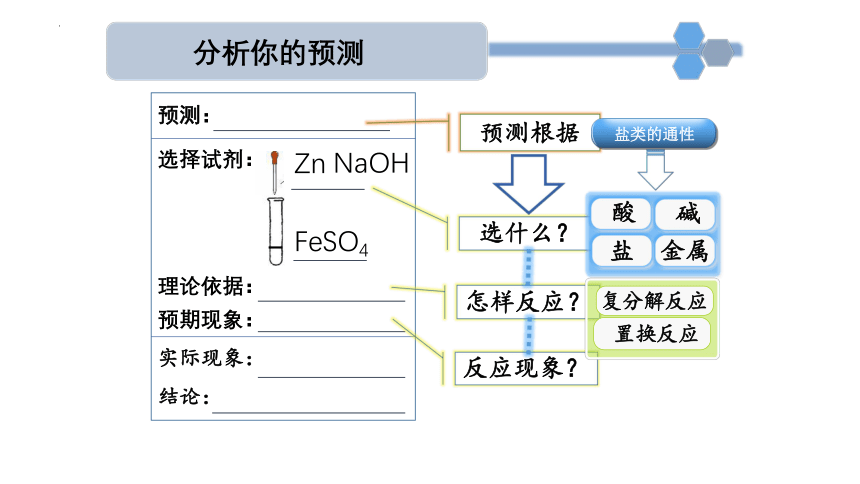
FeSO4
选什么?
怎样反应?
预测根据
分析你的预测
反应现象?
Zn
NaOH
酸
碱
盐
金属
复分解反应
置换反应
盐类的通性
预测:
选择试剂:
理论依据:
预期现象:
实际现象:
结论:
FeSO4
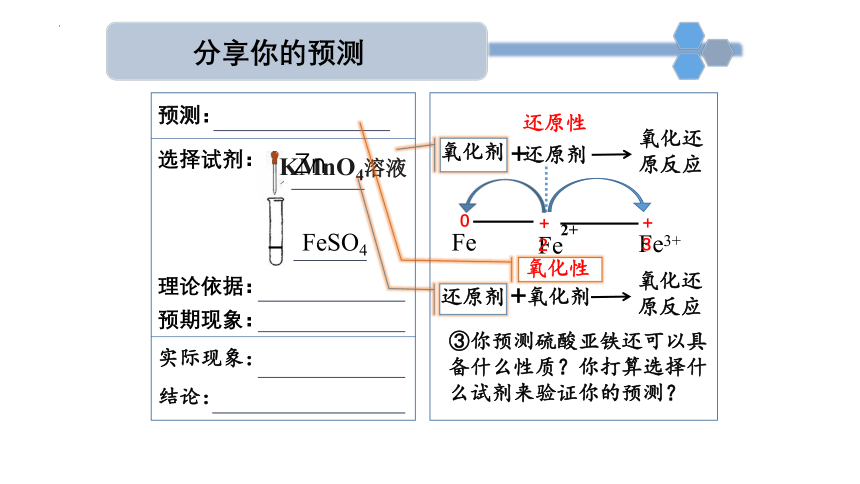
分享你的预测
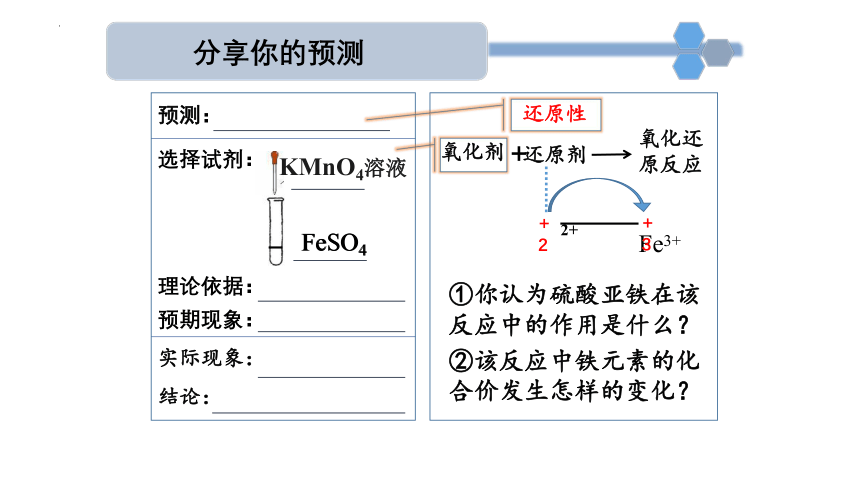
KMnO4溶液
FeSO4
+2
①你认为硫酸亚铁在该反应中的作用是什么?
Fe3+
+3
2+
还原剂
氧化剂
+
氧化还原反应
②该反应中铁元素的化合价发生怎样的变化?
还原性
预测:
选择试剂:
理论依据:
预期现象:
实际现象:
结论:
FeSO4
分享你的预测
KMnO4溶液
FeSO4
+2
Fe3+
+3
2+
还原剂
氧化剂
+
氧化还原反应
还原性
0
Fe
氧化剂
③你预测硫酸亚铁还可以具备什么性质?你打算选择什么试剂来验证你的预测?
Zn
还原剂
+
氧化还原反应
氧化性
灵敏试剂--KSCN(硫氰化钾)溶液
FeCl3溶液
KSCN
Fe3+遇KSCN溶液显红色
Fe2+遇KSCN不显红色
Fe3+的检验
取半药匙硫酸亚铁晶体于烧杯中,加10mL水溶解,分成3份于试管中进行实验。
滴加其他试剂各5-6滴,Zn取2粒。
实 验
节约试剂
方法得当
白板衬底
认真观察
记录现象
用心思考
FeSO4
NaOH
FeSO4
Zn
FeSO4
KMnO4溶液或氯水
别忘检验产物哟!
预测:
选择试剂:
理论依据:
预期现象:
实际现象:
结论:
FeSO4
分享你的实验
盐的通性—与碱反应
NaOH溶液
复分解反应
产生白色沉淀
产生绿色沉淀
FeSO4能与碱反应
FeSO4+2NaOH =Fe(OH)2 +Na2SO4
4Fe(OH)2 + O2+2H2O = 4Fe(OH)3
预测:
选择试剂:
理论依据:
预期现象:
实际现象:
结论:
FeSO4
分享你的实验
FeSO4具有氧化性
Zn
置换反应
无明显现象
FeSO4具有氧化性
FeSO4+Zn=ZnSO4+Fe
锌表面附着黑色物质
预测:
选择试剂:
理论依据:
预期现象:
实际现象:
结论:
FeSO4
分享你的实验
KMnO4溶液
KMnO4具有氧化性
酸性KMnO4溶液褪色
酸性KMnO4溶液褪色
FeSO4具有还原性
FeSO4具有还原性
滴加KSCN试剂溶液变红,说明有Fe3+生成。
Fe
FeO
Fe2O3
Fe(OH)2
Fe(OH)3
单质
氧化物
氢氧化物
盐
物质类别
Fe2(SO4)3
FeSO4
化合价
0
+2
+3
你能预测它的化学性质吗?
三价铁盐的性质
1.盐类的性质
①与碱反应
Fe3+ + 3OH- = Fe(OH)3
②与金属单质反应
(如Zn等)
2Fe3+ + 3Zn = 3Zn2++2Fe
红褐色
2.氧化性
Fe3+
Fe2+
Fe
2Fe3+ + Fe = 3Fe2+
2Fe3+ + Cu = Cu2++2Fe2+
例如与Fe、Cu单质反应
与具有还原性的物质反应
解决问题
你认为硫酸亚铁溶液在空气中易变质的原因可能是什么?
你有什么好办法解决这个问题吗?
用于儿童各种原因引起的缺铁性贫血。
维生素C可促进铁的吸收
谢谢!再见!
铁及其化合物
将硫酸亚铁配成溶液喷于叶片上,可改善黄化效果。
硫酸亚铁容易变质
实验试剂:
1
铁 粉
2
锌 粒
3
NaOH溶液
4
氯 水
5
酸性KMnO4溶液
9
H2O2溶液
6
铜 丝
7
KSCN试剂
8
FeSO4溶液
10
盐 酸
我选择什么试剂?
我选择该试剂的理由是?
我认为它们可以发生什么类型的反应?
我预计试剂混合后能产生怎样的实验现象?
讨论 交流
预测:
选择试剂:
理论依据:
预期现象:
实际现象:
结论:
分享你的预测
预测:
选择试剂:
理论依据:
预期现象:
实际现象:
结论:
FeSO4
选什么?
怎样反应?
预测根据
分析你的预测
反应现象?
Zn
NaOH
酸
碱
盐
金属
复分解反应
置换反应
盐类的通性
预测:
选择试剂:
理论依据:
预期现象:
实际现象:
结论:
FeSO4
分享你的预测
KMnO4溶液
FeSO4
+2
①你认为硫酸亚铁在该反应中的作用是什么?
Fe3+
+3
2+
还原剂
氧化剂
+
氧化还原反应
②该反应中铁元素的化合价发生怎样的变化?
还原性
预测:
选择试剂:
理论依据:
预期现象:
实际现象:
结论:
FeSO4
分享你的预测
KMnO4溶液
FeSO4
+2
Fe3+
+3
2+
还原剂
氧化剂
+
氧化还原反应
还原性
0
Fe
氧化剂
③你预测硫酸亚铁还可以具备什么性质?你打算选择什么试剂来验证你的预测?
Zn
还原剂
+
氧化还原反应
氧化性
灵敏试剂--KSCN(硫氰化钾)溶液
FeCl3溶液
KSCN
Fe3+遇KSCN溶液显红色
Fe2+遇KSCN不显红色
Fe3+的检验
取半药匙硫酸亚铁晶体于烧杯中,加10mL水溶解,分成3份于试管中进行实验。
滴加其他试剂各5-6滴,Zn取2粒。
实 验
节约试剂
方法得当
白板衬底
认真观察
记录现象
用心思考
FeSO4
NaOH
FeSO4
Zn
FeSO4
KMnO4溶液或氯水
别忘检验产物哟!
预测:
选择试剂:
理论依据:
预期现象:
实际现象:
结论:
FeSO4
分享你的实验
盐的通性—与碱反应
NaOH溶液
复分解反应
产生白色沉淀
产生绿色沉淀
FeSO4能与碱反应
FeSO4+2NaOH =Fe(OH)2 +Na2SO4
4Fe(OH)2 + O2+2H2O = 4Fe(OH)3
预测:
选择试剂:
理论依据:
预期现象:
实际现象:
结论:
FeSO4
分享你的实验
FeSO4具有氧化性
Zn
置换反应
无明显现象
FeSO4具有氧化性
FeSO4+Zn=ZnSO4+Fe
锌表面附着黑色物质
预测:
选择试剂:
理论依据:
预期现象:
实际现象:
结论:
FeSO4
分享你的实验
KMnO4溶液
KMnO4具有氧化性
酸性KMnO4溶液褪色
酸性KMnO4溶液褪色
FeSO4具有还原性
FeSO4具有还原性
滴加KSCN试剂溶液变红,说明有Fe3+生成。
Fe
FeO
Fe2O3
Fe(OH)2
Fe(OH)3
单质
氧化物
氢氧化物
盐
物质类别
Fe2(SO4)3
FeSO4
化合价
0
+2
+3
你能预测它的化学性质吗?
三价铁盐的性质
1.盐类的性质
①与碱反应
Fe3+ + 3OH- = Fe(OH)3
②与金属单质反应
(如Zn等)
2Fe3+ + 3Zn = 3Zn2++2Fe
红褐色
2.氧化性
Fe3+
Fe2+
Fe
2Fe3+ + Fe = 3Fe2+
2Fe3+ + Cu = Cu2++2Fe2+
例如与Fe、Cu单质反应
与具有还原性的物质反应
解决问题
你认为硫酸亚铁溶液在空气中易变质的原因可能是什么?
你有什么好办法解决这个问题吗?
用于儿童各种原因引起的缺铁性贫血。
维生素C可促进铁的吸收
谢谢!再见!
