四川省各市2023年中考化学真题分类分层汇编-06填空题(基础提升)(含解析)
文档属性
| 名称 | 四川省各市2023年中考化学真题分类分层汇编-06填空题(基础提升)(含解析) | 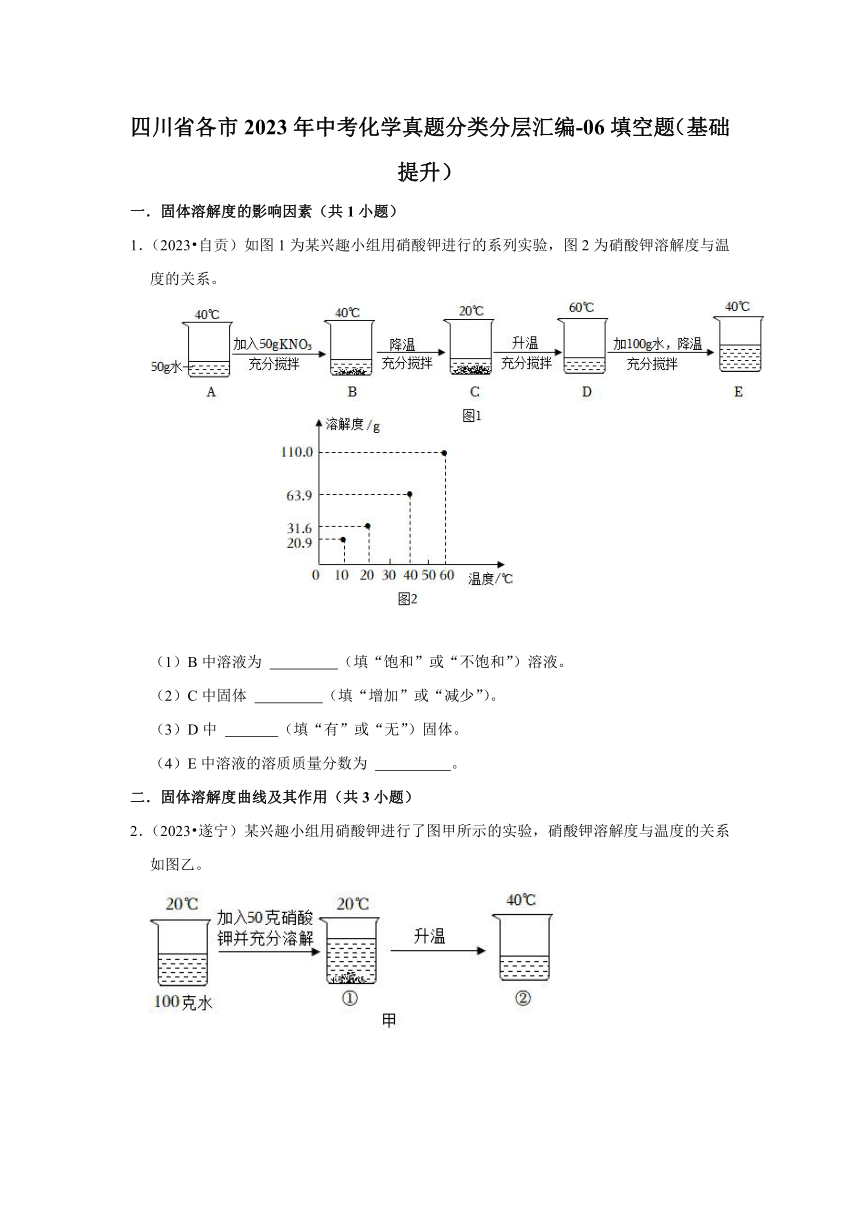 | |
| 格式 | doc | ||
| 文件大小 | 614.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-02 21:27:35 | ||
图片预览




文档简介
四川省各市2023年中考化学真题分类分层汇编-06填空题(基础提升)
一.固体溶解度的影响因素(共1小题)
1.(2023 自贡)如图1为某兴趣小组用硝酸钾进行的系列实验,图2为硝酸钾溶解度与温度的关系。
(1)B中溶液为 (填“饱和”或“不饱和”)溶液。
(2)C中固体 (填“增加”或“减少”)。
(3)D中 (填“有”或“无”)固体。
(4)E中溶液的溶质质量分数为 。
二.固体溶解度曲线及其作用(共3小题)
2.(2023 遂宁)某兴趣小组用硝酸钾进行了图甲所示的实验,硝酸钾溶解度与温度的关系如图乙。
(1)10℃时,硝酸钾的溶解度是 克;
(2)②中硝酸钾溶液是 (选填“饱和”或“不饱和”)溶液;
(3)通过查阅资料知道氯化钠的溶解度受温度影响较小。从硝酸钾溶液(含有少量氯化钠)中提纯硝酸钾的方法是 结晶。
3.(2023 凉山州)中国为2022年卡塔尔世界杯提供了大量科技支持,如光伏发电、海水淡化等。
(1)检验淡化后的海水是否属于硬水,最简便的方法是加入 。
(2)下列有关水的说法错误的是 。
A.为倡导节约用水,可在公共用水区域张贴图1标志
B.用水灭火,是利用水蒸发吸热使温度降到可燃物的着火点以下
C.用水可鉴别硝酸铵、氢氧化钠、蔗糖三种白色固体
D.工业上的冷却水可重复利用
(3)水是常用的溶剂。请根据图2溶解度曲线回答问题:
①图2中P点的含义是 。
②t2℃时,将30g甲物质加到50g水中充分溶解,所得溶液的质量是 g。
③t2℃时,等质量的甲、乙、丙饱和溶液中溶剂的质量由多到少依次为 。
4.(2023 南充)溶液在日常生活、工农业生产和科学研究中具有广泛的用途。
(1)碘酒用于消毒杀菌,其溶剂是 (填化学式)。
(2)如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,回答下列问题:
①甲中混有少量乙时,提纯甲的方法是 。
②t2℃时,将30g甲固体加入到50g水中,充分溶解并恢复到原温度,所得溶液中溶质和溶液的质量之比为 (填最简整数比)。
③t2℃时,将甲、乙、丙的饱和溶液降温到t1℃,下列说法正确的是 (填选项)。
A.析出晶体质量最多的是甲
B.溶质质量分数大小关系是:乙>甲>丙
C.得到的都是饱和溶液
D.溶剂质量大小关系是:丙>乙>甲
三.氯化钠与粗盐提纯(共1小题)
5.(2023 眉山)红色经典影片《闪闪的红星》中有一段儿童团员潘冬子给红军送盐的故事。冬子开始把食盐装在竹筒中,打算扮作上山砍柴的人将食盐送给红军。途中发现敌人盘查严格,冬子急中生智跑到河边,把竹筒里的食盐全部溶成盐水,再用棉袄吸收,最终顺利地将食盐送给了红军。回答下列问题:
(1)从物质分类的角度分析,盐水属于 (填“纯净物”或“混合物”);从物质变化的角度分析,食盐溶成水属于 (填“物理变化”或“化学变化”);
(2)从棉袄中挤出盐水,过滤,蒸发得到食盐。其中用到的玻璃仪器有烧杯、玻璃棒、酒精灯和 ;
(3)氯化钠的溶解度如表。假设冬子的竹筒中有179g氯化钠,10℃时完全溶解所需水的质量至少为 g;
温度/℃ 0 10 20 30 40 50 60
氯化钠的溶解度/g 35.7 35.8 36.0 36.3 36.6 37.0 37.8
(4)氯化钠在生活中的用途: (任写一点即可)。
四.微粒观点及模型图的应用(共1小题)
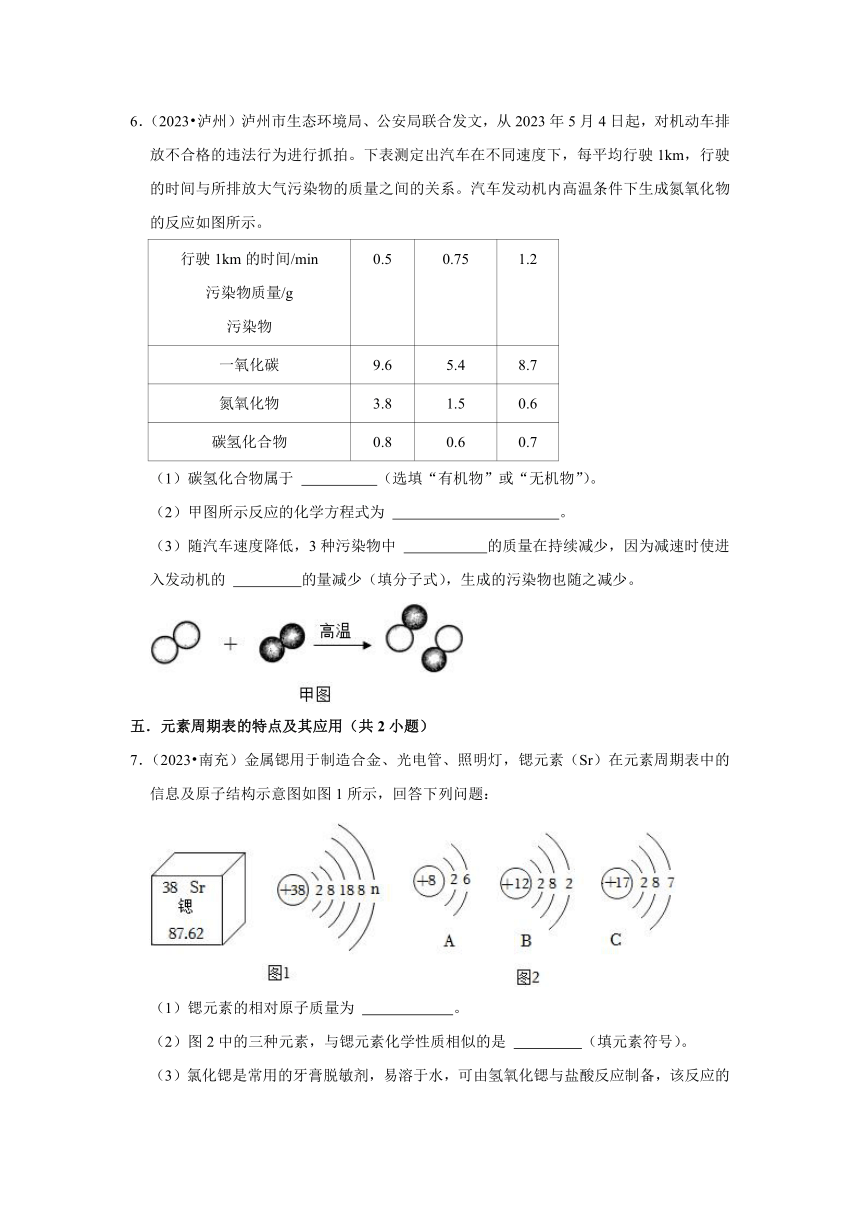
6.(2023 泸州)泸州市生态环境局、公安局联合发文,从2023年5月4日起,对机动车排放不合格的违法行为进行抓拍。下表测定出汽车在不同速度下,每平均行驶1km,行驶的时间与所排放大气污染物的质量之间的关系。汽车发动机内高温条件下生成氮氧化物的反应如图所示。
行驶1km的时间/min污染物质量/g污染物 0.5 0.75 1.2
一氧化碳 9.6 5.4 8.7
氮氧化物 3.8 1.5 0.6
碳氢化合物 0.8 0.6 0.7
(1)碳氢化合物属于 (选填“有机物”或“无机物”)。
(2)甲图所示反应的化学方程式为 。
(3)随汽车速度降低,3种污染物中 的质量在持续减少,因为减速时使进入发动机的 的量减少(填分子式),生成的污染物也随之减少。
五.元素周期表的特点及其应用(共2小题)
7.(2023 南充)金属锶用于制造合金、光电管、照明灯,锶元素(Sr)在元素周期表中的信息及原子结构示意图如图1所示,回答下列问题:
(1)锶元素的相对原子质量为 。
(2)图2中的三种元素,与锶元素化学性质相似的是 (填元素符号)。
(3)氯化锶是常用的牙膏脱敏剂,易溶于水,可由氢氧化锶与盐酸反应制备,该反应的化学方程式为 。
8.(2023 达州)元素周期表是学习和研究化学、探索未知世界最有力的工具之一。图一是元素周期表的部分信息,图二是两种粒子的结构示意图。请回答下列问题。
(1)在前人的研究基础上得到第一张元素周期表的化学家是 (填字母编号,下同)。
A.徐寿
B.卢瑟福
C.侯德榜
D.门捷列夫
(2)图一中镁元素与铝元素之间最本质的区别是 不同。
A.中子数
B.质子数
C.核外电子数
D.相对原子质量
(3)图一中氖原子的相对原子质量为 。
(4)图二中两种粒子形成的化合物化学式为 。
六.标签上标示的物质成分及其含量(共1小题)
9.(2023 泸州)某品牌饮用矿泉水的说明书如表所示。回答相关问题:
XXX(饮用矿泉水)净含量:350mL配料表:纯净水、硫酸镁、氯化钾保质期:12个月主要成分:水钾离子:1.0~27.3mg/L镁离子:0.1~4.9mg/L氯离子:1.0~27.3mg/L硫酸根离子:0.4~19.5mg/L
(1)该品牌饮用矿泉水配料中加了 种盐(填数字)。
(2)检验饮用矿泉水中含有硫酸根离子的方法是:取2mL浓缩后的矿泉水于试管中,滴加 ,观察到 现象时,即可证明。
(3)主要成分中,最外层电子数为8的阴离子的符号是 。
七.化学符号及其周围数字的意义(共1小题)
10.(2023 达州)化学用语是最简明、信息丰富、化学世界通用的语言。请用化学用语填空。
(1)银离子 ;
(2)二氧化硫 ;
(3)6个氧分子 ;
(4)6个钙原子 。
八.根据化学反应方程式的计算(共2小题)
11.(2023 泸州)泸州的天然气化工实力雄厚,天然气可制备多种化工产品,由天然气→氢气→氨气→硝酸各步转化的反应如下(反应条件未给出)。回答相关问题:
①CH4+2H2O═CO2+4H2;②N2+3H2═2NH3;③NH3+2O2═HNO3+H2O
(1)属于化合反应的是 (填反应的序号)。
(2)③反应中氮的化合价升高了 价。若③恰好完全反应,所得硝酸溶液的溶质质量分数为 (列出计算式即可)。
12.(2023 遂宁)小贤向154.9gCuSO4和H2SO4的混合溶液中加入50g16%的NaOH溶液,充分反应后,产生蓝色沉淀,过滤,得到固体4.9g和无色滤液,向无色滤液中滴加酚酞试液,无明显现象。
(1)蓝色沉淀的物质名称为 ;
(2)发生中和反应的化学方程式为 ;
(3)无色滤液中溶质的质量分数为 。
九.复合材料、纳米材料(共1小题)
13.(2023 成都)根据图文回答下列问题。
(1)潜航时,必须调节舱内氧气、水蒸气和 的含量。制造“蛟龙号”外壳的合金应选择 (填字母)。
a.黄铜
b.不锈钢
c.钛合金
(2)航天食品有脱水米饭、宫爆鸡丁、茶饮等,米饭富含的营养素主要是 。为保证营养均衡,提供了水果,作用是 。
(3)高铁制造用到铝合金、玻璃钢、碳纤维等,属于复合材料的是 。座椅内填充了“聚氨酯高回弹发泡”新材料,具有防火阻燃、吸音性好、 (写一条)等特点。
(4)大运会场馆地下车库通过一氧化碳传感器反馈值来确定送排风系统的开启与关闭。车库内一氧化碳主要来源于 ,危害是 。
一十.生命活动与六大营养素(共1小题)
14.(2023 泸州)泸州白酒酿制“始于商周,盛于明清,纵横二千余年”,发展为以高梁与曲药为原料的独特酿造技术,其中曲药富含各种微生物,以及微生物所分泌的酶。回答下列问题:
(1)曲药能加快高梁中的 转化为葡萄糖。
(2)在酵母菌的作用下,将葡萄糖(C6H12O6) 分解成乙醇(C2H5OH),还有一种气体产物,该反应的化学方程式为 。
(3)发酵后的混合物得到白酒的最佳方法是 (选填“蒸馏”或“过滤”)。
(4)泸州曲药制酒的独特酿造技术是几百年来经过酿酒师们的不断劳动实践形成的,如果技术不精,“火候”把握不好会有酸味,影响口感,主要是因为产生了 。
(5)白酒的酒度通常是指20℃时酒精的体积百分数。如60度(60°)白酒是指100mL白酒中含酒精60mL。如何用500mL有刻度的器皿,将50°白酒勾兑出500mL40°白酒? 。
一十一.食品、药品与健康食品中的有机营养素(共1小题)
15.(2023 南充)化学来源于生活,服务于生活,回答下列问题。
(1)下列南充名小吃都富含蛋白质的是 (填选项)。
A.川北凉粉、南部肥肠
B.营山凉面、西充狮子糕
C.张飞牛肉、河舒豆腐
(2)生产自来水的过程中,可用高铁酸钾(K2FeO4)作净水剂,高铁酸钾中铁元素的化合价为 ,在一定条件下可发生反应:4K2FeO4+10X═4Fe(OH)3↓+8KOH+3O2↑,则X的化学式为 。
(3)空气中的氮气可合成氨气,其微观反应示意图如图,下列说法正确的是 (填选项)。
A.该反应的基本反应类型为复分解反应
B.该反应中分子的种类发生了变化
C.生成物的分子个数比为1:1
D.6000L氨气可压缩保存在40L的钢瓶中,说明气体分子间间隔较大
四川省各市2023年中考化学真题分类分层汇编-06填空题(基础提升)
参考答案与试题解析
一.固体溶解度的影响因素(共1小题)
1.(2023 自贡)如图1为某兴趣小组用硝酸钾进行的系列实验,图2为硝酸钾溶解度与温度的关系。
(1)B中溶液为 饱和 (填“饱和”或“不饱和”)溶液。
(2)C中固体 增加 (填“增加”或“减少”)。
(3)D中 无 (填“有”或“无”)固体。
(4)E中溶液的溶质质量分数为 25% 。
【答案】(1)饱和;
(2)增加;
(3)无;
(4)25%。
【解答】解:(1)40℃时,硝酸钾的溶解度为63.9g,则该温度下的50g水中的最多能溶解31.95g硝酸钾,则B中硝酸钾不能全部溶解,所得溶液为饱和溶液;故答案为:饱和;
(2)硝酸钾的溶解度随温度的降低而减小,因此B中硝酸钾的饱和溶液降温至20℃时,硝酸钾会部分结晶析出,所以C中固体增加;故答案为:增加;
(3)60℃时,硝酸钾的溶解度为110.0g,则该温度下的50g水中最多能溶解硝酸钾的质量为55.0g,因此加入的50g硝酸钾晶体全部溶解,D中没有固体;故答案为:无;
(4)40℃时,硝酸钾的溶解度为63.9g,则该温度下的150g水中的最多能溶解硝酸钾的质量为63.9g×1.5=95.85g,所以50g硝酸钾完全溶解,所得溶液中溶质的质量分数为=25%;故答案为:25%。
二.固体溶解度曲线及其作用(共3小题)
2.(2023 遂宁)某兴趣小组用硝酸钾进行了图甲所示的实验,硝酸钾溶解度与温度的关系如图乙。
(1)10℃时,硝酸钾的溶解度是 20.6 克;
(2)②中硝酸钾溶液是 不饱和 (选填“饱和”或“不饱和”)溶液;
(3)通过查阅资料知道氯化钠的溶解度受温度影响较小。从硝酸钾溶液(含有少量氯化钠)中提纯硝酸钾的方法是 降温 结晶。
【答案】(1)20.6;
(2)不饱和;
(3)降温。
【解答】解:(1)由硝酸钾溶解度与温度的关系图,10℃时,硝酸钾的溶解度是20.6g。
(2)40℃时,硝酸钾的溶解度是63.9g,则40℃时,100g水中最多能溶解63.9g硝酸钾,溶液达到饱和状态,则②中硝酸钾溶液是不饱和溶液。
(3)硝酸钾的溶解度受温度影响较大,而氯化钠受温度影响较小,则从硝酸钾溶液(含有少量氯化钠)中提纯硝酸钾的方法是降温结晶。
故答案为:
(1)20.6;
(2)不饱和;
(3)降温。
3.(2023 凉山州)中国为2022年卡塔尔世界杯提供了大量科技支持,如光伏发电、海水淡化等。
(1)检验淡化后的海水是否属于硬水,最简便的方法是加入 肥皂水 。
(2)下列有关水的说法错误的是 A 。
A.为倡导节约用水,可在公共用水区域张贴图1标志
B.用水灭火,是利用水蒸发吸热使温度降到可燃物的着火点以下
C.用水可鉴别硝酸铵、氢氧化钠、蔗糖三种白色固体
D.工业上的冷却水可重复利用
(3)水是常用的溶剂。请根据图2溶解度曲线回答问题:
①图2中P点的含义是 在t1℃时,甲和丙的溶解度相等 。
②t2℃时,将30g甲物质加到50g水中充分溶解,所得溶液的质量是 75 g。
③t2℃时,等质量的甲、乙、丙饱和溶液中溶剂的质量由多到少依次为 丙>乙>甲 。
【答案】(1)肥皂水;
(2)A;
(3)①在t1℃时,甲和丙的溶解度相等;
②75g;
③丙>乙>甲。
【解答】解:(1)向水中加入肥皂水时,如果产生的泡沫很多,是软水;如果不产生泡沫或产生的泡沫很少,是硬水。
(2)A、图1为中国节能标志,为倡导节约用水,可在公共用水区域张贴节水标志,故错误;
B、用水灭火的原理主要是利用水蒸发吸热,使温度降到可燃物的着火点以下,故正确;
C、可用水鉴别硝酸铵、氢氧化钠、蔗糖三种白色固体,溶于水温度几乎不变的是蔗糖,溶于水放热使温度升高的是氢氧化钠,溶于水吸热使温度降低的是硝酸铵,故正确;
D、工业上冷却水重复利用,能节约用水,利于保护水资源,故正确;
(3)①图2中P点的含义是:在t1℃时,甲和丙的溶解度相等;
②t2℃时甲的溶解度是50g,将30g甲物质加到50g水中,充分溶解后,能够溶解25g,所得溶液的质量为75g;
③t2℃时,:甲>乙>丙,所以等质量的甲、乙、丙饱和溶液中溶剂的质量由多到少依次为:丙>乙>甲。
故答案为:(1)肥皂水;
(2)A;
(3)①在t1℃时,甲和丙的溶解度相等;
②75g;
③丙>乙>甲。
4.(2023 南充)溶液在日常生活、工农业生产和科学研究中具有广泛的用途。
(1)碘酒用于消毒杀菌,其溶剂是 C2H5OH (填化学式)。
(2)如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,回答下列问题:
①甲中混有少量乙时,提纯甲的方法是 降温结晶 。
②t2℃时,将30g甲固体加入到50g水中,充分溶解并恢复到原温度,所得溶液中溶质和溶液的质量之比为 2:7 (填最简整数比)。
③t2℃时,将甲、乙、丙的饱和溶液降温到t1℃,下列说法正确的是 B (填选项)。
A.析出晶体质量最多的是甲
B.溶质质量分数大小关系是:乙>甲>丙
C.得到的都是饱和溶液
D.溶剂质量大小关系是:丙>乙>甲
【答案】(1)C2H5OH;
(2)①降温结晶;②2:7;③B。
【解答】解:(1)碘酒用于消毒杀菌,其溶剂是酒精,化学式为:C2H5OH。
(2)①由图可知,甲、乙的溶解度都随温度的降低而减小,甲的溶解度受温度变化影响较大,则甲中混有少量乙时,提纯甲的方法是降温结晶。
②t2℃时,甲的溶解度是40g,即100g水中最多溶解40g甲,则50g水中最多溶解20g甲;将30g甲固体加入到50g水中,充分溶解并恢复到原温度,只能溶解20g的甲,则所得溶液中含有20g溶质和50g溶剂,溶质和溶液的质量之比为20g:(20g+50g)=2:7。
③A、将t2℃时甲、乙、丙的饱和溶液降温到t1℃,由于不知道溶液的质量,无法判断析出晶体的质量,故选项说法错误;
B、甲、乙的溶解度随温度的降低而减小,丙的溶解度随温度的降低而增大,将t2℃时甲、乙、丙的饱和溶液降温到t1℃,甲、乙溶液中有晶体析出,此时甲、乙的溶质质量分数为t1℃时甲、乙饱和溶液的溶质质量分数,大小关系为:乙>甲,而丙的溶质质量分数不变,等于t2℃时丙饱和溶液的溶质质量分数,所以溶质质量分数大小关系是:乙>甲>丙,故选项说法正确;
C、丙的溶解度随温度的降低而增大,所以得到的丙溶液不是饱和溶液,故选项说法错误;
D、由于不知道t2℃时甲、乙、丙饱和溶液的质量,所以无法判断溶剂质量的大小,故选项说法错误;
故选:B。
故答案为:
(1)C2H5OH;
(2)①降温结晶;②2:7;③B。
三.氯化钠与粗盐提纯(共1小题)
5.(2023 眉山)红色经典影片《闪闪的红星》中有一段儿童团员潘冬子给红军送盐的故事。冬子开始把食盐装在竹筒中,打算扮作上山砍柴的人将食盐送给红军。途中发现敌人盘查严格,冬子急中生智跑到河边,把竹筒里的食盐全部溶成盐水,再用棉袄吸收,最终顺利地将食盐送给了红军。回答下列问题:
(1)从物质分类的角度分析,盐水属于 混合物 (填“纯净物”或“混合物”);从物质变化的角度分析,食盐溶成水属于 物理变化 (填“物理变化”或“化学变化”);
(2)从棉袄中挤出盐水,过滤,蒸发得到食盐。其中用到的玻璃仪器有烧杯、玻璃棒、酒精灯和 漏斗 ;
(3)氯化钠的溶解度如表。假设冬子的竹筒中有179g氯化钠,10℃时完全溶解所需水的质量至少为 500 g;
温度/℃ 0 10 20 30 40 50 60
氯化钠的溶解度/g 35.7 35.8 36.0 36.3 36.6 37.0 37.8
(4)氯化钠在生活中的用途: 作调味品(合理即可) (任写一点即可)。
【答案】(1)混合物;物理变化;
(2)漏斗;
(3)500;
(4)作调味品(合理即可)。
【解答】解:(1)从物质分类的角度分析,盐水中含有氯化钠、水,属于混合物。
从物质变化的角度分析,食盐溶成水,没有新物质生成,属于物理变化。
(2)过滤是把不溶于液体的固体与液体分离的一种方法,过滤操作的装置由铁架台、烧杯、玻璃棒、漏斗四种仪器组成;蒸发操作的装置由铁架台、玻璃棒、酒精灯、蒸发皿四种仪器组成;其中用到的玻璃仪器有烧杯、玻璃棒、酒精灯和漏斗。
(3)10℃时氯化钠的溶解度为35.8g,冬子的竹筒中有179g氯化钠,10℃时完全溶解所需水的质量至少为100g×=500g。
(4)氯化钠在生活中可用作调味品,用于腌制咸菜,用于制造生理盐水,农业生产中用于选种,用于融雪等。
故答案为:
(1)混合物;物理变化;
(2)漏斗;
(3)500;
(4)作调味品(合理即可)。
四.微粒观点及模型图的应用(共1小题)
6.(2023 泸州)泸州市生态环境局、公安局联合发文,从2023年5月4日起,对机动车排放不合格的违法行为进行抓拍。下表测定出汽车在不同速度下,每平均行驶1km,行驶的时间与所排放大气污染物的质量之间的关系。汽车发动机内高温条件下生成氮氧化物的反应如图所示。
行驶1km的时间/min污染物质量/g污染物 0.5 0.75 1.2
一氧化碳 9.6 5.4 8.7
氮氧化物 3.8 1.5 0.6
碳氢化合物 0.8 0.6 0.7
(1)碳氢化合物属于 有机物 (选填“有机物”或“无机物”)。
(2)甲图所示反应的化学方程式为 N2+O22NO 。
(3)随汽车速度降低,3种污染物中 氮氧化物 的质量在持续减少,因为减速时使进入发动机的 N2 的量减少(填分子式),生成的污染物也随之减少。
【答案】(1)有机物;
(2)N2+O22NO;
(3)氮氧化物;N2。
【解答】解:(1)碳氢化合物是一种含碳元素的化合物,属于有机物;故答案为:有机物;
(2)由微观反应示意图可知,该反应是由氮气与氧气在高温的条件下反应生成一氧化氮,化学方程式为N2+O22NO;故答案为:N2+O22NO;
(3)由表格中的数据可知,随汽车速度降低,3种污染物中氮氧化物的质量在持续减少,因为减速时使进入发动机的氮气的量减少,生成的污染物也随之减少,氮气的化学式为N2;故答案为:氮氧化物;N2。
五.元素周期表的特点及其应用(共2小题)
7.(2023 南充)金属锶用于制造合金、光电管、照明灯,锶元素(Sr)在元素周期表中的信息及原子结构示意图如图1所示,回答下列问题:
(1)锶元素的相对原子质量为 87.62 。
(2)图2中的三种元素,与锶元素化学性质相似的是 Mg (填元素符号)。
(3)氯化锶是常用的牙膏脱敏剂,易溶于水,可由氢氧化锶与盐酸反应制备,该反应的化学方程式为 Sr(OH)2+2HCl═SrCl2+2H2O 。
【答案】(1)87.62;
(2)Mg。
(3)Sr(OH)2+2HCl═SrCl2+2H2O。
【解答】解:(1)根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为87.62。
(2)原子中,质子数=核外电子数,则38=2+8+18+8+n,n=2。
元素的化学性质跟它的原子的最外层电子数目关系非常密切,决定元素化学性质的是原子中的最外层电子数,图2中的三种元素,与锶元素化学性质相似的是B,它们原子的最外层电子数均为2,核内质子数为12,为镁元素,其元素符号为Mg。
(3)氢氧化锶与盐酸反应生成氯化锶和水,反应的化学方程式为Sr(OH)2+2HCl═SrCl2+2H2O。
故答案为:
(1)87.62;
(2)Mg。
(3)Sr(OH)2+2HCl═SrCl2+2H2O。
8.(2023 达州)元素周期表是学习和研究化学、探索未知世界最有力的工具之一。图一是元素周期表的部分信息,图二是两种粒子的结构示意图。请回答下列问题。
(1)在前人的研究基础上得到第一张元素周期表的化学家是 D (填字母编号,下同)。
A.徐寿
B.卢瑟福
C.侯德榜
D.门捷列夫
(2)图一中镁元素与铝元素之间最本质的区别是 B 不同。
A.中子数
B.质子数
C.核外电子数
D.相对原子质量
(3)图一中氖原子的相对原子质量为 20.18 。
(4)图二中两种粒子形成的化合物化学式为 NaF 。
【答案】(1)D;
(2)B;
(3)20.18;
(4)NaF。
【解答】解:(1)门捷列夫在化学上的主要贡献是在前人的研究基础上编制出第一张元素周期表。
(2)元素是质子数(即核电荷数)相同的一类原子的总称,不同种元素最本质的区别是质子数(即核电荷数)不同,所以镁元素与铝元素之间的本质区别是质子数(即核电荷数)不同。
(3)根据氖元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为20.18。
(4)图二中两种粒子的核内质子数分别是11、9,分别是钠元素和氟元素,钠原子的最外层电子数为1,在化学反应中易失去1个电子而形成带1个单位正电荷的阳离子,化合价的数值等于离子所带电荷的数值,且符号一致,则该元素的化合价为+1价;氟原子的最外层电子数为7,在化学反应中易得到1个电子而形成1个单位负电荷的阴离子,化合价的数值等于离子所带电荷的数值,且符号一致,则该元素的化合价为﹣1价;钠元素显+1价,氟元素显﹣1价,组成化合物的化学式为NaF。
故答案为:
(1)D;
(2)B;
(3)20.18;
(4)NaF。
六.标签上标示的物质成分及其含量(共1小题)
9.(2023 泸州)某品牌饮用矿泉水的说明书如表所示。回答相关问题:
XXX(饮用矿泉水)净含量:350mL配料表:纯净水、硫酸镁、氯化钾保质期:12个月主要成分:水钾离子:1.0~27.3mg/L镁离子:0.1~4.9mg/L氯离子:1.0~27.3mg/L硫酸根离子:0.4~19.5mg/L
(1)该品牌饮用矿泉水配料中加了 2 种盐(填数字)。
(2)检验饮用矿泉水中含有硫酸根离子的方法是:取2mL浓缩后的矿泉水于试管中,滴加 用硝酸酸化的硝酸钡溶液 ,观察到 产生白色沉淀 现象时,即可证明。
(3)主要成分中,最外层电子数为8的阴离子的符号是 Cl﹣ 。
【答案】(1)2;
(2)用硝酸酸化的硝酸钡溶液;产生白色沉淀;
(3)Cl﹣。
【解答】解:(1)由配料表,硫酸镁、氯化钾均是由金属离子和酸根离子构成的化合物,均属于盐。
(2)检验饮用矿泉水中含有硫酸根离子的方法是:取2mL浓缩后的矿泉水于试管中,滴加用硝酸酸化的硝酸钡溶液,观察到产生白色沉淀,即可证明。
(3)主要成分中,最外层电子数为8的阴离子是氯离子,其离子符号为Cl﹣。
故答案为:
(1)2;
(2)用硝酸酸化的硝酸钡溶液;产生白色沉淀;
(3)Cl﹣。
七.化学符号及其周围数字的意义(共1小题)
10.(2023 达州)化学用语是最简明、信息丰富、化学世界通用的语言。请用化学用语填空。
(1)银离子 Ag+ ;
(2)二氧化硫 SO2 ;
(3)6个氧分子 6O2 ;
(4)6个钙原子 6Ca 。
【答案】(1)Ag+;
(2)SO2;
(3)6O2;
(4)6Ca。
【解答】解:(1)由离子的表示方法,在表示该离子的元素符号或原子团的右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个单位电荷时,1要省略。银离子可表示为Ag+。
(2)二氧化硫的化学式为SO2。
(3)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则6个氧分子可表示为6O2。
(4)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故6个钙原子表示为6Ca。
故答案为:
(1)Ag+;
(2)SO2;
(3)6O2;
(4)6Ca。
八.根据化学反应方程式的计算(共2小题)
11.(2023 泸州)泸州的天然气化工实力雄厚,天然气可制备多种化工产品,由天然气→氢气→氨气→硝酸各步转化的反应如下(反应条件未给出)。回答相关问题:
①CH4+2H2O═CO2+4H2;②N2+3H2═2NH3;③NH3+2O2═HNO3+H2O
(1)属于化合反应的是 ② (填反应的序号)。
(2)③反应中氮的化合价升高了 8 价。若③恰好完全反应,所得硝酸溶液的溶质质量分数为 100% (列出计算式即可)。
【答案】(1)②;
(2)8;100%。
【解答】解:(1)②N2+3H2═2NH3,该反应符合“多变一”的形式,符合化合反应的特征,属于化合反应。
(2)NH3中氮元素的化合价为﹣3价,HNO3中氮元素的化合价为+5价,则③反应中氮的化合价升高了8价。
设生成的硝酸的质量为63g,同时生成水的质量为x。
NH3+2O2═HNO3+H2O
63 18
63g x
x=18g
所得硝酸溶液的溶质质量分数为×100%=100%。
故答案为:
(1)②;
(2)8;100%。
12.(2023 遂宁)小贤向154.9gCuSO4和H2SO4的混合溶液中加入50g16%的NaOH溶液,充分反应后,产生蓝色沉淀,过滤,得到固体4.9g和无色滤液,向无色滤液中滴加酚酞试液,无明显现象。
(1)蓝色沉淀的物质名称为 氢氧化铜 ;
(2)发生中和反应的化学方程式为 2NaOH+H2SO4═Na2SO4+2H2O ;
(3)无色滤液中溶质的质量分数为 7.1% 。
【答案】(1)氢氧化铜;
(2)2NaOH+H2SO4═Na2SO4+2H2O;
(3)7.1%。
【解答】解:(1)硫酸铜和氢氧化钠溶液反应生成氢氧化铜沉淀和硫酸钠,蓝色沉淀的物质名称为氢氧化铜。
(2)硫酸和氢氧化钠反应生成硫酸钠和水,属于中和反应,反应的化学方程式为2NaOH+H2SO4═Na2SO4+2H2O。
(3)氢氧化钠溶液先与硫酸反应生成硫酸钠和水,硫酸反应完,再与硫酸铜溶液反应生成氢氧化铜沉淀和硫酸钠,充分反应后,产生蓝色沉淀,过滤,得到固体4.9g和无色滤液,说明硫酸铜已经完全反应;向无色滤液中滴加酚酞试液,无明显现象,说明氢氧化钠溶液已完全反应。
由2NaOH+H2SO4═Na2SO4+2H2O、2NaOH+CuSO4═Na2SO4+Cu(OH)2↓,可得:
2NaOH~Na2SO4
80 142
50g×16% x
x=14.2g
无色滤液中溶质的质量分数为×100%=7.1%。
故答案为:
(1)氢氧化铜;
(2)2NaOH+H2SO4═Na2SO4+2H2O;
(3)7.1%。
九.复合材料、纳米材料(共1小题)
13.(2023 成都)根据图文回答下列问题。
(1)潜航时,必须调节舱内氧气、水蒸气和 二氧化碳 的含量。制造“蛟龙号”外壳的合金应选择 c (填字母)。
a.黄铜
b.不锈钢
c.钛合金
(2)航天食品有脱水米饭、宫爆鸡丁、茶饮等,米饭富含的营养素主要是 糖类 。为保证营养均衡,提供了水果,作用是 补充维生素 。
(3)高铁制造用到铝合金、玻璃钢、碳纤维等,属于复合材料的是 玻璃钢 。座椅内填充了“聚氨酯高回弹发泡”新材料,具有防火阻燃、吸音性好、 弹性好 (写一条)等特点。
(4)大运会场馆地下车库通过一氧化碳传感器反馈值来确定送排风系统的开启与关闭。车库内一氧化碳主要来源于 汽车尾气 ,危害是 造成中毒 。
【答案】(1)二氧化碳;c;
(2)糖类;补充维生素;
(3)玻璃钢;弹性好;
(4)汽车尾气;造成中毒。
【解答】解:(1)呼吸作用消耗氧气,呼出二氧化碳,因此潜航时,必须调节舱内氧气、水蒸气和二氧化碳的含量。钛合金的强度大、机械性能好、耐腐蚀性强,因此制造“蛟龙号”外壳的合金应选择钛合金;
故答案为:二氧化碳;c;
(2)米饭富含的营养素主要是糖类。为保证营养均衡,提供了水果,作用是补充维生素;
故答案为:糖类;补充维生素;
(3)玻璃钢是由玻璃纤维和合成材料复合而成的,属于复合材料;座椅内填充了“聚氨酯高回弹发泡”新材料,具有防火阻燃、吸音性好、弹性好等特点;故答案为:玻璃钢;弹性好;
(4)一氧化碳有毒,车库内一氧化碳主要来源于汽车尾气,危害是造成中毒;
故答案为:汽车尾气;造成中毒。
一十.生命活动与六大营养素(共1小题)
14.(2023 泸州)泸州白酒酿制“始于商周,盛于明清,纵横二千余年”,发展为以高梁与曲药为原料的独特酿造技术,其中曲药富含各种微生物,以及微生物所分泌的酶。回答下列问题:
(1)曲药能加快高梁中的 淀粉 转化为葡萄糖。
(2)在酵母菌的作用下,将葡萄糖(C6H12O6) 分解成乙醇(C2H5OH),还有一种气体产物,该反应的化学方程式为 C6H12O62C2H5OH+2CO2↑ 。
(3)发酵后的混合物得到白酒的最佳方法是 蒸馏 (选填“蒸馏”或“过滤”)。
(4)泸州曲药制酒的独特酿造技术是几百年来经过酿酒师们的不断劳动实践形成的,如果技术不精,“火候”把握不好会有酸味,影响口感,主要是因为产生了 醋酸或乙酸 。
(5)白酒的酒度通常是指20℃时酒精的体积百分数。如60度(60°)白酒是指100mL白酒中含酒精60mL。如何用500mL有刻度的器皿,将50°白酒勾兑出500mL40°白酒? 用带有刻度的容器量取400mL50°的白酒,然后再向容器内加入蒸馏水至500mL即可 。
【答案】(1)淀粉;
(2)C6H12O62C2H5OH+2CO2↑;
(3)蒸馏;
(4)醋酸或乙酸;
(5)用带有刻度的容器量取400mL50°的白酒,然后再向容器内加入蒸馏水至500mL即可。
【解答】解:(1)曲药能加快高梁中的淀粉转化为葡萄糖;故答案为:淀粉;
(2)在酵母菌的作用下,将葡萄糖(C6H12O6) 分解成乙醇(C2H5OH),还有一种气体产物——二氧化碳,该反应的化学方程式为C6H12O62C2H5OH+2CO2↑;故答案为:C6H12O62C2H5OH+2CO2↑;
(3)酒精和水能以任意比互溶,但酒精和水的沸点不同,因此发酵后的混合物得到白酒的最佳方法是蒸馏;故答案为:蒸馏;
(4)泸州曲药制酒的独特酿造技术是几百年来经过酿酒师们的不断劳动实践形成的,如果技术不精,“火候”把握不好会有酸味,影响口感,主要是因为产生了乙酸,俗称醋酸;故答案为:醋酸或乙酸;
(5)设需要50°白酒的体积为x,则:
x×50%=500mL×40%
x=400mL
需要水的体积为500mL﹣400mL=100mL
即配制方法是用带有刻度的容器量取400mL50°的白酒,然后再向容器内加入蒸馏水至500mL即可;
故答案为:用带有刻度的容器量取400mL50°的白酒,然后再向容器内加入蒸馏水至500mL即可。
一十一.食品、药品与健康食品中的有机营养素(共1小题)
15.(2023 南充)化学来源于生活,服务于生活,回答下列问题。
(1)下列南充名小吃都富含蛋白质的是 C (填选项)。
A.川北凉粉、南部肥肠
B.营山凉面、西充狮子糕
C.张飞牛肉、河舒豆腐
(2)生产自来水的过程中,可用高铁酸钾(K2FeO4)作净水剂,高铁酸钾中铁元素的化合价为 +6 ,在一定条件下可发生反应:4K2FeO4+10X═4Fe(OH)3↓+8KOH+3O2↑,则X的化学式为 H2O 。
(3)空气中的氮气可合成氨气,其微观反应示意图如图,下列说法正确的是 BD (填选项)。
A.该反应的基本反应类型为复分解反应
B.该反应中分子的种类发生了变化
C.生成物的分子个数比为1:1
D.6000L氨气可压缩保存在40L的钢瓶中,说明气体分子间间隔较大
【答案】(1)C;
(2)+6;H2O;
(3)BD。
【解答】解:(1)A.川北凉粉富含糖类;南部肥肠富含蛋白质和与油脂,不合题意;
B.营山凉面富含糖类;西充狮子糕富含糖类和油脂,不合题意;
C.张飞牛肉和河舒豆腐均富含蛋白质,符合题意;
故答案为:C;
(2)在K2FeO4中,钾元素的化合价为+1价,氧元素的化合价为﹣2价,设该化合物中铁元素的化合价为x,由化学式和化合物中正负化合价的代数和为零,则(+1)×2+x+(﹣2)×4=0,解得x=+6;由质量守恒定律可知:反应前后原子的种类和个数不变,等号左边除10X外,有8个钾原子、4个铁原子、16个氧原子,等号右边有4个铁原子、8个钾原子、20个氢原子和26个氧原子,则10X中含有20个氢原子和10个氧元素,则X为H2O;故答案为:+6;H2O;
(3)由微观反应示意图可知,氮气和水在催化剂的作用下反应生成氨气和氧气,该反应的化学方程式是:6H2O+2N23O2+4NH3。
A.该反应是由一种单质与一种化合物反应生成另一种单质与另一种化合物的反应,基本反应类型为置换反应,说法错误;
B.由分子结构模型可知,该反应中分子的种类发生了变化,说法正确;
C.由化学方程式可知,生成物的分子个数比为3:4或4:3,说法错误;
D.6000L氨气可压缩保存在40L的钢瓶中,说明气体分子间间隔较大,说法正确。
故答案为:BD。
一.固体溶解度的影响因素(共1小题)
1.(2023 自贡)如图1为某兴趣小组用硝酸钾进行的系列实验,图2为硝酸钾溶解度与温度的关系。
(1)B中溶液为 (填“饱和”或“不饱和”)溶液。
(2)C中固体 (填“增加”或“减少”)。
(3)D中 (填“有”或“无”)固体。
(4)E中溶液的溶质质量分数为 。
二.固体溶解度曲线及其作用(共3小题)
2.(2023 遂宁)某兴趣小组用硝酸钾进行了图甲所示的实验,硝酸钾溶解度与温度的关系如图乙。
(1)10℃时,硝酸钾的溶解度是 克;
(2)②中硝酸钾溶液是 (选填“饱和”或“不饱和”)溶液;
(3)通过查阅资料知道氯化钠的溶解度受温度影响较小。从硝酸钾溶液(含有少量氯化钠)中提纯硝酸钾的方法是 结晶。
3.(2023 凉山州)中国为2022年卡塔尔世界杯提供了大量科技支持,如光伏发电、海水淡化等。
(1)检验淡化后的海水是否属于硬水,最简便的方法是加入 。
(2)下列有关水的说法错误的是 。
A.为倡导节约用水,可在公共用水区域张贴图1标志
B.用水灭火,是利用水蒸发吸热使温度降到可燃物的着火点以下
C.用水可鉴别硝酸铵、氢氧化钠、蔗糖三种白色固体
D.工业上的冷却水可重复利用
(3)水是常用的溶剂。请根据图2溶解度曲线回答问题:
①图2中P点的含义是 。
②t2℃时,将30g甲物质加到50g水中充分溶解,所得溶液的质量是 g。
③t2℃时,等质量的甲、乙、丙饱和溶液中溶剂的质量由多到少依次为 。
4.(2023 南充)溶液在日常生活、工农业生产和科学研究中具有广泛的用途。
(1)碘酒用于消毒杀菌,其溶剂是 (填化学式)。
(2)如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,回答下列问题:
①甲中混有少量乙时,提纯甲的方法是 。
②t2℃时,将30g甲固体加入到50g水中,充分溶解并恢复到原温度,所得溶液中溶质和溶液的质量之比为 (填最简整数比)。
③t2℃时,将甲、乙、丙的饱和溶液降温到t1℃,下列说法正确的是 (填选项)。
A.析出晶体质量最多的是甲
B.溶质质量分数大小关系是:乙>甲>丙
C.得到的都是饱和溶液
D.溶剂质量大小关系是:丙>乙>甲
三.氯化钠与粗盐提纯(共1小题)
5.(2023 眉山)红色经典影片《闪闪的红星》中有一段儿童团员潘冬子给红军送盐的故事。冬子开始把食盐装在竹筒中,打算扮作上山砍柴的人将食盐送给红军。途中发现敌人盘查严格,冬子急中生智跑到河边,把竹筒里的食盐全部溶成盐水,再用棉袄吸收,最终顺利地将食盐送给了红军。回答下列问题:
(1)从物质分类的角度分析,盐水属于 (填“纯净物”或“混合物”);从物质变化的角度分析,食盐溶成水属于 (填“物理变化”或“化学变化”);
(2)从棉袄中挤出盐水,过滤,蒸发得到食盐。其中用到的玻璃仪器有烧杯、玻璃棒、酒精灯和 ;
(3)氯化钠的溶解度如表。假设冬子的竹筒中有179g氯化钠,10℃时完全溶解所需水的质量至少为 g;
温度/℃ 0 10 20 30 40 50 60
氯化钠的溶解度/g 35.7 35.8 36.0 36.3 36.6 37.0 37.8
(4)氯化钠在生活中的用途: (任写一点即可)。
四.微粒观点及模型图的应用(共1小题)
6.(2023 泸州)泸州市生态环境局、公安局联合发文,从2023年5月4日起,对机动车排放不合格的违法行为进行抓拍。下表测定出汽车在不同速度下,每平均行驶1km,行驶的时间与所排放大气污染物的质量之间的关系。汽车发动机内高温条件下生成氮氧化物的反应如图所示。
行驶1km的时间/min污染物质量/g污染物 0.5 0.75 1.2
一氧化碳 9.6 5.4 8.7
氮氧化物 3.8 1.5 0.6
碳氢化合物 0.8 0.6 0.7
(1)碳氢化合物属于 (选填“有机物”或“无机物”)。
(2)甲图所示反应的化学方程式为 。
(3)随汽车速度降低,3种污染物中 的质量在持续减少,因为减速时使进入发动机的 的量减少(填分子式),生成的污染物也随之减少。
五.元素周期表的特点及其应用(共2小题)
7.(2023 南充)金属锶用于制造合金、光电管、照明灯,锶元素(Sr)在元素周期表中的信息及原子结构示意图如图1所示,回答下列问题:
(1)锶元素的相对原子质量为 。
(2)图2中的三种元素,与锶元素化学性质相似的是 (填元素符号)。
(3)氯化锶是常用的牙膏脱敏剂,易溶于水,可由氢氧化锶与盐酸反应制备,该反应的化学方程式为 。
8.(2023 达州)元素周期表是学习和研究化学、探索未知世界最有力的工具之一。图一是元素周期表的部分信息,图二是两种粒子的结构示意图。请回答下列问题。
(1)在前人的研究基础上得到第一张元素周期表的化学家是 (填字母编号,下同)。
A.徐寿
B.卢瑟福
C.侯德榜
D.门捷列夫
(2)图一中镁元素与铝元素之间最本质的区别是 不同。
A.中子数
B.质子数
C.核外电子数
D.相对原子质量
(3)图一中氖原子的相对原子质量为 。
(4)图二中两种粒子形成的化合物化学式为 。
六.标签上标示的物质成分及其含量(共1小题)
9.(2023 泸州)某品牌饮用矿泉水的说明书如表所示。回答相关问题:
XXX(饮用矿泉水)净含量:350mL配料表:纯净水、硫酸镁、氯化钾保质期:12个月主要成分:水钾离子:1.0~27.3mg/L镁离子:0.1~4.9mg/L氯离子:1.0~27.3mg/L硫酸根离子:0.4~19.5mg/L
(1)该品牌饮用矿泉水配料中加了 种盐(填数字)。
(2)检验饮用矿泉水中含有硫酸根离子的方法是:取2mL浓缩后的矿泉水于试管中,滴加 ,观察到 现象时,即可证明。
(3)主要成分中,最外层电子数为8的阴离子的符号是 。
七.化学符号及其周围数字的意义(共1小题)
10.(2023 达州)化学用语是最简明、信息丰富、化学世界通用的语言。请用化学用语填空。
(1)银离子 ;
(2)二氧化硫 ;
(3)6个氧分子 ;
(4)6个钙原子 。
八.根据化学反应方程式的计算(共2小题)
11.(2023 泸州)泸州的天然气化工实力雄厚,天然气可制备多种化工产品,由天然气→氢气→氨气→硝酸各步转化的反应如下(反应条件未给出)。回答相关问题:
①CH4+2H2O═CO2+4H2;②N2+3H2═2NH3;③NH3+2O2═HNO3+H2O
(1)属于化合反应的是 (填反应的序号)。
(2)③反应中氮的化合价升高了 价。若③恰好完全反应,所得硝酸溶液的溶质质量分数为 (列出计算式即可)。
12.(2023 遂宁)小贤向154.9gCuSO4和H2SO4的混合溶液中加入50g16%的NaOH溶液,充分反应后,产生蓝色沉淀,过滤,得到固体4.9g和无色滤液,向无色滤液中滴加酚酞试液,无明显现象。
(1)蓝色沉淀的物质名称为 ;
(2)发生中和反应的化学方程式为 ;
(3)无色滤液中溶质的质量分数为 。
九.复合材料、纳米材料(共1小题)
13.(2023 成都)根据图文回答下列问题。
(1)潜航时,必须调节舱内氧气、水蒸气和 的含量。制造“蛟龙号”外壳的合金应选择 (填字母)。
a.黄铜
b.不锈钢
c.钛合金
(2)航天食品有脱水米饭、宫爆鸡丁、茶饮等,米饭富含的营养素主要是 。为保证营养均衡,提供了水果,作用是 。
(3)高铁制造用到铝合金、玻璃钢、碳纤维等,属于复合材料的是 。座椅内填充了“聚氨酯高回弹发泡”新材料,具有防火阻燃、吸音性好、 (写一条)等特点。
(4)大运会场馆地下车库通过一氧化碳传感器反馈值来确定送排风系统的开启与关闭。车库内一氧化碳主要来源于 ,危害是 。
一十.生命活动与六大营养素(共1小题)
14.(2023 泸州)泸州白酒酿制“始于商周,盛于明清,纵横二千余年”,发展为以高梁与曲药为原料的独特酿造技术,其中曲药富含各种微生物,以及微生物所分泌的酶。回答下列问题:
(1)曲药能加快高梁中的 转化为葡萄糖。
(2)在酵母菌的作用下,将葡萄糖(C6H12O6) 分解成乙醇(C2H5OH),还有一种气体产物,该反应的化学方程式为 。
(3)发酵后的混合物得到白酒的最佳方法是 (选填“蒸馏”或“过滤”)。
(4)泸州曲药制酒的独特酿造技术是几百年来经过酿酒师们的不断劳动实践形成的,如果技术不精,“火候”把握不好会有酸味,影响口感,主要是因为产生了 。
(5)白酒的酒度通常是指20℃时酒精的体积百分数。如60度(60°)白酒是指100mL白酒中含酒精60mL。如何用500mL有刻度的器皿,将50°白酒勾兑出500mL40°白酒? 。
一十一.食品、药品与健康食品中的有机营养素(共1小题)
15.(2023 南充)化学来源于生活,服务于生活,回答下列问题。
(1)下列南充名小吃都富含蛋白质的是 (填选项)。
A.川北凉粉、南部肥肠
B.营山凉面、西充狮子糕
C.张飞牛肉、河舒豆腐
(2)生产自来水的过程中,可用高铁酸钾(K2FeO4)作净水剂,高铁酸钾中铁元素的化合价为 ,在一定条件下可发生反应:4K2FeO4+10X═4Fe(OH)3↓+8KOH+3O2↑,则X的化学式为 。
(3)空气中的氮气可合成氨气,其微观反应示意图如图,下列说法正确的是 (填选项)。
A.该反应的基本反应类型为复分解反应
B.该反应中分子的种类发生了变化
C.生成物的分子个数比为1:1
D.6000L氨气可压缩保存在40L的钢瓶中,说明气体分子间间隔较大
四川省各市2023年中考化学真题分类分层汇编-06填空题(基础提升)
参考答案与试题解析
一.固体溶解度的影响因素(共1小题)
1.(2023 自贡)如图1为某兴趣小组用硝酸钾进行的系列实验,图2为硝酸钾溶解度与温度的关系。
(1)B中溶液为 饱和 (填“饱和”或“不饱和”)溶液。
(2)C中固体 增加 (填“增加”或“减少”)。
(3)D中 无 (填“有”或“无”)固体。
(4)E中溶液的溶质质量分数为 25% 。
【答案】(1)饱和;
(2)增加;
(3)无;
(4)25%。
【解答】解:(1)40℃时,硝酸钾的溶解度为63.9g,则该温度下的50g水中的最多能溶解31.95g硝酸钾,则B中硝酸钾不能全部溶解,所得溶液为饱和溶液;故答案为:饱和;
(2)硝酸钾的溶解度随温度的降低而减小,因此B中硝酸钾的饱和溶液降温至20℃时,硝酸钾会部分结晶析出,所以C中固体增加;故答案为:增加;
(3)60℃时,硝酸钾的溶解度为110.0g,则该温度下的50g水中最多能溶解硝酸钾的质量为55.0g,因此加入的50g硝酸钾晶体全部溶解,D中没有固体;故答案为:无;
(4)40℃时,硝酸钾的溶解度为63.9g,则该温度下的150g水中的最多能溶解硝酸钾的质量为63.9g×1.5=95.85g,所以50g硝酸钾完全溶解,所得溶液中溶质的质量分数为=25%;故答案为:25%。
二.固体溶解度曲线及其作用(共3小题)
2.(2023 遂宁)某兴趣小组用硝酸钾进行了图甲所示的实验,硝酸钾溶解度与温度的关系如图乙。
(1)10℃时,硝酸钾的溶解度是 20.6 克;
(2)②中硝酸钾溶液是 不饱和 (选填“饱和”或“不饱和”)溶液;
(3)通过查阅资料知道氯化钠的溶解度受温度影响较小。从硝酸钾溶液(含有少量氯化钠)中提纯硝酸钾的方法是 降温 结晶。
【答案】(1)20.6;
(2)不饱和;
(3)降温。
【解答】解:(1)由硝酸钾溶解度与温度的关系图,10℃时,硝酸钾的溶解度是20.6g。
(2)40℃时,硝酸钾的溶解度是63.9g,则40℃时,100g水中最多能溶解63.9g硝酸钾,溶液达到饱和状态,则②中硝酸钾溶液是不饱和溶液。
(3)硝酸钾的溶解度受温度影响较大,而氯化钠受温度影响较小,则从硝酸钾溶液(含有少量氯化钠)中提纯硝酸钾的方法是降温结晶。
故答案为:
(1)20.6;
(2)不饱和;
(3)降温。
3.(2023 凉山州)中国为2022年卡塔尔世界杯提供了大量科技支持,如光伏发电、海水淡化等。
(1)检验淡化后的海水是否属于硬水,最简便的方法是加入 肥皂水 。
(2)下列有关水的说法错误的是 A 。
A.为倡导节约用水,可在公共用水区域张贴图1标志
B.用水灭火,是利用水蒸发吸热使温度降到可燃物的着火点以下
C.用水可鉴别硝酸铵、氢氧化钠、蔗糖三种白色固体
D.工业上的冷却水可重复利用
(3)水是常用的溶剂。请根据图2溶解度曲线回答问题:
①图2中P点的含义是 在t1℃时,甲和丙的溶解度相等 。
②t2℃时,将30g甲物质加到50g水中充分溶解,所得溶液的质量是 75 g。
③t2℃时,等质量的甲、乙、丙饱和溶液中溶剂的质量由多到少依次为 丙>乙>甲 。
【答案】(1)肥皂水;
(2)A;
(3)①在t1℃时,甲和丙的溶解度相等;
②75g;
③丙>乙>甲。
【解答】解:(1)向水中加入肥皂水时,如果产生的泡沫很多,是软水;如果不产生泡沫或产生的泡沫很少,是硬水。
(2)A、图1为中国节能标志,为倡导节约用水,可在公共用水区域张贴节水标志,故错误;
B、用水灭火的原理主要是利用水蒸发吸热,使温度降到可燃物的着火点以下,故正确;
C、可用水鉴别硝酸铵、氢氧化钠、蔗糖三种白色固体,溶于水温度几乎不变的是蔗糖,溶于水放热使温度升高的是氢氧化钠,溶于水吸热使温度降低的是硝酸铵,故正确;
D、工业上冷却水重复利用,能节约用水,利于保护水资源,故正确;
(3)①图2中P点的含义是:在t1℃时,甲和丙的溶解度相等;
②t2℃时甲的溶解度是50g,将30g甲物质加到50g水中,充分溶解后,能够溶解25g,所得溶液的质量为75g;
③t2℃时,:甲>乙>丙,所以等质量的甲、乙、丙饱和溶液中溶剂的质量由多到少依次为:丙>乙>甲。
故答案为:(1)肥皂水;
(2)A;
(3)①在t1℃时,甲和丙的溶解度相等;
②75g;
③丙>乙>甲。
4.(2023 南充)溶液在日常生活、工农业生产和科学研究中具有广泛的用途。
(1)碘酒用于消毒杀菌,其溶剂是 C2H5OH (填化学式)。
(2)如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,回答下列问题:
①甲中混有少量乙时,提纯甲的方法是 降温结晶 。
②t2℃时,将30g甲固体加入到50g水中,充分溶解并恢复到原温度,所得溶液中溶质和溶液的质量之比为 2:7 (填最简整数比)。
③t2℃时,将甲、乙、丙的饱和溶液降温到t1℃,下列说法正确的是 B (填选项)。
A.析出晶体质量最多的是甲
B.溶质质量分数大小关系是:乙>甲>丙
C.得到的都是饱和溶液
D.溶剂质量大小关系是:丙>乙>甲
【答案】(1)C2H5OH;
(2)①降温结晶;②2:7;③B。
【解答】解:(1)碘酒用于消毒杀菌,其溶剂是酒精,化学式为:C2H5OH。
(2)①由图可知,甲、乙的溶解度都随温度的降低而减小,甲的溶解度受温度变化影响较大,则甲中混有少量乙时,提纯甲的方法是降温结晶。
②t2℃时,甲的溶解度是40g,即100g水中最多溶解40g甲,则50g水中最多溶解20g甲;将30g甲固体加入到50g水中,充分溶解并恢复到原温度,只能溶解20g的甲,则所得溶液中含有20g溶质和50g溶剂,溶质和溶液的质量之比为20g:(20g+50g)=2:7。
③A、将t2℃时甲、乙、丙的饱和溶液降温到t1℃,由于不知道溶液的质量,无法判断析出晶体的质量,故选项说法错误;
B、甲、乙的溶解度随温度的降低而减小,丙的溶解度随温度的降低而增大,将t2℃时甲、乙、丙的饱和溶液降温到t1℃,甲、乙溶液中有晶体析出,此时甲、乙的溶质质量分数为t1℃时甲、乙饱和溶液的溶质质量分数,大小关系为:乙>甲,而丙的溶质质量分数不变,等于t2℃时丙饱和溶液的溶质质量分数,所以溶质质量分数大小关系是:乙>甲>丙,故选项说法正确;
C、丙的溶解度随温度的降低而增大,所以得到的丙溶液不是饱和溶液,故选项说法错误;
D、由于不知道t2℃时甲、乙、丙饱和溶液的质量,所以无法判断溶剂质量的大小,故选项说法错误;
故选:B。
故答案为:
(1)C2H5OH;
(2)①降温结晶;②2:7;③B。
三.氯化钠与粗盐提纯(共1小题)
5.(2023 眉山)红色经典影片《闪闪的红星》中有一段儿童团员潘冬子给红军送盐的故事。冬子开始把食盐装在竹筒中,打算扮作上山砍柴的人将食盐送给红军。途中发现敌人盘查严格,冬子急中生智跑到河边,把竹筒里的食盐全部溶成盐水,再用棉袄吸收,最终顺利地将食盐送给了红军。回答下列问题:
(1)从物质分类的角度分析,盐水属于 混合物 (填“纯净物”或“混合物”);从物质变化的角度分析,食盐溶成水属于 物理变化 (填“物理变化”或“化学变化”);
(2)从棉袄中挤出盐水,过滤,蒸发得到食盐。其中用到的玻璃仪器有烧杯、玻璃棒、酒精灯和 漏斗 ;
(3)氯化钠的溶解度如表。假设冬子的竹筒中有179g氯化钠,10℃时完全溶解所需水的质量至少为 500 g;
温度/℃ 0 10 20 30 40 50 60
氯化钠的溶解度/g 35.7 35.8 36.0 36.3 36.6 37.0 37.8
(4)氯化钠在生活中的用途: 作调味品(合理即可) (任写一点即可)。
【答案】(1)混合物;物理变化;
(2)漏斗;
(3)500;
(4)作调味品(合理即可)。
【解答】解:(1)从物质分类的角度分析,盐水中含有氯化钠、水,属于混合物。
从物质变化的角度分析,食盐溶成水,没有新物质生成,属于物理变化。
(2)过滤是把不溶于液体的固体与液体分离的一种方法,过滤操作的装置由铁架台、烧杯、玻璃棒、漏斗四种仪器组成;蒸发操作的装置由铁架台、玻璃棒、酒精灯、蒸发皿四种仪器组成;其中用到的玻璃仪器有烧杯、玻璃棒、酒精灯和漏斗。
(3)10℃时氯化钠的溶解度为35.8g,冬子的竹筒中有179g氯化钠,10℃时完全溶解所需水的质量至少为100g×=500g。
(4)氯化钠在生活中可用作调味品,用于腌制咸菜,用于制造生理盐水,农业生产中用于选种,用于融雪等。
故答案为:
(1)混合物;物理变化;
(2)漏斗;
(3)500;
(4)作调味品(合理即可)。
四.微粒观点及模型图的应用(共1小题)
6.(2023 泸州)泸州市生态环境局、公安局联合发文,从2023年5月4日起,对机动车排放不合格的违法行为进行抓拍。下表测定出汽车在不同速度下,每平均行驶1km,行驶的时间与所排放大气污染物的质量之间的关系。汽车发动机内高温条件下生成氮氧化物的反应如图所示。
行驶1km的时间/min污染物质量/g污染物 0.5 0.75 1.2
一氧化碳 9.6 5.4 8.7
氮氧化物 3.8 1.5 0.6
碳氢化合物 0.8 0.6 0.7
(1)碳氢化合物属于 有机物 (选填“有机物”或“无机物”)。
(2)甲图所示反应的化学方程式为 N2+O22NO 。
(3)随汽车速度降低,3种污染物中 氮氧化物 的质量在持续减少,因为减速时使进入发动机的 N2 的量减少(填分子式),生成的污染物也随之减少。
【答案】(1)有机物;
(2)N2+O22NO;
(3)氮氧化物;N2。
【解答】解:(1)碳氢化合物是一种含碳元素的化合物,属于有机物;故答案为:有机物;
(2)由微观反应示意图可知,该反应是由氮气与氧气在高温的条件下反应生成一氧化氮,化学方程式为N2+O22NO;故答案为:N2+O22NO;
(3)由表格中的数据可知,随汽车速度降低,3种污染物中氮氧化物的质量在持续减少,因为减速时使进入发动机的氮气的量减少,生成的污染物也随之减少,氮气的化学式为N2;故答案为:氮氧化物;N2。
五.元素周期表的特点及其应用(共2小题)
7.(2023 南充)金属锶用于制造合金、光电管、照明灯,锶元素(Sr)在元素周期表中的信息及原子结构示意图如图1所示,回答下列问题:
(1)锶元素的相对原子质量为 87.62 。
(2)图2中的三种元素,与锶元素化学性质相似的是 Mg (填元素符号)。
(3)氯化锶是常用的牙膏脱敏剂,易溶于水,可由氢氧化锶与盐酸反应制备,该反应的化学方程式为 Sr(OH)2+2HCl═SrCl2+2H2O 。
【答案】(1)87.62;
(2)Mg。
(3)Sr(OH)2+2HCl═SrCl2+2H2O。
【解答】解:(1)根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为87.62。
(2)原子中,质子数=核外电子数,则38=2+8+18+8+n,n=2。
元素的化学性质跟它的原子的最外层电子数目关系非常密切,决定元素化学性质的是原子中的最外层电子数,图2中的三种元素,与锶元素化学性质相似的是B,它们原子的最外层电子数均为2,核内质子数为12,为镁元素,其元素符号为Mg。
(3)氢氧化锶与盐酸反应生成氯化锶和水,反应的化学方程式为Sr(OH)2+2HCl═SrCl2+2H2O。
故答案为:
(1)87.62;
(2)Mg。
(3)Sr(OH)2+2HCl═SrCl2+2H2O。
8.(2023 达州)元素周期表是学习和研究化学、探索未知世界最有力的工具之一。图一是元素周期表的部分信息,图二是两种粒子的结构示意图。请回答下列问题。
(1)在前人的研究基础上得到第一张元素周期表的化学家是 D (填字母编号,下同)。
A.徐寿
B.卢瑟福
C.侯德榜
D.门捷列夫
(2)图一中镁元素与铝元素之间最本质的区别是 B 不同。
A.中子数
B.质子数
C.核外电子数
D.相对原子质量
(3)图一中氖原子的相对原子质量为 20.18 。
(4)图二中两种粒子形成的化合物化学式为 NaF 。
【答案】(1)D;
(2)B;
(3)20.18;
(4)NaF。
【解答】解:(1)门捷列夫在化学上的主要贡献是在前人的研究基础上编制出第一张元素周期表。
(2)元素是质子数(即核电荷数)相同的一类原子的总称,不同种元素最本质的区别是质子数(即核电荷数)不同,所以镁元素与铝元素之间的本质区别是质子数(即核电荷数)不同。
(3)根据氖元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为20.18。
(4)图二中两种粒子的核内质子数分别是11、9,分别是钠元素和氟元素,钠原子的最外层电子数为1,在化学反应中易失去1个电子而形成带1个单位正电荷的阳离子,化合价的数值等于离子所带电荷的数值,且符号一致,则该元素的化合价为+1价;氟原子的最外层电子数为7,在化学反应中易得到1个电子而形成1个单位负电荷的阴离子,化合价的数值等于离子所带电荷的数值,且符号一致,则该元素的化合价为﹣1价;钠元素显+1价,氟元素显﹣1价,组成化合物的化学式为NaF。
故答案为:
(1)D;
(2)B;
(3)20.18;
(4)NaF。
六.标签上标示的物质成分及其含量(共1小题)
9.(2023 泸州)某品牌饮用矿泉水的说明书如表所示。回答相关问题:
XXX(饮用矿泉水)净含量:350mL配料表:纯净水、硫酸镁、氯化钾保质期:12个月主要成分:水钾离子:1.0~27.3mg/L镁离子:0.1~4.9mg/L氯离子:1.0~27.3mg/L硫酸根离子:0.4~19.5mg/L
(1)该品牌饮用矿泉水配料中加了 2 种盐(填数字)。
(2)检验饮用矿泉水中含有硫酸根离子的方法是:取2mL浓缩后的矿泉水于试管中,滴加 用硝酸酸化的硝酸钡溶液 ,观察到 产生白色沉淀 现象时,即可证明。
(3)主要成分中,最外层电子数为8的阴离子的符号是 Cl﹣ 。
【答案】(1)2;
(2)用硝酸酸化的硝酸钡溶液;产生白色沉淀;
(3)Cl﹣。
【解答】解:(1)由配料表,硫酸镁、氯化钾均是由金属离子和酸根离子构成的化合物,均属于盐。
(2)检验饮用矿泉水中含有硫酸根离子的方法是:取2mL浓缩后的矿泉水于试管中,滴加用硝酸酸化的硝酸钡溶液,观察到产生白色沉淀,即可证明。
(3)主要成分中,最外层电子数为8的阴离子是氯离子,其离子符号为Cl﹣。
故答案为:
(1)2;
(2)用硝酸酸化的硝酸钡溶液;产生白色沉淀;
(3)Cl﹣。
七.化学符号及其周围数字的意义(共1小题)
10.(2023 达州)化学用语是最简明、信息丰富、化学世界通用的语言。请用化学用语填空。
(1)银离子 Ag+ ;
(2)二氧化硫 SO2 ;
(3)6个氧分子 6O2 ;
(4)6个钙原子 6Ca 。
【答案】(1)Ag+;
(2)SO2;
(3)6O2;
(4)6Ca。
【解答】解:(1)由离子的表示方法,在表示该离子的元素符号或原子团的右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个单位电荷时,1要省略。银离子可表示为Ag+。
(2)二氧化硫的化学式为SO2。
(3)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则6个氧分子可表示为6O2。
(4)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故6个钙原子表示为6Ca。
故答案为:
(1)Ag+;
(2)SO2;
(3)6O2;
(4)6Ca。
八.根据化学反应方程式的计算(共2小题)
11.(2023 泸州)泸州的天然气化工实力雄厚,天然气可制备多种化工产品,由天然气→氢气→氨气→硝酸各步转化的反应如下(反应条件未给出)。回答相关问题:
①CH4+2H2O═CO2+4H2;②N2+3H2═2NH3;③NH3+2O2═HNO3+H2O
(1)属于化合反应的是 ② (填反应的序号)。
(2)③反应中氮的化合价升高了 8 价。若③恰好完全反应,所得硝酸溶液的溶质质量分数为 100% (列出计算式即可)。
【答案】(1)②;
(2)8;100%。
【解答】解:(1)②N2+3H2═2NH3,该反应符合“多变一”的形式,符合化合反应的特征,属于化合反应。
(2)NH3中氮元素的化合价为﹣3价,HNO3中氮元素的化合价为+5价,则③反应中氮的化合价升高了8价。
设生成的硝酸的质量为63g,同时生成水的质量为x。
NH3+2O2═HNO3+H2O
63 18
63g x
x=18g
所得硝酸溶液的溶质质量分数为×100%=100%。
故答案为:
(1)②;
(2)8;100%。
12.(2023 遂宁)小贤向154.9gCuSO4和H2SO4的混合溶液中加入50g16%的NaOH溶液,充分反应后,产生蓝色沉淀,过滤,得到固体4.9g和无色滤液,向无色滤液中滴加酚酞试液,无明显现象。
(1)蓝色沉淀的物质名称为 氢氧化铜 ;
(2)发生中和反应的化学方程式为 2NaOH+H2SO4═Na2SO4+2H2O ;
(3)无色滤液中溶质的质量分数为 7.1% 。
【答案】(1)氢氧化铜;
(2)2NaOH+H2SO4═Na2SO4+2H2O;
(3)7.1%。
【解答】解:(1)硫酸铜和氢氧化钠溶液反应生成氢氧化铜沉淀和硫酸钠,蓝色沉淀的物质名称为氢氧化铜。
(2)硫酸和氢氧化钠反应生成硫酸钠和水,属于中和反应,反应的化学方程式为2NaOH+H2SO4═Na2SO4+2H2O。
(3)氢氧化钠溶液先与硫酸反应生成硫酸钠和水,硫酸反应完,再与硫酸铜溶液反应生成氢氧化铜沉淀和硫酸钠,充分反应后,产生蓝色沉淀,过滤,得到固体4.9g和无色滤液,说明硫酸铜已经完全反应;向无色滤液中滴加酚酞试液,无明显现象,说明氢氧化钠溶液已完全反应。
由2NaOH+H2SO4═Na2SO4+2H2O、2NaOH+CuSO4═Na2SO4+Cu(OH)2↓,可得:
2NaOH~Na2SO4
80 142
50g×16% x
x=14.2g
无色滤液中溶质的质量分数为×100%=7.1%。
故答案为:
(1)氢氧化铜;
(2)2NaOH+H2SO4═Na2SO4+2H2O;
(3)7.1%。
九.复合材料、纳米材料(共1小题)
13.(2023 成都)根据图文回答下列问题。
(1)潜航时,必须调节舱内氧气、水蒸气和 二氧化碳 的含量。制造“蛟龙号”外壳的合金应选择 c (填字母)。
a.黄铜
b.不锈钢
c.钛合金
(2)航天食品有脱水米饭、宫爆鸡丁、茶饮等,米饭富含的营养素主要是 糖类 。为保证营养均衡,提供了水果,作用是 补充维生素 。
(3)高铁制造用到铝合金、玻璃钢、碳纤维等,属于复合材料的是 玻璃钢 。座椅内填充了“聚氨酯高回弹发泡”新材料,具有防火阻燃、吸音性好、 弹性好 (写一条)等特点。
(4)大运会场馆地下车库通过一氧化碳传感器反馈值来确定送排风系统的开启与关闭。车库内一氧化碳主要来源于 汽车尾气 ,危害是 造成中毒 。
【答案】(1)二氧化碳;c;
(2)糖类;补充维生素;
(3)玻璃钢;弹性好;
(4)汽车尾气;造成中毒。
【解答】解:(1)呼吸作用消耗氧气,呼出二氧化碳,因此潜航时,必须调节舱内氧气、水蒸气和二氧化碳的含量。钛合金的强度大、机械性能好、耐腐蚀性强,因此制造“蛟龙号”外壳的合金应选择钛合金;
故答案为:二氧化碳;c;
(2)米饭富含的营养素主要是糖类。为保证营养均衡,提供了水果,作用是补充维生素;
故答案为:糖类;补充维生素;
(3)玻璃钢是由玻璃纤维和合成材料复合而成的,属于复合材料;座椅内填充了“聚氨酯高回弹发泡”新材料,具有防火阻燃、吸音性好、弹性好等特点;故答案为:玻璃钢;弹性好;
(4)一氧化碳有毒,车库内一氧化碳主要来源于汽车尾气,危害是造成中毒;
故答案为:汽车尾气;造成中毒。
一十.生命活动与六大营养素(共1小题)
14.(2023 泸州)泸州白酒酿制“始于商周,盛于明清,纵横二千余年”,发展为以高梁与曲药为原料的独特酿造技术,其中曲药富含各种微生物,以及微生物所分泌的酶。回答下列问题:
(1)曲药能加快高梁中的 淀粉 转化为葡萄糖。
(2)在酵母菌的作用下,将葡萄糖(C6H12O6) 分解成乙醇(C2H5OH),还有一种气体产物,该反应的化学方程式为 C6H12O62C2H5OH+2CO2↑ 。
(3)发酵后的混合物得到白酒的最佳方法是 蒸馏 (选填“蒸馏”或“过滤”)。
(4)泸州曲药制酒的独特酿造技术是几百年来经过酿酒师们的不断劳动实践形成的,如果技术不精,“火候”把握不好会有酸味,影响口感,主要是因为产生了 醋酸或乙酸 。
(5)白酒的酒度通常是指20℃时酒精的体积百分数。如60度(60°)白酒是指100mL白酒中含酒精60mL。如何用500mL有刻度的器皿,将50°白酒勾兑出500mL40°白酒? 用带有刻度的容器量取400mL50°的白酒,然后再向容器内加入蒸馏水至500mL即可 。
【答案】(1)淀粉;
(2)C6H12O62C2H5OH+2CO2↑;
(3)蒸馏;
(4)醋酸或乙酸;
(5)用带有刻度的容器量取400mL50°的白酒,然后再向容器内加入蒸馏水至500mL即可。
【解答】解:(1)曲药能加快高梁中的淀粉转化为葡萄糖;故答案为:淀粉;
(2)在酵母菌的作用下,将葡萄糖(C6H12O6) 分解成乙醇(C2H5OH),还有一种气体产物——二氧化碳,该反应的化学方程式为C6H12O62C2H5OH+2CO2↑;故答案为:C6H12O62C2H5OH+2CO2↑;
(3)酒精和水能以任意比互溶,但酒精和水的沸点不同,因此发酵后的混合物得到白酒的最佳方法是蒸馏;故答案为:蒸馏;
(4)泸州曲药制酒的独特酿造技术是几百年来经过酿酒师们的不断劳动实践形成的,如果技术不精,“火候”把握不好会有酸味,影响口感,主要是因为产生了乙酸,俗称醋酸;故答案为:醋酸或乙酸;
(5)设需要50°白酒的体积为x,则:
x×50%=500mL×40%
x=400mL
需要水的体积为500mL﹣400mL=100mL
即配制方法是用带有刻度的容器量取400mL50°的白酒,然后再向容器内加入蒸馏水至500mL即可;
故答案为:用带有刻度的容器量取400mL50°的白酒,然后再向容器内加入蒸馏水至500mL即可。
一十一.食品、药品与健康食品中的有机营养素(共1小题)
15.(2023 南充)化学来源于生活,服务于生活,回答下列问题。
(1)下列南充名小吃都富含蛋白质的是 C (填选项)。
A.川北凉粉、南部肥肠
B.营山凉面、西充狮子糕
C.张飞牛肉、河舒豆腐
(2)生产自来水的过程中,可用高铁酸钾(K2FeO4)作净水剂,高铁酸钾中铁元素的化合价为 +6 ,在一定条件下可发生反应:4K2FeO4+10X═4Fe(OH)3↓+8KOH+3O2↑,则X的化学式为 H2O 。
(3)空气中的氮气可合成氨气,其微观反应示意图如图,下列说法正确的是 BD (填选项)。
A.该反应的基本反应类型为复分解反应
B.该反应中分子的种类发生了变化
C.生成物的分子个数比为1:1
D.6000L氨气可压缩保存在40L的钢瓶中,说明气体分子间间隔较大
【答案】(1)C;
(2)+6;H2O;
(3)BD。
【解答】解:(1)A.川北凉粉富含糖类;南部肥肠富含蛋白质和与油脂,不合题意;
B.营山凉面富含糖类;西充狮子糕富含糖类和油脂,不合题意;
C.张飞牛肉和河舒豆腐均富含蛋白质,符合题意;
故答案为:C;
(2)在K2FeO4中,钾元素的化合价为+1价,氧元素的化合价为﹣2价,设该化合物中铁元素的化合价为x,由化学式和化合物中正负化合价的代数和为零,则(+1)×2+x+(﹣2)×4=0,解得x=+6;由质量守恒定律可知:反应前后原子的种类和个数不变,等号左边除10X外,有8个钾原子、4个铁原子、16个氧原子,等号右边有4个铁原子、8个钾原子、20个氢原子和26个氧原子,则10X中含有20个氢原子和10个氧元素,则X为H2O;故答案为:+6;H2O;
(3)由微观反应示意图可知,氮气和水在催化剂的作用下反应生成氨气和氧气,该反应的化学方程式是:6H2O+2N23O2+4NH3。
A.该反应是由一种单质与一种化合物反应生成另一种单质与另一种化合物的反应,基本反应类型为置换反应,说法错误;
B.由分子结构模型可知,该反应中分子的种类发生了变化,说法正确;
C.由化学方程式可知,生成物的分子个数比为3:4或4:3,说法错误;
D.6000L氨气可压缩保存在40L的钢瓶中,说明气体分子间间隔较大,说法正确。
故答案为:BD。
同课章节目录
